Пассивное курение

Пассивное курение — это вдыхание табачного дыма , называемого пассивным курением , пассивным курением ( SHS ) или табачным дымом окружающей среды ( ETS ), лицами, не являющимися активными курильщиками . Это происходит, когда табачный дым распространяется в окружающую атмосферу в виде аэрозольного загрязнителя , что приводит к его вдыханию окружающими людьми в той же среде. Воздействие пассивного табачного дыма вызывает во многом такие же последствия для здоровья, как и активное курение . [1] [2] хотя и с меньшей распространенностью из-за пониженной концентрации дыма, попадающего в дыхательные пути .
Согласно последнему докладу ВОЗ, ежегодно во всем мире пассивное курение приводит к более чем 1,3 миллиона смертей. [3] Риски для здоровья, связанные с пассивным курением, являются предметом научного консенсуса . [4] [5] [6] и были основным мотивом для введения запрета на курение на рабочих местах и в закрытых помещениях, включая рестораны , бары и ночные клубы , а также в некоторых открытых общественных местах . [7]
Обеспокоенность по поводу пассивного курения сыграла центральную роль в дебатах о вреде и регулировании табачных изделий. С начала 1970-х годов табачная промышленность рассматривала обеспокоенность общественности по поводу пассивного курения как серьезную угрозу своим деловым интересам. [8] Несмотря на осознание табачной промышленностью вреда пассивного курения еще в 1980-х годах, табачная промышленность координировала научную полемику с целью прекращения регулирования своей продукции. [4] : 1242 [6]
Терминология
Фриц Ликинт ввел термин «пассивное курение» («Passivrauchen») в публикации на немецком языке в 1930-х годах. [9] [10] [11] Используемые термины включают «табачный дым в окружающей среде» для обозначения переносимых по воздуху веществ, а «непроизвольное курение» и «пассивное курение» относятся к воздействию пассивного курения. [12] [13] Термин «табачный дым в окружающей среде» восходит к спонсируемому промышленностью совещанию 1974 года, состоявшемуся на Бермудских островах , а термин «пассивное курение» впервые был использован в названии научной статьи в 1970 году. [13] Главный хирург США предпочитает использовать фразу «пассивное курение», а не «табачный дым в окружающей среде», заявляя, что «дескриптор «пассивное курение» отражает непроизвольный характер воздействия, а слово «окружающий» - нет». [1] : 9 Большинство исследователей считают термин «пассивное курение» синонимом «пассивного курения». [14] Напротив, в комментарии 2011 года в журнале Environmental Health Perspectives утверждается, что исследование «третьего курения» делает неуместным называть пассивное курение термином «пассивное курение», который, по мнению авторов, представляет собой pars pro toto . [14]
Термин « побочный дым » иногда используется для обозначения дыма, который выходит в воздух непосредственно из горящей сигареты , сигары или трубки . [15] в то время как «основной дым» относится к дыму, который выдыхает курильщик.
Влияние на здоровье
Пассивное курение вызывает многие из тех же заболеваний, что и прямое курение , включая сердечно-сосудистые заболевания , рак легких и респираторные заболевания . [1] [2] [16] К ним относятся:
- Рак :
- Общие: общий повышенный риск; [17] Анализируя данные, накопленные во всем мире, Международное агентство по исследованию рака в 2004 году пришло к выводу, что «вынужденное курение (воздействие пассивного или «экологического» табачного дыма) канцерогенно для человека». [2] Центры по контролю и профилактике заболеваний сообщают, что около 70 химических веществ, присутствующих в пассивном курении, являются канцерогенными. [18]
- Рак легких : Пассивное курение является фактором риска рака легких. [19] [20] По оценкам, в Соединенных Штатах пассивное курение является причиной более 7000 смертей от рака легких в год среди некурящих. [21] Четверть всех случаев приходится на людей, которые никогда не курили. [22]
- Рак молочной железы : Калифорнийское агентство по охране окружающей среды в 2005 году пришло к выводу, что пассивное курение увеличивает риск рака молочной железы у более молодых женщин, преимущественно в пременопаузе, на 70%. [16] США и главный хирург пришел к выводу, что доказательства являются «наводящими на размышления», но все же недостаточными, чтобы утверждать такую причинно-следственную связь. [1] Напротив, Международное агентство по исследованию рака в 2004 году пришло к выводу, что «не существует причинно-следственной связи между непроизвольным воздействием табачного дыма и раком молочной железы у никогда не куривших». [2] Метаанализ 2015 года показал, что доказательства того, что пассивное курение умеренно увеличивает риск рака молочной железы, стали «более существенными, чем несколько лет назад». [23]
- Рак шейки матки : обзор систематических обзоров 2015 года показал, что пассивное курение увеличивает риск развития рака шейки матки. [24]
- Рак мочевого пузыря : систематический обзор и метаанализ 2016 года показали, что пассивное курение связано со значительным увеличением риска развития рака мочевого пузыря. [25]
- Система кровообращения : риск сердечно-сосудистых заболеваний [26] [27] и снижение вариабельности сердечного ритма. [28]
- Проблемы с легкими :
- Риск астмы [31]
- Риск хронической обструктивной болезни легких (ХОБЛ) [32]
- Согласно обзору 2015 года, пассивное курение может увеличить риск заражения туберкулезом и ускорить прогрессирование заболевания, но доказательства остаются слабыми. [33]
- Большинство исследований связи между пассивным курением и синуситом выявили значительную связь между ними. [34]
- Когнитивные нарушения и деменция . Воздействие пассивного курения может повысить риск когнитивных нарушений и деменции у взрослых в возрасте 50 лет и старше. [35] У детей, подвергшихся пассивному курению, наблюдается снижение словарного запаса и навыков рассуждения по сравнению с детьми, не подвергавшимися воздействию табачного дыма, а также более общие когнитивные и интеллектуальные нарушения. [36]
- Психическое здоровье . Воздействие пассивного курения связано с повышенным риском развития симптомов депрессии. [37]
- Во время беременности :
- Выкидыш : метаанализ 2014 года показал, что пассивное курение матери увеличивает риск выкидыша на 11%. [38]
- Низкий вес при рождении [16] , часть Б, гл. 3 . [39]
- Преждевременные роды [16] , часть Б, гл. 3 [40] (Доказательства причинно-следственной связи описаны главным хирургом США в его отчете за 2006 год только как «наводящие на размышления». [41] ) Законы, ограничивающие курение, снижают число преждевременных родов. [42]
- Мертворождение и врожденные пороки развития у детей [43]
- Недавние исследования, сравнивающие женщин, подвергшихся пассивному курению, и женщин, не подвергавшихся воздействию табачного дыма, показывают, что женщины, подвергшиеся воздействию табачного дыма во время беременности, имеют более высокий риск рождения ребенка с врожденными аномалиями, большей длиной тела, меньшими окружностями головы и дефектами нервной трубки . [44] [45]
- Общий:
- Обострение астмы, аллергии и других состояний. [46] Систематический обзор и метаанализ 2014 года показали, что пассивное курение связано с несколько повышенным риском аллергических заболеваний среди детей и подростков; доказательства связи были слабее для взрослых. [47]
- Диабет 2 типа . [48] [49] [50] Остается неясным, является ли связь между пассивным курением и диабетом причинной. [51]
- Риск переноса Neisseria meningitidis или Streptococcus pneumoniae . [24]
- Возможный повышенный риск пародонтита . [52]
- Общий повышенный риск смерти у обоих взрослых: по оценкам, в 1991 году в США от него погибало 53 000 некурящих в год. [53] [54] и у детей. [55] Всемирная организация здравоохранения заявляет, что пассивное курение является причиной около 600 000 смертей в год и составляет около 1% глобального бремени болезней. [56] По состоянию на 2017 год пассивное курение является причиной около 900 000 смертей в год, что составляет около 1/8 всех смертей, вызванных курением. [57]
- Кожные заболевания: систематический обзор и метаанализ 2016 года показали, что пассивное курение связано с более высоким уровнем развития атопического дерматита . [58]
Риск для детей
- Синдром внезапной детской смерти (СВДС). [59] В своем отчете за 2006 год главный хирург США заключает: «Доказательств достаточно, чтобы сделать вывод о причинно-следственной связи между воздействием пассивного курения и синдромом внезапной детской смерти». [60] По оценкам, пассивное курение является причиной 430 смертей от СВДС в Соединенных Штатах ежегодно. [61]
- Астма . [62] [63] [64] Воздействие пассивного курения также связано с почти удвоенным риском госпитализации по поводу обострения астмы среди детей с астмой. [65]
- Легочные инфекции, [66] [67] [68] также включая более тяжелое заболевание с бронхиолитом [69] и бронхит , [70] и худший исход, [69] а также повышенный риск развития туберкулеза при контакте с носителем. [71] По оценкам, в Соединенных Штатах пассивное курение связано с от 150 000 до 300 000 инфекций нижних дыхательных путей у младенцев и детей в возрасте до 18 месяцев, что приводит к от 7 500 до 15 000 госпитализаций каждый год. [61]
- Impaired respiratory function and slowed lung growth[70]
- Allergies[72]
- Maternal passive smoking increases the risk of non-syndromic orofacial clefts by 50% among their children.[73]
- Learning difficulties, developmental delays, executive function problems,[74] and neurobehavioral effects.[75][76] Animal models suggest a role for nicotine and carbon monoxide in neurocognitive problems.[68]
- An increase in tooth decay (as well as related salivary biomarkers) has been associated with passive smoking in children.[77]
- Increased risk of middle ear infections.[68][78][79]
- Invasive meningococcal disease.[24][80]
- Anesthesia complications and some negative surgical outcomes.[81]
- Sleep disordered breathing: Most studies have found a significant association between passive smoking and sleep disordered breathing in children, but further studies are needed to determine whether this association is causal.[82]
- Adverse effects on the cardiovascular system of children.[83]
Evidence

Epidemiological studies show that non-smokers exposed to secondhand smoke are at risk for many of the health problems associated with direct smoking.
In 1992, a review estimated that secondhand smoke exposure was responsible for 35,000 to 40,000 deaths per year in the United States in the early 1980s.[84] The absolute risk increase of heart disease due to ETS was 2.2%, while the attributable risk percent was 23%. A 1997 meta-analysis found that secondhand smoke exposure increased the risk of heart disease by a quarter,[85] and two 1999 meta-analyses reached similar conclusions.[86][87]
Evidence shows that inhaled sidestream smoke, the main component of secondhand smoke, is about four times more toxic than mainstream smoke. This fact has been known to the tobacco industry since the 1980s, though it kept its findings secret.[88][89][90][91] Some scientists believe that the risk of passive smoking, in particular the risk of developing coronary heart diseases, may have been substantially underestimated.[92]
In 1997, a meta-analysis on the relationship between secondhand smoke exposure and lung cancer concluded that such exposure caused lung cancer. The increase in risk was estimated to be 24% among non-smokers who lived with a smoker.[93] In 2000, Copas and Shi reported that there was clear evidence of publication bias in the studies included in this meta-analysis. They further concluded that after correcting for publication bias, and assuming that 40% of all studies are unpublished, this increased risk decreased from 24% to 15%.[94] This conclusion has been challenged on the basis that the assumption that 40% of all studies are unpublished was "extreme".[2]: 1269 In 2006, Takagi et al. reanalyzed the data from this meta-analysis to account for publication bias and estimated that the relative risk of lung cancer among those exposed to secondhand smoke was 1.19, slightly lower than the original estimate.[95] A 2000 meta-analysis found a relative risk of 1.48 for lung cancer among men exposed to secondhand smoke, and a relative risk of 1.16 among those exposed to it at work.[96] Another meta-analysis confirmed the finding of an increased risk of lung cancer among women with spousal exposure to secondhand smoke the following year. It found a relative risk of lung cancer of 1.29 for women exposed to secondhand smoke from their spouses.[97] A 2014 meta-analysis noted that "the association between exposure to secondhand smoke and lung cancer risk is well established."[98]
A minority of epidemiologists have found it hard to understand how secondhand smoke, which is more diluted than actively inhaled smoke, could have an effect that is such a large fraction of the added risk of coronary heart disease among active smokers.[99][100] One proposed explanation is that secondhand smoke is not simply a diluted version of "mainstream" smoke, but has a different composition with more toxic substances per gram of total particulate matter.[99] Passive smoking appears to be capable of precipitating the acute manifestations of cardio-vascular diseases (atherothrombosis) and may also have a negative impact on the outcome of patients who have acute coronary syndromes.[101]
In 2004, the International Agency for Research on Cancer (IARC) of the World Health Organization (WHO) reviewed all significant published evidence related to tobacco smoking and cancer. It concluded:
These meta-analyses show that there is a statistically significant and consistent association between lung cancer risk in spouses of smokers and exposure to second-hand tobacco smoke from the spouse who smokes. The excess risk is of the order of 20% for women and 30% for men and remains after controlling for some potential sources of bias and confounding.[2]
Subsequent meta-analyses have confirmed these findings.[102][103]
The National Asthma Council of Australia cites studies showing that secondhand smoke is probably the most important indoor pollutant, especially around young children:[104]
- Smoking by either parent, particularly by the mother, increases the risk of asthma in children.
- The outlook for early childhood asthma is less favourable in smoking households.
- Children with asthma who are exposed to smoking in the home generally have more severe disease.
- Many adults with asthma identify ETS as a trigger for their symptoms.
- Doctor-diagnosed asthma is more common among non-smoking adults exposed to ETS than those not exposed. Among people with asthma, higher ETS exposure is associated with a greater risk of severe attacks.
In France, exposure to secondhand smoke has been estimated to cause between 3,000[105] and 5,000 premature deaths per year, with the larger figure cited by Prime Minister Dominique de Villepin during his announcement of a nationwide smoke-free law: "That makes more than 13 deaths a day. It is an unacceptable reality in our country in terms of public health."[106]
There is good observational evidence that smoke-free legislation reduces the number of hospital admissions for heart disease.[107][108]
Exposure and risk levels
The International Agency for Research on Cancer of the World Health Organization concluded in 2004 that there was sufficient evidence that secondhand smoke caused cancer in humans.[2] Those who work in environments where smoke is not regulated are at higher risk.[109][103] Workers particularly at risk of exposure include those in installation repair and maintenance, construction and extraction, and transportation.[110]
Much research has come from studies of nonsmokers who are married to a smoker. The US Surgeon General, in his 2006 report, estimated that living or working in a place where smoking is permitted increases the non-smokers' risk of developing heart disease by 25–30% and lung cancer by 20–30%.[111]
Similarly, children who are exposed to environmental tobacco smoke are shown to experience a range of adverse effects[112][113][114] and a higher risk of becoming smokers later in life.[115] The WHO has identified reduction of exposure to environmental tobacco smoke as key element for actions to encourage healthy child development.[116]
The US Centers for Disease Control and Prevention monitors the extent of and trends in exposure to environmental tobacco smoke by measuring serum cotinine in national health surveys.[117] The prevalence of secondhand smoke exposure among U.S. nonsmokers declined from 87.5% in 1988 to 25.2% in 2014. However, nearly half of blacks and the poor were exposed in 2014.
Interventions to reduce environmental tobacco smoke
A systematic review compared smoking control programmes and their effects on smoke exposure in children. The review distinguishes between community-based, ill-child and healthy-child settings and the most common types of interventions were counselling or brief advice during clinical visits. The review did not find superior outcomes for any intervention, and the authors caution that evidence from adult settings may not generalise well to children.[118]
Biomarkers
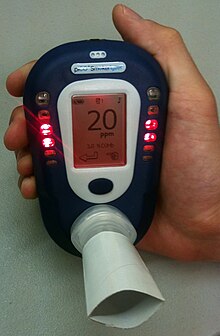
Environmental tobacco smoke can be evaluated either by directly measuring tobacco smoke pollutants found in the air or by using biomarkers, an indirect measure of exposure. Carbon monoxide monitored through breath, nicotine, cotinine, thiocyanates, and proteins are the most specific biological markers of tobacco smoke exposure.[119][120] Biochemical tests are a much more reliable biomarker of secondhand smoke exposure than surveys. Certain groups of people are reluctant to disclose their smoking status and exposure to tobacco smoke, especially pregnant women and parents of young children. This is due to their smoking being socially unacceptable. Also, it may be difficult for individuals to recall their exposure to tobacco smoke.[121]
A 2007 study in the Addictive Behaviors journal found a positive correlation between secondhand tobacco smoke exposure and concentrations of nicotine and/or biomarkers of nicotine in the body. Significant biological levels of nicotine from secondhand smoke exposure were equivalent to nicotine levels from active smoking and levels that are associated with behaviour changes due to nicotine consumption.[122]
Cotinine
Cotinine, the metabolite of nicotine, is a biomarker of secondhand smoke exposure. Typically, cotinine is measured in the blood, saliva, and urine. Hair analysis has recently become a new, noninvasive measurement technique. Cotinine accumulates in hair during hair growth, which results in a measure of long-term, cumulative exposure to tobacco smoke.[123] Urinary cotinine levels have been a reliable biomarker of tobacco exposure and have been used as a reference in many epidemiological studies.[118] However, cotinine levels found in the urine reflect exposure only over the preceding 48 hours. Cotinine levels of the skin, such as the hair and nails, reflect tobacco exposure over the previous three months and are a more reliable biomarker.[119]
Carbon monoxide (CO)
Carbon monoxide monitored via breath is also a reliable biomarker of secondhand smoke exposure as well as tobacco use. With high sensitivity and specificity, it not only provides an accurate measure, but the test is also non-invasive, highly reproducible, and low in cost. Breath CO monitoring measures the concentration of CO in an exhalation in parts per million, and this can be directly correlated to the blood CO concentration (carboxyhemoglobin).[124] Breath CO monitors can also be used by emergency services to identify patients who are suspected of having CO poisoning.
Pathophysiology
A 2004 study by the International Agency for Research on Cancer of the World Health Organization concluded that non-smokers are exposed to the same carcinogens as active smokers. Sidestream smoke contains more than 4,000 chemicals, including 69 known carcinogens. Of special concern are polynuclear aromatic hydrocarbons, tobacco-specific N-nitrosamines, and aromatic amines, such as 4-aminobiphenyl, all known to be highly carcinogenic. Mainstream smoke, sidestream smoke, and secondhand smoke contain largely the same components, however the concentration varies depending on type of smoke.[2] Several well-established carcinogens have been shown by the tobacco companies' own research to be present at higher concentrations in sidestream smoke than in mainstream smoke.[125]
Secondhand smoke has been shown to produce more particulate-matter (PM) pollution than an idling low-emission diesel engine. In an experiment conducted by the Italian National Cancer Institute, three cigarettes were left smoldering, one after the other, in a 60 m3 garage with a limited air exchange. The cigarettes produced PM pollution exceeding outdoor limits, as well as PM concentrations up to 10-fold that of the idling engine.[126]
Secondhand tobacco smoke exposure has immediate and substantial effects on blood and blood vessels in a way that increases the risk of a heart attack, particularly in people already at risk.[127] Exposure to tobacco smoke for 30 minutes significantly reduces coronary flow velocity reserve in healthy nonsmokers.[128] Secondhand smoke is also associated with impaired vasodilation among adult nonsmokers.[129] Secondhand smoke exposure also affects platelet function, vascular endothelium, and myocardial exercise tolerance at levels commonly found in the workplace.[130]
Pulmonary emphysema can be induced in rats through acute exposure to sidestream tobacco smoke (30 cigarettes per day) over a period of 45 days.[131] Degranulation of mast cells contributing to lung damage has also been observed.[132]
The term "third-hand smoke" was recently coined to identify the residual tobacco smoke contamination that remains after the cigarette is extinguished and secondhand smoke has cleared from the air.[133][134][135] Preliminary research suggests that by-products of third-hand smoke may pose a health risk,[136]though the magnitude of risk, if any, remains unknown. In October 2011, it was reported that Christus St. Frances Cabrini Hospital in Alexandria, Louisiana, would seek to eliminate third-hand smoke beginning in July 2012, and that employees whose clothing smelled of smoke would not be allowed to work. This prohibition was enacted because third-hand smoke poses a special danger for the developing brains of infants and small children.[137]
In 2008, there were more than 161,000 deaths attributed to lung cancer in the United States. Of these deaths, an estimated 10% to 15% were caused by factors other than first-hand smoking; equivalent to 16,000 to 24,000 deaths annually. Slightly more than half of the lung cancer deaths caused by factors other than first-hand smoking were found in nonsmokers. Lung cancer in non-smokers may well be considered one of the most common cancer mortalities in the United States. Clinical epidemiology of lung cancer has linked the primary factors closely tied to lung cancer in non-smokers as exposure to secondhand tobacco smoke, carcinogens including radon, and other indoor air pollutants.[138]
Opinion of public health authorities
There is widespread scientific consensus that exposure to secondhand smoke is harmful.[4] The link between passive smoking and health risks is accepted by every major medical and scientific organisation, including:
- World Health Organization[2]
- U.S. National Institutes of Health[139]
- Centers for Disease Control[140]
- United States Surgeon General[1]
- U.S. National Cancer Institute[141]
- United States Environmental Protection Agency[142]
- California Environmental Protection Agency[16]
- American Heart Association,[143] American Lung Association,[144] and American Cancer Society[145]
- American Medical Association[146]
- American Academy of Pediatrics[147]
- Australian National Health and Medical Research Council[148]
- United Kingdom Scientific Committee on Tobacco and Health[149]
Public opinion
Recent major surveys conducted by the U.S. National Cancer Institute and Centers for Disease Control have found widespread public awareness that secondhand smoke is harmful. In both 1992 and 2000 surveys, more than 80% of respondents agreed with the statement that secondhand smoke was harmful. A 2001 study found that 95% of adults agreed that secondhand smoke was harmful to children, and 96% considered tobacco-industry claims that secondhand smoke was not harmful to be untruthful.[150]
A 2007 Gallup poll found that 56% of respondents felt that secondhand smoke was "very harmful", a number that has held relatively steady since 1997. Another 29% believe that secondhand smoke is "somewhat harmful"; 10% answered "not too harmful", while 5% said "not at all harmful".[151]
Controversy over harm
As part of its attempt to prevent or delay tighter regulation of smoking, the tobacco industry funded a number of scientific studies and, where the results cast doubt on the risks associated with secondhand smoke, sought wide publicity for those results. The industry also funded libertarian and conservative think tanks, such as the Cato Institute in the United States and the Institute of Public Affairs in Australia which criticised both scientific research on passive smoking and policy proposals to restrict smoking.[152][153] New Scientist and the European Journal of Public Health have identified these industry-wide coordinated activities as one of the earliest expressions of corporate denialism. Further, they state that the disinformation spread by the tobacco industry has created a tobacco denialism movement, sharing many characteristics of other forms of denialism, such as HIV-AIDS denialism.[154][155]
Industry-funded studies and critiques
Enstrom and Kabat
A 2003 study by James Enstrom and Geoffrey Kabat, published in the British Medical Journal, argued that the harms of passive smoking had been overstated.[156] Their analysis reported no statistically significant relationship between passive smoking and lung cancer, coronary heart disease (CHD), or chronic obstructive pulmonary disease, though the accompanying editorial noted that "they may overemphasise the negative nature of their findings."[157] This paper was widely promoted by the tobacco industry as evidence that the harms of passive smoking were unproven.[158][159] The American Cancer Society (ACS), whose database Enstrom and Kabat used to compile their data, criticized the paper as "neither reliable nor independent", stating that scientists at the ACS had repeatedly pointed out serious flaws in Enstrom and Kabat's methodology prior to publication.[160] Notably, the study had failed to identify a comparison group of "unexposed" persons.[161]
Enstrom's ties to the tobacco industry also drew scrutiny; in a 1997 letter to Philip Morris, Enstrom requested a "substantial research commitment... in order for me to effectively compete against the large mountain of epidemiologic data and opinions that already exist regarding the health effects of ETS and active smoking."[162] In a US racketeering lawsuit against tobacco companies, the Enstrom and Kabat paper was cited by the US District Court as "a prime example of how nine tobacco companies engaged in criminal racketeering and fraud to hide the dangers of tobacco smoke."[163] The Court found that the study had been funded and managed by the Center for Indoor Air Research,[164] a tobacco industry front group tasked with "offsetting" damaging studies on passive smoking, as well as by Philip Morris who stated that Enstrom's work was "clearly litigation-oriented".[165] A 2005 paper in Tobacco Control argued that the disclosure section in the Enstrom and Kabat BMJ paper, although it met the journal's requirements, "does not reveal the full extent of the relationship the authors had with the tobacco industry."[166]
In 2006, Enstrom and Kabat published a meta-analysis of studies regarding passive smoking and coronary heart disease in which they reported a very weak association between passive smoking and heart disease mortality.[167] They concluded that exposure to secondhand smoke increased the risk of death from CHD by only 5%, although this analysis has been criticized for including two previous industry-funded studies that suffered from widespread exposure misclassification.[6]
Gori
Gio Batta Gori, a tobacco industry spokesman and consultant[168][169][170] and an expert on risk utility and scientific research, wrote in the libertarian Cato Institute's magazine Regulation that "...of the 75 published studies of ETS and lung cancer, some 70% did not report statistically significant differences of risk and are moot. Roughly 17% claim an increased risk and 13% imply a reduction of risk."[171]
Milloy
Steven Milloy, the "junk science" commentator for Fox News and a former Philip Morris consultant,[172][173] claimed that "of the 19 studies" on passive smoking "only 8— slightly more than 42%— reported statistically significant increases in heart disease incidence."[174]
Another component of criticism cited by Milloy focused on relative risk and epidemiological practices in studies of passive smoking. Milloy, who has a master's degree from the Johns Hopkins School of Hygiene and Public Health, argued that studies yielding relative risks of less than 2 were meaningless junk science. This approach to epidemiological analysis was criticized in the American Journal of Public Health:
A major component of the industry attack was the mounting of a campaign to establish a "bar" for "sound science" that could not be fully met by most individual investigations, leaving studies that did not meet the criteria to be dismissed as "junk science."[175]
The tobacco industry and affiliated scientists also put forward a set of "Good Epidemiology Practices" which would have the practical effect of obscuring the link between secondhand smoke and lung cancer; the privately stated goal of these standards was to "impede adverse legislation".[176] However, this effort was largely abandoned when it became clear that no independent epidemiological organization would agree to the standards proposed by Philip Morris et al.[177]
Levois and Layard
In 1995, Levois and Layard, both tobacco industry consultants, published two analyses in the journal Regulatory Toxicology and Pharmacology regarding the association between spousal exposure to secondhand smoke and heart disease. Both of these papers reported no association between secondhand smoke and heart disease.[178][179] These analyses have been criticized for failing to distinguish between current and former smokers, despite the fact that former smokers, unlike current ones, are not at a significantly increased risk of heart disease.[6][180]
World Health Organization controversy
A 1998 study by the International Agency for Research on Cancer (IARC) on environmental tobacco smoke (ETS) found "weak evidence of a dose–response relationship between risk of lung cancer and exposure to spousal and workplace ETS."[181]
In March 1998, before the study was published, reports appeared in the media alleging that the IARC and the World Health Organization (WHO) were suppressing information. The reports, appearing in the British Sunday Telegraph[182] and The Economist,[183] among other sources,[184][185][186] alleged that the WHO withheld from publication of its own report that supposedly failed to prove an association between passive smoking and a number of other diseases (lung cancer in particular).
In response, the WHO issued a press release stating that the results of the study had been "completely misrepresented" in the popular press and were in fact very much in line with similar studies demonstrating the harms of passive smoking.[187] The study was published in the Journal of the National Cancer Institute in October of the same year, and concluded the authors found "no association between childhood exposure to ETS and lung cancer risk" but "did find weak evidence of a dose–response relationship between risk of lung cancer and exposure to spousal and workplace ETS."[181] An accompanying editorial summarized:
When all the evidence, including the important new data reported in this issue of the Journal, is assessed, the inescapable scientific conclusion is that ETS is a low-level lung carcinogen.[188]
With the release of formerly classified tobacco industry documents through the Tobacco Master Settlement Agreement, it was found (by Elisa Ong and Stanton Glantz) that the controversy over the WHO's alleged suppression of data had been engineered by Philip Morris, British American Tobacco, and other tobacco companies in an effort to discredit scientific findings which would harm their business interests.[189] A WHO inquiry, conducted after the release of the tobacco-industry documents, found that this controversy was generated by the tobacco industry as part of its larger campaign to cut the WHO's budget, distort the results of scientific studies on passive smoking, and discredit the WHO as an institution. This campaign was carried out using a network of ostensibly independent front organizations and international and scientific experts with hidden financial ties to the industry.[190]
EPA lawsuit
In 1993, the United States Environmental Protection Agency (EPA) issued a report estimating that 3,000 lung cancer related deaths in the United States were caused by passive smoking annually.[191]
Philip Morris, R.J. Reynolds Tobacco Company, and groups representing growers, distributors and marketers of tobacco took legal action, claiming that the EPA had manipulated this study and ignored accepted scientific and statistical practices.
The United States District Court for the Middle District of North Carolina ruled in favor of the tobacco industry in 1998, finding that the EPA had failed to follow proper scientific and epidemiologic practices and had "cherry picked" evidence to support conclusions which they had committed to in advance.[192] The court stated in part, "EPA publicly committed to a conclusion before research had begun...adjusted established procedure and scientific norms to validate the Agency's public conclusion... In conducting the ETS Risk Assessment, disregarded information and made findings on selective information; did not disseminate significant epidemiologic information; deviated from its Risk Assessment Guidelines; failed to disclose important findings and reasoning..."
In 2002, the EPA successfully appealed this decision to the United States Court of Appeals for the Fourth Circuit. The EPA's appeal was upheld on the preliminary grounds that their report had no regulatory weight, and the earlier finding was vacated.[193]
In 1998, the U.S. Department of Health and Human Services, through the publication by its National Toxicology Program of the 9th Report on Carcinogens, listed environmental tobacco smoke among the known carcinogens, observing of the EPA assessment that "The individual studies were carefully summarized and evaluated."[194]
Tobacco-industry funding of research
The tobacco industry's role in funding scientific research on secondhand smoke has been controversial.[195] A review of published studies found that tobacco-industry affiliation was strongly correlated with findings exonerating secondhand smoke; researchers affiliated with the tobacco industry were 88 times more likely than independent researchers to conclude that secondhand smoke was not harmful.[196] In a specific example which came to light with the release of tobacco-industry documents, Philip Morris executives successfully encouraged an author to revise his industry-funded review article to downplay the role of secondhand smoke in sudden infant death syndrome.[197] The 2006 U.S. Surgeon General's report criticized the tobacco industry's role in the scientific debate:
The industry has funded or carried out research that has been judged to be biased, supported scientists to generate letters to editors that criticized research publications, attempted to undermine the findings of key studies, assisted in establishing a scientific society with a journal, and attempted to sustain controversy even as the scientific community reached consensus.[198]
This strategy was outlined at an international meeting of tobacco companies in 1988, at which Philip Morris proposed to set up a team of scientists, organized by company lawyers, to "carry out work on ETS to keep the controversy alive."[199] All scientific research was subject to oversight and "filtering" by tobacco-industry lawyers:
Philip Morris then expect the group of scientists to operate within the confines of decisions taken by PM scientists to determine the general direction of research, which apparently would then be 'filtered' by lawyers to eliminate areas of sensitivity.[199]
Philip Morris reported that it was putting "...vast amounts of funding into these projects... in attempting to coordinate and pay so many scientists on an international basis to keep the ETS controversy alive."[199]
Tobacco industry response
Measures to tackle secondhand smoke pose a serious economic threat to the tobacco industry, having broadened the definition of smoking beyond a personal habit to something with a social impact. In a confidential 1978 report, the tobacco industry described increasing public concerns about secondhand smoke as "the most dangerous development to the viability of the tobacco industry that has yet occurred."[200] In United States of America v. Philip Morris et al., the District Court for the District of Columbia found that the tobacco industry "... recognized from the mid-1970s forward that the health effects of passive smoking posed a profound threat to industry viability and cigarette profits," and that the industry responded with "efforts to undermine and discredit the scientific consensus that ETS causes disease."[4]
Accordingly, the tobacco industry have developed several strategies to minimise the impact on their business:
- The industry has sought to position the secondhand smoke debate as essentially concerned with civil liberties and smokers' rights rather than with health, by funding groups such as FOREST.[201]
- Funding bias in research;[8] in all reviews of the effects of secondhand smoke on health published between 1980 and 1995, the only factor associated with concluding that secondhand smoke is not harmful was whether an author was affiliated with the tobacco industry.[196] However, not all studies that failed to find evidence of harm were by industry-affiliated authors.
- Delaying and discrediting legitimate research (see[8] for an example of how the industry attempted to discredit Takeshi Hirayama's landmark study, and[202] for an example of how it attempted to delay and discredit a major Australian report on passive smoking)
- Promoting "good epidemiology" and attacking so-called junk science (a term popularised by industry lobbyist Steven Milloy): attacking the methodology behind research showing health risks as flawed and attempting to promote sound science. Ong & Glantz (2001) cite an internal Phillip Morris memo giving evidence of this as company policy.[177]
- Creation of outlets for favourable research. In 1989, the tobacco industry established the International Society of the Built Environment, which published the peer-reviewed journal Indoor and Built Environment. This journal did not require conflict-of-interest disclosures from its authors. With documents made available through the Master Settlement, it was found that the executive board of the society and the editorial board of the journal were dominated by paid tobacco-industry consultants. The journal published a large amount of material on passive smoking, much of which was "industry-positive".[203]
Citing the tobacco industry's production of biased research and efforts to undermine scientific findings, the 2006 U.S. Surgeon General's report concluded that the industry had "attempted to sustain controversy even as the scientific community reached consensus... industry documents indicate that the tobacco industry has engaged in widespread activities... that have gone beyond the bounds of accepted scientific practice."[204] The U.S. District Court, in U.S.A. v. Philip Morris et al., found that "...despite their internal acknowledgment of the hazards of secondhand smoke, Defendants have fraudulently denied that ETS causes disease."[205]
Position of major tobacco companies
The positions of major tobacco companies on the issue of secondhand smoke is somewhat varied. In general, tobacco companies have continued to focus on questioning the methodology of studies showing that secondhand smoke is harmful. Some (such as British American Tobacco and Philip Morris) acknowledge the medical consensus that secondhand smoke carries health risks, while others continue to assert that the evidence is inconclusive. Several tobacco companies advocate the creation of smoke-free areas within public buildings as an alternative to comprehensive smoke-free laws.[206]
US racketeering lawsuit against tobacco companies
On September 22, 1999, the U.S. Department of Justice filed a racketeering lawsuit against Philip Morris and other major cigarette manufacturers.[207] Almost 7 years later, on August 17, 2006, U.S. District Court Judge Gladys Kessler found that the Government had proven its case and that the tobacco company defendants had violated the Racketeer Influenced Corrupt Organizations Act (RICO).[4] In particular, Judge Kessler found that PM and other tobacco companies had:
- conspired to minimize, distort and confuse the public about the health hazards of smoking;
- publicly denied, while internally acknowledging, that secondhand tobacco smoke is harmful to nonsmokers, and
- destroyed documents relevant to litigation.
The ruling found that tobacco companies undertook joint efforts to undermine and discredit the scientific consensus that secondhand smoke causes disease, notably by controlling research findings via paid consultants. The ruling also concluded that tobacco companies were fraudulently continuing to deny the health effects of ETS exposure.[4]
On May 22, 2009, a three-judge panel of the U.S. Court of Appeals for the District of Columbia Circuit unanimously upheld the lower court's 2006 ruling.[208][209][210]
Smoke-free laws
As a consequence of the health risks associated with secondhand smoke, many national and local governments have outlawed smoking in indoor public places, including restaurants, cafés, and nightclubs, as well as some outdoor open areas.[211] Ireland was the first country in the world to institute a comprehensive national ban on smoking in all indoor workplaces on 29 March 2004. Since then, many others have followed suit. The countries which have ratified the WHO Framework Convention on Tobacco Control (FCTC) have a legal obligation to implement effective legislation "for protection from exposure to tobacco smoke in indoor workplaces, public transport, indoor public places and, as appropriate, other public places." (Article 8 of the FCTC[212]) The parties to the FCTC have further adopted Guidelines on the Protection from Exposure to secondhand Smoke which state that "effective measures to provide protection from exposure to tobacco smoke ... require the total elimination of smoking and tobacco smoke in a particular space or environment in order to create a 100% smoke-free environment."[213]
Opinion polls have shown considerable support for smoke-free laws. In June 2007, a survey of 15 countries found 80% approval for such laws.[214] A survey in France, reputedly a nation of smokers, showed 70% support.[106]
Effects
Smoking bans by governments result in decreased harm from secondhand smoke, including less admissions for acute coronary syndrome.[215] In the first 18 months after the town of Pueblo, Colorado, enacted a smoke-free law in 2003, hospital admissions for heart attacks dropped 27%. Admissions in neighbouring towns without smoke-free laws showed no change, and the decline in heart attacks in Pueblo was attributed to the resulting reduction in secondhand smoke exposure.[216] A 2004 smoking ban instituted in Massachusetts workplaces decreased workers' secondhand smoke exposure from 8% of workers in 2003 to 5.4% of workers in 2010.[110] A 2016 review also found that bans and policy changes in specific locations such as hospitals or universities can lead to reduced smoking rates. In prison settings bans might lead to reduced mortality and to lower exposure to secondhand smoke.[217]
In 2001, a systematic review for the Guide to Community Preventive Services acknowledged strong evidence of the effectiveness of smoke-free policies and restrictions in reducing expose to secondhand smoke. A follow-up to this review, identified the evidence on which the effectiveness of smoking bans reduced the prevalence of tobacco use. Articles published until 2005, were examined to further support this evidence. The examined studies provided sufficient evidence that smoke-free policies reduce tobacco use among workers when implemented in worksites or by communities.[218]
While a number of studies funded by the tobacco industry have claimed a negative economic impact from smoke-free laws, no independently funded research has shown any such impact. A 2003 review reported that independently funded, methodologically sound research consistently found either no economic impact or a positive impact from smoke-free laws.[219]
Air nicotine levels were measured in Guatemalan bars and restaurants before and after an implemented smoke-free law in 2009. Nicotine concentrations significantly decreased in both the bars and restaurants measured. Also, the employees' support for a smoke-free workplace substantially increased in the post-implementation survey compared to pre-implementation survey.[220]
Public opinion
Recent surveys taken by the Society for Research on Nicotine and Tobacco demonstrate supportive attitudes of the public, towards smoke-free policies in outdoor areas. A vast majority of the public supports restricting smoking in various outdoor settings. The respondents' support for the policies were for varying reasons such as litter control, establishing positive smoke-free role models for youth, reducing youth opportunities to smoke, and avoiding exposure to secondhand smoke.[221]
Alternative forms
Альтернативы законам о запрете курения также предлагались как средство снижения вреда , особенно в барах и ресторанах. Например, критики законов о запрете табачного дыма цитируют исследования, в которых предлагается, чтобы вентиляция была средством снижения содержания загрязняющих веществ табачного дыма и улучшения качества воздуха. [222] Табачная промышленность также активно пропагандирует вентиляцию как альтернативу прямым запретам через сеть якобы независимых экспертов, часто не раскрывающих связей с табачной промышленностью. [223] Однако не все критики связаны с индустрией.
Американское общество инженеров по отоплению, охлаждению и кондиционированию воздуха (ASHRAE) в 2005 году официально пришло к выводу, что, хотя полностью изолированные курительные комнаты действительно устраняют риск для близлежащих зон для некурящих, запрет на курение является единственным средством устранения рисков для здоровья, связанных с воздействием в помещении. . Они также пришли к выводу, что никакая система разбавления или очистки не эффективна для устранения риска. [224] Главный хирург США и Объединенный исследовательский центр Европейской комиссии пришли к аналогичным выводам. [204] [225] В руководящих принципах реализации Рамочной конвенции ВОЗ по борьбе против табака говорится, что инженерные подходы, такие как вентиляция, неэффективны и не защищают от пассивного курения. [213] Однако это не обязательно означает, что такие меры бесполезны для снижения вреда, а лишь то, что они не достигают цели полного снижения воздействия до нуля.
Другие предложили систему продаваемых разрешений на загрязнение от курения, аналогичную системе разрешений на выбросы квотами и торговлей, используемой Агентством по охране окружающей среды США в последние десятилетия для сдерживания других типов загрязнения. [226] Это гарантировало бы, что часть баров/ресторанов в юрисдикции будет свободной от курения, оставив при этом решение на усмотрение рынка.
У животных
Было проведено множество исследований для определения канцерогенности табачного дыма из окружающей среды для животных. Эти исследования обычно подпадают под категории моделирования табачного дыма в окружающей среде, введения конденсатов побочного дыма или наблюдательных исследований рака среди домашних животных.
Чтобы имитировать табачный дым в окружающей среде, ученые подвергают животных воздействию побочного дыма, который исходит от горящего конуса сигареты и через ее бумагу, или комбинации основного и побочного дыма. [2] В монографиях IARC делается вывод, что у мышей, подвергшихся длительному воздействию искусственного табачного дыма в окружающей среде, то есть по шесть часов в день, пять дней в неделю, в течение пяти месяцев с последующим четырехмесячным интервалом перед диссекцией, будет наблюдаться значительно более высокий уровень заболеваемости и множественности опухолей легких. чем в контрольных группах.
В монографиях IARC сделан вывод, что конденсаты побочного дыма оказывают значительно более сильное канцерогенное воздействие на мышей, чем конденсаты основного дыма. [2]
Наблюдательные исследования
Пассивное курение широко признано фактором риска развития рака у домашних животных. [227] Исследование, проведенное Школой ветеринарной медицины Университета Тафтса и Массачусетским университетом в Амхерсте, связало возникновение рака полости рта у кошек с воздействием табачного дыма в окружающей среде через сверхэкспрессию гена p53 . [228] Другое исследование, проведенное в тех же университетах, пришло к выводу, что кошки, живущие с курильщиком, с большей вероятностью заболеют кошачьей лимфомой ; риск увеличивался с увеличением продолжительности воздействия пассивного курения и количества курильщиков в семье. [229] Исследование, проведенное учеными из Университета штата Колорадо , посвященное случаям рака легких у собак, в целом оказалось безрезультатным, хотя авторы сообщили о слабой связи с раком легких у собак, подвергшихся воздействию табачного дыма в окружающей среде. Количество курильщиков в доме, количество пачек, выкуриваемых дома в день, и количество времени, которое собака проводила дома, не влияли на риск заболевания раком легких у собаки. [230]
См. также
Ссылки
- ^ Jump up to: а б с д и «Последствия непроизвольного воздействия табачного дыма на здоровье: отчет главного хирурга» (PDF) . Главный хирург США . 27 июня 2006 г. Архивировано из оригинала (PDF) 26 февраля 2019 г. Проверено 24 июля 2012 г.
Пассивное курение вызывает преждевременную смерть и болезни у детей и взрослых, которые не курят.
- ^ Jump up to: а б с д и ж г час я дж к IARC 2004 «Имеется достаточно доказательств того, что принудительное курение (воздействие пассивного или «экологического» табачного дыма) вызывает рак легких у людей»
- ^ «Табак» . www.who.int . Проверено 24 февраля 2024 г.
- ^ Jump up to: а б с д и ж Кесслер 2006 г.
- ^ Самет Дж. М. (2008). «Пассивное курение: факты и ложь» . Salud Pública de México . 50 (5): 428–34. дои : 10.1590/S0036-36342008000500016 . ПМИД 18852940 .
- ^ Jump up to: а б с д Тонг, Элиза К.; Гланц, Стэнтон А. (16 октября 2007 г.). «Усилия табачной промышленности, подрывающие доказательства связи пассивного курения с сердечно-сосудистыми заболеваниями» . Тираж . 116 (16): 1845–1854. doi : 10.1161/CIRCULATIONAHA.107.715888 . ПМИД 17938301 . S2CID 4021497 .
- ^ «CDC – Информационный бюллетень – Политика по созданию бездымной среды сокращает курение – Курение и употребление табака» . Курение и употребление табака . Проверено 24 апреля 2015 г.
- ^ Jump up to: а б с Дитхельм, Паскаль; Макки, Мартин (2006). Снятие дымовой завесы: стратегия табачной промышленности по борьбе с политикой и законодательством, запрещающим курение (PDF) . п. 5. ISBN 978-1-904097-57-0 . OCLC 891398524 .
Отрасль быстро поняла, что для дальнейшего процветания крайне важно, чтобы исследования не доказывали, что табачный дым является опасным загрязнителем воздуха в обществе. Это требование было центральным элементом политики пассивного курения с начала 1970-х годов до наших дней.
- ^ Тыква, Кэтрин (2014). «Фриц Ликинт» . «Ланцет». Респираторная медицина . 2 (5). Ланцет : 358–359. дои : 10.1016/S2213-2600(14)70064-5 . ПМИД 24726404 . Проверено 7 декабря 2023 г.
- ^ «Глава 32 История табака» (PDF) . www.afro.who.int . Всемирная организация здравоохранения . 2017 . Проверено 7 декабря 2023 г.
- ^ Броули, Отис В.; Глинн, Томас Дж.; Хури, Фадло Р.; Вендер, Ричард К. (18 ноября 2013 г.). «Первый доклад генерального хирурга о курении и здоровье: 50-летие» . КА . 64 (1): 5–8. дои : 10.3322/caac.21210 . ПМИД 24249254 .
- ^ «Влияние пассивного курения на здоровье» . Агентство по охране окружающей среды США. Архивировано из оригинала 5 сентября 2015 года . Проверено 6 сентября 2015 г.
- ^ Jump up to: а б Чепмен, С. (1 июня 2003 г.). «Чужой дым: что в имени?» . Контроль над табаком . 12 (2): 113–4. дои : 10.1136/tc.12.2.113 . ПМЦ 1747703 . ПМИД 12773710 .
- ^ Jump up to: а б Протано, Кармела; Виталий, Маттео (1 октября 2011 г.). «Новая опасность пассивного курения: почему пассивное курение не ограничивается пассивным курением» . Перспективы гигиены окружающей среды . 119 (10): а422. дои : 10.1289/ehp.1103956 . ПМК 3230455 . ПМИД 21968336 .
- ^ МАИР 2004 , стр. 1191: «При курении сигарет, сигар, трубок и других табачных изделий, кроме основного потока дыма, втягиваемого и вдыхаемого курильщиками, между затяжками в воздух из горящего конуса выделяется струя дыма. После выпуска этот поток (также известный как побочный дым) смешивается с выдыхаемым основным потоком дыма, а также с воздухом в помещении, образуя пассивный дым, из которого..."
- ^ Jump up to: а б с д и Калифорнийское агентство по охране окружающей среды: Совет по воздушным ресурсам (24 июня 2005 г.). Предлагаемая идентификация табачного дыма в окружающей среде как токсичного загрязнителя воздуха (отчет).
- ^ Главный хирург, 2006 , стр. 30–46.
- ^ «Факты о пассивном курении (SHS)» . CDC . 5 января 2021 г. Проверено 5 августа 2021 г.
- ^ Альберг, Энтони Дж.; Брок, Малкольм В.; Форд, Джин Г.; Самет, Джонатан М.; Спивак, Саймон Д. (1 мая 2013 г.). «Эпидемиология рака легких» . Грудь . 143 (5_дополнение): e1S – e29S. дои : 10.1378/сундук.12-2345 . ПМК 4694610 . ПМИД 23649439 .
- ^ Бхатнагар, А; Уитсел, LP; Рибисл, К.М.; Буллен, К; Чалупка, Ф; Фортепиано, MR; Робертсон, РМ; Маколи, Т; Гофф, Д; Беновиц, Н.; Координационный комитет Американской кардиологической ассоциации, Совет по сердечно-сосудистым заболеваниям и сестринскому делу при инсульте, Совет по клинической кардиологии и Совет по качеству медицинской помощи и результатам исследований (14 октября 2014 г.). «Электронные сигареты: политическое заявление Американской кардиологической ассоциации» . Тираж . 130 (16): 1418–36. doi : 10.1161/CIR.0000000000000107 . ПМЦ 7643636 . ПМИД 25156991 . S2CID 16075813 .
- ^ «Влияние пассивного курения на здоровье» . 24 ноября 2014 года . Проверено 30 мая 2015 г.
- ^ Паллис, Афанасиос Г.; Сиригос, Константинос Н. (декабрь 2013 г.). «Рак легких у никогда не куривших: характеристики заболевания и факторы риска» . Критические обзоры по онкологии/гематологии . 88 (3): 494–503. дои : 10.1016/j.critrevonc.2013.06.011 . ISSN 1040-8428 . ПМИД 23921082 .
- ^ Макаку, Алина; Отье, Филипп; Бониоль, Матье; Бойл, Питер (ноябрь 2015 г.). «Активное и пассивное курение и риск рака молочной железы: метаанализ» (PDF) . Исследование и лечение рака молочной железы . 154 (2): 213–224. дои : 10.1007/s10549-015-3628-4 . ПМИД 26546245 . S2CID 4680641 .
- ^ Jump up to: а б с Ли, Чиен-Чанг; Миддо, Николь А.; Хауи, Стивен RC; Эззати, Маджид (7 декабря 2010 г.). «Связь воздействия пассивного курения с детскими инвазивными бактериальными заболеваниями и бактерионосительством: систематический обзор и метаанализ» . ПЛОС Медицина . 7 (12): e1000374. Бибкод : 2015PLoSO..1039907C . doi : 10.1371/journal.pmed.1000374 . ПМК 4595077 . ПМИД 21151890 .
- ^ Камбербэтч, Маркус Дж.; Рота, Маттео; Катто, Джеймс В.Ф.; Ла Веккья, Карло (сентябрь 2016 г.). «Роль табачного дыма в канцерогенезе мочевого пузыря и почек: сравнение воздействий и метаанализ рисков заболеваемости и смертности» (PDF) . Европейская урология . 70 (3): 458–466. дои : 10.1016/j.eururo.2015.06.042 . ПМИД 26149669 .
- ^ Главный хирург 2006 , гл. 8
- ^ Льв, Х; Сан, Дж; Би, Ю; Сюй, М; Лу, Дж; Чжао, Л; Сюй, Ю (15 ноября 2015 г.). «Риск смертности от всех причин и сердечно-сосудистых заболеваний, связанных с пассивным курением: систематический обзор и метаанализ». Международный журнал кардиологии . 199 : 106–15. дои : 10.1016/j.ijcard.2015.07.011 . ПМИД 26188829 .
- ^ Динас, ПК; Кутедакис, Ю; Флорис, AD (20 февраля 2013 г.). «Влияние активного и пассивного курения сигарет на вариабельность сердечного ритма». Международный журнал кардиологии . 163 (2): 109–15. дои : 10.1016/j.ijcard.2011.10.140 . ПМИД 22100604 .
- ^ Цзоу, Н; Хонг, Дж; Дай, Кнессет (20 февраля 2009 г.). «Пассивное курение сигарет вызывает воспалительное поражение стенок артерий человека» . Китайский медицинский журнал . 122 (4): 444–448. doi : 10.3760/cma.j.issn.0366-6999.2009.04.0016 . ПМИД 19302752 .
- ^ Ооно, ИП; Маккей, DF; Пелл, JP (декабрь 2011 г.). «Метаанализ связи между пассивным курением и инсультом» . Журнал общественного здравоохранения . 33 (4): 496–502. doi : 10.1093/pubmed/fdr025 . ПМИД 21422014 .
- ^ Главный хирург, 2006 , стр. 555–8.
- ^ Бентаеб, Малек; Симони, Марция; Норбак, Дэн; Бальдаччи, Сандра; Майо, Сара; Вьеги, Джованни; Аннеси-Маэсано, Изабелла (6 декабря 2013 г.). «Загрязнение воздуха в помещении и здоровье органов дыхания пожилых людей». Журнал экологических наук и здоровья, часть A. 48 (14): 1783–1789. дои : 10.1080/10934529.2013.826052 . ПМИД 24007433 . S2CID 41862447 .
- ^ Догар, ОФ; Пиллаи, Н.; Сафдар, Н.; Шах, СК; Захид, Р.; Сиддики, К. (ноябрь 2015 г.). «Пассивное курение и риск туберкулеза: систематический обзор и метаанализ» . Эпидемиология и инфекции . 143 (15): 3158–3172. дои : 10.1017/S0950268815001235 . ПМЦ 9150979 . ПМИД 26118887 . S2CID 206285892 .
- ^ Ура, Кевин; Лян, Джонатан; Лин, Сандра Ю. (январь 2014 г.). «Роль пассивного курения при синусите: систематический обзор: синусит и пассивное курение» . Международный форум аллергологии и ринологии . 4 (1): 22–28. дои : 10.1002/alr.21232 . ПМИД 24574074 . S2CID 9537143 .
- ^ Чен, Р; Ху, З; Ортон, С; Чен, РЛ; Вэй, Л. (декабрь 2013 г.). «Связь пассивного курения с когнитивными нарушениями у некурящих пожилых людей: систематический обзор литературы и новое исследование китайской когорты». Журнал гериатрической психиатрии и неврологии . 26 (4): 199–208. дои : 10.1177/0891988713496165 . hdl : 2436/621630 . ПМИД 23877565 . S2CID 43097513 .
- ^ Линг, Джонатан; Хеффернан, Томас (24 марта 2016 г.). «Когнитивный дефицит, связанный с пассивным курением» . Границы в психиатрии . 7 : 46. doi : 10.3389/fpsyt.2016.00046 . ПМК 4805605 . ПМИД 27047401 .
- ^ Цзэн, Ян-Ни; Ли, Я-Мин (10 декабря 2015 г.). «Воздействие пассивного курения и психическое здоровье взрослых: метаанализ перекрестных исследований». Социальная психиатрия и психиатрическая эпидемиология . 51 (9): 1339–48. дои : 10.1007/s00127-015-1164-5 . ПМИД 26661619 . S2CID 7772929 .
- ^ Пинелес, БЛ; Парк, Э.; Самет, Дж. М. (10 февраля 2014 г.). «Систематический обзор и метаанализ выкидыша и воздействия табачного дыма на мать во время беременности» . Американский журнал эпидемиологии . 179 (7): 807–823. дои : 10.1093/aje/kwt334 . ПМЦ 3969532 . ПМИД 24518810 .
- ^ Главный хирург, 2006 , стр. 198–205.
- ^ Кюи, Х; Гонг, ТТ; Лю, CX; Ву, QJ (25 января 2016 г.). «Связь между пассивным материнским курением во время беременности и преждевременными родами: данные метаанализа наблюдательных исследований» . ПЛОС ОДИН . 11 (1): e0147848. Бибкод : 2016PLoSO..1147848C . дои : 10.1371/journal.pone.0147848 . ПМК 4726502 . ПМИД 26808045 .
- ^ Главный хирург, 2006 , стр. 194–7.
- ^ Был, Джаспер; Нурматов, УБ; Кокс, Б; Наврот, Т.С.; Ван Шайк, CP; Шейх, А. (28 марта 2014 г.). «Влияние законодательства о бездымной среде на перинатальное и детское здоровье: систематический обзор и метаанализ». Ланцет . 383 (9928): 1549–60. дои : 10.1016/S0140-6736(14)60082-9 . ПМИД 24680633 . S2CID 8532979 .
- ^ Леонарди-Би, Дж; Бриттон, Дж; Венн, А. (апрель 2011 г.). «Пассивное курение и неблагоприятные последствия для плода у некурящих беременных женщин: метаанализ». Педиатрия . 127 (4): 734–41. дои : 10.1542/пед.2010-3041 . ПМИД 21382949 . S2CID 19866471 .
- ^ Салмаси Дж., Грейди Р., Джонс Дж., Макдональд С.Д. (2010). «Воздействие табачного дыма на окружающую среду и перинатальные исходы: систематический обзор и метаанализ» . Acta Obstet Gynecol Scand . 89 (4): 423–41. дои : 10.3109/00016340903505748 . ПМИД 20085532 . S2CID 9206564 .
- ^ Ван, Мэн; Ван, Чжи-Пин; Чжан, Мэн; Чжао, Чжун-Тан (13 августа 2013 г.). «Пассивное курение матери во время беременности и дефекты нервной трубки у потомства: метаанализ». Архив гинекологии и акушерства . 289 (3): 513–521. дои : 10.1007/s00404-013-2997-3 . ПМИД 23942772 . S2CID 6526042 .
- ^ Янсон С (2004). «Влияние пассивного курения на здоровье органов дыхания у детей и взрослых». Int J Tuberc Lung Dis . 8 (5): 510–6. ПМИД 15137524 .
- ^ Саулите, Юргита; Регейра, Карлос; Монтес-Мартинес, Агустин; Худяков, Полина; Таккуче, Бахи; Новотный, Томас Э. (11 марта 2014 г.). «Активное или пассивное воздействие табакокурения и аллергический ринит, аллергический дерматит и пищевая аллергия у взрослых и детей: систематический обзор и метаанализ» . ПЛОС Медицина . 11 (3): e1001611. дои : 10.1371/journal.pmed.1001611 . ПМЦ 3949681 . ПМИД 24618794 .
- ^ Вэй, Х; Э, М; Ю, С (январь 2015 г.). «Метаанализ пассивного курения и риска развития сахарного диабета 2 типа». Исследования диабета и клиническая практика . 107 (1): 9–14. дои : 10.1016/j.diabres.2014.09.019 . ПМИД 25488377 .
- ^ Ван, Ю; Джи, Дж; Лю, Ю.Дж.; Дэн, X; Он, QQ (2013). «Пассивное курение и риск диабета 2 типа: метаанализ проспективных когортных исследований» . ПЛОС ОДИН . 8 (7): е69915. Бибкод : 2013PLoSO...869915W . дои : 10.1371/journal.pone.0069915 . ПМЦ 3724674 . ПМИД 23922856 .
- ^ Солнце, К; Лю, Д; Ван, К; Рен, М; Ян, С; Ян, Л. (ноябрь 2014 г.). «Пассивное курение и риск диабета: метаанализ проспективных исследований». Эндокринный . 47 (2): 421–7. дои : 10.1007/s12020-014-0194-1 . ПМИД 24532101 . S2CID 3276501 .
- ^ Пан, Ан; Ван, Йели; Талаи, Мохаммед; Ху, Фрэнк Б; У, Танчунь (декабрь 2015 г.). «Связь активного, пассивного курения и отказа от курения с диабетом 2 типа: систематический обзор и метаанализ» . Журнал «Диабет и эндокринология» . 3 (12): 958–967. дои : 10.1016/S2213-8587(15)00316-2 . ПМК 4656094 . ПМИД 26388413 .
- ^ Акинкугбе, Адеронке А.; Слэйд, Гэри Д.; Диварис, Кимон; Пул, Чарльз (ноябрь 2016 г.). «Систематический обзор и метаанализ связи между воздействием табачного дыма в окружающей среде и конечными показателями пародонтита среди некурящих» . Исследования никотина и табака . 18 (11): 2047–56. дои : 10.1093/ntr/ntw105 . ПМК 5055738 . ПМИД 27083214 .
- ^ Гланц С.А., Пармли В.В. (1991). «Пассивное курение и болезни сердца. Эпидемиология, физиология и биохимия» . Тираж . 83 (1): 1–12. дои : 10.1161/01.cir.83.1.1 . ПМИД 1984876 .
- ^ Тейлор А.Э., Джонсон, округ Колумбия, Каземи Х (1992). «Табачный дым в окружающей среде и сердечно-сосудистые заболевания. Документ с изложением позиции Совета по сердечно-легочной и интенсивной терапии Американской кардиологической ассоциации» . Тираж . 86 (2): 699–702. дои : 10.1161/01.cir.86.2.699 . ПМИД 1638735 .
- ^ Главный хирург, 2006 , стр. 376–380.
- ^ «Пассивное курение» . Сайт ВОЗ . Проверено 24 апреля 2015 г.
- ^ «Последний вздох» . Экономист . 19 июля 2017 года . Проверено 20 июля 2017 г.
- ^ Кантор, Р; Ким, А; Тиссен, JP; Сильверберг, Дж.И. (декабрь 2016 г.). «Связь атопического дерматита с курением: систематический обзор и метаанализ» . Журнал Американской академии дерматологии . 75 (6): 1119–1125.e1. дои : 10.1016/j.jaad.2016.07.017 . ПМК 5216172 . ПМИД 27542586 .
- ^ Андерсон, HR; Кук, генеральный директор (ноябрь 1997 г.). «Пассивное курение и синдром внезапной детской смерти: обзор эпидемиологических данных» . Торакс . 52 (11): 1003–9. дои : 10.1136/thx.52.11.1003 . ПМК 1758452 . ПМИД 9487351 .
- ^ Главный хирург 2006 , с. 194
- ^ Jump up to: а б «Информационный бюллетень о пассивном курении и детях», Американская ассоциация легких , август 2006 г.
- ^ Главный хирург, 2006 , стр. 311–9.
- ^ Ворк К.Л., Бродвин Р.Л., Блейсделл Р.Дж. (2007). «Развитие астмы в детстве в результате воздействия пассивного табачного дыма: выводы метарегрессии» . Окружающая среда. Перспектива здоровья. 115 (10): 1394–400. дои : 10.1289/ehp.10155 . ПМК 2022647 . ПМИД 17938726 .
- ^ Тинуойе, О.; Пелл, JP; Маккей, ДФ (28 марта 2013 г.). «Метаанализ связи между воздействием пассивного курения и детской астмой, диагностированной врачом». Исследования никотина и табака . 15 (9): 1475–1483. дои : 10.1093/ntr/ntt033 . ПМИД 23539174 .
- ^ Ван, Чжэнь; Мэй, Сара М.; Чароенлап, Сувани; Пайл, Риган; Отт, Нэнси Л.; Мохаммед, Халед; Джоши, Авни Ю. (ноябрь 2015 г.). «Влияние пассивного курения на заболеваемость астмой и обращение за медицинской помощью у детей: систематический обзор и метаанализ» . Анналы аллергии, астмы и иммунологии . 115 (5): 396–401.e2. дои : 10.1016/j.anai.2015.08.005 . ПМИД 26411971 .
- ^ де Йонгсте Дж. К., Шилдс, доктор медицины (2003). «Кашель • 2: Хронический кашель у детей» . Торакс . 58 (11): 998–1003. дои : 10.1136/торакс.58.11.998 . ПМК 1746521 . ПМИД 14586058 .
- ^ Дайбинг Э., Саннер Т. (1999). «Пассивное курение, синдром внезапной детской смерти (СВДС) и детские инфекции». Hum Exp Токсикол . 18 (4): 202–5. дои : 10.1191/096032799678839914 . ПМИД 10333302 . S2CID 21365217 .
- ^ Jump up to: а б с ДиФранца-младший, Элин К.А., Вейцман М. (2004). «Пренатальное и послеродовое воздействие табачного дыма на окружающую среду и здоровье детей» . Педиатрия . 113 (4 приложения): 1007–15. дои : 10.1542/peds.113.S3.1007 . ПМИД 15060193 . S2CID 248349 .
- ^ Jump up to: а б Хацимихаэль, А; Цалкидис, А; Кассимос, Д; Гардикис, С; Трипсианис, Г; Дефтереос, С; Ктениду-Картали, С; Цанакас, я (июнь 2007 г.). «Роль грудного вскармливания и пассивного курения в развитии тяжелого бронхиолита у детей раннего возраста» . Минерва Педиатрика . 59 (3): 199–206. ПМИД 17519864 .
- ^ Jump up to: а б Предотвращение курения и воздействия пассивного курения до, во время и после беременности. Архивировано 11 сентября 2011 г. в Wayback Machine . Центры по контролю и профилактике заболеваний. Июль 2007.
- ^ Джафта, Н.; Джина, премьер-министр; Баррегард, Л; Найду, Р.Н. (май 2015 г.). «Детский туберкулез и воздействие загрязнения воздуха в помещениях: систематический обзор и метаанализ». Международный журнал туберкулеза и болезней легких . 19 (5): 596–602. дои : 10.5588/ijtld.14.0686 . ПМИД 25868030 .
- ^ Фелешко, Ж; Рущинский, М; Яворска, Дж; Стржелак, А; Залевский, Б.М.; Кулус, М. (ноябрь 2014 г.). «Воздействие табачного дыма на окружающую среду и риск аллергической сенсибилизации у детей: систематический обзор и метаанализ». Архив болезней в детстве . 99 (11): 985–92. doi : 10.1136/archdischild-2013-305444 . ПМИД 24958794 . S2CID 206856566 .
- ^ Саббах, HJ; Хасан, Миннесота; Иннес, Северная Каролина; Элькодари, ХМ; Литтл, Дж; Мосси, Пенсильвания (2015). «Пассивное курение в этиологии несиндромальных орофациальных расщелин: систематический обзор и метаанализ» . ПЛОС ОДИН . 10 (3): e0116963. Бибкод : 2015PLoSO..1016963S . дои : 10.1371/journal.pone.0116963 . ПМЦ 4356514 . ПМИД 25760440 .
- ^ Пагани, Линда С. (июль 2014 г.). «Воздействие табачного дыма на окружающую среду и развитие мозга: случай синдрома дефицита внимания / гиперактивности». Неврологические и биоповеденческие обзоры . 44 : 195–205. doi : 10.1016/j.neubiorev.2013.03.008 . ПМИД 23545330 . S2CID 20470659 .
- ^ «Заявление о научном консенсусе в отношении факторов окружающей среды, связанных с нарушениями нервного развития» (PDF) . Совместная инициатива по вопросам здоровья и окружающей среды в области обучения и развития. 1 июля 2008 г. Архивировано из оригинала (PDF) 27 марта 2009 г.
- ^ Чен, Руолин; Клиффорд, Анджела; Ланг, Линда; Ансти, Каарин Дж. (октябрь 2013 г.). «Связано ли воздействие пассивного курения с когнитивными параметрами детей и подростков? — систематический обзор литературы» . Анналы эпидемиологии . 23 (10): 652–661. doi : 10.1016/j.annepidem.2013.07.001 . hdl : 1885/10932 . ПМИД 23969303 .
- ^ Авшар, А.; Дарка, О.; Топалоглу, Б.; Бек, Ю. (октябрь 2008 г.). «Связь пассивного курения с кариесом и связанными с ним биомаркерами слюны у маленьких детей». Архивы оральной биологии . 53 (10): 969–974. дои : 10.1016/j.archorlbio.2008.05.007 . ПМИД 18672230 .
- ^ Главный хирург, 2006 , стр. 293–309.
- ^ Джонс, Лаура Л.; Хассаниен, А; Кук, генеральный директор; Бриттон, Дж; Леонарди-Би, Дж. (1 января 2012 г.). «Родительское курение и риск заболеваний среднего уха у детей: систематический обзор и метаанализ» . Архив педиатрии и подростковой медицины . 166 (1): 18–27. doi : 10.1001/archpediatrics.2011.158 . ПМИД 21893640 .
- ^ Ли, Чиен-Чанг; Миддо, Николь А.; Хауи, Стивен RC; Эззати, Маджид; Ланфир, Брюс П. (7 декабря 2010 г.). «Связь воздействия пассивного курения с детскими инвазивными бактериальными заболеваниями и бактерионосительством: систематический обзор и метаанализ» . ПЛОС Медицина . 7 (12): e1000374. doi : 10.1371/journal.pmed.1000374 . ПМК 2998445 . ПМИД 21151890 .
- ^ Чизуэлл, К; Акрам, Ю (февраль 2017 г.). «Влияние воздействия табачного дыма на результаты анестезии и хирургических операций у детей: систематический обзор и метаанализ» . Архив болезней в детстве . 102 (2): 123–130. doi : 10.1136/archdischild-2016-310687 . ПМК 5284464 . ПМИД 27417307 .
- ^ Хара, С.М.; Бенке, младший; Лин, С.Ю.; Ишман, С.Л. (январь 2015 г.). «Связь между пассивным курением и нарушением дыхания во сне у детей: систематический обзор». Ларингоскоп . 125 (1): 241–7. дои : 10.1002/lary.24833 . ПМИД 25130300 . S2CID 23401780 .
- ^ Рагхувир, Гита; Уайт, Дэвид А.; Хейман, Лаура Л.; Ву, Джессика Дж.; Виллафане, Хуан; Селермайер, Дэвид; Уорд, Кеннет Д.; де Ферранти, Сара Д.; Захария, Джастин (18 октября 2016 г.). «Сердечно-сосудистые последствия пассивного воздействия табачного дыма в детстве: преобладающие данные, бремя, а также расовые и социально-экономические различия: научное заявление Американской кардиологической ассоциации» . Тираж . 134 (16): e336–59. doi : 10.1161/CIR.0000000000000443 . ПМК 5207215 . ПМИД 27619923 .
- ^ Стинленд, К. (1 января 1992 г.). «Пассивное курение и риск сердечно-сосудистых заболеваний». ДЖАМА . 267 (1): 94–99. дои : 10.1001/jama.267.1.94 . ПМИД 1727204 .
- ^ Закон, MR; Моррис, Дж. К.; Уолд, Нью-Джерси (18 октября 1997 г.). «Воздействие табачного дыма на окружающую среду и ишемическая болезнь сердца: оценка доказательств» . БМЖ . 315 (7114): 973–980. дои : 10.1136/bmj.315.7114.973 . ПМК 2127675 . ПМИД 9365294 .
- ^ Тун, М; Хенли, Дж; Апичелла, Л. (декабрь 1999 г.). «Эпидемиологические исследования фатальных и несмертельных сердечно-сосудистых заболеваний и воздействия ETS в результате курения супругов» . Перспективы гигиены окружающей среды . 107 (приложение 6): 841–846. дои : 10.1289/ehp.99107s6841 . JSTOR 3434563 . ПМК 1566204 . ПМИД 10592140 .
- ^ Он, Цзян; Вуппутури, Сума; Аллен, Криста; Прерост, Моника Р.; Хьюз, Джанет; Велтон, Пол К. (25 марта 1999 г.). «Пассивное курение и риск ишемической болезни сердца — метаанализ эпидемиологических исследований» . Медицинский журнал Новой Англии . 340 (12): 920–926. дои : 10.1056/NEJM199903253401204 . ПМИД 10089185 .
- ^ Дитхельм П.А., Риэль Дж.К., Макки М. (2005). «Вся правда и ничего кроме правды? Исследование, которое Филип Моррис не хотела, чтобы вы видели». Ланцет . 366 (9479): 86–92. дои : 10.1016/S0140-6736(05)66474-4 . ПМИД 15993237 . S2CID 10442244 .
- ^ Шик С., Гланц С. (2005). «Токсикологические эксперименты Philip Morris со свежим побочным дымом: более токсичны, чем основной дым» . Контроль над табаком . 14 (6): 396–404. дои : 10.1136/tc.2005.011288 . ПМК 1748121 . ПМИД 16319363 .
- ^ Шик С., Гланц С.А. (2006). «Токсичность побочного сигаретного дыма увеличивается с возрастом и продолжительностью воздействия» . Контроль над табаком . 15 (6): 424–9. дои : 10.1136/tc.2006.016162 . ПМЦ 2563675 . ПМИД 17130369 .
- ^ Шик, Сан-Франциско; Гланц, С. (1 августа 2007 г.). «Концентрация канцерогена 4-(Метилнитрозамино)-1-(3-пиридил)-1-бутанона в побочном сигаретном дыме увеличивается после выброса в воздух помещения: результаты неопубликованных исследований табачной промышленности» . Эпидемиология рака, биомаркеры и профилактика . 16 (8): 1547–1553. doi : 10.1158/1055-9965.EPI-07-0210 . ПМИД 17684127 . S2CID 690030 .
- ^ Уинкап, Питер Х; Гилг, Джули А; Эмберсон, Джонатан Р.; Джарвис, Мартин Дж; Фейерабенд, Колин; Брайант, Эндрю; Уокер, Мэри; Кук, Дерек Дж. (24 июля 2004 г.). «Пассивное курение и риск ишемической болезни сердца и инсульта: проспективное исследование с измерением котинина» . БМЖ . 329 (7459): 200–205. дои : 10.1136/bmj.38146.427188.55 . ПМЦ 487731 . ПМИД 15229131 .
- ^ Хэкшоу, АК; Закон, MR; Уолд, Нью-Джерси (18 октября 1997 г.). «Накопленные данные о раке легких и табачном дыме в окружающей среде» . БМЖ . 315 (7114): 980–988. дои : 10.1136/bmj.315.7114.980 . ПМК 2127653 . ПМИД 9365295 .
- ^ Копас, Дж.Б.; Ши, JQ (12 февраля 2000 г.). «Реанализ эпидемиологических данных о раке легких и пассивном курении» . БМЖ . 320 (7232): 417–418. дои : 10.1136/bmj.320.7232.417 . ПМК 27286 . ПМИД 10669446 .
- ^ Такаги, Хисато; Секино, Сейширо; Като, Такаёси; Мацуно, Юкихиро; Умэмото, Такуя (февраль 2006 г.). «Пересмотр данных о раке легких и пассивном курении: корректировка предвзятости публикации с помощью алгоритма «обрезать и заполнить»». Рак легких . 51 (2): 245–246. дои : 10.1016/j.lungcan.2005.11.004 . PMID 16386820 .
- ^ Чжун, Лицзе; Гольдберг, Марк С; Родитель, Мари-Элиза; Хэнли, Джеймс А. (январь 2000 г.). «Воздействие табачного дыма в окружающей среде и риск рака легких: метаанализ». Рак легких . 27 (1): 3–18. дои : 10.1016/s0169-5002(99)00093-8 . ПМИД 10672779 .
- ^ Тейлор, Ричард; Гамминг, Роберт; Вудворд, Алистер; Блэк, Меган (июнь 2001 г.). «Пассивное курение и рак легких: совокупный метаанализ» . Австралийский и новозеландский журнал общественного здравоохранения . 25 (3): 203–211. дои : 10.1111/j.1467-842x.2001.tb00564.x . ПМИД 11494987 . S2CID 25724906 .
- ^ Ким, Клэр Х.; Ли, Юань-Чин Эми; Хунг, Райжан Дж.; Макналлан, Шейла Р.; Кот, Мишель Л.; Лим, Вэй-Йен; Чанг, Шен-Чи; Ким, Джин Хи; Уголини, Донателла; Чен, Ин; Лилоглу, Триантафиллос; Эндрю, Анджелина С.; Онега, Трейси; Дуэлл, Эрик Дж.; Филд, Джон К.; Лазарь, Филипп; Ле Маршан, Лоик; Нери, Моника; Винейс, Паоло; Киёхара, Чикако; Хонг, Юн-Чул; Моргенштерн, Хэл; Мацуо, Кейтаро; Тадзима, Кадзуо; Кристиани, Дэвид С.; Маклафлин, Джон Р.; Бенько, Владимир; Холчатова Ивана; Боффетта, Паоло; Бреннан, Пол; Фабианова, Элеонора; Форетова, Ленка; Жанут, Владимир; Лиссовская, Иоланта; Товарищи, Дана; Руднаи, Питер; Шешеня-Добровская, Неонила; Мукерия, Ануш; Заридзе, Давид; Сью, Аделина; Шварц, Энн Г.; Ян, Пин; Чжан, Цзо-Фэн (15 октября 2014 г.). «Воздействие пассивного табачного дыма и рак легких по гистологическому типу: объединенный анализ Международного консорциума по раку легких (ILCCO): пассивное табачное курение и рак легких» . Международный журнал рака . 135 (8): 1918–1930. дои : 10.1002/ijc.28835 . ПМК 4126868 . ПМИД 24615328 .
- ^ Jump up to: а б Новак К (2007). «Пассивное курение: выход из дымки» . Природа . 447 (7148): 1049–51. Бибкод : 2007Natur.447.1049N . дои : 10.1038/4471049а . ПМИД 17597735 . S2CID 9627500 .
- ^ Бейлар, Джон К. (25 марта 1999 г.). «Пассивное курение, ишемическая болезнь сердца и метаанализ». Медицинский журнал Новой Англии . 340 (12): 958–959. дои : 10.1056/NEJM199903253401211 . ПМИД 10089192 .
- ^ Раупак, Тобиас; Шефер, Катрин; Константинидес, Ставрос; Андреас, Стефан (1 февраля 2006 г.). «Пассивное курение как острая угроза сердечно-сосудистой системе: смена парадигмы» . Европейский кардиологический журнал . 27 (4): 386–392. дои : 10.1093/eurheartj/ehi601 . ПМИД 16230308 .
- ^ Тейлор, Р.; Наджафи, Ф.; Добсон, А. (1 октября 2007 г.). «Метаанализ исследований пассивного курения и рака легких: влияние типа исследования и континента» . Международный журнал эпидемиологии . 36 (5): 1048–1059. дои : 10.1093/ije/dym158 . ПМИД 17690135 .
- ^ Jump up to: а б Стейнер, Лесли; Бена, Джеймс; Саско, Энни Дж.; Смит, Рэндалл; Стинленд, Кайл; Крейцер, Микаэла; Стрейф, Курт (март 2007 г.). «Риск рака легких и воздействие табачного дыма на рабочем месте» . Американский журнал общественного здравоохранения . 97 (3): 545–551. дои : 10.2105/AJPH.2004.061275 . ПМК 1805004 . ПМИД 17267733 .
- ^ «Влияние загрязнения воздуха внутри помещений на здоровье» . Архивировано из оригинала 5 августа 2006 г. Проверено 26 июля 2006 г.
- ^ Вирт, Н.; Абу-Хамдан, К.; Спиноза, А.; Бохадана, А.; Мартине, Ю. (март 2005 г.). «Пассивное курение». Revue de Pneumologie Clinique (на французском языке). 61 (1): 7–15. дои : 10.1016/s0761-8417(05)84776-5 . ПМИД 15772574 .
- ^ Jump up to: а б «Франция запретит курение в общественных местах» . Би-би-си . 08.10.2006 . Проверено 9 октября 2006 г.
- ^ Мейерс, Дэвид Г.; Нойбергер, Джон С.; Хэ, Цзянхуа (сентябрь 2009 г.). «Сердечно-сосудистое влияние запрета на курение в общественных местах» . Журнал Американского колледжа кардиологов . 54 (14): 1249–1255. дои : 10.1016/j.jacc.2009.07.022 . ПМИД 19778665 .
- ^ Линь, Хуалян; Ван, Хунчун; Ву, Вэй; Ланг, Линлинг; Ван, Циньчжоу; Тиан, Линьвэй (декабрь 2013 г.). «Влияние законодательства о бездымной среде на острый инфаркт миокарда: систематический обзор и метаанализ» . BMC Общественное здравоохранение . 13 (1): 529. дои : 10.1186/1471-2458-13-529 . ПМК 3671962 . ПМИД 23721370 .
- ^ Уэллс, Эй Джей (июль 1998 г.). «Рак легких от пассивного курения на работе» . Американский журнал общественного здравоохранения . 88 (7): 1025–1029. дои : 10.2105/ajph.88.7.1025 . ПМЦ 1508269 . ПМИД 9663148 .
- ^ Jump up to: а б Фицсиммонс, Кэтлин (21 ноября 2013 г.). «Снижение воздействия ETS на работников» . Национальный институт охраны труда и здоровья (NIOSH) . Проверено 14 января 2015 г.
- ^ Управление по охране здоровья от курения (США) (2006 г.). Последствия для здоровья непроизвольного воздействия табачного дыма: доклад главного хирурга . Публикации и отчеты главного хирурга. Центры по контролю и профилактике заболеваний (США). ПМИД 20669524 . Проверено 24 апреля 2015 г.
- ^ Пагмайр, Джулиана; Свитинг, Хелен; Мур, Лоуренс (февраль 2017 г.). «Воздействие табачного дыма на младенцев, детей и молодых людей: сейчас не время расслабляться» . Архив болезней в детстве . 102 (2): 117–118. doi : 10.1136/archdischild-2016-311652 . ПМИД 28100555 . S2CID 41806496 .
- ^ Страчан, ДП; Кук, генеральный директор (октябрь 1997 г.). «Влияние пассивного курения на здоровье. 1. Курение родителей и заболевания нижних дыхательных путей в младенчестве и раннем детстве» . Торакс . 52 (10): 905–914. дои : 10.1136/thx.52.10.905 . ПМЦ 1758431 . ПМИД 9404380 .
- ^ Страчан, ДП; Кук, генеральный директор (1 января 1998 г.). «Влияние пассивного курения на здоровье. 4. Курение родителей, заболевания среднего уха и аденотонзиллэктомия у детей» . Торакс . 53 (1): 50–56. дои : 10.1136/thx.53.1.50 . ПМЦ 1758689 . ПМИД 9577522 .
- ^ Песня, Анна В.; Гланц, Стэнтон А.; Халперн-Фельшер, Бонни Л. (декабрь 2009 г.). «Восприятие рисков пассивного курения предсказывает будущее начало курения подростками» . Журнал здоровья подростков . 45 (6): 618–625. дои : 10.1016/j.jadohealth.2009.04.022 . ПМЦ 2814413 . ПМИД 19931835 .
- ^ «Рамочная конвенция ВОЗ по борьбе против табака (РКБТ ВОЗ)» . www.who.int . Проверено 12 июня 2024 г.
- ^ Цай, Джеймс; Хома, Дэвид М.; Генцке, Андреа С.; Махони, Маргарет; Шарапова, Саида Р.; Соснофф, Конни С.; Кэрон, Кевин Т.; Ван, Ланьцин; Мелстром, Пол С.; Триверс, Катрина Ф. (7 декабря 2018 г.). «Воздействие пассивного курения среди некурящих — США, 1988–2014 гг.» . ММВР. Еженедельный отчет о заболеваемости и смертности . 67 (48): 1342–1346. дои : 10.15585/mmwr.mm6748a3 . ПМК 6329485 . ПМИД 30521502 .
- ^ Jump up to: а б Бехбод, Бехруз; Шарма, Мохит; Бакси, Ручи; Роузби, Роберт; Вебстер, Премила (31 января 2018 г.). «Программы борьбы с курением в семье и среди лиц, осуществляющих уход, для снижения воздействия на детей табачного дыма в окружающей среде» . Кокрейновская база данных систематических обзоров . 1 (1): CD001746. дои : 10.1002/14651858.CD001746.pub4 . ПМК 6491082 . ПМИД 29383710 .
- ^ Jump up to: а б Мец-Фавр С, Донней С, де Блей Ф (февраль 2005 г.). «[Маркеры воздействия табачного дыма в окружающей среде (ETS)]». Преподобный Мал Респир (на французском языке). 22 (1 Пт 1): 81–92. дои : 10.1016/S0761-8425(05)85439-7 . ПМИД 15968761 .
- ^ МакКлюр Дж. Б. (апрель 2002 г.). «Являются ли биомаркеры полезными средствами лечения для содействия изменению поведения в отношении здоровья? Эмпирический обзор». Am J Prev Med . 22 (3): 200–7. дои : 10.1016/S0749-3797(01)00425-1 . ПМИД 11897465 .
- ^ Клессес Р.К., Дебон М., Рэй Дж.В. (октябрь 1995 г.). «Являются ли самоотчеты об уровне курения предвзятыми? Данные Второго национального обследования здоровья и питания». Дж. Клин Эпидемиол . 48 (10): 1225–33. дои : 10.1016/0895-4356(95)00020-5 . ПМИД 7561984 .
- ^ Околи CT, Келли Т., Хан Э.Дж. (октябрь 2007 г.). «Пассивное курение и воздействие никотина: краткий обзор». Поведение наркомана . 32 (10): 1977–88. дои : 10.1016/j.addbeh.2006.12.024 . ПМИД 17270359 .
- ^ Флореску А., Ферренс Р., Эйнарсон Т., Селби П., Солдин О., Корен Г. (февраль 2009 г.). «Методы количественной оценки воздействия курения сигарет и табачного дыма в окружающей среде: внимание к токсикологии развития» . The Drug Monit . 31 (1): 14–30. дои : 10.1097/FTD.0b013e3181957a3b . ПМЦ 3644554 . ПМИД 19125149 .
- ^ Ирвинг Дж. М., Кларк ЕС, Кромби И. К., Смит У. К. (январь 1988 г.). «Оценка портативного средства измерения содержания угарного газа в выдыхаемом воздухе». Предыдущий Мед . 17 (1): 109–15. дои : 10.1016/0091-7435(88)90076-X . ПМИД 3362796 .
- ^ Шик С., Гланц С. (2005). «Токсикологические эксперименты Philip Morris со свежим побочным дымом: более токсичны, чем основной дым» . Тоб. Контроль . 14 (6): 396–404. дои : 10.1136/tc.2005.011288 . ПМК 1748121 . ПМИД 16319363 .
- ^ Инверницци Г., Рупрехт А., Мацца Р. и др. (2004). «Табачные частицы в сравнении с выхлопами дизельных автомобилей: образовательная перспектива» . Контроль над табаком . 13 (3): 219–21. дои : 10.1136/tc.2003.005975 . ПМК 1747905 . ПМИД 15333875 .
- ^ Барная Дж., Гланц С.А. (2005). «Сердечно-сосудистые последствия пассивного курения: почти такие же серьезные, как и курение» . Тираж . 111 (20): 2684–98. doi : 10.1161/CIRCULATIONAHA.104.492215 . ПМИД 15911719 . S2CID 2291566 .
- ^ Оцука Р., Ватанабэ Х., Хирата К. и др. (2001). «Острые последствия пассивного курения на коронарное кровообращение у здоровых молодых людей» . ДЖАМА . 286 (4): 436–41. дои : 10.1001/jama.286.4.436 . ПМИД 11466122 .
- ^ Селермайер, Дэвид С.; Адамс, Марк Р.; Кларксон, Питер; Робинсон, Жаки; МакКреди, Робин; Дональд, Энн; Динфилд, Джон Э. (18 января 1996 г.). «Пассивное курение и нарушение эндотелий-зависимой артериальной дилатации у здоровых молодых людей» . Медицинский журнал Новой Англии . 334 (3): 150–155. дои : 10.1056/NEJM199601183340303 . ПМИД 8531969 .
- ^ Ховард, Дж; Тун, MJ (декабрь 1999 г.). «Почему табачный дым в окружающей среде более сильно связан с ишемической болезнью сердца, чем ожидалось? Обзор потенциальных предубеждений и экспериментальных данных» . Перспективы гигиены окружающей среды . 107 (Приложение 6): 853–8. дои : 10.2307/3434565 . JSTOR 3434565 . ПМК 1566209 . ПМИД 10592142 .
- ^ Сендон, СП; Баттленер, К.; Лоренци-Фильо, Г.; Дольников, М.; Перейра, премьер-министр; Консейсан, GMS; Беппу, ОС; Салдива, PHN (октябрь 1997 г.). «Эмфизема легких, вызванная пассивным курением: экспериментальное исследование на крысах» . Бразильский журнал медицинских и биологических исследований . 30 (10): 1241–1247. дои : 10.1590/s0100-879x1997001000017 . ПМИД 9496445 .
- ^ Эрен, У.; Кум, С.; Сандикчи, М.; Кара, Э. (2006). «Влияние длительного пассивного курения на тучные клетки легких крыс» . Ревю ветеринарной медицины . 6 : 319–322.
- ^ Мэтт Дж.Э., Кинтана П.Дж., Ховелл М.Ф. и др. (март 2004 г.). «Домохозяйства, загрязненные табачным дымом: источники воздействия на младенцев» . Контроль над табаком . 13 (1): 29–37. дои : 10.1136/tc.2003.003889 . ПМЦ 1747815 . ПМИД 14985592 .
- ^ Виникофф Дж.П., Фрибели Дж., Тански С.Е. и др. (январь 2009 г.). «Мнения о влиянии курения из третьих рук на здоровье и запрете на курение в домашних условиях» . Педиатрия . 123 (1): e74–9. дои : 10.1542/пед.2008-2184 . ПМЦ 3784302 . ПМИД 19117850 .
- ^ Рабин, Рони Кэрин (2 января 2009 г.). «Новая опасность сигарет: курение из третьих рук » . Нью-Йорк Таймс . Проверено 12 января 2009 г.
- ^ Сулейман, М.; Гундел, Луизиана; Панков, Дж. Ф.; Джейкоб, П.; Сингер, Британская Колумбия; Детайлатс, Х. (13 апреля 2010 г.). «Образование канцерогенов в помещении в результате поверхностных реакций никотина с азотистой кислотой, что приводит к потенциальной опасности курения от третьих рук» . Труды Национальной академии наук . 107 (15): 6576–6581. дои : 10.1073/pnas.0912820107 . ПМЦ 2872399 . ПМИД 20142504 .
- ↑ Больница Луизианы запретит запах дыма на одежде рабочих , Fox News, 3 октября 2011 г.
- ^ Самет, Дж. М.; Авила-Танг, Э.; Боффетта, П.; Ханнан, LM; Оливо-Марстон, С.; Тун, MJ; Рудин, CM (15 сентября 2009 г.). «Рак легких у никогда не куривших: клиническая эпидемиология и факторы риска окружающей среды» . Клинические исследования рака . 15 (18): 5626–5645. дои : 10.1158/1078-0432.CCR-09-0376 . ПМК 3170525 . ПМИД 19755391 .
- ^ «Экологический табачный дым» (PDF) . 11-й доклад о канцерогенах . США Национальные институты здравоохранения . Архивировано (PDF) из оригинала 16 июля 2008 г. Проверено 27 августа 2007 г.
- ^ «Информационный бюллетень о пассивном курении» . Центры США по контролю и профилактике заболеваний . 21 февраля 2017 г.
- ^ «Влияние на здоровье воздействия табачного дыма» . США Национальный институт рака . Архивировано из оригинала 5 сентября 2007 г. Проверено 22 августа 2007 г.
- ^ «Влияние пассивного курения на здоровье» . Агентство по охране окружающей среды США . Проверено 24 сентября 2007 г.
- ^ «Правда о пассивном курении» . Американская кардиологическая ассоциация . Проверено 27 августа 2007 г.
- ^ «Информационный бюллетень о пассивном курении» . Американская ассоциация легких . Архивировано из оригинала 18 сентября 2007 г. Проверено 24 сентября 2007 г.
- ^ «Пассивное курение» . Американское онкологическое общество . Архивировано из оригинала 14 сентября 2007 г. Проверено 27 августа 2007 г.
- ^ «АМА: Сообщение о пассивном курении Главного хирурга стало тревожным сигналом для законодателей» (пресс-релиз). Американская медицинская ассоциация . Проверено 27 августа 2007 г.
- ^ «Плата за табак: последствия для педиатра» . Американская академия педиатрии . Архивировано из оригинала 15 октября 2007 г. Проверено 2 октября 2007 г.
- ^ «Национальный ответ на пассивное курение в закрытых общественных местах и на рабочих местах» (PDF) . Австралийское национальное партнерство общественного здравоохранения. Ноябрь 2000 г. Архивировано из оригинала (PDF) 12 февраля 2014 г. Проверено 11 сентября 2007 г.
- ^ Научный комитет опубликовал два соответствующих отчета:
- В отчете SCOTH за 1998 год был сделан вывод, что пассивное курение является причиной рака легких, болезней сердца и других проблем со здоровьем.
- Обновление 2004 года, опубликованное SCOTH , заархивировано 6 февраля 2012 года в Wayback Machine , в котором рассматриваются новые данные, опубликованные после отчета 1998 года, обнаружено, что недавние исследования подтвердили первоначально сообщаемую связь между пассивным курением и рисками для здоровья.
- ^ Главный хирург 2006 , с. 588 гл. 10
- ^ Саад, Лидия (25 июля 2007 г.). «Все больше курильщиков чувствуют себя оскорбленными запретом на курение» . Гэллап . Проверено 20 февраля 2015 г.
- ^ « Катон и табачная промышленность ». По состоянию на 8 апреля 2011 г.
- ^ Нахан, Майк. Австралиец , 10 апреля 2000 г.: «IPA поет свою песню».
- ^ Шермер, Майкл (май 2010 г.). «Я скептик, но я не отрицатель». Новый учёный . 206 (2760): 36–37. Бибкод : 2010NewSc.206R..36S . дои : 10.1016/S0262-4079(10)61210-9 .
- ^ Дитхельм, П.; Макки, М. (16 октября 2008 г.). «Дениализм: что это такое и как должны реагировать ученые?» . Европейский журнал общественного здравоохранения . 19 (1): 2–4. дои : 10.1093/eurpub/ckn139 . ПМИД 19158101 . S2CID 8098426 .
- ^ Энстром Дж. Э., Кабат Г. К. (2003). «Табачный дым в окружающей среде и смертность, связанная с табаком, в проспективном исследовании жителей Калифорнии, 1960-98 годы» . БМЖ . 326 (7398): 1057. doi : 10.1136/bmj.326.7398.1057 . ПМК 155687 . ПМИД 12750205 .
- ^ Дэйви Смит Дж. (2003). «Влияние пассивного курения на здоровье: доступно больше информации, но споры все еще сохраняются» . БМЖ . 326 (7398): 1048–9. дои : 10.1136/bmj.326.7398.1048 . ПМЦ 1125974 . ПМИД 12750182 .
- ^ Кесслер 2006 , с. 1383
- ^ Тонг ЭК, Гланц С.А. (2007). «Усилия табачной промышленности подрывают доказательства связи пассивного курения с сердечно-сосудистыми заболеваниями» . Тираж . 116 (16): 1845–54. doi : 10.1161/CIRCULATIONAHA.107.715888 . ПМИД 17938301 . S2CID 4021497 .
- ^ «Американское онкологическое общество осуждает исследование табачной промышленности за неточное использование данных» (PDF) (пресс-релиз). Американское онкологическое общество . 13 мая 2003 г. Проверено 29 августа 2007 г.
- ^ Тун, Майкл Дж. (4 октября 2003 г.). «Более вводящая в заблуждение наука табачной промышленности». БМЖ . 327 (7418): Е237–Е238. дои : 10.1136/bmjusa.03070002 . S2CID 74351979 .
- ^ «Предлагаемое исследование связи низкого уровня активного курения со смертностью: письмо Джеймса Энстрома в научный отдел Philip Morris» . 01.01.1997 . Проверено 29 августа 2007 г.
- ^ Далтон Р. (март 2007 г.). «Исследование пассивного курения подлежит пересмотру» . Природа . 446 (7133): 242. Бибкод : 2007Natur.446..242D . дои : 10.1038/446242а . ПМИД 17361147 . S2CID 27691890 .
- ^ Кесслер 2006 , с. 1380
- ^ Кесслер 2006 , стр. 1380–3.
- ^ Беро, Луизиана; Гланц, С; Хонг, депутат Кнессета (апрель 2005 г.). «Пределы раскрытия конкурирующих интересов» . Контроль над табаком . 14 (2): 118–26. ПМК 1748015 . ПМИД 15791022 .
- ^ Энстром, Дж. Э.; Кабат, GC (март 2006 г.). «Экологический табачный дым и смертность от ишемической болезни сердца в Соединенных Штатах - метаанализ и критика». Ингаляционная токсикология . 18 (3): 199–210. CiteSeerX 10.1.1.495.2191 . дои : 10.1080/08958370500434255 . ПМИД 16399662 . S2CID 7457133 .
- ^ Кесслер 2006 , с. 162
- ^ Соединенные Штаты Америки против Philip Morris et al. , Меморандум о фактах США в соответствии с приказом № 470, раздел V, Окружной суд США по округу Колумбия. п. 44
- ^ НАУЧНЫЕ КОНСУЛЬТАНТЫ ETS / IAQ , из Архива документов по табачным изделиям Legacy. Проверено 19 июля 2007 г.
- ^ Гори, Гио Батта (весна 2007 г.). «Разжигание сфальсифицированного террора пассивного курения» (PDF) . Регулирование . 30 (1): 14–7. Архивировано из оригинала (PDF) 16 января 2009 г.
- ^ Smoked Out: Эксперт по найму , Пол Д. Такер. Опубликовано в The New Republic 26 января 2006 г. Проверено 22 августа 2007 г.
- ^ Бюджет Philip Morris на «Стратегию и социальную ответственность» , в котором Миллой указан как платный консультант. Проверено 22 августа 2007 г.
- ^ «Буконные шутки» , Стивен Миллой . Проверено 31 мая 2013 г.
- ^ Самет Дж. М., Берк Т. А. (2001). «Превращение науки в мусор: табачная промышленность и пассивное курение» . Am J Общественное здравоохранение . 91 (11): 1742–4. дои : 10.2105/AJPH.91.11.1742 . ПМЦ 1446866 . ПМИД 11684591 .
- ^ Научные коммуникации через СМИ [ постоянная мертвая ссылка ] , из архива документов Philip Morris. Проверено 3 октября 2007 г. Также цитируется в Онг, Элиза К.; Гланц, Стэнтон А. (ноябрь 2001 г.). «Создание «надежной науки» и «хорошей эпидемиологии»: табак, юристы и фирмы по связям с общественностью» . Американский журнал общественного здравоохранения . 91 (11): 1749–1757. дои : 10.2105/ajph.91.11.1749 . ПМК 1446868 . ПМИД 11684593 .
- ^ Jump up to: а б Онг ЭК, Гланц С.А. (2001). «Создание «здравой науки» и «хорошей эпидемиологии»: табак, юристы и фирмы по связям с общественностью» . Am J Общественное здравоохранение . 91 (11): 1749–57. дои : 10.2105/AJPH.91.11.1749 . ПМЦ 1446868 . ПМИД 11684593 .
- ^ Лейард, Миссури (февраль 1995 г.). «Ишемическая болезнь сердца и супружеское курение в национальном исследовании смертности». Нормативная токсикология и фармакология . 21 (1): 180–183. дои : 10.1006/rtph.1995.1022 . ПМИД 7784629 .
- ^ Левуа, Мэн; Лейард, Миссури (февраль 1995 г.). «Предвзятость публикаций в эпидемиологической литературе по табачному дыму и ишемической болезни сердца в окружающей среде». Нормативная токсикология и фармакология . 21 (1): 184–191. дои : 10.1006/rtph.1995.1023 . ПМИД 7784630 .
- ^ Закон, Малкольм Р.; Уолд, Николас Дж. (июль 2003 г.). «Экологический табачный дым и ишемическая болезнь сердца». Прогресс в сердечно-сосудистых заболеваниях . 46 (1): 31–38. дои : 10.1016/s0033-0620(03)00078-1 . ПМИД 12920699 .
- ^ Jump up to: а б Боффетта, Паоло; Агудо, Антонио; Аренс, Вольфганг; Бенаму, Эллен; Бенаму, Симона; Дарби, Сара С.; Ферро, Жиль; Фортес, Кристина; Гонсалес, Карлос А.; Йокель, Карл-Хайнц; Краусс, Мартин; Крейенброк, Лотар; Крейцер, Микаэла; Мендес, Анабела; Мерлетти, Франко; Нюберг, Фредрик; Першаген, Горан; Похлабельн, Герман; Риболи, Элио; Шмид, Джованни; Симонато, Лоренцо; Тре'Дэниел, Джин; Уитли, Элиза; Вихманн, Хайнц-Эрих; Винк, Карлос; Замбон, Паола; Сараччи, Родольфо (7 октября 1998 г.). «Многоцентровое исследование случай-контроль воздействия табачного дыма в окружающей среде и рака легких в Европе» . JNCI: Журнал Национального института рака . 90 (19): 1440–1450. дои : 10.1093/jnci/90.19.1440 . ПМИД 9776409 .
- ^ «Пассивное курение не вызывает рак — официально» . Архивировано из оригинала 13 октября 2007 г.
- ^ «Дымовые завесы – Всемирная организация здравоохранения демонстрирует признаки того, что позволяет политике встать на пути к истине. The Economist, 14 марта 1998 г.» (PDF) . Архивировано из оригинала (PDF) 29 ноября 2007 г.
- ^ Le Grand C. Антикурильщики поражены учебой. Австралия, 1998 год, 10 марта.
- ^ ВОЗ отвергает связь курения с раком легких. Независимость Зимбабве, 1998 г., 23 октября.
- ^ Нет связи между пассивным курением и раком легких. «Таймс» , 1998 г., 9 марта.
- ^ «Пассивное курение действительно вызывает рак легких, не позволяйте им обмануть вас». Цейлонский медицинский журнал . 43 (2): 98. Июнь 1998 г. PMID 9704550 .
- ^ Блот, Уильям Дж.; Маклафлин, Джозеф К. (7 октября 1998 г.). «Пассивное курение и риск рака легких: как обстоят дела сейчас?» . JNCI: Журнал Национального института рака . 90 (19): 1416–1417. дои : 10.1093/jnci/90.19.1416 . ПМИД 9776401 .
- ^ Онг ЭК, Гланц С.А. (2000). «Усилия табачной промышленности подрывают исследование Международного агентства по исследованию рака о пассивном курении». Ланцет . 355 (9211): 1253–9. дои : 10.1016/S0140-6736(00)02098-5 . ПМИД 10770318 . S2CID 25145666 .
- ^ «Стратегии табачных компаний по подрыву деятельности Всемирной организации здравоохранения по борьбе против табака» (PDF) . Архивировано из оригинала (PDF) 21 августа 2004 г. Проверено 30 декабря 2008 г.
- ^ Агентство по охране окружающей среды США. «Влияние пассивного курения на здоровье органов дыхания: рак легких и другие заболевания» .
- ^ «Решение Остина» . Архивировано из оригинала 15 августа 2000 г.
- ^ «Кооператив дымового табака против Агентства по охране окружающей среды» (PDF) . Архивировано из оригинала (PDF) 9 октября 2008 г. Проверено 30 декабря 2008 г.
- ^ Министерство здравоохранения США; социальные службы; Национальная программа токсикологии, ред. (2–3 декабря 1998 г.). «Итоговый отчет о канцерогенах - справочный документ по табачному дыму в окружающей среде». Заседание Совета научных консультантов НТП – Отчет подкомитета по канцерогенам (PDF) . Исследовательский Треугольник-Парк, Северная Каролина. п. 24. Архивировано из оригинала (PDF) 29 ноября 2007 г.
{{cite book}}: CS1 maint: отсутствует местоположение издателя ( ссылка ) - ^ Тун М.Дж. (2003). «Пассивное курение: Табачная индустрия публикует дезинформацию» . БМЖ . 327 (7413): 502–3, ответ автора 504–5. дои : 10.1136/bmj.327.7413.502-c . ПМК 188400 . ПМИД 12946979 .
- ^ Jump up to: а б Барнс Д.Э., Беро Л.А. (1998). «Почему обзорные статьи о влиянии пассивного курения на здоровье приводят к разным выводам». ДЖАМА . 279 (19): 1566–70. дои : 10.1001/jama.279.19.1566 . ПМИД 9605902 .
- ^ Тонг Э.К., Англия Л., Гланц С.А. (2005). «Изменение выводов о пассивном курении в обзоре синдрома внезапной детской смерти, финансируемом табачной промышленностью» . Педиатрия . 115 (3): e356–66. дои : 10.1542/пед.2004-1922 . ПМИД 15741361 . S2CID 33226933 .
- ^ «Последствия непроизвольного воздействия табачного дыма на здоровье» (PDF) . Управляющее резюме . Главный хирург США . 2006. с. 21 . Проверено 28 января 2009 г.
- ^ Jump up to: а б с «Протокол встречи Philip Morris с британскими табачными компаниями по обсуждению стратегии табачной индустрии по пассивному курению» . Архивировано из оригинала 13 октября 2007 г. Проверено 27 августа 2007 г.
- ^ Исследование общественного отношения к курению сигарет и табачной промышленности в 1978 году , подготовленное для Института табака и выпущенное в соответствии с условиями Генерального соглашения по табакокурению .
- ^ Смит, Э.А.; Мэлоун, RE (5 января 2007 г.). « Мы будем говорить как курильщики»: группы защиты прав курильщиков табачной промышленности» . Европейский журнал общественного здравоохранения . 17 (3): 306–313. дои : 10.1093/eurpub/ckl244 . ПМЦ 2794244 . ПМИД 17065174 .
- ^ Троттер Л., Чепмен С. (2003). « Выводы о воздействии ETS и здоровье, которые будут для нас бесполезны»*: Как табачная промышленность пыталась задержать и дискредитировать доклад Австралийского национального совета по здравоохранению и медицинским исследованиям 1997 года о пассивном курении» . Контроль над табаком . 12 (Приложение 3:iii): 102–6. дои : 10.1136/tc.12.suppl_3.iii102 . ПМК 1766130 . ПМИД 14645955 .
- ^ Гарн Д., Уотсон М., Чепмен С., Бирн Ф. (2005). «Исследование экологического табачного дыма, опубликованное в журнале «Внутренняя и построенная среда» и ассоциациях табачной промышленности». Ланцет . 365 (9461): 804–9. дои : 10.1016/S0140-6736(05)17990-2 . ПМИД 15733724 . S2CID 23160158 .
- ^ Jump up to: а б «Последствия непроизвольного воздействия табачного дыма на здоровье» (PDF) . Управляющее резюме . Главный хирург США . 2006 год . Проверено 28 января 2009 г.
- ^ Кесслер 2006 , с. 1523
- ^ Самые актуальные позиции крупных табачных компаний по вопросу пассивного курения можно найти на их сайтах. По состоянию на 13 января 2009 г. следующие веб-сайты содержат позиции табачной промышленности по этой теме:
- Бритиш Американ Тобакко : [1]
- Империал Табак : «Imperial Tobacco Group PLC - СМИ - Наш взгляд - Курение и здоровье - Экологический табачный дым» . Архивировано из оригинала 16 января 2009 г. Проверено 25 октября 2008 г.
- Philip Morris : США. Архивировано 6 октября 2010 г. в Wayback Machine and International.
- Табачная компания RJ Reynolds : «Табачная компания RJ Reynolds – Курение и здоровье – Сводка мнений» . Архивировано из оригинала 18 ноября 2006 г. Проверено 19 ноября 2006 г.
- ^ Судебный процесс против табачных компаний, Министерство юстиции США.
- ↑ Постановление по апелляции , Апелляционный суд США по округу Колумбия, 22 мая 2009 г.
- ^ Altria, Производители сигарет потеряли апелляцию по решению суда «Lights» Новости Bloomberg, 22 мая 2009 г.
- ↑ Апелляционный суд США признал, что табачные компании лгали Reuters, 22 мая 2009 г.
- ↑ Курильщики осмеливаются, чтобы Блумберг наложил на них запрет на парковку. Архивировано 26 ноября 2013 г. в Wayback Machine.
- ^ «Рамочная конвенция ВОЗ по борьбе против табака» (PDF) . Всемирная организация здравоохранения . 27 февраля 2005 г. Проверено 12 января 2009 г.
Стороны признают, что научные данные недвусмысленно установили, что воздействие табака вызывает смерть, болезни и инвалидность.
- ^ Jump up to: а б «Руководство по защите от пассивного курения» (PDF) . Рамочная конвенция по борьбе против табака . Всемирная организация здравоохранения . 2007 . Проверено 29 января 2009 г.
- ^ Мир маркетинговых исследований
- ^ Фрейзер, Кейт; Каллинан, Джоан Э; Макхью, Джек; ван Баарсел, Сьюзен; Кларк, Анна; Доэрти, Кирстен; Келлехер, Сесили (4 февраля 2016 г.). «Законодательный запрет на курение для снижения вреда от пассивного курения, распространенности курения и потребления табака» . Кокрейновская база данных систематических обзоров . 2016 (2): CD005992. дои : 10.1002/14651858.CD005992.pub3 . ПМК 6486282 . ПМИД 26842828 .
- ^ Центры по контролю и профилактике заболеваний (CDC) (январь 2009 г.). «Снижение количества госпитализаций по поводу острого инфаркта миокарда после принятия постановления о запрете курения - город Пуэбло, Колорадо, 2002–2006 гг.» . MMWR Морб. Смертный. Еженедельно. Представитель . 57 (51): 1373–7. ПМИД 19116606 .
- ^ Фрейзер, Кейт; Макхью, Джек; Каллинан, Джоан Э; Келлехер, Сесили (27 мая 2016 г.). «Влияние институциональных запретов на курение на снижение вреда и воздействия пассивного курения» . Кокрейновская база данных систематических обзоров . 2016 (5): CD011856. дои : 10.1002/14651858.CD011856.pub2 . ПМЦ 10164285 . ПМИД 27230795 .
- ^ Хопкинс Д.П., Рази С., Ликс К.Д., Прия Калра Г., Чаттопадхьяй С.К., Солер Р.Э. (2010). «Политика бездымной среды для сокращения употребления табака. Систематический обзор». Am J Prev Med . 38 (2 Приложения): S275–89. дои : 10.1016/j.amepre.2009.10.029 . ПМИД 20117612 .
- ^ Сколло М., Лал А., Хайланд А., Гланц С. (март 2003 г.). «Обзор качества исследований экономического воздействия политики бездымной среды на индустрию гостеприимства» . Контроль над табаком . 12 (1): 13–20. дои : 10.1136/tc.12.1.13 . ПМК 1759095 . ПМИД 12612356 .
- ^ Барнойя Дж., Арвизу М., Джонс М.Р., Эрнандес Х.К., Брейсс П.Н., Навас-Асьен А. (ноябрь 2010 г.). «Воздействие пассивного курения в барах и ресторанах Гватемалы: до и после оценки запрета на курение». Рак вызывает контроль . 22 (1): 151–6. дои : 10.1007/s10552-010-9673-8 . ПМИД 21046446 . S2CID 673901 .
- ^ Томсон, Джордж; Уилсон, Ник; Эдвардс, Ричард (июнь 2009 г.). «На переднем крае борьбы против табака: краткий обзор отношения общественности к местам на открытом воздухе, свободным от курения» . Исследования никотина и табака . 11 (6): 584–590. дои : 10.1093/ntr/ntp046 . ПМИД 19359392 .
- ^ «Никаких если и задниц» . Здание . 7 марта 2005 г.
- ^ Дропе Дж., Биалос С.А., Гланц С.А. (март 2004 г.). «Усилия табачной промышленности представить вентиляцию как альтернативу средам, свободным от табачного дыма, в Северной Америке» . Контроль над табаком . 13 (Приложение 1): i41–7. дои : 10.1136/tc.2003.004101 . ПМК 1766145 . ПМИД 14985616 .
Промышленность создала сеть «экспертов» по вентиляции, чтобы продвигать свою позицию о том, что создание свободных от табачного дыма сред не является необходимым, часто не раскрывая финансовых отношений между этими экспертами и отраслью.
- ^ «Документ о позиции ASHRAE в отношении табачного дыма в окружающей среде» (PDF) . Американское общество инженеров по отоплению, охлаждению и кондиционированию воздуха . июль 2020.
- ^ «Отчет о деятельности Института здравоохранения и защиты потребителей за 2003 год» (PDF) . Европейской комиссии Объединенный исследовательский центр . 2003. Архивировано из оригинала (PDF) 27 марта 2009 года . Проверено 28 января 2009 г.
- ^ Хавман, Роберт; Джон Маллахи (25 сентября 2005 г.). «Пусть бары покупают, продают разрешения на курение» . Государственный журнал Висконсина . п. Б2. Архивировано из оригинала 4 января 2009 года . Проверено 28 января 2009 г.
- ^ Томпсон, Андреа (31 августа 2007 г.). «Пассивное курение вызывает рак у домашних животных» . ЖиваяНаука . Проверено 31 августа 2007 г.
- ^ Снайдер Л.А., Бертоне Э.Р., Яковски Р.М., Дунер М.С., Дженнингс-Ричи Дж., Мур А.С. (2004). «Экспрессия p53 и воздействие табачного дыма на окружающую среду при плоскоклеточном раке полости рта у кошек» . Ветеринар Патол . 41 (3): 209–14. дои : 10.1354/vp.41-3-209 . ПМИД 15133168 . S2CID 24749614 .
- ^ Бертоне Э.Р., Снайдер Л.А., Мур А.С. (2002). «Табачный дым в окружающей среде и риск злокачественной лимфомы у домашних кошек» . Американский журнал эпидемиологии . 156 (3): 268–273. дои : 10.1093/aje/kwf044 . ПМИД 12142262 .
- ^ Рейф Дж.С., Данн К., Огилви Г.К., Харрис К.К. (1992). «Пассивное курение и риск рака легких у собак». Am J Epidemiol . 135 (3): 234–9. doi : 10.1093/oxfordjournals.aje.a116276 . ПМИД 1546698 .
Внешние ссылки
- Научные организации
- Влияние на здоровье воздействия табачного дыма в окружающей среде , данные Национального института рака США.
- «Экологический табачный дым» (PDF) . Архивировано (PDF) из оригинала 16 июля 2008 г. (219 КБ) . Из 11-го доклада о канцерогенах Национального института здравоохранения США.
- Министерство здравоохранения и социальных служб США; Центры по контролю и профилактике заболеваний; Координационный центр укрепления здоровья; Национальный центр профилактики хронических заболеваний и укрепления здоровья; Управление по курению и здоровью (27 июня 2006 г.). «Последствия для здоровья непроизвольного воздействия табачного дыма: отчет главного хирурга» . Публикации и отчеты главного хирурга. Атланта, Джорджия: Главный хирург США . ПМИД 20669524 . O2NLM: WA 754 H4325 2006.
Пассивное курение вызывает заболевания и преждевременную смерть у некурящих детей и взрослых.
{{cite journal}}: Для цитирования журнала требуется|journal=( помощь ) - Всемирная организация здравоохранения ; Международное агентство по исследованию рака (2004 г.). Табачный дым и принудительное курение (PDF) . Монографии МАИР по оценке канцерогенного риска для человека. Том. 83. Лион, Франция: Рабочая группа МАИР по оценке канцерогенных рисков для человека. ISBN 978-92-832-1283-6 .
- Информационный бюллетень о пассивном курении от Центров США по контролю и профилактике заболеваний
- Табачный дым на рабочем месте : Центры США по контролю и профилактике заболеваний
- Влияние на здоровье воздействия табачного дыма в окружающей среде , от Калифорнийского агентства по охране окружающей среды.
- Воздействие табачного дыма на окружающую среду среди детей в возрасте 3–19 лет с астмой и без нее в США, 1999–2010 гг. Национальный центр статистики здравоохранения
- Оберг, Маттиас; Яаккола, Маритта С; Вудворд, Алистер; Перуга, Армандо; Прюсс-Устюн, Аннет (январь 2011 г.). «Мировое бремя болезней от воздействия вторичного табачного дыма: ретроспективный анализ данных из 192 стран». Ланцет . 377 (9760): 139–146. дои : 10.1016/S0140-6736(10)61388-8 . ПМИД 21112082 . S2CID 7179156 .
- Табачная промышленность
- «Стратегии табачных компаний, направленные на подрыв деятельности по борьбе против табака» (PDF) . Архивировано из оригинала (PDF) 21 августа 2004 г. Проверено 5 октября 2020 г. (1,55 МБ) : Отчет Комитета экспертов по табачной промышленности. Документы Всемирной организации здравоохранения.
- Библиотека документов Legacy Tobacco и Архив документов British American Tobacco . Калифорнийского университета в Сан-Франциско
- Архив документов Philip Morris USA , обнародованный в результате Генерального соглашения по урегулированию споров в отношении табачных изделий.
- Другие ссылки
- Рекомендации по защите от пассивного курения , Рамочная конвенция ВОЗ по борьбе против табака
- Политические рекомендации ВОЗ по защите от воздействия вторичного табачного дыма
- Маленькая, Элизия; Шах, Хина П.; Давенпорт, Джейк Дж.; Гейер, Жаклин Э.; Яварович, Катя Р.; Ямада, Хидетака; Сабаринатх, Шридхаран Н.; Дерендорф, Хартмут; Поли, Джеймс Р.; Голд, Марк С.; Брейнзель, Адри В. (январь 2010 г.). «Воздействие табачного дыма вызывает никотиновую зависимость у крыс» . Психофармакология . 208 (1): 143–158. дои : 10.1007/s00213-009-1716-z . ПМК 3586198 . ПМИД 19936715 .
- Кесслер, Глэдис (17 августа 2006 г.). «Соединенные Штаты Америки против Филип Моррис и др.: Окончательное мнение судьи Глэдис Кесслер» (PDF) . Окружной суд США по округу Колумбия .
- «Как пассивное курение меняет ваши гены»
