Витамин С
Витамин С (также известный как аскорбиновая кислота и аскорбат ) — водорастворимый витамин, содержащийся в цитрусовых и других фруктах, ягодах и овощах. Это также непатентованный отпускаемая без рецепта препарат, отпускаемый по рецепту, и в некоторых странах он продается как пищевая добавка, . В качестве терапии его используют для профилактики и лечения цинги — заболевания, вызванного витамина С. дефицитом
Витамин С является важным питательным веществом, участвующим в восстановлении тканей , образовании коллагена и ферментативном производстве некоторых нейротрансмиттеров . Он необходим для функционирования нескольких ферментов и важен для функции иммунной системы . [6] Он также действует как антиоксидант . Витамин С можно принимать внутрь или внутримышечными, подкожными или внутривенными инъекциями. Существуют различные заявления о вреде для здоровья, основанные на том, что умеренный дефицит витамина С увеличивает риск заболеваний, таких как простуда , рак или COVID -19 . [ нужны разъяснения ] Есть также заявления о пользе добавок витамина С, превышающих рекомендуемую норму потребления для людей, у которых не считается дефицитом витамина С. [ нужны разъяснения ] Витамин С обычно хорошо переносится. Большие дозы могут вызвать желудочно-кишечный дискомфорт , головную боль, проблемы со сном и покраснение кожи. США Институт медицины не рекомендует употреблять большие количества. [7] : 155–165
Большинство животных способны синтезировать собственный витамин С. Однако обезьяны (включая людей) и обезьяны (но не все приматы ), большинство летучих мышей , большинство рыб, некоторые грызуны и некоторые другие животные должны получать его из пищевых источников, поскольку ген синтезирующего фермента имеет мутации, которые делают его дисфункциональным.
Витамин С был открыт в 1912 году, выделен в 1928 году, а в 1933 году стал первым витамином, полученным химическим путем . Частично за это открытие Альберт Сент-Дьёрдьи был удостоен Нобелевской премии по физиологии и медицине 1937 года .
Химия
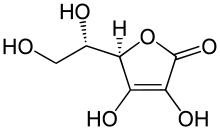
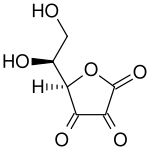
[ редактировать ]Название «витамин С» всегда относится к l -энантиомер и аскорбиновой кислоты ее окисленная форма дегидроаскорбат (ДГК). Поэтому, если не указано иное, «аскорбат» и «аскорбиновая кислота» в литературе по питанию относятся к л- аскорбат и l -аскорбиновая кислота соответственно. Аскорбиновая кислота — слабая сахарная кислота, структурно родственная глюкозе . В биологических системах аскорбиновую кислоту можно обнаружить только при низком pH , но в растворах с pH выше 5 она преимущественно содержится в ионизированной форме — аскорбате. [8]
Для обнаружения аскорбиновой кислоты было разработано множество аналитических методов. Например, содержание витамина С в образце пищевого продукта, такого как фруктовый сок, можно рассчитать, измеряя объем образца, необходимый для обесцвечивания раствора дихлорфенолиндофенола (DCPIP), а затем калибруя результаты путем сравнения с известной концентрацией витамина С. [9] [10]
Дефицит
[ редактировать ]Уровень витамина С в плазме является наиболее широко применяемым тестом на определение статуса витамина С. [8] Адекватные уровни определяются как около 50 мкмоль/л. Гиповитаминоз витамина С определяют при уровне менее 23 мкмоль/л, дефицит – менее 11,4 мкмоль/л. [11] США в 2017–2018 годах для людей в возрасте 20 лет и старше Данные Национального исследования здоровья и питания показали, что средние концентрации в сыворотке составляют 53,4 мкмоль/л. Процент людей, зарегистрированных как дефицитные, составил 5,9%. [12] Во всем мире дефицит витамина С распространен в странах с низким и средним уровнем дохода, а также нередко в странах с высоким уровнем дохода. В последнем случае распространенность выше у мужчин, чем у женщин. [13]
Уровни в плазме считаются насыщенными при уровне около 65 мкмоль/л, достигаемом при приеме от 100 до 200 мг/день, что значительно превышает рекомендуемые дозы. Даже более высокий пероральный прием не приводит к дальнейшему повышению концентрации в плазме или тканях, поскольку эффективность абсорбции снижается, и любой всасываемый избыток выводится с мочой. [8]
Диагностическое тестирование
[ редактировать ]Содержание витамина С в плазме используется для определения витаминного статуса. В исследовательских целях концентрации могут быть оценены в лейкоцитах и тканях, которые обычно поддерживаются на порядок выше, чем в плазме, через энергозависимую транспортную систему, истощаются медленнее, чем концентрации в плазме во время диетического дефицита, и быстрее восстанавливаются во время диетического насыщения. [7] : 103–109 но эти анализы трудно измерить, и, следовательно, они не являются частью стандартного диагностического тестирования. [8] [14]
Diet
[edit]Recommended consumption
[edit]Recommendations for vitamin C intake by adults have been set by various national agencies:
- 40 mg/day: India National Institute of Nutrition, Hyderabad[15]
- 45 mg/day or 300 mg/week: the World Health Organization[16]
- 80 mg/day: the European Commission Council on nutrition labeling[17]
- 90 mg/day (males) and 75 mg/day (females): Health Canada 2007[18]
- 90 mg/day (males) and 75 mg/day (females): United States National Academy of Sciences[7]: 134–152
- 100 mg/day: Japan National Institute of Health and Nutrition[19]
- 110 mg/day (males) and 95 mg/day (females): European Food Safety Authority[20]
| US vitamin C recommendations (mg per day)[7]: 134–152 | |
|---|---|
| RDA (children ages 1–3 years) | 15 |
| RDA (children ages 4–8 years) | 25 |
| RDA (children ages 9–13 years) | 45 |
| RDA (girls ages 14–18 years) | 65 |
| RDA (boys ages 14–18 years) | 75 |
| RDA (adult female) | 75 |
| RDA (adult male) | 90 |
| RDA (pregnancy) | 85 |
| RDA (lactation) | 120 |
| UL (adult female) | 2,000 |
| UL (adult male) | 2,000 |
In 2000, the chapter on Vitamin C in the North American Dietary Reference Intake was updated to give the Recommended Dietary Allowance (RDA) as 90 milligrams per day for adult men, 75 mg/day for adult women, and setting a Tolerable upper intake level (UL) for adults of 2,000 mg/day.[7]: 134–152 The table (right) shows RDAs for the United States and Canada for children, and for pregnant and lactating women,[7]: 134–152 as well as the ULs for adults.
For the European Union, the EFSA set higher recommendations for adults, and also for children: 20 mg/day for ages 1–3, 30 mg/day for ages 4–6, 45 mg/day for ages 7–10, 70 mg/day for ages 11–14, 100 mg/day for males ages 15–17, 90 mg/day for females ages 15–17. For pregnancy 100 mg/day; for lactation 155 mg/day.[20]
Cigarette smokers and people exposed to secondhand smoke have lower serum vitamin C levels than nonsmokers.[11] The thinking is that inhalation of smoke causes oxidative damage, depleting this antioxidant vitamin.[7]: 152–153 The US Institute of Medicine estimated that smokers need 35 mg more vitamin C per day than nonsmokers, but did not formally establish a higher RDA for smokers.[7]: 152–153
The US National Center for Health Statistics conducts biannual National Health and Nutrition Examination Survey (NHANES) to assess the health and nutritional status of adults and children in the United States. Some results are reported as What We Eat In America. The 2013–2014 survey reported that for adults ages 20 years and older, men consumed on average 83.3 mg/d and women 75.1 mg/d. This means that half the women and more than half the men are not consuming the RDA for vitamin C.[21] The same survey stated that about 30% of adults reported they consumed a vitamin C dietary supplement or a multi-vitamin/mineral supplement that included vitamin C, and that for these people total consumption was between 300 and 400 mg/d.[22]
Tolerable upper intake level
[edit]In 2000, the Institute of Medicine of the US National Academy of Sciences set a Tolerable upper intake level (UL) for adults of 2,000 mg/day. The amount was chosen because human trials had reported diarrhea and other gastrointestinal disturbances at intakes of greater than 3,000 mg/day. This was the Lowest-Observed-Adverse-Effect Level (LOAEL), meaning that other adverse effects were observed at even higher intakes. ULs are progressively lower for younger and younger children.[7]: 155–165 In 2006, the European Food Safety Authority (EFSA) also pointed out the disturbances at that dose level, but reached the conclusion that there was not sufficient evidence to set a UL for vitamin C,[23] as did the Japan National Institute of Health and Nutrition in 2010.[19]
Food labeling
[edit]For US food and dietary supplement labeling purposes, the amount in a serving is expressed as a percent of Daily Value (%DV). For vitamin C labeling purposes, 100% of the Daily Value was 60 mg, but as of May 27, 2016, it was revised to 90 mg to bring it into agreement with the RDA.[24][25] A table of the old and new adult daily values is provided at Reference Daily Intake.
European Union regulations require that labels declare energy, protein, fat, saturated fat, carbohydrates, sugars, and salt. Voluntary nutrients may be shown if present in significant amounts. Instead of Daily Values, amounts are shown as percent of Reference Intakes (RIs). For vitamin C, 100% RI was set at 80 mg in 2011.[26]
Sources
[edit]Although also present in other plant-derived foods, the richest natural sources of vitamin C are fruits and vegetables.[4][6] Vitamin C is the most widely taken dietary supplement.[6]
Plant sources
[edit]The following table is approximate and shows the relative abundance in different raw plant sources.[4][6][27] The amount is given in milligrams per 100 grams of the edible portion of the fruit or vegetable:
| Raw plant source[28] | Amount (mg / 100g) |
|---|---|
| Kakadu plum | 1000–5300[29] |
| Camu camu | 2800[30] |
| Acerola | 1677[31] |
| Indian gooseberry | 445[32][33] |
| Rose hip | 426 |
| Common sea-buckthorn | 400[34] |
| Guava | 228 |
| Blackcurrant | 200 |
| Yellow bell pepper/capsicum | 183 |
| Red bell pepper/capsicum | 128 |
| Kale | 120 |
| Broccoli | 90 |
| Kiwifruit | 90 |
| Raw plant source[28] | Amount (mg / 100g) |
|---|---|
| Green bell pepper/capsicum | 80 |
| Brussels sprouts | 80 |
| Loganberry, redcurrant | 80 |
| Cloudberry, elderberry | 60 |
| Strawberry | 60 |
| Papaya | 60 |
| Orange, lemon | 53 |
| Cauliflower | 48 |
| Pineapple | 48 |
| Cantaloupe | 40 |
| Passion fruit, raspberry | 30 |
| Grapefruit, lime | 30 |
| Cabbage, spinach | 30 |
| Raw plant source[28] | Amount (mg / 100g) |
|---|---|
| Mango | 28 |
| Blackberry, cassava | 21 |
| Potato | 20 |
| Honeydew melon | 20 |
| Tomato | 14 |
| Cranberry | 13 |
| Blueberry, grape | 10 |
| Apricot, plum, watermelon | 10 |
| Avocado | 8.8 |
| Onion | 7.4 |
| Cherry, peach | 7 |
| Apple | 6 |
| Carrot, asparagus | 6 |
Animal sources
[edit]Compared to plant sources, animal-sourced foods do not provide so great an amount of vitamin C, and what there is is largely destroyed by the heat used when it is cooked. For example, raw chicken liver contains 17.9 mg/100 g, but fried, the content is reduced to 2.7 mg/100 g. Vitamin C is present in human breast milk at 5.0 mg/100 g. Cow's milk contains 1.0 mg/100 g, but the heat of pasteurization destroys it.[35]
Food preparation
[edit]Vitamin C chemically decomposes under certain conditions, many of which may occur during the cooking of food. Vitamin C concentrations in various food substances decrease with time in proportion to the temperature at which they are stored.[36] Cooking can reduce the vitamin C content of vegetables by around 60%, possibly due to increased enzymatic destruction.[37] Longer cooking times may add to this effect.[38] Another cause of vitamin C loss from food is leaching, which transfers vitamin C to the cooking water, which is decanted and not consumed.[39]
Supplements
[edit]Vitamin C dietary supplements are available as tablets, capsules, drink mix packets, in multi-vitamin/mineral formulations, in antioxidant formulations, and as crystalline powder.[40] Vitamin C is also added to some fruit juices and juice drinks. Tablet and capsule content ranges from 25 mg to 1500 mg per serving. The most commonly used supplement compounds are ascorbic acid, sodium ascorbate and calcium ascorbate.[40] Vitamin C molecules can also be bound to the fatty acid palmitate, creating ascorbyl palmitate, or else incorporated into liposomes.[41]
Food fortification
[edit]Countries fortify foods with nutrients to address known deficiencies.[42] While many countries mandate or have voluntary programs to fortify wheat flour, maize (corn) flour or rice with vitamins,[43] none include vitamin C in those programs.[43] As described in Vitamin C Fortification of Food Aid Commodities (1997), the United States provides rations to international food relief programs, later under the asupices of the Food for Peace Act and the Bureau for Humanitarian Assistance.[44] Vitamin C is added to corn-soy blend and wheat-soy blend products at 40 mg/100 grams. (along with minerals and other vitamins). Supplemental rations of these highly fortified, blended foods are provided to refugees and displaced persons in camps and to beneficiaries of development feeding programs that are targeted largely toward mothers and children.[39] The report adds: "The stability of vitamin C (L-ascorbic acid) is of concern because this is one of the most labile vitamins in foods. Its main loss during processing and storage is from oxidation, which is accelerated by light, oxygen, heat, increased pH, high moisture content (water activity), and the presence of copper or ferrous salts. To reduce oxidation, the vitamin C used in commodity fortification is coated with ethyl cellulose (2.5 percent). Oxidative losses also occur during food processing and preparation, and additional vitamin C may be lost if it dissolves into cooking liquid and is then discarded."[39]
Food preservation additive
[edit]Ascorbic acid and some of its salts and esters are common additives added to various foods, such as canned fruits, mostly to slow oxidation and enzymatic browning.[45] It may be used as a flour treatment agent used in breadmaking.[46] As food additives, they are assigned E numbers, with safety assessment and approval the responsibility of the European Food Safety Authority.[47] The relevant E numbers are:
- E300 ascorbic acid (approved for use as a food additive in the UK,[48] US[49] Canada,[50] Australia and New Zealand[51])
- E301 sodium ascorbate (approved for use as a food additive in the UK,[48] US,[52] Canada,[50] Australia and New Zealand[51])
- E302 calcium ascorbate (approved for use as a food additive in the UK,[48] US[49] Canada,[50] Australia and New Zealand[51])
- E303 potassium ascorbate (approved in Australia and New Zealand,[51] but not in the UK, US or Canada)
- E304 fatty acid esters of ascorbic acid such as ascorbyl palmitate (approved for use as a food additive in the UK,[48] US,[49] Canada,[50] Australia and New Zealand[51])
The stereoisomers of Vitamin C have a similar effect in food despite their lack of efficacy in humans. They include erythorbic acid and its sodium salt (E315, E316).[48]
Pharmacology
[edit]Pharmacodynamics is the study of how the drug – in this instance vitamin C – affects the organism, whereas pharmacokinetics is the study of how an organism affects the drug.
Pharmacodynamics
[edit]Pharmacodynamics includes enzymes for which vitamin C is a cofactor, with function potentially compromised in a deficiency state, and any enzyme cofactor or other physiological function affected by administration of vitamin C, orally or injected, in excess of normal requirements. At normal physiological concentrations, vitamin C serves as an enzyme substrate or cofactor and an electron donor antioxidant. The enzymatic functions include the synthesis of collagen, carnitine, and neurotransmitters; the synthesis and catabolism of tyrosine; and the metabolism of microsomes. In nonenzymatic functions it acts as a reducing agent, donating electrons to oxidized molecules and preventing oxidation in order to keep iron and copper atoms in their reduced states.[8] At non-physiological concentrations achieved by intravenous dosing, vitamin C may function as a pro-oxidant, with therapeutic toxicity against cancer cells.[53][54]
Vitamin C functions as a cofactor for the following enzymes:[8]
- Three groups of enzymes (prolyl-3-hydroxylases, prolyl-4-hydroxylases, and lysyl hydroxylases) that are required for the hydroxylation of proline and lysine in the synthesis of collagen. These reactions add hydroxyl groups to the amino acids proline or lysine in the collagen molecule via prolyl hydroxylase and lysyl hydroxylase, both requiring vitamin C as a cofactor. The role of vitamin C as a cofactor is to oxidize prolyl hydroxylase and lysyl hydroxylase from Fe2+ to Fe3+ and to reduce it from Fe3+ to Fe2+. Hydroxylation allows the collagen molecule to assume its triple helix structure, and thus vitamin C is essential to the development and maintenance of scar tissue, blood vessels, and cartilage.
- Two enzymes (ε-N-trimethyl-L-lysine hydroxylase and γ-butyrobetaine hydroxylase) are necessary for synthesis of carnitine. Carnitine is essential for the transport of fatty acids into mitochondria for ATP generation.
- Hypoxia-inducible factor-proline dioxygenase enzymes (isoforms: EGLN1, EGLN2, and EGLN3) allows cells to respond physiologically to low concentrations of oxygen.
- Dopamine beta-hydroxylase participates in the biosynthesis of norepinephrine from dopamine.
- Peptidylglycine alpha-amidating monooxygenase amidates peptide hormones by removing the glyoxylate residue from their c-terminal glycine residues. This increases peptide hormone stability and activity.
As an antioxidant, ascorbate scavenges reactive oxygen and nitrogen compounds, thus neutralizing the potential tissue damage of these free radical compounds. Dehydroascorbate, the oxidized form, is then recycled back to ascorbate by endogenous antioxidants such as glutathione.[7]: 98–99 In the eye, ascorbate is thought to protect against photolytically generated free-radical damage; higher plasma ascorbate is associated with lower risk of cataracts.[55] Ascorbate may also provide antioxidant protection indirectly by regenerating other biological antioxidants such as α-tocopherol back to an active state.[7]: 98–99 In addition, ascorbate also functions as a non-enzymatic reducing agent for mixed-function oxidases in the microsomal drug-metabolizing system that inactivates a wide variety of substrates such as drugs and environmental carcinogens.[7]: 98–99
Pharmacokinetics
[edit]Ascorbic acid is absorbed in the body by both active transport and passive diffusion.[56] Approximately 70%–90% of vitamin C is active-transport absorbed when intakes of 30–180 mg/day from a combination of food sources and moderate-dose dietary supplements such as a multi-vitamin/mineral product are consumed. However, when large amounts are consumed, such as a vitamin C dietary supplement, the active transport system becomes saturated, and while the total amount being absorbed continues to increase with dose, absorption efficiency falls to less than 50%.[4] Active transport is managed by Sodium-Ascorbate Co-Transporter proteins (SVCTs) and Hexose Transporter proteins (GLUTs). SVCT1 and SVCT2 import ascorbate across plasma membranes.[57] The Hexose Transporter proteins GLUT1, GLUT3 and GLUT4 transfer only the oxydized dehydroascorbic acid (DHA) form of vitamin C.[58][59] The amount of DHA found in plasma and tissues under normal conditions is low, as cells rapidly reduce DHA to ascorbate.[60]
SVCTs are the predominant system for vitamin C transport within the body.[57] In both vitamin C synthesizers (example: rat) and non-synthesizers (example: human) cells maintain ascorbic acid concentrations much higher than the approximately 50 micromoles/liter (μmol/L) found in plasma. For example, the ascorbic acid content of pituitary and adrenal glands can exceed 2,000 μmol/L, and muscle is at 200–300 μmol/L.[61] The known coenzymatic functions of ascorbic acid do not require such high concentrations, so there may be other, as yet unknown functions. A consequence of all this high concentration organ content is that plasma vitamin C is not a good indicator of whole-body status, and people may vary in the amount of time needed to show symptoms of deficiency when consuming a diet very low in vitamin C.[61]
Excretion (via urine) is as ascorbic acid and metabolites. The fraction that is excreted as unmetabolized ascorbic acid increases as intake increases. In addition, ascorbic acid converts (reversibly) to DHA and from that compound non-reversibly to 2,3-diketogulonate and then oxalate. These three metabolites are also excreted via urine. During times of low dietary intake, vitamin C is reabsorbed by the kidneys rather than excreted. This salvage process delays onset of deficiency. Humans are better than guinea pigs at converting DHA back to ascorbate, and thus take much longer to become vitamin C deficient.[8][59]
Synthesis
[edit]Most animals and plants are able to synthesize vitamin C through a sequence of enzyme-driven steps, which convert monosaccharides to vitamin C. Yeasts do not make l-ascorbic acid but rather its stereoisomer, erythorbic acid.[62] In plants, synthesis is accomplished through the conversion of mannose or galactose to ascorbic acid.[63][64] In animals, the starting material is glucose. In some species that synthesize ascorbate in the liver (including mammals and perching birds), the glucose is extracted from glycogen; ascorbate synthesis is a glycogenolysis-dependent process.[65] In humans and in animals that cannot synthesize vitamin C, the enzyme l-gulonolactone oxidase (GULO), which catalyzes the last step in the biosynthesis, is highly mutated and non-functional.[66][67][68][69]
Animal synthesis
[edit]There is some information on serum vitamin C concentrations maintained in animal species that are able to synthesize vitamin C. One study of several breeds of dogs reported an average of 35.9 μmol/L.[70] A report on goats, sheep and cattle reported ranges of 100–110, 265–270 and 160–350 μmol/L, respectively.[71]
The biosynthesis of ascorbic acid in vertebrates starts with the formation of UDP-glucuronic acid. UDP-glucuronic acid is formed when UDP-glucose undergoes two oxidations catalyzed by the enzyme UDP-glucose 6-dehydrogenase. UDP-glucose 6-dehydrogenase uses the co-factor NAD+ as the electron acceptor. The transferase UDP-glucuronate pyrophosphorylase removes a UMP and glucuronokinase, with the cofactor ADP, removes the final phosphate leading to d-glucuronic acid. The aldehyde group of this compound is reduced to a primary alcohol using the enzyme glucuronate reductase and the cofactor NADPH, yielding l-gulonic acid. This is followed by lactone formation—utilizing the hydrolase gluconolactonase—between the carbonyl on C1 and hydroxyl group on C4. l-Gulonolactone then reacts with oxygen, catalyzed by the enzyme L-gulonolactone oxidase (which is nonfunctional in humans and other Haplorrhini primates; see Unitary pseudogenes) and the cofactor FAD+. This reaction produces 2-oxogulonolactone (2-keto-gulonolactone), which spontaneously undergoes enolization to form ascorbic acid.[64][72][59] Reptiles and older orders of birds make ascorbic acid in their kidneys. Recent orders of birds and most mammals make ascorbic acid in their liver.[64]
Non-synthesizers
[edit]Some mammals have lost the ability to synthesize vitamin C, including simians and tarsiers, which together make up one of two major primate suborders, Haplorhini. This group includes humans. The other more primitive primates (Strepsirrhini) have the ability to make vitamin C. Synthesis does not occur in some species in the rodent family Caviidae, which includes guinea pigs and capybaras, but does occur in other rodents, including rats and mice.[73]
Synthesis does not occur in most bat species,[74] but there are at least two species, frugivorous bat Rousettus leschenaultii and insectivorous bat Hipposideros armiger, that retain (or regained) their ability of vitamin C production.[75][76] A number of species of passerine birds also do not synthesize, but not all of them, and those that do not are not clearly related; it has been proposed that the ability was lost separately a number of times in birds.[77] In particular, the ability to synthesize vitamin C is presumed to have been lost and then later re-acquired in at least two cases.[78] The ability to synthesize vitamin C has also been lost in about 96% of extant fish[79] (the teleosts).[78]
On a milligram consumed per kilogram of body weight basis, simian non-synthesizer species consume the vitamin in amounts 10 to 20 times higher than what is recommended by governments for humans.[80] This discrepancy constituted some of the basis of the controversy on human recommended dietary allowances being set too low.[81] However, simian consumption does not indicate simian requirements. Merck's veterinary manual states that daily intake of vitamin C at 3–6 mg/kg prevents scurvy in non-human primates.[82] By way of comparison, across several countries, the recommended dietary intake for adult humans is in the range of 1–2 mg/kg.
Evolution of animal synthesis
[edit]Ascorbic acid is a common enzymatic cofactor in mammals used in the synthesis of collagen, as well as a powerful reducing agent capable of rapidly scavenging a number of reactive oxygen species (ROS). Given that ascorbate has these important functions, it is surprising that the ability to synthesize this molecule has not always been conserved. In fact, anthropoid primates, Cavia porcellus (guinea pigs), teleost fishes, most bats, and some passerine birds have all independently lost the ability to internally synthesize vitamin C in either the kidney or the liver.[83][78] In all of the cases where genomic analysis was done on an ascorbic acid auxotroph, the origin of the change was found to be a result of loss-of-function mutations in the gene that encodes L-gulono-γ-lactone oxidase, the enzyme that catalyzes the last step of the ascorbic acid pathway outlined above.[84] One explanation for the repeated loss of the ability to synthesize vitamin C is that it was the result of genetic drift; assuming that the diet was rich in vitamin C, natural selection would not act to preserve it.[85][86]
In the case of the simians, it is thought that the loss of the ability to make vitamin C may have occurred much farther back in evolutionary history than the emergence of humans or even apes, since it evidently occurred soon after the appearance of the first primates, yet sometime after the split of early primates into the two major suborders Haplorrhini (which cannot make vitamin C) and its sister suborder of non-tarsier prosimians, the Strepsirrhini ("wet-nosed" primates), which retained the ability to make vitamin C.[87] According to molecular clock dating, these two suborder primate branches parted ways about 63 to 60 million years ago.[88] Approximately three to five million years later (58 million years ago), only a short time afterward from an evolutionary perspective, the infraorder Tarsiiformes, whose only remaining family is that of the tarsier (Tarsiidae), branched off from the other haplorrhines.[89][90] Since tarsiers also cannot make vitamin C, this implies the mutation had already occurred, and thus must have occurred between these two marker points (63 to 58 million years ago).[87]
It has also been noted that the loss of the ability to synthesize ascorbate strikingly parallels the inability to break down uric acid, also a characteristic of primates. Uric acid and ascorbate are both strong reducing agents. This has led to the suggestion that, in higher primates, uric acid has taken over some of the functions of ascorbate.[91]
Plant synthesis
[edit]
There are many different biosynthesis pathways to ascorbic acid in plants. Most proceed through products of glycolysis and other metabolic pathways. For example, one pathway utilizes plant cell wall polymers.[66] The principal plant ascorbic acid biosynthesis pathway seems to be via l-galactose. The enzyme l-galactose dehydrogenase catalyzes the overall oxidation to the lactone and isomerization of the lactone to the C4-hydroxyl group, resulting in l-galactono-1,4-lactone.[72] l-Galactono-1,4-lactone then reacts with the mitochondrial flavoenzyme l-galactonolactone dehydrogenase[92] to produce ascorbic acid.[72] l-Ascorbic acid has a negative feedback on l-galactose dehydrogenase in spinach.[93] Ascorbic acid efflux by embryos of dicot plants is a well-established mechanism of iron reduction and a step obligatory for iron uptake.[a]
All plants synthesize ascorbic acid. Ascorbic acid functions as a cofactor for enzymes involved in photosynthesis, synthesis of plant hormones, as an antioxidant and regenerator of other antioxidants.[95] Plants use multiple pathways to synthesize vitamin C. The major pathway starts with glucose, fructose or mannose (all simple sugars) and proceeds to l-galactose, l-galactonolactone and ascorbic acid.[95][96] This biosynthesis is regulated following a diurnal rhythm.[96] Enzyme expression peaks in the morning to supporting biosynthesis for when mid-day sunlight intensity demands high ascorbic acid concentrations.[96][97] Minor pathways may be specific to certain parts of plants; these can be either identical to the vertebrate pathway (including the GLO enzyme), or start with inositol and get to ascorbic acid via l-galactonic acid to l-galactonolactone.[95]
Industrial synthesis
[edit]Vitamin C can be produced from glucose by two main routes. The no longer utilized Reichstein process, developed in the 1930s, used a single fermentation followed by a purely chemical route. The modern two-step fermentation process, originally developed in China in the 1960s, uses additional fermentation to replace part of the later chemical stages. The Reichstein process and the modern two-step fermentation processes both use glucose as the starting material, convert that to sorbitol, and then to sorbose using fermentation.[98] The two-step fermentation process then converts sorbose to 2-keto-l-gulonic acid (KGA) through another fermentation step, avoiding an extra intermediate. Both processes yield approximately 60% vitamin C from the glucose starting point.[99] Researchers are exploring means for one-step fermentation.[100][101]
China produces about 70% of the global vitamin C market. The rest is split among European Union, India and North America. The global market is expected to exceed 141 thousand metric tons in 2024.[102] Cost per metric ton (1000 kg) in US dollars was $2,220 in Shanghai, $2,850 in Hamburg and $3,490 in the US.[103]
Medical uses
[edit]
Vitamin C has a definitive role in treating scurvy, which is a disease caused by vitamin C deficiency. Beyond that, a role for vitamin C as prevention or treatment for various diseases is disputed, with reviews often reporting conflicting results. No effect of vitamin C supplementation reported for overall mortality.[104] It is on the World Health Organization's List of Essential Medicines and on the World Health Organization's Model Forumulary.[105] In 2021, it was the 255th most commonly prescribed medication in the United States, with more than 1 million prescriptions.[106]
Scurvy
[edit]Scurvy is a disease resulting from a deficiency of vitamin C. Without this vitamin, collagen made by the body is too unstable to perform its function and several other enzymes in the body do not operate correctly. Early symptoms are malaise and lethargy, progressing to shortness of breath, bone pain and susceptibility to bruising. As the disease progressed, it is characterized by spots on and bleeding under the skin and bleeding gums. The skin lesions are most abundant on the thighs and legs. A person with the ailment looks pale, feels depressed, and is partially immobilized. In advanced scurvy there is fever, old wounds may become open and suppurating, loss of teeth, convulsions and, eventually, death. Until quite late in the disease the damage is reversible, as healthy collagen replaces the defective collagen with vitamin C repletion.[6][40][107]
Notable human dietary studies of experimentally induced scurvy were conducted on conscientious objectors during World War II in Britain and on Iowa state prisoners in the late 1960s to the 1980s. Men in the prison study developed the first signs of scurvy about four weeks after starting the vitamin C-free diet, whereas in the earlier British study, six to eight months were required, possibly due to the pre-loading of this group with a 70 mg/day supplement for six weeks before the scorbutic diet was fed. Men in both studies had blood levels of ascorbic acid too low to be accurately measured by the time they developed signs of scurvy. These studies both reported that all obvious symptoms of scurvy could be completely reversed by supplementation of only 10 mg a day.[108][109] Treatment of scurvy can be with vitamin C-containing foods or dietary supplements or injection.[40][7]: 101
Sepsis
[edit]People in sepsis may have micronutrient deficiencies, including low levels of vitamin C.[110] An intake of 3.0 g/day, which requires intravenous administration, appears to be needed to maintain normal plasma concentrations in people with sepsis or severe burn injury.[111][112] Sepsis mortality may be reduced with administration of intravenous vitamin C.[113][114]
Common cold
[edit]
Research on vitamin C in the common cold has been divided into effects on prevention, duration, and severity. Oral intakes of more than 200 mg/day taken on a regular basis was not effective in prevention of the common cold. Restricting analysis to trials that used at least 1000 mg/day also saw no prevention benefit. However, taking a vitamin C supplement on a regular basis did reduce the average duration of the illness by 8% in adults and 14% in children, and also reduced the severity of colds.[115] Vitamin C taken on a regular basis reduced the duration of severe symptoms but had no effect on the duration of mild symptoms.[116] Therapeutic use, meaning that the vitamin was not started unless people started to feel the beginnings of a cold, had no effect on the duration or severity of the illness.[115]
Vitamin C distributes readily in high concentrations into immune cells, promotes natural killer cell activities, promotes lymphocyte proliferation, and is depleted quickly during infections, effects suggesting a prominent role in immune system function.[117] The European Food Safety Authority concluded there is a cause and effect relationship between the dietary intake of vitamin C and functioning of a normal immune system in adults and in children under three years of age.[118][119]
COVID-19
[edit]During March through July 2020, vitamin C was the subject of more US FDA warning letters than any other ingredient for claims for prevention and/or treatment of COVID-19.[120] In April 2021, the US National Institutes of Health (NIH) COVID-19 Treatment Guidelines stated that "there are insufficient data to recommend either for or against the use of vitamin C for the prevention or treatment of COVID-19."[121] In an update posted December 2022, the NIH position was unchanged:
- There is insufficient evidence for the COVID-19 Treatment Guidelines Panel (the Panel) to recommend either for or against the use of vitamin C for the treatment of COVID-19 in nonhospitalized patients.
- There is insufficient evidence for the Panel to recommend either for or against the use of vitamin C for the treatment of COVID-19 in hospitalized patients.[122]
For people hospitalized with severe COVID-19 there are reports of a significant reduction in the risk of all-cause, in-hospital mortality with the administration of vitamin C relative to no vitamin C. There were no significant differences in ventilation incidence, hospitalization duration or length of intensive care unit stay between the two groups. The majority of the trials incorporated into these meta-analyses used intravenous administration of the vitamin.[123][124][125] Acute kidney injury was lower in people treated with vitamin C treatment. There were no differences in the frequency of other adverse events due to the vitamin.[125] The conclusion was that further large-scale studies are needed to affirm its mortality benefits before issuing updated guidelines and recommendations.[123][124][125]
Cancer
[edit]There is no evidence that vitamin C supplementation reduces the risk of lung cancer in healthy people or those at high risk due to smoking or asbestos exposure.[126] It has no effect on the risk of prostate cancer,[127] and there is no good evidence vitamic C supplementation affects the risk of colorectal cancer[128] or breast cancer.[129]
Cardiovascular disease
[edit]There is no evidence that vitamin C supplementation decreases the risk cardiovascular disease,[130] although there may be an association between higher circulating vitamin C levels or dietary vitamin C and a lower risk of stroke.[131] There is a positive effect of vitamin C on endothelial dysfunction when taken at doses greater than 500 mg per day. (The endothelium is a layer of cells that line the interior surface of blood vessels.)[132]
Blood pressure
[edit]Serum vitamin C was reported to be 15.13 μmol/L lower in people with hypertension compared to normotensives. The vitamin was inversely associated with both systolic blood pressure (SBP) and diastolic blood pressure (DBP).[133] Oral supplementation of the vitamin resulted in a very modest but statistically significant decrease in SBP in people with hypertension.[134][135] The proposed explanation is that vitamin C increases intracellular concentrations of tetrahydrobiopterin, an endothelial nitric oxide synthase cofactor that promotes the production of nitric oxide, which is a potent vasodilator. Vitamin C supplementation might also reverse the nitric oxide synthase inhibitor NG-monomethyl-L-arginine 1, and there is also evidence cited that vitamin C directly enhances the biological activity of nitric oxide[134]
Type 2 diabetes
[edit]There are contradictory reviews. From one, vitamin C supplementation cannot be recommended for management of type 2 diabetes.[136] However, another reported that supplementation with high doses of vitamin C can decrease blood glucose, insulin and hemoglobin A1c.[137]
Iron deficiency
[edit]One of the causes of iron-deficiency anemia is reduced absorption of iron. Iron absorption can be enhanced through ingestion of vitamin C alongside iron-containing food or supplements. Vitamin C helps to keep iron in the reduced ferrous state, which is more soluble and more easily absorbed.[138]
Cognitive impairment and Alzheimer's disease
[edit]Lower plasma vitamin C concentrations were reported in people with cognitive impairment and Alzheimer's disease compared to people with normal cognition.[139][140][141]
Eye health
[edit]Higher dietary intake of vitamin C was associated with lower risk of age-related cataracts.[55][142] Vitamin C supplementation did not prevent age-related macular degeneration.[143]
Periodontal disease
[edit]Low intake and low serum concentration were associated with greater progression of periodontal disease.[144][145]
Adverse effects
[edit]Oral intake of dietary supplements vitamin C in excess of requirements is poorly absorbed,[4] and excess amounts in the blood are rapidly excreted in the urine, so it exhibits low acute toxicity.[6] More than two to three grams, consumed orally, may cause nausea, abdominal cramps and diarrhea. These effects are attributed to the osmotic effect of unabsorbed vitamin C passing through the intestine.[7]: 156 In theory, high vitamin C intake may cause excessive absorption of iron. A summary of reviews of supplementation in healthy subjects did not report this problem, but left as untested the possibility that individuals with hereditary hemochromatosis might be adversely affected.[7]: 158
There is a longstanding belief among the mainstream medical community that vitamin C increases risk of kidney stones.[146] "Reports of kidney stone formation associated with excess ascorbic acid intake are limited to individuals with renal disease".[7]: 156–157 A review states that "data from epidemiological studies do not support an association between excess ascorbic acid intake and kidney stone formation in apparently healthy individuals",[147] although one large, multi-year trial did report a nearly two-fold increase in kidney stones in men who regularly consumed a vitamin C supplement.[148]
There is extensive research on the purported benefits of intravenous vitamin C for treatment of sepsis,[111] severe COVID-19[123][124] and cancer.[149] Reviews list trials with doses as high as 24 grams per day.[123] Concerns about possible adverse effects are that intravenous high-dose vitamin C leads to a supraphysiological level of vitamin C followed by oxidative degradation to dehydroascorbic acid and hence to oxalate, increasing the risk of oxalate kidney stones and oxalate nephropathy. The risk may be higher in people with renal impairment, as kidneys efficiently excrete excess vitamin C. Second, treatment with high dose vitamin C should be avoided in patients with glucose-6-phosphate dehydrogenase deficiency as it can lead to acute hemolysis. Third, treatment might interfere with the accuracy of glucometer measurement of blood glucose levels, as both vitamin C and glucose have similar molecular structure, which could lead to false high blood glucose readings. Despite all these concerns, meta-analyses of patients in intensive care for sepsis, septic shock, COVID-19 and other acute conditions reported no increase in new-onset kidney stones, acute kidney injury or requirement for renal replacement therapy for patients receiving short-term, high-dose, intravenous vitamin C treatment. This suggests that intravenous vitamin C is safe under these short-term applications.[150][151][152]
История
[ редактировать ]Цинга была известна Гиппократу , описана во второй книге его Prorreticorum и в его Liber de internisaffibus и цитирована Джеймсом Линдом. [153] Симптомы цинги были описаны и Плинием Старшим : (i) Плиний. «49». Естественные истории . Том. 3. ; и (ii) Страбон в Geographicorum , книга 16, цитируемая в Международной энциклопедии хирургии 1881 года. [154]
Цинга на море
[ редактировать ]
В экспедиции Васко да Гамы 1497 года было известно о целебном действии цитрусовых. [155] В 1500-х годах португальские моряки прибыли на остров Святой Елены, чтобы насладиться посаженными огородами и дикорастущими фруктовыми деревьями. [156] Власти иногда рекомендовали растительную пищу для предотвращения цинги во время длительных морских путешествий. Джон Вудалл , первый хирург Британской Ост-Индской компании , рекомендовал профилактическое и лечебное использование лимонного сока в своей книге 1617 года «Помощник хирурга» . [157] В 1734 году голландский писатель Иоганн Бахстрем высказал твердое мнение: «Цинга возникает исключительно вследствие полного воздержания от свежей растительной пищи и зелени». [158] [159] Цинга долгое время была основной причиной смерти моряков во время длительных морских путешествий. [160] По словам Джонатана Лэмба, «В 1499 году Васко да Гама потерял 116 человек из своей команды из 170 человек; В 1520 году Магеллан потерял 208 человек из 230; ... все в основном из-за цинги». [161]

Первую попытку дать научное обоснование причины этого заболевания предпринял корабельный хирург Королевского Джеймс флота Линд . Находясь в море в мае 1747 года, Линд снабжал некоторых членов экипажа двумя апельсинами и одним лимоном в день в дополнение к обычному рациону, в то время как другие продолжали получать сидр , уксус , серную кислоту или морскую воду вместе со своим обычным рационом в одном из первые в мире контролируемые эксперименты. [162] Результаты показали, что цитрусовые предотвращают заболевание. Линд опубликовал свою работу в 1753 году в «Трактате о цинге» . [163]
Свежие фрукты было дорого хранить на борту, тогда как вываривание их до сока позволяло легко хранить, но разрушало витамин (особенно, если их варили в медных котлах). [38] Это было в 1796 году, когда британский флот принял лимонный сок в качестве стандартного продукта на море. В 1845 году корабли в Вест-Индии вместо этого снабжались соком лайма , а в 1860 году сок лайма стал использоваться во всем Королевском флоте, что привело к тому, что американцы стали использовать прозвище «лайм» для британцев. [162] Капитан Джеймс Кук ранее продемонстрировал преимущества ношения на борту «кислой капусты» , взяв свою команду в путешествие по Тихому океану в 1772–1775 годах, не потеряв ни одного из своих людей из-за цинги. [164] За отчет о своих методах Британское королевское общество наградило его медалью Копли в 1776 году. [165]
Название противоцинготное средство использовалось в восемнадцатом и девятнадцатом веках для обозначения продуктов, которые, как известно, предотвращали цингу. В число этих продуктов входили лимоны, лаймы, апельсины, квашеная капуста, капуста, солод и портативный суп . [166] В 1928 году канадский арктический антрополог Вильялмур Стефанссон показал, что инуиты избегали цинги, питаясь преимущественно сырым мясом. Более поздние исследования традиционного пищевого рациона Юкона коренных народов , дене , инуитов и метисов Северной Канады показали, что их ежедневное потребление витамина С составляло в среднем от 52 до 62 мг/день. [167]
Открытие
[ редактировать ]Витамин С был открыт в 1912 году, выделен в 1928 году и синтезирован в 1933 году, что сделало его первым синтезированным витамином. [168] Вскоре после этого Тадеусу Райхштейну удалось синтезировать витамин в больших количествах с помощью того, что сейчас называется процессом Райхштейна . [169] Это сделало возможным недорогое массовое производство витамина С. В 1934 году Хоффманн-Ла Рош купила патент на процесс Райхштейна, зарегистрировала синтетический витамин С под торговой маркой Redoxon и начала продавать его как пищевую добавку. [170] [171]
обнаружили лабораторную модель животного, которая помогла бы идентифицировать году норвежские врачи Аксель Хольст и Теодор Фрёлих противоцинготный В фактор . 1907 бери-бери. Неизвестный в то время, этот вид не вырабатывает собственный витамин С (будучи кавиоморфом ) , в отличие от мышей и крыс. [172] В 1912 году польский биохимик Казимир Функ разработал концепцию витаминов . Считалось, что одним из них является противоцинготный фактор. В 1928 году его называли «водорастворимым С», хотя его химическая структура еще не была определена. [173]

С 1928 по 1932 год венгерская команда Альберта Сент-Дьёрдьи и Джозефа Л. Свирбели, а также американская команда Чарльза Глена Кинга выявили противоцинготный фактор. Сент-Дьёрдьи выделил гексуроновую кислоту из надпочечников животных и предположил, что она является противоцинготным фактором. [175] В конце 1931 года Сент-Дьёрдьи дал Свирбели остатки гексуроновой кислоты, полученной из надпочечников, предположив, что она может быть противоцинготным фактором. К весне 1932 года лаборатория Кинга доказала это, но опубликовала результат, не отдав должное Сент-Дьёрдьи. Это привело к ожесточенному спору о приоритете. [175] В 1933 году Уолтер Норман Хаворт химически определил витамин как l -гексуроновая кислота, доказав это синтезом в 1933 году. [176] [177] [178] [179] Хаворт и Сент-Дьёрдьи предложили называть L-гексуроновую кислоту а-скорбиновой кислотой, а по химическому составу l- аскорбиновая кислота в честь ее активности против цинги. [179] [168] Этимология этого термина происходит от латыни, где «a-» означает «вдали» или «от», а -scorbic происходит от средневекового латинского scorbuticus (относящегося к цинге), родственного древнескандинавскому skyrbjugr , французскому scorbut , голландскому scheurbuik и нижненемецкому scharbock . [180] Частично за это открытие Сент-Дьёрдьи был удостоен Нобелевской премии по медицине 1937 года . [174] того года и Хаворт разделили Нобелевскую премию по химии . [181]
В 1957 году Дж. Дж. Бернс показал, что некоторые млекопитающие подвержены цинге, поскольку их печень не вырабатывает фермент. L -гулонолактоноксидаза , последний из цепочки четырех ферментов, синтезирующих витамин С. [182] [183] Американский биохимик Ирвин Стоун был первым, кто использовал витамин С как консервант для пищевых продуктов. Позже он разработал идею о том, что люди обладают мутировавшей формой Ген, кодирующий l- гулонолактоноксидазу. [184] Стоун познакомил Лайнуса Полинга с теорией о том, что людям необходимо потреблять витамин С в количествах, намного превышающих рекомендуемую ежедневную дозу, чтобы оптимизировать здоровье. [185]
В 2008 году исследователи обнаружили, что у людей и других приматов эритроциты развили механизм, позволяющий более эффективно использовать витамин С, присутствующий в организме, путем переработки окисленного витамина С. L- дегидроаскорбиновая кислота (DHA) возвращается в аскорбиновую кислоту для повторного использования организмом. Этот механизм не был обнаружен у млекопитающих, которые синтезируют собственный витамин С. [186]
История терапии большими дозами
[ редактировать ]Мегадозировка витамина С — это термин, описывающий потребление или введение витамина С в дозах, сравнимых или превышающих количества, вырабатываемые печенью млекопитающих, способных синтезировать витамин С. Был описан аргумент в пользу этого, хотя и не сам термин. в 1970 году в статье Лайнуса Полинга . Вкратце, его позиция заключалась в том, что для оптимального здоровья люди должны потреблять не менее 2300 мг витамина С в день, чтобы компенсировать неспособность синтезировать витамин С. Рекомендация также подпадала под диапазон потребления для горилл — несинтезирующего близкого родственника человека. . [81] Вторым аргументом в пользу высокого потребления является то, что концентрация аскорбиновой кислоты в сыворотке увеличивается по мере увеличения потребления, пока не стабилизируется на уровне примерно 190–200 микромолей на литр (мкмоль/л), как только потребление превышает 1250 миллиграммов. [187] Как уже отмечалось, правительственные рекомендации предусматривают диапазон от 40 до 110 мг/день, а нормальная концентрация в плазме составляет примерно 50 мкмоль/л, поэтому «норма» составляет около 25% от того, что может быть достигнуто при пероральном приеме в предлагаемом диапазоне мегадоз.
Полинг популяризировал концепцию высоких доз витамина С для профилактики и лечения простуды в 1970 году. Несколько лет спустя он предположил, что витамин С предотвращает сердечно-сосудистые заболевания и что 10 граммов витамина С в день, вводимые сначала внутривенно, а затем перорально, излечивают. рак поздней стадии. [188] У мегадозирования аскорбиновой кислоты есть и другие чемпионы, среди них химик Ирвин Стоун. [185] и спорные Маттиас Рат и Патрик Холфорд , которых обвиняют в необоснованных заявлениях о лечении рака и ВИЧ- инфекции. [189] [190] Идея о том, что большие количества аскорбиновой кислоты внутривенно можно использовать для лечения рака на поздних стадиях или снижения токсичности химиотерапии, — спустя примерно сорок лет после основополагающей статьи Полинга — все еще считается недоказанной и все еще нуждается в высококачественных исследованиях. [191] [192] [149]
Направления исследований
[ редактировать ]Рак
[ редактировать ]Существуют исследования, изучающие, будет ли внутривенное введение высоких доз витамина С в качестве сопутствующего лечения подавлять стволовые клетки рака , которые ответственны за рецидив опухоли, метастазирование и химиорезистентность. [193] [194] может существовать обратная зависимость Предварительные исследования предполагают, что между потреблением витамина С и раком легких . [195]
Старение кожи
[ редактировать ]Также продолжаются исследования по местному применению витамина С для предотвращения признаков старения кожи. Кожа человека физиологически содержит небольшое количество витамина С, который поддерживает синтез коллагена, уменьшает деградацию коллагена и способствует антиоксидантной защите от фотостарения, вызванного УФ-излучением, включая фотоканцерогенез . Эти знания часто используются в качестве обоснования для маркетинга витамина С в качестве ингредиента «сыворотки» для местного применения для предотвращения или лечения старения кожи лица, мелазмы (темных пигментных пятен) и морщин, однако эти утверждения необоснованны и не подтверждаются исследованиями. проведено до сих пор; предполагаемая эффективность местного лечения по сравнению с пероральным приемом плохо изучена. [196] [197] Предполагаемый механизм предполагаемой пользы местного применения витамина С для замедления старения кожи заключается в том, что витамин С действует как антиоксидант, нейтрализуя свободные радикалы от воздействия солнечного света, загрязнителей воздуха или нормальных метаболических процессов. [198] Литература по клиническим исследованиям характеризуется как недостаточная для подтверждения заявлений о полезности для здоровья; Одна из причин заключалась в том, что «во всех исследованиях витамин С использовался в сочетании с другими ингредиентами или терапевтическими механизмами, что усложняло любые конкретные выводы относительно эффективности витамина С». [199] [200]
Примечания
[ редактировать ]- ^ Двудольные растения переносят только двухвалентное железо (Fe 2+ ), но если железо циркулирует в виде трехвалентных комплексов (Fe 3+ ), он должен подвергнуться сокращению, прежде чем его можно будет активно транспортировать. Эмбрионы растений выделяют большое количество аскорбата, который химически восстанавливает железо(III) из комплексов железа. [94]
Ссылки
[ редактировать ]- ^ «Аскорбиновая кислота для инъекций 500мг/5мл» . (эмс) . 15 июля 2015 года. Архивировано из оригинала 14 октября 2020 года . Проверено 12 октября 2020 г.
- ^ «Аскорбиновая кислота таблетки 100 мг» . (эмс) . 29 октября 2018 года. Архивировано из оригинала 21 сентября 2020 года . Проверено 12 октября 2020 г.
- ^ «Аскор-аскорбиновая кислота для инъекций» . ДейлиМед . 2 октября 2020 г. Архивировано из оригинала 29 октября 2020 г. Проверено 12 октября 2020 г.
- ^ Jump up to: а б с д и «Витамин С: Информационный бюллетень для медицинских работников» . Управление пищевых добавок, Национальные институты здравоохранения США. 26 марта 2021 года. Архивировано из оригинала 30 июля 2017 года . Проверено 25 февраля 2024 г.
- ^ «Витамин С» . Химический паук . Королевское химическое общество. Архивировано из оригинала 24 июля 2020 года . Проверено 25 июля 2020 г.
- ^ Jump up to: а б с д и ж «Витамин С» . Информационный центр по микроэлементам, Институт Лайнуса Полинга, Университет штата Орегон, Корваллис, Орегон. 1 июля 2018 года. Архивировано из оригинала 12 июля 2019 года . Проверено 19 июня 2019 г.
- ^ Jump up to: а б с д и ж г час я дж к л м н тот п Комиссия Института медицины (США) по соединениям, родственным диетическим антиоксидантам (2000). «Витамин С» . Рекомендуемая диетическая норма витамина С, витамина Е, селена и каротиноидов . Вашингтон, округ Колумбия: Издательство национальных академий. стр. 95–185. дои : 10.17226/9810 . ISBN 978-0-309-06935-9 . ПМИД 25077263 . Архивировано из оригинала 2 сентября 2017 года . Проверено 1 сентября 2017 г.
- ^ Jump up to: а б с д и ж г Марриотт М.П., Бирт Д.Ф., Столлингс В.А., Йейтс А.А., ред. (2020). «Витамин С». Современные знания в области питания, одиннадцатое издание . Лондон, Великобритания: Academic Press (Elsevier). стр. 155–70. ISBN 978-0-323-66162-1 .
- ^ «Тестирование продуктов на содержание витамина С (аскорбиновой кислоты)» (PDF) . Британский фонд питания. 2004. Архивировано (PDF) из оригинала 23 ноября 2015 года.
- ^ «Измерение содержания витамина С в пищевых продуктах и фруктовых соках» . Фонд Наффилда. 24 ноября 2011 г. Архивировано из оригинала 21 июля 2015 г.
- ^ Jump up to: а б Шлейхер Р.Л., Кэрролл, доктор медицинских наук, Форд Э.С., Лачер Д.А. (ноябрь 2009 г.). «Сывороточный витамин C и распространенность дефицита витамина C в Соединенных Штатах: Национальное обследование здоровья и питания (NHANES) 2003-2004 гг.» . Американский журнал клинического питания . 90 (5): 1252–63. дои : 10.3945/ajcn.2008.27016 . ПМИД 19675106 .
- ^ Нарайанан С., Кумар С.С., Мангуво А., Фридман Э. (июнь 2021 г.). «Текущие оценки дефицита витамина С в сыворотке крови и витамина С в Соединенных Штатах» . Курр Дев Нутр . 7 (5): 1067. doi : 10.1093/cdn/nzab053_060 . ПМК 8180804 .
- ^ Роу С., Карр AC (июль 2020 г.). «Глобальный статус витамина С и распространенность его дефицита: повод для беспокойства?» . Питательные вещества . 12 (7): 2008. doi : 10.3390/nu12072008 . ПМК 7400810 . ПМИД 32640674 .
- ^ Эмади-Конджин П., Верджи З., Левин А.В., Адели К. (май 2005 г.). «Измерение внутриклеточных уровней витамина С в лимфоцитах человека методом обращенно-фазовой высокоэффективной жидкостной хроматографии (ВЭЖХ)». Клиническая биохимия . 38 (5): 450–6. doi : 10.1016/j.clinbiochem.2005.01.018 . ПМИД 15820776 .
- ^ «Диетические рекомендации для индийцев» (PDF) . Национальный институт питания, Индия. 2011. с. 90. Архивировано из оригинала (PDF) 22 декабря 2018 года . Проверено 10 февраля 2019 г.
- ^ Всемирная организация здравоохранения (2005). «Глава 7: Витамин С». Потребность в витаминах и минералах в питании человека (2-е изд.). Женева: Всемирная организация здравоохранения. hdl : 10665/42716 . ISBN 978-92-4-154612-6 .
- ^ «Директива Комиссии 2008/100/EC от 28 октября 2008 г., вносящая поправки в Директиву Совета 90/496/EEC о маркировке пищевых продуктов в отношении рекомендуемых суточных норм, коэффициентов преобразования энергии и определений» . Комиссия Европейских Сообществ. 29 октября 2008 г. Архивировано из оригинала 2 октября 2016 г.
- ^ «Витамин С» . Монография о натуральных продуктах для здоровья . Здоровье Канады. Архивировано из оригинала 3 апреля 2013 года.
- ^ Jump up to: а б «Обзор рекомендуемого рациона питания японцев» (PDF) . Министерство здравоохранения, труда и социального обеспечения (Япония) . 2015. с. 29. Архивировано (PDF) из оригинала 21 октября 2022 года . Проверено 19 августа 2021 г.
- ^ Jump up to: а б «Научное мнение о диетических нормах витамина С» . Журнал EFSA . 11 (11). Ноябрь 2013 г. doi : 10.2903/j.efsa.2013.3418 .
- ^ «ТАБЛИЦА 1: Потребление питательных веществ из продуктов питания и напитков» (PDF) . Национальное обследование здоровья и питания: что мы едим в Америке, интеграция диетического исследования DHHS-USDA . Центры по контролю и профилактике заболеваний Министерства здравоохранения и социальных служб США. Архивировано из оригинала (PDF) 24 февраля 2017 г.
- ^ «ТАБЛИЦА 37: Потребление питательных веществ из пищевых добавок» (PDF) . Национальное обследование здоровья и питания: что мы едим в Америке, интеграция диетического исследования DHHS-USDA . Центры по контролю и профилактике заболеваний Министерства здравоохранения и социальных служб США. Архивировано из оригинала (PDF) 6 октября 2017 г.
- ^ «Верхний допустимый уровень потребления витаминов и минералов» (PDF) . Европейское агентство по безопасности пищевых продуктов. 2006. Архивировано (PDF) из оригинала 16 марта 2016 года.
- ^ «Федеральный реестр, 27 мая 2016 г. Маркировка пищевых продуктов: пересмотр этикеток с информацией о пищевой ценности и пищевых добавках. Страница FR 33982» (PDF) . Архивировано (PDF) из оригинала 8 августа 2016 г.
- ^ «Справочник по дневной норме базы данных этикеток пищевых добавок (DSLD)» . База данных этикеток пищевых добавок (DSLD) . Архивировано из оригинала 7 апреля 2020 года . Проверено 16 мая 2020 г.
- ^ РЕГЛАМЕНТ (ЕС) № 1169/2011 ЕВРОПЕЙСКОГО ПАРЛАМЕНТА И СОВЕТА. Архивировано 26 июля 2017 г. в Wayback Machine Официальном журнале Европейского Союза . стр. 304/61. (2009).
- ^ «Домашняя страница базы данных о составе пищевых продуктов NDL/FNIC» . Лаборатория данных о питательных веществах Министерства сельского хозяйства США, Информационный центр по продуктам питания и питанию и Отдел информационных систем Национальной сельскохозяйственной библиотеки. Архивировано из оригинала 15 января 2023 года . Проверено 30 ноября 2014 г.
- ^ Jump up to: а б с «Национальная база данных питательных веществ Министерства сельского хозяйства США для стандартных справочных материалов: витамин С» (PDF) . Министерство сельского хозяйства США, Служба сельскохозяйственных исследований . 2018. Архивировано (PDF) из оригинала 18 ноября 2021 года . Проверено 27 сентября 2020 г.
- ^ Брэнд Дж.С., Рэй С., Макдоннелл Дж., Ли А., Черикофф В., Трасуэлл А.С. (1987). «Пищевой состав продуктов австралийских аборигенов. I». Пищевые технологии в Австралии . 35 (6): 293–6.
- ^ Джастис К.С., Визентейнер СП, Соуза Н., Мацусита М. (декабрь 2000 г.). «Пищевой состав и стабильность витамина С в хранящейся мякоти каму-каму ( Myrciaria dubia )». Латиноамериканские архивы питания . 50 (4): 405–8. ПМИД 11464674 .
- ^ Вендрамини А.Л., Труго Л.К. (2000). «Химический состав плодов ацеролы (Malpighia punicifolia L.) на трех стадиях зрелости». Пищевая химия . 71 (2): 195–8. дои : 10.1016/S0308-8146(00)00152-7 .
- ^ Бегум Р.М. (2008). Учебник по продуктам питания, питанию и диетологии . Стерлинг Паблишерс Пвт. ООО с. 72. ИСБН 978-81-207-3714-3 .
- ^ Синха Н., Сидху Дж., Барта Дж., Ву Дж., Кано, член парламента (2012). Справочник по фруктам и их переработке . Джон Уайли и сыновья. ISBN 978-1-118-35263-2 .
- ^ Гутцайт Д., Баляну Г., Винтерхальтер П., Йерц Г. (2008). «Содержание витамина С в ягодах облепихи (Hippophaë rhamnoides L. ssp. rhamnoides) и родственных продуктах: кинетическое исследование стабильности при хранении и определение эффектов обработки». J Food Sci . 73 (9): C615–C20. дои : 10.1111/j.1750-3841.2008.00957.x . ПМИД 19021790 .
- ^ Кларк С. (8 января 2007 г.). «Сравнение молока: человеческого, коровьего, козьего и коммерческих детских смесей» . Университет штата Вашингтон . Архивировано из оригинала 29 января 2007 года . Проверено 28 февраля 2007 г.
- ^ Ройг М.Г., Ривера З.С., Кеннеди Дж.Ф. (май 1995 г.). «Модельное исследование скорости разложения L-аскорбиновой кислоты во время обработки с использованием концентратов соков домашнего производства». Международный журнал пищевых наук и питания . 46 (2): 107–15. дои : 10.3109/09637489509012538 . ПМИД 7621082 .
- ^ Аллен М.А., Берджесс С.Г. (1950). «Потери аскорбиновой кислоты при массовой варке зеленых овощей разными способами» . Британский журнал питания . 4 (2–3): 95–100. дои : 10.1079/BJN19500024 . ПМИД 14801407 .
- ^ Jump up to: а б «Данные о безопасности (MSDS) аскорбиновой кислоты» . Оксфордский университет . 9 октября 2005 года. Архивировано из оригинала 9 февраля 2007 года . Проверено 21 февраля 2007 г.
- ^ Jump up to: а б с "Введение" . Обогащение продуктов продовольственной помощи витамином С: окончательный отчет . Издательство национальных академий (США). 1997. Архивировано из оригинала 21 января 2024 года . Проверено 3 января 2024 г.
- ^ Jump up to: а б с д «Аскорбиновая кислота (Монография)» . Американское общество фармацевтов системы здравоохранения. Архивировано из оригинала 30 декабря 2016 года . Проверено 8 декабря 2016 г.
- ^ Дэвис Дж.Л., Пэрис Х.Л., Билс Дж.В., Биннс С.Е., Джордано Г.Р., Скальцо Р.Л. и др. (2016). «Аскорбиновая кислота, инкапсулированная в липосомы: влияние на биодоступность витамина С и способность защищать от ишемически-реперфузионного повреждения» . Информация о питании и метаболизме . 9 : 25–30. дои : 10.4137/NMI.S39764 . ПМЦ 4915787 . ПМИД 27375360 .
- ^ «Зачем укреплять?» . Инициатива по обогащению пищевых продуктов . Декабрь 2023. Архивировано из оригинала 8 марта 2023 года . Проверено 3 января 2024 г.
- ^ Jump up to: а б «Карта: количество питательных веществ в стандартах обогащения» . Глобальный обмен данными по обогащению пищевых продуктов . Архивировано из оригинала 11 апреля 2019 года . Проверено 3 января 2024 г.
- ^ «Веб-сайт Бюро гуманитарной помощи USAID» . 21 ноября 2023 г.
- ^ Уошберн С., Дженсен С. (2017). «Предварительная обработка для предотвращения потемнения фруктов перед консервированием или обезвоживанием» . Университет штата Юта. Архивировано из оригинала 15 декабря 2020 года . Проверено 26 января 2020 г.
- ^ «Ингредиенты» . Федерация пекарей. Архивировано из оригинала 26 февраля 2021 года . Проверено 3 апреля 2021 г.
- ^ «Часто задаваемые вопросы | зачем пищевые добавки» . Ассоциация пищевых добавок и ингредиентов Великобритании и Ирландии – Делаем жизнь вкуснее . Архивировано из оригинала 1 июня 2019 года . Проверено 27 октября 2010 г.
- ^ Jump up to: а б с д и Агентство по пищевым стандартам Великобритании: «Разрешенные добавки и их номера E» . Архивировано из оригинала 7 октября 2010 года . Проверено 27 октября 2011 г.
- ^ Jump up to: а б с Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США: «Список статуса пищевых добавок, часть I» . Управление по контролю за продуктами и лекарствами . Архивировано из оригинала 17 января 2012 года . Проверено 27 октября 2011 г.
- ^ Jump up to: а б с д Здоровье Канады «Список разрешенных консервантов (списки разрешенных пищевых добавок) – Правительство Канады» . Правительство Канады . 27 ноября 2006 г. Архивировано из оригинала 27 октября 2022 г. Проверено 27 октября 2022 г.
- ^ Jump up to: а б с д и Кодекс пищевых стандартов Австралии и Новой Зеландии «Стандарт 1.2.4 – Маркировка ингредиентов» . 8 сентября 2011 года. Архивировано из оригинала 2 сентября 2013 года . Проверено 27 октября 2011 г.
- ^ «Список статусов пищевых добавок, часть II» . Управление по контролю за продуктами и лекарствами США . Архивировано из оригинала 8 ноября 2011 года . Проверено 27 октября 2011 г.
- ^ Беттгер Ф., Валлес-Марти А., Кан Л., Хименес Ч.Р. (октябрь 2021 г.). «Высокие дозы витамина С для внутривенного введения — многообещающий многоцелевой агент в лечении рака» . J Exp Clin Cancer Res . 40 (1): 343. doi : 10.1186/s13046-021-02134-y . ПМЦ 8557029 . ПМИД 34717701 .
- ^ Пак С, Ан С, Шин Й, Ян Й, Ём CH (2018). «Витамин С при раке: взгляд на метаболизм» . Фронт Физиол . 9 : 762. дои : 10.3389/fphys.2018.00762 . ПМК 6018397 . ПМИД 29971019 .
- ^ Jump up to: а б Сидери О, Цаусис К.Т., Ли Х.Дж., Вискадураки М., Цинопулос И.Т. (2019). «Потенциальная роль питания в патологии хрусталика: систематический обзор и метаанализ». Сурв Офтальмол . 64 (5): 668–78. doi : 10.1016/j.survophthal.2019.03.003 . ПМИД 30878580 . S2CID 81981938 .
- ^ Ликкесфельдт Дж., Тведен-Нюборг П. (октябрь 2019 г.). «Фармакокинетика витамина С» . Питательные вещества . 11 (10): 2412. дои : 10.3390/nu11102412 . ПМЦ 6835439 . ПМИД 31601028 .
- ^ Jump up to: а б Савини И, Росси А, Пьеро С, Авильяно Л, Катани М.В. (апрель 2008 г.). «SVCT1 и SVCT2: ключевые белки для усвоения витамина С». Аминокислоты . 34 (3): 347–55. дои : 10.1007/s00726-007-0555-7 . ПМИД 17541511 . S2CID 312905 .
- ^ Рамси С.К., Квон О., Сюй Г.В., Бурант К.Ф., Симпсон И., Левин М. (июль 1997 г.). «Изоформы переносчиков глюкозы GLUT1 и GLUT3 транспортируют дегидроаскорбиновую кислоту» . Журнал биологической химии . 272 (30): 18982–9. дои : 10.1074/jbc.272.30.18982 . ПМИД 9228080 .
- ^ Jump up to: а б с Линстер К.Л., Ван Шафтинген Э. (январь 2007 г.). «Витамин С. Биосинтез, переработка и деградация у млекопитающих» . Журнал ФЭБС . 274 (1): 1–22. дои : 10.1111/j.1742-4658.2006.05607.x . ПМИД 17222174 . S2CID 21345196 .
- ^ Мэй Дж.М., Цюй З.К., Нил Д.Р., Ли Х (май 2003 г.). «Переработка витамина С из его окисленных форм эндотелиальными клетками человека». Biochimica et Biophysical Acta (BBA) - Исследования молекулярных клеток . 1640 (2–3): 153–61. дои : 10.1016/S0167-4889(03)00043-0 . ПМИД 12729925 .
- ^ Jump up to: а б Падаятти С.Дж., Левин М. (сентябрь 2016 г.). «Витамин С: известное, неизвестное и Златовласка» . Заболевания полости рта . 22 (6): 463–93. дои : 10.1111/odi.12446 . ПМЦ 4959991 . ПМИД 26808119 .
- ^ Брандуарди П., Фоссати Т., Зауэр М., Пагани Р., Маттанович Д., Порро Д. (октябрь 2007 г.). «Биосинтез витамина С дрожжами приводит к повышению стрессоустойчивости» . ПЛОС ОДИН . 2 (10): е1092. Бибкод : 2007PLoSO...2.1092B . дои : 10.1371/journal.pone.0001092 . ПМК 2034532 . ПМИД 17971855 .
- ^ Уиллер Г.Л., Джонс М.А., Смирнофф Н. (май 1998 г.). «Путь биосинтеза витамина С у высших растений». Природа . 393 (6683): 365–9. Бибкод : 1998Natur.393..365W . дои : 10.1038/30728 . ПМИД 9620799 . S2CID 4421568 .
- ^ Jump up to: а б с Камень I (1972). «Естественная история аскорбиновой кислоты в эволюции млекопитающих и приматов и ее значение для современной человеческой эволюции млекопитающих и приматов» (PDF) . Журнал ортомолекулярной психиатрии . 1 (2): 82–9. Архивировано (PDF) оригинала 2 октября 2023 г. Проверено 31 декабря 2023 г.
- ^ Банхедьи Г., Мандл Дж (2001). «Печеночная гликогеноретикулярная система». Патологические и онкологические исследования . 7 (2): 107–10. CiteSeerX 10.1.1.602.5659 . дои : 10.1007/BF03032575 . ПМИД 11458272 . S2CID 20139913 .
- ^ Jump up to: а б Вальпуэста В., Ботелла М.А. (2004). «Биосинтез L-аскорбиновой кислоты в растениях: новые пути использования старого антиоксиданта» (PDF) . Тенденции в науке о растениях . 9 (12): 573–7. Бибкод : 2004TPS.....9..573В . doi : 10.1016/j.tplants.2004.10.002 . ПМИД 15564123 . Архивировано (PDF) из оригинала 25 декабря 2020 г. Проверено 8 октября 2018 г.
- ^ Нисикими М., Яги К. (декабрь 1991 г.). «Молекулярные основы дефицита у человека гулонолактоноксидазы, ключевого фермента биосинтеза аскорбиновой кислоты» . Amer J Clin Nutr . 54 (6 Доп.): 1203С–8С. дои : 10.1093/ajcn/54.6.1203s . ПМИД 1962571 .
- ^ Нисикими М., Каваи Т., Яги К. (октябрь 1992 г.). «Морские свинки обладают сильно мутированным геном L-гулоно-гамма-лактоноксидазы, ключевого фермента биосинтеза L-аскорбиновой кислоты, отсутствующего у этого вида» . Журнал биологической химии . 267 (30): 21967–72. дои : 10.1016/S0021-9258(19)36707-9 . ПМИД 1400507 .
- ^ Охта Ю., Нисикими М. (октябрь 1999 г.). «Случайные нуклеотидные замены в нефункциональном гене приматов L-гулоно-гамма-лактоноксидазы, недостающего фермента в биосинтезе L-аскорбиновой кислоты». Biochimica et Biophysical Acta (BBA) – Общие предметы . 1472 (1–2): 408–11. дои : 10.1016/S0304-4165(99)00123-3 . ПМИД 10572964 .
- ^ Ван С., Берге Г.Е., Сунд Р.Б. (август 2001 г.). «Концентрация аскорбиновой кислоты в плазме у здоровых собак». Рез. Ветеринар. Наука . 71 (1): 33–5. дои : 10.1053/rvsc.2001.0481 . ПМИД 11666145 .
- ^ Ранджан Р., Ранджан А., Даливал Г.С., Патра Р.К. (2012). «Добавка l-аскорбиновой кислоты (витамина С) для оптимизации здоровья и воспроизводства крупного рогатого скота». Ветеринар К. 32 (3–4): 145–50. дои : 10.1080/01652176.2012.734640 . ПМИД 23078207 . S2CID 1674389 .
- ^ Jump up to: а б с Дьюик ПМ (2009). Лекарственные натуральные продукты: биосинтетический подход (3-е изд.). Джон Уайли и сыновья. п. 493. ИСБН 978-0-470-74167-2 .
- ^ Миллер Р.Э., Фаулер М.Э. (2014). Зоопарк Фаулера и медицина диких животных, том 8 . Elsevier Науки о здоровье. п. 389. ИСБН 978-1-4557-7399-2 . Архивировано из оригинала 7 декабря 2016 года . Проверено 2 июня 2016 г.
- ^ Дженнесс Р., Бирни Э., Аяз К. (1980). «Изменение активности l-гулонолактоноксидазы у плацентарных млекопитающих». Сравнительная биохимия и физиология Б . 67 (2): 195–204. дои : 10.1016/0305-0491(80)90131-5 .
- ^ Цуй Дж., Пан Ю.Х., Чжан Ю., Джонс Дж., Чжан С. (февраль 2011 г.). «Прогрессивная псевдогенизация: синтез витамина С и его потеря у летучих мышей» . Молекулярная биология и эволюция . 28 (2): 1025–31. дои : 10.1093/molbev/msq286 . ПМИД 21037206 .
- ^ Цуй Дж, Юань Х, Ван Л, Джонс Дж, Чжан С (ноябрь 2011 г.). «Недавняя потеря способности к биосинтезу витамина С у летучих мышей» . ПЛОС ОДИН . 6 (11): e27114. Бибкод : 2011PLoSO...627114C . дои : 10.1371/journal.pone.0027114 . ПМК 3206078 . ПМИД 22069493 .
- ^ Мартинес дель Рио С (июль 1997 г.). «Могут ли воробьиные синтезировать витамин С?» . Аук . 114 (3): 513–6. дои : 10.2307/4089257 . JSTOR 4089257 .
- ^ Jump up to: а б с Друэн Дж., Годен-младший, Пейдж Б. (август 2011 г.). «Генетика потери витамина С у позвоночных» . Современная геномика . 12 (5): 371–8. дои : 10.2174/138920211796429736 . ПМК 3145266 . ПМИД 22294879 .
- ^ Берра ТМ (2008). Распространение пресноводной рыбы . Издательство Чикагского университета . п. 55. ИСБН 978-0-226-04443-9 .
- ^ Милтон К. (июнь 1999 г.). «Пищевые характеристики продуктов диких приматов: есть ли для нас уроки в рационе наших ближайших ныне живущих родственников?» (PDF) . Питание . 15 (6): 488–98. CiteSeerX 10.1.1.564.1533 . дои : 10.1016/S0899-9007(99)00078-7 . ПМИД 10378206 . Архивировано (PDF) из оригинала 10 августа 2017 г.
- ^ Jump up to: а б Полинг Л. (декабрь 1970 г.). «Эволюция и потребность в аскорбиновой кислоте» . Труды Национальной академии наук Соединенных Штатов Америки . 67 (4): 1643–8. Бибкод : 1970PNAS...67.1643P . дои : 10.1073/pnas.67.4.1643 . ПМК 283405 . ПМИД 5275366 .
- ^ Пэррот Т. (октябрь 2022 г.). «Пищевые болезни нечеловекообразных приматов» . Ветеринарное руководство Merck . Архивировано из оригинала 24 декабря 2023 года . Проверено 24 декабря 2023 г.
- ^ Лашапель М.Ю., Друэн Дж. (февраль 2011 г.). «Даты инактивации генов витамина С человека и морских свинок». Генетика . 139 (2): 199–207. дои : 10.1007/s10709-010-9537-x . ПМИД 21140195 . S2CID 7747147 .
- ^ Ян Х (июнь 2013 г.). «Консервация или утрата: молекулярная эволюция ключевого гена GULO в биосинтезе витамина С у позвоночных». Биохимическая генетика . 51 (5–6): 413–25. дои : 10.1007/s10528-013-9574-0 . ПМИД 23404229 . S2CID 14393449 .
- ^ Чжан З.Д., Фрэнкиш А., Хант Т., Харроу Дж., Герштейн М. (2010). «Идентификация и анализ унитарных псевдогенов: исторические и современные потери генов у человека и других приматов» . Геномная биология . 11 (3): Р26. дои : 10.1186/gb-2010-11-3-r26 . ПМЦ 2864566 . ПМИД 20210993 .
- ^ Кошизака Т., Нисикими М., Одзава Т., Яги К. (февраль 1988 г.). «Выделение и анализ последовательности комплементарной ДНК, кодирующей L-гулоно-гамма-лактоноксидазу печени крысы, ключевой фермент биосинтеза L-аскорбиновой кислоты» . Журнал биологической химии . 263 (4): 1619–21. дои : 10.1016/S0021-9258(19)77923-X . ПМИД 3338984 .
- ^ Jump up to: а б Поллок Дж.И., Маллин Р.Дж. (1987). «Биосинтез витамина С у полуобезьян: доказательства родства Tarsius с антропоидами». Американский журнал физической антропологии . 73 (1): 65–70. дои : 10.1002/ajpa.1330730106 . ПМИД 3113259 .
- ^ Пу С., Дузери Э.Дж. (2004). «Филогения приматов, изменения скорости эволюции и время дивергенции: вклад ядерного гена IRBP». Американский журнал физической антропологии . 124 (1): 01–16. дои : 10.1002/ajpa.10322 . ПМИД 15085543 .
- ^ Гудман М., Портер К.А., Челюсняк Дж., Пейдж С.Л., Шнайдер Х., Шошани Дж. и др. (июнь 1998 г.). «К филогенетической классификации приматов, основанной на данных ДНК, дополненных данными окаменелостей». Молекулярная филогенетика и эволюция . 9 (3): 585–98. Бибкод : 1998МОЛПЭ...9..585Г . дои : 10.1006/mpev.1998.0495 . ПМИД 9668008 . S2CID 23525774 .
- ^ Портер К.А., Пейдж С.Л., Челюсняк Дж., Шнайдер Х., Шнайдер М.П., Сампайо И. и др. (апрель 1997 г.). «Филогения и эволюция выбранных приматов, определяемая последовательностями локуса ε-глобина и 5'-фланкирующих областей». Инт Дж Приматол . 18 (2): 261–95. дои : 10.1023/А:1026328804319 . hdl : 2027.42/44561 . S2CID 1851788 .
- ^ Проктор П. (1970). «Похожие функции мочевой кислоты и аскорбата у человека?» . Природа . 228 (5274): 868. Бибкод : 1970Natur.228..868P . дои : 10.1038/228868a0 . ПМИД 5477017 . S2CID 4146946 .
- ^ Леферинк Н.Г., ван ден Берг В.А., ван Беркель В.Дж. (февраль 2008 г.). «L-галактоно-гамма-лактондегидрогеназа из Arabidopsis thaliana, флавопротеин, участвующий в биосинтезе витамина С» . Журнал ФЭБС . 275 (4): 713–26. дои : 10.1111/j.1742-4658.2007.06233.x . ПМИД 18190525 . S2CID 25096297 .
- ^ Миеда Т., Ябута Ю., Раполу М., Мотоки Т., Такеда Т., Йошимура К. и др. (сентябрь 2004 г.). «Ингибирование L-галактозодегидрогеназы шпината с помощью L-аскорбата» . Физиология растений и клеток . 45 (9): 1271–9. дои : 10.1093/pcp/pch152 . ПМИД 15509850 .
- ^ Грилье Л., Уэрдан Л., Флис П., Хоанг М.Т., Исауре М.П., Лобински Р. и др. (январь 2014 г.). «Выброс аскорбата как новая стратегия восстановления и транспорта железа в растениях» . Журнал биологической химии . 289 (5): 2515–25. дои : 10.1074/jbc.M113.514828 . ПМЦ 3908387 . ПМИД 24347170 .
- ^ Jump up to: а б с Галли ДР (2013). «L-аскорбиновая кислота: многофункциональная молекула, поддерживающая рост и развитие растений» . Научка . 2013 : 1–24. дои : 10.1155/2013/795964 . ПМЦ 3820358 . ПМИД 24278786 .
- ^ Jump up to: а б с Меллиду И, Канеллис АК (2017). «Генетический контроль биосинтеза и переработки аскорбиновой кислоты в садовых культурах» . Границы в химии . 5 : 50. Бибкод : 2017FrCh....5...50M . дои : 10.3389/fchem.2017.00050 . ПМК 5504230 . ПМИД 28744455 .
- ^ Булли С., Лэнг В. (октябрь 2016 г.). «Регуляция биосинтеза аскорбата». Современное мнение в области биологии растений . SI: 33: Передача сигналов в клетках и регуляция генов, 2016. 33 : 15–22. Бибкод : 2016COPB...33...15B . дои : 10.1016/j.pbi.2016.04.010 . ПМИД 27179323 .
- ^ Эггерсдорфер М., Лаудерт Д., Летинуа Ю., МакКлимонт Т., Медлок Дж., Нетшер Т. и др. (декабрь 2012 г.). «Сто лет витаминов – история успеха естественных наук». Ангеванде Хеми . 51 (52): 12960–12990. дои : 10.1002/anie.201205886 . ПМИД 23208776 .
- ^ «Производство витамина С» (PDF) . Конкурсная комиссия. 2001. Архивировано из оригинала (PDF) 19 января 2012 года . Проверено 20 февраля 2007 г.
- ^ Чжоу М, Би Ю, Дин М, Юань Ю (2021). «Одностадийный биосинтез витамина С в Saccharomyces cerevisiae» . Передний микробиол . 12 : 643472. doi : 10.3389/fmicb.2021.643472 . ПМЦ 7947327 . ПМИД 33717042 .
- ^ Тянь Ю.С., Дэн Ю.Д., Чжан В.Х., Ю-Ван, Сюй Дж., Гао Дж.Дж. и др. (август 2022 г.). «Метаболическая инженерия Escherichia coli для прямого производства витамина С из D-глюкозы» . Биотехнологии Биотопливо Биопрод . 15 (1): 86. Бибкод : 2022BBB....15...86T . дои : 10.1186/s13068-022-02184-0 . ПМЦ 9396866 . ПМИД 35996146 .
- ^ «Исследование рынка Vantage: размер и доля мирового рынка витамина С превысят 1,8 миллиарда долларов к 2028 году» . Globe Newswire (Пресс-релиз). 8 ноября 2022 года. Архивировано из оригинала 21 декабря 2023 года . Проверено 21 декабря 2023 г.
- ^ «Тенденция и прогноз цен на витамин С» . Химический аналитик . Сентябрь 2023. Архивировано из оригинала 21 декабря 2023 года . Проверено 21 декабря 2023 г.
- ^ Белакович Г., Николова Д., Глуд Л.Л., Симонетти Р.Г., Глууд С. (март 2012 г.). «Антиоксидантные добавки для профилактики смертности здоровых участников и пациентов с различными заболеваниями» . Кокрановская база данных систематических обзоров . 2012 (3): CD007176. дои : 10.1002/14651858.CD007176.pub2 . hdl : 10138/136201 . ПМЦ 8407395 . ПМИД 22419320 .
- ^ Всемирная организация здравоохранения (2009). Стюарт М.К., Куимци М., Хилл С.Р. (ред.). Модельный формуляр ВОЗ 2008 г. Всемирная организация здравоохранения. hdl : 10665/44053 . ISBN 978-92-4-154765-9 .
- ^ «Аскорбиновая кислота – статистика применения лекарств» . КлинКальк . Архивировано из оригинала 18 января 2024 года . Проверено 14 января 2024 г.
- ^ Магиоркинис Э., Белукас А., Диамантис А. (апрель 2011 г.). «Цинга: прошлое, настоящее и будущее». Европейский журнал внутренней медицины . 22 (2): 147–52. дои : 10.1016/j.ejim.2010.10.006 . ПМИД 21402244 .
- ^ Ходжес Р.Э., Бейкер Э.М., Худ Дж., Зауберлих Х.Э., Марч СК (май 1969 г.). «Экспериментальная цинга у человека». Американский журнал клинического питания . 22 (5): 535–48. дои : 10.1093/ajcn/22.5.535 . ПМИД 4977512 .
- ^ Пембертон Дж (июнь 2006 г.). «Медицинские эксперименты, проведенные в Шеффилде над отказниками от военной службы по убеждениям во время войны 1939-45 годов» . Международный журнал эпидемиологии . 35 (3): 556–8. дои : 10.1093/ije/dyl020 . ПМИД 16510534 .
- ^ Бельский Дж.Б., Вира Ч.Р., Джейкоб В., Сатер Дж.Э., Ли П.Дж. (декабрь 2018 г.). «Обзор микроэлементов при сепсисе: роль тиамина, L-карнитина, витамина С, селена и витамина D». Обзоры исследований в области питания . 31 (2): 281–90. дои : 10.1017/S0954422418000124 . ПМИД 29984680 . S2CID 51599526 .
- ^ Jump up to: а б Лян Б., Су Дж, Шао Х, Чен Х, Се Б (март 2023 г.). «Результаты внутривенной терапии витамином С у пациентов с сепсисом или септическим шоком: метаанализ рандомизированных контролируемых исследований» . Критический уход . 27 (1): 109. дои : 10.1186/s13054-023-04392-y . ПМЦ 10012592 . ПМИД 36915173 .
- ^ Бергер М.М., Одеманс-ван Страатен Х.М. (март 2015 г.). «Добавка витамина С тяжелобольным пациентам». Curr Opin Clin Nutr Metab Care . 18 (2): 193–201. дои : 10.1097/MCO.0000000000000148 . ПМИД 25635594 . S2CID 37895257 .
- ^ Сюй С, Йи Т, Тан С, Сюй Х, Ху Ю, Ма Дж и др. (апрель 2023 г.). «Связь перорального или внутривенного приема витамина С со смертностью: систематический обзор и метаанализ» . Питательные вещества . 15 (8): 1848. doi : 10.3390/nu15081848 . ПМЦ 10146309 . ПМИД 37111066 .
- ^ Лян Х., Му Ц., Сунь В., Лю Л., Цю С., Сюй З. и др. (2023). «Влияние внутривенного введения витамина С на взрослых пациентов с сепсисом: систематический обзор и метаанализ» . Передняя гайка . 10 : 1211194. дои : 10.3389/fnut.2023.1211194 . ПМЦ 10437115 . ПМИД 37599680 .
- ^ Jump up to: а б Хемила Х., Чалкер Э. (январь 2013 г.). «Витамин С для профилактики и лечения простуды» . Кокрановская база данных систематических обзоров . 2013 (1): CD000980. дои : 10.1002/14651858.CD000980.pub4 . ПМК 1160577 . ПМИД 23440782 .
- ^ Хемила Х., Чалкер Э. (декабрь 2023 г.). «Витамин С снижает тяжесть простудных заболеваний: метаанализ» . BMC Общественное здравоохранение . 23 (1): 2468. doi : 10.1186/s12889-023-17229-8 . ПМЦ 10712193 . ПМИД 38082300 .
- ^ Винтергерст Э.С., Маггини С., Хорниг Д.Х. (2006). «Иммуноукрепляющая роль витамина С и цинка и влияние на клинические состояния» (PDF) . Анналы питания и обмена веществ . 50 (2): 85–94. дои : 10.1159/000090495 . ПМИД 16373990 . S2CID 21756498 . Архивировано (PDF) из оригинала 22 июля 2018 г. Проверено 25 августа 2019 г.
- ^ Комиссия EFSA по диетическим продуктам, питанию и аллергии (2009 г.). «Научное заключение по обоснованию заявлений о пользе витамина С и защите ДНК, белков и липидов от окислительного повреждения (ID 129, 138, 143, 148), антиоксидантной функции лютеина (ID 146), поддержании зрения (ID 141) , 142), образование коллагена (ID 130, 131, 136, 137, 149), функция нервной системы (ID 133), функция иммунной системы (ID 134), функция иммунной системы во время и после экстремальных физических нагрузок (ID 144), абсорбция негемового железа (ID 132, 147), энергетический метаболизм (ID 135) и облегчение при раздражении верхних дыхательных путей (ID 1714, 1715) в соответствии со статьей 13(1) Регламента (ЕС) № 1924/2006» . Журнал EFSA . 7 (9): 1226. doi : 10.2903/j.efsa.2009.1226 .
- ^ Группа EFSA по диетическим продуктам, питанию и аллергии (2015 г.). «Витамин С и вклад в нормальную функцию иммунной системы: оценка заявления о здоровье в соответствии со статьей 14 Регламента (ЕС) № 1924/2006» . Журнал EFSA . 13 (11): 4298. doi : 10.2903/j.efsa.2015.4298 . hdl : 11380/1296052 .
- ^ Брамстедт К.А. (октябрь 2020 г.). «Какашки единорога и благословенные воды: шарлатанство о COVID-19 и предупреждающие письма FDA» . Ther Innov Regul Sci . 55 (1): 239–44. дои : 10.1007/s43441-020-00224-1 . ПМЦ 7528445 . ПМИД 33001378 .
- ^ «Витамин С» . Рекомендации по лечению COVID-19 . 21 апреля 2021 года. Архивировано из оригинала 20 ноября 2021 года . Проверено 2 января 2022 г.
- ^ «Руководство по лечению COVID-19» . Национальные институты здравоохранения США . 26 декабря 2022 года. Архивировано из оригинала 20 ноября 2021 года . Проверено 18 декабря 2023 г.
- ^ Jump up to: а б с д Коу К.С., Хасан С.С., Рамачандрам Д.С. (декабрь 2023 г.). «Влияние витамина С на риск смертности у пациентов с COVID-19: систематический обзор и метаанализ рандомизированных контролируемых исследований» . Инфламмофармакология . 31 (6): 3357–62. дои : 10.1007/s10787-023-01200-5 . ПМЦ 10111321 . ПМИД 37071316 .
- ^ Jump up to: а б с Хуан Вайоминг, Хун Дж., Ан Си, Хан Б.К., Ким Ю.Дж. (декабрь 2022 г.). «Связь лечения витамином С с клиническими результатами у пациентов с COVID-19: систематический обзор и метаанализ» . Здравоохранение . 10 (12): 2456. doi : 10.3390/healthcare10122456 . ПМЦ 9777834 . ПМИД 36553979 .
- ^ Jump up to: а б с Ольчак-Прук М., Свечковски Д., Ладни Дж.Р., Прюк М., Хуарес-Вела Р., Рафик З. и др. (октябрь 2022 г.). «Добавка витамина С для лечения COVID-19: систематический обзор и метаанализ» . Питательные вещества . 14 (19): 4217. дои : 10.3390/nu14194217 . ПМЦ 9570769 . ПМИД 36235869 .
- ^ Кортес-Жофре М., Руэда Х.Р., Асенхо-Лобос К., Мадрид Е., Бонфилл Косп X (март 2020 г.). «Препараты для профилактики рака легких у здоровых людей» . Кокрановская база данных систематических обзоров . 2020 (3): CD002141. дои : 10.1002/14651858.CD002141.pub3 . ПМК 7059884 . ПМИД 32130738 .
- ^ Страттон Дж., Годвин М. (июнь 2011 г.). «Влияние дополнительных витаминов и минералов на развитие рака простаты: систематический обзор и метаанализ» . Семейная практика . 28 (3): 243–52. дои : 10.1093/fampra/cmq115 . ПМИД 21273283 .
- ^ Heine-Bröring RC, Winkels RM, Renkema JM, Kragt L, van Orten-Luiten AC, Tigchelaar EF и др. (май 2015 г.). «Употребление пищевых добавок и риск колоректального рака: систематический обзор и метаанализ проспективных когортных исследований». Инт Дж Рак . 136 (10): 2388–401. дои : 10.1002/ijc.29277 . ПМИД 25335850 . S2CID 44706004 .
- ^ Фулан Х., Чансин Дж., Байна В.Ю., Вэньцуй З., Чуньцин Л., Фань В. и др. (октябрь 2011 г.). «Ретинол, витамины А, С и Е и риск рака молочной железы: метаанализ и метарегрессия». Причины рака и борьба с ним . 22 (10): 1383–96. дои : 10.1007/s10552-011-9811-y . ПМИД 21761132 . S2CID 24867472 .
- ^ Аль-Худайри Л., Флауэрс Н., Уилхаус Р., Ганнам О., Хартли Л., Стрэнджс С. и др. (март 2017 г.). «Добавка витамина С для первичной профилактики сердечно-сосудистых заболеваний» . Кокрановская база данных систематических обзоров . 2017 (3): CD011114. дои : 10.1002/14651858.CD011114.pub2 . ПМК 6464316 . ПМИД 28301692 .
- ^ Чен Г.К., Лу Д.Б., Пан З., Лю Ц.Ф. (ноябрь 2013 г.). «Потребление витамина С, циркулирующий витамин С и риск инсульта: метаанализ проспективных исследований» . J Am Heart Assoc . 2 (6): e000329. дои : 10.1161/JAHA.113.000329 . ПМЦ 3886767 . ПМИД 24284213 .
- ^ Ашор А.В., Лара Дж., Мазерс Дж.К., Сиерво М. (июль 2014 г.). «Влияние витамина С на функцию эндотелия в здоровье и при заболеваниях: систематический обзор и метаанализ рандомизированных контролируемых исследований». Атеросклероз . 235 (1): 9–20. doi : 10.1016/j.atherosclerosis.2014.04.004 . ПМИД 24792921 .
- ^ Ран Л., Чжао В., Тан Х., Ван Х., Мизуно К., Такаги К. и др. (апрель 2020 г.). «Связь между витамином С в сыворотке и артериальным давлением: систематический обзор и метаанализ наблюдательных исследований» . Кардиоваск Тер . 2020 : 4940673. doi : 10.1155/2020/4940673 . ПМЦ 7211237 . ПМИД 32426036 .
- ^ Jump up to: а б Гуань Ю, Дай П, Ван Х (февраль 2020 г.). «Влияние добавок витамина С на эссенциальную гипертонию: систематический обзор и метаанализ» . Медицина (Балтимор) . 99 (8): e19274. дои : 10.1097/MD.0000000000019274 . ПМК 7034722 . ПМИД 32080138 .
- ^ Лббан Э., Квон К., Ашор А., Стефан Б., Идрис И., Цинцас К. и др. (декабрь 2023 г.). «Добавка витамина С показала большее влияние на систолическое артериальное давление у пациентов с гипертонической болезнью и диабетом: обновленный систематический обзор и метаанализ рандомизированных клинических исследований» . Int J Food Sci Nutr . 74 (8): 814–25. дои : 10.1080/09637486.2023.2264549 . ПМИД 37791386 . S2CID 263621742 . Архивировано из оригинала 21 января 2024 года . Проверено 23 декабря 2023 г.
- ^ Мейсон С.А., Кеске М.А., Уодли Г.Д. (февраль 2021 г.). «Влияние добавок витамина С на гликемический контроль и факторы риска сердечно-сосудистых заболеваний у людей с диабетом 2 типа: систематический обзор и метаанализ рандомизированных контролируемых исследований с оценкой GRADE» . Уход при диабете . 44 (2): 618–30. дои : 10.2337/dc20-1893 . hdl : 10536/DRO/DU:30147432 . ПМИД 33472962 . Архивировано из оригинала 21 января 2024 года . Проверено 21 декабря 2023 г.
- ^ Носратабади С., Аштари-Ларки Д., Хоссейни Ф., Намкха З., Мохаммади С., Саламат С. и др. (август 2023 г.). «Влияние добавок витамина С на гликемический контроль у пациентов с диабетом 2 типа: систематический обзор и метаанализ». Диабет и метаболический синдром . 17 (8): 102824. doi : 10.1016/j.dsx.2023.102824 . ПМИД 37523928 . S2CID 259581695 .
- ^ ДеЛогери Т.Г. (март 2017 г.). «Железодефицитная анемия». Med Clin North Am (обзор). 101 (2): 319–32. дои : 10.1016/j.mcna.2016.09.004 . ПМИД 28189173 .
- ^ Лопес да Силва С., Веллас Б., Элеманс С., Лухсингер Дж., Камфуис П., Яффе К. и др. (2014). «Статус питательных веществ в плазме пациентов с болезнью Альцгеймера: систематический обзор и метаанализ» . Болезнь Альцгеймера и деменция . 10 (4): 485–502. дои : 10.1016/j.jalz.2013.05.1771 . ПМИД 24144963 .
- ^ Ли Ф.Дж., Шен Л., Цзи Х.Ф. (2012). «Диетическое потребление витамина Е, витамина С и β-каротина и риск болезни Альцгеймера: метаанализ». Журнал болезни Альцгеймера . 31 (2): 253–8. дои : 10.3233/JAD-2012-120349 . ПМИД 22543848 .
- ^ Харрисон Ф.Е. (2012). «Критический обзор витамина С для профилактики возрастного снижения когнитивных функций и болезни Альцгеймера» . Журнал болезни Альцгеймера . 29 (4): 711–26. дои : 10.3233/JAD-2012-111853 . ПМЦ 3727637 . ПМИД 22366772 .
- ^ Цзян Х, Инь Ю, Ву ЧР, Лю Ю, Го Ф, Ли М и др. (январь 2019 г.). «Потребление диетических витаминов и каротиноидов и риск возрастной катаракты» . Ам Дж Клин Нутр . 109 (1): 43–54. doi : 10.1093/ajcn/nqy270 . ПМИД 30624584 .
- ^ Эванс-младший, Лоуренсон Дж.Г. (июль 2017 г.). «Антиоксидантные витаминно-минеральные добавки для профилактики возрастной макулярной дегенерации» . Cochrane Database Syst Rev. 2017 (7): CD000253. дои : 10.1002/14651858.CD000253.pub4 . ПМК 6483250 . ПМИД 28756617 .
- ^ Ми Н, Чжан М, Ин З, Линь Икс, Цзинь Ю (январь 2024 г.). «Потребление витаминов и заболевания пародонта: метаанализ наблюдательных исследований» . BMC Здоровье полости рта . 24 (1): 117. дои : 10.1186/s12903-024-03850-5 . ПМЦ 10799494 . ПМИД 38245765 .
- ^ Тада А., Миура Х. (июль 2019 г.). «Взаимосвязь между витамином С и заболеваниями пародонта: систематический обзор» . Int J Environ Res Public Health . 16 (14): 2472. doi : 10.3390/ijerph16142472 . ПМК 6678404 . ПМИД 31336735 .
- ^ Гудвин Дж. С., Тангум М. Р. (ноябрь 1998 г.). «Борьба с шарлатанством: отношение к добавкам микроэлементов в американской академической медицине». Архив внутренней медицины . 158 (20): 2187–91. дои : 10.1001/archinte.158.20.2187 . ПМИД 9818798 .
- ^ Найду К.А. (август 2003 г.). «Витамин С в здоровье и болезнях человека все еще остается загадкой? Обзор» (PDF) . Журнал питания . 2 (7): 7. дои : 10.1186/1475-2891-2-7 . ПМК 201008 . ПМИД 14498993 . Архивировано (PDF) из оригинала 18 сентября 2012 г.
- ^ Томас Л.Д., Элиндер К.Г., Тиселиус Х.Г., Волк А., Акессон А. (март 2013 г.). «Добавки аскорбиновой кислоты и заболеваемость камнями в почках среди мужчин: проспективное исследование» . JAMA Внутренняя медицина . 173 (5): 386–8. doi : 10.1001/jamainternmed.2013.2296 . ПМИД 23381591 .
- ^ Jump up to: а б Джейкобс С., Хаттон Б., Нг Т., Шорр Р., Клемонс М. (февраль 2015 г.). «Имеет ли значение пероральный или внутривенный аскорбат (витамин С) в лечении больных раком? Систематический обзор» . Онколог . 20 (2): 210–23. doi : 10.1634/теонколог.2014-0381 . ПМК 4319640 . ПМИД 25601965 .
- ^ Шреста Д.Б., Будхатоки П., Седхай Ю.Р., Мандал С.К., Шихракар С., Карки С. и др. (октябрь 2021 г.). «Витамин С у пациентов в критическом состоянии: обновленный систематический обзор и метаанализ» . Питательные вещества . 13 (10): 3564. дои : 10.3390/nu13103564 . ПМЦ 8539952 . ПМИД 34684565 .
- ^ Холфорд П., Карр А.С., Завари М., член парламента Вискайчипи (ноябрь 2021 г.). «Вмешательство витамина С при критической ситуации с COVID-19: прагматический обзор текущего уровня доказательств» . Жизнь . 11 (11): 1166. Бибкод : 2021Life...11.1166H . дои : 10.3390/life11111166 . ПМЦ 8624950 . ПМИД 34833042 .
- ^ Абобейкер А., Альцви А., Альраид А.Х. (декабрь 2020 г.). «Обзор возможной роли витамина С в лечении COVID-19» . Представитель Фармакол . 72 (6): 1517–28. дои : 10.1007/s43440-020-00176-1 . ПМЦ 7592143 . ПМИД 33113146 .
- ^ Линд Дж. (1772 г.). Трактат о цинге (3-е изд.). Лондон, Англия: Г. Пирч и В. Вудфолл. п. 285. Архивировано из оригинала 1 января 2016 года.
- ^ Эшхерст Дж., изд. (1881). Международная энциклопедия хирургии . Том. 1. Нью-Йорк, Нью-Йорк: Уильям Вуд и Ко. с. 278. Архивировано из оригинала 5 мая 2016 года.
- ^ Раджакумар К. (октябрь 2001 г.). «Детская цинга: историческая перспектива» . Педиатрия . 108 (4): Е76. CiteSeerX 10.1.1.566.5857 . дои : 10.1542/peds.108.4.e76 . ПМИД 11581484 . Архивировано из оригинала 4 сентября 2015 года.
Плывя дальше по восточному побережью Африки, они встретили местных торговцев, которые продавали им свежие апельсины. В течение шести дней после употребления апельсинов команда да Гамы полностью выздоровела.
- ^ Ливермор Х (2004). «Санта-Хелена, забытое португальское открытие» (PDF) . Estudos Em Homenagem a Luis Antonio de Oliveira Ramos [ Этюды в честь Луиса Антонио де Оливейры Рамоса. ]: 623–631. Архивировано из оригинала (PDF) 29 мая 2011 года.
По возвращении корабль Лопеса оставил его на острове Святой Елены, где с поразительной проницательностью и трудолюбием он сажал овощи и создавал питомники, благодаря которым проходящие корабли прекрасно питались. [...] Там были «дикие рощи» апельсинов, лимонов и других фруктов, созревавших круглый год, большие гранаты и инжир.
- ^ Вудалл Дж (1617 г.). Помощник хирурга . Лондон, Англия: Эдвард Гриффин. п. 89. Архивировано из оригинала 11 апреля 2016 года.
Succus Limonum, или сок лимонов... [является] самым ценным средством против цинги, когда-либо обнаруженным,[;] которое следует пить всегда; ...
- ^ Армстронг А. (1858 г.). «Наблюдения за морской гигиеной и цингой, особенно той, которая появилась позже во время полярного путешествия» . Британский и зарубежный медико-хирургический обзор: или Ежеквартальный журнал практической медицины и хирургии . 22 : 295–305.
- ^ Бахстрем Дж. Ф. (1734). о цинге ( Наблюдения на латыни). Лейден (голландский), Нидерланды: Конрад Вишоф. п. 16. Архивировано из оригинала 1 января 2016 года.
...но [эта беда] очень хорошо объясняется нашей [предполагаемой] причиной, которая заключается в отсутствии, нехватке и воздержании от свежих овощей,...
- ^ Лэмб Дж. (17 февраля 2011 г.). «Капитан Кук и бич цинги» . Британская история в глубине . Би-би-си. Архивировано из оригинала 21 февраля 2011 года.
- ^ Лэмб Дж (2001). Сохранение себя в южных морях, 1680–1840 гг . Издательство Чикагского университета. п. 117. ИСБН 978-0-226-46849-5 . Архивировано из оригинала 30 апреля 2016 года.
- ^ Jump up to: а б с Барон Дж. Х. (июнь 2009 г.). «Цинга моряков до и после Джеймса Линда - переоценка». Обзоры питания . 67 (6): 315–32. дои : 10.1111/j.1753-4887.2009.00205.x . ПМИД 19519673 . S2CID 20435128 .
- ^ Линд Дж. (1753 г.). Трактат о цинге . Лондон: А. Миллар. В издании своей работы 1757 года Линд обсуждает свой эксперимент, начиная с «Трактат о цинге» . п. 149. Архивировано из оригинала 20 марта 2016 года.
- ^ Биглхол Дж. Х., Кук Дж. Д., Эдвардс П. Р. (1999). Журналы капитана Кука . Хармондсворт [англ.]: Пингвин. ISBN 978-0-14-043647-1 .
- ^ «Медаль Копли, прошлые победители» . Королевское общество . Архивировано из оригинала 6 сентября 2015 года . Проверено 1 января 2024 г.
- ^ Рив Дж., Стивенс Д.А. (2006). «Путешествия Кука 1768–1780» . Флот и нация: влияние флота на современную Австралию . Академик Аллена и Анвина. п. 74. ИСБН 978-1-74114-200-6 .
- ^ Кунляйн Х.В., Ресевер О., Суэйда Р., Эгеланд Г.М. (июнь 2004 г.). «Коренные народы Арктики переживают изменения в питании, сопровождающиеся изменением рациона питания и ожирением» . Журнал питания . 134 (6): 1447–53. дои : 10.1093/jn/134.6.1447 . ПМИД 15173410 .
- ^ Jump up to: а б Сквайрс ВР (2011). Роль продовольствия, сельского хозяйства, лесного хозяйства и рыболовства в питании человека – Том IV . Публикации EOLSS. п. 121. ИСБН 978-1-84826-195-2 . Архивировано из оригинала 11 января 2023 года . Проверено 17 сентября 2017 г.
- ^ Стейси М., диджей Manners (1978). «Эдмунд Лэнгли Херст». Достижения в области химии и биохимии углеводов . Том. 35. стр. 1–29. дои : 10.1016/S0065-2318(08)60217-6 . ISBN 978-0-12-007235-4 . ПМИД 356548 .
- ^ «Информация о торговой марке Redoxon от Hoffman-la Roche, Inc. (1934 г.)» . Архивировано из оригинала 16 ноября 2018 года . Проверено 25 декабря 2017 г.
- ^ Ван В, Сюй Х (2016). «Промышленная ферментация витамина С» . В Vandamme EJ, Revuelta JI (ред.). Промышленная биотехнология витаминов, биопигментов и антиоксидантов . Wiley-VCH Verlag GmbH & Co. КГаА. п. 161. ИСБН 978-3-527-33734-7 .
- ^ Норум КР, Грав Х.Дж. (июнь 2002 г.). «[Аксель Хольст и Теодор Фролих — пионеры борьбы с цингой]». Журнал Норвежской медицинской ассоциации (на норвежском языке). 122 (17): 1686–7. ПМИД 12555613 .
- ^ Розенфельд Л. (апрель 1997 г.). «Витамин-витамин. Первые годы открытий» . Клиническая химия . 43 (4): 680–5. дои : 10.1093/клинчем/43.4.680 . ПМИД 9105273 .
- ^ Jump up to: а б Зеттерстрем Р. (май 2009 г.). «Нобелевская премия 1937 года Альберту фон Сент-Дьёрдьи: идентификация витамина С как противоцинготного фактора». Акта Педиатрика . 98 (5): 915–19. дои : 10.1111/j.1651-2227.2009.01239.x . ПМИД 19239412 . S2CID 11077461 .
- ^ Jump up to: а б Свирбели Дж. Л., Сент-Дьёрдьи А (1932). «Химическая природа витамина С» . Биохимический журнал . 26 (3): 865–70. Бибкод : 1932Sci....75..357K . дои : 10.1126/science.75.1944.357-a . ПМК 1260981 . ПМИД 16744896 .
- ^ Юхас-Надь С. (март 2002 г.). «[Альберт Сент-Дьёрдьи - биография свободного гения]». Медицинский еженедельник (на венгерском языке). 143 (12): 611–4. ПМИД 11963399 .
- ^ Кенез Дж. (декабрь 1973 г.). «[Насыщенная жизнь учёного. 80-летие со дня рождения лауреата Нобелевской премии Альберта Сент-Дьёрдьи]». Мюнхенский медицинский еженедельник (на немецком языке). 115 (51): 2324–6. ПМИД 4589872 .
- ^ Размещение А (декабрь 1974 г.). «[2 интересные ранние статьи Альберта Сент-Дьёрдьи]». Медицинский еженедельник (на венгерском языке). 115 (52): 3118–9. ПМИД 4612454 .
- ^ Jump up to: а б «Документы Альберта Сент-Дьёрдьи: Сегед, 1931–1947: витамин С, мышцы и Вторая мировая война» . Профили в науке . Национальная медицинская библиотека США. Архивировано из оригинала 5 мая 2009 года.
- ^ «Цинга» . Интернет-энтимологический словарь. Архивировано из оригинала 15 декабря 2020 года . Проверено 19 ноября 2017 г.
- ^ Херст Э.Л. (апрель 1950 г.). «Сэр Норман Хаворт». Природа . 165 (4198): 587. Бибкод : 1950Natur.165..587H . дои : 10.1038/165587a0 . ПМИД 15416703 .
- ^ Бернс Джей-Джей, Эванс С. (декабрь 1956 г.). «Синтез L-аскорбиновой кислоты у крыс из D-глюкуронолактона и L-гулонолактона» (PDF) . Журнал биологической химии . 223 (2): 897–905. дои : 10.1016/S0021-9258(18)65088-4 . ПМИД 13385237 . Архивировано из оригинала 3 декабря 2022 года . Проверено 3 декабря 2022 г.
- ^ Бернс Дж. Дж., Мольц А., Пейзер П. (декабрь 1956 г.). «Отсутствует этап у морских свинок, необходимый для биосинтеза L-аскорбиновой кислоты». Наука . 124 (3232): 1148–9. Бибкод : 1956Sci...124.1148B . дои : 10.1126/science.124.3232.1148-a . ПМИД 13380431 .
- ^ Хенсон Д.Э., Блок G, Левин М. (апрель 1991 г.). «Аскорбиновая кислота: биологические функции и связь с раком» . Журнал Национального института рака . 83 (8): 547–50. дои : 10.1093/jnci/83.8.547 . ПМИД 1672383 . Архивировано из оригинала 25 декабря 2020 года . Проверено 18 марта 2020 г.
- ^ Jump up to: а б Сол А. «Зал славы ортомолекулярной медицины - Ирвин Стоун, доктор философии». Ортомолекулярная организация . Архивировано из оригинала 9 августа 2011 года . Проверено 25 декабря 2023 г.
- ^ Монтель-Хаген А., Кинет С., Манель Н., Монгеллаз С., Прохаска Р., Баттини Дж.Л. и др. (март 2008 г.). «Эритроциты Glut1 запускают усвоение дегидроаскорбиновой кислоты у млекопитающих, неспособных синтезировать витамин С» . Клетка . 132 (6): 1039–48. дои : 10.1016/j.cell.2008.01.042 . ПМИД 18358815 . S2CID 18128118 .
- ^ Мандл Дж., Шарка А., Банхедьи Г. (август 2009 г.). «Витамин С: последние новости по физиологии и фармакологии» . Британский журнал фармакологии . 157 (7): 1097–110. дои : 10.1111/j.1476-5381.2009.00282.x . ПМЦ 2743829 . ПМИД 19508394 .
- ^ Кэмерон Э., Полинг Л. (октябрь 1976 г.). «Дополнительный аскорбат при поддерживающем лечении рака: продление времени выживания при неизлечимом раке человека» . Труды Национальной академии наук Соединенных Штатов Америки . 73 (10): 3685–9. Бибкод : 1976PNAS...73.3685C . дои : 10.1073/pnas.73.10.3685 . ПМК 431183 . ПМИД 1068480 .
- ^ Бозли С. (12 сентября 2008 г.). «Падение витаминного доктора: Матиас Рат отказывается от иска о клевете» . Хранитель . Архивировано из оригинала 1 декабря 2016 года . Проверено 5 января 2024 г.
- ^ Колкухун Д. (15 августа 2007 г.). «Эпоха затемнения | Наука | Guardian.co.uk» . Хранитель . Архивировано из оригинала 6 марта 2023 года . Проверено 5 января 2024 г.
- ^ Баррет С. (14 сентября 2014 г.). «Темная сторона наследия Лайнуса Полинга» . www.quackwatch.org . Архивировано из оригинала 4 сентября 2018 года . Проверено 18 декабря 2018 г. [ ненадежный источник? ]
- ^ Уилсон М.К., Багули Б.К., Уолл С., Джеймсон М.Б., Финдли член парламента (март 2014 г.). «Обзор высоких доз витамина С для внутривенного введения как противоракового средства» . Азиатско-Тихоокеанский журнал клинической онкологии . 10 (1): 22–37. дои : 10.1111/ajco.12173 . ПМИД 24571058 . S2CID 206983069 .
- ^ Ли Ю (ноябрь 2023 г.). «Роль витамина С в воздействии на раковые стволовые клетки и клеточную пластичность» . Раки . 15 (23): 5657. doi : 10.3390/cancers15235657 . ПМЦ 10705783 . ПМИД 38067361 .
- ^ Сатиш, Нью-Джерси, Сэмюэл С.М., Бюссельберг Д. (январь 2020 г.). «Комбинированная терапия с витамином С может уничтожить стволовые клетки рака» . Биомолекулы . 10 (1): 79. дои : 10.3390/biom10010079 . ПМК 7022456 . ПМИД 31947879 .
- ^ Ло Дж, Шен Л, Чжэн Д (2014). «Связь между потреблением витамина С и раком легких: метаанализ доза-реакция» . Научные отчеты . 4 : 6161. Бибкод : 2014NatSR...4E6161L . дои : 10.1038/srep06161 . ПМЦ 5381428 . ПМИД 25145261 .
- ^ Пуллар Дж. М., Карр AC, Vissers MC (август 2017 г.). «Роль витамина С в здоровье кожи» . Питательные вещества . 9 (8): 866. дои : 10.3390/nu9080866 . ПМЦ 5579659 . ПМИД 28805671 .
- ^ Аль-Ниайми Ф., Чианг, штат Нью-Йорк (июль 2017 г.). «Витамин С для местного применения и кожа: механизмы действия и клиническое применение» . J Clin Aesthet Дерматол . 10 (7): 14–17. ПМК 5605218 . ПМИД 29104718 .
- ^ Натан Н., Патель П. (10 ноября 2021 г.). «Почему местное применение витамина С важно для здоровья кожи?» . Издательство Harvard Health Publishing, Гарвардская медицинская школа . Архивировано из оригинала 14 октября 2022 года . Проверено 14 октября 2022 г.
- ^ Санабриа Б., Бергер Л.Е., Мохд Х., Бенуа Л., Труонг Т.М., Михняк-Кон Б.Б. и др. (сентябрь 2023 г.). «Клиническая эффективность местного применения витамина С в отношении появления морщин: систематический обзор литературы» . Журнал лекарств в дерматологии . 22 (9): 898–904. doi : 10.36849/JDD.7332 (неактивен 5 марта 2024 г.). ПМИД 37683066 . Архивировано из оригинала 25 февраля 2024 года . Проверено 25 февраля 2024 г.
{{cite journal}}: CS1 maint: DOI неактивен по состоянию на март 2024 г. ( ссылка ) - ^ Коррейя Г., Магина С. (июль 2023 г.). «Эффективность местного применения витамина С при мелазме и фотостарении: систематический обзор» . J Космет Дерматол . 22 (7): 1938–45. дои : 10.1111/jocd.15748 . ПМИД 37128827 . S2CID 258439047 .
Внешние ссылки
[ редактировать ]- Витамин С
- 3-гидроксипропеналы
- Биомолекулы
- Коэнзимы
- Комбинированные препараты
- Диетические антиоксиданты
- Дигидрофураны
- Добавки для электронного номера
- Энедиолы
- Пищевые антиоксиданты
- Фураноны
- Органические кислоты
- Ортомолекулярная медицина
- Основные лекарства Всемирной организации здравоохранения
- Офтальмологические препараты