Содержание химических элементов
Распространенность химических элементов является мерой распространенности химических элементов по отношению ко всем другим элементам в данной среде. Изобилие измеряется одним из трех способов: по массовой доле (в коммерческом контексте часто называемой весовой долей ), по мольной доле (доля атомов при численном подсчете или иногда доля молекул в газах) или по объемной доле . Объемная доля является общепринятой мерой содержания в смешанных газах, таких как атмосферы планет, и по значению аналогична молекулярной мольной доле для газовых смесей при относительно низких плотностях и давлениях, а также для идеальных газовых смесей. Большинство значений численности в этой статье даны в виде массовых долей.
В изобилии химических элементов во Вселенной преобладают большие количества водорода и гелия, которые образовались во время Большого взрыва . Остальные элементы, составляющие лишь около 2% Вселенной, были в основном произведены сверхновыми . Элементы с четными атомными номерами обычно встречаются чаще, чем их соседи в таблице Менделеева , из-за благоприятной энергетики образования, известной как правило Оддо-Харкинса .
Обилие элементов на Солнце и внешних планетах аналогично таковому во Вселенной. Из-за солнечного нагрева элементы Земли и внутренних каменистых планет Солнечной системы подверглись дополнительному истощению летучих водорода, гелия, неона, азота и углерода (который улетучивается в виде метана). Кора, мантия и ядро Земли демонстрируют признаки химической сегрегации плюс некоторую секвестрацию по плотности. В земной коре встречаются более легкие силикаты алюминия, в мантии больше силикатов магния, а ядро составляют металлические железо и никель. Обилие элементов в специализированных средах, таких как атмосфера, океаны или человеческое тело, является прежде всего продуктом химического взаимодействия со средой, в которой они находятся.
Значения изобилия
[ редактировать ]Обилие каждого элемента выражается относительным числом. Астрономия использует логарифмическую шкалу изобилия. элемента X относительно Водорода, определяемого формулой для плотности числа ; в этом масштабе. [ 1 ] Другая шкала — массовая доля или, что то же самое, процент по массе. [ 2 ]
Например, содержание кислорода в чистой воде можно измерить двумя способами: массовая доля составляет около 89%, поскольку именно эту долю массы воды составляет кислород. Однако мольная доля составляет около 33%, поскольку только 1 атом из 3 в воде, H 2 O, является кислородом. В качестве другого примера, если посмотреть на содержание массовой доли водорода и гелия как во Вселенной в целом, так и в атмосферах планет -газовых гигантов, таких как Юпитер , то оно составляет 74% для водорода и 23–25% для гелия ; в то время как (атомная) мольная доля водорода в этих средах составляет 92%, а гелия - 8%. Изменение данной среды на внешнюю атмосферу Юпитера , где водород является двухатомным , а гелий нет, изменяет молекулярную мольную долю (долю общего количества молекул газа), а также объемную долю атмосферы водорода примерно до 86%, а гелия до 13%. Под внешней атмосферой Юпитера объемные доли значительно отличаются от мольных из-за высоких температур (ионизация и диспропорционирование) и высокой плотности, где Закон идеального газа неприменим.
Вселенная
[ редактировать ]
| С | Элемент | Массовая доля (ppm) |
|---|---|---|
| 1 | Водород | 739,000 |
| 2 | Гелий | 240,000 |
| 8 | Кислород | 10,400 |
| 6 | Углерод | 4,600 |
| 10 | Неон | 1,340 |
| 26 | Железо | 1,090 |
| 7 | Азот | 960 |
| 14 | Кремний | 650 |
| 12 | Магний | 580 |
| 16 | сера | 440 |
| Общий | 999,060 |
В изобилии химических элементов во Вселенной преобладают большие количества водорода и гелия, которые образовались во время Большого взрыва . Остальные элементы, составляющие лишь около 2% Вселенной, были в основном произведены сверхновыми и некоторыми звездами-красными гигантами . Литий , бериллий и бор , несмотря на их низкий атомный номер, редки, потому что, хотя они и производятся в результате ядерного синтеза, они разрушаются в результате других реакций в звездах. [ 4 ] [ 5 ] Их естественное возникновение является результатом расщепления углерода, азота и кислорода космическими лучами в результате реакции ядерного деления. Элементы от углерода до железа относительно более распространены во Вселенной из-за легкости их получения в ходе нуклеосинтеза сверхновых . Элементы с более высокими атомными номерами, чем железо (элемент 26), становятся все более редкими во Вселенной, поскольку при своем производстве они все больше поглощают звездную энергию. Кроме того, элементы с четными атомными номерами обычно встречаются чаще, чем их соседи в таблице Менделеева , из-за благоприятной энергетики образования (см. Правило Оддо-Харкинса ), а среди самых легких нуклидов от гелия до серы наиболее распространены изотопы с равным числом протонов. и нейтроны.
Водород — самый распространенный элемент во Вселенной; гелий на втором месте. Все остальные встречаются на порядки реже. После этого ранг обилия перестает соответствовать атомному номеру . Кислород имеет ранг содержания 3, но атомный номер 8.

Известно 80 стабильных элементов, а 16 самых легких составляют 99,9% обычного вещества Вселенной. Эти же 16 элементов, от водорода до серы, попадают в начальную линейную часть Таблицы нуклидов (также называемой графиком Сегре ), графика зависимости числа протонов от нейтронов во всей материи, как обычной, так и экзотической, содержащей сотни стабильных изотопов и еще тысячи нестабильных. График Сегре изначально линеен, поскольку (кроме водорода) подавляющее большинство обычного вещества (99,4% в Солнечной системе) [ 6 ] ) содержит равное количество протонов и нейтронов (Z=N). Конечно, 74% обычной материи существует в виде мононуклонных протонов (водорода). Но когда нуклоны объединяются, образуя стабильные нуклиды, они объединяются в соотношении одна часть протона к одной части нейтрона в 99,4% обычной материи. Структурная основа равенства числа нуклонов в барионной материи — одна из самых простых и глубоких неразгаданных загадок атомного ядра.
Обилие легчайших элементов хорошо предсказывается стандартной космологической моделью , поскольку они в основном образовались вскоре (то есть в течение нескольких сотен секунд) после Большого взрыва в процессе, известном как нуклеосинтез Большого взрыва . Более тяжелые элементы в основном образовались гораздо позже, внутри звезд .
По оценкам, водород и гелий составляют примерно 74% и 24% всей барионной материи во Вселенной соответственно. Несмотря на то, что они составляют лишь очень небольшую часть Вселенной, оставшиеся «тяжелые элементы» могут сильно влиять на астрономические явления. Лишь около 2% (по массе) диска галактики Млечный Путь состоит из тяжелых элементов.
Эти другие элементы генерируются звездными процессами. [ 7 ] [ 8 ] [ 9 ] В астрономии «металл» — это любой элемент, кроме водорода и гелия. Это различие важно, поскольку водород и гелий — единственные элементы, которые образовались в значительных количествах во время Большого взрыва. , металличность галактики Таким образом или другого объекта является показателем звездной активности после Большого взрыва.
В общем, элементы вплоть до железа производятся крупными звездами в процессе превращения в сверхновые или меньшими звездами в процессе умирания. Один тип железа, Железо-56 , особенно распространен, поскольку это наиболее стабильный нуклид (поскольку он имеет самую высокую энергию связи ядра на нуклон) и его можно легко получить из альфа-частиц (являющихся продуктом распада радиоактивного никеля) . -56 , в конечном итоге состоящие из 14 ядер гелия). Элементы тяжелее железа образуются в результате энергопоглощающих процессов в крупных звездах, и их содержание во Вселенной (и на Земле) обычно уменьшается с увеличением атомного номера.
В таблице показаны десять наиболее распространенных элементов в нашей галактике (по оценкам спектроскопически), измеряемые в частях на миллион по массе. [ 3 ] Близлежащие галактики, которые развивались по схожему пути, имеют соответствующее обогащение элементами тяжелее водорода и гелия. Более отдаленные галактики рассматриваются такими, какими они выглядели в прошлом, поэтому содержание в них элементов кажется более близким к первичной смеси. Однако, поскольку физические законы и процессы, по-видимому, одинаковы во всей Вселенной, ожидается, что в этих галактиках также возникло одинаковое содержание элементов.
Как показано в таблице Менделеева , содержание элементов соответствует их происхождению. Очень распространенные водород и гелий являются продуктами Большого взрыва. Следующие три элемента таблицы Менделеева ( литий , бериллий и бор ) встречаются редко, несмотря на их низкий атомный номер. У них было мало времени для формирования в результате Большого взрыва. Они производятся в небольших количествах в результате ядерного синтеза в умирающих звездах или в результате распада более тяжелых элементов в межзвездной пыли, вызванного расщеплением космических лучей . В сверхновых они образуются в результате ядерного синтеза, но затем разрушаются в результате других реакций. [ 4 ]
Более тяжелые элементы, начиная с углерода , производятся в умирающих звездах или сверхновых звездах путем накопления альфа-частиц (ядер гелия), что способствует поочередному увеличению содержания элементов с четными атомными номерами (они также более стабильны). Эффект того, что химические элементы с нечетными номерами обычно встречаются во Вселенной более редко, был эмпирически замечен в 1914 году и известен как правило Оддо-Харкинса .
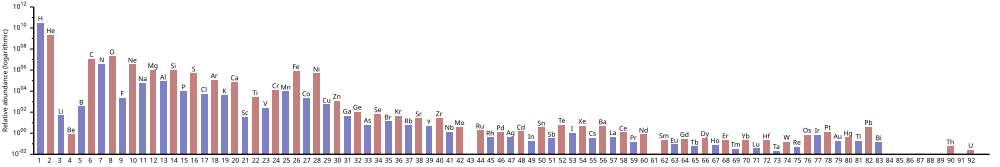
Следующий график (примечание логарифмического масштаба) показывает содержание элементов в Солнечной системе .
| Нуклид | А | Массовая доля в частях на миллион | Атомная доля в частях на миллион |
|---|---|---|---|
| Водород-1 | 1 | 705,700 | 909,964 |
| Гелий-4 | 4 | 275,200 | 88,714 |
| Кислород-16 | 16 | 9,592 | 477 |
| Углерод-12 | 12 | 3,032 | 326 |
| Азот-14 | 14 | 1,105 | 102 |
| Неон-20 | 20 | 1,548 | 100 |
| Другие нуклиды: | 3,616 | 172 | |
| Кремний-28 | 28 | 653 | 30 |
| Магний-24 | 24 | 513 | 28 |
| Железо-56 | 56 | 1,169 | 27 |
| Сера-32 | 32 | 396 | 16 |
| Гелий-3 | 3 | 35 | 15 |
| Водород-2 | 2 | 23 | 15 |
| Неон-22 | 22 | 208 | 12 |
| Магний-26 | 26 | 79 | 4 |
| Углерод-13 | 13 | 37 | 4 |
| Магний-25 | 25 | 69 | 4 |
| Алюминий-27 | 27 | 58 | 3 |
| Аргон-36 | 36 | 77 | 3 |
| Кальций-40 | 40 | 60 | 2 |
| Натрий-23 | 23 | 33 | 2 |
| Железо-54 | 54 | 72 | 2 |
| Кремний-29 | 29 | 34 | 2 |
| Никель-58 | 58 | 49 | 1 |
| Кремний-30 | 30 | 23 | 1 |
| Железо-57 | 57 | 28 | 1 |
Связь с ядерной энергией связи
[ редактировать ]
Слабые корреляции наблюдались между оценками содержания элементов во Вселенной и кривой энергии связи ядра (также называемой энергией связи на нуклон ). Грубо говоря, относительная стабильность различных атомных нуклидов в условиях чрезвычайно энергетических условий нуклеосинтеза Большого взрыва (BBN) оказала сильное влияние на относительное содержание элементов, образовавшихся в результате Большого взрыва и в ходе развития Вселенной после него. [ 10 ]
См. статью о нуклеосинтезе , где объясняется, как определенные процессы ядерного синтеза в звездах (например, горение углерода и т. д.) создают элементы тяжелее водорода и гелия.
Еще одной наблюдаемой особенностью является неравномерное чередование относительного содержания и дефицита соседних атомных номеров в предполагаемых содержаниях химических элементов, в которых относительное содержание четных атомных номеров примерно на 2 порядка превышает относительное содержание нечетных атомных номеров ( Правило Оддо-Харкинса ). Подобное чередование четных и нечетных атомных номеров можно наблюдать на кривой энергии связи ядра в окрестности углерода и кислорода, но здесь заканчивается слабая корреляция между относительным содержанием и энергией связи. Например, энергия связи бериллия (четный атомный номер) меньше , чем энергия связи бора (нечетный атомный номер), как показано на кривой энергии связи ядра. Кроме того, чередование энергии связи ядра между четными и нечетными атомными номерами разрешается выше кислорода, поскольку график неуклонно увеличивается до своего пика у железа. Полуэмпирическая формула массы (SEMF), также называемая формулой Вайцзеккера. или формула массы Бете-Вайцзеккера , дает теоретическое объяснение общей формы кривой энергии связи ядра. [ 11 ]
Солнце
[ редактировать ]Современная астрономия опирается на понимание обилия элементов на Солнце как часть космологических моделей. Значения численности получить трудно: даже фотосферная или наблюдательная численность зависит от моделей солнечной атмосферы и взаимодействия радиации. [ 1 ] Эти астрономические значения содержания представлены как логарифмы отношения к водороду. По этой шкале содержание водорода установлено на уровне 12. Фотосфера Солнца состоит в основном из водорода и гелия; содержание гелия колеблется примерно от 10,3 до 10,5 в зависимости от фазы солнечного цикла; [ 12 ] углерод 8,47, неон 8,29, кислород 7,69. [ 13 ] а железо оценивается в 7,62. [ 14 ]
Земля
[ редактировать ]
Земля разный образовалась из того же облака материи, из которого образовалось Солнце, но в ходе формирования и эволюции Солнечной системы планеты приобрели состав . В свою очередь, естественная история Земли привела к тому, что некоторые части этой планеты имели разную концентрацию элементов.
Масса Земли составляет примерно 5,97 × 10 24 кг. В основном по массе он состоит преимущественно из железа (32,1 %), кислорода (30,1 %), кремния (15,1 %), магния (13,9 %), серы (2,9 %), никеля (1,8 %), кальция (1,5 %). %) и алюминий (1,4%); остальные 1,2% состоят из следовых количеств других элементов. [ 15 ]
Основной состав Земли по элементарной массе примерно аналогичен общему составу Солнечной системы, с основным отличием в том, что на Земле отсутствует большое количество летучих элементов: водорода, гелия, неона и азота, а также углерод, который был потерян в виде летучих углеводородов.
Остальной элементный состав примерно типичен для «каменистых» внутренних планет, образовавшихся в термической зоне, где солнечное тепло выбрасывало в космос летучие соединения.
Земля сохраняет кислород как второй по величине компонент своей массы (и наибольшую атомную долю), главным образом за счет того, что этот элемент сохраняется в силикатных минералах , которые имеют очень высокую температуру плавления и низкое давление паров.
Корочка
[ редактировать ]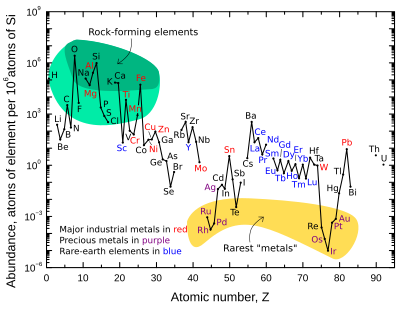
Массовое содержание девяти наиболее распространенных элементов в земной коре составляет примерно: кислород 46%, кремний 28%, алюминий 8,3%, железо 5,6%, кальций 4,2%, натрий 2,5%, магний 2,4%, калий 2,0% и титан 0,61%. Остальные элементы встречаются в количестве менее 0,15%. Полный список см. в разделе « Обилие элементов в земной коре» .
График справа иллюстрирует относительное атомное содержание химических элементов в верхней континентальной коре Земли — той части, которая относительно доступна для измерений и оценок.
Многие из элементов, показанных на графике, классифицированы по (частично перекрывающимся) категориям:
- породообразующие элементы (большие элементы - зеленое поле, второстепенные - светло-зеленое поле);
- редкоземельные элементы (лантаниды (La–Lu), Sc и Y; отмечены синим цветом);
- основные промышленные металлы (мировое производство >~3×10 7 кг/год; отмечено красным);
- драгоценные металлы (обозначены фиолетовым цветом);
- девять самых редких «металлов» — шесть элементов платиновой группы плюс Au , Re и Te (металлоид) — в желтом поле. Они редко встречаются в земной коре, поскольку растворимы в железе и поэтому сконцентрированы в ядре Земли. Теллур — единственный наиболее обедненный элемент в силикатной Земле по сравнению с космическим содержанием, поскольку он не только концентрировался в виде плотных халькогенидов в ядре, но и был сильно истощен в результате преаккреционной сортировки в туманности в виде летучего теллурида водорода . [ 17 ]
Есть два разрыва, где могут находиться нестабильные элементы технеций (атомный номер 43) и прометий (номер 61). Эти элементы окружены стабильными элементами, однако их наиболее стабильные изотопы имеют относительно короткий период полураспада (~ 4 миллиона лет и ~ 18 лет соответственно). Таким образом, они чрезвычайно редки, поскольку любые первичные количества этих элементов уже давно распались. Эти два элемента теперь производятся естественным путем только в результате спонтанного деления очень тяжелых радиоактивных элементов (таких как уран , торий или следовые количества плутония , которые существуют в урановых рудах) или в результате взаимодействия некоторых других элементов с космическими лучами . И технеций, и прометий были идентифицированы спектроскопически в атмосферах звезд, где они производятся в результате продолжающихся процессов нуклеосинтеза.
На графике содержания также есть разрывы там, где могли бы находиться шесть благородных газов , поскольку они химически не связаны в земной коре, и поэтому их содержание в земной коре четко не определено.
Восемь встречающихся в природе очень редких и высокорадиоактивных элементов ( полоний , астат , франций , радий , актиний , протактиний , нептуний и плутоний ) не включены, поскольку любой из этих элементов, присутствовавших при формировании Земли, распался много веков назад. , а их количество сегодня ничтожно и образуется только в результате радиоактивного распада урана и тория.
Кислород и кремний являются наиболее распространенными элементами в земной коре. На Земле и на каменистых планетах в целом кремний и кислород встречаются гораздо чаще, чем их космическое изобилие. Причина в том, что они соединяются друг с другом, образуя силикатные минералы . [ 17 ] Другие космически распространенные элементы, такие как водород , углерод и азот, образуют летучие соединения, такие как аммиак и метан , которые легко испаряются в космос под воздействием тепла планетарного образования и/или солнечного света.
Редкоземельные элементы
[ редактировать ]Термин «редкие» земные элементы — историческое неверное название. Сохранение этого термина отражает скорее незнакомство, чем истинную редкость. Более распространенные редкоземельные элементы так же сконцентрированы в земной коре по сравнению с обычными промышленными металлами, такими как хром, никель, медь, цинк, молибден, олово, вольфрам или свинец. Два наименее распространенных стабильных редкоземельных элемента ( тулий и лютеций ) встречаются почти в 200 раз чаще, чем золото . Однако, в отличие от обычных цветных и драгоценных металлов, редкоземельные элементы имеют очень небольшую склонность к концентрации в пригодных для эксплуатации рудных месторождениях. Следовательно, большая часть мировых поставок редкоземельных элементов поступает лишь из нескольких источников. Более того, все редкоземельные металлы химически очень похожи друг на друга, и поэтому их довольно трудно разделить на чистые элементы.
Различия в содержаниях отдельных редкоземельных элементов в верхней континентальной коре Земли представляют собой суперпозицию двух эффектов: ядерного и геохимического. Во-первых, редкоземельные элементы с четными атомными номерами ( 58 Ce, 60 Nd, ...) имеют большее космическое и земное распространение, чем соседние редкоземельные элементы с нечетными атомными номерами ( 57 La, 59 Pr, ...). Во-вторых, более легкие редкоземельные элементы более несовместимы (поскольку они имеют больший ионный радиус) и, следовательно, более сильно концентрируются в континентальной коре, чем более тяжелые редкоземельные элементы. В большинстве месторождений редкоземельных руд первые четыре редкоземельных элемента — лантан , церий , празеодим и неодим — составляют от 80% до 99% общего количества редкоземельных металлов, которые можно найти в руде.
Мантия
[ редактировать ]Массовое содержание семи наиболее распространенных элементов в мантии Земли составляет примерно: кислорода 44,3%, магния 22,3%, кремния 21,3%, железа 6,32%, кальция 2,48%, алюминия 2,29%, никеля 0,19%. [ 18 ]
Основной
[ редактировать ]Считается, что из-за массовой сегрегации ядро Земли состоит в основном из железа (88,8%) с меньшим количеством никеля (5,8%), серы (4,5%) и менее 1% микроэлементов. [ 6 ]
Океан
[ редактировать ]Наиболее распространенными элементами в океане по массовым процентам являются кислород (85,84 %), водород (10,82 %), хлор (1,94 %), натрий (1,08 %), магний (0,13 %), сера (0,09 %), кальций (0,04%), калий (0,04%), бром (0,007%), углерод (0,003%) и бор (0,0004%).
Атмосфера
[ редактировать ]Порядок элементов по объемной доле (что примерно соответствует молекулярной мольной доле) в атмосфере : азот (78,1%), кислород (20,9%), [ 19 ] аргон (0,96%), за которым следуют (в неопределенном порядке) углерод и водород, поскольку водяной пар и углекислый газ, которые составляют большую часть этих двух элементов в воздухе, являются переменными компонентами. Сера, фосфор и все остальные элементы присутствуют в значительно меньших пропорциях.
Судя по графику кривой содержания, аргон, значимый, если не основной компонент атмосферы, вообще не появляется в земной коре. Это связано с тем, что атмосфера имеет гораздо меньшую массу, чем кора, поэтому аргон, остающийся в коре, мало влияет на ее массовую долю, в то время как в то же время накопление аргона в атмосфере стало достаточно большим, чтобы быть значительным.
Городские почвы
[ редактировать ]Полный список содержания элементов в городских почвах см. в разделе « Содержание элементов» (страница данных)#Urban Soils .
Человеческое тело
[ редактировать ]
По массе клетки человека на 65–90% состоят из воды (H 2 O), а значительная часть оставшейся части состоит из углеродсодержащих органических молекул. Таким образом, кислород составляет большую часть массы человеческого тела, за ним следует углерод. Почти 99% массы человеческого тела состоит из шести элементов: водорода (Н), углерода (С), азота (N), кислорода (О), кальция (Са) и фосфора (Р). Следующие 0,75% составляют следующие пять элементов: калий (K), сера (S), хлор (Cl), натрий (Na) и магний (Mg). Достоверно известно, что только 17 элементов необходимы для жизни человека, а еще один элемент (фтор) считается полезным для прочности зубной эмали. Еще несколько микроэлементов могут играть определенную роль в здоровье млекопитающих. Бор и кремний особенно необходимы растениям, но их роль в организме животных неясна. Элементы алюминий и кремний, хотя и очень распространены в земной коре, заметно редки в организме человека. [ 20 ]
Ниже представлена таблица Менделеева с указанием питательных элементов. [ 21 ]
| Основные элементы [ 22 ] [ 23 ] [ 24 ] [ 25 ] [ 26 ] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ЧАС | Он | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Что | Быть | Б | С | Н | ТО | Ф | Ne | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Уже | мг | Ал | И | П | С | кл. | С | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| К | Что | наук | Из | V | Кр | Мин. | Фе | Ко | В | С | Зн | Здесь | Ге | Как | Се | Бр | НОК | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| руб. | старший | И | Зр | Нб | Мо | Тс | Ру | резус | ПД | В | компакт-диск | В | Сн | Сб | я | Машина | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Cs | Нет | * | Лу | хф | Облицовка | В | Ре | Ты | И | Пт | В | ртуть | Тл | Pb | С | Po | В | Рн | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Пт | Солнце | ** | лр | РФ | ДБ | Сг | Бх | Хс | гора | Дс | Рг | Сп | Нд | В | Мак | Лев | Ц | И | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| * | La | Этот | Пр | Нд | вечера | см | Евросоюз | Б-г | Тб | Те | К | Является | Тм | Ыб | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ** | И | че | Хорошо | В | Например | Мог | Являюсь | См | Бк | См. | Является | Фм | Мэриленд | Нет | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Легенда:
Количественные элементы
Основные микроэлементы
Существенность или функция у млекопитающих обсуждаются.
Нет доказательств биологического действия на млекопитающих, но он необходим для некоторых организмов.
(В случае с лантанидами определение незаменимого питательного вещества как незаменимого и незаменимого не вполне применимо из-за их чрезвычайного сходства. Известно, что стабильные ранние лантаноиды La – Nd стимулируют рост различных организмов, использующих лантаноиды, и Sm–Gd оказывает меньшее воздействие на некоторые такие организмы. Более поздние элементы ряда лантаноидов, по-видимому, не оказывают такого воздействия.) [ 27 ] |
См. также
[ редактировать ]- Обилие элементов (страница данных)
- Содержание элементов в земной коре
- Природное изобилие - изотопное изобилие
- Классификация Гольдшмидта - Геохимическая классификация
- Первичный нуклид - Нуклиды, существовавшие до образования Земли (обнаруженные на Земле).
- Радиационная левитация
- Список справочников по химическим элементам
Ссылки
[ редактировать ]Сноски
[ редактировать ]- ^ Jump up to: а б Асплунд, М.; Амарси, AM; Гревесс, Н. (01 сентября 2021 г.). «Химический состав Солнца: видение 2020 года» . Астрономия и астрофизика . 653 : А141. arXiv : 2105.01661 . дои : 10.1051/0004-6361/202140445 . ISSN 0004-6361 .
- ^ химии (ИЮПАК), Международный союз теоретической и прикладной химии. «ИЮПАК – массовая фракция (М03722)» . goldbook.iupac.org . Проверено 29 мая 2024 г.
- ^ Jump up to: а б Кросвелл, Кен (февраль 1996 г.). Алхимия Небес . Якорь. ISBN 0-385-47214-5 . Архивировано из оригинала 13 мая 2011 г.
- ^ Jump up to: а б Ванджиони-Флам, Элизабет; Кассе, Мишель (2012). Злоба, Моник (ред.). Эволюция галактик: связь далекой Вселенной с местной летописью окаменелостей . Springer Science & Business Media . стр. 77–86. ISBN 978-9401142137 .
- ^ Тримбл, Вирджиния (1996). «Происхождение и эволюция химических элементов». В Малкане, Мэтью А.; Цукерман, Бен (ред.). Происхождение и эволюция Вселенной . Садбери, Массачусетс: Издательство Jones and Bartlett . п. 101. ИСБН 0-7637-0030-4 .
- ^ Jump up to: а б с Арнетт, Дэвид (1996). Сверхновые и нуклеосинтез (Первое изд.). Принстон, Нью-Джерси: Издательство Принстонского университета . п. 11. ISBN 0-691-01147-8 . OCLC 33162440 .
- ^ Зюсс, Ганс; Юри, Гарольд (1956). «Изобилие стихий». Обзоры современной физики . 28 (1): 53. Бибкод : 1956РвМП...28...53С . дои : 10.1103/RevModPhys.28.53 .
- ^ Кэмерон, AGW (1973). «Распространенность элементов в Солнечной системе». Обзоры космической науки . 15 (1): 121. Бибкод : 1973ССРв...15..121С . дои : 10.1007/BF00172440 . S2CID 120201972 .
- ^ Андерс, Э.; Эбихара, М. (1982). «Распространенность элементов Солнечной системы». Geochimica et Cosmochimica Acta . 46 (11): 2363. Бибкод : 1982GeCoA..46.2363A . дои : 10.1016/0016-7037(82)90208-3 .
- ^ Белл, Джерри А.; Редакционная/писательская группа GenChem (2005). «Глава 3: Происхождение атомов». Химия: проект Американского химического общества . Нью-Йорк [ua]: Фриман. стр. 191–193. ISBN 978-0-7167-3126-9 .
Корреляции между численностью и энергией связи ядра [название подраздела]
- ^ Бэйли, Дэвид. «Полуэмпирическая формула ядерной массы» . PHY357: Струны и энергия связи . Университет Торонто . Архивировано из оригинала 24 июля 2011 г. Проверено 31 марта 2011 г.
- ^ Альтерман, Бенджамин Л.; Каспер, Джастин С.; Лимон, Роберт Дж.; Макинтош, Скотт В. (апрель 2021 г.). «Обилие гелия в солнечном ветре предвещает начало солнечного цикла». Солнечная физика . 296 (4): 67. arXiv : 2006.04669 . Бибкод : 2021SoPh..296...67A . дои : 10.1007/s11207-021-01801-9 . S2CID 233738140 .
- ^ Петроу, годовое общее собрание акционеров; Хоппе, Р.; Бергеманн, М.; Кальво, Ф. (2023). «Содержание кислорода на Солнце с использованием наблюдений SST/CRISP от центра до конечностей линии OI 7772 Å». Астрономия и астрофизика . 672 (4): Л6. arXiv : 2304.01048 . Бибкод : 2023A&A...672L...6P . дои : 10.1051/0004-6361/202346387 . S2CID 257912497 .
- ^ «Соотношение численности и галактическая химическая эволюция - Эндрю МакВильям» . ned.ipac.caltech.edu . Проверено 24 мая 2024 г.
- ^ Морган, JW; Андерс, Э. (1980). «Химический состав Земли, Венеры и Меркурия» . Труды Национальной академии наук . 77 (12): 6973–6977. Бибкод : 1980PNAS...77.6973M . дои : 10.1073/pnas.77.12.6973 . ПМК 350422 . ПМИД 16592930 .
- ^ Jump up to: а б Уильям Ф. Макдоно Состав Земли . quake.mit.edu, заархивировано Internet Archive Wayback Machine.
- ^ Jump up to: а б с Андерсон, Дон Л.; «Химический состав мантии» в «Теории Земли» , стр. 147–175. ISBN 0865421234
- ^ Ван, Хайян С.; Лайнвивер, Чарльз Х.; Ирландия, Тревор Р. (01 января 2018 г.). «Содержание элементов (с неточностями) на самой похожей на Землю планете» . Икар . 299 : 460–474. дои : 10.1016/j.icarus.2017.08.024 . hdl : 1885/139094 . ISSN 0019-1035 . S2CID 119434532 .
- ^ Циммер, Карл (3 октября 2013 г.). «Кислород Земли: загадка, которую легко принять как должное» . Нью-Йорк Таймс . Архивировано из оригинала 3 октября 2013 года . Проверено 3 октября 2013 г.
- ^ Данные таблицы из Чанг, Раймонд (2007). Химия (Девятое изд.). МакГроу-Хилл . п. 52. ИСБН 978-0-07-110595-8 .
- ^ Нильсен, Форрест Х. (1998). «Ультраследовые минералы». У Мориса Э. Шилса; Джеймс А. Олсен; Моше Шайн; А. Кэтрин Росс (ред.). Современное питание в здоровье и болезни . Балтимор: Липпинкотт Уильямс и Уилкинс. стр. 283–303. hdl : 10113/46493 . ISBN 978-0683307696 .
- ^ Ультраследовые минералы. Авторы: Нильсен, Форрест Х. Министерство сельского хозяйства США, ARS Источник: Современное питание для здоровья и болезней / редакторы Морис Э. Шилс ... и др. Балтимор: Уильямс и Уилкинс, 1999 г., с. 283-303. Дата выпуска: 1999 г. URI: [1]
- ^ Шклярска Д., Ржимски П. (май 2019 г.). «Является ли литий микроэлементом? От биологической активности и эпидемиологического наблюдения до обогащения продуктов питания» . Биол Трейс Элем Рес . 189 (1): 18–27. дои : 10.1007/s12011-018-1455-2 . ПМК 6443601 . ПМИД 30066063 .
- ^ Эндерле Дж., Клинк У., ди Джузеппе Р., Кох М., Зайдель У., Вебер К., Бирринджер М., Ратьен И., Римбах Г., Либ В. (август 2020 г.). «Уровни лития в плазме у населения в целом: перекрестный анализ метаболических и диетических корреляций» . Питательные вещества . 12 (8): 2489. дои : 10.3390/nu12082489 . ПМЦ 7468710 . ПМИД 32824874 .
- ^ МакКолл А.С., Каммингс К.Ф., Бхаве Дж., Ванакор Р., Пейдж-Маккоу А., Хадсон Б.Г. (июнь 2014 г.). «Бром является важным микроэлементом для сборки каркасов коллагена IV в развитии и архитектуре тканей» . Клетка . 157 (6): 1380–92. дои : 10.1016/j.cell.2014.05.009 . ПМК 4144415 . ПМИД 24906154 .
- ^ Зородду, Мария-Антуанетта; Аасет, Ян; Криспони, Гвидо; Медичи, Серенелла; Паан, Максимилиан; Нурчи, Валерия Марина (2019). «Незаменимые для человека металлы: краткий обзор». Журнал неорганической биохимии . 195 : 120–129. дои : 10.1016/j.jinorgbio.2019.03.013 .
- ^ Дауманн, Лена Дж. (25 апреля 2019 г.). «Необходимое и повсеместное: появление металлобиохимии лантаноидов» . Angewandte Chemie, международное издание . дои : 10.1002/anie.201904090 . Проверено 15 июня 2019 г.
Примечания
[ редактировать ]Обозначения
[ редактировать ]- «Редкоземельные элементы — важнейшие ресурсы для высоких технологий | Информационный бюллетень Геологической службы США 087-02» . geopubs.wr.usgs.gov .
- «Представь Вселенную! Словарь» . 3 декабря 2003 г. Архивировано из оригинала 3 декабря 2003 г.
Внешние ссылки
[ редактировать ]- Список элементов в порядке распространенности в земной коре (с учетом только двадцати наиболее распространенных элементов)
- Космическое изобилие элементов и нуклеосинтез
- WebElements.com Списки содержания элементов во Вселенной, Солнце, метеоритах, Земле, океане, ручьях и т. д.