Оксид свинца(II,IV)
Эта статья нуждается в дополнительных цитатах для проверки . ( декабрь 2023 г. ) |
 | |
| Имена | |
|---|---|
| Предпочтительное название ИЮПАК Четырехокись свинца [1] | |
| Другие имена Сурик, свинцовый сурик, трехпламбовый четырехокись | |
| Идентификаторы | |
3D model ( JSmol ) | |
| ХимическийПаук | |
| Информационная карта ECHA | 100.013.851 |
| Номер ЕС |
|
ПабХим CID | |
| НЕКОТОРЫЙ | |
| Число | 1479 |
Панель управления CompTox ( EPA ) | |
| Характеристики | |
| Pb 3 О 4 | |
| Молярная масса | 685.6 g·mol −1 |
| Появление | Яркие оранжевые кристаллы |
| Плотность | 8,3 г/см 3 |
| Температура плавления | 500 °С (разложение) |
| Давление пара | 1,3 кПа (при 0 °C) |
| Структура | |
| Четырехугольный , tP28 | |
| Р4 2 /мбк, №135 | |
| Опасности | |
| СГС Маркировка : | |
   | |
| Опасность | |
| Х272 , Х302 , Х332 , Х360 , Х373 , Х410 | |
| П201 , П220 , П273 , П308+П313 , П501 | |
| NFPA 704 (огненный алмаз) | |
| Родственные соединения | |
| Оксид свинца(II) Оксид свинца(IV) | |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
Оксид свинца(II,IV) , также называемый свинцовым суриком или суриком , представляет собой неорганическое соединение с формулой Pb 3 О 4 . Ярко-красное или оранжевое твердое вещество, используется в качестве пигмента , при производстве аккумуляторов и нержавеющих грунтовочных красок . Это пример соединения смешанной валентности , состоящего из Pb(II) и Pb(IV) в соотношении два к одному. [2]
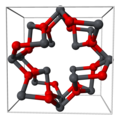
Структура
[ редактировать ]Оксид свинца(II,IV) представляет собой ортоплюмбат(IV) свинца(II). [Пб 2+ ] 2 [PbO 4− 4 ] . [3] Он имеет тетрагональную кристаллическую структуру при комнатной температуре , которая затем переходит в ромбическую ( символ Пирсона oP 28, пространственная группа Pbam, № 55) форму при температуре 170 К (-103 ° C). Этот фазовый переход лишь меняет симметрию кристалла и незначительно изменяет межатомные расстояния и углы. [4]
- Часть кристаллической структуры тетрагонального свинцового сурика.
Подготовка
[ редактировать ]Оксид свинца (II, IV) получают путем прокаливания оксида свинца (II) (PbO; также называемый глет ) на воздухе при температуре около 450–480 ° C: [5]
- 6 PbO + O 2 → 2 Pb 3 O 4
Полученный материал загрязнен PbO. Если требуется чистое соединение, PbO можно удалить раствором гидроксида калия :
- PbO + КОН + H 2 O → K[Pb(OH) 3 ]
Другой метод получения основан на отжиге карбоната свинца (II) ( церуссита ) на воздухе:
- 6 PbCO 3 + O 2 → 2 Pb 3 O 4 + 6 CO 2
Еще один метод — окислительный отжиг свинцовых белил :
- 3 Pb 2 CO 3 (OH) 2 + O 2 → 2 Pb 3 O 4 + 3 CO 2 + 3 H 2 O
В растворе оксид свинца (II, IV) можно получить реакцией плюмбата калия с ацетатом свинца (II) оксида свинца (II, IV). с образованием желтого нерастворимого моногидрата Pb 3 O 4 ·H 2 O , который можно перевести в безводную форму при осторожном нагревании:
- K 2 PbO 3 + 2 Pb(OCOCH 3 ) 2 + H 2 O → Pb 3 O 4 + 2 KOCOCH 3 + 2 CH 3 COOH
Природный сурик встречается редко, образуясь лишь в экстремальных окислительных условиях свинцовых рудных тел. Самые известные природные образцы происходят из Брокен-Хилла , Новый Южный Уэльс , Австралия, где они образовались в результате пожара на шахте . [6]
Реакции
[ редактировать ]Свинцовый сурик практически нерастворим в воде и этаноле . Однако он растворим в соляной кислоте, присутствующей в желудке , и поэтому токсичен при проглатывании. Он также растворяется в ледяной уксусной кислоте и разбавленной смеси азотной кислоты и перекиси водорода .
При нагревании до 500 °C он разлагается на оксид свинца(II) и кислород. При 580°С реакция завершается.
- 2 Pb 3 O 4 → 6 PbO + O 2
Азотная кислота растворяет компонент оксида свинца (II), оставляя после себя нерастворимый оксид свинца (IV) :
- Pb 3 O 4 + 4 HNO 3 → PbO 2 + 2 Pb(NO 3 ) 2 + 2 H 2 O
С оксидами железа и с элементарным железом оксид свинца(II,IV) образует нерастворимые плюбаты железа(II) и железа(III) , что является основой антикоррозионных свойств красок на основе свинца, наносимых на железные предметы.
Использовать
[ редактировать ]Свинцовый сурик использовался в качестве пигмента для грунтовочных красок для железных предметов. Из-за токсичности его применение ограничено. Он находит ограниченное применение в некоторых любительских пиротехниках в качестве заряда задержки и в прошлом использовался при изготовлении из драконьего яйца пиротехнических звезд .
Свинцовый сурик используется в качестве отвердителя в некоторых смесях полихлоропренового каучука. Он используется вместо оксида магния для обеспечения лучших свойств водостойкости.
Свинцовый сурик использовался для очистки инженеров , а затем был заменен инженерным синим .
Он также используется в качестве фальсификатора в порошке куркумы .
Физиологические эффекты
[ редактировать ]При вдыхании оксид свинца(II,IV) раздражает легкие. В случае высокой дозы пострадавший испытывает металлический привкус, боль в груди и животе. При попадании в организм он растворяется в желудочной кислоте и всасывается, что приводит к отравлению свинцом . Высокие концентрации могут проникать и через кожу, поэтому при работе с красками на основе свинца важно соблюдать меры предосторожности.
Длительный контакт с оксидом свинца(II,IV) может привести к накоплению соединений свинца в организме с развитием симптомов острого отравления свинцом. Хроническое отравление проявляется возбуждением, раздражительностью, нарушением зрения, гипертонией , сероватым оттенком лица.
Установлено, что оксид свинца(II,IV) канцерогенен для лабораторных животных . Его канцерогенность для человека не доказана.

История
[ редактировать ]этого соединения Латинское название «миниум» происходит от названия реки Миниус на северо-западе Иберии , где оно было впервые добыто.
Оксид свинца(II,IV) использовался в качестве красного пигмента в Древнем Риме , где его готовили путем прокаливания свинцовых белил . В древние и средневековые периоды он использовался в качестве пигмента при изготовлении иллюминированных рукописей и дал название миниуму или миниатюре — стилю изображения, написанного этим цветом.
Свинцовый сурик, приготовленный из льняного масла , использовался в качестве стойкой краски для защиты наружных металлических изделий. В 1504 году решетка замка Стерлинг в Шотландии была окрашена свинцовым суриком, как и пушки, в том числе Монс Мег . [7]
В виде мелкодисперсного порошка его также насыпали на диэлектрические поверхности для изучения фигур Лихтенберга .
В традиционной китайской медицине свинцовый сурик используется для лечения стригущего лишая и язв , хотя эта практика ограничена из-за его токсичности. Кроме того, азаркон , мексиканское народное средство от желудочно-кишечных расстройств, содержит до 95% оксида свинца(II,IV). [8]
Его также использовали до 18 века в качестве лекарства. [9]
См. также
[ редактировать ]- Свинцовая краска
- Оксид свинца(II) , PbO
- оксид свинца(IV) , PbO 2
- Список неорганических пигментов
- Миниум (минерал)
- Миниум (пигмент)
Ссылки
[ редактировать ]- ^ «ДОКЛАД О ДОБРОВОЛЬНОЙ ОЦЕНКЕ РИСКА СВИНЦА И НЕКОТОРЫХ НЕОРГАНИЧЕСКИХ СОЕДИНЕНИЙ СВИНЦА» . Проверено 25 декабря 2012 г.
- ^ Гринвуд, Норман Н .; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн . ISBN 978-0-08-037941-8 .
- ^ Эгон Виберг; Нильс Виберг; Арнольд Фредерик Холлеман (2001). Неорганическая химия . Академическая пресса. стр. 920. ISBN 0-12-352651-5 .
- ^ Гаварри, Дж; Вайгель, Доминик; Хьюат, AW (1978). «Оксиды свинца. IV. Структурная эволюция оксида Pb 3 O 4 между 240 и 5 К и механизм перехода» [Окислы свинца. IV. Структурная эволюция оксида Pb 3 O 4 между 240 и 5 К и механизм перехода. Журнал химии твердого тела . 23 (3–4): 327. Бибкод : 1978ЖССЧ..23..327Г . дои : 10.1016/0022-4596(78)90081-6 .
- ^ Карр, Додд С. «Соединения свинца». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. дои : 10.1002/14356007.a15_249 . ISBN 978-3527306732 .
- ^ Миниум
- ^ Джеймс Бальфур Пол , Отчеты казначея Шотландии , том. 2 (Эдинбург, 1900), с. 277.
- ^ Бозе, А.; Вашиштха, К; О'Локлин, Би Джей (1983). « Azarcón por empacho – еще одна причина отравления свинцом». Педиатрия . 72 : 108–118. дои : 10.1542/педс.72.1.106 . S2CID 37730169 .
- ^ «Лондонский ланцет: журнал британской и зарубежной медицины, физиологии, хирургии, химии, критики, литературы и новостей» . 1853.