Пятиокись мышьяка

| |
| Имена | |
|---|---|
| Другие имена
Оксид мышьяка(V)
Нейтральный оксид мышьяка (2:5) Мышьяковый ангидрид | |
| Идентификаторы | |
3D model ( JSmol )
|
|
| ХимическийПаук | |
| Информационная карта ECHA | 100.013.743 |
| Номер ЕС |
|
ПабХим CID
|
|
| номер РТЭКС |
|
| НЕКОТОРЫЙ | |
| Число | 1559 |
Панель управления CompTox ( EPA )
|
|
| Характеристики | |
| Как 2 О 5 | |
| Молярная масса | 229.8402 g/mol |
| Появление | белый гигроскопичный порошок |
| Плотность | 4,32 г/см 3 |
| Температура плавления | 315 ° C (599 ° F, 588 К) (разлагается) |
| 59,5 г/100 мл (0 °С) 65,8 г/100 мл (20 °С) 8,20 г/100 мл (100 °С) | |
| Растворимость | растворим в спирте |
| Кислотность ( pKa ) | 7 |
| Опасности | |
| СГС Маркировка : | |
  
| |
| Опасность | |
| Х301 , Х331 , Х350 , Х410 | |
| P201 , P202 , P261 , P264 , P270 , P271 , P273 , P281 , P301+P310 , P304+P340 , P308+P313 , P311 , P321 , P330 , P391 , P403+P233 , P405 , P 501 | |
| NFPA 704 (огненный алмаз) | |
| Летальная доза или концентрация (LD, LC): | |
ЛД 50 ( средняя доза )
|
8 мг/кг (крыса, перорально) |
| NIOSH (пределы воздействия на здоровье в США): | |
ПЭЛ (допустимо)
|
[1910.1018] СВВ 0,010 мг/м 3 [1] |
РЕЛ (рекомендуется)
|
Са С 0,002 мг/м 3 [15 минут] [1] |
IDLH (Непосредственная опасность)
|
Са [5 мг/м 3 (как как)] [1] |
| Родственные соединения | |
Другие катионы
|
Пятиокись фосфора Пятиокись сурьмы |
Родственные соединения
|
Триоксид мышьяка Мышьяковая кислота |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа).
| |
Пятиокись мышьяка — неорганическое соединение формулы As 2 O 5 . [2] Это стекловидное белое расплывающееся твердое вещество относительно нестабильно, что соответствует редкости степени окисления As(V). Более распространенным и гораздо более важным с коммерческой точки зрения является оксид мышьяка (III) (As 2 O 3 ). Все неорганические соединения мышьяка высокотоксичны и поэтому находят лишь ограниченное коммерческое применение.
Структура
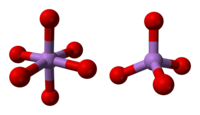
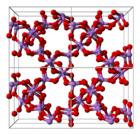
[ редактировать ]Структура состоит из тетраэдрических {AsO 4 } и октаэдрических {AsO 6 } центров, связанных общими углами. [3] Структура отличается от структуры соответствующего оксида фосфора (V) ; в результате, хотя твердый раствор с этим оксидом все еще существует, он достигает только эквимолярной точки, после чего фосфор замещает мышьяк во всех его тетраэдрических положениях. Точно так же пятиокись мышьяка также может растворять вплоть до эквимолярного количества пятиокиси сурьмы , поскольку сурьма заменяет мышьяк только в его октаэдрических участках. [4]
 |
 |
|
| В качестве координации | элементарная ячейка | клеточная упаковка |
Синтез
[ редактировать ]Исторический
[ редактировать ]Пьер Маккер обнаружил кристаллизующуюся соль, которую он назвал «нейтральным мышьяком». Эта соль представляла собой остаток, полученный после отгонки азотной кислоты из смеси нитрата калия и триоксида мышьяка . Ранее Парацельс нагревал смесь триоксида мышьяка и нитрата калия. Он применил к продукту термин «arsenicum fixum». Тот же продукт А. Либавиус назвал «butyrum arsenici» (мышьяковое масло), хотя на самом деле этот термин употреблялся для обозначения трихлорида мышьяка. Все продукты, которые обнаружили Парацельс и Либавиус, представляли собой нечистые арсенаты щелочных металлов. [5] Шееле получил ряд арсенатов действием мышьяковой кислоты на щелочи. Одним из арсенатов, которые он приготовил, был пятиокись мышьяка. [6] Вода в щелочах испарялась при 180°С, а пятиокись мышьяка была стабильна при температуре ниже 400°С. [5]
Современные методы
[ редактировать ]Пятиокись мышьяка можно кристаллизовать при нагревании As 2 O 3 в атмосфере кислорода. Эта реакция обратима: [3]
- Ас 2 О 5 ⇌ Ас 2 О 3 + О 2
Сильные окислители, такие как озон , перекись водорода и азотная кислота , превращают триоксид мышьяка в пятиокись.
Мышьяковую кислоту можно получить путем обычной обработки соединений мышьяка, включая окисление мышьяка и мышьяксодержащих минералов на воздухе. Показательным является обжиг аурипигмента , типичной сульфидной мышьяковистой руды: [7]
- 2 Ас 2 С 3 + 11 О 2 → 2 Ас 2 О 5 + 6 СО 2
Безопасность
[ редактировать ]Как и все неорганические соединения мышьяка, пентоксид очень токсичен. Его восстановленное производное арсенит, представляющее собой соединение As(III), еще более токсично, поскольку обладает высоким сродством к тиоловым группам остатков цистеина в белках.
Он классифицируется как чрезвычайно опасное вещество в Соединенных Штатах, как это определено в разделе 302 Закона США о чрезвычайном планировании и праве общества на информацию (42 USC 11002), и на него распространяются строгие требования отчетности со стороны предприятий, которые производят, хранят, или использовать его в значительных количествах. [8]
Ссылки
[ редактировать ]- ^ Jump up to: а б с Карманный справочник NIOSH по химическим опасностям. «#0038» . Национальный институт охраны труда и здоровья (NIOSH).
- ^ Гринвуд, Норман Н .; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн . ISBN 978-0-08-037941-8 .
- ^ Jump up to: а б Мартин Янсен (1977). «Кристаллическая структура As 2 O 5 ». Angewandte Chemie International Edition на английском языке . 16 (5): 314–315. дои : 10.1002/anie.197703142 .
- ^ Гринвуд, Норман Н .; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн . ISBN 978-0-08-037941-8 .
- ^ Jump up to: а б Дж. В. Меллор. «Всеобъемлющий трактат по неорганической и теоретической химии» . Архивировано из оригинала 11 мая 2012 г. Проверено 30 марта 2013 г.
- ^ К.В. Зенгер; и др. «Мышьяк 149» . Архивировано из оригинала 9 апреля 2013 г.
- ^ Грунд, Южная Каролина; Хануш, К.; Вольф, Х.У. «Мышьяк и соединения мышьяка». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. дои : 10.1002/14356007.a03_113.pub2 . ISBN 978-3527306732 .
- ^ «40 CFR: Приложение A к Части 355 — Список чрезвычайно опасных веществ и их пороговых плановых количеств» (PDF) (изд. от 1 июля 2008 г.). Государственная типография . Архивировано из оригинала (PDF) 25 февраля 2012 года . Проверено 29 октября 2011 г.
{{cite journal}}: Для цитирования журнала требуется|journal=( помощь )
Внешние ссылки
[ редактировать ]- Карманный справочник NIOSH по химическим опасностям
- Монография МАИР – Мышьяк и соединения мышьяка
- Отчет НТП о канцерогенах – неорганических соединениях мышьяка
- ESIS: Европейская информационная система по химическим веществам
- Линстрем, Питер Дж.; Маллард, Уильям Г. (ред.); Интернет-книга NIST по химии , Справочная база данных стандартов NIST № 69 , Национальный институт стандартов и технологий, Гейтерсбург (Мэриленд)
