Хеликобактер пилори
| Хеликобактер пилори | |
|---|---|

| |
| Электронная микрофотография H. pylori с множественными жгутиками ( негативное окрашивание ) | |
| Научная классификация | |
| Домен: | Бактерии |
| Тип: | кампилобактерия |
| Сорт: | «Кампилобактерии» |
| Заказ: | Кампилобактерии |
| Семья: | Хеликобактерии |
| Род: | Хеликобактер |
| Разновидность: | H. pylori
|
| Биномиальное имя | |
| Хеликобактер пилори (Маршалл и др., 1985) Гудвин и др. , 1989
| |
| Синонимы | |
| |
Helicobacter pylori , ранее известный как Campylobacter pylori , представляет собой грамотрицательную , жгутиковую , спиральную бактерию . Мутанты могут иметь форму стержня или изогнутого стержня, и они менее эффективны. [ 1 ] [ 2 ] Его спиральное тело (от которого рода происходит название Helicobacter ), как полагают, развилось для того, чтобы проникать в оболочку желудка слизистую с помощью жгутиков и тем самым вызывать инфекцию. [ 3 ] [ 2 ] Бактерия была впервые идентифицирована как возбудитель язвы желудка в 1983 году австралийскими врачами Барри Маршаллом и Робином Уорреном . [ 4 ] [ 5 ] За это открытие в 2005 году им была присуждена Нобелевская премия по физиологии и медицине . [ 6 ]
Инфекция желудка H. pylori сама по себе не является причиной заболевания; более половины населения планеты инфицировано, но большинство из них протекает бессимптомно. [ 7 ] [ 8 ] Стойкая колонизация более вирулентными штаммами может вызвать ряд желудочных и внежелудочных расстройств. [ 9 ] Желудочные расстройства, вызванные инфекцией, начинаются с гастрита — воспаления слизистой оболочки желудка . [ 10 ] При персистирующей инфекции длительное воспаление переходит в хронический гастрит . Первоначально это будет неатрофический гастрит, но повреждение слизистой оболочки желудка может привести к переходу в атрофический гастрит и развитию язв как в самом желудке, так и в двенадцатиперстной кишке , ближайшем отделе кишечника. [ 10 ] риск развития рака желудка . На этой стадии высок [ 11 ] Однако развитие язвы двенадцатиперстной кишки имеет меньший риск развития рака. [ 12 ] Helicobacter pylori является канцерогеном 1 класса , а потенциальные раковые заболевания включают лимфоидной ткани, ассоциированной со слизистой оболочкой желудка (MALT) лимфомы , и рак желудка . [ 10 ] [ 11 ] Инфекция H. pylori является причиной около 89 процентов всех случаев рака желудка и связана с развитием 5,5 процентов всех случаев рака во всем мире. [ 13 ] [ 14 ] H. pylori — единственная бактерия, вызывающая рак. [ 15 ]
Внежелудочные осложнения, связанные с H. pylori , включают анемию , вызванную дефицитом железа или витамина B12, сахарный диабет, сердечно-сосудистые и некоторые неврологические расстройства. [ 16 ] Также была заявлена обратная связь с H. pylori , оказывающей положительный защитный эффект при многих заболеваниях, включая астму , рак пищевода , ВЗК (включая ГЭРБ и болезнь Крона ) и другие расстройства. [ 16 ]
Некоторые исследования показывают, что H. pylori играет важную роль в естественной экологии желудка, влияя на тип бактерий, колонизирующих желудочно-кишечный тракт. [ 17 ] [ 18 ] Другие исследования показывают, что непатогенные штаммы H. pylori могут нормализовать секрецию желудочной кислоты и регулировать аппетит. [ 19 ]
По оценкам, в 2023 году около двух третей населения мира были инфицированы H. pylori , причем этот вирус чаще встречается в развивающихся странах . [ 20 ] Распространенность снизилась во многих странах благодаря эрадикационному лечению антибиотиками и ингибиторами протонной помпы , а также повышению уровня жизни . [ 21 ] [ 22 ]
Микробиология
[ редактировать ]Helicobacter pylori — разновидность грамотрицательных бактерий рода Helicobacter . [ 23 ] Около половины населения мира инфицировано H. pylori являются лишь несколько штаммов , но патогенными . H. pylori представляет собой спиральную бактерию , имеющую преимущественно спиральную форму , которую также часто описывают как имеющую спиральную или S- образную форму. [ 24 ] [ 25 ] Его спиральная форма лучше подходит для прохождения через вязкую слизистую оболочку желудка и поддерживается рядом ферментов клеточной стенки пептидогликана . [ 1 ] Бактерии достигают менее кислой слизистой оболочки с помощью жгутиков . [ 26 ] Три изученных штамма показали вариацию длины в пределах 2,8–3,3 мкм, но довольно постоянный диаметр 0,55–0,58 мкм. [ 24 ] H. pylori может превращаться из спиральной формы в неактивную коккоидную форму, которая может уклоняться от иммунной системы и, возможно, стать жизнеспособной, известной как жизнеспособная, но некультивируемая (VBNC). [ 27 ] [ 28 ]
Helicobacter pylori микроаэрофильна в – то есть требует кислорода , но в меньшей концентрации, чем атмосфере . Он содержит гидрогеназу , которая может производить энергию путем окисления молекулярного водорода (H 2 ), вырабатываемого кишечными бактериями . [ 29 ]
H. pylori можно выявить в тканях с помощью окраски по Граму , окраски по Гимзе , окраски H&E , окраски серебром Вартина-Старри , окраски акридиновым оранжевым и фазово-контрастной микроскопии . Он способен образовывать биопленки . Биопленки помогают препятствовать действию антибиотиков и могут способствовать неудаче лечения. [ 30 ] [ 31 ]
Для успешной колонизации своего хозяина H. pylori использует множество различных факторов вирулентности, включая оксидазу , каталазу и уреазу . [ 32 ] Уреаза является наиболее распространенным белком, ее экспрессия составляет около 10% от общей массы белка. [ 33 ]
H. pylori содержит пять основных семейств белков внешней мембраны . [ 32 ] Самое большое семейство включает известные и предполагаемые адгезины . Остальные четыре семейства — это порины , транспортеры железа, белки, ассоциированные с жгутиками , и белки с неизвестной функцией. Как и у других типичных грамотрицательных бактерий, внешняя мембрана H. pylori состоит из фосфолипидов и липополисахаридов (ЛПС). О -антиген ЛПС может быть фукозилированным и имитировать антигены группы крови Льюиса, обнаруженные на эпителии желудка. [ 32 ]
Геном
[ редактировать ]Helicobacter pylori состоит из большого разнообразия штаммов, и сотни геномов были полностью секвенированы . [ 34 ] [ 35 ] [ 36 ] Геном штамма 26695 состоит примерно из 1,7 миллиона пар оснований и содержит около 1576 генов. [ 37 ] [ 38 ] Пангеном , то есть объединенный набор из 30 секвенированных штаммов, кодирует 2239 семейств белков ( ортологичные группы OG). [ 39 ] Среди них 1248 OG консервативны во всех 30 штаммах и представляют собой универсальное ядро . Остальные 991 ОГ соответствуют акцессорному геному , в котором 277 ОГ уникальны для одного штамма. [ 40 ]
имеется одиннадцать систем рестрикции-модификации В геноме H. pylori . [ 38 ] Это необычно большое количество, обеспечивающее защиту от бактериофагов . [ 38 ]
Транскриптом
[ редактировать ]Транскриптомика отдельных клеток с использованием секвенирования одноклеточной РНК позволила получить полный транскриптом H. pylori , который был опубликован в 2010 году. Этот анализ его транскрипции подтвердил известную кислотную индукцию основных локусов вирулентности , включая оперон уреазы (ure) и Cag. Остров патогенности. [ 41 ] Всего 1907 сайтов начала транскрипции , 337 первичных оперонов , 126 дополнительных субоперонов и 66 моноцистронов . было идентифицировано До 2010 года у этого вида было известно всего около 55 сайтов начала транскрипции (TSS). 27% первичных TSS также являются антисмысловыми TSS, что указывает на то, что, как и в случае с E. coli , антисмысловая транскрипция происходит по всему геному H. pylori . По крайней мере, один антисмысловой TSS связан примерно с 46% всех открытых рамок считывания , включая многие гены домашнего хозяйства . [ 41 ] Около 50% 5' - UTR (лидерных последовательностей) имеют длину 20–40 нуклеотидов (нт) и поддерживают мотив AAGGag, расположенный примерно на 6 нт (среднее расстояние) выше стартовых кодонов, как консенсусная последовательность Шайна-Дальгарно в H. pylori. . [ 41 ]
Протеом
[ редактировать ]Протеом белков был H. pylori систематически проанализирован, и более 70% его было обнаружено с помощью масс-спектрометрии и других методов. Около 50% протеома было определено количественно, что дает информацию о количестве копий белка в типичной клетке. [ 42 ]
Исследования интерактома выявили более 3000 белок-белковых взаимодействий . Это позволило получить информацию о том, как белки взаимодействуют друг с другом, либо в стабильных белковых комплексах , либо в более динамичных, временных взаимодействиях, что может помочь определить функции белка. Это, в свою очередь, помогает исследователям выяснить, какова функция неохарактеризованных белков, например, когда неохарактеризованный белок взаимодействует с несколькими белками рибосомы ( то есть, вероятно, он также участвует в функции рибосомы). Около трети из примерно 1500 белков H. pylori остаются неохарактеризованными, и их функция в значительной степени неизвестна. [ 43 ]
Инфекция
[ редактировать ]
Инфекция Helicobacter pylori может либо не иметь симптомов даже на протяжении всей жизни, либо может нанести вред слизистой оболочке желудка и двенадцатиперстной кишки в результате воспалительных реакций, вызванных несколькими механизмами, связанными с рядом факторов вирулентности . Колонизация может первоначально вызвать гастрит, вызванный H. pylori , - воспаление слизистой оболочки желудка , которое внесено в список заболеваний в МКБ-11 . [ 44 ] [ 45 ] [ 46 ] это перерастет в хронический гастрит Если не лечить, . Хронический гастрит может привести к атрофии слизистой оболочки желудка и развитию язвенной болезни (желудка или двенадцатиперстной кишки). Эти изменения можно рассматривать как стадии развития рака желудка , известного как каскад Корреа . [ 47 ] [ 48 ] Внежелудочные осложнения, связанные с H. pylori , включают анемию , вызванную дефицитом железа или витамина B12, сахарный диабет, сердечно-сосудистые и некоторые неврологические расстройства. [ 16 ]
Пептические язвы являются следствием воспаления, которое позволяет желудочной кислоте и пищеварительному ферменту пепсину подавлять защитные механизмы слизистых оболочек . Место колонизации H. pylori , влияющее на расположение язвы, зависит от кислотности желудка. [ 49 ] У людей, вырабатывающих большое количество кислоты, H. pylori колонизируется вблизи антрального отдела привратника (выход в двенадцатиперстную кишку), чтобы избежать париетальных клеток, секретирующих кислоту, на дне желудка (около входа в желудок). [ 32 ] G-клетки экспрессируют относительно высокие уровни PD-L1 , который защищает эти клетки от иммунного разрушения, вызванного H. pylori . [ 50 ] У людей, вырабатывающих нормальное или пониженное количество кислоты, H. pylori может также колонизировать остальную часть желудка.
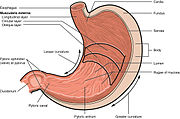
Воспалительная реакция, вызванная бактериями, колонизирующими около пилорического отдела антрального отдела, индуцирует G-клетки в антральном отделе секретировать гормон гастрин , который попадает через кровоток в париетальные клетки глазного дна. [ 51 ] Гастрин стимулирует париетальные клетки выделять больше кислоты в просвет желудка, а также со временем увеличивает количество париетальных клеток. [ 52 ] Повышенная кислотная нагрузка повреждает двенадцатиперстную кишку, что со временем может привести к образованию язв.
Helicobacter pylori I класса является канцерогеном , а потенциальные раковые заболевания включают лимфоидной ткани, ассоциированной со слизистой оболочкой желудка (MALT) лимфомы , и рак желудка . [ 10 ] [ 11 ] [ 53 ] Реже риск представляет собой диффузная крупноклеточная В-клеточная лимфома желудка. [ 54 ] Инфекция H. pylori является причиной около 89 процентов всех случаев рака желудка и связана с развитием 5,5 процентов всех случаев рака во всем мире. [ 13 ] [ 14 ] Хотя данные различаются в разных странах, в целом от 1% до 3% людей, инфицированных Helicobacter pylori, в течение жизни заболевают раком желудка по сравнению с 0,13% людей, у которых не было инфекции H. pylori . [ 55 ] [ 32 ] Рак желудка, вызванный H. pylori, является третьей по величине причиной смертности от рака в мире по состоянию на 2018 год. [ 56 ] Из-за обычного отсутствия симптомов рак желудка, когда его наконец диагностируют, часто бывает на довольно поздней стадии. Более половины больных раком желудка имеют метастазы в лимфатические узлы при первоначальной диагностике. [ 57 ]
Хроническое воспаление, являющееся особенностью развития рака, характеризуется инфильтрацией нейтрофилов и макрофагов эпителия желудка, что способствует накоплению провоспалительных цитокинов , активных форм кислорода (АФК) и активных форм азота (РНС), которые вызывают повреждение ДНК . [ 58 ] Окислительное повреждение ДНК и уровень окислительного стресса можно определить с помощью биомаркера 8-oxo-dG . [ 58 ] [ 59 ] Другие повреждения ДНК включают двухцепочечные разрывы . [ 60 ]
Небольшие желудка и полипы толстой кишки представляют собой аденомы , которые чаще встречаются в сочетании с повреждением слизистой оболочки, вызванным гастритом H. pylori . [ 61 ] [ 62 ] Более крупные полипы со временем могут стать раковыми. [ 63 ] [ 61 ] Была установлена умеренная связь H. pylori с развитием колоректального рака , но по состоянию на 2020 год причинно-следственная связь еще не была доказана. [ 64 ] [ 63 ]
Признаки и симптомы
[ редактировать ]У большинства людей, инфицированных H. pylori, никогда не возникает никаких симптомов или осложнений, но риск развития пептической язвы составляет от 10% до 20% , а риск рака желудка - от 0,5% до 2%. [ 8 ] [ 65 ] Гастрит, вызванный H. pylori, может проявляться как острый гастрит с болью в животе , тошнотой и продолжающейся диспепсией (расстройством пищеварения), которая иногда сопровождается депрессией и тревогой. [ 8 ] [ 66 ] Если гастрит перерастает в хронический гастрит или язву, симптомы одинаковы и могут включать расстройство желудка, боли в желудке или животе, тошноту, вздутие живота , отрыжку , чувство голода по утрам, слишком быстрое чувство насыщения, а иногда и рвоту , изжогу, неприятный запах изо рта и потеря веса. [ 67 ] [ 68 ]
Осложнения язвы могут вызывать серьезные признаки и симптомы, такие как черный или смолистый стул, указывающий на кровотечение в желудок или двенадцатиперстную кишку; кровь – либо красная, либо цвета кофейной гущи в рвотных массах; постоянные резкие или сильные боли в животе; головокружение и учащенное сердцебиение. [ 67 ] [ 68 ] Кровотечение является наиболее частым осложнением. В случаях, вызванных H. pylori, возникла большая потребность в гемостазе, часто требующем резекции желудка. [ 69 ] Длительное кровотечение может вызвать анемию, приводящую к слабости и утомляемости. Воспаление антрального отдела привратника, соединяющего желудок с двенадцатиперстной кишкой, чаще приводит к язвам двенадцатиперстной кишки, тогда как воспаление тела желудка может привести к язве желудка.
Рак желудка может вызывать тошноту, рвоту, диарею, запор и необъяснимую потерю веса. [ 70 ] Полипы желудка представляют собой аденомы , которые обычно протекают бессимптомно и доброкачественно, но могут быть причиной диспепсии, изжоги, желудочного кровотечения и, реже, обструкции выходного отдела желудка. [ 61 ] [ 71 ] Более крупные полипы могут стать раковыми . [ 61 ] Колоректальные полипы могут быть причиной ректального кровотечения, анемии, запора, диареи, потери веса и болей в животе. [ 72 ]
Патофизиология
[ редактировать ]Факторы вирулентности помогают патогену уклоняться от иммунного ответа хозяина и успешно колонизировать его . Многие факторы вирулентности H. pylori включают жгутики, выработку уреазы, адгезинов, сериновой протеазы HtrA (требование высокой температуры A) и основных экзотоксинов CagA и VacA. [ 30 ] [ 73 ] Наличие VacA и CagA связано с более отдаленными исходами . [ 74 ] CagA — онкопротеин, связанный с развитием рака желудка. [ 7 ]

Инфекция H. pylori связана с эпигенетическим снижением эффективности механизма репарации ДНК , что способствует накоплению мутаций и геномной нестабильности, а также канцерогенезу желудка. [ 75 ] Было показано, что экспрессия двух белков репарации ДНК, ERCC1 и PMS2 , резко снижалась, когда инфекция H. pylori прогрессировала и вызывала диспепсию . [ 76 ] Диспепсия возникает примерно у 20% инфицированных. [ 77 ] эпигенетическое снижение экспрессии белков репарации ДНК MLH1 , MGMT и MRE11 Также очевидно . Снижение репарации ДНК при наличии повышенного повреждения ДНК увеличивает канцерогенные мутации и, вероятно, является важной причиной канцерогенеза желудка. [ 59 ] [ 78 ] [ 79 ] Эти эпигенетические изменения обусловлены H. pylori индуцированным метилированием сайтов CpG в промоторах генов. [ 78 ] и H. pylori -индуцированная измененная экспрессия множества микроРНК . [ 79 ]
два связанных механизма, с помощью которых H. pylori Были предложены может способствовать развитию рака. Один из механизмов включает усиленное производство свободных радикалов вблизи H. pylori и повышенную скорость мутаций клеток-хозяев . Другой предложенный механизм получил название «перигенетический путь». [ 80 ] и включает усиление фенотипа трансформированной клетки-хозяина посредством изменений в клеточных белках, таких как белки адгезии . H. pylori Предполагается, что индуцирует воспаление и локально высокие уровни фактора некроза опухоли (TNF) (также известного как фактор некроза опухоли альфа (TNFα) и/или интерлейкина 6 (IL-6). [ 81 ] Согласно предложенному перигенетическому механизму, сигнальные молекулы, связанные с воспалением, такие как TNF, могут изменять адгезию эпителиальных клеток желудка и приводить к дисперсии и миграции мутированных эпителиальных клеток без необходимости дополнительных мутаций в генах-супрессорах опухоли , таких как гены, которые кодируют для белков клеточной адгезии. [ 82 ]
Жгутик
[ редактировать ]Первым фактором вирулентности Helicobacter pylori , способствующим колонизации, является ее жгутик . [ 83 ] H. pylori имеет от двух до семи жгутиков в одном и том же полярном месте, что придает ему высокую подвижность. Жгутиковые нити имеют длину около 3 мкм и состоят из двух сополимеризованных флагеллинов , FlaA и FlaB, кодируемых генами flaA и flaB . [ 26 ] [ 73 ] Минорный флагеллин FlaB расположен в проксимальной области, а основной флагеллин FlaA составляет остальную часть жгутика. [ 84 ] Жгутики покрыты продолжением внешней бактериальной мембраны, которая обеспечивает защиту от кислотности желудка. Оболочка также является местом происхождения везикул внешней мембраны, обеспечивающих защиту бактерии от бактериофагов. [ 84 ]
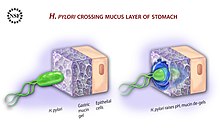
Подвижность жгутиков обеспечивается движущей силой протонов , обеспечиваемой гидролизом, управляемым уреазой, что обеспечивает хемотаксическое движение в направлении менее кислого градиента pH в слизистой оболочке. [ 30 ] Достигнув слизистой оболочки, H. pylori может проникать в слизь, а также в нижележащий слой эпителиальных клеток и желудочные ямки , где они колонизируются и живут в желудочных железах . [ 84 ] [ 85 ] Иногда бактерии обнаруживаются внутри самих эпителиальных клеток. [ 86 ] Использование бактериями чувства кворума позволяет формировать биопленку, которая способствует стойкой колонизации. В слоях биопленки H. pylori может ускользать от действия антибиотиков, а также защищаться от иммунных реакций хозяина. [ 87 ] [ 88 ] В биопленке H pylori может изменять жгутики, превращаясь в адгезивные структуры. [ 89 ]
Уреаза
[ редактировать ]
В дополнение к использованию хемотаксиса, чтобы избежать областей с высокой кислотностью (низким pH), H. pylori также производит большое количество уреазы , фермента , который расщепляет мочевину присутствующую в желудке с образованием аммиака и бикарбоната , которые высвобождаются в бактериальный цитозоль. и в окружающую среду, создавая нейтральную зону. [ 90 ] Пониженная кислотность (более высокий pH) изменяет слой слизи из гелеобразного состояния в более вязкое, что позволяет жгутикам легче перемещать бактерии через слизистую оболочку и прикрепляться к эпителиальным клеткам желудка. [ 90 ] Helicobacter pylori — один из немногих известных типов бактерий, у которых цикл мочевины уникально настроен в бактерии. [ 91 ] 10% клетки состоит из азота, и этот баланс необходимо поддерживать. Любой избыток сохраняется в мочевине, выделяемой в цикле мочевины. [ 91 ]
Ферментом последней стадии цикла мочевины является аргиназа, фермент, который имеет решающее значение для патогенеза H. pylori . Аргиназа производит орнитин и мочевину, которые фермент уреаза расщепляет на угольную кислоту и аммиак. Уреаза является наиболее распространенным белком бактерий, на его долю приходится 10–15% общего содержания белка в бактерии. Его экспрессия необходима не только для установления начальной колонизации при расщеплении мочевины до угольной кислоты и аммиака, но и необходима для поддержания хронической инфекции. [ 92 ] [ 65 ] Аммиак снижает кислотность желудка, позволяя бактериям обосноваться локально. Аргиназа способствует сохранению инфекции за счет потребления аргинина; аргинин используется макрофагами для производства оксида азота, который оказывает сильное противомикробное действие. [ 91 ] [ 93 ] Аммиак, вырабатываемый для регулирования pH , токсичен для эпителиальных клеток. [ 94 ]
Адгезины
[ редактировать ]H. pylori должен прикрепляться к эпителиальным клеткам, чтобы предотвратить его вымывание при постоянном движении и обновлении слизи. Чтобы обеспечить им эту адгезию, бактериальные белки внешней мембраны , являющиеся факторами вирулентности, называемые адгезинами . вырабатываются [ 95 ] BabA (адгезин, связывающий антиген группы крови) наиболее важен во время начальной колонизации, а SabA (адгезин, связывающий сиаловую кислоту) важен для персистенции. BabA прикрепляется к гликанам и муцинам эпителия. [ 95 ] BabA (кодируемый геном babA2 ) также связывается с антигеном Льюиса b, присутствующим на поверхности эпителиальных клеток. [ 96 ] Адгезия через BabA чувствительна к кислоте и может быть полностью отменена снижением pH. Было высказано предположение, что чувствительность BabA к кислоте обеспечивает прилипание, а также позволяет эффективно избегать неблагоприятной среды, такой как низкий pH, вредной для организма. [ 97 ] SabA (кодируемый геном sabA ) связывается с повышенным уровнем сиалила-Льюиса. Х антиген экспрессируется на слизистой оболочке желудка. [ 98 ]
Холестерин глюкозид
[ редактировать ]Наружная мембрана содержит холестерин-глюкозид , стерол-глюкозид, который H. pylori гликозилирует из холестерина в клетках желудочных желез и встраивает его в его внешнюю мембрану. [ 99 ] Этот холестерин-глюкозид важен для стабильности мембран, морфологии и уклонения от иммунитета и редко встречается у других бактерий. [ 100 ] [ 101 ]
За это ответственен фермент холестерин-α-глюкозилтрансфераза (αCgT) или (Cgt), кодируемый геном HP0421 . [ 102 ] Основным эффектом истощения холестерина хозяина под действием Cgt является разрушение богатых холестерином липидных рафтов в эпителиальных клетках. Липидные рафты участвуют в передаче сигналов клетками, и их разрушение вызывает снижение иммунного воспалительного ответа, в частности, за счет снижения гамма-интерферона . [ 103 ] Cgt также секретируется системой секреции типа IV и секретируется избирательно, так что создаются желудочные ниши, где может процветать патоген. [ 102 ] Было показано, что его отсутствие делает бактерии уязвимыми к стрессу окружающей среды, а также нарушает взаимодействия, опосредованные CagA. [ 99 ]
Каталаза
[ редактировать ]Колонизация вызывает интенсивную противовоспалительную реакцию в качестве первой линии защиты иммунной системы. Фагоцитарные лейкоциты и моноциты инфильтрируют место инфекции и производят антитела. [ 104 ] H. pylori способен прикрепляться к поверхности фагоцитов и препятствовать их действию. На это фагоцит отвечает генерацией и выбросом метаболитов кислорода в окружающее пространство. H. pylori может пережить этот ответ благодаря активности каталазы при ее прикреплении к поверхности фагоцитирующих клеток. Каталаза разлагает перекись водорода на воду и кислород, защищая бактерии от токсичности. Было показано, что каталаза почти полностью ингибирует фагоцитарный окислительный ответ. [ 104 ] Он кодируется геном katA . [ 105 ]
Кончик
[ редактировать ]TNF-индуцирующий белок альфа (Tipα) представляет собой канцерогенный белок, кодируемый HP0596, уникальный для H. pylori , который индуцирует экспрессию фактора некроза опухоли . [ 82 ] [ 106 ] Tipα проникает в клетки рака желудка, где связывается с нуклеолином клеточной поверхности и индуцирует экспрессию виментина . Виментин играет важную роль в эпителиально-мезенхимальном переходе, связанном с прогрессированием опухолей. [ 107 ]
КагА
[ редактировать ]CagA (цитотоксин-ассоциированный антиген А) является основным фактором вирулентности H. pylori , онкопротеина , кодируемого геном cagA . Бактериальные штаммы с геном cagA связаны со способностью вызывать язвы, MALT-лимфомы и рак желудка. [ 108 ] [ 109 ] Ген cagA кодирует относительно длинный (1186 аминокислот ) белок. Остров CAG патогенности (PAI) имеет около 30 генов, часть из которых кодирует сложную систему секреции IV типа (T4SS или TFSS). Низкое содержание GC в cag PAI по сравнению с остальной частью генома Helicobacter позволяет предположить, что остров был приобретен в результате горизонтального переноса от другого вида бактерий. [ 38 ] Сериновая протеаза HtrA также играет важную роль в патогенезе H. pylori . Белок HtrA позволяет бактерии мигрировать через эпителий клеток-хозяев, а также необходим для транслокации CagA. [ 110 ]
Вирулентность H. pylori может повышаться генами острова патогенности CAG ; около 50–70% штаммов H. pylori в западных странах переносят его. [ 111 ] Жители Запада, инфицированные штаммами, несущими CAG PAI, имеют более сильную воспалительную реакцию в желудке и подвергаются большему риску развития язвенной болезни или рака желудка, чем те, кто инфицирован штаммами, не имеющими острова. [ 32 ] После прикрепления H. pylori к эпителиальным клеткам желудка система секреции типа IV, экспрессируемая CAG PAI , «впрыскивает» индуцирующий воспаление агент, пептидогликан, из собственных клеточных стенок в эпителиальные клетки. Введенный пептидогликан распознается рецептором распознавания цитоплазматических образов (иммунным сенсором) Nod1, который затем стимулирует экспрессию цитокинов , способствующих воспалению. [ 112 ]
типа IV Аппарат секреции также вводит кодируемый cag PAI белок CagA в эпителиальные клетки желудка, где он разрушает цитоскелет , прикрепление к соседним клеткам, внутриклеточную передачу сигналов, полярность клеток и другие клеточные активности. [ 113 ] Попав внутрь клетки, белок CagA фосфорилируется по остаткам тирозина связанной с мембраной клетки-хозяина с помощью тирозинкиназы, (ТК). Затем CagA аллостерически активирует протеинтирозинфосфатазу / протоонкоген Shp2 . [ 114 ] Эти белки непосредственно токсичны для клеток, выстилающих желудок, и дают сильный сигнал иммунной системе о начале вторжения. В результате присутствия бактерий нейтрофилы и макрофаги обосновались в тканях для борьбы с атакой бактерий. [ 115 ] патогенные штаммы H. pylori Было показано, что активируют рецептор эпидермального фактора роста (EGFR), мембранный белок ТК с доменом . Активация EGFR H. pylori связана с измененной сигнальной трансдукцией и экспрессией генов в эпителиальных клетках хозяина, что может способствовать патогенезу. Также было высказано предположение, что С -концевая область белка CagA (аминокислоты 873–1002) способна регулировать транскрипцию гена клетки-хозяина независимо от фосфорилирования тирозина белка. [ 109 ] существует большое разнообразие Между штаммами H. pylori , и штамм, который заражает человека, может предсказать исход.
Корова
[ редактировать ]VacA (вакуолирующий автопереносчик цитотоксина) является еще одним основным фактором вирулентности, кодируемым геном vacA . [ 116 ] Все штаммы H. pylori несут этот ген, но существует большое разнообразие, и только 50% продуцируют закодированный цитотоксин. [ 92 ] [ 33 ] Четыре основных подтипа vacA — это s1/m1, s1/m2, s2/m1 и s2/m2 . s1/m1 и s1/m2 вызывают повышенный риск рака желудка. Известно, что [ 117 ] VacA представляет собой олигомерный белковый комплекс, вызывающий прогрессирующую вакуолизацию эпителиальных клеток, приводящую к их гибели. [ 118 ] Вакуолизация также была связана с усилением внутриклеточных резервуаров H. pylori путем разрушения клеточной мембраны кальциевых каналов TRPML1 . [ 119 ] Было показано, что VacA повышает уровень COX2 , повышающую регуляцию, которая увеличивает выработку простагландина, что указывает на сильную воспалительную реакцию клетки-хозяина. [ 118 ] [ 120 ]
Белки и везикулы наружной мембраны
[ редактировать ]Около 4% генома кодируют белки внешней мембраны , которые можно сгруппировать в пять семейств. [ 121 ] К самому большому семейству относятся бактериальные адгезины . Остальные четыре семейства — это порины , транспортеры железа, белки, ассоциированные с жгутиками , и белки с неизвестной функцией. Как и у других типичных грамотрицательных бактерий, внешняя мембрана H. pylori состоит из фосфолипидов и липополисахаридов (ЛПС). О -антиген ЛПС может быть фукозилированным и имитировать антигены группы крови Льюиса, обнаруженные на эпителии желудка. [ 32 ]
H. pylori образует пузырьки на внешней мембране, которые отщипываются в виде везикул внешней мембраны, обеспечивая альтернативную систему доставки факторов вирулентности, включая CagA. [ 99 ]
иммунный ответ, вызывая воспаление. Helicobacter запускает Известно, что богатый цистеином белок HcpA [ 122 ] Helicobacter pylori Фактор вирулентности DupA связан с развитием язв двенадцатиперстной кишки. [ 123 ]
Механизмы толерантности
[ редактировать ]Необходимость выживания привела к развитию различных механизмов толерантности, которые обеспечивают персистенцию H. pylori . [ 124 ] Эти механизмы также могут помочь преодолеть воздействие антибиотиков. [ 124 ] H. pylori приходится выдерживать не только резкую кислотность желудка, но и выведение слизи посредством непрерывной перистальтики и фагоцитарной атаки, сопровождающейся высвобождением активных форм кислорода . [ 125 ] Все организмы кодируют генетические программы реагирования на стрессовые состояния, в том числе вызывающие повреждение ДНК. [ 126 ] Стрессовые условия активируют механизмы бактериального ответа, которые регулируются белками, экспрессируемыми генами-регуляторами . [ 124 ] Окислительный стресс может индуцировать потенциально летальные мутагенные аддукты ДНК в его геноме. Выживание после такого повреждения ДНК поддерживается трансформацией , опосредованной рекомбинационной репарацией , которая способствует успешной колонизации. [ 127 ] [ 128 ] H. pylori естественным образом способен к трансформации. В то время как многие организмы компетентны только при определенных условиях окружающей среды, таких как голодание, H. pylori компетентна в течение всего логарифмического роста. [ 126 ]
Трансформация (перенос ДНК из одной бактериальной клетки в другую через промежуточную среду), по-видимому, является частью адаптации к репарации ДНК . [ 126 ] Гомологичная рекомбинация необходима для восстановления двухцепочечных разрывов (DSB). Комплекс хеликазы-нуклеазы AddAB резецирует DSB и загружает RecA в одноцепочечную ДНК (оцДНК), что затем опосредует обмен цепей, что приводит к гомологичной рекомбинации и репарации. Потребность RecA плюс AddAB для эффективной колонизации желудка предполагает, что H. pylori либо подвергается двухцепочечному повреждению ДНК, которое необходимо восстановить, либо требует какого-либо другого события, опосредованного рекомбинацией. В частности, естественная трансформация усиливается при повреждении ДНК у H. pylori , и существует связь между реакцией на повреждение ДНК и поглощением ДНК у H. pylori . [ 126 ] Эта естественная компетентность способствует сохранению H. pylori . H. pylori имеет гораздо более высокий уровень рекомбинации и мутаций, чем другие бактерии. [ 3 ] Генетически разные штаммы могут быть обнаружены у одного и того же хозяина, а также в разных участках желудка. [ 129 ] Общий ответ на несколько стрессоров может быть результатом взаимодействия механизмов. [ 124 ]
Белки RuvABC необходимы для процесса рекомбинационной репарации, поскольку они расщепляют промежуточные соединения в этом процессе, называемые соединениями Холлидея . Мутанты H. pylori , дефектные по RuvC, обладают повышенной чувствительностью к агентам, повреждающим ДНК, и к окислительному стрессу, демонстрируют пониженную выживаемость в макрофагах и не способны успешно заразиться на мышиной модели. [ 130 ] Аналогично, белок RecN играет важную роль в репарации DSB. [ 131 ] Мутант RecN H. pylori демонстрирует ослабленную способность колонизировать желудки мышей, что подчеркивает важность рекомбинационной репарации ДНК для выживания H. pylori внутри хозяина. [ 131 ]
Биопленка
[ редактировать ]Эффективной устойчивой реакцией колонизации является образование биопленки . Сначала прикрепившись к клеточной поверхности, бактерии производят и секретируют внеклеточное полимерное вещество (ЭПС). ЭПС состоит в основном из биополимеров и обеспечивает основу структуры биопленки. [ 90 ] H. pylori способствует образованию биопленки, превращая жгутики в адгезивные структуры, которые обеспечивают адгезию между клетками. [ 89 ] Слои агрегированных бактерий в виде микроколоний накапливаются, утолщая биопленку.
Матрица EPS предотвращает проникновение антибиотиков и иммунных клеток, а также обеспечивает защиту от тепла и конкуренции со стороны других микроорганизмов. [ 90 ] Между клетками в матриксе биопленки образуются каналы, позволяющие транспортировать питательные вещества, ферменты, метаболиты и отходы. [ 90 ] Клетки в глубоких слоях могут быть лишены питательных веществ и перейти в коккоподобное состояние покоя. [ 132 ] [ 133 ] При изменении формы бактерии на кокковидную форму воздействие ЛПС (на которое действуют антибиотики) становится ограниченным и поэтому ускользает от обнаружения иммунной системой. [ 134 ] Показано также, что при коккоидной форме остров патогенности CAG остается интактным. [ 134 ] Некоторые из этих устойчивых к антибиотикам клеток могут оставаться в организме хозяина в виде клеток-персистеров . После эрадикации клетки-персистеры могут вызвать рецидив инфекции. [ 132 ] [ 133 ] Бактерии могут отделяться от биопленки, перемещаться и колонизировать другие части желудка, образуя другие биопленки. [ 90 ]
Диагностика
[ редактировать ]
Колонизация H. pylori не является заболеванием сама по себе, а состоянием, связанным с рядом заболеваний желудка . [ 32 ] Тестирование рекомендуется в случаях язвенной болезни желудка желудка низкой степени злокачественности или MALT-лимфомы ; после эндоскопической резекции раннего рака желудка ; для родственников первой степени родства, больных раком желудка, а также в некоторых случаях расстройства пищеварения. Другие показания, требующие проведения тестирования на H. pylori , включают длительный прием аспирина или других нестероидных противовоспалительных средств, необъяснимую железодефицитную анемию или случаи иммунной тромбоцитопенической пурпуры . [ 135 ] Существует несколько методов тестирования, как инвазивных, так и неинвазивных.
Неинвазивные тесты на инфекцию H. pylori включают серологические тесты на антитела , анализы кала и дыхательные тесты на мочевину . Дыхательные тесты на углерод-мочевину включают использование углерода-13 или радиоактивного углерода-14, производящего меченый диоксид углерода, который можно обнаружить в выдыхаемом воздухе. [ 136 ] Углеводородные дыхательные тесты обладают высокой чувствительностью и специфичностью для диагностики H. pylori . [ 136 ]
Прием ингибиторов протонной помпы и антибиотиков следует прекратить как минимум за 30 дней до проведения тестирования на инфекцию или эрадикацию H. pylori , поскольку оба препарата ингибируют рост H. pylori и могут привести к ложноотрицательным результатам. [ 135 ] Тестирование для подтверждения эрадикации рекомендуется проводить через 30 или более дней после завершения лечения инфекции H. pylori . Тестирование дыхания на H. pylori или тестирование на антиген в кале являются разумными тестами для подтверждения эрадикации. [ 135 ] Серологические тесты на H. pylori , включая антитела IgG, не рекомендуются в качестве теста на эрадикацию, поскольку их уровень может оставаться повышенным в течение многих лет после успешного лечения инфекции. [ 135 ]
Эндоскопическая биопсия является инвазивным методом диагностики инфекции H. pylori . Инфекции низкого уровня могут быть пропущены при биопсии, поэтому рекомендуется брать несколько образцов. Наиболее точным методом выявления инфекции H. pylori является гистологическое исследование из двух участков после эндоскопической биопсии в сочетании либо с быстрым уреазным тестом , либо с микробным посевом. [ 137 ] не рекомендуется Как правило, повторная эндоскопия для подтверждения эрадикации H. pylori , если нет особых показаний к повторению процедуры. [ 135 ]
Передача инфекции
[ редактировать ]Helicobacter pylori заразен и передается при прямом контакте либо со слюной (орально-оральный), либо с фекалиями ( фекально-оральный путь ), но преимущественно орально-оральным путем. [ 8 ] В соответствии с этими путями передачи бактерии были выделены из фекалий , слюны и зубного налета . [ 138 ] H. pylori также может передаваться при употреблении зараженной пищи или воды. [ 139 ] Передача вируса происходит главным образом внутри семей в развитых странах, но также и от более широкого сообщества в развивающихся странах. [ 140 ]
Профилактика
[ редактировать ]Чтобы предотвратить развитие заболеваний, связанных с H. pylori , при подозрении на инфекцию рекомендуются схемы терапии на основе антибиотиков для уничтожения бактерий . [ 46 ] В случае успеха прогрессирование заболевания останавливается. Терапия первой линии рекомендуется, если диагностирована MALT-лимфома желудка низкой степени злокачественности, независимо от наличия H. pylori . Однако при тяжелом состоянии атрофического гастрита с поражением желудка схемы лечения на основе антибиотиков не рекомендуются, поскольку такие поражения часто необратимы и могут прогрессировать до рака желудка. [ 46 ] Если рак удается вылечить, рекомендуется следовать программе эрадикации, чтобы предотвратить рецидив инфекции или уменьшить рецидив рака, известный как метахронный. [ 46 ] [ 141 ] [ 142 ]
Из-за роли H. pylori как основной причины некоторых заболеваний (особенно рака) и его постоянно растущей устойчивости к антибиотикотерапии существует очевидная необходимость в альтернативных методах лечения. [ 143 ] Вакцина, направленная на развитие рака желудка, включая MALT-лимфому, также предотвратит развитие язвы желудка. [ 5 ] Главной целью является создание вакцины, которая будет профилактической для использования у детей и которая впоследствии будет иметь терапевтическое значение. Проблемой для этого являются чрезвычайное геномное разнообразие, демонстрируемое H. pylori , и сложные иммунные реакции хозяина. [ 143 ] [ 144 ]
Предыдущие исследования в Нидерландах и США показали, что такая программа профилактической вакцинации в конечном итоге будет экономически эффективной. [ 145 ] [ 146 ] Однако по состоянию на конец 2019 года не было ни одной передовой вакцины-кандидата, и только одна вакцина находилась в фазе I клинических испытаний. Более того, разработка вакцины против H. pylori не является приоритетом крупных фармацевтических компаний. [ 147 ] Ключевой мишенью для потенциальной терапии является протон-управляемый канал мочевины , поскольку секреция уреазы обеспечивает выживание бактерии. [ 148 ]
Уход
[ редактировать ]В Маастрихтском консенсусном отчете 2022 года вызванный H. pylori гастрит, , признан гастритом, индуцированным Helicobacter pylori , и был включен в МКБ11 . [ 44 ] [ 45 ] [ 46 ] Первоначально инфекция имеет тенденцию быть поверхностной и локализоваться в верхних слоях слизистой оболочки желудка. [ 149 ] Интенсивность хронического воспаления связана с цитотоксичностью штамма H. pylori . Большая цитотоксичность приведет к переходу от неатрофического гастрита к атрофическому гастриту с поражением слизистых желез . Это состояние является предпосылкой развития язвенной болезни и аденокарциномы желудка. [ 149 ]
эрадикация H. pylori Для лечения инфекции рекомендуется , в том числе при прогрессировании пептической язвенной болезни . Рекомендации по лечению первой линии — квадротерапия, состоящая из ингибитора протонной помпы , амоксициллина , кларитромицина и метронидазола . До лечения рекомендуется тестирование на устойчивость к антибиотикам. В регионах с известной резистентностью к кларитромицину терапию первой линии заменяют на схему на основе висмута , включающую тетрациклин и метронидазол, на 14 дней. Установлен высокий уровень резистентности к метронидазолу. Если один из этих курсов лечения оказался неэффективным, предлагается использовать альтернативный вариант. [ 44 ]
Неудача лечения может быть связана с устойчивостью к антибиотикам, а также с неадекватным подавлением кислоты ингибиторами протонной помпы. [ 150 ] После клинических испытаний блокатора кислоты, конкурирующего с калием, вонопразана , который обладает более сильным подавляющим кислоту действием. в 2022 году в США было одобрено использование [ 151 ] [ 150 ] Рекомендуется применять в сочетании с амоксициллином, с кларитромицином или без него. Было показано, что он оказывает более быстрое действие и может использоваться с пищей или без нее. [ 150 ] Успешные схемы эрадикации произвели революцию в лечении пептических язв. [ 152 ] [ 153 ] Эрадикация H. pylori также связана с последующим снижением риска рецидива язвы двенадцатиперстной кишки или желудка. [ 135 ]
Растительные экстракты и пробиотические продукты все чаще используются в качестве дополнения к обычному лечению. Пробиотические йогурты, содержащие молочнокислые бактерии , бифидобактерии и лактобактерии, оказывают подавляющее действие на инфекцию H. pylori , и было показано, что их использование улучшает скорость эрадикации. [ 14 ] Некоторые комменсальные кишечные бактерии, входящие в состав микробиоты кишечника, производят бутират , который действует как пребиотик и усиливает иммунный барьер слизистой оболочки. Их использование в качестве пробиотиков может помочь сбалансировать дисбактериоз кишечника, который сопровождает применение антибиотиков. [ 154 ] Было показано, что некоторые пробиотические штаммы обладают бактерицидной и бактериостатической активностью в отношении H. pylori , а также помогают сбалансировать дисбактериоз кишечника. [ 155 ] [ 134 ] Антибиотики оказывают негативное влияние на микробиоту желудочно-кишечного тракта и вызывают тошноту, диарею и тошноту , которые могут облегчить пробиотики. [ 134 ]
Устойчивость к антибиотикам
[ редактировать ]Повышение устойчивости к антибиотикам является основной причиной неудачи первоначального лечения. Факторы, связанные с резистентностью, включают мутации, откачивающие насосы и образование биопленок . [ 156 ] [ 157 ] Одним из основных антибиотиков, используемых при эрадикационной терапии, является кларитромицин , но штаммы, устойчивые к кларитромицину, стали широко распространенными, и необходимо рассмотреть возможность использования альтернативных антибиотиков. К счастью, стали доступны неинвазивные тесты кала на кларитромицин, которые позволяют отбирать пациентов, которые с большой вероятностью будут реагировать на терапию. [ 158 ] Также возросла множественная лекарственная устойчивость. [ 157 ] Могут быть использованы дополнительные курсы антибиотиков или другие методы лечения. [ 159 ] [ 160 ] [ 161 ] Секвенирование следующего поколения призвано выявить первоначальную специфическую устойчивость к антибиотикам, что поможет подобрать более эффективное лечение. [ 162 ]
В 2018 году ВОЗ включила H. pylori в список высокоприоритетных патогенов для исследования и открытия новых лекарств и методов лечения. [ 163 ] Растущая устойчивость к антибиотикам стимулировала интерес к разработке альтернативных методов лечения с использованием ряда растительных соединений. [ 164 ] [ 165 ] Растительные соединения имеют меньше побочных эффектов, чем синтетические лекарства. Большинство растительных экстрактов содержат сложную смесь компонентов, которые сами по себе не действуют как противомикробные препараты, но могут работать вместе с антибиотиками, улучшая лечение и преодолевая резистентность. [ 164 ] Растительные соединения имеют другой механизм действия, который оказался полезным в борьбе с устойчивостью к противомикробным препаратам. Различные соединения могут действовать, например, ингибируя ферменты, такие как уреаза, и адгезию к слизистой оболочке. [ 166 ] Было показано , что серосодержащие соединения растений с высокими концентрациями полисульфидов, кумаринов и терпенов эффективны против H. pylori . [ 164 ]
H. pylori обнаруживается в слюне и зубных бляшках . Известно, что передача инфекции осуществляется орально-орально, что позволяет предположить, что биопленка зубного налета может выступать в качестве резервуара для бактерий. Поэтому пародонтальная терапия или удаление зубного камня и строгание корней были предложены в качестве дополнительного лечения для повышения скорости эрадикации, но необходимы дополнительные исследования. [ 139 ] [ 167 ]
Рак
[ редактировать ]Рак желудка
[ редактировать ]Helicobacter pylori является фактором риска развития аденокарциномы желудка . [ 168 ] Лечение очень агрессивное: даже локализованное заболевание лечат последовательно химиотерапией и лучевой терапией перед хирургической резекцией. [ 169 ] Поскольку этот рак, однажды развившийся, не зависит от инфекции H. pylori , схемы эрадикации не используются. [ 170 ]
Желудочная MALT-лимфома и DLBCL
[ редактировать ]MALT-лимфомы представляют собой злокачественные новообразования лимфоидной ткани, ассоциированной со слизистой оболочкой . Ранние MALTомы желудка, вызванные H. pylori, можно успешно лечить (70–95% случаев) с помощью одной или нескольких программ эрадикации . [ 14 ] Примерно у 50–80% пациентов, у которых наблюдается эрадикация возбудителя, в течение 3–28 месяцев развивается ремиссия и длительный клинический контроль над лимфомой. Лучевая терапия желудка и окружающих (т.е. околожелудочных) лимфатических узлов также использовалась для успешного лечения этих локализованных случаев. Пациентов с нелокализованным (т.е. системным заболеванием III и IV стадии по Анн-Арбору), у которых отсутствуют симптомы, лечили с осторожным ожиданием или, при наличии симптомов, иммунотерапевтическим препаратом ритуксимабом (в течение 4 недель) в сочетании с химиотерапевтическим препаратом. , хлорамбуцил , в течение 6–12 месяцев; 58% этих пациентов достигают 58%-ной выживаемости без прогрессирования в течение 5 лет. Ослабленные пациенты III/IV стадии успешно лечатся только ритуксимабом или химиотерапевтическим препаратом циклофосфамидом . [ 171 ] Эрадикационная терапия антибиотиками-ингибиторами протонной помпы и локализованная лучевая терапия успешно используются для лечения H. pylori-положительных MALT-лимфом прямой кишки; однако лучевая терапия дала немного лучшие результаты, и поэтому ее предложили использовать в качестве предпочтительного лечения этого заболевания. [ 172 ] Однако общепризнанным методом выбора для пациентов с системными поражениями являются различные химиотерапевтические препараты, часто в сочетании с ритуксимабом.
MALT-лимфома редко может трансформироваться в более агрессивную диффузную крупноклеточную B-клеточную лимфому (DLBCL). [ 173 ] Если это связано с инфекцией H. pylori , DLBCL менее агрессивен и более поддается лечению. [ 174 ] [ 175 ] [ 176 ] Когда они ограничены желудком, их иногда успешно лечат с помощью программ эрадикации H. pylori . [ 54 ] [ 175 ] [ 177 ] [ 176 ] Если нет ответа или наблюдается ухудшение, можно рассмотреть более традиционную химиотерапию ( CHOP ), иммунотерапию или местную лучевую терапию, и любой из них или их комбинация успешно лечат эти более сложные типы. [ 175 ] [ 176 ]
Прогноз
[ редактировать ]Helicobacter pylori колонизирует желудок у большинства людей на протяжении десятилетий и вызывает хронический гастрит — длительное воспаление желудка. В большинстве В таких случаях симптомы никогда не проявляются, но примерно у 10–20% инфицированных в конечном итоге развиваются язвы желудка и двенадцатиперстной кишки, и возможный пожизненный риск развития рака желудка составляет 1–2%. [ 65 ]
H. pylori процветает при диете с высоким содержанием соли, что рассматривается как фактор риска окружающей среды, связанный с раком желудка. Диета с высоким содержанием соли усиливает колонизацию, усиливает воспаление, увеличивает экспрессию факторов вирулентности H. pylori и усиливает хронический гастрит. [ 178 ] [ 179 ] Парадоксально, но было обнаружено, что экстракты кимчи , соленой пробиотической пищи, оказывают профилактическое действие на H. pylori желудка, связанный с канцерогенез . [ 180 ]
При отсутствии лечения инфекция H. pylori обычно сохраняется на всю жизнь. [ 181 ] Инфекция может исчезнуть у пожилых людей, поскольку слизистая оболочка желудка становится все более атрофичной и невосприимчивой к колонизации. Некоторые исследования на детях до двух лет показали, что в этой возрастной группе инфекция может быть преходящей. [ 182 ] [ 183 ]
может H. pylori восстановиться у человека после эрадикации. Этот рецидив может быть вызван исходным штаммом ( рецидив ) или другим штаммом ( реинфекция ). Метаанализ 2017 года показал, что глобальные годовые показатели рецидивов, реинфекций и рецидивов на душу населения составляют 4,3%, 3,1% и 2,2% соответственно. Неясно, каковы основные факторы риска. [ 184 ]
Все больше данных свидетельствует о том, что H. pylori играет важную роль в защите от некоторых заболеваний. [ 16 ] Заболеваемость кислотным рефлюксом , пищеводом Барретта и раком пищевода резко возросла, в то время как присутствие H. pylori уменьшилось . [ 185 ] В 1996 году Мартин Дж. Блейзер выдвинул гипотезу о том, что H. pylori оказывает благотворное влияние, регулируя кислотность содержимого желудка. [ 51 ] [ 185 ] Гипотеза не является общепринятой, поскольку в нескольких рандомизированных контролируемых исследованиях не удалось продемонстрировать ухудшение симптомов кислотного рефлюкса после эрадикации H. pylori . [ 186 ] [ 187 ] Тем не менее, Блазер подтвердил свою точку зрения о том, что H. pylori является представителем нормальной микробиоты желудка . [ 17 ] Он постулирует, что изменения в физиологии желудка, вызванные потерей H. pylori , объясняют недавнее увеличение заболеваемости несколькими заболеваниями, включая диабет 2 типа , ожирение и астму. [ 17 ] [ 188 ] Его группа недавно показала, что колонизация H. pylori связана с более низкой заболеваемостью астмой у детей. [ 189 ]
Эпидемиология
[ редактировать ]По оценкам, в 2023 году около двух третей населения мира были инфицированы инфекцией H. pylori , которая чаще встречается в развивающихся странах . [ 20 ] Инфекция H. pylori более распространена в Южной Америке, странах Африки к югу от Сахары и на Ближнем Востоке. [ 153 ] Глобальная распространенность заметно снизилась в течение десятилетия после 2010 года, особенно в Африке. [ 21 ]
Возраст, в котором человек заражается этой бактерией, по-видимому, влияет на патологический исход инфекции. У людей, инфицированных в раннем возрасте, вероятно, разовьется более интенсивное воспаление, за которым может последовать атрофический гастрит с более высоким последующим риском развития язвы желудка, рака желудка или того и другого. Приобретение в более старшем возрасте вызывает различные изменения желудка, которые с большей вероятностью приводят к язве двенадцатиперстной кишки. [ 181 ] Во всех странах инфекции обычно приобретаются в раннем детстве. [ 32 ] Однако уровень инфицирования детей в развивающихся странах выше, чем в промышленно развитых странах , вероятно, из-за плохих санитарных условий, возможно, в сочетании с меньшим использованием антибиотиков при несвязанных патологиях. В развитых странах в настоящее время редко можно встретить инфицированных детей, но процент инфицированных людей увеличивается с возрастом. Более высокая распространенность среди пожилых людей отражает более высокий уровень инфицирования в детстве. [ 32 ] В Соединенных Штатах распространенность выше среди афроамериканцев и латиноамериканцев , скорее всего, из-за социально-экономических факторов. [ 190 ] [ 191 ] Более низкий уровень заражения на Западе во многом объясняется более высокими стандартами гигиены и широким использованием антибиотиков. Несмотря на высокие показатели инфицирования в некоторых регионах мира, общая частота инфицирования H. pylori снижается. [ 192 ] появляется устойчивость к антибиотикам Однако у H. pylori ; многие штаммы, устойчивые к метронидазолу и кларитромицину, обнаружены в большинстве частей мира. [ 193 ]
История
[ редактировать ]Helicobacter pylori мигрировала из Африки вместе со своим человеком-хозяином около 60 000 лет назад. [ 194 ] Исследования показали, что генетическое разнообразие H. pylori , как и его хозяина, уменьшается по мере географического удаления от Восточной Африки . Используя данные о генетическом разнообразии, исследователи создали модели, показывающие, что бактерии, по-видимому, распространились из Восточной Африки около 58 000 лет назад. Их результаты показывают, что современные люди уже были инфицированы H. pylori еще до их миграции из Африки, и с тех пор он остается связанным с людьми-хозяевами. [ 195 ]
H. pylori был впервые обнаружен в желудке пациентов с гастритом и язвой в 1982 году Барри Маршаллом и Робином Уорреном из Перта, Западная Австралия . В то время общепринято было считать, что ни одна бактерия не может жить в кислой среде человеческого желудка. В знак признания своего открытия Маршалл и Уоррен были удостоены Нобелевской премии по физиологии и медицине 2005 года . [ 196 ]
До исследований Маршалла и Уоррена немецкие ученые в 1875 году обнаружили спиралевидные бактерии в слизистой оболочке человеческого желудка, но им не удалось их культивировать , и результаты в конечном итоге были забыты. [ 185 ] Итальянский исследователь Джулио Биццозеро в 1893 году описал бактерии аналогичной формы, живущие в кислой среде желудка собак. [ 197 ] Профессор Валерий Яворский из Ягеллонского университета в Кракове исследовал осадки промывных вод желудка, полученные при промывании человека в 1899 году. Среди некоторых палочковидных бактерий он также обнаружил бактерии с характерной спиральной формой, которые он назвал Vibrio Rugula . Он первым предположил возможную роль этого организма в патогенезе желудочных заболеваний. Его работа была включена в « Справочник желудочных болезней» , но не имела большого значения, так как была опубликована только на польском языке. [ 198 ] Несколько небольших исследований, проведенных в начале 20 века, продемонстрировали наличие изогнутых стержней в желудке многих людей с язвенной болезнью и раком желудка. [ 199 ] Однако интерес к бактериям угас, когда американское исследование, опубликованное в 1954 году, не смогло обнаружить бактерии в 1180 биоптатах желудка. [ 200 ]
Интерес к пониманию роли бактерий в заболеваниях желудка возродился в 1970-х годах, когда были обнаружены бактерии в желудке людей с язвой желудка. [ 201 ] Бактерии также наблюдались в 1979 году Робином Уорреном, который исследовал их дальше вместе с Барри Маршаллом с 1981 года. После безуспешных попыток культивирования бактерий из желудка им, наконец, удалось визуализировать колонии в 1982 году, когда они непреднамеренно оставили свои чашки Петри. инкубация в течение пяти дней в пасхальные выходные. В своей оригинальной статье Уоррен и Маршалл утверждали, что большинство язв желудка и гастрита вызвано бактериальной инфекцией, а не стрессом или острой пищей , как предполагалось ранее. [ 202 ]
Первоначально был выражен некоторый скептицизм, но в течение нескольких лет несколько исследовательских групп подтвердили связь H. pylori с гастритом и, в меньшей степени, язвой. [ 203 ] Чтобы продемонстрировать, что H. pylori вызывает гастрит, а не был просто сторонним наблюдателем, Маршалл выпил стакан с H. pylori культурой . Через несколько дней он почувствовал тошноту и рвоту. При эндоскопии через 10 дней после прививки выявлены признаки гастрита и наличие H. pylori . Эти результаты позволили предположить, что H. pylori возбудителем был . Маршалл и Уоррен продемонстрировали, что антибиотики эффективны при лечении многих случаев гастрита. В 1994 году Национальные институты здравоохранения заявили, что большинство рецидивирующих язв двенадцатиперстной кишки и желудка вызваны H. pylori , и рекомендовали включить антибиотики в схему лечения. [ 204 ]
Первоначально бактерия называлась Campylobacter pyloridis , затем была переименована в C. pylori в 1987 году ( pylori — родительный падеж от слова pylori , круглого отверстия, ведущего из желудка в двенадцатиперстную кишку, от древнегреческого слова πυλωρός , что означает «привратник») . [ 205 ] ). [ 206 ] Когда рибосомальной РНК в 1989 году секвенирование гена и другие исследования показали, что бактерия не принадлежит к роду Campylobacter , ее поместили в отдельный род Helicobacter 16S от древнегреческого έλιξ ( hělix ) «спираль» или «спираль». [ 205 ] [ 207 ]
В октябре 1987 года группа экспертов встретилась в Копенгагене, чтобы основать Европейскую группу по изучению Helicobacter (EHSG), международную междисциплинарную исследовательскую группу и единственное учреждение, занимающееся H. pylori . [ 208 ] Группа участвует в ежегодном международном семинаре по хеликобактеру и родственным бактериям. [ 209 ] (переименована в Европейскую группу по изучению хеликобактера и микробиоты). [ 210 ] ), Отчеты Маастрихтского консенсуса (Европейский консенсус по лечению H. pylori ), [ 211 ] [ 212 ] [ 213 ] [ 214 ] и другие образовательные и исследовательские проекты, включая два международных долгосрочных проекта:
- Европейский регистр по лечению H. pylori (Hp-EuReg) – база данных, систематически регистрирующая рутинную клиническую практику европейских гастроэнтерологов. [ 215 ]
- Оптимальное лечение H. pylori в первичной медико-санитарной помощи (OptiCare) – долгосрочный образовательный проект, направленный на распространение научно обоснованных рекомендаций Маастрихтского IV консенсуса среди врачей первичной медико-санитарной помощи в Европе, финансируемый за счет образовательного гранта United European Gastroenterology . [ 216 ] [ 217 ]
Исследовать
[ редактировать ]Результаты исследований in vitro позволяют предположить, что жирные кислоты , главным образом полиненасыщенные жирные кислоты , обладают бактерицидным действием против H. pylori , но их действие in vivo не доказано. [ 218 ]
Устойчивость к антибиотикам, обеспечиваемая биопленками, вызвала множество исследований, направленных на изучение механизмов определения кворума, используемых при формировании биопленок. [ 88 ]
Подходящая вакцина против H.pylori , профилактическая или терапевтическая, является постоянной целью исследований. [ 8 ] работает Детский научно-исследовательский институт Мердока над разработкой вакцины, которая вместо того, чтобы конкретно воздействовать на бактерии, направлена на подавление вызванного воспаления, которое приводит к сопутствующим заболеваниям. [ 147 ]
Органоиды желудка могут быть использованы в качестве моделей для изучения патогенеза H. pylori . [ 95 ]
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Перейти обратно: а б Мартинес Л.Е., О'Брайен вице-президент, Леверих К.К., Ноблау С.Э., Салама Н.Р. (июль 2019 г.). «Неспиральные мутанты Helicobacter pylori демонстрируют измененную колонизацию желез и вызывают меньшую патологию желудка, чем спиральные бактерии во время хронической инфекции» . Заразить иммунитет . 87 (7). дои : 10.1128/IAI.00904-18 . ПМК 6589060 . ПМИД 31061142 .
- ^ Перейти обратно: а б Салама НР (апрель 2020 г.). «Морфология клеток как фактор вирулентности: уроки Helicobacter pylori» . Curr Opin Микробиол . 54 : 11–17. дои : 10.1016/j.mib.2019.12.002 . ПМЦ 7247928 . ПМИД 32014717 .
- ^ Перейти обратно: а б Раст М., Швайницер Т., Йозенханс С. (2008). «Жгутики Helicobacter, подвижность и хемотаксис» . В Ямаоке Ю. (ред.). Helicobacter pylori : молекулярная генетика и клеточная биология . Кайстер Академик Пресс. ISBN 978-1-904455-31-8 . Архивировано из оригинала 18 августа 2016 года . Проверено 1 апреля 2008 г.
- ^ Уоррен-младший, Маршалл Б. (июнь 1983 г.). «Неопознанные изогнутые бациллы на эпителии желудка при активном хроническом гастрите». Ланцет . 1 (8336): 1273–5. дои : 10.1016/S0140-6736(83)92719-8 . ПМИД 6134060 . S2CID 1641856 .
- ^ Перейти обратно: а б Фитцджеральд Р., Смит С.М. (2021). «Обзор инфекции Helicobacter pylori». Хеликобактер пилори . Методы Мол Биол. Том. 2283. стр. 1–14. дои : 10.1007/978-1-0716-1302-3_1 . ISBN 978-1-0716-1301-6 . ПМИД 33765303 . S2CID 232365068 .
- ^ Уоттс Дж. (октябрь 2005 г.). «Нобелевская премия присуждается врачам, открывшим H. pylori» . БМЖ . 331 (7520): 795. doi : 10.1136/bmj.331.7520.795 . ПМК 1246068 . ПМИД 16210262 .
- ^ Перейти обратно: а б «Хеликобактер пилори (H. pylori) и рак – НЦИ» . www.cancer.gov . 25 сентября 2013 г. Архивировано из оригинала 19 октября 2023 г. Проверено 18 октября 2023 г.
- ^ Перейти обратно: а б с д и де Бриту Б.Б., да Силва Ф.А., Соареш А.С., Перейра В.А., Сантос М.Л., Сампайо М.М. и др. (октябрь 2019 г.). «Патогенез и клиническое лечение инфекции желудка Helicobacter pylori» . Mundo J Гастроэнтерол . 25 (37): 5578–5589. дои : 10.3748/wjg.v25.i37.5578 . ПМК 6785516 . ПМИД 31602159 .
- ^ Чен CC, Лю Дж. М., Ли Ю. К., Хун Т. К., Эль-Омар Э. М., Ву М. С. (2021). «Взаимодействие Helicobacter pylori и желудочно-кишечной микробиотой» . Кишечные микробы . 13 (1): 1–22. дои : 10.1080/19490976.2021.1909459 . ПМЦ 8096336 . ПМИД 33938378 .
- ^ Перейти обратно: а б с д Мацуо Ю, Кидо Ю, Ямаока Ю (март 2017 г.). «Патогенез, связанный с белками наружной мембраны Helicobacter pylori» . Токсины . 9 (3): 101. doi : 10.3390/toxins9030101 . ПМК 5371856 . ПМИД 28287480 .
- ^ Перейти обратно: а б с Маргалани А.М., Бин Салман Т.О., Факих Ф.Дж., Асири М.К., Кабель А.М. (июнь 2020 г.). «Рак желудка: понимание факторов риска, методов диагностики, возможных направлений лечения и роли первичной медико-санитарной помощи» . J Family Med Prim Care . 9 (6): 2659–2663. дои : 10.4103/jfmpc.jfmpc_527_20 . ПМЦ 7491774 . ПМИД 32984103 .
- ^ Кога Ю. (декабрь 2022 г.). «Микробиота желудка и применение пробиотиков при гастродуоденальных заболеваниях» . Мир Дж Гастроэнтерол . 28 (47): 6702–6715. дои : 10.3748/wjg.v28.i47.6702 . ПМЦ 9813937 . ПМИД 36620346 .
- ^ Перейти обратно: а б Шин В.С., Се Ф., Чен Б., Ю Дж., Ло К.В., Цзе Г.М. и др. (октябрь 2023 г.). «Изучение микробиома при раке желудка: оценка потенциальных последствий и контекстуализация микроорганизмов, помимо H. pylori и вируса Эпштейна-Барра» . Раки . 15 (20): 4993. doi : 10.3390/cancers15204993 . ПМЦ 10605912 . ПМИД 37894360 .
- ^ Перейти обратно: а б с д Виолета Филип П., Кучуряну Д., Сорина Дьякону Л., Мария Владэряну А., Сильвия Поп С. (2018). «MALT-лимфома: эпидемиология, клиническая диагностика и лечение» . Журнал медицины и жизни . 11 (3): 187–193. дои : 10.25122/jml-2018-0035 . ПМК 6197515 . ПМИД 30364585 .
- ^ Руджеро П. (ноябрь 2014 г.). «Использование пробиотиков в борьбе с Helicobacter pylori» . World J Gastrointest Патофизиология . 5 (4): 384–91. дои : 10.4291/wjgp.v5.i4.384 . ПМК 4231502 . ПМИД 25400981 .
- ^ Перейти обратно: а б с д Сантос М.Л., де Бриту Б.Б., да Силва Ф.А., Сампайо М.М., Маркес Х.С., Оливейра Э. и др. (июль 2020 г.). «Инфекция Helcobacter pylori: помимо желудочных проявлений» . Mundo J Гастроэнтерол . 26 (28): 4076–4093. дои : 10.3748/wjg.v26.i28.4076 . ПМЦ 7403793 . ПМИД 32821071 .
- ^ Перейти обратно: а б с Блазер MJ (октябрь 2006 г.). «Кто мы? Коренные микробы и экология болезней человека» . Отчеты ЭМБО . 7 (10): 956–60. дои : 10.1038/sj.embor.7400812 . ПМЦ 1618379 . ПМИД 17016449 .
- ^ Гравина А.Г., Загари Р.М., Де Мусис С, Романо Л., Логерсио С., Романо М. (август 2018 г.). «Helicobacter pylori и внежелудочные заболевания: обзор» . Всемирный журнал гастроэнтерологии (обзор). 24 (29): 3204–3221. дои : 10.3748/wjg.v24.i29.3204 . ПМК 6079286 . ПМИД 30090002 .
- ^ Акерман Дж. (июнь 2012 г.). «Лучшая социальная сеть». Научный американец . Том. 306, нет. 6. С. 36–43. doi : 10.1038/scientificamerican0612-36 . ПМИД 22649992 .
- ^ Перейти обратно: а б «Helicobacter pylori | Желтая книга CDC 2024» . wwwnc.cdc.gov . Архивировано из оригинала 22 октября 2023 года . Проверено 20 октября 2023 г.
- ^ Перейти обратно: а б Ли Ю, Чхве Х., Люн К., Цзян Ф., Грэм Д.Ю., Люнг В.К. (19 апреля 2023 г.). «Глобальная распространенность инфекции Helicobacter pylori в период с 1980 по 2022 год: систематический обзор и метаанализ». Ланцет Гастроэнтерология и гепатология . 8 (6): 553–564. дои : 10.1016/S2468-1253(23)00070-5 . ПМИД 37086739 . S2CID 258272798 .
- ^ Хоой Дж.К., Лай В.Ю., Нг В.К., Суен М.М., Андервуд Ф.Е., Таньинго Д. и др. (август 2017 г.). «Глобальная распространенность инфекции Helicobacter pylori: систематический обзор и метаанализ» . Гастроэнтерология . 153 (2): 420–429. дои : 10.1053/j.gastro.2017.04.022 . ПМИД 28456631 .
- ^ Гудвин К.С., Армстронг Дж.А., Чилверс Т. и др. (1989). «Перенос Campylobacter pylori и Campylobacter mustelae в Helicobacter gen. nov. как Helicobacter pylori com. nov. и Helicobacter mustelae com. nov. соответственно» . Межд. Дж. Сист. Бактериол . 39 (4): 397–405. дои : 10.1099/00207713-39-4-397 .
- ^ Перейти обратно: а б Мартинес Л.Е., Хардкасл Дж.М., Ван Дж., Пинкус З., Цанг Дж., Гувер Т.Р. и др. (январь 2016 г.). «Штаммы Helicobacter pylori варьируют форму клеток и количество жгутиков, чтобы поддерживать устойчивую подвижность в вязкой среде» . Мол Микробиол . 99 (1): 88–110. дои : 10.1111/mmi.13218 . ПМЦ 4857613 . ПМИД 26365708 .
- ^ О'Рурк Дж., Боде Дж. (2001). Морфология и ультраструктура . АСМ Пресс. ISBN 978-1-55581-213-3 . ПМИД 21290748 .
- ^ Перейти обратно: а б Као С.И., Шеу Б.С., Ву Дж.Дж. (февраль 2016 г.). «Инфекция Helicobacter pylori: обзор бактериальных факторов вирулентности и патогенеза» . Биомедицинский журнал . 39 (1): 14–23. дои : 10.1016/j.bj.2015.06.002 . ПМК 6138426 . ПМИД 27105595 .
- ^ Иерарди Э., Лосурдо Г., Милети А., Паолильо Р., Джорджио Ф., Принципи М. и др. (май 2020 г.). «Загадка кокковидных форм Helicobacter pylori: за пределами фундаментальной науки» . Антибиотики . 9 (6): 293. doi : 10.3390/antibiotics9060293 . ПМЦ 7345126 . ПМИД 32486473 .
- ^ Луо Ц, Лю Н, Пу С, Чжуан З, Гун Х, Чжан Д (2023). «Обзор результатов исследований по немедикаментозной терапии Helicobacter pylori» . Передний микробиол . 14 : 1134254. doi : 10.3389/fmicb.2023.1134254 . ПМЦ 10063898 . ПМИД 37007498 .
- ^ Олсон Дж. В., Майер Р. Дж. (ноябрь 2002 г.). «Молекулярный водород как источник энергии для Helicobacter pylori». Наука . 298 (5599): 1788–90. Бибкод : 2002Sci...298.1788O . дои : 10.1126/science.1077123 . ПМИД 12459589 . S2CID 27205768 .
- ^ Перейти обратно: а б с Бадж Дж., Форма А., Ситарз М., Портинказа П., Гаррути Г., Красовска Д. и др. (декабрь 2020 г.). «Факторы вирулентности Helicobacter pylori – механизмы патогенности бактерий в микроокружении желудка» . Клетки . 10 (1): 27. doi : 10.3390/cells10010027 . ПМЦ 7824444 . ПМИД 33375694 .
- ^ Эльшенави Ю., Ху С., Хатроуби С. (июль 2023 г.). «Биопленка Helicobacter pylori: жизненный цикл, особенности и варианты лечения» . Антибиотики . 12 (8): 1260. doi : 10.3390/antibiotics12081260 . ПМЦ 10451559 . ПМИД 37627679 .
- ^ Перейти обратно: а б с д и ж г час я дж Кастерс Дж.Г., ван Влит А.Х., Кейперс Э.Дж. (июль 2006 г.). «Патогенез инфекции Helicobacter pylori» . Обзоры клинической микробиологии . 19 (3): 449–90. дои : 10.1128/CMR.00054-05 . ПМЦ 1539101 . ПМИД 16847081 .
- ^ Перейти обратно: а б Альзарани С., Лина Т.Т., Гонсалес Дж., Пинчук И.В., Бесвик Э.Дж., Рейес В.Е. (сентябрь 2014 г.). «Влияние Helicobacter pylori на эпителиальные клетки желудка» . Мир Дж Гастроэнтерол . 20 (36): 12767–80. дои : 10.3748/wjg.v20.i36.12767 . ПМК 4177462 . ПМИД 25278677 .
- ^ «Информация о геноме штаммов H. pylori 26695 и J99» . Институт Пастера. 2002. Архивировано из оригинала 26 ноября 2017 года . Проверено 1 сентября 2008 г.
- ^ « Helicobacter pylori J99, полный геном» . Национальный центр биотехнологической информации. Архивировано из оригинала 6 апреля 2011 года . Проверено 1 сентября 2008 г.
- ^ О Дж.Д., Клинг-Бекхед Х., Яннакис М., Сюй Дж., Фултон Р.С., Фултон Л.А. и др. (июнь 2006 г.). «Полная последовательность генома штамма Helicobacter pylori хронического атрофического гастрита: эволюция во время прогрессирования заболевания» . Труды Национальной академии наук Соединенных Штатов Америки . 103 (26): 9999–10004. Бибкод : 2006PNAS..103.9999O . дои : 10.1073/pnas.0603784103 . ПМК 1480403 . ПМИД 16788065 .
- ^ «Сборка генома Helicobacter pylori 26695 ASM30779v1» . НКБИ . Проверено 4 июня 2024 г.
- ^ Перейти обратно: а б с д Могила Дж.Ф., Уайт О., Керлаваж А.Р., Клейтон Р.А., Саттон Г.Г., Флейшманн Р.Д. и др. (август 1997 г.). «Полная последовательность генома желудочного возбудителя Helicobacter pylori» . Природа . 388 (6642): 539–47. Бибкод : 1997Natur.388..539T . дои : 10.1038/41483 . ПМИД 9252185 . S2CID 4411220 .
- ^ ван Влит АХ (январь 2017 г.). «Использование пангеномного анализа для идентификации генов, специфичных для линии Helicobacter pylori» . Письма FEMS по микробиологии . 364 (2): fnw296. дои : 10.1093/femsle/fnw296 . ПМИД 28011701 .
- ^ Утияма И., Албриттон Дж., Фукуё М., Кодзима К.К., Яхара К., Кобаяши И. (9 августа 2016 г.). «Новый подход к пангеномному анализу Helicobacter pylori для идентификации геномных островов» . ПЛОС ОДИН . 11 (8): e0159419. Бибкод : 2016PLoSO..1159419U . дои : 10.1371/journal.pone.0159419 . ПМЦ 4978471 . ПМИД 27504980 .
- ^ Перейти обратно: а б с Шарма С.М., Хоффман С., Дарфей Ф., Рейнье Дж., Финдейсс С., Ситтка А. и др. (март 2010 г.). «Первичный транскриптом основного патогена человека Helicobacter pylori». Природа . 464 (7286): 250–5. Бибкод : 2010Natur.464..250S . дои : 10.1038/nature08756 . ПМИД 20164839 . S2CID 205219639 .
- ^ Мюллер С.А., Перницш С.Р., Хаанге С.Б., Уетц П., фон Берген М., Шарма С.М. и др. (3 августа 2015 г.). «Мечение стабильных изотопов аминокислотами в протеомике на основе клеточных культур выявляет различия в содержании белка между спиральной и коккоидной формами желудочного патогена Helicobacter pylori» . Журнал протеомики . 126 : 34–45. дои : 10.1016/j.jprot.2015.05.011 . ISSN 1874-3919 . ПМИД 25979772 . S2CID 415255 . Архивировано из оригинала 27 июля 2021 года . Проверено 26 июля 2021 г.
- ^ Вухти С., Мюллер С.А., Кофилд Дж.Х., Хойзер Р., Элой П., Калкхоф С. и др. (май 2018 г.). «Данные о протеоме улучшают прогнозирование функции белка в интерактоме Helicobacter pylori» . Мол клеточная протеомика . 17 (5): 961–973. дои : 10.1074/mcp.RA117.000474 . ПМЦ 5930399 . ПМИД 29414760 .
- ^ Перейти обратно: а б с Мальфертайнер П., Меграуд Ф., Роккас Т., Гисберт Дж.П., Лиу Дж.М., Шульц С. и др. (август 2022 г.). «Лечение инфекции Helicobacter pylori: консенсусный отчет Маастрихта VI / Флоренции». Гут . 71 (9): 1724–1762. дои : 10.1136/gutjnl-2022-327745 . ПМИД 35944925 .
- ^ Перейти обратно: а б «МКБ-11 по статистике смертности и заболеваемости» . icd.who.int . Архивировано из оригинала 15 октября 2023 года . Проверено 9 января 2024 г.
- ^ Перейти обратно: а б с д и «Изменения, внесенные в новый консенсус экспертов по H. pylori» . Медскейп . Архивировано из оригинала 9 января 2024 года . Проверено 9 января 2024 г.
- ^ Репетто О, Веттори Р, Стеффан А, Канниццаро Р, Де Ре В (ноябрь 2023 г.). «Циркулирующие белки как диагностические маркеры рака желудка» . Int J Mol Sci . 24 (23): 16931. doi : 10.3390/ijms242316931 . ПМЦ 10706891 . ПМИД 38069253 .
- ^ Ливзан М.А., Мозговой С.И., Гаус О.В., Шиманская А.Г., Кононов А.В. (июль 2023 г.). «Гистопатологическая оценка атрофии слизистой оболочки желудка для прогнозирования риска рака желудка: проблемы и решения» . Диагностика . 13 (15): 2478. doi : 10.3390/diagnostics13152478 . ПМЦ 10417051 . PMID 37568841 .
- ^ Диксон М.Ф. (февраль 2000 г.). «Модели воспаления, связанные с язвенной болезнью». Лучшие практики и исследования Байьера. Клиническая гастроэнтерология . 14 (1): 27–40. дои : 10.1053/bega.1999.0057 . ПМИД 10749087 .
- ^ Моммерстег М.С., Ю Б.Т., ван ден Бош Т.П., фон дер Тюзен Дж.Х., Куйперс Э.Дж., Дукас М. и др. (октябрь 2022 г.). «Конститутивная экспрессия лиганда запрограммированной смерти 1 защищает G-клетки желудка от воспаления, вызванного Helicobacter pylori» . Хеликобактер . 27 (5): e12917. дои : 10.1111/hel.12917 . ПМЦ 9542424 . ПМИД 35899973 . S2CID 251132578 .
- ^ Перейти обратно: а б Блазер М.Дж., Атертон Дж.К. (февраль 2004 г.). «Персистенция Helicobacter pylori: биология и болезни» . Журнал клинических исследований . 113 (3): 321–33. дои : 10.1172/JCI20925 . ПМК 324548 . ПМИД 14755326 .
- ^ Шуберт М.Л., Пеура Д.А. (июнь 2008 г.). «Контроль секреции желудочной кислоты в норме и при заболеваниях». Гастроэнтерология . 134 (7): 1842–60. дои : 10.1053/j.gastro.2008.05.021 . ПМИД 18474247 . S2CID 206210451 .
- ^ Аббас Х., Ниязи М., Маккер Дж. (май 2017 г.). «Лимфома толстой кишки, ассоциированная со слизистой оболочкой (MALT): описание случая и обзор литературы» . Американский журнал клинических случаев . 18 : 491–497. дои : 10.12659/AJCR.902843 . ПМК 5424574 . ПМИД 28469125 .
- ^ Перейти обратно: а б Пайдас С (апрель 2015 г.). «Эрадикация Helicobacter pylori при диффузной крупноклеточной В-клеточной лимфоме желудка» . Всемирный журнал гастроэнтерологии . 21 (13): 3773–6. дои : 10.3748/wjg.v21.i13.3773 . ПМЦ 4385524 . ПМИД 25852262 .
- ^ Койперс Э.Дж. (март 1999 г.). «Обзорная статья: изучение связи между Helicobacter pylori и раком желудка». Алиментарная фармакология и терапия . 13 (Приложение 1): 3–11. дои : 10.1046/j.1365-2036.1999.00002.x . ПМИД 10209681 . S2CID 19231673 .
- ^ Ферлей Дж., Коломбет М., Сёрджоматарам И., Мазерс С., Паркин Д.М., Пиньерос М. и др. (апрель 2019 г.). «Оценка глобальной заболеваемости и смертности от рака в 2018 году: источники и методы GLOBOCAN» . Международный журнал рака . 144 (8): 1941–1953. дои : 10.1002/ijc.31937 . ПМИД 30350310 .
- ^ Дэн Цзюй, Лян Х (апрель 2014 г.). «Клиническое значение метастазирования в лимфатические узлы при раке желудка» . Всемирный журнал гастроэнтерологии . 20 (14): 3967–75. дои : 10.3748/wjg.v20.i14.3967 . ПМЦ 3983452 . ПМИД 24744586 .
- ^ Перейти обратно: а б Валенсуэла М.А., Каналес Х., Корвалан А.Х., Quest AF (декабрь 2015 г.). «Воспаление, вызванное Helicobacter pylori, и эпигенетические изменения во время канцерогенеза желудка» . Всемирный журнал гастроэнтерологии . 21 (45): 12742–56. дои : 10.3748/wjg.v21.i45.12742 . ПМК 4671030 . ПМИД 26668499 .
- ^ Перейти обратно: а б Раза Ю., Хан А., Фаруки А., Мубарак М., Фациста А., Ахтар С.С. и др. (октябрь 2014 г.). «Окислительное повреждение ДНК как потенциальный ранний биомаркер канцерогенеза, связанного с Helicobacter pylori». Патологические и онкологические исследования . 20 (4): 839–46. дои : 10.1007/s12253-014-9762-1 . ПМИД 24664859 . S2CID 18727504 .
- ^ Кеппель М., Гарсия-Алькальде Ф., Гловински Ф., Шлаерманн П., Мейер Т.Ф. (июнь 2015 г.). «Инфекция Helicobacter pylori вызывает характерные повреждения ДНК в клетках человека» . Отчеты по ячейкам . 11 (11): 1703–13. дои : 10.1016/j.celrep.2015.05.030 . ПМИД 26074077 .
- ^ Перейти обратно: а б с д Марковский А.Р., Марковская А., Гузинска-Устимович К. (октябрь 2016 г.). «Патофизиологические и клинические аспекты гиперпластических полипов желудка» . Всемирный журнал гастроэнтерологии . 22 (40): 8883–8891. дои : 10.3748/wjg.v22.i40.8883 . ПМК 5083793 . ПМИД 27833379 .
- ^ Донг Ю.Ф., Го Т., Ян Х., Цянь Дж.М., Ли Дж.Н. (февраль 2019 г.). «[Корреляция между инфекцией Helicobacter pylori желудка и колоректальными полипами или раком]». Чжунхуа Нэй Кэ За Чжи (на китайском языке). 58 (2): 139–142. doi : 10.3760/cma.j.issn.0578-1426.2019.02.011 . ПМИД 30704201 .
- ^ Перейти обратно: а б Цзо Ю, Цзин З, Би М, Сюй С, Хао Икс, Ван Б (сентябрь 2020 г.). «Связь между инфекцией Helicobacter pylori и риском колоректального рака: систематический обзор и метаанализ» . Медицина (Балтимор) . 99 (37): e21832. дои : 10.1097/MD.0000000000021832 . ПМЦ 7489651 . ПМИД 32925719 .
- ^ Папастергиу В., Каратапанис С., Георгопулос С.Д. (январь 2016 г.). «Helicobacter pylori и колоректальная неоплазия: есть ли причинно-следственная связь?» . Мир Дж Гастроэнтерол . 22 (2): 649–58. дои : 10.3748/wjg.v22.i2.649 . ПМК 4716066 . ПМИД 26811614 .
- ^ Перейти обратно: а б с Дебовски А.В., Уолтон С.М., Чуа Э.Г., Тай А.С., Ляо Т., Ламичхане Б. и др. (июнь 2017 г.). «Подавление гена Helicobacter pylori in vivo демонстрирует, что уреаза необходима для хронической инфекции» . ПЛОС Патогены . 13 (6): e1006464. дои : 10.1371/journal.ppat.1006464 . ПМК 5500380 . ПМИД 28644872 .
- ^ Аль Кораан А.М., Беривал Н., Сангай П., Намгьял Т. (октябрь 2019 г.). «Психотическое влияние хеликобактерного гастрита и функциональной диспепсии на депрессию: систематический обзор» . Куреус . 11 (10): е5956. дои : 10.7759/cureus.5956 . ПМК 6863582 . ПМИД 31799095 .
- ^ Перейти обратно: а б «Тесты на Helicobacter Pylori (H. Pylori): медицинский тест MedlinePlus» . medlineplus.gov . Архивировано из оригинала 16 февраля 2024 года . Проверено 16 февраля 2024 г.
- ^ Перейти обратно: а б «Симптомы и причины язвенной болезни (язвы желудка или двенадцатиперстной кишки) - NIDDK» . Национальный институт диабета, заболеваний органов пищеварения и почек . Архивировано из оригинала 17 февраля 2024 года . Проверено 17 февраля 2024 г.
- ^ Попа Д.Г., Облеагэ К.В., Соча Б., Сербан Д., Чуря М.Е., Диаконеску М. и др. (октябрь 2021 г.). «Роль Helicobacter pylori в возникновении и развитии геморрагических гастродуоденальных поражений» . Exp Ther Med . 22 (4): 1147. doi : 10.3892/etm.2021.10582 . ПМЦ 8392874 . ПМИД 34504592 .
- ^ Аль-Азри М., Аль-Кинди Дж., Аль-Харти Т., Аль-Дахри М., Панчатчарам С.М., Аль-Манири А. (июнь 2019 г.). «Осведомленность о факторах риска рака желудка и колоректального рака, симптомах и времени, необходимом для обращения за медицинской помощью среди населения, посещающего учреждения первичной медико-санитарной помощи в провинции Маскат, Оман» . Журнал онкологического образования . 34 (3): 423–434. дои : 10.1007/s13187-017-1266-8 . ISSN 0885-8195 . ПМИД 28782080 . S2CID 4017466 . Архивировано из оригинала 24 февраля 2024 года . Проверено 20 января 2024 г.
- ^ У Ц, Ян ЗП, Сюй П, Гао LC, Фань ДМ (июль 2013 г.). «Связь между инфекцией Helicobacter pylori и риском колоректальной неоплазии: систематический обзор и метаанализ». Колоректальное заболевание . 15 (7): е352-64. дои : 10.1111/codi.12284 . ПМИД 23672575 . S2CID 5444584 .
- ^ Соетикно Р.М., Кальтенбах Т., Роуз Р.В., Парк В., Махешвари А., Сато Т. и др. (март 2008 г.). «Распространенность неполипоидных (плоских и вдавленных) колоректальных новообразований у бессимптомных и симптоматических взрослых» . ДЖАМА . 299 (9): 1027–35. дои : 10.1001/jama.299.9.1027 . ПМИД 18319413 .
- ^ Перейти обратно: а б Ямаока Ю., Саруулджавхлан Б., Альфарай Р.И., Линц Б. (2023). «Патогеномика Helicobacter pylori». Хеликобактер пилори и рак желудка . Актуальные темы микробиологии и иммунологии. Том. 444. стр. 117–155. дои : 10.1007/978-3-031-47331-9_5 . ISBN 978-3-031-47330-2 . ПМИД 38231217 .
- ^ Альфарук К.О., Башир А.Х., Альжарбу А.Н., Рамадан А.М., Муддатир А.К., АльХуфи С.Т. и др. (22 февраля 2019 г.). «Helicobacter pylori при раке желудка и его лечение» . Границы онкологии . 9:75 . doi : 10.3389/fonc.2019.00075 . ПМК 6395443 . ПМИД 30854333 .
- ^ Сантос Х.К., Рибейро М.Л. (август 2015 г.). «Эпигенетическая регуляция механизма репарации ДНК при канцерогенезе желудка, индуцированном Helicobacter pylori» . Всемирный журнал гастроэнтерологии . 21 (30): 9021–37. дои : 10.3748/wjg.v21.i30.9021 . ПМЦ 4533035 . ПМИД 26290630 .
- ^ Раза Ю., Ахмед А., Хан А., Чишти А.А., Ахтер С.С., Мубарак М. и др. (май 2020 г.). «Helicobacter pylori серьезно снижает экспрессию белков репарации ДНК PMS2 и ERCC1 при гастрите и раке желудка» . Восстановление ДНК . 89 : 102836. doi : 10.1016/j.dnarep.2020.102836 . ПМИД 32143126 .
- ^ Доре М.П., Пес Г.М., Бассотти Дж., Усай-Сатта П. (2016). «Диспепсия: когда и как проверить наличие инфекции Helicobacter pylori» . Гастроэнтерологические исследования и практика . 2016 : 8463614. doi : 10.1155/2016/8463614 . ПМЦ 4864555 . ПМИД 27239194 .
- ^ Перейти обратно: а б Мухаммад Дж.С., Эладл М.А., Ходер Г. (февраль 2019 г.). «Метилирование ДНК, вызванное Helicobacter pylori, как эпигенетический модулятор рака желудка: недавние результаты и будущее направление» . Патогены . 8 (1): 23. doi : 10.3390/pathogens8010023 . ПМК 6471032 . ПМИД 30781778 .
- ^ Перейти обратно: а б Ното Дж. М., Пик Р. М. (2011). «Роль микроРНК в патогенезе Helicobacter pylori и канцерогенезе желудка» . Границы клеточной и инфекционной микробиологии . 1 : 21. дои : 10.3389/fcimb.2011.00021 . ПМЦ 3417373 . ПМИД 22919587 .
- ^ Цудзи С., Каваи Н., Цудзи М., Кавано С., Хори М. (июль 2003 г.). «Обзорная статья: стимулирование желудочно-кишечного канцерогенеза, связанное с воспалением - перигенетический путь» . Алиментарная фармакология и терапия . 18 (Приложение 1): 82–9. дои : 10.1046/j.1365-2036.18.s1.22.x . ПМИД 12925144 . S2CID 22646916 .
- ^ Ю Б., де Вос Д., Го X, Пэн С., Се В., Пеппеленбош М.П. и др. (апрель 2024 г.). «IL-6 способствует перекрестному взаимодействию между эпителиальными клетками и опухолеассоциированными макрофагами при канцерогенезе желудка, связанном с Helicobacter pylori» . Неоплазия . 50 : 100981. дои : 10.1016/j.neo.2024.100981 . ПМЦ 10912637 . ПМИД 38422751 .
- ^ Перейти обратно: а б Суганума М., Ямагути К., Оно Ю., Мацумото Х., Хаяши Т., Огава Т. и др. (июль 2008 г.). «Белок, индуцирующий TNF-альфа, канцерогенный фактор, секретируемый H. pylori, проникает в клетки рака желудка» . Международный журнал рака . 123 (1): 117–22. дои : 10.1002/ijc.23484 . ПМИД 18412243 . S2CID 5532769 .
- ^ Дуань Ц, Чжоу М, Чжу Л, Чжу Г (январь 2013 г.). «Жгутики и патогенность бактерий». J Базовая микробиол . 53 (1): 1–8. дои : 10.1002/jobm.201100335 . ПМИД 22359233 . S2CID 22002199 .
- ^ Перейти обратно: а б с Неделькович М., Састре Д.Е., Сундберг Э.Ю. (июль 2021 г.). «Бактериальная жгутиковая нить: супрамолекулярная многофункциональная наноструктура» . Int J Mol Sci . 22 (14): 7521. doi : 10.3390/ijms22147521 . ПМК 8306008 . ПМИД 34299141 .
- ^ Эльбехири А., Марзук Э., Алдубайб М., Абалхаил А., Анагрейя С., Анаджири Н. и др. (январь 2023 г.). «Инфекция Helicobacter pylori: текущее состояние и перспективы на будущее в области диагностики, терапии и контроля» . Антибиотики . 12 (2): 191. doi : 10.3390/antibiotics12020191 . ПМЦ 9952126 . ПМИД 36830102 .
- ^ Петерсен А.М., Крогфельт К.А. (май 2003 г.). «Helicobacter pylori: вторгающийся микроорганизм? Обзор» . ФЭМС Иммунология и медицинская микробиология (обзор). 36 (3): 117–26. дои : 10.1016/S0928-8244(03)00020-8 . ПМИД 12738380 .
- ^ Али А., Аль-Хусайни К.И. (январь 2024 г.). «Helicobacter pylori: современный взгляд на патогенез, диагностику и стратегии лечения» . Микроорганизмы . 12 (1): 222. doi : 10.3390/microorganisms12010222 . ПМЦ 10818838 . ПМИД 38276207 .
- ^ Перейти обратно: а б Зафер М.М., Мохамед Г.А., Ибрагим С.Р., Гош С., Борнман С., Эльфаки М.А. (февраль 2024 г.). «Инфекции, опосредованные биопленками, вызванные микробами с множественной лекарственной устойчивостью: всестороннее исследование и перспективы» . Арка Микробиол . 206 (3): 101. Бибкод : 2024ArMic.206..101Z . дои : 10.1007/s00203-023-03826-z . ПМЦ 10867068 . ПМИД 38353831 .
- ^ Перейти обратно: а б Сунь Ц, Юань С, Чжоу С, Лу Дж, Цзэн М, Цай Икс и др. (2023). «Инфекция Helicobacter pylori: динамический процесс от диагностики до лечения» . Передняя клетка заражает микробиол . 13 : 1257817. doi : 10.3389/fcimb.2023.1257817 . ПМЦ 10621068 . ПМИД 37928189 .
- ^ Перейти обратно: а б с д и ж Линь Ц, Линь С, Фань З, Лю Дж, Е Д, Го П (май 2024 г.). «Обзор механизмов бактериальной колонизации кишечника млекопитающих» . Микроорганизмы . 12 (5): 1026. doi : 10.3390/microorganisms12051026 . ПМЦ 11124445 . ПМИД 38792855 .
- ^ Перейти обратно: а б с Эрнандес В.М., Артеага А., Данн М.Ф. (ноябрь 2021 г.). «Разнообразие, свойства и функции бактериальных аргиназ». FEMS Микробиол Ред . 45 (6). дои : 10.1093/femsre/fuab034 . ПМИД 34160574 .
- ^ Перейти обратно: а б Ли С, Чжао В, Ся Л, Конг Л, Ян Л (2023). «Сколько времени потребуется для запуска эффективной вакцины против Helicobacter pylori для людей?» . Заразить устойчивость к лекарствам . 16 : 3787–3805. дои : 10.2147/IDR.S412361 . ПМЦ 10278649 . ПМИД 37342435 .
- ^ Джордж Г., Комбрабайл М., Ранинга Н., Сау А.К. (март 2017 г.). «Аргиназа желудочных возбудителей Helicobacter использует уникальный набор некаталитических остатков для катализа» . Биофизический журнал . 112 (6): 1120–1134. Бибкод : 2017BpJ...112.1120G . дои : 10.1016/j.bpj.2017.02.009 . ПМК 5376119 . ПМИД 28355540 .
- ^ Смут Д.Т. (декабрь 1997 г.). «Как Helicobacter pylori вызывает повреждение слизистой оболочки? Прямые механизмы» . Гастроэнтерология . 113 (6 Доп.): S31-4, обсуждение S50. дои : 10.1016/S0016-5085(97)80008-X . ПМИД 9394757 .
- ^ Перейти обратно: а б с Духан Д., Резкита Я.А., Васкито Л.А., Ямаока Ю., Мифтахуссурур М. (июль 2021 г.). «Ключевая роль Helicobacter pylori BabA-SabA на этапе приверженности: синергический механизм успешной колонизации и развития заболевания» . Токсины . 13 (7): 485. doi : 10.3390/toxins13070485 . ПМК 8310295 . ПМИД 34357957 .
- ^ Рад Р., Герхард М., Ланг Р., Шёнигер М., Рёш Т., Шепп В. и др. (15 марта 2002 г.). «Антигенсвязывающий антиген группы крови клей Helicobacter pylori облегчает бактериальную колонизацию и усиливает неспецифический иммунный ответ» . Журнал иммунологии . 168 (6): 3033–3041. doi : 10.4049/jimmunol.168.6.3033 . ПМИД 11884476 .
- ^ Бугайцова Ю.А., Бьернхам О., Чернов Ю.А., Гидеонссон П., Хенрикссон С., Мендес М. и др. (март 2017 г.). «Helicobacter pylori адаптируется к хронической инфекции и заболеванию желудка посредством рН-зависимого присоединения, опосредованного BabA» . Клетка-хозяин и микроб . 21 (3): 376–389. дои : 10.1016/j.chom.2017.02.013 . ПМЦ 5392239 . ПМИД 28279347 .
- ^ Махдави Дж., Соден Б., Хуртиг М., Ольфат Ф.О., Форсберг Л., Рош Н. и др. (июль 2002 г.). «Адгезин Helicobacter pylori SabA при персистирующей инфекции и хроническом воспалении» . Наука . 297 (5581): 573–8. Бибкод : 2002Sci...297..573M . дои : 10.1126/science.1069076 . ПМК 2570540 . ПМИД 12142529 .
- ^ Перейти обратно: а б с Тестерман Т.Л., Моррис Дж. (сентябрь 2014 г.). «За пределами желудка: обновленный взгляд на патогенез, диагностику и лечение Helicobacter pylori» . Всемирный журнал гастроэнтерологии (обзор). 20 (36): 12781–808. дои : 10.3748/wjg.v20.i36.12781 . ПМЦ 4177463 . ПМИД 25278678 .
- ^ Чжан Л., Се Дж. (сентябрь 2023 г.). «Биосинтез, структура и биологическая функция холестерина глюкозида у Helicobacter pylori: обзор» . Медицина (Балтимор) . 102 (36): e34911. дои : 10.1097/MD.0000000000034911 . ПМЦ 10489377 . ПМИД 37682174 .
- ^ Ридьярд К.Э., Оверхейдж Дж. (май 2021 г.). «Потенциал человеческого пептида LL-37 в качестве антимикробного и антибиопленочного агента» . Антибиотики . 10 (6): 650. doi : 10.3390/antibiotics10060650 . ПМК 8227053 . ПМИД 34072318 .
- ^ Перейти обратно: а б Hsu CY, Yeh JY, Chen CY, Wu HY, Chiang MH, Wu CL и др. (декабрь 2021 г.). «Холестерол-α-глюкозилтрансфераза Helicobacter pylori манипулирует холестерином, обеспечивая прикрепление бактерий к эпителиальным клеткам желудка» . Вирулентность . 12 (1): 2341–2351. дои : 10.1080/21505594.2021.1969171 . ПМЦ 8437457 . ПМИД 34506250 .
- ^ Мори П., Пфанкух Л., Панг Э., Бокчеллато Ф., Сигал М., Имаи-Мацушима А. и др. (апрель 2018 г.). «Helicobacter pylori истощает уровень холестерина в железах желудка, чтобы предотвратить передачу сигналов гамма-интерферона и избежать воспалительной реакции». Гастроэнтерология . 154 (5): 1391–1404.e9. дои : 10.1053/j.gastro.2017.12.008 . hdl : 21.11116/0000-0001-3B12-9 . ПМИД 29273450 .
- ^ Перейти обратно: а б Рамарао Н., Грей-Оуэн С.Д., Мейер Т.Ф. (октябрь 2000 г.). «Helicobacter pylori индуцирует, но выдерживает внеклеточное высвобождение кислородных радикалов из профессиональных фагоцитов, используя свою каталазную активность». Мол Микробиол . 38 (1): 103–13. дои : 10.1046/j.1365-2958.2000.02114.x . hdl : 11858/00-001M-0000-000E-C7AD-8 . ПМИД 11029693 .
- ^ «ЮниПрот» . www.uniprot.org . Проверено 20 марта 2024 г.
- ^ «Белок, индуцирующий TNF-альфа» . www.uniprot.org . Проверено 8 апреля 2024 г.
- ^ Ватанабэ Т., Такахаши А., Сузуки К., Курусу-Канно М., Ямагути К., Фуджики Х. и др. (15 мая 2014 г.). «Эпителиально-мезенхимальный переход в клеточных линиях рака желудка человека, индуцированный TNF-α-индуцирующим белком Helicobacter pylori: миграция клеток, индуцированная Tipα H. pylori». Международный журнал рака . 134 (10): 2373–2382. дои : 10.1002/ijc.28582 . ПМИД 24249671 .
- ^ Уоллден К., Ривера-Кальсада А., Ваксман Г. (сентябрь 2010 г.). «Системы секреции типа IV: универсальность и разнообразие функций» . Клеточная микробиол . 12 (9): 1203–12. дои : 10.1111/j.1462-5822.2010.01499.x . ПМК 3070162 . ПМИД 20642798 .
- ^ Перейти обратно: а б Бруте Н., Марэ А., Ламульятт Х., де Маскарель А., Самойо Р., Саламон Р. и др. (апрель 2001 г.). «Статус CagA и результаты эрадикационного лечения тройной терапией против Helicobacter pylori у пациентов с неязвенной диспепсией» . Журнал клинической микробиологии . 39 (4): 1319–22. doi : 10.1128/JCM.39.4.1319-1322.2001 . ПМЦ 87932 . ПМИД 11283049 .
- ^ Завилак-Павлик А., Зажецка У., Жила-Уклеевич Д., Лах Дж., Страпагель Д., Тегтмейер Н. и др. (август 2019 г.). «Появление мутантов сериновой протеазы htrA у Helicobacter pylori связано с мутациями secA» . Научные отчеты 9 (1): 11794. Бибкод : 2019NatSR... 911794Z. дои : 10.1038/ s41598-019-48030-6 ПМК 6692382 . ПМИД 31409845 .
- ^ Пик Р.М., Крэбтри Дж.Э. (январь 2006 г.). «Хеликобактерная инфекция и неоплазия желудка» . Журнал патологии . 208 (2): 233–48. дои : 10.1002/путь.1868 . ПМИД 16362989 . S2CID 31718278 .
- ^ Виала Дж., Чапут С., Бонека И.Г., Кардона А., Жирардин С.Е., Моран А.П. и др. (ноябрь 2004 г.). «Nod1 реагирует на пептидогликан, доставляемый островом патогенности Helicobacter pylori cag». Природная иммунология . 5 (11): 1166–74. дои : 10.1038/ni1131 . ПМИД 15489856 . S2CID 2898805 .
- ^ Бакерт С., Зельбах М. (август 2008 г.). «Роль секреции типа IV в патогенезе Helicobacter pylori» . Клеточная микробиология . 10 (8): 1573–81. дои : 10.1111/j.1462-5822.2008.01156.x . ПМИД 18410539 . S2CID 37626 .
- ^ Хатакеяма М. (сентябрь 2004 г.). «Онкогенные механизмы белка CagA Helicobacter pylori». Обзоры природы. Рак . 4 (9): 688–94. дои : 10.1038/nrc1433 . ПМИД 15343275 . S2CID 1218835 .
- ^ Ким В., Мосс С.Ф. (2008). «Роль Helicobacter pylori в патогенезе злокачественных новообразований желудка». Обзоры онкологии . 2 (3): 131–140. дои : 10.1007/s12156-008-0068-y .
- ^ «ЮниПрот» . www.uniprot.org . Проверено 21 марта 2024 г.
- ^ Мильке С., Ю. Дж., Шупплер М., Фрингс С., Кирш С., Неграшус Н. и др. (апрель 2001 г.). «Статус Helicobacter pylori vacA, IceA и CagA и картина гастрита у пациентов со злокачественными и доброкачественными заболеваниями гастродуоденальной зоны» . Американский журнал гастроэнтерологии . 96 (4): 1008–13. дои : 10.1111/j.1572-0241.2001.03685.x . ПМИД 11316139 . S2CID 24024542 . Архивировано из оригинала 23 февраля 2022 года . Проверено 24 июня 2020 г.
- ^ Перейти обратно: а б Хисацунэ Дж., Ямасаки Э., Накаяма М., Ширасака Д., Куразоно Х., Катагата Ю. и др. (сентябрь 2007 г.). «Helicobacter pylori VacA усиливает выработку простагландина E2 за счет индукции экспрессии циклооксигеназы 2 через каскад p38-митоген-активируемой протеинкиназы/активирующего транскрипционного фактора 2 в клетках AZ-521» . Заразить иммунитет . 75 (9): 4472–81. дои : 10.1128/IAI.00500-07 . ЧВК 1951161 . ПМИД 17591797 .
- ^ Капурро М.И., Гринфилд Л.К., Прашар А., Ся С., Абдулла М., Вонг Х. и др. (август 2019 г.). «VacA создает защитный внутриклеточный резервуар для Helicobacter pylori, который устраняется путем активации лизосомального кальциевого канала TRPML1» . Природная микробиология . 4 (8): 1411–1423. дои : 10.1038/s41564-019-0441-6 . ПМЦ 6938649 . ПМИД 31110360 .
- ^ Саджиб С., Захра Ф.Т., Лионакис М.С., Герман Н.А., Микелис К.М. (февраль 2018 г.). «Механизмы ангиогенеза при микробно-регулируемых воспалительных и неопластических состояниях». Ангиогенез . 21 (1): 1–14. дои : 10.1007/s10456-017-9583-4 . ПМИД 29110215 . S2CID 3346742 .
- ^ да Кошта ДМ, Перейра Эдос С, Рабенхорст СХ (октябрь 2015 г.). «Что существует помимо cagA и vacA? Гены Helicobacter pylori при заболеваниях желудка» . Мир Дж Гастроэнтерол . 21 (37): 10563–72. дои : 10.3748/wjg.v21.i37.10563 . ПМК 4588078 . ПМИД 26457016 .
- ^ Думрезе С., Сломянка Л., Зиглер У., Чой С.С., Калия А., Фулурия А. и др. (май 2009 г.). «Секретируемый богатый цистеином белок А Helicobacter вызывает прилипание моноцитов человека и дифференцировку в макрофагоподобный фенотип» . Письма ФЭБС . 583 (10): 1637–43. Бибкод : 2009FEBSL.583.1637D . дои : 10.1016/j.febslet.2009.04.027 . ПМЦ 2764743 . ПМИД 19393649 .
- ^ Алам Дж., Саркар А., Кармакар Б.С., Гангули М., Пол С., Мухопадьяй А.К. (август 2020 г.). «Новый фактор вирулентности dupA Helicobacter pylori как важный фактор риска проявления заболевания: обзор» . Мир Дж Гастроэнтерол . 26 (32): 4739–4752. дои : 10.3748/wjg.v26.i32.4739 . ПМЦ 7459207 . ПМИД 32921954 .
- ^ Перейти обратно: а б с д Трастой Р., Мансо Т., Фернандес-Гарсиа Л., Бласко Л., Амброа А., Перес Дель Молино М.Л. и др. (октябрь 2018 г.). «Механизмы толерантности и устойчивости бактерий в желудочно-кишечной и респираторной среде» . Клин Микробиол Ред. 31 (4). дои : 10.1128/CMR.00023-18 . ПМК 6148185 . ПМИД 30068737 .
- ^ Ольчак А.А., Олсон Дж.В., Майер Р.Дж. (июнь 2002 г.). «Мутанты Helicobacter pylori, устойчивые к окислительному стрессу» . Журнал бактериологии . 184 (12): 3186–93. дои : 10.1128/JB.184.12.3186-3193.2002 . ПМК 135082 . ПМИД 12029034 .
- ^ Перейти обратно: а б с д Дорер М.С., Феро Дж., Салама Н.Р. (июль 2010 г.). Бланке С.Р. (ред.). «Повреждение ДНК запускает генетический обмен у Helicobacter pylori» . ПЛОС Патогены . 6 (7): e1001026. дои : 10.1371/journal.ppat.1001026 . ПМЦ 2912397 . ПМИД 20686662 .
- ^ О'Рурк Э.Дж., Шевалье С., Пинто А.В., Тиберг Дж.М., Иелпи Л., Лабинь А. и др. (март 2003 г.). «ДНК патогена как мишень для окислительного стресса, вызванного хозяином: роль в восстановлении бактериальных повреждений ДНК при колонизации Helicobacter pylori» . Труды Национальной академии наук Соединенных Штатов Америки . 100 (5): 2789–94. Бибкод : 2003PNAS..100.2789O . дои : 10.1073/pnas.0337641100 . ПМК 151419 . ПМИД 12601164 .
- ^ Мишод Р.Э., Бернштейн Х., Недельку А.М. (май 2008 г.). «Адаптационное значение пола у микробных патогенов». Инфекция, генетика и эволюция . 8 (3): 267–85. Бибкод : 2008InfGE...8..267M . дои : 10.1016/j.meegid.2008.01.002 . ПМИД 18295550 .
- ^ Айлуд Ф., Дидло Х., Волтемейт С., Пфаффингер Г., Оверманн Дж., Бадер Р.К. и др. (май 2019 г.). «Эволюция Helicobacter pylori внутри хозяина формируется за счет специфической ниши адаптации, внутрижелудочной миграции и избирательного охвата» . Нат Коммун . 10 (1): 2273. Бибкод : 2019NatCo..10.2273A . дои : 10.1038/s41467-019-10050-1 . ПМК 6531487 . ПМИД 31118420 .
- ^ Лафлин М.Ф., Барнард Ф.М., Дженкинс Д., Шарплс Г.Дж., Дженкс П.Дж. (апрель 2003 г.). «Мутанты Helicobacter pylori, дефектные по резолвазе соединения Холлидея RuvC, демонстрируют снижение выживаемости макрофагов и спонтанного клиренса из слизистой оболочки желудка мышей» . Инфекция и иммунитет . 71 (4): 2022–31. дои : 10.1128/IAI.71.4.2022-2031.2003 . ПМК 152077 . ПМИД 12654822 .
- ^ Перейти обратно: а б Ван Джи, Майер Р.Дж. (январь 2008 г.). «Критическая роль RecN в рекомбинационной репарации ДНК и выживании Helicobacter pylori» . Инфекция и иммунитет . 76 (1): 153–60. дои : 10.1128/IAI.00791-07 . ПМК 2223656 . ПМИД 17954726 .
- ^ Перейти обратно: а б Бахманинежад П., Гафурян С., Махмуди М., Малеки А., Садегифард Н., Бадахш Б. (апрель 2021 г.). «Сохраняющиеся клетки как возможная причина неудачи антибиотикотерапии при Helicobacter pylori» . JGH Открыть . 5 (4): 493–497. дои : 10.1002/jgh3.12527 . ПМЦ 8035453 . ПМИД 33860100 .
- ^ Перейти обратно: а б Каммарота Дж., Сангинетти М., Галло А., Постераро Б. (август 2012 г.). «Обзорная статья: образование биопленок Helicobacter pylori как мишень для искоренения резистентной инфекции» . Алиментарная фармакология и терапия . 36 (3): 222–230. дои : 10.1111/j.1365-2036.2012.05165.x . ПМИД 22650647 . S2CID 24026187 . Проверено 3 марта 2024 г.
- ^ Перейти обратно: а б с д Шадвар Н., Акрами С., Мусави Сагарчи С.М., Аскандар Р.Х., Мерати А., Агаяри М. и др. (7 мая 2024 г.). «Обзор лечения Helicobacter pylori без антибиотиков: новое понимание» . Границы микробиологии . 15 . дои : 10.3389/fmicb.2024.1379209 . ISSN 1664-302X . ПМЦ 11106852 . ПМИД 38774508 .
- ^ Перейти обратно: а б с д и ж Crowe SE (21 марта 2019 г.). «Инфекция Хеликобактер пилори». Медицинский журнал Новой Англии . 380 (12): 1158–1165. дои : 10.1056/NEJMcp1710945 . ПМИД 30893536 . S2CID 84843669 .
- ^ Перейти обратно: а б Джамби Л.К. (7 октября 2022 г.). «Систематический обзор и метаанализ чувствительности и специфичности (13)C/(14)C-мочевинных дыхательных тестов в диагностике инфекции Helicobacter pylori» . Диагностика . 12 (10): 2428. doi : 10.3390/diagnostics12102428 . ПМК 9600925 . ПМИД 36292117 .
- ^ Логан Р.П., Уокер М.М. (октябрь 2001 г.). «Азбука верхних отделов желудочно-кишечного тракта: Эпидемиология и диагностика хеликобактерной инфекции» . БМЖ . 323 (7318): 920–2. дои : 10.1136/bmj.323.7318.920 . ПМЦ 1121445 . ПМИД 11668141 .
- ^ Решетняк В.И., Бурмистров А.И., Маев ИВ. (февраль 2021 г.). «Хеликобактер пилори: комменсал, симбионт или патоген?» . Мир Дж Гастроэнтерол . 27 (7): 545–560. дои : 10.3748/wjg.v27.i7.545 . ПМК 7901052 . ПМИД 33642828 .
- ^ Перейти обратно: а б Рахат М., Сакиб М., Ахмед М., Сулеман М., Исмаил С.М., Мумтаз Х. и др. (июнь 2023 г.). «Использование эрадикационной терапии в дополнение к пародонтальной терапии по сравнению с монотерапией для лечения инфекций Helicobacter pylori: мини-обзор» . Энн Мед Сург (Лондон) . 85 (6): 2756–2760. дои : 10.1097/MS9.0000000000000741 . ПМЦ 10289787 . ПМИД 37363585 .
- ^ Дельпорт В., ван дер Мерве С.В. (2007). «Передача Helicobacter pylori: влияние метода анализа и исследуемой популяции на выводы». Лучшие практики и исследования. Клиническая гастроэнтерология . 21 (2): 215–36. дои : 10.1016/j.bpg.2006.10.001 . hdl : 2263/4083 . ПМИД 17382274 .
- ^ Цукамото Т., Накагава М., Кирияма Ю., Тойода Т., Цао Х. (август 2017 г.). «Профилактика рака желудка: искоренение Helicobacter Pylori и не только» . Международный журнал молекулярных наук . 18 (8): 1699. doi : 10.3390/ijms18081699 . ПМК 5578089 . ПМИД 28771198 .
- ^ Ли Л, Ю С (2019). «Инфекция Helicobacter pylori после эндоскопической резекции раннего рака желудка» . БиоМед Исследования Интернэшнл . 2019 . дои : 10.1155/2019/9824964 . ПМК 6816031 . ПМИД 31737682 .
- ^ Перейти обратно: а б Талеби Безмин Абади А (март 2016 г.). «Вакцина против Helicobacter pylori: неизбежный подход» . Мир Дж Гастроэнтерол . 22 (11): 3150–7. дои : 10.3748/wjg.v22.i11.3150 . ПМЦ 4789989 . ПМИД 27003991 .
- ^ Бланшар Т.Г., Недруд Дж.Г. (2010). «9. Вакцины против Хеликобактер пилори » . В Саттон П., Митчелл Х. (ред.). Хеликобактер пилори в XXI веке . КАБИ. стр. 167–189. ISBN 978-1-84593-594-8 . Проверено 7 августа 2013 г.
- ^ де Врис Р., Клок Р.М., Брауэрс-младший, Постма М.Дж. (февраль 2009 г.). «Экономическая эффективность потенциальной будущей вакцины против Helicobacter pylori в Нидерландах: влияние изменения ставки дисконтирования на здравоохранение» . Вакцина . 27 (6): 846–52. doi : 10.1016/j.vaccine.2008.11.081 . ПМИД 19084566 . Архивировано из оригинала 10 мая 2021 года . Проверено 7 августа 2013 г.
- ^ Рупноу М.Ф., Чанг А.Х., Шахтер Р.Д., Оуэнс Д.К., Парсоннет Дж. (октябрь 2009 г.). «Экономическая эффективность потенциальной профилактической вакцины против Helicobacter pylori в США» . Журнал инфекционных болезней . 200 (8): 1311–7. дои : 10.1086/605845 . ПМИД 19751153 .
- ^ Перейти обратно: а б Саттон П., Боаг Дж. М. (ноябрь 2019 г.). «Состояние исследований и разработок вакцины против Helicobacter pylori» . Вакцина . 37 (50): 7295–7299. doi : 10.1016/j.vaccine.2018.01.001 . ПМЦ 6892279 . ПМИД 29627231 .
- ^ «PDB101: Молекула месяца: протон-управляемый канал мочевины» . RCSB: PDB-101 . Архивировано из оригинала 6 ноября 2023 года . Проверено 6 ноября 2023 г.
- ^ Перейти обратно: а б Азер С.А., Ахонди Х. (2019). "Гастрит". СтатПерлс . ПМИД 31334970 .
- ^ Перейти обратно: а б с Ширли М. (март 2024 г.). «Вонопразан: обзор инфекции Helicobacter pylori» . Наркотики . 84 (3): 319–327. дои : 10.1007/s40265-023-01991-5 . ПМК 11090951 . ПМИД 38388872 .
- ^ «Два новых режима лечения получили одобрение FDA для лечения инфекции H. Pylori» . www.medpagetoday.com . 4 мая 2022 года. Архивировано из оригинала 25 марта 2023 года . Проверено 25 марта 2023 г.
- ^ Раувс Э.А., Титгат Г.Н. (май 1990 г.). «Лечение язвенной болезни двенадцатиперстной кишки, связанное с эрадикацией Helicobacter pylori». Ланцет . 335 (8700): 1233–5. дои : 10.1016/0140-6736(90)91301-П . ПМИД 1971318 . S2CID 41888935 .
- ^ Перейти обратно: а б Беркитт, доктор медицинских наук, Дакворт, Калифорния, Уильямс, Дж. М., Притчард, Д. М. (февраль 2017 г.). «Патология желудка, вызванная Helicobacter pylori: данные моделей in vivo и ex vivo» . Модели и механизмы заболеваний . 10 (2): 89–104. дои : 10.1242/dmm.027649 . ПМК 5312008 . ПМИД 28151409 .
- ^ Чжу Л.Б., Чжан Ю.К., Хуан Х.Х., Линь Дж. (сентябрь 2021 г.). «Перспективы клинического применения бутиратпродуцирующих бактерий» . World J Clin Педиатр . 10 (5): 84–92. дои : 10.5409/wjcp.v10.i5.84 . ПМЦ 8465514 . ПМИД 34616650 .
- ^ Сарачино И.М., Павони М., Саккоманно Л., Фиорини Г., Пеши В., Фоски С. и др. (май 2020 г.). «Антимикробная эффективность пяти пробиотических штаммов против Helicobacter pylori» . Антибиотики . 9 (5): 244. doi : 10.3390/antibiotics9050244 . ПМЦ 7277513 . ПМИД 32403331 .
- ^ Сото С.М. (апрель 2013 г.). «Роль откачивающих насосов в устойчивости к антибиотикам бактерий, встроенных в биопленку» . Вирулентность . 4 (3): 223–9. дои : 10.4161/viru.23724 . ПМК 3711980 . ПМИД 23380871 .
- ^ Перейти обратно: а б Цай Ю, Ван С, Чен З, Сюй З, Ли Х, Ли В и др. (август 2020 г.). «Транспортеры HP0939, HP0497 и HP0471 участвуют в внутренней множественной лекарственной устойчивости и формировании биопленок у Helicobacter pylori путем усиления оттока лекарств» . Хеликобактер . 25 (4): e12715. дои : 10.1111/hel.12715 . PMID 32548895 . S2CID 219726485 . Архивировано из оригинала 15 февраля 2024 года . Проверено 15 февраля 2024 г.
- ^ Моммерстиг М.С., Ньювенбург С.А., Вольтерс Л.М., Руверс Б.Х., ван Вуурен Х.А., Верхаар А.П. и др. (ноябрь 2023 г.). «Использование неинвазивных тестов кала для проверки эрадикации Helicobacter pylori и устойчивости к кларитромицину» . Объединенный Европейский Гастроэнтерол Дж . 11 (9): e894-903. дои : 10.1002/ueg2.12473 . ПМЦ 10637120 . ПМИД 37854002 .
- ^ Стенстрем Б., Мендис А., Маршалл Б. (август 2008 г.). «Хеликобактер пилори – новейшие достижения в диагностике и лечении». Австралийский семейный врач . 37 (8): 608–12. ПМИД 18704207 .
- ^ Фишбах Л., Эванс Э.Л. (август 2007 г.). «Метаанализ: влияние статуса устойчивости к антибиотикам на эффективность тройной и четверной терапии первой линии Helicobacter pylori». Алиментарная фармакология и терапия (метаанализ). 26 (3): 343–57. дои : 10.1111/j.1365-2036.2007.03386.x . ПМИД 17635369 . S2CID 20973127 .
- ^ Грэм Д.Ю., Шиотани А. (июнь 2008 г.). «Новые концепции резистентности в лечении инфекций Helicobacter pylori» . Природная клиническая практика. Гастроэнтерология и гепатология . 5 (6): 321–31. дои : 10.1038/ncpgasthep1138 . ПМЦ 2841357 . ПМИД 18446147 .
- ^ Пол Д., Келлер П.М., Бордье В., Вагнер К. (август 2019 г.). «Обзор современных методов диагностики и достижений в диагностике Helicobacter pylori в эпоху секвенирования нового поколения» . Мир Дж Гастроэнтерол . 25 (32): 4629–4660. дои : 10.3748/wjg.v25.i32.4629 . ПМК 6718044 . ПМИД 31528091 .
- ^ Сукри А., Ханафия А., Патил С., Лопес Б.С. (апрель 2023 г.). «Потенциал альтернативных методов лечения и вакцин-кандидатов против Helicobacter pylori» . Фармацевтика . 16 (4): 552. дои : 10.3390/ph16040552 . ПМЦ 10141204 . ПМИД 37111309 .
- ^ Перейти обратно: а б с Вау Н., Ставропулу Э., Войдару С., Цигалу С., Безирцоглу Э. (сентябрь 2021 г.). «На пути к достижениям в области противомикробной активности лекарственных растений: обзорное исследование проблем и будущих перспектив» . Микроорганизмы . 9 (10): 2041. doi : 10.3390/microorganisms9102041 . ПМЦ 8541629 . ПМИД 34683362 .
- ^ Мун Дж.К., Ким-младший, Ан Ю.Дж., Сибамото Т. (июнь 2010 г.). «Анализ и антихеликобактерная активность сульфорафана и родственных соединений, присутствующих в ростках брокколи (Brassica oleracea L.)». Журнал сельскохозяйственной и пищевой химии . 58 (11): 6672–7. дои : 10.1021/jf1003573 . ПМИД 20459098 .
- ^ Сатианарайан С., Амманат А.В., Бисвас Р., Б.А., Сукумаран С., Венкидасами Б. (июль 2022 г.). «Новый подход к борьбе с Helicobacter pylori с использованием растений и его компонентов: обзорное исследование». Микроб Патог . 168 : 105594. doi : 10.1016/j.micpath.2022.105594 . ПМИД 35605740 . S2CID 248975163 .
- ^ Моради И., Маджиди Л., Хатери С., Аж Н., Гешлаг Р.Г., Сание Н. и др. (июль 2023 г.). «Связь между заболеваниями пародонта и Helicobacter pylori: обновленный метаанализ наблюдательных исследований» . BMC Здоровье полости рта . 23 (1): 523. doi : 10.1186/s12903-023-03232-3 . ПМЦ 10369707 . ПМИД 37496045 .
- ^ Смит Э.К., Нильссон М., Грабш Х.И., ван Грикен Н.К., Лордик Ф. (август 2020 г.). «Рак желудка». Ланцет . 396 (10251): 635–648. дои : 10.1016/S0140-6736(20)31288-5 . ПМИД 32861308 .
- ^ Бэджвелл Б., Дас П., Аджани Дж. (август 2017 г.). «Лечение локализованной аденокарциномы желудка и гастроэзофагеала: роль точного стадирования и предоперационной терапии» . Журнал гематологии и онкологии . 10 (1): 149. дои : 10.1186/s13045-017-0517-9 . ПМЦ 5558742 . ПМИД 28810883 .
- ^ Лэрд-Фик Х.С., Сайни С., Хиллард-младший (август 2016 г.). «Аденокарцинома желудка: роль Helicobacter pylori в патогенезе и профилактике». Последипломный медицинский журнал . 92 (1090): 471–7. doi : 10.1136/postgradmedj-2016-133997 . ПМИД 27222587 . S2CID 20739020 .
- ^ Брон Д., Меулеман Н. (сентябрь 2019 г.). «Лимфомы маргинальной зоны: вторые по распространенности лимфомы у пожилых пациентов». Современное мнение в онкологии . 31 (5): 386–393. doi : 10.1097/CCO.0000000000000554 . ПМИД 31246587 . S2CID 195765608 .
- ^ Кобаяши Т., Такахаши Н., Хагивара И., Тамару Дж., Каяно Х., Джин-най И. и др. (январь 2008 г.). «Успешная лучевая терапия у пациента с первичной лимфомой лимфоидной ткани, ассоциированной со слизистой оболочкой прямой кишки, без слитого гена API2-MALT1: описание случая и обзор литературы». Исследования лейкемии . 32 (1): 173–5. doi : 10.1016/j.leukres.2007.04.017 . ПМИД 17570523 .
- ^ Матысяк-Будник Т., Прядко К., Боссар С., Шапель Н., Русконе-Фурместро А. (июль 2023 г.). «Клиническое ведение пациентов с MALT-лимфомой желудка: точка зрения гастроэнтеролога» . Раки . 15 (15): 3811. doi : 10.3390/cancers15153811 . ПМЦ 10417821 . ПМИД 37568627 .
- ^ Казуло С., Фридберг Дж. (2017). «Трансформация лимфомы маргинальной зоны (и ассоциация с другими лимфомами)». Лучшие практики и исследования. Клиническая гематология . 30 (1–2): 131–138. дои : 10.1016/j.beha.2016.08.029 . ПМИД 28288708 .
- ^ Перейти обратно: а б с Куо Ш., Йе К.Х., Чен Л.Т., Линь К.В., Сюй П.Н., Сюй С. и др. (июнь 2014 г.). «Диффузная крупноклеточная В-клеточная лимфома желудка, связанная с Helicobacter pylori: отдельное заболевание с меньшей агрессивностью и более высокой химиочувствительностью» . Журнал рака крови . 4 (6): е220. дои : 10.1038/bcj.2014.40 . ПМК 4080211 . ПМИД 24949857 .
- ^ Перейти обратно: а б с Ченг Ю, Сяо Ю, Чжоу Р, Ляо Ю, Чжоу Дж, Ма Х (август 2019 г.). «Прогностическое значение инфекции Helicobacter pylori при диффузной крупноклеточной В-клеточной лимфоме желудка» . БМК Рак . 19 (1): 842. doi : 10.1186/s12885-019-6067-5 . ПМК 6712724 . PMID 31455250 .
- ^ Цай Х.Дж., Тай Дж.Дж., Чен Л.Т., Ву М.С., Йе К.Х., Лин К.В. и др. (июль 2020 г.). «Многоцентровое проспективное исследование антибиотикотерапии первой линии при лимфоме лимфоидной ткани, ассоциированной со слизистой оболочкой желудка, на ранней стадии и диффузной крупноклеточной В-клеточной лимфоме с гистологическими признаками лимфоидной ткани, ассоциированной со слизистой оболочкой» . Гематологическая . 105 (7): е349–е354. doi : 10.3324/haematol.2019.228775 . ПМЦ 7327622 . ПМИД 31727764 .
- ^ Балендра В., Аморосо С., Галасси Б., Эспосто Дж., Бареджи С., Луу Дж. и др. (август 2023 г.). «Диета с высоким содержанием соли усугубляет инфекцию H. pylori и увеличивает риск рака желудка» . Дж. Перс Мед . 13 (9): 1325. дои : 10.3390/jpm13091325 . ПМЦ 10533117 . ПМИД 37763093 .
- ^ Джароенлапноппарат А., Бхатия К., Кобан С. (июнь 2022 г.). «Воспаление и рак желудка» . Болезни . 10 (3): 35. doi : 10.3390/diseases10030035 . ПМЦ 9326573 . ПМИД 35892729 .
- ^ Пак Дж.М., Хан Ю.М., О Дж.И., Ли Д.И., Чой Ш., Хам К.Б. (сентябрь 2021 г.). «Профилирование транскриптома влияет на благотворное действие экстрактов кимчи против инфекции Helicobacter pylori» . J Clin Biochem Nutr . 69 (2): 171–187. дои : 10.3164/jcbn.20-116 . ПМЦ 8482382 . ПМИД 34616109 .
- ^ Перейти обратно: а б Браун Л.М. (2000). «Хеликобактер пилори: эпидемиология и пути передачи» . Эпидемиологические обзоры . 22 (2): 283–97. doi : 10.1093/oxfordjournals.epirev.a018040 . ПМИД 11218379 .
- ^ Пасифико Л., Осборн Дж. Ф., Бончи Э., Ромаджиоли С., Бальдини Р., Кьеза К. (январь 2014 г.). «Пробиотики для лечения хеликобактерной инфекции у детей» . Мир Дж Гастроэнтерол . 20 (3): 673–83. дои : 10.3748/wjg.v20.i3.673 . ПМЦ 3921477 . ПМИД 24574741 .
- ^ Гудман К.Дж., О'Рурк К., Дэй Р.С., Ван С., Нургалиева З., Филлипс К.В. и др. (декабрь 2005 г.). «Динамика инфекции Helicobacter pylori в когорте США и Мексики в течение первых двух лет жизни» . Международный журнал эпидемиологии . 34 (6): 1348–55. дои : 10.1093/ije/dyi152 . ПМИД 16076858 .
- ^ Ли Р, Чжан П, Ху Цзы, И Ю, Чен Л, Чжан Х (14 мая 2021 г.). «Реинфекция Helicobacter pylori и ее факторы риска после первоначальной эрадикации: протокол систематического обзора и метаанализа» . Лекарство . 100 (19): e25949. дои : 10.1097/MD.0000000000025949 . ПМК 8133036 . ПМИД 34106668 .
- ^ Перейти обратно: а б с Блазер MJ (февраль 2005 г.). «Вымирающий вид в желудке». Научный американец . 292 (2): 38–45. Бибкод : 2005SciAm.292b..38B . doi : 10.1038/scientificamerican0205-38 . ПМИД 15715390 .
- ^ Грэм Д.Ю., Ямаока Ю., Малати Х.М. (ноябрь 2007 г.). «Размышляя о будущем без Helicobacter pylori и гипотезе ужасных последствий» . Хеликобактер . 12 (Приложение 2): 64–8. дои : 10.1111/j.1523-5378.2007.00566.x . ПМК 3128250 . ПМИД 17991179 .
- ^ Делани Б., МакКолл К. (август 2005 г.). «Обзорная статья: Helicobacter pylori и гастроэзофагеальная рефлюксная болезнь». Алиментарная фармакология и терапия (обзор). 22 (Приложение 1): 32–40. дои : 10.1111/j.1365-2036.2005.02607.x . ПМИД 16042657 . S2CID 34921548 .
- ^ Блазер М.Дж., Чен Ю., Рейбман Дж. (май 2008 г.). «Защищает ли Helicobacter pylori от астмы и аллергии?» . Гут . 57 (5): 561–7. дои : 10.1136/gut.2007.133462 . ПМЦ 3888205 . ПМИД 18194986 .
- ^ Чен Ю, Blaser MJ (август 2008 г.). «Колонизация Helicobacter pylori обратно пропорциональна детской астме» . Журнал инфекционных болезней . 198 (4): 553–60. дои : 10.1086/590158 . ПМК 3902975 . ПМИД 18598192 .
- ^ Смоак Б.Л., Келли П.В., Тейлор Д.Н. (март 1994 г.). «Серораспространенность инфекций Helicobacter pylori в когорте новобранцев армии США». Американский журнал эпидемиологии . 139 (5): 513–9. doi : 10.1093/oxfordjournals.aje.a117034 . ПМИД 8154475 .
- ^ Эверхарт Дж. Э., Крузон-Моран Д., Перес-Перес Г.И., Тралка Т.С., Маккуиллан Г. (апрель 2000 г.). «Серораспространенность и этнические различия инфекции Helicobacter pylori среди взрослых в Соединенных Штатах» . Журнал инфекционных болезней . 181 (4): 1359–63. дои : 10.1086/315384 . ПМИД 10762567 .
- ^ Малаты Х.М. (2007). «Эпидемиология инфекции Helicobacter pylori». Лучшие практики и исследования. Клиническая гастроэнтерология . 21 (2): 205–14. дои : 10.1016/j.bpg.2006.10.005 . ПМИД 17382273 .
- ^ Мегра Ф. (сентябрь 2004 г.). «Устойчивость H. pylori к антибиотикам: распространенность, важность и достижения в тестировании» . Гут . 53 (9): 1374–84. дои : 10.1136/gut.2003.022111 . ПМЦ 1774187 . ПМИД 15306603 .
- ^ Корреа П., Пьясуэло М.Б. (январь 2012 г.). «Эволюционная история генома Helicobacter pylori: последствия для канцерогенеза желудка» . Кишечник и печень . 6 (1): 21–8. дои : 10.5009/gnl.2012.6.1.21 . ПМЦ 3286735 . ПМИД 22375167 .
- ^ Линц Б., Баллу Ф., Мудли И., Маника А., Лю Х., Руманьяк П. и др. (февраль 2007 г.). «Африканское происхождение тесной связи между людьми и Helicobacter pylori» . Природа . 445 (7130): 915–918. Бибкод : 2007Natur.445..915L . дои : 10.1038/nature05562 . ПМЦ 1847463 . ПМИД 17287725 .
- ^ «Нобелевская премия по физиологии и медицине 2005 г.» . Архивировано из оригинала 23 мая 2020 года . Проверено 30 августа 2018 г.
- ^ Биззеро Г (1893). «О трубчатых железах желудочно-кишечного канала и взаимоотношениях их эпителия с поверхностным эпителием слизистой оболочки» . Архив микроскопической анатомии . 42 :82-152. дои : 10.1007/BF02975307 . S2CID 85338121 . Архивировано из оригинала 2 декабря 2020 года . Проверено 29 июня 2019 г.
- ^ Контурек Дж. В. (декабрь 2003 г.). «Открытие Яворским Helicobacter pylori и ее патогенетической роли при язвенной болезни, гастрите и раке желудка» (PDF) . Журнал физиологии и фармакологии . 54 (Приложение 3): 23–41. ПМИД 15075463 . Архивировано из оригинала (PDF) 30 сентября 2004 года . Проверено 25 августа 2008 г.
- ^ Иган Б.Дж., О'Морейн, Калифорния (2007). «Исторический взгляд на хеликобактерный гастродуоденит и его осложнения». Лучшие практики и исследования. Клиническая гастроэнтерология . 21 (2): 335–46. дои : 10.1016/j.bpg.2006.12.002 . ПМИД 17382281 .
- ^ Палмер Э.Д. (август 1954 г.). «Исследование спирохет слизистой оболочки желудка человека». Гастроэнтерология . 27 (2): 218–20. дои : 10.1016/S0016-5085(19)36173-6 . ПМИД 13183283 .
- ^ Стир HW (август 1975 г.). «Ультраструктура миграции клеток через [ sic ] эпителий желудка и ее связь с бактериями» . Журнал клинической патологии . 28 (8): 639–46. дои : 10.1136/jcp.28.8.639 . ПМЦ 475793 . ПМИД 1184762 .
- ^ Маршалл Б.Дж., Уоррен-младший (июнь 1984 г.). «Неопознанные изогнутые палочки в желудке больных гастритом и язвенной болезнью». Ланцет . 1 (8390): 1311–5. дои : 10.1016/S0140-6736(84)91816-6 . ПМИД 6145023 . S2CID 10066001 .
- ^ Этвуд К.И. (2004). «Бактерии, язвы и остракизм? H. pylori и создание мифа» . Архивировано из оригинала 5 ноября 2009 года . Проверено 2 августа 2008 г.
- ^ Helicobacter pylori при язвенной болезни (отчет). Заявление о консенсусе НИЗ в Интернете. Том. 12. 7–9 января 1994 г., стр. 1–23. Архивировано из оригинала 19 августа 2011 года . Проверено 21 декабря 2004 г.
- ^ Перейти обратно: а б Лидделл Х.Г. , Скотт Р. (1966). Лексикон: сокращение из греко-английского лексикона Лидделла и Скотта . Оксфорд, Великобритания: Издательство Оксфордского университета. ISBN 978-0-19-910207-5 .
- ^ Маршалл Б.С., Гудвин К.С. (1987). «Пересмотренная номенклатура Campylobacter pyloridis » . Международный журнал систематической бактериологии . 37 (1): 68. doi : 10.1099/00207713-37-1-68 .
- ^ Гудвин К.С., Армстронг Дж.А., Чилверс Т., Питерс М., Коллинз М.Д., Слай Л. и др. (1989). «Перенос Campylobacter pylori и Campylobacter mustelae в Helicobacter gen. nov. как Helicobacter pylori com. nov. и Helicobacter mustelae com. nov. соответственно» . Международный журнал систематической бактериологии . 39 (4): 397–405. дои : 10.1099/00207713-39-4-397 .
- ^ Бакли М.Дж., О'Морейн, Калифорния (1998). «Биология хеликобактера – открытие» . Британский медицинский бюллетень . 54 (1): 7–16. doi : 10.1093/oxfordjournals.bmb.a011681 . ПМИД 9604426 .
- ^ Меграуд Ф. и др. (Европейская группа по изучению хеликобактера) (ноябрь 2007 г.). «Эволюция исследований Helicobacter pylori, наблюдаемая на семинарах Европейской исследовательской группы Helicobacter». Хеликобактер . 12 Приложение 2 (Приложение 2): 1–5. дои : 10.1111/j.1523-5378.2007.00581.x . ПМИД 17991169 . S2CID 45841196 .
- ^ «ЭХМСГ» . Эхмсг2019 . Архивировано из оригинала 11 января 2024 года . Проверено 11 января 2024 г.
- ^ Малфертайнер П., Меград Ф., О'Морейн К.А., Атертон Дж., Аксон А.Т., Базцоли Ф. и др. (Европейская группа по изучению Helicobacter) (май 2012 г.). «Лечение инфекции Helicobacter pylori – Маастрихтский IV/Флорентийский консенсусный отчет» . Гут . 61 (5): 646–64. дои : 10.1136/gutjnl-2012-302084 . hdl : 1765/64813 . ПМИД 22491499 . S2CID 1401974 . Архивировано из оригинала 4 июля 2021 года . Проверено 7 декабря 2012 г.
- ^ Малфертайнер П., Меграуд Ф., О'Морейн С., Базцоли Ф., Эль-Омар Э., Грэм Д. и др. (июнь 2007 г.). «Современные концепции лечения инфекции Helicobacter pylori: Маастрихтский консенсусный отчет III» . кишка 56 (6): 772–81. дои : 10.1136/gut.2006.101634 . ЧВК 1954853 . ПМИД 17170018 .
- ^ Малфертайнер П., Меград Ф., О'Морейн С., Хунгин А.П., Джонс Р., Аксон А. и др. (Европейская группа по изучению Helicobacter Pylori (EHPSG)) (февраль 2002 г.). «Современные концепции лечения инфекции Helicobacter pylori - Маастрихтский консенсусный отчет 2-2000 г.». Алиментарная фармакология и терапия . 16 (2): 167–80. дои : 10.1046/j.1365-2036.2002.01169.x . ПМИД 11860399 . S2CID 6166458 .
- ^ Малфертайнер П., Меград Ф., О'Морейн С., Белл Д., Бьянки Порро Г., Дельтенр М. и др. (Европейская группа по изучению Helicobacter Pylori (EHPSG)) (январь 1997 г.). «Современные европейские концепции борьбы с инфекцией Helicobacter pylori - Маастрихтский консенсусный отчет. Европейская группа по изучению Helicobacter Pylori (EHPSG)». Европейский журнал гастроэнтерологии и гепатологии . 9 (1): 1–2. дои : 10.1097/00042737-199701000-00002 . ПМИД 9031888 . S2CID 36930542 .
- ^ МакНичолл А.Г., Гасбаррини А., Тепеш Б. и др. (сентябрь 2014 г.). «Общеевропейский реестр по лечению H. pylori (Hp-EuReg): промежуточный анализ 5792 пациентов». Хеликобактер . 2014 : 69.
- ^ «Лечение инфекции Helicobacter pylori » . Онлайн курсы. Объединенная Европейская Гастроэнтерология . Архивировано из оригинала 2 апреля 2015 года.
- ^ «Годовой отчет 2012» . Объединенная Европейская Гастроэнтерология . Архивировано из оригинала 4 июня 2016 года . Проверено 25 февраля 2015 г.
- ^ Юнг С.В., Ли С.В. (январь 2016 г.). «Антибактериальное действие жирных кислот на инфекцию Helicobacter pylori» . Корейский журнал внутренней медицины (обзор). 31 (1): 30–5. дои : 10.3904/kjim.2016.31.1.30 . ПМЦ 4712431 . ПМИД 26767854 .
Внешние ссылки
[ редактировать ]- «Информация о тестах на H. pylori » . Национальные институты здравоохранения . Министерство здравоохранения и социальных служб США. Архивировано из оригинала 13 июня 2013 года.
- «Европейская группа по изучению хеликобактера (EHSG)» .
- «Типовой штамм Helicobacter pylori в Bac Dive » . База метаданных по бактериальному разнообразию .
- «Хеликобактер пилори» . Геном . КЕГГ. Япония. 26695.