Циклический гуанозинмонофосфат
 | |
 | |
| Имена | |
|---|---|
| Название ИЮПАК Гуанозин 3',5'-(фосфат водорода) | |
| Систематическое название ИЮПАК 2-Амино-9-[(4a R ,6 R ,7 R ,7a S )-2,7-дигидрокси-2-оксотетрагидро-2 H ,4 H -2λ 5 -фуро[3,2- d ][1,3,2]диоксафосфол-6-ил]-3,9-дигидро- 6H -пурин-6-он | |
| Другие имена цГМФ; 3',5'-циклический ГМП; 3':5'-циклический ГМП; Гуанозинциклический монофосфат; Циклический 3',5'-ГМП; Гуанозин-3',5'-циклический фосфат | |
| Идентификаторы | |
3D model ( JSmol ) | |
| ЧЭБИ | |
| ЧЕМБЛ | |
| ХимическийПаук | |
| Информационная карта ECHA | 100.028.765 |
| МеШ | Циклический+GMP |
ПабХим CID | |
| НЕКОТОРЫЙ | |
Панель управления CompTox ( EPA ) | |
| Характеристики | |
| С 10 Ч 12 Н 5 О 7 П | |
| Молярная масса | 345.208 g·mol −1 |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
Циклический гуанозинмонофосфат ( цГМФ ) представляет собой циклический нуклеотид, полученный из гуанозинтрифосфата (ГТФ). цГМФ действует как второй мессенджер , подобно циклическому АМФ . действия является активация внутриклеточных протеинкиназ в ответ на связывание мембранонепроницаемых Наиболее вероятным механизмом его пептидных гормонов с внешней поверхностью клетки. [1] Благодаря активации протеинкиназ цГМФ может расслаблять гладкие мышцы. [2] Концентрацию цГМФ в моче можно измерить для определения функции почек и выявления диабета. [3]
Синтез
[ редактировать ]Гуанилатциклаза (ГЦ) катализирует синтез цГМФ. Этот фермент превращает ГТФ в цГМФ. Пептидные гормоны, такие как предсердный натрийуретический фактор, активируют мембраносвязанные GC, тогда как растворимые GC (sGC) обычно активируются оксидом азота для стимуляции синтеза цГМФ. sGC можно ингибировать ODQ (1H-[1,2,4]оксадиазоло[4,3-a]хиноксалин-1-он). [4]
Функции
[ редактировать ]цГМФ является распространенным регулятором ионных каналов проводимости , гликогенолиза и клеточного апоптоза . Он также расслабляет гладкие мышечные ткани. В кровеносных сосудах расслабление гладких мышц сосудов приводит к расширению сосудов и усилению кровотока . В пресинаптических окончаниях полосатого тела цГМФ контролирует эффективность высвобождения нейромедиатора . [5]
цГМФ является вторичным посредником при фототрансдукции в глазу. В фоторецепторах глаз млекопитающих свет активирует фосфодиэстеразу , которая разрушает цГМФ. Каналы ионов натрия в фоторецепторах контролируются цГМФ, поэтому деградация цГМФ вызывает закрытие натриевых каналов, что приводит к гиперполяризации плазматической мембраны фоторецептора и, в конечном итоге, к отправке визуальной информации в мозг. [6]
Также показано, что цГМФ опосредует включение притяжения апикальных дендритов пирамидных клеток к V кортикального слоя семафорину -3А (Sema3a). [7] В то время как аксоны пирамидных клеток отталкиваются Sema3a, апикальные дендриты притягиваются к нему. Привлечение опосредовано повышенным уровнем растворимой гуанилатциклазы (SGC), присутствующей в апикальных дендритах. SGC генерирует цГМФ, что приводит к последовательности химических активаций, которые приводят к привлечению Sema3a. Отсутствие SGC в аксоне вызывает отталкивание от Sema3a. Эта стратегия обеспечивает структурную поляризацию пирамидных нейронов и имеет место в эмбриональном развитии.
цГМФ, как и цАМФ, синтезируется, когда обонятельные рецепторы получают запах. цГМФ вырабатывается медленно и имеет более продолжительный срок действия, чем цАМФ, что приводит к его участию в долгосрочных клеточных реакциях на стимуляцию запахами, таких как долговременное потенцирование . цГМФ в обонятельной системе синтезируется как мембранной гуанилилциклазой (мГЦ), так и растворимой гуанилилциклазой (рГЦ). Исследования показали, что синтез цГМФ в обонятельной системе происходит за счет активации рГЦ оксидом азота, нейромедиатором. цГМФ также требует повышения внутриклеточных уровней цАМФ, и связь между двумя вторичными мессенджерами, по-видимому, обусловлена повышением внутриклеточных уровней кальция. [8]
Деградация
[ редактировать ]Многочисленные циклические нуклеотидфосфодиэстеразы (ФДЭ) могут разрушать цГМФ путем гидролиза цГМФ до 5'-ГМФ. ФДЭ 5, -6 и -9 специфичны для цГМФ, тогда как ФДЭ1, -2, -3, -10 и -11 могут гидролизовать как цАМФ, так и цГМФ.
Ингибиторы фосфодиэстеразы предотвращают деградацию цГМФ, тем самым усиливая и/или продлевая его действие. Например, силденафил (виагра) и подобные препараты усиливают сосудорасширяющее действие цГМФ в пещеристых телах путем ингибирования ФДЭ 5 (или ФДЭ V). Используется для лечения эректильной дисфункции . Однако препарат может ингибировать ФДЭ6 в сетчатке (хотя и с меньшим сродством, чем ФДЭ5). Было показано, что это приводит к потере зрительной чувствительности, но вряд ли повлияет на выполнение обычных зрительных задач, за исключением условий ограниченной видимости, когда объекты уже находятся вблизи зрительного порога. [9] Этого эффекта в значительной степени удается избежать при использовании других ингибиторов ФДЭ5, таких как тадалафил . [10]
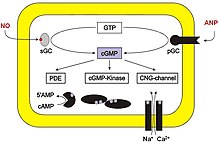
Активация протеинкиназы
[ редактировать ]цГМФ участвует в регуляции некоторых протеинзависимых киназ. Например, ПКГ ( протеинкиназа G ) представляет собой димер, состоящий из одной каталитической и одной регуляторной единицы, причем регуляторные единицы блокируют активные центры каталитических единиц.
цГМФ связывается с участками регуляторных единиц PKG и активирует каталитические единицы, позволяя им фосфорилировать свои субстраты. В отличие от активации некоторых других протеинкиназ, особенно PKA, PKG активируется, но каталитические и регуляторные единицы не диссоциируют.
См. также
[ редактировать ]- Циклический аденозинмонофосфат (цАМФ)
- 8-Бромгуанозин-3',5'-циклический монофосфат (8-Br-цГМФ)
Ссылки
[ редактировать ]- ^ Фрэнсис С.Х., Корбин Дж.Д. (август 1999 г.). «Циклические нуклеотид-зависимые протеинкиназы: внутриклеточные рецепторы действия цАМФ и цГМФ». Критические обзоры клинических лабораторных наук . 36 (4): 275–328. дои : 10.1080/10408369991239213 . ПМИД 10486703 .
- ^ Карвахал Х.А., Жермен А.М., Уидобро-Торо Дж.П., Вайнер К.П. (сентябрь 2000 г.). «Молекулярный механизм релаксации гладких мышц, опосредованной цГМФ» . Журнал клеточной физиологии . 184 (3): 409–420. doi : 10.1002/1097-4652(200009)184:3<409::aid-jcp16>3.0.co;2-k . ПМИД 10911373 . S2CID 22530053 .
- ^ Чайковская Л., Хойниш Ф., фон Эйнем Г., Хохер К.Ф., Цуприков О., Павкович М. и др. (12 апреля 2018 г.). Симосава Т. (ред.). «Мочевой цГМФ предсказывает серьезные неблагоприятные почечные явления у пациентов с легкой почечной недостаточностью и/или сахарным диабетом до воздействия контрастного вещества» . ПЛОС ОДИН . 13 (4): e0195828. Бибкод : 2018PLoSO..1395828C . дои : 10.1371/journal.pone.0195828 . ПМК 5896998 . ПМИД 29649334 .
- ^ Гартуэйт Дж., Саутэм Э., Бултон К.Л., Нильсен Э.Б., Шмидт К., Майер Б. (август 1995 г.). «Мощное и селективное ингибирование чувствительной к оксиду азота гуанилилциклазы 1H-[1,2,4]оксадиазоло[4,3-а]хиноксалин-1-оном» . Молекулярная фармакология . 48 (2): 184–188. ПМИД 7544433 .
- ^ Фиблингер Т., Перес-Альварес А., Ламот-Молина П.Дж., Джи К.Э., Ортнер Т.Г. (август 2022 г.). «Пресинаптический цГМФ устанавливает синаптическую силу в полосатом теле и важен для двигательного обучения» . Отчеты ЭМБО . 23 (8): e54361. дои : 10.15252/эмбр.202154361 . ПМЦ 9346481 . ПМИД 35735260 .
- ^ Браун Р.Л., Штрасмайер Т., Брейди Дж.Д., Карпен Дж.В. (2006). «Фармакология циклических нуклеотидных каналов: выход из тьмы» . Текущий фармацевтический дизайн . 12 (28): 3597–3613. дои : 10.2174/138161206778522100 . ПМЦ 2467446 . ПМИД 17073662 . НИХМСИД: NIHMS47625.
- ^ Полле Ф., Морроу Т., Гош А. (апрель 2000 г.). «Семафорин 3А является хемоаттрактантом кортикальных апикальных дендритов». Природа . 404 (6778): 567–573. Бибкод : 2000Natur.404..567P . дои : 10.1038/35007001 . ПМИД 10766232 . S2CID 4365085 .
- ^ Пьетробон М., Зампаро И., Маритан М., Франки С.А., Поццан Т., Лодовичи С. (июнь 2011 г.). «Взаимодействие цГМФ, цАМФ и Ca2+ в живых обонятельных сенсорных нейронах in vitro и in vivo» . Журнал неврологии . 31 (23): 8395–8405. doi : 10.1523/JNEUROSCI.6722-10.2011 . ПМЦ 6623327 . ПМИД 21653844 .
- ^ Стокман А., Шарп Л.Т., Туфаил А., Келл П.Д., Рипамонти С., Джеффри Дж. (июнь 2007 г.). «Влияние цитрата силденафила (Виагры) на зрительную чувствительность» . Журнал видения . 7 (8): 4. дои : 10.1167/7.8.4 . ПМИД 17685811 .
- ^ Дауган А., Гронден П., Руо С., Ле Монье де Гувиль АС, Косте Х., Линже Ж.М. и др. (октябрь 2003 г.). «Открытие тадалафила: нового и высокоселективного ингибитора ФДЭ5. 2:2,3,6,7,12,12a-гексагидропиразино[1',2':1,6]пиридо[3,4-b]индол- 1,4-дионовые аналоги». Журнал медицинской химии . 46 (21): 4533–4542. дои : 10.1021/jm0300577 . ПМИД 14521415 .