Химия
| Часть серии на |
| Химия |
|---|
 |
Химия - это научное исследование свойств и поведения материи . [ 1 ] Это физическая наука в естественных науках , которая изучает химические элементы , которые составляют материю и соединения, изготовленные из атомов , молекул и ионов : их состав, структура, свойства, поведение и изменения, которые они подвергают реакциям с другими веществами . [ 2 ] [ 3 ] [ 4 ] [ 5 ] Химия также рассматривает природу химических связей в химических соединениях .
В сфере его предмета химия занимает промежуточную позицию между физикой и биологией . [ 6 ] Иногда его называют центральной наукой , потому что она обеспечивает основу для понимания как основных , так и прикладных научных дисциплин на фундаментальном уровне. [ 7 ] Например, химия объясняет аспекты роста растений ( ботаника ), образование магматических пород ( геология ), как образуется атмосферный озон и как загрязняющие экологические вещества деградируются ( экология ), свойства почвы на луне ( космохимия ), как Лекарства работают ( фармакология ), и как собирать доказательства ДНК на месте преступления ( судебная экспертиза ).
Химия существовала под различными именами с древних времен. [ 8 ] Он развивался, и в настоящее время химия охватывает различные области специализации или субдисциплинар, которые продолжают увеличиваться в количестве и взаимосвязи для создания дополнительных междисциплинарных областей исследования. Применение различных областей химии часто используется для экономических целей в химической промышленности .
Этимология
Слово химия происходит из -за модификации во время эпохи Возрождения слова Алхимия , которая относилась к более раннему набору практик, которые охватывали элементы химии, металлургии , философии , астрологии , астрономии , мистики и медицины . Алхимия часто ассоциируется с стремлением превратить лидерство или другие базовые металлы в золото, хотя алхимики также интересовались многими вопросами современной химии. [ 9 ] [ 10 ]
Современная алхимия слова , в свою очередь, происходит от арабского слова аль-кимиа ( الكیمیاء ). Это может иметь египетское происхождение, так как аль-Кимиа происходит от древнегреческого χημία , которое, в свою очередь, происходит от слова Kemet , которое является древним именем Египта на египетском языке. [ 11 ] Альтернативно, аль-кими может получить из химии «разбросана». [ 12 ]
Современные принципы

Текущая модель атомной структуры является квантовой механической моделью . [ 13 ] Традиционная химия начинается с изучения элементарных частиц , атомов , молекул , [ 14 ] вещества , металлы , кристаллы и другие агрегаты материи . Вещество может быть изучено в твердых, жидких, газовых и плазменных состояниях , в изоляции или в комбинации. Взаимодействия, реакции и преобразования, которые изучаются в химии, обычно являются результатом взаимодействия между атомами, что приводит к перестройке химических связей , которые содержит атомы вместе. Такое поведение изучается в химической лаборатории .
Химическая лабораторная лаборатория стереотипно использует различные формы лабораторной стеклянной посуды . Однако стеклянная посуда не является центральной для химии, и без нее выполняется большая экспериментальная (а также прикладная/промышленная) химия.

- Химическая реакция это трансформация некоторых веществ в одно или несколько разных веществ. [ 15 ] Основой такого химического преобразования является перестройка электронов в химических связях между атомами. Это может быть символически изображена с помощью химического уравнения , которое обычно включает атомы в качестве субъектов. Количество атомов слева и справа в уравнении для химического преобразования равны. (Когда количество атомов с обеих сторон неравное, трансформация называется ядерной реакцией или радиоактивным распадом .) Тип химических реакций, которые может подвергнуться веществу, и изменения энергии, которые могут сопровождать его, ограничены определенными основными правилами. известные как химические законы .
Соображения энергии и энтропии неизменно важны практически во всех химических исследованиях. Химические вещества классифицируются с точки зрения их структуры , фазы, а также их химических композиций . Они могут быть проанализированы с использованием инструментов химического анализа , например, спектроскопии и хроматографии . Ученые, занимающиеся химическими исследованиями, известны как химики . [ 16 ] Большинство химиков специализируются на одном или нескольких субдисциплинах. Несколько концепций необходимы для изучения химии; Некоторые из них: [ 17 ]
Иметь значение
В химии материя определяется как все, что имеет массу и объем отдыха (он занимает место) и состоит из частиц . Частицы, которые составляют материю, также имеют массу отдыха - не все частицы имеют массу отдыха, такие как фотон . Вещество может быть чистым химическим веществом или смесью веществ. [ 18 ]
Атом

Атом . является основной единицей химии Он состоит из плотного ядра, называемого атомным ядром, окруженным пространством, занятым электронным облаком . Ядро состоит из положительно заряженных протонов и незаряженных нейтронов (вместе называемых нуклеонов ), в то время как электронное облако состоит из отрицательно заряженных электронов , которые вращаются в ядре. В нейтральном атоме отрицательно заряженный электроны уравновесите положительный заряд протонов. Ядро плотно; Масса нуклеона примерно в 1836 раз больше, чем у электрона, но радиус атома примерно в 10 000 раз больше, чем у его ядра. [ 19 ] [ 20 ]
Атом также является наименьшей сущностью, которую можно предположить, чтобы сохранить химические свойства элемента, такие как электроотрицательность , потенциал ионизации , предпочтительное состояние (ы), координационное число и предпочтительные типы связей (например, металлический , ионный , ковалент ).
Элемент

которое состоит из одного типа атома, характеризующегося его конкретным количеством протонов в ядрах его атомов, известных как атомное число и представленное символом Z. Химический элемент - это чистое вещество , Массовое число - это сумма количества протонов и нейтронов в ядре. Хотя все ядра всех атомов, принадлежащих к одному элементу, будут иметь одинаковое атомное число, они не обязательно имеют одинаковое массовое число; Атомы элемента, которые имеют разные массовые числа, известны как изотопы . Например, все атомы с 6 протонами в их ядрах являются атомами углерода химического элемента , но атомы углерода могут иметь массовое количество 12 или 13. [ 20 ]
Стандартное представление химических элементов заключается в периодической таблице , которая заказывает элементы по атомному числу. Периодическая таблица расположена в группах или столбцах, а также периодах , или рядах. Периодическая таблица полезна при определении периодических тенденций . [ 21 ]
Сложный
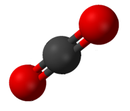
Соединение . - это чисто химическое вещество, состоящее из более чем одного элемента Свойства соединения мало сходства с свойствами его элементов. [ 22 ] Стандартная номенклатура соединений устанавливается Международным союзом чистой и прикладной химии (IUPAC). Органические соединения названы в соответствии с органической номенклатурной системой. [ 23 ] Названия неорганических соединений создаются в соответствии с неорганической номенклатурной системой. Когда соединение имеет более одного компонента, они разделены на два класса: электропозитивные и электроотрицательные компоненты. [ 24 ] Кроме того, служба химических тезисов разработала метод индекса химических веществ. В этой схеме каждое химическое вещество идентифицируется по номеру, известному как номер его реестра CAS .
Молекула

Молекула , которая обладает своим уникальным набором химических свойств, то - это наименьшая неделимая часть чистого химического вещества есть его потенциал для проведения определенного набора химических реакций с другими веществами. Тем не менее, это определение хорошо работает только для веществ, которые состоят из молекул, что не относится к многим веществам (см. Ниже). Молекулы, как правило, представляют собой набор атомов, связанных с ковалентными связями , так что структура является электрически нейтральной, и все валентные электроны соединены с другими электронами в связи или в одиноких парах .
Таким образом, молекулы существуют в виде электрически нейтральных единиц, в отличие от ионов. Когда это правило нарушено, придавая «молекуле» заряд, результат иногда называется молекулярным ионом или полиатомным ионом. Тем не менее, дискретная и отдельная природа молекулярной концепции обычно требует, чтобы молекулярные ионы присутствовали только в хорошо разделенной форме, такой как направленный луч в вакууме в масс-спектрометре . Заряженные полиатомические коллекции, находящиеся в твердых веществах (например, общие сульфат или нитратные ионы), как правило, не считаются «молекулами» в химии. Некоторые молекулы содержат один или несколько непарных электронов, создавая радикалы . Большинство радикалов сравнительно реактивны, но некоторые, такие как оксид азота (NO), могут быть стабильными.
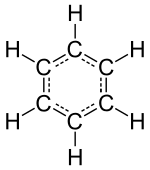
Элементы «инертный» или благородный газ ( гелий , неоновый , аргон , криптон , ксенон и радон ) состоят из одиноких атомов в качестве их наименьшей дискретной единицы, но другие изолированные химические элементы состоят из молекул или сетей атомов, связанных друг с другом, связаны друг с другом каким -то образом. Идентифицируемые молекулы составляют знакомые вещества, такие как вода, воздух и многие органические соединения, такие как алкоголь, сахар, бензин и различные фармацевтические препараты .
Однако не все вещества или химические соединения состоят из дискретных молекул, и, действительно, большинство твердых веществ, которые составляют твердую кору, мантию и ядро Земли, являются химическими соединениями без молекул. Эти другие типы веществ, такие как ионные соединения и сетевые твердые вещества , организованы таким образом, чтобы отсутствовать существование идентифицируемых молекул как таковых . Вместо этого эти вещества обсуждаются с точки зрения единиц формул или единичных ячеек в качестве наименьшей повторной структуры внутри вещества. Примерами таких веществ являются минеральные соли (такие как столовая соль ), твердые вещества, такие как углерод и алмаз, металлы, а также знакомые кремния и минералы силиката , такие как кварц и гранит.
Одной из основных характеристик молекулы является ее геометрия, которую часто называют ее структурой . В то время как структура диатомных, триатомных или тетратомических молекул может быть тривиальной (линейной, угловой пирамидальной и т. Д.) Полем
Вещество и смесь
  | |
  | |
  | |
| Примеры чистых химических веществ. Слева направо: элементы олова (SN) и сера (S), алмаз ( аллотроп углерода соединениями ), саза (чистый сахар) и хлорид натрия (соль) и бикарбонат натрия (пищевая сода), которые являются ионными Полем |
Химическое вещество - это своего рода материя с определенной композицией и набором свойств . [ 25 ] Коллекция веществ называется смесью. Примерами смесей являются воздух и сплавы . [ 26 ]
Родинка и количество вещества
Моль является единой измерением, которая обозначает количество вещества (также называемого химическим количеством). Один моль определяется, чтобы содержать ровно 6,022 140 76 × 10 23 Частицы ( атомы , молекулы , ионы или электроны ), где количество частиц на моль известно как постоянная авогадро . [ 27 ] Молярная концентрация - это количество конкретного вещества на объем раствора и обычно сообщается в моль/ дм 3 . [ 28 ]
Фаза
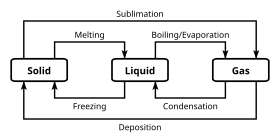
В дополнение к конкретным химическим свойствам, которые различают различные химические классификации, химические вещества могут существовать в нескольких фазах. По большей части химические классификации не зависят от этих массовых фазовых классификаций; Однако некоторые более экзотические фазы несовместимы с определенными химическими свойствами. Фаза представляет собой набор состояний химической системы, которая обладает сходными объемными структурными свойствами, в диапазоне условий, таких как давление или температура .
Физические свойства, такие как плотность и показатель преломления, имеют тенденцию попадать в значения, характерные для фазы. Фаза вещества определяется фазовым переходом , который, когда энергия, вкладываемая в систему или извлеченную из системы, переходит в перестройку структуры системы, а не изменяет объемные условия.
Иногда различие между фазами может быть непрерывным, а не иметь дискретной границы »в данном случае этот вопрос считается в суперкритическом состоянии. Когда три штата встречаются на основе условий, он известен как тройная точка , и, поскольку это инвариантно, это удобный способ определить набор условий.
Наиболее знакомыми примерами фаз являются твердые вещества , жидкости и газы . Многие вещества демонстрируют несколько твердых фаз. Например, существует три фазы твердого железа (альфа, гамма и дельта), которые варьируются в зависимости от температуры и давления. Основное различие между твердыми фазами - кристаллическая структура или расположение атомов. Другой фазой, обычно встречающейся при изучении химии, - это водная фаза, которая представляет собой состояние веществ, растворенных в водном растворе (то есть в воде).
Менее знакомые фазы включают в себя плазму , конденсаты Бозе -Эйнштейна и фермионные конденсаты , а также парамагнитные и ферромагнитные фазы магнитных материалов. В то время как большинство знакомых фаз связаны с трехмерными системами, также можно определить аналоги в двумерных системах, которые привлекли внимание к его актуальности для систем в области биологии .
Связывание
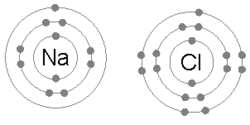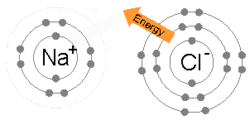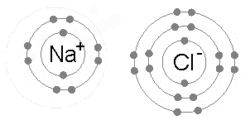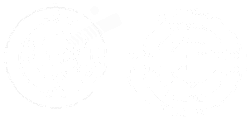
Говорят, что атомы, прикрепленные к молекулам или кристаллам, связаны друг с другом. Химическая связь может быть визуализирована в виде мультипольного баланса между положительными зарядами в ядрах и отрицательными зарядами, колеблющимися вокруг них. [ 29 ] Больше, чем простое притяжение и отталкивание, энергии и распределения характеризуют доступность электрона с связью с другим атомом.
Химическая связь может быть ковалентной связью , ионной связью , водородной связью или только из -за силы Ван -дер -Ваальса . Каждый из этих видов связей приписывается некоторому потенциалу. Эти потенциалы создают взаимодействия, которые содержит атомы в молекулах или кристаллах . Во многих простых соединениях, теории валентных связей , модели отталкивания электронов валентной оболочки ( VSEPR ) и концепции числа окисления можно использовать для объяснения молекулярной структуры и состава.
Ионная связь образуется, когда металл теряет один или несколько своих электронов, становясь положительно заряженным катионом, а затем электроны получают неметал-атом, становясь отрицательно заряженным анионом. Два противоположных заряженных иона привлекают друг друга, и ионная связь является электростатической силой притяжения между ними. Например, натрий (NA), металл, теряет один электрон, чтобы стать NA + катион в то время как хлор (CL), неметальный, получает этот электрон, чтобы стать CL − Полем Ионы удерживаются вместе из -за электростатического притяжения, и составной хлорид натрия образуется (NaCl), или общая табличная соль.

В ковалентной связи одна или несколько пар валентных электронов разделяется двумя атомами: полученная электрически нейтральная группа связанных атомов называется молекулой . Атомы будут делиться валентными электронами таким образом, чтобы создать конфигурацию благородного газа (восемь электронов в их самой внешней оболочке) для каждого атома. Говорят, что атомы, которые имеют тенденцию объединяться таким образом, что у каждого из них восемь электронов в их валентной оболочке следуют правилу октета . Тем не менее, некоторые элементы, такие как водород и литий, нуждаются только в двух электронах во внешней оболочке, чтобы достичь этой стабильной конфигурации; Говорят, что эти атомы следуют правилу дуэта , и таким образом они достигают конфигурации электронов благородного газового гелия , который имеет два электрона во внешней оболочке.
Точно так же теории классической физики могут быть использованы для прогнозирования многих ионных структур. С помощью более сложных соединений, таких как комплексы металлов , теория валентных связей является менее применимым, а альтернативные подходы, такие как теория молекулярной орбитали , обычно используются. Смотрите диаграмму на электронных орбиталях.
Энергия
В контексте химии энергия является атрибутом вещества в результате его атомной , молекулярной или агрегатной структуры . Поскольку химическая трансформация сопровождается изменением одного или нескольких таких структур, она неизменно сопровождается увеличением уменьшением энергии вовлеченных веществ или . Некоторая энергия передается между окружением и реагентами реакции в виде тепла или света ; Таким образом, продукты реакции могут иметь более или меньшую энергию, чем реагенты.
Говорят, что реакция является экспертикой , если окончательное состояние ниже по шкале энергии, чем начальное состояние; В случае эндергонических реакций ситуация наоборот. Говорят, что реакция является экзотермической , если реакция высвобождает тепло до окружающей среды; В случае эндотермических реакций реакция поглощает тепло из окружающей среды.
Химические реакции неизменно невозможны, если только реагенты преодолевают энергетический барьер, известный как энергия активации . Скорость химической реакции (при заданной температуре T) связана с энергией активации E, с помощью популяционного фактора Больцмана - Это вероятность того, что молекула иметь энергию, превышающую или равную E при данной температуре T. Эта экспоненциальная зависимость скорости реакции от температуры известна как уравнение Аррениуса . Энергия активации, необходимая для возникновения химической реакции, может быть в форме тепла, света, электричества или механической силы в форме ультразвука . [ 30 ]
Связанная концепция свободная энергия , которая также включает в себя соображения энтропии, является очень полезным средством для прогнозирования осуществимости реакции и определения состояния равновесия химической реакции в химической термодинамике . Реакция осуществляется только в том случае, если общее изменение свободной энергии Гиббса является отрицательным, ; Если он равен нулю, химическая реакция, как говорят, находится в равновесии .
Существуют только ограниченные возможные состояния энергии для электронов, атомов и молекул. Они определяются правилами квантовой механики , которые требуют квантования энергии связанной системы. Говорят, что атомы/молекулы в более высоком энергетическом состоянии возбуждены. Молекулы/атомы вещества в возбужденном энергетическом состоянии часто гораздо более реактивны; То есть больше поддается химическим реакциям.
Фаза вещества неизменно определяется его энергией и энергией его окружения. Когда межмолекулярные силы вещества таковы, что энергии окружающей среды недостаточно для их преодоления, это происходит в более упорядоченной фазе, такой как жидкость или твердое вещество, как в случае с водой (H 2 O); жидкость при комнатной температуре, потому что ее молекулы связаны водородными связями . [ 31 ] Принимая во внимание, что сероводород (H 2 S) представляет собой газ при комнатной температуре и стандартном давлении, поскольку его молекулы связаны более слабыми диполь -дипольными взаимодействиями .
Передача энергии из одного химического вещества в другое зависит от размера энергии, излучаемой из одного вещества. Тем не менее, тепловая энергия часто легче переносится практически от любого вещества в другое, потому что фононы, ответственные за вибрационную и вращательную энергию в веществе, имеют гораздо меньшую энергию, чем фотоны, вызываемые для электронного переноса энергии. Таким образом, поскольку уровни колебательной и вращательной энергии находятся более близко, чем электронные уровни энергии, тепло легче переносится между веществами относительно света или других форм электронной энергии. Например, ультрафиолетовое электромагнитное излучение не переносится с такой же эффективностью от одного вещества в другое, как термическая или электрическая энергия.
Существование характерных уровней энергии для различных химических веществ полезно для их идентификации путем анализа спектральных линий . Различные виды спектров часто используются при химической спектроскопии , например, IR , микроволновой печи , ЯМР , СПР и т. Д. Спектроскопия также используется для идентификации композиции удаленных объектов - таких как звезды и отдаленные галактики - путем анализа их спектра излучения.

Термин химическая энергия часто используется для обозначения потенциала химического вещества для преобразования с помощью химической реакции или для трансформации других химических веществ.
Реакция

Когда химическое вещество трансформируется в результате его взаимодействия с другим веществом или с энергией, говорят, что химическая реакция произошла. - Следовательно, химическая реакция это концепция, связанная с «реакцией» вещества, когда она входит в тесный контакт с другим, будь то в виде смесью или раствора ; воздействие на некоторую форму энергии или обоих. Это приводит к некоторому энергетическому обмену между составляющими реакции, а также с системной средой, которая может быть разработана сосудами - часто лабораторная стеклянная посуда .
Химические реакции могут привести к образованию или диссоциации молекул, то есть молекулы разбиваются, образуя две или более молекулы или перестройку атомов внутри или по молекулам. Химические реакции обычно включают изготовление или разрушение химических связей. Окисление, восстановление , диссоциация , кислотная нейтрализация и молекулярная перестройка являются некоторыми примерами общих химических реакций.
Химическая реакция может быть символически изображена с помощью химического уравнения . В то время как в неядерной химической реакции число и вид атомов на обеих сторонах уравнения равны, для ядерной реакции это относится только к ядерным частицам, а именно. Протоны и нейтроны. [ 32 ]
Последовательность этапов, в которых реорганизация химических связей может происходить в ходе химической реакции, называется его механизмом . Химическая реакция может быть представлена в нескольких шагах, каждая из которых может иметь различную скорость. Таким образом, многие реакционные промежуточные соединения с переменной стабильностью можно предусмотреть во время реакции. Механизмы реакции предлагаются для объяснения кинетики и относительного продукта -смесь реакции. Многие физические химики специализируются на изучении и предложении механизмов различных химических реакций. Несколько эмпирических правил, таких как правила Вудворда - Хоффманн, часто пригодится, предлагая механизм химической реакции.
Согласно книге золота IUPAC , химическая реакция - это «процесс, который приводит к взаимосвязи химических видов». [ 33 ] Соответственно, химическая реакция может быть элементарной реакцией или пошаговой реакцией . Сделано дополнительное предостережение в том смысле, что это определение включает в себя случаи, когда взаимосвязь конформеров экспериментально наблюдается. Такие обнаруживаемые химические реакции обычно включают наборы молекулярных сущностей, как указано в этом определении, но часто концептуально удобно использовать термин также для изменений, включающих отдельные молекулярные объекты (то есть микроскопические химические события »).
Ионы и соли

Ион является заряженным видом, атом или молекулой, которая потеряла или получила один или несколько электронов. Когда атом теряет электрон и, следовательно, имеет больше протонов, чем электронов, атом является положительно заряженным ионом или катионом . Когда атом получает электрон и, следовательно, имеет больше электронов, чем протонов, атом является отрицательно заряженным ионом или анионом . Катионы и анионы могут образовывать кристаллическую решетку нейтральных солей , таких как NA + и кл − Ионы, образующие хлорид натрия , или NaCl. Примеры полиатомных ионов , которые не распадаются во время кислотных базовых реакций, представляют собой гидроксид (OH − ) и фосфат (PO 4 3− ).
Плазма состоит из газообразного вещества, которая была полностью ионизирована, обычно благодаря высокой температуре.
Кислотность и основность
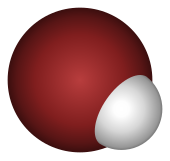
Вещество часто можно классифицировать как кислоту или основание . Есть несколько разных теорий, которые объясняют кислотное поведение. Самым простым является теория Аррениуса , которая утверждает, что кислота является вещество, которое производит ионы гидрония , когда она растворяется в воде, а основание является те, которая производит гидроксидные ионы при растворенности в воде. Согласно теории Brønsted -Lowry -Base -Base , кислоты являются веществами, которые жертвуют положительный водорода ион на другое вещество в химической реакции; По расширению основание - это вещество, которое получает этот водород ион.
Третья общая теория - это теория кислотной базы Льюиса , которая основана на формировании новых химических связей. Теория Льюиса объясняет, что кислота - это вещество, которое способно принимать пару электронов из другого вещества в процессе образования связей, в то время как основание - это вещество, которое может обеспечить пару электронов для формирования новой связи. Есть несколько других способов, которыми вещество может быть классифицировано как кислота или основание, как видно из истории этой концепции. [ 34 ]
Прочность кислоты обычно измеряется двумя методами. Одним из измерений, основанное на определении кислотности Аррениуса, является рН , который представляет собой измерение концентрации ионов гидрония в растворе, выраженной в отрицательной логарифмической шкале. Таким образом, растворы, имеющие низкий pH, имеют высокую концентрацию ионов гидрония и можно сказать, что являются более кислыми. Другим измерением, основанным на определении Brønsted -Lowry, является константа диссоциации кислоты (K a ), которая измеряет относительную способность вещества действовать как кислоту при определении Brønsted -Lowry of Acid. То есть вещества с более высоким K A с большей вероятностью пожертвовают ионы водорода в химических реакциях, чем вещания с более низкими k A. значениями
Окислительно -восстановительный
окислительно-восстановительного ( красный Uction- Oxe Реакции ) включают в себя все химические реакции , в которых атомы имеют изменение своего окислительного состояния либо путем получения электронов (восстановление), либо потери электронов (окисление). Вещества, которые обладают способностью окислять другие вещества, считаются окислительными и известны как окислительные агенты , окислители или окислители. Окислитель удаляет электроны из другого вещества. Точно так же вещества, которые имеют способность уменьшать другие вещества, являются восстановительными и известны как восстановительные агенты , редукты или редукторы.
Редактный передает электроны в другое вещество и, таким образом, окисляется. И поскольку это «жертвует» электроны, это также называется донором электронов. Окисление и восстановление должным образом относятся к изменению числа окисления - фактический перенос электронов может никогда не произойти. Таким образом, окисление лучше определяется как увеличение количества окисления и снижение как уменьшение количества окисления.
Равновесие
Хотя концепция равновесия широко используется во всех науках, в контексте химии она возникает всякий раз, когда можно, как, например, в смеси нескольких химических соединений, которые могут реагировать друг с другом, можно реагировать друг с другом, которые могут реагировать друг с другом или когда вещество может присутствовать более чем в одном виде фазы.
Система химических веществ в равновесии, даже если иметь неизменную композицию, чаще всего не является статичной ; Молекулы веществ продолжают реагировать друг с другом, что приводит к динамическому равновесию . Таким образом, концепция описывает состояние, в котором параметры, такие как химический состав, остаются неизменными с течением времени.
Химические законы
Химические реакции регулируются определенными законами, которые стали фундаментальными понятиями в химии. Некоторые из них:
- Закон Авогадро
- Пиво -ламберт закон
- Закон Бойла (1662 г., связанный с давлением и объемом)
- Закон Чарльза (1787 г., связанный с объемом и температурой)
- Законы распространения Фика
- Закон Гей-Луссака (1809 г., связывающий давление и температуру)
- Принцип болта
- Закон Генри
- Закон Хесса
- Закон о сохранении энергии приводит к важным понятиям равновесия , термодинамики и кинетики .
- Закон о сохранении массы по -прежнему сохраняется в изолированных системах , даже в современной физике. Тем не менее, специальная относительность показывает, что из-за эквивалентности массовой энергии всякий раз, когда нематериальная «энергия» (тепло, свет, кинетическая энергия) удаляется из неизолированной системы, с ней будет потеряна некоторая масса. Высокие потери энергии приводят к потере взвешиваемого количества массы, что является важной темой в ядерной химии .
- Закон определенного состава , хотя во многих системах (особенно биомакромолекулах и минералах) соотношения, как правило, требуют большого количества и часто представлены в виде фракции.
- Закон множества пропорций
- Закон Рауля
История
История химии охватывает период от древнего прошлого до настоящего. Начиная с нескольких тысячелетий до нашей эры, цивилизации использовали технологии, которые в конечном итоге составляли основу различных ветвей химии. Примеры включают извлечение металлов из руд , изготовление керамики и глазури, ферментирование пива и вина, извлечение химических веществ из растений для медицины и духов, превращение жира в мыло , изготовление стакана и изготовление сплавов , таких как бронза .
Химии предшествовали его протологию «Алхимия» , которая управляла ненаучным подходом к пониманию составляющих материи и их взаимодействия. Несмотря на то, что они не увенчались успехом в объяснении природы материи и ее преобразований, алхимики закладывают основу для современной химии, проводя эксперименты и записывая результаты. Роберт Бойл , хотя и скептически относится к элементам и убежден в алхимии, сыграл ключевую роль в повышении «священного искусства» как независимой, фундаментальной и философской дисциплины в своей работе скептической химиста (1661). [ 35 ]
В то время как алхимия и химия связаны с веществом и ее преобразованием, важное различие было дано научным методом , который химики использовали в своей работе. Химия, как совокупность знаний, отличных от алхимии, стала устоявшейся наукой с работой Антуана Лавуазье , у которого развился закон сохранения массы , который требовал тщательного измерения и количественных наблюдений за химическими явлениями. История химии впоследствии переплетается с историей термодинамики , особенно благодаря работе Уилларда Гиббса . [ 36 ]
Определение
Определение химии изменилось с течением времени, поскольку новые открытия и теории добавляют к функциональности науки. Термин «химилия», по мнению известного ученого Роберта Бойла в 1661 году, означал предмет материальных принципов смешанных тел. [ 37 ] В 1663 году химик Кристофер Глейзер описал «химию» как научное искусство, с помощью которого кто -то учится растворять тела и извлекать из них различные вещества на их композиции и как их снова объединить, и превзойти их до более высокого совершенства. [ 38 ]
Определение слова «химия» 1730 года, используемое Георгом Эрнстом Шталом , означало искусство разрешения смешанных, составных или совокупных тел в их принципы; и сочинения таких тел из этих принципов. [ 39 ] В 1837 году Жан-Батист Дюма рассмотрел слово «химия» для обозначения науки, заинтересованной в законах и последствиях молекулярных сил. [ 40 ] Это определение также развивалось до тех пор, пока в 1947 году оно не стало означать науку о веществах: их структуру, их свойства и реакции, которые изменяют их на другие вещества - характеристика, принятая Линусом Полингом . [ 41 ] Совсем недавно, в 1998 году, профессор Рэймонд Чанг расширил определение «химии», чтобы означать изучение материи и изменения, которые он претерпевает. [ 42 ]
Фон

Ранние цивилизации, такие как египтяне [ 43 ] Вавилоняне и индейцы [ 44 ] Полученные практическими знаниями, касающимися искусства металлургии, керамики и красителей, но не разработали систематическую теорию.
Основная химическая гипотеза, впервые возникшая в классической Греции с теорией четырех элементов , как это было окончательно выдвинуто Аристотелем, утверждая, что огонь , воздух , земля и вода были фундаментальными элементами, из которых все образуется как комбинация. Греческий атомизм восходит к 440 г. до н.э., возникающие в работах таких философов, как Демократ и Эпикур . В 50 году до нашей эры римский философ Лукреции расширил теорию в своем стихотворении De Rerum Natura (о природе вещей). [ 45 ] [ 46 ] В отличие от современных концепций науки, греческий атомизм носил чисто философский характер, не имея особого беспокойства по поводу эмпирических наблюдений и не заботиться о химических экспериментах. [ 47 ]
Ранняя форма идеи сохранения массы - это представление о том, что « ничего не исходит из ничто » в древнегреческой философии , которую можно найти в EmpeDocles (ок. Из того, что нет, и это не может быть вызвано или слышал о том, что должно быть полностью уничтожено ». [ 48 ] и Epicurus (3 -й век до нашей эры), который, описывая природу вселенной, писал, что «совокупность вещей всегда была такой, как сейчас, и всегда будет». [ 49 ]

В эллинистическом мире искусство алхимии впервые распространилось, смешивая магию и оккультизм в изучение естественных веществ с конечной целью трансмутации элементов в золото и обнаружение эликсира вечной жизни. [ 50 ] Работа, особенно развитие дистилляции , продолжалась в начале византийского периода, а самым известным практикующим является грек-египетский Зозимос 4-го века . [ 51 ] Алхимия продолжала развиваться и практиковать во всем арабском мире после мусульманских завоеваний , [ 52 ] и оттуда и из византийских остатков, [ 53 ] Распространен в средневековую и ренессансную Европу через латинские переводы.
Арабские работы, приписанные Джабиру Ибн Хайяну , ввели систематическую классификацию химических веществ и предоставили инструкции по получению неорганического соединения ( саль аммоний или хлорид аммония ) из органических веществ (таких как растения, кровь и волосы) химическими средствами. [ 54 ] Некоторые арабские джабирийские произведения (например, «Книга милосердия» и «Книга семидесяти») были позже переведены на латынь под латинизированным именем «Гебер», [ 55 ] А в Европе 13-го века анонимный писатель, обычно называемый псевдогебером , начал производить алхимические и металлургические сочинения под этим именем. [ 56 ] Поздние влиятельные мусульманские философы, такие как Абу аль-Райхан аль-Бируни [ 57 ] и Авиценна [ 58 ] оспаривал теории алхимии, особенно теорию трансмутации металлов .

Улучшения переработки руд и их извлечения для падения металлов были широко использованы источником информации для ранних химиков в 16 -м веке, в том числе Георг Агрикола (1494–1555), который опубликовал свою основную работу De re Metallica в 1556 году. Его работа, Описание высокоразвитых и сложных процессов горнодобывающих металлических руд и экстракции металлов было вершиной металлургии за это время. Его подход удалил всю мистику, связанную с предметом, создав практическую базу, на которой другие могли и будут строить другие. Работа описывает множество видов печи, используемой для падения руды, и стимулировал интерес к минералам и их составу. Агрикола была описана как «отец металлургии» и основатель геологии как научную дисциплину. [ 62 ] [ 60 ] [ 61 ]
Под влиянием новых эмпирических методов, выдвинутых сэром Фрэнсисом Бэконом и другими, группа химиков в Оксфорде , Роберт Бойл , Роберт Хук и Джон Мейоу начали превращать старые алхимические традиции в научную дисциплину. Бойл, в частности, ставил под сомнение некоторые обычно продуманные химические теории и утверждал, что химические практики являются более «философскими» и менее коммерчески сосредоточенными на скептическом Chemyst . [ 35 ] Он сформулировал закон Бойла , отверг классические «четыре элемента» и предложил механистическую альтернативу атомов и химических реакций , которые могут подвергаться строгому эксперименту. [ 63 ]

В последующие десятилетия было сделано много важных открытий, таких как природа «воздуха», который был обнаружен, состоящий из множества различных газов. Шотландский химик Джозеф Блэк и фламандский баптист Яна Ван Хельмонт обнаружили углекислый газ , или то, что Блэк назвал «фиксированным воздухом» в 1754 году; Генри Кавендиш обнаружил водород и выяснил свои свойства и Джозеф Пристли и, независимо от того, что Карл Вильгельм Шеле изолировал чистый кислород . Теория флогистона (вещество в корне всего сжигания) была выдвинута немецкой Георгом Эрнстом Шталом в начале 18 -го века и была отменена только к концу века французским химиком Антуан Лавуазье , химическим аналогом Ньютона в физика. Lavoisier сделал больше, чем любой другой, чтобы установить новую науку о правильной теоретической основе, выяснив принцип сохранения массы и разработки новой системы химической номенклатуры, используемой по сей день. [ 65 ]
Английский ученый Джон Далтон предложил современную теорию атомов ; что все вещества состоят из неделимых «атомов» материи и что разные атомы имеют различные атомные веса.
Развитие электрохимической теории химических комбинаций произошло в начале 19 -го века в результате работы двух ученых, в частности, Йенса Джейкоба Берзелиуса и Хамфри Дэви , ставших возможными благодаря предыдущему изобретению вольтасайской кучи Алессандро Вольта . Дэви обнаружил девять новых элементов, включая щелочные металлы , извлекая их из оксидов с помощью электрического тока. [ 66 ]

Британский Уильям Прут впервые предложил заказать все элементы по их атомному весу, так как у всех атомов был вес, который был точным кратным атомным весом водорода. Jar Newlands разработала раннюю таблицу элементов, которая затем была разработана в современную периодическую таблицу элементов [ 69 ] В 1860 -х годах Дмитрий Менделейв и независимо несколькими другими учеными, включая Юлия Лотара Мейера . [ 70 ] [ 71 ] Инертные газы, позже называемые благородными газами, были обнаружены Уильямом Рамси в сотрудничестве с лордом Рэлеем в конце столетия, тем самым заполняя основную структуру таблицы.

Внизу: наблюдаемые результаты: небольшая часть частиц была отклонена, что указывает на небольшой, концентрированный заряд .
На рубеже двадцатого века теоретические основы химии были окончательно поняты из -за ряда замечательных открытий, которые удалось исследовать и обнаружить саму природу внутренней структуры атомов. В 1897 году Дж.Дж. Томсон из Кембриджского университета обнаружил электрон , и вскоре после того, как французский ученый Беккерл, а также пара Пьер и Мари Кюри исследовали феномен радиоактивности . В серии новаторских экспериментов по рассеянию Эрнест Резерфорд в Манчестерском университете обнаружил внутреннюю структуру атома и существование протона, классифицировал и объяснил различные типы радиоактивности и успешно трансформировал первый элемент путем бомбардировки азота с альфа -частицами .
Его работа по атомной структуре была улучшена его учениками, датским физиком Нильсом Бором , англичанином Генри Мозли и немецким Отто Хан , который продолжил развивающуюся ядерную химию и обнаружил ядерную деление . Электронная теория химических связей и молекулярных орбиталей была разработана американскими учеными Линусом Полингом и Гилбертом Н. Льюисом .
2011 год был объявлен Организацией Объединенных Наций как международный год химии. [ 72 ] Это была инициатива Международного союза чистой и прикладной химии, а также образовательной, научной и культурной организации Организации Объединенных Наций и включает химические общества, ученые и учреждения по всему миру и опирались на отдельные инициативы по организации местной и региональной деятельности.
Органическая химия была разработана Юстусом фон Либигом и другими после Фридриха Вёлера синтеза мочевины . [ 73 ] Другие важные достижения 19 -го века были; Понимание валентной связи ( Эдвард Франкленд в 1852 году) и применения термодинамики к химии ( JW Gibbs и Svante Arrenius в 1870 -х годах).
Упражняться
В практике химии чистая химия является изучением фундаментальных принципов химии, в то время как прикладная химия применяет эти знания для разработки технологий и решения реальных проблем.
Субдисциплинарные
Химия обычно делится на несколько основных субдисциплин. Есть также несколько основных междисциплинарных и более специализированных областей химии. [ 74 ]
- Аналитическая химия - это анализ образцов материала, чтобы получить понимание их химического состава и структуры . Аналитическая химия включает в себя стандартизированные экспериментальные методы в химии. Эти методы могут использоваться во всех субдисциплинах химии, за исключением чисто теоретической химии. [ 75 ]

В аналитической химии, спектроскопические исследования взаимодействия между электромагнитным излучением (светом) и веществом. [ 76 ] Спектрофотометр - это машина , используемая для измерения света эффекта на материю. На фото модель-Бекман Дю-640 - Биохимия - это изучение химических веществ , химических реакций и взаимодействий, которые происходят на молекулярном уровне в живых организмах . Биохимия очень междисциплинарная, охватывающая лекарственную химию , нейрохимию , молекулярную биологию , криминалистику , науку о растениях и генетику . [ 77 ]
- Неорганическая химия - это изучение свойств и реакций неорганических соединений, таких как металлы и минералы. [ 78 ] Различие между органическими и неорганическими дисциплинами не является абсолютным, и существует много совпадений, что наиболее важно в субдисциплинах органометаллической химии .

Каминский катализатор - это органометаллический комплекс, в котором изображены циркониевые или металлические центры. катализатора В зависимости от размещения циклопентадиеновых лигандов , он может продуцировать полипропилены с различной тактикой . [ 79 ] 1 Создает атактический полипропилен, который является мягким и аморфным с свободной композицией. 2 Создает изотактический полипропилен, который твердый и используется в многоразовых пластиковых контейнерах. 3 Создает синдитаксический полипропилен, который является резиновым и полукристаллическим. [ 80 ] - Химия материалов - это подготовка, характеристика и понимание компонентов или устройств твердого состояния с полезным током или будущей функцией. [ 81 ] Эта область представляет собой новую широту исследования в рамках программ для выпускников, и она интегрирует элементы из всех классических областей химии, таких как органическая химия , неорганическая химия и кристаллография с акцентом на фундаментальные проблемы, которые являются уникальными для материалов . Первичные системы исследования включают химию конденсированных фаз (твердые тела, жидкости, полимеры ) и раздела между различными фазами.
- Нейрохимия - это изучение нейрохимических веществ ; включая передатчики, пептиды, белки, липиды, сахара и нуклеиновые кислоты; их взаимодействие и роли, которые они играют в формировании, поддержании и изменении нервной системы.
- Ядерная химия - это изучение того, как субатомные частицы объединяются и делают ядра. Современная трансмутация является большим компонентом ядерной химии, а таблица нуклидов является важным результатом и инструментом для этой области. В дополнение к медицинскому применению , ядерная химия охватывает ядерную инженерию , которая исследует тему использования источников ядерной энергии для получения энергии [ 82 ] [ 83 ]

Маленький мальчик -это атомная бомба , использующая урана-235 реакцию деления . [ 84 ] Запустив суб-критическое уран в другую массу субритического урана в бомбе, самоподдерживающаяся ядерная реакция ( критическая масса ). Он вызвал взрывную силу более 15 000 тонн эквивалентного TNT - Органическая химия - это изучение структуры, свойств, состава, механизмов и реакций органических соединений . Органическое соединение определяется как любое соединение на основе углеродного скелета. Органические соединения могут быть классифицированы, организованы и поняты по реакциям по их функциональным группам , единичным атомам или молекулам, которые показывают характерные химические свойства в соединении. [ 85 ]
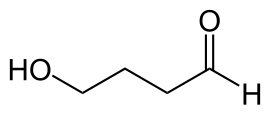
4-гидроксибутанал-это органическое соединение с функциональной группой альдегида (справа) и функциональной группой алкоголя (слева). - Физическая химия - это изучение физической и фундаментальной основы химических систем и процессов. В частности, энергетика и динамика таких систем и процессов представляют интерес для физических химиков. Важные области исследования включают химическую термодинамику , химическую кинетику , электрохимию , статистическую механику , спектроскопию , а в последнее время - астрохимия . Физическая химия имеет большое перекрытие с молекулярной физикой . Физическая химия включает в себя использование бесконечно массивного исчисления в получении уравнений. Обычно это связано с квантовой химией и теоретической химией. Физическая химия - это отдельная дисциплина химической физики , но опять же, есть очень сильное совпадение.
- Теоретическая химия - это изучение химии посредством фундаментальных теоретических рассуждений (обычно в рамках математики или физики ). В частности, применение квантовой механики к химии называется квантовой химией . С момента окончания Второй мировой войны разработка компьютеров позволила систематическому развитию вычислительной химии , которая является искусством разработки и применения компьютерных программ для решения химических задач. Теоретическая химия имеет большое перекрытие с (теоретической и экспериментальной) физикой конденсированного вещества и молекулярной физикой .

На конференции Solvay 1927 года была представлена основополагающих ученых в области теоретической химии и физики. На этой конференции обсуждались электроны и фотоны
Другие подразделения включают электрохимию , фемтохимию , химию вкуса , химию потока , иммуногистохимию , химию гидрирования , математическую химию , молекулярную механику , химию натуральных продуктов , органическая химия , нефтехимия , фотохимия , физическая органическая химия , химия полимера , радиохимия , супрачеолекалярная химия, синтетическая химия, синтетическая химия, супремолекалярная химии, синтетическая химия, Сондхейства , супраликалярная химия , супра. химия и многие другие.
Междисциплинарный
Междисциплинарные поля включают агрохимию , астрохимию (и космохимию ), химию атмосферы , химическую инженерию , химическую биологию , химио-информитику , химию окружающей среды , геохимия , зеленая химия , иммунохимия , морская химия , материаловая наука , механохимия , лекарственная химия, молекулярная биология, наноотехнология, механическая наука, механохимия , лекарственная химия , молекулярная биология , наноотехнология . Энология , фармакология , фитохимия , твердотельная химия , наука о поверхности , термохимия и многие другие.
Промышленность
Химическая промышленность представляет собой важную экономическую деятельность по всему миру. Глобальные 50 лучших производителей химических веществ в 2013 году составили 980,5 млрд. Долл. США с прибылью 10,3%. [ 86 ]
Профессиональные общества
- Американское химическое общество
- Американское общество нейрохимии
- Химический институт Канады
- Химическое общество Перу
- Международный союз чистой и прикладной химии
- Королевский австралийский химический институт
- Королевское химическое общество Королевского Нидерланда
- Королевское химическое общество
- Общество химической промышленности
- Всемирная ассоциация теоретических и вычислительных химиков
- Список химических обществ
Смотрите также
- Сравнение программного обеспечения для моделирования молекулярной механики
- Глоссарий химических терминов
- Международный год химии
- Список химиков
- Список соединений
- Список важных публикаций в химии
- Список нерешенных проблем в химии
- Схема химии
- Периодические системы малых молекул
- Философия химии
- Научный туризм
Ссылки
- ^ Браун, Теодор Л.; Lemay, H. Eugene Jr.; Bursten, Bruce E.; Мерфи, Кэтрин Дж.; Вудворд, Патрик М.; Столцфус, Мэтью В.; Lufaso, Michael W. (2018). «Введение: материя, энергия и измерение». Химия: центральная наука (14 -е изд.). Нью -Йорк: Пирсон. С. 46–85. ISBN 978-0134414232 .
- ^ "Что такое химия?" Полем Chemweb.ucc.ie. Архивировано с оригинала 3 октября 2018 года . Получено 12 июня 2011 года .
- ^ «Определение химии» . Мерриам-Уэбстер . Архивировано из оригинала 7 августа 2020 года . Получено 24 августа 2020 года .
- ^ «Определение химии | Dictionary.com» . www.dictionary.com . Архивировано с оригинала 5 марта 2016 года . Получено 24 августа 2020 года .
- ^ «Химия повсюду» . Американское химическое общество . Архивировано с оригинала 29 ноября 2020 года . Получено 1 декабря 2020 года .
- ^ Карстен Рейнхардт. Химические науки в 20 -м веке: соединение границ . Wiley-VCH, 2001. ISBN 3-527-30271-9 . С. 1–2.
- ^ Теодор Л. Браун, Х. Евгений Лемей, Брюс Эдвард Берен, Х. Лемей. Химия: центральная наука . Prentice Hall; 8 изд. (1999). ISBN 0-13-010310-1 . стр. 3-4.
- ^ «Химия - химия и общество» . Британская . Архивировано из оригинала 6 мая 2023 года . Получено 6 мая 2023 года .
- ^ Ихде, Аарон Дж. (1984). Развитие современной химии . Нью -Йорк: Дувер. ISBN 978-0-486-64235-2 .
- ^ Ньюман, Уильям Р. (2011). «Что мы узнали из недавней историографии алхимии?» Полем ИГИЛ . 102 (2): 313–321. doi : 10.1086/660140 . ISSN 0021-1753 . PMID 21874691 .
- ^ «Алхимия», запись в Оксфордском английском словаре , JA Simpson и Esc Weiner, Vol. 1, 2 -е изд., 1989, ISBN 0-19-861213-3 .
- ^ Weekley, Ernest (1967). Этимологический словарь современного английского. Нью -Йорк: Dover Publications. ISBN 0-486-21873-2
- ^ «Химическая связь» . Британская . Encyclopædia Britannica. Архивировано из оригинала 26 апреля 2012 года . Получено 1 ноября 2012 года .
- ^ Дело: атомы от Демократа до Далтона Архивировали 28 февраля 2007 года на машине Wayback Энтони Карпи, доктор философии.
- ^ ИУПАК ЗОЛОТО
- ^ «Калифорнийский профессиональный гид № 22: Химики» . Calmis.ca.gov. 29 октября 1999 года. Архивировано с оригинала 10 июня 2011 года . Получено 12 июня 2011 года .
- ^ «Общая химия онлайн - сопутствующие примечания: материя» . Antoine.frostburg.edu. Архивировано из оригинала 24 июня 2011 года . Получено 12 июня 2011 года .
- ^ Армстронг, Джеймс (2012). Общая, органическая и биохимия: прикладной подход . Брукс/Коул . п. 48. ISBN 978-0-534-49349-3 .
- ^ Burrows et al. 2009 , с. 13
- ^ Jump up to: а беременный HouseCroft & Sharpe 2008 , с. 2
- ^ Burrows et al. 2009 , с. 110.
- ^ Burrows et al. 2009 , с. 12
- ^ «Иупак номенклатура органической химии» . Acdlabs.com. Архивировано из оригинала 8 июня 2011 года . Получено 12 июня 2011 года .
- ^ Коннелли, Нил Дж.; Дамхус, Туре; Хартшом, Ричард М.; Хаттон, Алан Т. (2005). Номенклатура неорганической химии рекомендаций IUPAC 2005 . Кембридж: Королевское общество химии издательство / IUPAC. ISBN 0854044388 Полем Получено 13 июня 2022 года .
- ^ Хилл, JW; Petrucci, RH; МакКрири, TW; Perry, SS (2005). Общая химия (4 -е изд.). Верхняя Седл -Ривер, Нью -Джерси: Пирсон Прентис Холл. п. 37
- ^ ММ Авензиан; Хью Бейкер. Магниевые и магниевые сплавы . ASM International. п. 59
- ^ Burrows et al. 2009 , с. 16
- ^ Atkins & De Paula 2009 , с. 9
- ^ Visionlearning. «Химическая связь Энтони Карпи, pH» . Visionlearning. Архивировано из оригинала 17 июля 2011 года . Получено 12 июня 2011 года .
- ^ Рейли, Майкл. (2007). Механическая сила индуцирует химическую реакцию, архивируя 14 августа 2014 года на The Wayback Machine , NewsCientist.com Service, Reilly
- ^ Изменяющиеся состояния материи архивировали 28 апреля 2007 года в The Wayback Machine - Chemforkids.com
- ^ Уравнение химической реакции Архивировано 12 октября 2007 года на машине Wayback - IUPAC Goldbook
- ^ Золотая книга Химическая реакция архивирована 4 марта 2007 года на машине Wayback Iupac Goldbook
- ^ «История кислотности» . Би -би -си. 27 мая 2004 года. Архивировано из оригинала 27 февраля 2009 года . Получено 12 июня 2011 года .
- ^ Jump up to: а беременный Принципи Л. (2011). «В ретроспективе: скептический химист» . Природа . 469 (7328): 30–31. Bibcode : 2011natur.469 ... 30 с . doi : 10.1038/469030a . ISSN 1476-4687 . S2CID 6490305 .
- ^ «Избранные классические документы из истории химии» . Архивировано с оригинала 17 сентября 2018 года . Получено 8 октября 2017 года .
- ^ Бойл, Роберт (1661). Скептический химист . Нью -Йорк: Dover Publications, Inc. (Перепечатка). ISBN 978-0-486-42825-3 .
- ^ Глейзер, Кристофер (1663). Имеет дело с Chymie . Париж. Как найдено в: Ким, Ми Гюнг (2003). Аффинность, эта неуловимая мечта - генеалогия химической революции . MIT Press. ISBN 978-0-262-11273-4 .
- ^ Шталь, Джордж (1730). Философские принципы универсальной химии . Лондон
- ^ Дюма, JB (1837). «Affinite» (Notes Rote), VII, стр. 4. «Химическая статика», Париж: Академия наук
- ^ Полинг, Линус (1947). Общая химия . Dover Publications, Inc. ISBN 978-0-486-65622-9 .
- ^ Чанг, Раймонд (1998). Химия, 6 -е изд . Нью -Йорк: МакГроу Хилл. ISBN 978-0-07-115221-1 .
- ^ Первые химики архивировали 8 января 2015 года на машине Wayback , 13 февраля 1999 г., Новый ученый
- ^ Барнс, Рут (2004). Текстиль в обществах Индийского океана . Routledge. п. 1 ISBN 978-0415297660 .
- ^ Лукреция. «de rerum natura (о природе вещей)» . Архив интернет -классики . Массачусетский технологический институт. Архивировано из оригинала 29 июня 2011 года . Получено 9 января 2007 года .
- ^ Симпсон, Дэвид (29 июня 2005 г.). «Лукреция (ок. 99–55 г. до н.э.» . История философии в Интернете . Архивировано из оригинала 28 мая 2010 года . Получено 10 ноября 2020 года .
- ^ Стродах, Джордж К. (2012). Искусство счастья . Нью -Йорк: Penguin Classics. С. 7–8. ISBN 978-0-14-310721-7 .
- ^ 12; См. Pp.291–2 Of Кирк, GS; Je Raven; Малкольм Шофилд (1983). Прессократические философы (2 -е изд.). Кембридж: издательство Кембриджского университета . ISBN 978-0-521-27455-5 .
- ^ Долго, аа; Д.Н. Седли (1987). «Эпикуреанство: принципы сохранения». Эллинистические философы. Том 1: Переводы основных источников с философским комментарием . Кембридж: издательство Кембриджского университета. С. 25–26. ISBN 978-0-521-27556-9 .
- ^ «Международный год химии - история химии» . Git Laboratory Journal Europe. 25 февраля 2011 года. Архивировано с оригинала 15 июня 2013 года . Получено 12 марта 2013 года .
- ^ Брайан Х. Банч и Александр Хеллеманс (2004). История науки и техники . Хоутон Миффлин Харкорт. п. 88 ISBN 978-0-618-22123-3 .
- ^ Моррис Клайн (1985) Математика для нематематического архивирования 5 сентября 2015 года на машине Wayback . Публикации курьера. п. 284 ISBN 0-486-24823-2
- ^ Marcelin Berthelot , Collection des Anciens Alchimistes Grecs (3 тома, Париж, 1887–1888, стр. 161); Ф. Шервуд Тейлор, «Происхождение греческой алхимии», Амбикс 1 (1937), 40.
- ^ Стэплтон, Генри Э .; Азо, RF; Хидаят Хусейн, М. (1927). «Химия в Ираке и Персии в десятом веке нашей эры» Мемуары Азиатского общества Бенгалии . VIII (6): 317–418. OCLC 706947607 . С. 338–340; Краус, Павел (1942–1943). Джабир ибн Хеййн: вклад в историю научных идей в исламе. I. Корпус писаний Джабириенса. II Джабир и греческая наука . Каир: Французский институт восточной археологии. ISBN 978-3-487-09115-0 Полем OCLC 468740510 . тол. II, с. 41–42.
- ^ ДАРМСТЕДЕР, Эрнст. «Liber Misericordiae Geber: Eine Lateinische übersetzung des Gröishere kitâb l-raḥma», Archite für Geschichte der Medizin , 17/4, 1925, с. 181–197; Бертелот, Марцеллин. «Archéologie et Histoire Des Sciences», Mémoires de l'Académie des Sciences de l'ostitut de France , 49, 1906, с. 308–363; См. Также Форстер, Регула. « Ябир . б
- ^ Ньюман, Уильям Р. «Новый свет на личность Гебер», Sudhoffs Archiv , 1985, 69, pp. 76–90; Ньюман, Уильям Р. Summa Perfectionis of Pseudogeber: критическое изд., Перевод и исследование , Лейден: Брилл, 1991, с. 57–103. Ахмад Ю. Аль-Хасан утверждал, что произведения псевдогебер были фактически переведены на латынь с арабского языка (см. Аль-Хасан, Ахмад Й. ». Арабское происхождение латиноамериканских работ Суммы и Гебер: опровержение Бертелота , Ruska и Newman на основе арабских источников », в: Ахмад Ю. Аль-Хасан. Исследования в« Аль-Кимье »: критические проблемы в латинской и арабской алхимии и химии . Хильдесхайм: Георг Олмс Верлаг, 2009, с. 53–104. Также доступно онлайн -архив 25 февраля 2021 года на машине Wayback ).
- ^ Marmura, Michael E.; NASR, Seyyed Hossein (1965). « Введение в исламские космологические доктрины. Концепции природы и методов, используемых для его исследования Ихван Аль-Сафанан, аль-Бируни и Ибн Сина Сейед Хоссейн Наср» . Зеркало . 40 (4): 744–746. doi : 10.2307/2851429 . JSTOR 2851429 .
- ^ Роберт Брифо (1938). Создание человечества , с. 196–197.
- ^ Маршалл, Джеймс Л.; Маршалл, Вирджиния Р. (Осень 2005). «Повторное открытие элементов: Агрикола» (PDF) . Гексагон . 96 (3). Альфа Чи Сигма: 59. ISSN 0164-6109 . OCLC 4478114 . Получено 7 января 2024 года .
- ^ Jump up to: а беременный «Георгия Агрикола» . Калифорнийский университет - Музей палеонтологии . Получено 4 апреля 2019 года .
- ^ Jump up to: а беременный Рафферти, Джон П. (2012). Геологические науки; Геология: рельеф, минералы и скалы . Нью -Йорк: Британская образовательная публикация, с. 10 ISBN 9781615305445
- ^ Карл Альфред фон Циттель (1901) История геологии и палеонтологии , с. 15
- ^ «История - Роберт Бойл (1627–1691)» . Би -би -си. Архивировано из оригинала 9 января 2011 года . Получено 12 июня 2011 года .
- ^ Орел, Кассандра Т.; Дженнифер Слоан (1998). «Мари Энн Полце Лавуазье: мать современной химии». Химический педагог . 3 (5): 1–18. doi : 10.1007/s00897980249a . S2CID 97557390 .
- ^ Ми Гюнг Ким (2003). Аффинность, эта неуловимая мечта: генеалогия химической революции . MIT Press. п. 440 . ISBN 978-0-262-11273-4 .
- ^ Дэви, Хамфри (1808). «О некоторых новых явлениях химических изменений, вызванных электричеством, в частности, разложения фиксированных щелочи и выставки новых веществ, которые составляют их основания» . Философские транзакции Королевского общества . 98 : 1–45. doi : 10.1098/rstl.1808.0001 . Архивировано из оригинала 18 апреля 2021 года . Получено 30 ноября 2020 года .
- ^ «Краткая история развития периодической таблицы» . Химия 412 Примечания к курсу . Западный Орегонский университет. Архивировано из оригинала 9 февраля 2020 года . Получено 20 июля 2015 года .
- ^ Обратите внимание на архив 24 сентября 2015 года на машине Wayback : «... безусловно, правда, что, если бы Менделев никогда не жил современные химики, использовал бы периодическую таблицу» и «Дмитрий Менделейв» . Королевское общество химии. Архивировано из оригинала 2 июля 2014 года . Получено 18 июля 2015 года .
- ^ Зима, Марк. «WebElements: периодическая таблица в Интернете» . Университет Шеффилда . Архивировано с оригинала 4 января 2014 года . Получено 27 января 2014 года .
- ^ «Юлиус Лотар Мейер и Дмитрий Иванович Менделейв» . Институт истории науки. Июнь 2016 года. Архивировано с оригинала 21 марта 2018 года . Получено 20 марта 2018 года .
- ^ "Что делает эти семейные сходства среди элементов? Соляная рудник в Виличке в 1859 году. " Броновски, Джейкоб (1973). Восхождение человека . Литтл, Браун и Компания. п. 322 . ISBN 978-0-316-10930-7 .
- ^ «Химия» . Chemistry2011.org. Архивировано из оригинала 8 октября 2011 года . Получено 10 марта 2012 года .
- ^ Ихде, Аарон Джон (1984). Развитие современной химии . Публикации курьера. п. 164. ISBN 978-0-486-64235-2 .
- ^ «Химия субдисциплин» . www.thecanadianencyclopedia.ca . Получено 1 апреля 2024 года .
- ^ «Аналитическая химия» . Американское химическое общество . Получено 1 апреля 2024 года .
- ^ Skoog, Douglas A.; Холлер, Ф. Джеймс; Крауч, Стэнли Р. (2018). Принципы инструментального анализа (7 -е изд.). Австралия: Cengage Learning. п. 120. ISBN 978-1-305-57721-3 .
- ^ «Изучение биохимии» . www.biochemistry.org . Получено 11 апреля 2024 года .
- ^ «Неорганическая химия» . Американское химическое общество . Получено 1 апреля 2024 года .
- ^ Каминский, Уолтер (1 января 1998 г.). «Высоко активные металлоценовые катализаторы для полимеризации олефина» . Журнал химического общества, Dalton Transactions (9): 1413–1418. doi : 10.1039/a800056e . ISSN 1364-5447 .
- ^ «Полипропилен» . PSLC.WS. Получено 11 апреля 2024 года .
- ^ Фальман, Брэдли Д. (2011). Химия материалов (1 -е изд.). Дордрехт: Springer Netherlands Springer E-Books отпечаток: Springer. С. 1–4. ISBN 978-94-007-0693-4 .
- ^ «Ядерная химия» . Американское химическое общество . Получено 11 апреля 2024 года .
- ^ «21: ядерная химия» . Либрексексы . 18 ноября 2014 года . Получено 11 апреля 2024 года .
- ^ «Маленький мальчик и толстый человек - ядерный музей» . ahf.nuclearmuseum.org/ . Получено 11 апреля 2024 года .
- ^ Браун, Уильям Генри; Айверсон, Брент Л.; Анслин, Эрик В.; Фут, Кристофер С. (2018). Органическая химия (8 -е изд.). Бостон, Массачусетс: Cengage Learning. п. 19. ISBN 978-1-305-58035-0 .
- ^ Тулло, Александр Х. (28 июля 2014 г.). «Глобальные 50 лучших химических фирм C & EN за 2014 год» . Химические и инженерные новости . Американское химическое общество . Архивировано из оригинала 26 августа 2014 года . Получено 22 августа 2014 года .
Библиография
- Аткинс, Питер ; Де Паула, Хулио (2009) [1992]. Элементы физической химии (5 -е изд.). Нью -Йорк: издательство Оксфордского университета . ISBN 978-0-19-922672-6 .
- Берроуз, Эндрю; Холман, Джон; Парсонс, Эндрю; Пивень, Гвен; Прайс, Гарет (2009). Химия 3 Полем Италия: издательство Оксфордского университета . ISBN 978-0-19-927789-6 .
- Housecroft, Кэтрин Э.; Шарп, Алан Г. (2008) [2001]. Неорганическая химия (3 -е изд.). Harlow, Essex: Pearson Education . ISBN 978-0-13-175553-6 .
Дальнейшее чтение
Популярное чтение
- Аткинс, PW Galileo's Finger ( Oxford University Press ) ISBN 0-19-860941-8
- Аткинс, молекулы PW Atkins (издательство Кембриджского университета) ISBN 0-521-82397-8
- Кин, Сэм. Исчезающая ложка - и другие настоящие истории из периодического стола (черный лебедь) Лондон, 2010 ISBN 978-0-552-77750-6
- Levi, Primo Периодическая таблица (Penguin Books) [1975] переведено с итальянского Рэймонда Розенталя (1984) ISBN 978-0-14-139944-7
- Стверка А. Руководство по элементам (издательство Оксфордского университета) ISBN 0-19-515027-9
- «Словарь истории идей» . Архивировано из оригинала 10 марта 2008 года.
- . Encyclopædia Britannica . Тол. 6 (11 -е изд.). 1911. С. 33–76.
Вводные учебники бакалавриата
- Atkins, PW, Overton, T., Rourke, J., Weller, M. и Armstrong, F. Shriver и Atkins Inorganic Chemistry (4 -е изд.) 2006 (издательство Оксфордского университета) ISBN 0-19-926463-5
- Чан, Рэймонд. Химия 6 -е изд. Бостон: Джеймс М. Смит, 1998. ISBN 0-07-115221-0 .
- Клейден, Джонатан ; Гривз, Ник; Уоррен, Стюарт ; Wothers, Peter (2001). Органическая химия (1 -е изд.). Издательство Оксфордского университета. ISBN 978-0-19-850346-0 .
- Нога и нога. Биохимия (Wiley) ISBN 0-471-58651-X
Усовершенствованные учебники на уровне бакалавриата или выпускники
- Аткинс, PW Physical Chemistry (издательство Оксфордского университета) ISBN 0-19-879285-9
- Аткинс, PW et al. Молекулярная квантовая механика (издательство Оксфордского университета)
- Маквини, валентность Р. Коулсона (Оксфордские научные публикации) ISBN 0-19-855144-4
- Полингинг Л. Характер химической связи (издательство Корнелльского университета) ISBN 0-8014-0333-2
- Полинг Л. и Уилсон, EB Введение в квантовую механику с применением к химии (Dover Publications) ISBN 0-486-64871-0
- Умный и Мур. Сплошная химия: введение (Чепмен и Холл) ISBN 0-412-40040-5
- Стивенсон, Г. Математические методы для студентов естественных наук (Лонгман) ISBN 0-582-44416-0






