Нитрил

При органической химии нитрил - это любое органическое соединение , которое имеет - C ≡ N Функциональная группа . Название соединения состоит из основания, которое включает углерод −c≡N , суффикс с «нитрилами», например, например, CH 3 CH 2 C≡N называется « пропионитрил » (или пропананитрил). [ 1 ] Префикс Cyano - используется взаимозаменяемо с термином нитрила в промышленной литературе. Нитрилы обнаружены во многих полезных соединениях, включая метил цианоакрилат , используемые в супер клей и нитрил-резин , нитрилсодержащий полимер , используемый в без латекса лабораторных и медицинских перчатках . Нитриловая резина также широко используется в качестве автомобильных и других уплотнений, поскольку она устойчива к топливу и маслам. Органические соединения, содержащие несколько нитрильных групп, известны как цианокарблеры .
Неорганические соединения, содержащие Группа −Cспеют не называется нитрилами, а цианидами вместо этого. [ 2 ] Хотя как нитрилы, так и цианиды могут быть получены из солей цианидов, большинство нитрилов не так токсичны.
Структура и основные свойства
[ редактировать ]Геометрия N -C -C является линейной по нитрилам, отражая гибридизацию SP трехстороннего углерода. Расстояние C - N короткое на уровне 1,16 Å , что согласуется с тройной связью . [ 3 ] Нитрилы полярны, о чем свидетельствует высокие дипольные моменты. Как жидкости, они имеют высокую относительную дифференциацию , часто в 30 -х годах.
История
[ редактировать ]Первое соединение гомологического ряда нитрилов, нитрила муравьиной кислоты , цианид водорода был сначала синтезирован CW Scheele в 1782 году. [ 4 ] [ 5 ] В 1811 году JL Gay-Lussac смог подготовить очень токсичную и летучую чистую кислоту. [ 6 ] Около 1832 года бензонитрил , нитрил бензойной кислоты , был приготовлен Фридрихом Вёлером и Юстусом фон Либигом , но из -за минимального выхода синтеза ни физических, ни химических свойств не определялись, ни предложенная структура. В 1834 году тефил-Желез синтезированный пропионитрил , предполагая, что он является эфиром пропионового спирта и гидроцианиновой кислоты. [ 7 ] Синтез бензонитрила Германом Фелингом в 1844 году путем нагрева бензоата аммония был первым методом, который дал достаточно вещества для химических исследований. Феринг определил структуру, сравнив его результаты с уже известным синтезом цианида водорода путем нагрева аммония . Он придумал название «нитрил» для вновь обретенного вещества, которое стало именем для этой группы соединений. [ 8 ]
Синтез
[ редактировать ]В промышленности основными методами производства нитрилов являются аммоксидирование и гидроцианинация . Оба маршрута зеленые в том смысле, что они не генерируют стехиометрические количества солей.
Аммоксидирование
[ редактировать ]При аммоксидировании углеводород . частично окисляется присутствии аммиака в Это преобразование практикуется в больших масштабах для акрилонитрила : [ 9 ]
При производстве акрилонитрила боковой продукт является ацетонитрилом . В промышленном масштабе несколько производных бензонитрила , фталонитрила , а также изобутиронитрила получают путем аммоксидирования. Процесс катализируется оксидами металлов и предполагается, что он проходит через имин.
Гидроцианинация
[ редактировать ]Гидроцианация является промышленным методом для производства нитрилов из цианида водорода и алкенов. Процесс требует однородных катализаторов . Примером гидроцианации является производство адипонитрила , предшественника нейлона-6,6 от 1,3-бутадиена :
Из органических галогенидов и солей цианидов
[ редактировать ]Две реакции метатезиса соли популярны для лабораторных реакций. В -синтезе Колбе нитриле алкилгалогениды подвергаются нуклеофильной алифатической замене щелочных металлов цианидами . Арил нитрилы готовятся в синтезе Розенмунда-прон Браун .
В целом, цианиды металлов в сочетании с алкилгалогентами, чтобы получить смесь нитрила и изонитрила , хотя соответствующий выбор противоречения и температуры может минимизировать последнее. Алкилсульфат синтез полностью устраняет проблему, особенно в невостовых условиях ( Pelouze ). [ 5 ]
Цианогидрины
[ редактировать ]
Цианогидрины - это специальный класс нитрилов. Классически они являются результатом добавления цианидов щелочных металлов к альдегидам в реакции цианогидрина . Из -за полярности органического карбонила эта реакция не требует катализатора, в отличие от гидроцианации алкенов. О-силиловые цианогидрины генерируются с помощью экземпляра триметилсилильного цианида в присутствии катализатора (силилсианация). Цианогидрины также получают реакциями трансицианогидрина, начинающимися, например, с ацетоновым цианогидрином в качестве источника HCN. [ 10 ]
Обезвоживание амидов
[ редактировать ]Нитрилы могут быть приготовлены путем обезвоживания первичных амидов . Общие реагенты для этого включают фосфор пентоксид ( P 2 O 5 ) [ 11 ] и тионилхлорид ( SOCL 2 ). [ 12 ] В связанном обезвоживании вторичные амиды дают нитрилы от деградации амида фон Браун . В этом случае одна связь CN расщеплена.
Окисление аминов
[ редактировать ]Существуют многочисленные традиционные методы для препарата нитрила путем окисления амина . [ 13 ] Кроме того, в последние десятилетия были разработаны несколько селективных методов для электрохимических процессов. [ 14 ]
От альдегидов и оксимов
[ редактировать ]Преобразование альдегидов в нитрилы через Aldoximes является популярным лабораторным путем. Альдегиды легко реагируют с солями гидроксиламина , иногда при температуре, столь же низкой, чтобы дать aldoximes. Они могут быть обезвожены до нитрилов с помощью простого отопления, [ 15 ] Хотя широкий спектр реагентов может помочь в этом, в том числе триэтиламина / диоксид серы , цеолиты или хлорид сульфури . Связанная гидроксиламин-о-сульфоновая кислота реагирует аналогично. [ 16 ]
В специализированных случаях реакцию Ван Леузена можно использовать . Биокатализаторы, такие как алифатическая альдокс -дегидратаза, также эффективны.
Песчаная реакция
[ редактировать ]Ароматические нитрилы часто готовятся в лаборатории из анилина через соединения диазония . Это реакция Sandmeyer . Это требует цианидов переходного металла. [ 17 ]
Другие методы
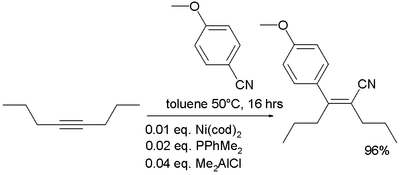
[ редактировать ]- Коммерческий источник для цианидной группы - диэтилалиминий цианид Et 2 alcn , который может быть получен из триэтилулиминия и HCN. [ 18 ] Он использовался в нуклеофильном дополнении к кетонам . [ 19 ] Для примера его использования см.: Куваджима таксол общий синтез
- Цианидные ионы облегчают сочетание дибромидов. Реакция α, α'-дибримо адипиновая кислота с цианидом натрия в этаноле дает цианоциклобутан : [ 20 ]

- Ароматические нитрилы могут быть приготовлены из базового гидролиза трихлорметилрил кетиминов ( RC (CCL 3 ) = NH ) в синтезе Houben-Fischer [ 21 ]
- Нитрилы могут быть получены из первичных аминов посредством окисления . Общие методы включают в себя использование перспективы калия , [ 22 ] Трихлороизоцианурустная кислота , [ 23 ] или анодный электросинтез . [ 24 ]
- α - аминокислоты образуют нитрилы и диоксид углерода с помощью различных средств окислительного декарбоксилирования . [ 25 ] [ 26 ] Генри Дрисдейл Дакин обнаружил это окисление в 1916 году. [ 27 ]
- Из арил карбоновых кислот ( Letts нитрил синтез )
Реакция
[ редактировать ]Нитрильные группы в органических соединениях могут подвергаться множеству реакций в зависимости от реагентов или условий. Нитриловая группа может быть гидролизована, уменьшена или выброшена из молекулы в качестве цианидного иона.
Гидролиз
[ редактировать ]Гидролиз дать нитрилов RCN проходит в отдельных этапах под кислотой или базовой обработкой, чтобы сначала карбоксамиды RC (= O) NH 2 , а затем карбоновые кислоты RCOOH. Гидролиз нитрилов в карбоновые кислоты эффективен. В кислоте или основе сбалансированные уравнения следующие:
Строго говоря, эти реакции опосредованы (в отличие от катализируемых ) кислотой или основанием, поскольку один эквивалент кислоты или основания потребляется с образованием аммония или карбоксилатной соли соответственно.
Кинетические исследования показывают, что константа скорости второго порядка для гидроксид-ионного катализируемого гидролиза ацетонитрила к ацетамиду составляет 1,6 × 10 −6 М −1 с −1 , который медленнее, чем гидролиз амида в карбоксилат (7,4 × 10 −5 М −1 с −1 ) Таким образом, базовый маршрут гидролиза будет позволить себе карбоксилат (или амид, загрязненный карбоксилатом). С другой стороны, кислотные катализируемые реакции требуют тщательного контроля температуры и соотношения реагентов, чтобы избежать образования полимеров, что способствует экзотермическому характеру гидролиза. [ 28 ] Классическая процедура для преобразования нитрила в соответствующий первичный амид требует добавления нитрила в холодную концентрированную серную кислоту . [ 29 ] Дальнейшее преобразование в карбоновую кислоту не подрывается низкой температурой и низкой концентрацией воды.
Два семейства ферментов катализируют гидролиз нитрилов. Нитрилазы гидролизуются нитрилы в карбоновые кислоты:
Нитрильные гидратазы представляют собой металлоферменты , которые гидролизуют нитрилы в амиды.
Эти ферменты используются коммерчески для производства акриламида .
«Безводная гидратация» нитрилов к амидам была продемонстрирована с использованием оксима в качестве источника воды: [ 30 ]
Снижение
[ редактировать ]Нитрилы восприимчивы к гидрированию по сравнению с разнообразными металлическими катализаторами. Реакция может позволить себе либо основной амин ( RCH 2 NH 2 ) или третичный амин ( (RCH 2 ) 3 N ), в зависимости от условий. [ 31 ] При обычном органическом восстановлении нитрил снижается при обработке литием -алюминиевым гидридом к амину. Сокращение до имина, сопровождаемое гидролизом в альдегид, происходит в синтезе Стефана альдегида , в котором используется хлорид станов в кислоте.
Депротонирование
[ редактировать ]Алкил -нитрилы достаточно кислой, чтобы подвергнуться депротонированию связей СН, прилегающей к группе CN. [ 32 ] [ 33 ] Требуются сильные основания, такие как литий -диизопропиламид и бутиловый литий . Продукт называется нитрильным анионом . Эти карбанионы алкилируют широкий спектр электрофилов. Ключом к исключительной нуклеофильности является небольшая стерическая потребность в блоке CN в сочетании с его индуктивной стабилизацией. Эти функции делают нитрилы идеальными для создания новых углеродных облигаций в стерически требовательных средах.
Нуклеофилы
[ редактировать ]Углеродный центр нитрила является электрофильным , следовательно, он подвержен реакциям нуклеофильного добавления :
- с соединением организма в реакции Blaise
- с спиртами в реакции Пиннера .
- с аминами, например, реакция амина саркозина с цианамидом дает креатин [ 34 ]
- с аренами для формирования кетонов в реакции Хоубен -Хосх через промежуточный имин .
- с реагентами Grignard для формирования первичных ктиминов в синтезе кетимина Moureau-Mignonac. [ 35 ] Хотя это и не классическая реакция Grignard , она может считаться одной под более широкими современными определениями.
Разное методы и соединения
[ редактировать ]- В восстановительной децинации нитриловая группа заменяется протоном. [ 36 ] Децины могут быть достигнуты путем растворения восстановления металлов (например, HMPA и калия в трет -бутаноле ) или путем слияния нитрила в Ко . [ 37 ] Аналогичным образом, α-аминонитрилы могут быть децины с другими восстановительными агентами, такими как гидрид лития алюминия . [ 36 ]
- В так называемой реакции Franchimont (разработанной бельгийским докторским студентом Антуан Пол Николас Франчамонт (1844-1919) в 1872 году), α-цианокарбоновая кислота, нагретая в кислотных гидролизах и декарбоксилирует на димер. [ 38 ]
- Самореакция нитрилов в присутствии основания в реакции Торпа в нуклеофильном добавлении
- В металлоорганической химии нитрилы, как известно, добавляют в алкины в карбоциане: [ 39 ]
Комплексообразование
[ редактировать ]Нитрилы являются предшественниками нитрильных комплексов переходного металла , которые являются реагентами и катализаторами. Примеры включают тетракис (ацетонитрил) медь (i) гексафторофосфат ( [С (mecn) 4 ] + и бис (бензонитрил) дихлорид палладий ( PDCL 2 (PHCN) 2 ). [ 40 ]

Нитрильные производные
[ редактировать ]Органические цианамиды
[ редактировать ]Цианамиды представляют собой соединения N -Киано с общей структурой Ведущий 1 Ведущий 2 N - C≡N и связан с родительским цианамидом . [ 41 ]
Нитрильные оксиды
[ редактировать ]Нитрильные оксиды имеют химическую формулу Rcno . Их общая структура R - C≡N + - − Полем R обозначает любую группу (обычно органильный , например, оксид ацетонитрила CH 3 -Cспеющих + - − , водород в случае фулминовой кислоты H - C≡N + - − , или галоген (например, хлор -фульнат Cl - C≡N + - − ). [ 42 ] : 1187–1192
Нитрильные оксиды сильно отличаются от нитрилов: они очень реакционноспособны 1,3-дипуля , и не могут быть синтезированы от прямого окисления нитрилов. [ 43 ] Вместо этого они могут быть синтезированы путем дегидрирования оксимов или обезвоживания нитроалканов ; [ 44 ] : 934–936 Они используются в 1,3-диполярных циклических веществах , [ 42 ] : 1187–1192 такие как изоксазолы . [ 44 ] : 1201–1202 Они подвергаются душевой перестройке типа 1 изоцианатов 1 . [ 42 ] : 1700
Появление и приложения
[ редактировать ]Нитрилы встречаются естественным образом в разнообразном наборе растений и животных источников. Более 120 природных нитрилов были изолированы из наземных и морских источников. Нитрилы обычно встречаются в фруктовых ямах, особенно миндаль, и во время приготовления курортов Brassica (таких как капуста, брюссельская капуста и цветная капуста), которые высвобождают нитрилы через гидролиз. Манделонитрил , цианогидрин, продуцируемый проглатыванием миндаля или некоторых фруктовых ям, высвобождает цианид водорода и отвечает за токсичность цианогенных гликозидов. [ 45 ]
В настоящее время более 30 нитрилосодержащих фармацевтических препаратов продаются для разнообразных лекарственных показаний с более чем 20 дополнительными нитрилосодержащими потенциальными клиническими данными. Типы фармацевтических препаратов, содержащих нитрилы разнообразны, от вилдаглиптина , антидиабетического препарата, до анастрозола , который является золотым стандартом при лечении рака молочной железы. Во многих случаях нитрил имитирует функциональность, присутствующую в субстратах для ферментов, тогда как в других случаях нитрил увеличивает растворимость воды или снижает восприимчивость к окислительному метаболизму в печени. [ 46 ] Функциональная группа нитрила встречается в нескольких препаратах.
-
Структура циталопрама , антидепрессантного препарата селективного серотонина -ингибитора ингибитора (SSRI).
-
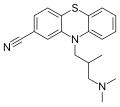
Структура циамемазина , антипсихотического препарата.
-
Структура фродрозола , ингибитор ароматазы для лечения рака молочной железы.
-
Структура летрозола , пероральный нестероидный ингибитор ароматазы для лечения определенных рака молочной железы.
Смотрите также
[ редактировать ]- Протонированные нитрилы: нитрилия
- Депротонированные нитрилы: нитрил анион
- Цианоуглерод
- Нитрил илид
Ссылки
[ редактировать ]- ^ IUPAC Gold Book Nitriles
- ^ Ncbi-mesh Нитрилы
- ^ Каракида, Кен-Ичи; Фукуяма, Цутуму; Кучицу, Козо (1974). «Молекулярные структуры цианида водорода и ацетонитрила, изученных с помощью газовой дифракции» . Бюллетень химического общества Японии . 47 (2): 299–304. doi : 10.1246/bcsj.47.299 .
- ^ См.:
- Карл В. Шил (1782) «Попытки по окраске темы в Берлинском синем» (эксперимент, касающийся цветного вещества в Берлинском голубом), Королевская шведская академия наук (Королевская шведская академия науки), 3: 264-275 (в Шведский).
- Перепечатано на латыни как: «Материал, погружающийся в синий Берлин» в: Карл Вильгельм Шельибус с Эрнстом Бенджамином Готлибом Хейнрихом (ред.) И Готфридом Шафером (транс.), Брош Химика и Физика (Лейпциг («Нью -Йорк») (Германия »), Брош Химика (Лейпциг (« Нью -Йорк ») (Германия»), Брош Химика (Лейпциг («Нью -Йорк») (Германия »), Брош Химика (Лейпциг (« Нью -Йорк ») (Германия»), Брош Химика (Лейпциг («Нью -Йорк») (Германия »), Брош Химика (Leipzig (« Нью -Йорк ») (Trans.) , (Германия "), (Германия"), (Германия "): Иоганн Годфрид Мюллер, 1789), вып. 2, страницы 148-174.
- ^ Jump up to: а беременный Дэвид Т. Моури (1948). «Приготовление нитрилов». Химические обзоры . 42 (2): 189–283. doi : 10.1021/cr60132a001 . PMID 18914000 .
- ^ Gay-Lussac вырабатывал чистый, жидкий водород цианид в: Gay-Lussac, J (1811). « Примечание о животной кислоте» (примечание на прусскую кислоту) » . Анналы химии . 44 : 128–133.
- ^ Дж. Пелуз (1834). «Примечание о новой циантере» [Примечание на новом эфире Cyano]. Анналы фармации . 10 (3): 249. doi : 10.1002/jlac.18340100302 .
- ^ Герман Фелин (1844). «О разложении бензоазавра аммиака теплом (о разложении бензоата аммония путем тепла)» . Анналы химии и фармации . 49 (1): 91–97. Doi : 10.1002/jlac.18440490106 . На странице 96 Фелинг пишет: «Поскольку Лоран уже назвал тело, которое он обнаружил нитробензоил, уже есть азобен зоил, так что вы можете назвать тело, созданное из аммиака Benzoësaurem». (С тех пор, как Лоран назвал вещество, которое обнаружило его «нитробензоил» - другими словами, «азобензоил» уже существует - так что можно назвать вещество, которое происходит от бензоата аммония, возможно, «бензонитрил».)
- ^ Поллак, Петр; Ромедер, Жерард; Хагедорн, Фердинанд; Гелбке, Хайнц-Петер (2000). "Нитрилы". Энциклопедия промышленной химии Уллмана . Вейнхайм: Wiley-VCH. doi : 10.1002/14356007.a17_363 . ISBN 3527306730 .
- ^ Грегори, Роберт Дж. Х. (1999). «Цианогидрины в природе и лаборатории: биология, препараты и синтетические применения». Химические обзоры . 99 (12): 3649–3682. doi : 10.1021/cr9902906 . PMID 11849033 .
- ^ "Osobutyronitrile". Органические синтезы . 25 : 61. 1945. doi : 10.15227/orgsyn.025.0061 .
- ^ «2-этилгексанонитрил». Органические синтезы . 32 : 65. 1952. DOI : 10.15227/Orgsyn.032.0065 .
- ^ Schümperli, Martin T.; Хаммонд, CERI; Германс, IVE (2021). «Разработки в аэробном окислении аминов». ACS Catal . 2 (6): 1108–1117. doi : 10.1021/cs300212q .
- ^ Сюй, Чинин; Ковач, Эрвин (2024). «Помимо традиционного синтеза: электрохимические подходы к окислению амина для нитрилов и иминов» . ACS org inorg au . doi : 10.1021/acsorginorgau.4c00025 .
- ^ Холод, Сэмюэль Т.; Мебейн, Роберт С. (18 сентября 2009 г.). «Облегченное преобразование альдегидов в одноналепию в нитрилы». Синтетическая связь . 39 (20): 3601–3606. doi : 10.1080/00397910902788174 . S2CID 97591561 .
- ^ C. fizet; Дж. Стрейт (1974). «Гидроксиламин -о -сульфоновая кислота: удобный реагент для окислительного превращения альдегидов в нитрилы». Тетраэдр Летт. (на немецком языке). 15 (36): 3187–3188. doi : 10.1016/s0040-4039 (01) 91857-x .
- ^ " o -tolunitrile и p -tolunitrile" ht clarke и RR Read Org. Синтезатор 1941, Coll. Тол. 1, 514.
- ^ У. Нагата и М. Йошиока (1988). «Диэтилалиминий цианид» . Органические синтезы ; Собранные объемы , вып. 6, с. 436 .
- ^ У. Нагата, М. Йошиока и М. Мураками (1988). «Приготовление соединений циано с использованием алкилалуминия промежуточных соединений: 1-циано-6-метокси-3,4-дигидронафталин» . Органические синтезы
{{cite journal}}: CS1 maint: multiple names: authors list (link); Собранные объемы , вып. 6, с. 307 - ^ Рейнольд С. Фусон; Оскар Р. Кримиер и Гилберт Л. Ниммо (1930). «Кольцо закрывается в серии циклобутанов. II. Циклизация α, α'-дибром-адипических сложных эфиров. J. Am. Химический Соц 52 (10): 4074–4 Doi : 10.1021/ j01373a046
- ^ J. Houben, Walter Fischer (1930) «На новом методе представления циклического нитрила через каталитическое демонтаж (I. Mitteil.)», Отчеты Германского химического общества (A и B Series) 63 (9): 2464 - 2472. два : 10.1002/cber.19300630920
- ^ Ямазаки, Шигеказу; Yamazaki, Yasuyuki (1990). «Катализируемое никель дегидрирование аминов к нитрилам» . Бюллетень химического общества Японии . 63 (1): 301–303. doi : 10.1246/bcsj.63.301 .
- ^ Чен, Фен-Эр; Куанг, Юн-Янь; Hui-Fang, Dai; Лу, Лян (2003). «Селективное и мягкое окисление первичных аминов до нитрилов трихлорузоцианурной кислотой». Синтез . 17 (17): 2629–2631. doi : 10.1055/s-2003-42431 .
- ^ Schäfer, HJ; Feldhues, U. (1982). «Окисление первичных алифатических аминов до нитрилов на гидроксидном электроде никеля». Синтез . 1982 (2): 145–146. doi : 10.1055/s-1982-29721 . S2CID 97172564 .
- ^ Хигель, Джин; Льюис, Джастин; Bae, Jason (2004). «Преобразование α-аминокислот в нитрилы путем окислительного декарбоксилирования с трихлороизоцианурной кислотой». Синтетическая связь . 34 (19): 3449–3453. doi : 10.1081/scc-2000958 . S2CID 52208189 .
- ^ Хэмпсон, н; Ли, J; Макдональд, К. (1972). «Окисление амино соединений в анодном серебре». Электрохимика Акта . 17 (5): 921–955. doi : 10.1016/0013-4686 (72) 90014-X .
- ^ Дакин, Генри Дрисдейл (1916). «Окисление аминокислот в цианиды» . Биохимический журнал . 10 (2): 319–323. doi : 10.1042/bj0100319 . PMC 1258710 . PMID 16742643 .
- ^ Kukushkin, V. Yu.; Pombeiro, AJL (2005). «Металл-опосредованный и катализируемый металлом гидролиз нитрилов». Inorg. Чим. Акт . 358 : 1–21. doi : 10.1016/j.ica.2004.04.029 .
- ^ Аббас, Хамис А. (1 января 2008 г.). «Заместительное влияние на гидролиз P замещенных бензонитрилов в растворах серной кислоты при (25,0 ± 0,1) ° C» . Журнал естественных исследований а . 63 (9): 603–608. Bibcode : 2008znata..63..603a . Doi : 10.1515/zna-2008-0912 . ISSN 1865-7109 .
- ^ Дахи Кан; Джинву Ли; Хи-Юн Ли (2012). «Безводная гидратация нитрилов к амидам: p -карбометоксибензамид» . Органические синтезы . 89 : 66. doi : 10.15227/orgsyn.089.0066 .
- ^ Barrault, J.; Pouilloux, Y. (1997). «Каталитические реакции аминации: синтез жирных аминов. Контроль селективности в присутствии многофункциональных катализаторов». Катализ сегодня . 1997 (2): 137–153. doi : 10.1016/s0920-5861 (97) 00006-0 .
- ^ Arseniyadis, Siméon; Кайлер, Кит С.; Уотт, Дэвид С. (1984). «Реакции с добавлением и заменой нитрил-стабилизированных карбанионов». Органические реакции . С. 1–364. doi : 10.1002/0471264180.or031.01 . ISBN 978-0-471-26418-7 .
- ^ Ян, Сюн; Флеминг, Фрейзер Ф. (2017). «C- и N-метал-нитрилы: взаимосвязь между структурой и селективностью». Счета химических исследований . 50 (10): 2556–2568. doi : 10.1021/acs.accounts.7b00329 . PMID 28930437 .
- ^ Смит, Андри Л.; Тан, Паула (2006). «Синтез креатина: эксперимент по лаборатории органической химии бакалавриата». J. Chem. Образовательный 83 (11): 1654. Bibcode : 2006jched..83.1654S . doi : 10.1021/ed083p1654 .
- ^ «Синтез кетимина Moureau-Mignonac». Комплексные органические реакции и реагенты . Хобокен, Нью -Джерси, США: John Wiley & Sons, Inc. 15 сентября 2010 года. С. 1988–1990. doi : 10.1002/9780470638859.conrr446 . ISBN 9780470638859 .
- ^ Jump up to: а беременный Реакция редуцирующей децинации: химические методы и синтетические применения Жан-Марк Мэтталия, Кэролайн Марки-Делапьер, Хасан Хазимех и Мишель Чанон Аркивок (AL-1755FR), стр. 90–118 2006 г. [ Постоянная мертвая ссылка ]
- ^ Беркофф, Чарльз Э.; Ривард, Дональд Э.; Киркпатрик, Дэвид; Айвз, Джеффри Л. (1980). «Редактивная децинация нитрилов путем щелочного слияния». Синтетическая связь . 10 (12): 939–945. doi : 10.1080/00397918008061855 .
- ^ Franchimont, Антуан Пол Николас (1872). «О дибензилдикарбоновой кислоте» [на 2,3-дифенилсукциновой кислоте]. Отчеты немецкого химического общества . 5 (2): 1048–1050. Doi : 10.1002/cber.187200502138 .
- ^ Йошиаки Накао; Акира Яда; Широ Эбата и Тамеджиро Хияма (2007). «Драматическое влияние катализаторов Льюиса на катализируемую никелем карбоцианации алкинов». J. Am. Химический Соц (Коммуникация). 129 (9): 2428–2429. doi : 10.1021/ja067364x . PMID 17295484 .
- ^ Рак, SF; Kühn, Fe (2009). «Нитрильные комплексы переходных металлов с слабо координирующими контрабаньями и их каталитическими применениями». Химические обзоры . 109 (5): 2061–2080. doi : 10.1021/cr800270h . PMID 19326858 .
- ^ Март, Джерри (1992), Advanced Organic Chemistry: реакции, механизмы и структура (4 -е изд.), Нью -Йорк: Wiley, p. 436–7, ISBN 0-471-60180-2
- ^ Jump up to: а беременный в Смит, Майкл Б.; Март, Джерри (2007). Продвинутая органическая химия марта (6 -е изд.). Джон Уайли и сыновья. ISBN 978-0-471-72091-1 .
- ^ Grundmann, Ch. (1970). «Нитрильные оксиды». В Раппопорте, Зви (ред.). Химия группы Cyano . Химия функциональных групп Патая. п. 794. DOI : 10.1002/9780470771242.CH14 . ISBN 978-0-471-70913-8 .
- ^ Jump up to: а беременный Клейден, Джонатан ; Гривз, Ник; Уоррен, Стюарт ; Wothers, Peter (2001). Органическая химия (1 -е изд.). Издательство Оксфордского университета. ISBN 978-0-19-850346-0 .
- ^ Натуральные отчеты о продуктах выпуск 5, нитрилсодержащие натуральные продукты 1999 г.
- ^ Флеминг, Фрейзер Ф.; Яо, Лихуа; Равикумар, ПК; Фанк, Ли; Шук, Брайан С. (ноябрь 2010 г.). «Нитрилсодержащие фармацевтические препараты: эффективная роль нитрилового фармакофора» . J Med Chem . 53 (22): 7902–17. doi : 10.1021/jm100762r . PMC 2988972 . PMID 20804202 .
Внешние ссылки
[ редактировать ]- IUPAC , сборник химической терминологии , 2 -е изд. («Золотая книга») (1997). Онлайн -исправленная версия: (2006–) « нитрил ». два : 10.1351/goldbook.n04151
- IUPAC , сборник химической терминологии , 2 -е изд. («Золотая книга») (1997). Онлайн -исправленная версия: (2006–) « Цианид ». два : 10.1351/goldbook.c01486