Терифлуномид
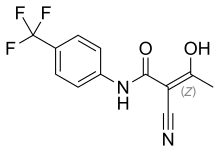 | |
 | |
| Клинические данные | |
|---|---|
| Торговые названия | Обаджо |
| Другие имена | А77 1726 |
| AHFS / Drugs.com | Монография |
| Медлайн Плюс | а613010 |
| Данные лицензии |
|
| Беременность категория | |
| Маршруты администрация | Через рот |
| код АТС | |
| Юридический статус | |
| Юридический статус | |
| Фармакокинетические данные | |
| Связывание с белками | >99,3% |
| Период полувыведения | 2 недели |
| Экскреция | Желчные протоки / каловые , почки |
| Идентификаторы | |
| Номер CAS | |
| ПабХим CID | |
| ИЮФАР/БПС | |
| Лекарственный Банк | |
| ХимическийПаук | |
| НЕКОТОРЫЙ | |
| КЕГГ | |
| ЧЭБИ | |
| ЧЕМБЛ | |
| Панель управления CompTox ( EPA ) | |
| Информационная карта ECHA | 100.170.077 |
| Химические и физические данные | |
| Формула | С 12 Ч 9 Ж 3 Н 2 О 2 |
| Молярная масса | 270.211 g·mol −1 |
| 3D model ( JSmol ) | |
| | |
Терифлуномид , продаваемый под торговой маркой Aubagio является активным метаболитом лефлуномида . , [6] Терифлуномид исследовался в рамках III фазы клинического исследования TEMSO как лекарство от рассеянного склероза (РС). Исследование было завершено в июле 2010 года. [7] Результаты через 2 года были положительными. [8] Однако последующее прямое сравнительное исследование TENERE показало, что «хотя окончательное прекращение [терапии] было значительно реже среди пациентов с рассеянным склерозом, получавших терифлуномид, по сравнению с интерфероном бета-1а , рецидивы были более распространены при приеме терифлуномида». [9] Препарат был одобрен к применению в США в сентябре 2012 года. [10] [11] и для использования в Европейском Союзе в августе 2013 г. [5]
Побочные эффекты
[ редактировать ]США Информация о назначении Управления по контролю за продуктами и лекарствами предупреждает о потенциальной гепатотоксичности (повреждения печени, включая печеночную недостаточность) и тератогенности (врожденные дефекты). [12] Повышение уровня фермента АЛТ является наиболее частым побочным эффектом (≥10% и ≥2% по сравнению с плацебо). [12]
Механизмы действия
[ редактировать ]Терифлуномид — иммуномодулирующий препарат, ингибирующий синтез пиримидина de novo путем блокирования фермента дигидрооротатдегидрогеназы . Неясно, объясняет ли это его влияние на поражения рассеянного склероза. [13]
Терифлуномид ингибирует быстро делящиеся клетки, включая активированные Т-клетки, которые, как полагают, управляют болезненным процессом при рассеянном склерозе. Терифлуномид может снизить риск инфекций по сравнению с химиотерапевтическими препаратами из-за его более ограниченного воздействия на иммунную систему. [14]
Установлено, что терифлуномид блокирует транскрипционный фактор NF-κB . Он также ингибирует ферменты тирозинкиназы , но только в высоких дозах, которые не используются клинически. [15]
Активация лефлуномида в терифлуномид
[ редактировать ]Фирменный препарат терифлуномид является основным активным in vivo метаболитом генерически доступного лефлуномида. При введении лефлуномида 70% введенного препарата превращается в терифлуномид. Единственное различие между молекулами — раскрытие изоксазольного кольца. Это считается простой структурной модификацией и технически простым одноэтапным синтетическим преобразованием. При пероральном введении лефлуномида in vivo изоксазольное кольцо лефлуномида открывается и образуется терифлуномид. [16]

«Независимо от вводимого вещества (лефлуномид или терифлуномид), это одна и та же молекула (терифлуномид), оказывающая фармакологическое, иммунологическое или метаболическое действие с целью восстановления, коррекции или модификации физиологических функций, и не присутствующая при клиническом использовании. , новое химическое вещество для пациентов». [16] По этой причине EMA изначально не рассматривала терифлуномид как новое активное вещество. [19]
Ссылки
[ редактировать ]- ^ Перейти обратно: а б «Использование терифлуномида (Аубаджио) во время беременности» . Наркотики.com . 11 сентября 2019 года . Проверено 2 марта 2020 г.
- ^ «Список всех лекарств с предупреждениями о черном ящике, полученный FDA (используйте ссылки «Загрузить полные результаты» и «Просмотреть запрос»)» . nctr-crs.fda.gov . FDA . Проверено 22 октября 2023 г.
- ^ Анвиса (31 марта 2023 г.). «РДК № 784 – Списки наркотических средств, психотропных веществ, прекурсоров и других веществ, находящихся под особым контролем» [Постановление Коллегии № 784 – Списки наркотических средств, психотропных веществ, прекурсоров и других веществ, находящихся под особым контролем» (на бразильском португальском языке). Официальный вестник Союза (опубликован 4 апреля 2023 г.). Архивировано из оригинала 3 августа 2023 года . Проверено 16 августа 2023 г.
- ^ «Аубагиотерифлуномид таблетка, покрытая пленочной оболочкой» . ДейлиМед . 21 ноября 2023 г. Проверено 13 июня 2024 г.
- ^ Перейти обратно: а б «Аубаджио ЭПАР» . Европейское агентство лекарственных средств (EMA) . 26 августа 2013 года . Проверено 13 июня 2024 г.
- ^ Магне Д., Мезин Ф., Палмер Г., Герн П.А. (ноябрь 2006 г.). «Активный метаболит лефлуномида, A77 1726, увеличивает пролиферацию синовиальных фибробластов человека в присутствии IL-1бета и TNF-альфа». Исследование воспаления . 55 (11): 469–75. дои : 10.1007/s00011-006-5196-x . ПМИД 17122964 . S2CID 47034503 .
- ^ Номер клинического исследования NCT00134563 «Исследование III фазы терифлуномида в снижении частоты рецидивов и накопления инвалидности у пациентов с рассеянным склерозом (TEMSO)» на сайте ClinicalTrials.gov.
- ^ «Терифлуномид компании Санофи-Авентис оказался козырем в двухлетнем исследовании III фазы рассеянного склероза» . Новости генной инженерии и биотехнологии . 15 октября 2010 г.
- ^ Гевер Дж. (4 июня 2012 г.). «Терифлуномид — скромная помощь, но безопасен для рассеянного склероза» . медицинская страница . Совместное заседание Консорциума центров рассеянного склероза и Американского комитета по лечению и исследованиям рассеянного склероза . Проверено 4 июня 2012 г.
- ^ «Упаковка одобренного препарата: таблетки аубаджио (терифлуномид), NDA № 202992» . США Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) . 5 ноября 2012 года . Проверено 1 марта 2020 г.
- ^ «FDA одобряет новый препарат для лечения рассеянного склероза — Обаджио» (пресс-релиз). США Управление по контролю за продуктами и лекарствами (FDA). Архивировано из оригинала 13 сентября 2012 года . Проверено 14 сентября 2012 г.
- ^ Перейти обратно: а б «Основная информация о назначении» (PDF) . Ассоциация пищевых продуктов и лекарств США . Проверено 24 февраля 2024 г.
- ^ Спрейцер Х (13 марта 2006 г.). «Новое действующее вещество – терифлуномид». Австрийская фармацевтическая газета (на немецком языке) (6/2006).
- ^ Фоллмер Т. (28 мая 2009 г.). «Терапия рассеянного склероза в разработке: терифлуномид». Новости EMS (28 мая 2009 г.).
- ^ Бридвелд, Дайер Дж. М. (ноябрь 2000 г.). «Лефлуномид: способ действия при лечении ревматоидного артрита» . Анналы ревматических болезней . 59 (11): 841–9. дои : 10.1136/ard.59.11.841 . ПМК 1753034 . ПМИД 11053058 .
- ^ Перейти обратно: а б Мельчиорри Д., ван Цвитен-Бут Б., Ромалдас М., Нела В., Карстен Б.С., Ян Х. и др. «Отчет об оценке. АУБАЖИО (международное непатентованное название: терифлуномид). Процедура № EMEA/H/C/002514/0000» (PDF) . Европейское агентство по лекарственным средствам . п. 119. Архивировано из оригинала (PDF) 17 июля 2015 года . Проверено 5 июня 2015 г.
- ^ Розман Б (2002). «Клиническая фармакокинетика лефлуномида». Клиническая фармакокинетика . 41 (6): 421–30. дои : 10.2165/00003088-200241060-00003 . ПМИД 12074690 . S2CID 33745823 .
- ^ «Обзор клинической фармакологии/биофармацевтики. Продукт: Арава (таблетки лефлуномида). Номер заявки: NDA 20905» (PDF) . США Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) . Проверено 15 апреля 2016 г.
- ^ «Краткое заключение (первоначальное разрешение): Абаджио (терифлуномид)» (PDF) . Европейское агентство лекарственных средств. Архивировано из оригинала (PDF) 13 марта 2016 года . Проверено 15 апреля 2016 г.