Полагать
 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Полагать | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Аллотропы | серебристо-белый, β (бета) ; серый, α (альфа) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Стандартный атомный вес A r ° (sn) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Олово в периодической таблице | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomic number (Z) | 50 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Group | group 14 (carbon group) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Period | period 5 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Block | p-block | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Electron configuration | [Kr] 4d10 5s2 5p2 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Electrons per shell | 2, 8, 18, 18, 4 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Physical properties | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Phase at STP | solid | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Melting point | 505.08 K (231.93 °C, 449.47 °F) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Boiling point | 2875 K (2602 °C, 4716 °F) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Density (at 20° C) | white (β): 7.289 g/cm3 gray (α): 5.770 g/cm3[3] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| when liquid (at m.p.) | 6.99 g/cm3 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Heat of fusion | white (β): 7.03 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Heat of vaporization | white (β): 296.1 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molar heat capacity | white (β): 27.112 J/(mol·K) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Vapor pressure
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomic properties | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Oxidation states | −4, −3, −2, −1, 0,[4] +1,[5] +2, +3,[6] +4 (an amphoteric oxide) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Electronegativity | Pauling scale: 1.96 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ionization energies |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomic radius | empirical: 140 pm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Covalent radius | 139±4 pm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Van der Waals radius | 217 pm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Other properties | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Natural occurrence | primordial | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Crystal structure | white (β): body-centered tetragonal (tI4) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Lattice constants | white (β): a = 583.13 pm c = 318.11 pm (at 20 °C)[3] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Crystal structure | gray (α): face-centered diamond-cubic (cF8) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Lattice constant | gray (α): a = 648.96 pm (at 20 °C)[3] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Thermal expansion | white (β): 21.76×10−6/K (at 20 °C)[a] gray (α): 5.20×10−6/K (at 20 °C)[3] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Thermal conductivity | 66.8 W/(m⋅K) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Electrical resistivity | 115 nΩ⋅m (at 0 °C) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Magnetic ordering | white (β): paramagnetic gray (α): diamagnetic[7] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molar magnetic susceptibility | white (β): +3.1×10−6 cm3/mol (298 K)[8] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Young's modulus | 50 GPa | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Shear modulus | 18 GPa | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Bulk modulus | 58 GPa | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Speed of sound thin rod | 2730 m/s (at r.t.) (rolled) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Poisson ratio | 0.36 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Mohs hardness | 1.5 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Brinell hardness | 50–440 MPa | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| CAS Number | 7440-31-5 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| History | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Discovery | protohistoric, around 35th century BC | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Symbol | "Sn": from Latin stannum | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Isotopes of tin | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Олово является химическим элементом ; Он имеет символ SN (от латинского Stannum ) и атомного числа 50. серебристый металл, олово достаточно мягкая, чтобы ее можно было разрезать с небольшим количеством силы, [ 10 ] и стержень с олова может быть согнут вручную с небольшим усилием. Когда согнут, так называемый « жестяной крик » можно услышать в результате двойника в жестяных кристаллах. [ 11 ]
Олово-это пост-трансферный металл в группе 14 периодической таблицы элементов. Он получен главным образом из минерального касситерита , который содержит оксид станинга , SNO
2 Олово показывает химическое сходство с обоими соседями в группе 14, Германия и свинца , и имеет два основных состояния окисления , +2 и немного более стабильный +4. TIN является 49 -м наиболее распространенным элементом на Земле, составляющий 0,00022% своей коры, и с 10 стабильными изотопами он имеет наибольшее количество стабильных изотопов в периодической таблице из -за его волшебного количества протонов.
It has two main allotropes: at room temperature, the stable allotrope is β-tin, a silvery-white, malleable metal; at low temperatures it is less dense grey α-tin, which has the diamond cubic structure. Metallic tin does not easily oxidize in air and water.
The first tin alloy used on a large scale was bronze, made of 1⁄8 tin and 7⁄8 copper (12.5% and 87.5% respectively), from as early as 3000 BC. After 600 BC, pure metallic tin was produced. Pewter, which is an alloy of 85–90% tin with the remainder commonly consisting of copper, antimony, bismuth, and sometimes lead and silver, has been used for flatware since the Bronze Age. In modern times, tin is used in many alloys, most notably tin-lead soft solders, which are typically 60% or more tin, and in the manufacture of transparent, electrically conducting films of indium tin oxide in optoelectronic applications. Another large application is corrosion-resistant tin plating of steel. Because of the low toxicity of inorganic tin, tin-plated steel is widely used for food packaging as "tin cans". Some organotin compounds can be extremely toxic.
Characteristics
[edit]Physical
[edit]
Tin is a soft, malleable, ductile and highly crystalline silvery-white metal. When a bar of tin is bent a crackling sound known as the "tin cry" can be heard from the twinning of the crystals.[11] This trait is shared by indium, cadmium, zinc, and mercury in its solid state. Tin melts at about 232 °C (450 °F), the lowest in group 14, and boils at 2,602 °C (4,716 °F), the second lowest (ahead of lead) in its group. The melting point is further lowered to 177.3 °C (351.1 °F) for 11 nm particles.[12][13]
| External videos | |
|---|---|
β-tin, also called white tin, is the allotrope (structural form) of elemental tin that is stable at and above room temperature. It is metallic and malleable, and has body-centered tetragonal crystal structure. α-tin, or gray tin, is the nonmetallic form. It is stable below 13.2 °C (55.8 °F) and is brittle. α-tin has a diamond cubic crystal structure, as do diamond and silicon. α-tin does not have metallic properties because its atoms form a covalent structure in which electrons cannot move freely. α-tin is a dull-gray powdery material with no common uses other than specialized semiconductor applications.[11] γ-tin and σ-tin exist at temperatures above 161 °C (322 °F) and pressures above several GPa.[14]
In cold conditions β-tin tends to transform spontaneously into α-tin, a phenomenon known as "tin pest" or "tin disease".[15] Some unverifiable sources also say that, during Napoleon's Russian campaign of 1812, the temperatures became so cold that the tin buttons on the soldiers' uniforms disintegrated over time, contributing to the defeat of the Grande Armée,[16] a persistent legend.[17][18][19]
The α-β transformation temperature is 13.2 °C (55.8 °F), but impurities (e.g. Al, Zn, etc.) lower it well below 0 °C (32 °F). With the addition of antimony or bismuth the transformation might not occur at all, increasing durability.[20]
Commercial grades of tin (99.8% tin content) resist transformation because of the inhibiting effect of small amounts of bismuth, antimony, lead, and silver present as impurities. Alloying elements such as copper, antimony, bismuth, cadmium, and silver increase the hardness of tin.[21] Tin easily forms hard, brittle intermetallic phases that are typically undesirable. It does not mix into a solution with most metals and elements so tin does not have much solid solubility. Tin mixes well with bismuth, gallium, lead, thallium and zinc, forming simple eutectic systems.[20]
Tin becomes a superconductor below 3.72 K[22] and was one of the first superconductors to be studied.[23] The Meissner effect, one of the characteristic features of superconductors, was first discovered in superconducting tin crystals.[23]
Chemical
[edit]Tin resists corrosion from water, but can be corroded by acids and alkalis. Tin can be highly polished and is used as a protective coat for other metals,[11] a protective oxide (passivation) layer prevents further oxidation.[24][25]
Isotopes
[edit]Tin has ten stable isotopes, the greatest number of any element. Their mass numbers are 112, 114, 115, 116, 117, 118, 119, 120, 122, and 124. Tin-120 makes up almost a third of all tin. Tin-118 and tin-116 are also common. Tin-115 is the least common stable isotope.[citation needed] The isotopes with even mass numbers have no nuclear spin, while those with odd mass numbers have a nuclear spin of 1/2. It is thought that tin has such a great multitude of stable isotopes because of tin's atomic number being 50, which is a "magic number" in nuclear physics.[citation needed]
Tin is one of the easiest elements to detect and analyze by NMR spectroscopy, which relies on molecular weight and its chemical shifts are referenced against tetramethyltin (SnMe
4).[b][26]
Of the stable isotopes, tin-115 has a high neutron capture cross section for fast neutron energies, at 30 barns. Tin-117 has a cross section of 2.3 barns, one order of magnitude smaller, while tin-119 has a slightly smaller cross section of 2.2 barns.[27] Before these cross sections were well known, it was proposed to use tin-lead solder as a reactor coolant for fast reactors because of its low melting point. Current studies are for lead or lead-bismuth reactor coolants because both heavy metals are nearly transparent to fast neutrons, with very low capture cross sections.[28] In order to use a tin or tin-lead coolant, the tin would first have to go through isotopic separation to remove the isotopes with odd mass number. Combined, these three isotopes make up about 17% of natural tin but represent nearly all of the capture cross section. Of the remaining seven isotopes tin-112 has a capture cross section of 1 barn. The other six isotopes forming 82.7% of natural tin have capture cross sections of 0.3 barns or less, making them effectively transparent to neutrons.[27]
Tin has 31 unstable isotopes, ranging in mass number from 99 to 139. The unstable tin isotopes have half-lives of less than a year except for tin-126, which has a half-life of about 230,000 years. Tin-100 and tin-132 are two of the very few nuclides with a "doubly magic" nucleus which despite being unstable, as they have very uneven neutron–proton ratios, are the endpoints beyond which tin isotopes lighter than tin-100 and heavier than tin-132 are much less stable.[29] Another 30 metastable isomers have been identified for tin isotopes between 111 and 131, the most stable being tin-121m, with a half-life of 43.9 years.[30]
The relative differences in the abundances of tin's stable isotopes can be explained by how they are formed during stellar nucleosynthesis. Tin-116 through tin-120, along with tin-122, are formed in the s-process (slow neutron capture) in most stars which leads to them being the most common tin isotopes, while tin-124 is only formed in the r-process (rapid neutron capture) in supernovae and neutron star mergers. Tin isotopes 115, 117 through 120, and 122 are produced via both the s-process and the r-process,[31] The two lightest stable isotopes, tin-112 and tin-114, cannot be made in significant amounts in the s- or r-processes and are among the p-nuclei whose origins are not well understood. Some theories about their formation include proton capture and photodisintegration. Tin-115 might be partially produced in the s-process, both directly and as the daughter of long-lived indium-115, and also from the decay of indium-115 produced via the r-process.[31][32]
Etymology
[edit]The word tin is shared among Germanic languages and can be traced back to reconstructed Proto-Germanic *tin-om; cognates include German Zinn, Swedish tenn and Dutch tin. It is not found in other branches of Indo-European, except by borrowing from Germanic (e.g., Irish tinne from English).[33][34]
The Latin name for tin, stannum, originally meant an alloy of silver and lead, and came to mean 'tin' in the fourth century[35]—the earlier Latin word for it was plumbum candidum, or "white lead". Stannum apparently came from an earlier stāgnum (meaning the same substance),[33] the origin of the Romance and Celtic terms for tin, such as French étain, Spanish estaño, Italian stagno, and Irish stán.[33][36] The origin of stannum/stāgnum is unknown; it may be pre-Indo-European.[37]
The Meyers Konversations-Lexikon suggests instead that stannum came from Cornish stean, and is evidence that Cornwall in the first centuries AD was the main source of tin.[citation needed]
History
[edit]
Извлечение и использование олова может быть датировано началом бронзового века около 3000 г. до н.э., когда было отмечено, что медные объекты, образованные из полиметаллических руд с различным содержанием металла, обладали разными физическими свойствами. [38] The earliest bronze objects had a tin or arsenic content of less than 2% and are believed to be the result of unintentional alloying due to trace metal content in the copper ore.[39] The addition of a second metal to copper increases its hardness, lowers the melting temperature, and improves the casting process by producing a more fluid melt that cools to a denser, less spongy metal.[39] Это было важное новшество, которое позволило для гораздо более сложных форм, отлитых в закрытых формах бронзового века. Бронзовые объекты мышьяка появляются первыми на Ближнем Востоке, где мышьяк обычно встречается с медной рудой, но риски для здоровья были быстро реализованы, и поиски источников гораздо менее опасных оловянных руд начались в начале бронзового века. [ 40 ] Это создало спрос на редкий оловянный металл и сформировал торговую сеть, которая связывала отдаленные источники олова с рынками культур бронзового века. [ Цитация необходима ]
Касситерит ( Sno
2 ), оксидная форма олова, была, скорее всего, исходным источником олова. Другие оловянные руды - это менее распространенные сульфиды, такие как станнит , которые требуют более вовлеченного процесса плавки . Касситерит часто накапливается в аллювиальных каналах в виде отложений трудного роста, потому что он сложнее, тяжелее и более устойчив к химически, чем сопровождающий гранит . [ 39 ] Касситерит обычно черный или темный цвет, и эти месторождения можно легко увидеть на берегах рек . Алкулиальные ( трудовой ) отложения могут быть случайно собираются и разделены методами, аналогичными панорамированию золота . [ 41 ]
Соединения и химия
[ редактировать ]В подавляющем большинстве своих соединений TIN имеет состояние окисления II или IV. Соединения, содержащие бивалентную олову, называются охраняемые , в то время как те, которые содержат тетравалентные олово, называются Станникс .
Неорганические соединения
[ редактировать ]Соединения галогенидов известны обоим состояниям окисления. Для SN (IV) все четыре галогеники хорошо известны: SNF 4 , SNCL 4 , SNBR 4 и SNI 4 . Три более тяжелых члена являются летучими молекулярными соединениями, тогда как тетрафлюрид является полимерным. Все четыре галогеники известны SN (II) также: SNF 2 , SNCL
2 , Snbr 2 и Sni 2 . Все полимерные твердые вещества. Из этих восьми соединений только йодиды окрашены. [ 42 ]
Олово (II) хлорид (также известный как растонный хлорид) является наиболее важным коммерческим галогеной. Иллюстрируя маршруты для таких соединений, хлор реагирует с помощью оловянного металла с получением SNCL 4, тогда как реакция соляной кислоты и олово производит SNCL
2 и водород газ. В качестве альтернативы SNCL 4 и SN объединяются с олово -хлоридом с помощью процесса, называемого комбо -штампором : [ 43 ]
- Sncl 4 + sn → 2 sncl
2
Олово может образовывать многие оксиды, сульфиды и другие халкогенидов производные . Диоксид Sno
2 (Касситерит) образуется, когда олово нагревается в присутствии воздуха . [ 42 ] Сно
2 является амфотерным , что означает, что он растворяется как в кислых, так и в основных растворах. [ 44 ] Станаты со структурой [ sn (OH)
6 ] 2− , как k
2 [ sn (OH)
6 ], также известны, хотя свободная становая кислота h
2 [ sn (OH)
6 ] неизвестно. [ Цитация необходима ]
Сульфиды олова существуют как в состояниях окисления +2 и +4: олово (II) сульфид и олово (IV) сульфид ( мозаичное золото ).

2 ) [ 45 ]
Гидриды
[ редактировать ]Стандарт ( SNH
4 ), с оловом в составе +4 окисления, нестабильна. Гидриды организма, однако, хорошо известны, например, гидрид трибутилтина (SN (C 4 H 9 ) 3 H). [ 11 ] Эти соединения выделяют переходные трибуловые оловянные радикалы, которые являются редкими примерами соединений олова (III). [ 46 ]
Соединения организма
[ редактировать ]организма Соединения , иногда называемые Stannanes, представляют собой химические соединения с оловянными углеродными связями. [ 47 ] Из оловянных соединений органические производные являются коммерчески наиболее полезными. [ 48 ] Некоторые органические соединения очень токсичны и использовались в качестве биоцидов . Первым соединением органотина, которое сообщалось, был диэтилтин -диодид ((C 2 H 5 ) 2 SNI 2 ), о котором сообщает Эдвард Франкленд в 1849 году. [ 49 ]
Большинство органических соединений - это бесцветные жидкости или твердые тела, которые являются стабильными для воздуха и воды. Они принимают тетраэдрическую геометрию. Соединения TetraAlcyl- и Tetraaryltin можно приготовлить с использованием реагентов Grignard : [ 48 ]
- Sncl
4 + 4 rmgbr → r
4 SN + 4 MGBRCL
Смешанные галогениды, которые являются более распространенными и более важными коммерчески, чем производные тетраоргано, готовятся реакциями перераспределения :
- Sncl
4 + р
4 sn → 2 sncl
2 r 2
Дивалентные соединения организма встречаются редко, хотя и более распространенными, чем родственные двухвалентные органогермании и органосиликонные соединения. Большая стабилизация, пользующаяся SN (II), объясняется « эффектом инертного пар ». Соединения органотина (II) включают как Stannylenes (формула: R 2 SN, как видно для синглетных карбенов ), так и дистанилен (R 4 SN 2 ), которые примерно эквивалентны алкенам . Оба класса демонстрируют необычную реакцию. [ 50 ]
Возникновение
[ редактировать ]
Олово генерируется с помощью длинного S -процесса в звездах массы низкого и среднего (с массами от 0,6 до 10 раз больше, чем у солнца ), и, наконец, бета-распадом тяжелых изотопов индиума . [ 51 ]
Олово является 49 -м наиболее распространенным элементом в коре Земли , представляющим 2 часа дня по сравнению с 75 ч / млн для цинка, 50 ч / млн для меди и 14 ч / млн для свинца. [ 52 ]
Олово не происходит как нативный элемент, но должен быть извлечен из различных руд. Касситерит ( Sno
2 ) является единственным коммерчески важным источником олова, хотя небольшие количества олова извлекаются из сложных сульфидов , таких как станнит , цилиндрит , франккеит , канфилфил и теллит . Минералы с оловом почти всегда ассоциируются с гранитной породой, обычно на уровне 1% содержания оксида олова. [ 53 ]
Из -за более высокой удельной тяжести диоксида олова около 80% добычей олова от вторичных отложений, обнаруженных ниже первичных ложан. Олово часто восстанавливается из гранул, промываемых вниз по течению в прошлом и осаждается в долинах или в море. Наиболее экономичными способами добычи добычи являются дноуглубительные работы , гидраулирование или открытые ямы . Большая часть мирового олова производится из отложений россыпения , которые могут содержать всего 0,015% олова. [ 54 ]
| Страна | Резервы |
|---|---|
| 1,500,000 | |
| 250,000 | |
| 310,000 | |
| 800,000 | |
| 590,000 | |
| 400,000 | |
| 350,000 | |
| 180,000 | |
| 170,000 | |
| Другой | 180,000 |
| Общий | 4,800,000 |
| Год | Миллион тонн |
|---|---|
| 1965 | 4,265 |
| 1970 | 3,930 |
| 1975 | 9,060 |
| 1980 | 9,100 |
| 1985 | 3,060 |
| 1990 | 7,100 |
| 2000 | 7,100 [ 55 ] |
| 2010 | 5,200 [ 55 ] |
В 2011 году было добыто около 253 000 тонн олова, в основном в Китае (110 000 т), Индонезии (51 000 т), Перу (34 600 т), Боливии (20 700 т) и Бразилии (12 000 т). [ 55 ] Оценки производства олова исторически варьировались в зависимости от рыночной и горнодобывающей технологии. Предполагается, что при текущих показателях потребления и технологий земля закончится из миной олова за 40 лет. [ 56 ] В 2006 году Лестер Браун предположил, что TIN может закончиться в течение 20 лет на основе консервативных оценок на 2% годового роста. [ 57 ]
Олово лома является важным источником металла. Восстановление олова за счет переработки быстро увеличивается с 2019 года. [ 58 ] В то время как Соединенные Штаты не добывали ни добычи (с 1993 года), ни выплачивали (с 1989 года) олова, это был крупнейший вторичный производитель, переработав почти 14 000 тонн в 2006 году. [ 55 ]
Новые месторождения сообщаются в Монголии , [ 59 ] А в 2009 году в Колумбии были обнаружены новые месторождения олова. [ 60 ]
Производство
[ редактировать ]Олово производится путем карботермического восстановления оксидной руды с помощью углерода или колы. как реверберационную печь , так и электрическую печь : Можно использовать [ 61 ] [ 62 ] [ 63 ]
- Sno 2 + c Sn + co 2 ↑
Добыча и плавка
[ редактировать ]Промышленность
[ редактировать ]Десять крупнейших компаний, производящих олово, производили большую часть мировой олова в 2007 году. [ Цитация необходима ]
Большая часть мирового олова торгуется на LME, из 8 стран, до 17 брендов. [ 64 ]
| Компания | Политинг | 2006 | 2007 | 2017 [ 66 ] | 2006–2017 % изменять |
|---|---|---|---|---|---|
| Юньнань Тин | Китай | 52,339 | 61,129 | 74,500 | 42.3 |
| Pt Timah | Индонезия | 44,689 | 58,325 | 30,200 | −32.4 |
| Малайзия плавичная корпорация | Малайзия | 22,850 | 25,471 | 27,200 | 19.0 |
| Юньнан Ченгфенг | Китай | 21,765 | 18,000 | 26,800 | 23.1 |
| Минсур | Перу | 40,977 | 35,940 | 18,000 | −56.1 |
| Винто | Боливия | 11,804 | 9,448 | 12,600 | 6.7 |
| Гуанси Китай олова | Китай | / | / | 11,500 | / |
| Thaisarco | Таиланд | 27,828 | 19,826 | 10,600 | −61.9 |
| Металло-химический | Бельгия | 8,049 | 8,372 | 9,700 | 20.5 |
| Гедзиу Зи Ли | Китай | / | / | 8,700 | / |
Международный совет олова был создан в 1947 году для контроля цены на олово. Он рухнул в 1985 году. В 1984 году была создана Ассоциация стран -продюсирующих стран, с Австралией, Боливией, Индонезией, Малайзией, Нигерией, Таиландом и Заиром в качестве членов. [ 67 ]
Цена и обмены
[ редактировать ]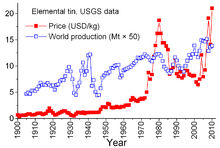
TIN уникален среди минеральных товаров из -за сложных соглашений между странами -производителями и странами -потребителями, начиная с 1921 года. Ранее соглашения, как правило, были несколько неформальными и привели к «Первому международному соглашению» в 1956 году, первое из серии, которые эффективно разрушились В 1985 году. Благодаря этим соглашениям Международный совет олова (ITC) оказал значительное влияние на цены на олова. ITC поддержал цену олова в течение периодов низких цен, покупая олово за запасы буфера и смог сдерживать цену в течение периодов высоких цен, продавая с запас. Это был подход по борьбе с бесстрашным рынком, предназначенный для обеспечения достаточного потока олова в потребительские страны и прибыль для стран-производителей. Тем не менее, запас буфера не был достаточно большим, и в течение большинства из этих 29 лет цены на олова выросли, иногда резко, особенно с 1973 по 1980 год, когда безудержная инфляция преследовала многие мировые экономики. [ 68 ]
В конце 1970 -х и начале 1980 -х годов США сократили свой стратегический запас олова, отчасти, чтобы воспользоваться исторически высокими ценами на олова. Рецессия 1981–82 гг. Повреяла оловянную промышленность. Потребление олова резко снизилось. ITC смог избежать действительно крутого снижения за счет ускоренной покупки для своего буферного запаса; Это занятие требовало обширных заимствований. ITC продолжал заимствовать до конца 1985 года, когда он достиг своего кредитного лимита. Сразу же последовал крупный «жестяной кризис» - Tin был исключен из переживания на обмене лондонской металлической биржей в течение около трех лет. Вскоре после этого ITC растворилась, и цена на олово, которая сейчас находится в среде свободного рынка, упала до 4 долларов за фунт и осталась на этом уровне до 1990-х годов. [ 68 ] Цена снова увеличилась к 2010 году с восстановлением потребления после экономического кризиса 2007–2008 гг. , Сопутствующим пополнением и дальнейшим ростом потребления. [ 55 ]

London Metal Exchange (LME) является основным торговым сайтом TIN. [ 55 ] Другими рынками жестяных контрактов являются рынок олова Куала -Лумпур (KLTM) и Индонезийский оловянный обмен (inatin). [ 69 ]
Из -за факторов, связанных с глобальным кризисом в цепочке поставок 2021 года , цены на олова почти удвоились в течение 2020–21 года и имели самый большой ежегодный рост за 30 лет. Глобальное рафинированное потребление олова упало на 1,6 процента в 2020 году, поскольку пандемия Covid-19 нарушила глобальную производственную отрасль. [ 70 ]
Приложения
[ редактировать ]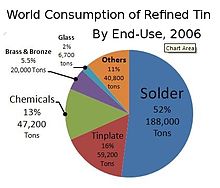
В 2018 году чуть менее половины всех произведенных олова использовалась в приповке. Остальное было разделено между оловянным покрытием, оловянными химическими веществами, латуниными и бронзовыми сплавами и нишевым использованием. [ 71 ]
Пигменты
[ редактировать ]Пигмент желтый 38, олово (IV) сульфид , известен как мозаичное золото . [ 72 ]
Фиолетовый из Кассия , пигмент Red 109, водный двойник золота , был главным образом с точки зрения живописи, ограниченной миниатюрами из -за его высокой стоимости. Это широко использовалось для изготовления клюквенного стекла . Он также использовался в искусстве для окрашивания фарфора . [ 73 ]
Желтый свинцовый тинет (который встречается в двух желтых формах- Stannate и силикат ) был пигментом , который исторически очень важен для живописи масла и который использовал в фреске в его силикатной форме. [ 74 ] Странно -свинец также известен в оранжевой форме, но не видел широкого использования в изобразительном искусстве. Он доступен для покупки в форме пигмента у поставщиков специализированных художников. Существует еще одна незначительная форма, с точки зрения художественного использования и доступности, желтого свинца, известного как сурьма свинцового тина . [ Цитация необходима ]
Cerulean Blue, несколько скучный голубой, химически известный как кобальт -Станнат, продолжает оставаться важным пигментом художников. Его оттенок похож на окрашивание марганцевого пигмента синего, пигментного синего 33, хотя ему не хватает красочности и более непрозрачна. [ 75 ] Художники, как правило, должны выбирать между кобальтовым Stannate и Manganese Blue имитациями, приготовленными с фталоцианиновым голубым оттенком (Pigment Blue 15: 3), поскольку промышленное производство марганцевого синего пигмента прекратилось в 1970 -х годах. [ 76 ] Однако Cerulean Blue, сделанный из Cobalt Stannate, был популярен среди художников до производства марганца Blue. [ Цитация необходима ]
Pigment Red 233, широко известный как Pinkcolor или Potter's Pink и точнее, точно известный как Chrome Tin Pink Sphene, является исторически важным пигментом в акварели . [ 77 ] Тем не менее, это получило большое возрождение популярности из-за интернет-из уст в уста . Он полностью легкий и химически стабильный как в масляных красках, так и в акварели. Другие неорганические смешанные металлические комплексные пигменты, произведенные с помощью кальцинирования , часто имеют олово в качестве компонента. Эти пигменты известны своей легкой постоянностью , погодными условиями, химической стабильностью, отсутствием токсичности и непрозрачности . Многие довольно скучно с точки зрения красота. Тем не менее, некоторые обладают достаточной красовой, чтобы быть конкурентоспособными для случаев использования, которые требуют более умеренного количества. Некоторые ценят за другие качества. Например, Pinkcolor выбирается многими аквалористами за его сильную грануляцию , хотя его хрома низкая. Недавно NTP Yellow ( пирохлор ) был выведен на рынок в качестве нетоксичной замены хромата свинца (II) с большей непрозрачностью, светостойкостью и устойчивостью к выветриванию, чем предлагаемые органические заместительные свинцовые хроматы. [ 78 ] NTP Yellow обладает самым высоким уровнем насыщения цветов этих современных неорганических смешанных металлических комплексных пигментов. Больше примеров этой группы включают пигментный желтый 158 (оловянный ванадий желтый касситерит ), [ 79 ] Пигмент желтый 216 (солаплекс желтый), [ 80 ] Пигмент желтый 219 ( титановая цинковая сурьмата Станнат ), [ 81 ] Пигментный оранжевый 82 (оксид оксида цинка олова, также известный как Sicopal Orange), [ 82 ] Pigment Red 121 (также известный как оловянный фиолетовый и хром -станов), [ 83 ] Пигмент красный 230 (хромированная глиноземная глинория Pink Corundum ), [ 84 ] Пигмент красный 236 (хромированная олова касситерит ), [ 85 ] и пигмент черный 23 (оловянная сурьма серая касситерит). [ 86 ] Еще один синий пигмент с оловом и кобальтом - пигмент синий 81, кобальтовая оловянная глиноземная алюминия . [ Цитация необходима ]
Пигмент белый 15, оксид олова (IV), используется для его переливки , чаще всего в виде керамической глазурьи . [ 87 ] Не существует зеленых пигментов, которые использовались художниками, которые имеют олово в качестве составляющих и пурпурных пигментов с оловом, классифицируются как красные, согласно Index Index Index . [ Цитация необходима ]
Припаяна
[ редактировать ]
Олово давно использовалась в сплавах с свинцом в качестве припоя , в размере от 5 до 70% мас./Мас. Олово с свинцом образует эвтектическую смесь при доле веса 61,9% олова и 38,1% свинца (атомная доля: 73,9% олова и 26,1% свинца) с температурой плавления 183 ° C (361,4 ° F). Такие припоя в основном используются для соединения труб или электрических цепей . Поскольку Европейское союз отходов отходов и директива электронного оборудования (Директива WEEE) и ограничение Директивы о опасных веществах вступило в силу 1 июля 2006 года, содержание свинца в таких сплавах уменьшилось. В то время как воздействие свинца связано с серьезными проблемами со здоровьем , припой без свинца не без проблем, включая более высокую температуру плавления и формирование оловянных усов , которые вызывают электрические проблемы. Tin Pest может возникнуть в припоре без свинца, что приводит к потере припакованного сустава. Заменяющие сплавы находятся, но проблемы солидной целостности остаются. [ 88 ] Обычный сплав без свинца составляет 99% олова, 0,7% меди и 0,3% серебра, с температурой плавления 217 ° C (422,6 ° F). [ 89 ]
Оловянное покрытие
[ редактировать ]
Оловянные связи легко с железом и используются для покрытия свинца , цинка и стали для предотвращения коррозии. Стальные контейнеры с осторожностью (или жестяные) широко используются для сохранения продуктов питания , и это составляет большую часть рынка для металлической олова. Канистра для сохранения продуктов питания была впервые изготовлена в Лондоне в 1812 году. [ 90 ] Спикеры британского английского называют такие контейнеры «банками», в то время как докладчики из нас, английский, называют их « банками » или «жестяными банками». Одним из выводов такого использования является сленговый термин « Тинни » или «жестяной», что означает «банка пива» в Австралии. Оловянный свисток называется так, потому что он был первым производством в стали с жестяной передачей. [ 91 ] [ 92 ]
Медные кулинарные сосуды, такие как кастрюля и сковороды, часто выровняются с тонким покрытием олова, гальванизацией или традиционными химическими методами, поскольку использование медной посуды с кислыми продуктами может быть токсичным. [ Цитация необходима ]
Специализированные сплавы
[ редактировать ]

Олово в сочетании с другими элементами образует широкий спектр полезных сплавов. Олово чаще всего лежит с медной. Оловянка составляет 85–99% олова, [ 93 ] и металл, содержащий подшипник , также имеет высокий процент олова. [ 94 ] [ 95 ] Бронза в основном медь с 12% оловой, в то время как добавление фосфора дает фосфориную бронзу . Bell Metal также представляет собой сплав меди -тин, содержащий 22% олова. Олово иногда использовалась в монете; Однажды он сформировал однозначный процент (обычно пять процентов или менее) американских копейки. [ 96 ] и канадский [ 97 ]
Соединение Niobium 3 –TIN NB критической SN коммерчески используется в катушках сверхпроводящих магнитов для его высокой температуры (18 К) и критического магнитного поля (25 т ). Сверхпроводящий магнит весом всего лишь два килограмма способен производить магнитное поле обычного электромагнитного взвешивания тонн. [ 98 ]
Небольшой процент олова добавляется в сплавы циркония для оболочки ядерного топлива. [ 99 ]
Большинство металлических труб в трубном органе имеют сплав оловянного/свинца, с 50/50 в качестве наиболее распространенной композиции. Доля олова в трубе определяет тон трубы, поскольку TIN имеет желательный тональный резонанс. Когда сплав оловянного/свинца охлаждается, сначала затвердевает свинцовая фаза, затем, когда температура эвтектики достигается, оставшаяся жидкость образует слоистую эвтектическую структуру с олова/свинцом, которая блестящая; Контраст с фазой свинца дает пятнистый или пятнистый эффект. Этот металлический сплав называется пятнистым металлом. Основные преимущества использования олова для труб включают его внешний вид, работоспособность и сопротивление коррозии. [ 100 ] [ 101 ]
Производство химикатов
[ редактировать ]Соединения олова используются при производстве различных химических веществ, включая стабилизаторы для ПВХ и катализаторов для промышленных процессов. Олово в форме слитков обеспечивает сырье, необходимое для этих химических реакций, обеспечивая постоянное качество и производительность. [ Цитация необходима ]
Оптоэлектроника
[ редактировать ]Оксиды индий и олова являются электрически проводящими и прозрачными, и используются для производства прозрачных электрически проводящих пленок с применениями в оптоэлектронических устройствах, таких как жидкокристаллические дисплеи . [ 102 ]
Другие приложения
[ редактировать ]
Петанная оловянная сталь, также называемая пронзительной оловой, представляет собой ремесленную технику, происходящую в Центральной Европе для создания функциональных и декоративных домохозяйств. Декоративные пронзительные дизайны существуют в широком разнообразии, основываясь на местных традициях и ремесленнике. Парные оловянные фонари являются наиболее распространенным применением этой техники ремесленника. Свет свечи, сияющего сквозь пирсинговый дизайн, создает декоративный световой рисунок в комнате, где она сидит. Фонари и другие перфорированные оловянные статьи были созданы в Новом Свете из самого раннего европейского поселения. Хорошо известным примером является «Реверевый фонарь», названный в честь Пола Ревера . [ 103 ]
В Америке сейфы и сейфы пищевых продуктов использовались за несколько дней до охлаждения. Это были деревянные шкафы различных стилей и размеров - либо пола стояли, либо подвесные шкафы, предназначенные для отговора паразитов и насекомых и не добывать пыли от скоропортящихся продуктов питания. Эти шкафы имели вставки для оловянной пластины в дверях, а иногда и по бокам, выбитые домовладельцем, шкафом или штифтом в различных конструкциях, чтобы обеспечить циркуляцию воздуха при исключении мух. Современные размножения этих статей остаются популярными в Северной Америке. [ 104 ]
Оконное стекло чаще всего производится с помощью плавающего расплавленного стекла на расплавленном олова ( поплавковое стекло ), что приводит к плоской и безупречной поверхности. Это также называется « процесс Пилкингтона ». [ 105 ]
Олово используется в качестве отрицательного электрода в усовершенствованных литий-ионных батареях . Его применение несколько ограничено тем фактом, что некоторые оловянные поверхности [ который? ] Катализация разложения электролитов на основе карбоната, используемых в литий-ионных батареях. [ 106 ]
Олово (II) фторид добавляется в некоторые продукты стоматологической помощи [ 107 ] в качестве оловористого фторида (SNF 2 ). Олово (II) фторид может быть смешан с абразивов кальциевыхвик , в то время как более распространенный фторид натрия постепенно становится биологически неактивным в присутствии кальциевых соединений. [ 108 ] Также было показано, что он более эффективен, чем фторид натрия при контроле гингивита . [ 109 ]
Олово используется в качестве цели для создания лазерной плазмы , которые действуют как источник света для экстремальной ультрафиолетовой литографии . [ 110 ]
Соединения организма
[ редактировать ]Соединения организма - это органометаллические соединения, содержащие жестяные связи. Всемирное промышленное производство органических соединений, вероятно, превышает 50 000 тонн . [ 111 ]
Стабилизаторы ПВХ
[ редактировать ]Основное коммерческое применение органических соединений заключается в стабилизации ПВХ -пластиков. В отсутствие таких стабилизаторов ПВХ быстро разлагается под жаром, светом и атмосферным кислородом, что приведет к обесцвеченным, хрупким продуктам. Оловянные хлорида лабила (CL ионы − ), который в противном случае лишил бы HCL из пластикового материала. [ 112 ] Типичными оловянными соединениями являются производные карбоновой кислоты дибутилтина дихлорида, таких как дибутиллин дилаурат . [ 113 ]
Биоциды
[ редактировать ]Некоторые органические соединения являются относительно токсичными, как с преимуществами, так и проблемами. Они используются для биоцидных свойств в качестве фунгицидов , пестицидов , альгаецидов , консервантов по дереву и антипрокативных агентов . [ 112 ] Оксид трибутилтина используется в качестве консерванта из дерева . [ 114 ] Tributyltin используется для различных промышленных целей, таких как контроль слизи на бумажных фабриках и дезинфекция циркулирующих промышленных охлаждающих вод. [ 115 ] Твибутилтин использовали в качестве добавки для судовой краски для предотвращения роста загрязненных организмов на кораблях, при этом использование снижалось после того, как соединения органических соединений были признаны как постоянные органические загрязнители с высокой токсичностью для некоторых морских организмов (например, собака , например). [ 116 ] ЕС запретил использование органических соединений в 2003 году, [ 117 ] В то время как опасения по поводу токсичности этих соединений с морской жизнью и повреждением воспроизводства и роста некоторых морских видов [ 112 ] (В некоторых сообщениях описывается биологические эффекты морской жизни на концентрации 1 нанограммы на литр) привели к мировому запрету международной морской организацией . [ 118 ] Многие страны в настоящее время ограничивают использование органических соединений на сосудам более 25 м (82 фута) длиной. [ 112 ] Постоянство трибутиллина в водной среде зависит от природы экосистемы. [ 119 ] Из -за этой устойчивости и его использования в качестве добавки в корабельной краске, высокие концентрации трибутилтина были обнаружены в морских отложениях, расположенных недалеко от военно -морских доков. [ 120 ] Tributyltin использовался в качестве биомаркера для Inposex у неогастропод , с не менее 82 известными видами. [ 121 ] С высоким уровнем TBT в местных прибрежных районах, из -за транспортных средств, моллюски оказали неблагоприятное действие. [ 119 ] INPOSEX - это навязывание мужских сексуальных характеристик на женских образцах, где они выращивают пенис и паллиальные VAS -оторван . [ 121 ] [ 122 ] Высокий уровень TBT может повредить эндокринные железы млекопитающих , репродуктивные и центральные нервные системы , структуру кости и желудочно -кишечный тракт . [ 122 ] Мало того, что трибултин влияет на млекопитающих, он влияет на морские выдры, китов, дельфинов и людей. [ 122 ]
Органическая химия
[ редактировать ]Некоторые оловянные реагенты полезны в органической химии . В крупнейшем применении хлорид -улово -кастрюли является распространенным восстановительным агентом для преобразования нитро и оксим групп в амины . Реакция STILE объединяет органические соединения с органическими галогениками или псевдогалидами . [ 123 ]
Литий-ионные батареи
[ редактировать ]Олово образует несколько межметаллических фаз с литием-металлом, что делает его потенциально привлекательным материалом для применений аккумулятора. Большое объемное расширение олова при легировании литиевым и нестабильностью границы раздела олово-органического электролита при низких электрохимических потенциалах является наибольшей проблемой для занятости в коммерческих ячеек. [ 124 ] TIN-межметаллическое соединение с кобальтом и углеродом было реализовано Sony в ее клетках Nexelion, высвобождаемых в конце 2000-х годов. Состав активного материала составляет приблизительно SN 0,3 CO 0,4 C 0,3 . Исследования показали, что только некоторые кристаллические аспекты тетрагональной (бета) SN ответственны за нежелательную электрохимическую активность. [ 125 ]
Меры предосторожности
[ редактировать ]Случаи отравления из жестяного металла, его оксидов и его солей почти неизвестны. С другой стороны, определенные органические соединения почти так же токсичны, как цианид . [ 48 ]
Воздействие олова на рабочем месте может происходить при вдыхании, контакте с кожей и зрительным контактом. США Управление по безопасности и гигиене труда (OSHA) установило допустимый предел воздействия для воздействия олова на рабочем месте как 2 мг/м 3 За 8 часов рабочего дня. Национальный институт безопасности и гигиены труда (NIOSH) определил рекомендуемый предел воздействия (REL) 2 мг/м. 3 За 8 часов рабочего дня. На уровнях 100 мг/м 3 Олово сразу же опасна для жизни и здоровья . [ 126 ]
Смотрите также
[ редактировать ]- Cassiterides (мифические жестяные острова)
- Стэннари
- Тупой
- Оловянный вредитель
- Майнинга олова в Британии
- Пенни
- Whisker (металлургия) (жестяные усы)
Примечания
[ редактировать ]- ^ Тепловое расширение β-SN является анизотропным : параметры (при 20 ° C) для каждой оси кристаллов α A = 16,19 × 10 −6 /K, α C = 32,89 × 10 −6 /K и α среднее = α v /3 = 21,76 × 10 −6 /K. [ 3 ]
- ^ Только водород, фтор, фосфор, таллий и ксенон легче использовать ЯМР -анализ с образцами, содержащими изотопы, при их естественной изобилии.
Ссылки
[ редактировать ]- ^ «Стандартные атомные веса: олово» . Ciaaw . 1983.
- ^ Прохаска, Томас; Irrgeher, Johanna; Благосостояние, Жаклин; Böhlke, John K.; Чессон, Лесли А.; Коплен, Тайлер Б.; Ding, наконечник; Данн, Филипп Дж.Х.; Грёнинг, Манфред; Холден, Норман Э.; Meijer, Harro AJ (4 мая 2022 г.). «Стандартные атомные веса элементов 2021 (технический отчет IUPAC)» . Чистая и прикладная химия . doi : 10.1515/pac-2019-0603 . ISSN 1365-3075 .
- ^ Jump up to: а беременный в дюймовый и Arblaster, John W. (2018). Выбранные значения кристаллографических свойств элементов . Материал Парк, штат Огайо: ASM International. ISBN 978-1-62708-155-9 .
- ^ «Новый тип составного соединения с нулевым валентным оловом» . Химия Европа . 27 августа 2016 года.
- ^ "HSN" . NIST Chemistry Webbook . Национальный институт стандартов и технологий . Получено 2013-01-23 .
- ^ "SNH3" . NIST Chemistry Webbook . Национальное учреждение стандартов и технологий . Получено 2013-01-23 .
- ^ Lide, Dr, ed. (2005). «Магнитная восприимчивость элементов и неорганических соединений». Справочник по химии и физике CRC (PDF) (86 -е изд.). Boca Raton (FL): CRC Press. ISBN 0-8493-0486-5 .
- ^ Weast, Robert (1984). CRC, Справочник по химии и физике . Boca Raton, Florida: Publishing Company Chemical Rubber Company. с. E110. ISBN 0-8493-0464-4 .
- ^ Kondev, FG; Ван, М.; Хуан, WJ; Naimi, S.; Audi, G. (2021). «Оценка ядерных свойств Nubase2020» (PDF) . Китайская физика c . 45 (3): 030001. DOI : 10.1088/1674-1137/Abddae .
- ^ Грей, Теодор (2007). «Жесткие изображения» . Элементы . Черная собака и левенталь.
- ^ Jump up to: а беременный в дюймовый и Холмен, Арнольд Ф.; Wiberg, Egon; Wiberg, Nils (1985). "Олово". Учебник неорганической химии (на немецком языке) (91–100 изд.). Уолтер де Грютер. С. ISBN 978-3-11-007511-3 .
- ^ «Чернила с оловянными наночастицами могут печатать будущие платы в кругах» . Phys.org . 12 апреля 2011 года. Архивировано с оригинала 16 сентября 2011 года.
- ^ Джо, Юн Хван; Юнг, Ино; Чой, Чунг Сок; Ким, Инюнг; Lee, Hyuck Mo (2011). «Синтез и характеристика низкотемпературных наночастиц SN для изготовления высокопроводных чернил». Нанотехнология . 22 (22): 225701. Bibcode : 2011nanot..22V5701J . doi : 10.1088/0957-4484/22/22/225701 . PMID 21454937 . S2CID 25202674 .
- ^ Molodets, Am; Набатов, С.С. (2000). «Термодинамические потенциалы, диаграмма состояния и фазовые переходы TIN при сжатии удара». Высокая температура . 38 (5): 715–721. Bibcode : 2000htemp..38..715m . doi : 10.1007/bf02755923 . S2CID 120417927 .
- ^ «Тин -вредители | Центр передового инженера жизненного цикла» . Calce.umd.edu . Получено 2022-11-04 .
- ^ Ле Курер, Пенни; Burreson, Jay (2004). Кнопки Наполеона: 17 молекул, которые изменили историю . Нью -Йорк: Penguin Group, США.
- ^ Öhrström, Lars (2013). Последний алхимик в Париже . Оксфорд: издательство Оксфордского университета. ISBN 978-0-19-966109-1 .
- ^ Коттон, Саймон (29 апреля 2014 г.). «Обзор книги: последний алхимик в Пари» . Мир химии . Королевское общество химии . Архивировано из оригинала 10 августа 2014 года . Получено 22 ноября 2019 года .
- ^ Эмсли, Джон (1 октября 2011 г.) [2001]. Строительные блоки природы: руководство AZ по элементам (новое изд.). Нью -Йорк, США: издательство Оксфордского университета . п. 552. ISBN 978-0-19-960563-7 Полем
Только офицеры были металлические пуговицы, и они были сделаны из латуни.
- ^ Jump up to: а беременный Шварц, Мел (2002). «Олово и сплавы, свойства». Энциклопедия материалов, деталей и отделки (2 -е изд.). CRC Press. ISBN 978-1-56676-661-6 .
- ^ «Оловянные сплавы - характеристики и используют» . Ядерная энергетика . Получено 2022-11-04 .
- ^ Dehaas, W.; Deboer, J.; Ванденберг, Г. (1935). «Электрическая устойчивость кадмия, таллий и олова при низких температурах». Физика . 2 (1–12): 453. Bibcode : 1935phy ..... 2..453d . doi : 10.1016/s0031-8914 (35) 90114-8 .
- ^ Jump up to: а беременный Meissner, W.; Р. Охсенфельд (1933). «Новый эффект, когда возникает надлежащая проводимость». Естественные науки . 21 (44): 787–788. Bibcode : 1933nw ..... 21..787m . Doi : 10.1007/bf01504252 . S2CID 37842752 .
- ^ Крейг, Брюс Д.; Андерсон, Дэвид С.; International, ASM (январь 1995 г.). Справочник по данным коррозии . ASM International. п. 126. ISBN 978-0-87170-518-1 Полем Архивировано с оригинала 2016-05-11.
- ^ Крутчлоу, Шарлотта (25 июня 2021 года). «Олово-формирование о элементе олова | периодическая таблица» . Chemtalk . Получено 2022-11-04 .
- ^ «Интерактивная частотная карта ЯМР» . Архивировано из оригинала 2011-06-04 . Получено 2009-05-05 .
- ^ Jump up to: а беременный Сирс, Варли Ф. (январь 1992 г.). «Длина рассеяния нейтронов и поперечные сечения» . Neutron News . 3 (3): 26–37. doi : 10.1080/10448639208218770 . ISSN 1044-8632 . Таблица поперечных сечений, доступная на NIST: длина рассеяния нейтронов и поперечные сечения .
- ^ «Westinghouse Nuclear> Energy Systems> Быстрый реактор с охлаждением, охлаждаемые свинцом» .
- ^ Уокер, Фил (1994). «Вдвойной магическое открытие олова-100». Мир физики . 7 (июнь): 28. doi : 10.1088/2058-7058/7/6/24 .
- ^ Audi, Жорж; Берсильон, Оливье; Блахто, Джин; Wapstra, Aaldert Hendrik (2003), «Оценка n Ubase ядерных и распадных свойств» , Ядерная физика A , 729 : 3–128, Bibcode : 2003nupha.729 .... 3a , doi : 10.1016/j.nuclphysa.2003.11 .001
- ^ Jump up to: а беременный Браганьи, Алессандро; Вомбахер, Фрэнк; Кирченбаур, Мария; Braukmüller, Ninja; Мюнкер, Карстен (2023). «Массозазависимое фракционирование SN и радиогенное 115SN в хондритах и наземных породах». Geochimica et Cosmochimica Acta . 344 : 40–58. doi : 10.1016/j.gca.2023.01.014 .
- ^ Cameron, AGW (1973). «Обилие элементов в солнечной системе» (PDF) . Обзоры космических наук . 15 (1): 121–146. Bibcode : 1973ssrv ... 15..121c . doi : 10.1007/bf00172440 . S2CID 120201972 . Архивировано из оригинала (PDF) 2011-10-21.
- ^ Jump up to: а беременный в "Олово" . Оксфордский английский словарь (онлайн изд.). Издательство Оксфордского университета . (Требуется членство в учреждении или участвующее учреждение .)
- ^ Харпер, Дуглас. "Олово" . Онлайн этимологический словарь .
- ^ Encyclopædia Britannica, 11th Edition , 1911, SV ' Tin ', цитируя H. Kopp
- ^ «Древняя добыча олова» . Oxleigh.freeserve.co.uk . Архивировано из оригинала на 2009-04-03 . Получено 2009-07-07 .
- ^ Американское словарь наследия
- ^ Cierny, J.; Weisgerber, G. (2003). «Оловянные шахты бронзового века в Центральной Азии». В Giumlia-mair, A.; Lo Schiavo, F. (eds.). Проблема ранней олова . Оксфорд: археопресс. С. 23–31. ISBN 978-1-84171-564-3 .
- ^ Jump up to: а беременный в Penhallurick, Rd (1986). Олово в древности: его добыча и торговля во всем древнем мире с особой ссылкой на Корнуолл . Лондон: Институт металлов. ISBN 978-0-904357-81-3 .
- ^ Ламберг-Карловский, CC; Франклин, Алан Д.; Олин, Жаклин С.; Wertime, Theodore A. , eds. (Июль 1980). «Развитие использования оловянного и жестяного бронзе: некоторые проблемы». Поиск древнего олова . Тол. 21. Вашингтон, округ Колумбия: семинар, организованный Теодором А. Вертимамом и состоялся в Смитсоновском институте и Национальном бюро стандартов, Вашингтон, округ Колумбия, 14–15 марта 1977 года. С. 474. doi : 10.2307/3103162 . JSTOR 3103162 .
{{cite book}}:|journal=игнорируется ( помощь ) - ^ Dube, RK (сентябрь 2006 г.). «Взаимосвязь между золотом и оловом: историческая перспектива» . Золотой бюллетень . 39 (3): 103–113. doi : 10.1007/bf03215537 .
- ^ Jump up to: а беременный Холмен, Арнольд Фредерик; Wiberg, Egon (2001), Wiberg, Nils (ed.), Неорганическая химия , переведенная Иглсоном, Мэри; Брюер, Уильям, Сан -Диего/Берлин: Академическая Пресса/Де Грюйтер, ISBN 0-12-352651-5
- ^ Гринвуд, Норман Н .; Эрншоу, Алан (1997). Химия элементов (2 -е изд.). Баттерворт-Хейнеманн . ISBN 978-0-08-037941-8 . [ страница необходима ]
- ^ Тейлор, Ф. Шервуд (1942). Неорганическая и теоретическая химия (6 -е изд.). Хейнеман.
- ^ Леже, JM; Хейнс, Дж.; Атуф А. (1996). "Поведение высокого давления котуннитовых и пост-котуннитских фаз PBCL 2 и SNCL
2 . - ^ Гаур, DP; Srivastava, G.; Мехротра, RC (1973). «Органические производные от олова. Журнал неорганической и общей химии . 398 : 72. DOI : 10.1002/Zaac.19733980109 .
- ^ Elschenbroich, Christoph (2006). Organometallics (3 -й, полностью Rev. И расширенное изд.). Вейнхайм: Wiley-VCH. ISBN 3-527-29390-6 Полем OCLC 64305455 .
- ^ Jump up to: а беременный в Граф, Гюнтер Г. (15 июня 2000 г.). «Олово, жестяные сплавы и жестяные соединения». Энциклопедия промышленной химии Уллмана . Вейнхайм: Wiley-VCH. doi : 10.1002/14356007.a27_049 .
- ^ Тоунен, Сандер HL; Дилман, причастчик-ян; Ван Котен, Джерард (2004). «Синтетические аспекты тетраорганотинов и галогенидов органотина (IV)» (PDF) . Журнал органометаллической химии . 689 (13): 2145–2157. doi : 10.1016/j.jorganchem.2004.03.027 . HDL : 1874/6594 . S2CID 100214292 . Архивировано из оригинала (PDF) 2011-08-07 . Получено 2009-07-31 .
- ^ Пэн, Ян; Эллис, Бобби Д.; Ван, Синдинг; Феттингер, Джеймс С.; Power, PP (2009). «Обратимые реакции этилена с дистаннинами в условиях окружающей среды». Наука . 325 (5948): 1668–1670. Bibcode : 2009Sci ... 325.1668p . doi : 10.1126/science.1176443 . PMID 19779193 . S2CID 3011002 .
- ^ Шу, Фрэнк Х. (1982). Физическая вселенная: введение в астрономию . Университетские научные книги. С. 119 –121. ISBN 978-0-935702-05-7 .
- ^ Emsley 2001 , с. 124, 231, 449 и 503.
- ^ Jump up to: а беременный «Олово: от руды до слитки» . Международный исследовательский институт. 1991. Архивировано из оригинала на 2009-03-22 . Получено 2009-03-21 .
- ^ Сатфин, Дэвид М.; Сабин, Эндрю Э.; Рид, Брюс Л. (1 июня 1992 г.). Олово - Международные стратегические минералы. Отчет об инвентаре . Диана. п. 9. ISBN 978-0-941375-62-7 Полем Архивировано с оригинала 2016-04-28.
- ^ Jump up to: а беременный в дюймовый и фон глин Карлин, Джеймс Ф. младший. «Олово: статистика и информация» (PDF) . Геологическая служба США. Архивировано из оригинала 2008-12-06 . Получено 2008-11-23 .
- ^ Рейли, Майкл (26 мая 2007 г.). "Как долго это продлится?". Новый ученый . 194 (2605): 38–39. Bibcode : 2007newsc.194 ... 38r . doi : 10.1016/s0262-4079 (07) 61508-5 .
- ^ Браун, Лестер (2006). План B 2.0 . Нью -Йорк: WW Norton. п. 109. ISBN 978-0-393-32831-8 .
- ^ Алвес, Бруна (15 февраля 2024 г.). «Ежегодная рециркуляция олова США 2023» . Статиста . Получено 2024-06-23 .
- ^ Коваленко, VI; Yarmolyuk, VV (1995). «Эндогенные редкие металлические формирования и редкая металлогена металла в Монголии». Экономическая геология . 90 (3): 520. Bibcode : 1995ecgeo..90..520K . doi : 10.2113/gsecongeo.90.3.520 .
- ^ «Seminole Group Colombia обнаруживает высокую оловянную руду в джунглях Amazon» . Freepr101 PressRelease. Архивировано из оригинала 2014-08-26.
- ^ Schrader, George F.; Elshennawy, Ahmad K.; Дойл, Лоуренс Э. (июль 2000 г.). Производственные процессы и материалы . Общество инженеров из производства. ISBN 978-0-87263-517-3 Полем Архивировано с оригинала 2016-05-11.
- ^ Луи, Генри (1911). Металлургия олова . McGraw-Hill Book Company.
- ^ Кнорр, Клаус (1945). Олово под контролем . Издательство Стэнфордского университета. ISBN 978-0-8047-2136-3 Полем Архивировано с оригинала 2016-05-19.
- ^ "LME TIN BRANDS" . Itri.co.uk. Международный исследовательский институт. Архивировано из оригинала 2008-12-07 . Получено 2009-05-05 .
- ^ «Десять лучших компаний по производству олова» . itri.co.uk. Международный исследовательский институт. Архивировано из оригинала 2008-12-07 . Получено 2009-05-05 .
- ^ «Крупнейшие в мире продюсеры» . Баланс . 13 января 2019 года.
- ^ «Соглашение о создании Ассоциации стран -производителей олова [1984] ATS 10» . Австралийский институт юридической информации, Австралийская библиотека договоров .
- ^ Jump up to: а беременный Карлин, Джеймс Ф. младший (1998). «Значительные события, влияющие на цены на олова с 1958 года» (PDF) . USGS. Архивировано из оригинала (PDF) 2011-10-28.
- ^ «12 января Пемасаран Пердана Инатин» . 15 декабря 2011 года. Архивировано из оригинала 2012-04-26.
- ^ Дейли, Том (5 декабря 2021 г.). «Оловянный всплеск ухудшает проблемы цепочки поставок для электроники, солнечных и автострам» . Рейтер . Получено 2021-12-07 .
- ^ «Оловянный спрос на отказ - Международная ассоциация олова» . Mining.com . 18 октября 2019 года . Получено 2021-07-03 .
- ^ «Цвет художественной базы данных пигмента - пигмент желтый - py» . ремесленка . 2024 . Получено 2024-08-17 .
{{cite web}}: Cs1 maint: url-status ( ссылка ) - ^ «Цвет художественной базы данных пигмента - пигмент красный - PR» . ремесленка . 2024 . Получено 2024-08-17 .
{{cite web}}: Cs1 maint: url-status ( ссылка ) - ^ «Цвет художественной базы данных пигмента - пигмент желтый - py» . ремесленка . 2024 . Получено 2024-08-17 .
{{cite web}}: Cs1 maint: url-status ( ссылка ) - ^ «Цвет художественной базы данных пигмента - пигмент синий - PB» . ремесленка . 2024 . Получено 2024-08-17 .
{{cite web}}: Cs1 maint: url-status ( ссылка ) - ^ «Цвет художественной базы данных пигмента - пигмент синий - PB» . ремесленка . 2024 . Получено 2024-08-17 .
{{cite web}}: Cs1 maint: url-status ( ссылка ) - ^ «Цвет художественной базы данных пигмента - пигмент красный - PR» . ремесленка . 2024 . Получено 2024-08-17 .
{{cite web}}: Cs1 maint: url-status ( ссылка ) - ^ «Цвет художественной базы данных пигмента - пигмент желтый - py» . ремесленка . 2024 . Получено 2024-08-17 .
{{cite web}}: Cs1 maint: url-status ( ссылка ) - ^ «Цвет художественной базы данных пигмента - пигмент желтый - py» . ремесленка . 2024 . Получено 2024-08-17 .
{{cite web}}: Cs1 maint: url-status ( ссылка ) - ^ «Цвет художественной базы данных пигмента - пигмент желтый - py» . ремесленка . 2024 . Получено 2024-08-17 .
{{cite web}}: Cs1 maint: url-status ( ссылка ) - ^ «Цвет художественной базы данных пигмента - пигмент желтый - py» . ремесленка . 2024 . Получено 2024-08-17 .
{{cite web}}: Cs1 maint: url-status ( ссылка ) - ^ «Цвет художественной базы данных пигмента - пигмент оранжевый - По» . ремесленка . 2024 . Получено 2024-08-17 .
{{cite web}}: Cs1 maint: url-status ( ссылка ) - ^ «Цвет художественной базы данных пигмента - пигмент красный - PR» . ремесленка . 2024 . Получено 2024-08-17 .
{{cite web}}: Cs1 maint: url-status ( ссылка ) - ^ «Цвет художественной базы данных пигмента - пигмент красный - PR» . ремесленка . 2024 . Получено 2024-08-17 .
{{cite web}}: Cs1 maint: url-status ( ссылка ) - ^ «Цвет художественной базы данных пигмента - пигмент красный - PR» . ремесленка . 2024 . Получено 2024-08-17 .
{{cite web}}: Cs1 maint: url-status ( ссылка ) - ^ «Цвет художественной базы данных пигмента - пигмент черный - PBK» . ремесленка . 2024 . Получено 2024-08-17 .
{{cite web}}: Cs1 maint: url-status ( ссылка ) - ^ «Цвет художественной базы данных пигмента - пигмент белый - PW» . ремесленка . 2024 . Получено 2024-08-17 .
{{cite web}}: Cs1 maint: url-status ( ссылка ) - ^ Блэк, Харви (2005). «Вывод о свинсе из электроники» . Перспективы здоровья окружающей среды . 113 (10): A682–5. doi : 10.1289/ehp.113-a682 . PMC 1281311 . PMID 16203230 .
- ^ «Технический лист данных - свободный сплав с свинцом» (PDF) . RS онлайн . Получено 2023-06-18 .
- ^ Чайлдс, Питер (июль 1995 г.). «Сказка о жестяном человеке» . Образование в химии . Тол. 32, нет. 4. Королевское химическое общество . п. 92 Получено 2018-06-19 .
- ^ Контроль, олово под (1945). Олово под контролем . С. 10–15. ISBN 978-0-8047-2136-3 Полем Архивировано с оригинала 2016-05-31.
- ^ Группа по олову, Национальный исследовательский совет (США). Комитет по техническим аспектам критических и стратегических материалов (1970). Тенденции в использовании олова . С. 10–22. Архивировано с оригинала 2016-05-22.
- ^ Халл, Чарльз (1992). Оловянная . Osprey Publishing. С. 1–5. ISBN 978-0-7478-0152-8 .
- ^ Тормоза, Джеймс (2009). "Введение" . Анализ Баббита . Bibliobazaar, LLC. С. 1–2. ISBN 978-1-110-11092-6 .
- ^ Уильямс, Роберт С. (2007). Принципы металлографии . Читать книги. С. 46–47. ISBN 978-1-4067-4671-6 .
- ^ «Композиция цента» . США монетный двор. Архивировано из оригинала 2011-10-25 . Получено 2011-10-28 .
- ^ «Композиция канадских монет» (PDF) . Канадский монетный двор. Архивировано (PDF) из оригинала 2012-01-13 . Получено 2011-10-28 .
- ^ Geballe, Theodore H. (октябрь 1993 г.). «Сверхпроводимость: от физики до технологии». Физика сегодня . 46 (10): 52–56. Bibcode : 1993pht .... 46J..52g . doi : 10.1063/1,881384 .
- ^ Кэмпбелл, Флейк С. (2008). "Цирконий" . Элементы металлургии и инженерных сплавов . ASM International. п. 597. ISBN 978-0-87170-867-0 Полем Архивировано с оригинала 2016-05-28.
- ^ Роберт Пальмиери, изд. (2006). "Трубовой металл" . Энциклопедия клавиатурных инструментов . Нью -Йорк: Гарленда. п. 411 . ISBN 978-0-415-94174-7 .
- ^ Джордж Эшдаун Одсли (1988). «Металлические трубы: и материалы, используемые в их конструкции» . Искусство строительства органов Аудсли, Джордж Эшдаун . Публикации курьера. п. 501 ISBN 978-0-486-21315-6 .
- ^ Ким, Х.; Гилмор, C.; Pique, A.; Horwitz, J.; Mattoussi, H .; Murata, H.; Kafafi, Z.; Криси, Д. (1999). «Электрические, оптические и структурные свойства тонких пленок из оксида индия для органических светодиодных устройств». Журнал прикладной физики . 86 (11): 6451. Bibcode : 1999jap .... 86.6451k . doi : 10.1063/1,371708 .
- ^ Бридж, Джанет (сентябрь 1996 г.). Создание и украшение картинных рамок . Книги North Light. ISBN 978-0-89134-739-2 .
- ^ "Жестяная удара" . Архивировано из оригинала 2011-08-11 . Получено 2011-08-15 .
- ^ Пилкингтон, Лаборатория (1969). «Обзор лекции. Процесс плавучего стекла». Труды Королевского общества Лондона. Серия A, математические и физические науки . 314 (1516): 1–25. Bibcode : 1969rspsa.314 .... 1p . doi : 10.1098/rspa.1969.0212 . JSTOR 2416528 . S2CID 109981215 .
- ^ Лукас, Иван Т.; Сиздек, Ярослав; Костеки, Роберт (2011). «Межфазные процессы на мокристаллических электродах β-SN в органических карбонатных электролитах». Электрохимические коммуникации . 13 (11): 1271–1275. doi : 10.1016/j.elecom.2011.08.026 .
- ^ "Colgate Gel-Kam" . Архивировано из оригинала на 2009-04-27 . Получено 2009-05-05 .
- ^ Хаттаб, Ф. (апрель 1989 г.). «Состояние фторидов в зубных пастах». Журнал стоматологии . 17 (2): 47–54. doi : 10.1016/0300-5712 (89) 90129-2 . PMID 2732364 .
- ^ Перлич, Массачусетс; Бакка, Ла; Болмер, BW; Lanzalaco, AC; МакКланахан, SF; Sewak, LK; Beiswanger, BB; Эйхолд, Вашингтон; Халл, младший; и др. (1995). «Клинический эффект стабилизированной зубной стоматологии фторида на образовании бляшек, гингивита и балова десны: шестимесячное исследование». Журнал клинической стоматологии . 6 (Специальный выпуск): 54–58. PMID 8593194 .
- ^ ARSOLATO, Оскар О. (2019). «Физика лазерной оловянной плазмы источников излучения EUV для нанолитографии». Плазма Источет наука и технология . 28 (8). doi : 10.1088/1361-6595/ab3302 .
- ^ Ebdon, L.; Королевское химическое общество (Грейт (2001 . Британия , ) ) 978-0-85404-459-7 Полем Архивировано с оригинала 2016-05-21.
- ^ Jump up to: а беременный в дюймовый Аткинс, Питер; Shriver, Duward F.; Овертон, Тина и Рурк, Джонатан (2006). Неорганическая химия (4 -е изд.). WH Freeman. с. 343, 345. ISBN 978-0-7167-4878-6 .
- ^ Уилкс, Чарльз Э.; Саммерс, Джеймс У.; Дэниелс, Чарльз Энтони; Берард, Марк Т. (август 2005 г.). Руководство из ПВХ . Гансер. п. 108. ISBN 978-1-56990-379-7 Полем Архивировано с оригинала 2016-05-09.
- ^ Дэвид Н.-С. Достопочтенный; Нобуо Ширайши, ред. (2001). "Сохранение дерева " Древесина и целлюлолическая химия Нью -Йорк, Нью -Йорк: Декер. п. 799. ISBN 978-0-8247-0024-9 .
- ^ Antizar-Ladislao, Blanca (1 февраля 2008 г.). «Уровень окружающей среды, токсичность и воздействие морской среды, загрязненной Tributyltin (TBT). Обзор». Environment International . 34 (2): 292–308. Bibcode : 2008enint..34..292a . doi : 10.1016/j.envint.2007.09.005 . PMID 17959247 .
- ^ Эйслер, Рональд. «Оловянные опасности для рыбы, дикой природы и беспозвоночных: синоптический обзор» (PDF) . Американская рыбавая служба и дикая природа Patuxent Research Center. Архивировано (PDF) из оригинала 2012-01-18.
- ^ «Регламент (ЕС) № 782/2003 Европейского парламента и Совета от 14 апреля 2003 года о запрете органических соединений на кораблях» . Europa.eu . Получено 2009-05-05 .
- ^ Дюрр, Симона; Томасон, Джереми, ред. (2008). «Загрязнение на доставке» . Биотонирование . Оксфорд: Блэквелл. п. 227. ISBN 978-1-4051-6926-4 .
- ^ Jump up to: а беременный Магуайр, Р. Джеймс (1987). «Экологические аспекты трибутилтина». Прикладная органометаллическая химия . 1 (6): 475–498. doi : 10.1002/aoc.590010602 .
- ^ de Mora, SJ; Стюарт, C.; Филлипс Д. (1 января 1995 г.). «Источники и скорость деградации Tri (N-Butyl) TIN в морских отложениях недалеко от Окленда, Новая Зеландия». Бюллетень загрязнения морской пехоты . 30 (1): 50–57. Bibcode : 1995marpb..30 ... 50d . doi : 10.1016/0025-326x (94) 00178-c .
- ^ Jump up to: а беременный Axiak, Victor; Микаллеф, Дайан; Маскат, Джоан; Велла, Альфред; Минтофф, Бернардет (1 марта 2003 г.). «INPOSEX в качестве инструмента биомониторинга для морского загрязнения Tributyltin: некоторые дальнейшие наблюдения». Environment International . Secotox Si 28 (8): 743–749. Bibcode : 2003enint..28..743a . doi : 10.1016/s0160-4120 (02) 00119-8 . PMID 12605923 .
- ^ Jump up to: а беременный в «Влияние трибултина на морскую среду» . Sciencebuzz . 17 ноября 2018 года. Архивировано с оригинала 2021-01-25 . Получено 2020-11-17 .
- ^ Фарина, Витторио; Кришнамурти, Венкат; Скотт, Уильям Дж. (1997). «Реакция Стиль». Органические реакции . С. 1–652. doi : 10.1002/0471264180.or050.01 . ISBN 0-471-26418-0 .
- ^ Мус, хайи; Сяо, Вэй; Мяо, Чанг; Ли, Руи; Ю, ограничение (2020). «Составные материалы олова и оловянного составления в виде анодов в литий-ионных и натриевых ионных батареях: обзор» . Границы в химии . 8 : 141. Bibcode : 2020FRCH .... 8..141M . doi : 10.3389/fchem.2020.00141 . PMC 7096543 . PMID 32266205 .
- ^ Лукас, Иван; Syzdek, Jaroslaw (2011). «Межфазные процессы на мокристаллических электродах β-SN в органических карбонатных электролитах». Электрохимические коммуникации . 13 (11): 1271. doi : 10.1016/j.elecom.2011.08.026 .
- ^ «Pocket Guide niosh к химическим опасностям - олово» . CDC . Архивировано с оригинала 2015-11-25 . Получено 2015-11-24 .
Библиография
[ редактировать ] Эта статья включает в себя текст из этого источника, который находится в общественном достоянии : Карлин, Джеймс Ф., младший (1998). «Значительные события, влияющие на цены на олова с 1958 года» . Национальная геодезическая служба США
Эта статья включает в себя текст из этого источника, который находится в общественном достоянии : Карлин, Джеймс Ф., младший (1998). «Значительные события, влияющие на цены на олова с 1958 года» . Национальная геодезическая служба США - Lide, David R., ed. (2006). Справочник по химии и физике (87 -е изд.). Бока Ратон, Флорида: CRC Press, Taylor & Francis Group. ISBN 978-0-8493-0487-3 .
- Эмсли, Джон (2001). "Олово" . Строительные блоки природы: руководство A - Z по элементам . Оксфорд, Англия, Великобритания: издательство Оксфордского университета. С. 445–450 . ISBN 978-0-19-850340-8 .
- Гринвуд, Норман Н .; Эрншоу, Алан (1997). Химия элементов (2 -е изд.). Баттерворт-Хейнеманн . ISBN 978-0-08-037941-8 .
- Хейзерман, Дэвид Л. (1992). «Элемент 50: олово» . Изучение химических элементов и их соединений . Нью -Йорк: книги в таблице. ISBN 978-0-8306-3018-9 .
- Макинтош, Роберт М. (1968). "Олово". В Клиффорде А. Хэмпел (ред.). Энциклопедия химических элементов . Нью -Йорк: Рейнхольд Корпорация. С. 722–732. LCCN 68-29938 .
- Стверка, Альберт (1998). "Олово" . Руководство по элементам (пересмотренный изд.). Издательство Оксфордского университета. ISBN 978-0-19-508083-4 .
Внешние ссылки
[ редактировать ]- Олова за периодической таблицей видео (Университет Ноттингема)
- Деревянный периодический стол Теодора Грея Стол : Образцы олова и отливки
- Базовые металлы: олова
- CDC - Pocket Guide Niosh к химической опасности
- Олова (доллар США за кг)


