Молибден
 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Молибден | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Произношение | / mə ˈ l ɪ b də nə n m m/ | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Появление | серый металлик | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Стандартный атомный вес А р °(Пн) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Молибден в таблице Менделеева | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Атомный номер ( Z ) | 42 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Группа | группа 6 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Период | период 5 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Блокировать | d-блок | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Электронная конфигурация | [ Кр ] 4д 5 5 с 1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Электроны на оболочку | 2, 8, 18, 13, 1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Физические свойства | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Фаза в СТП | твердый | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Температура плавления | 2896 К (2623 °С, 4753 °F) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Точка кипения | 4912 К (4639 °С, 8382 °F) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Плотность (при 20°С) | 10,223 г/см 3 [ 3 ] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| в жидком состоянии (при температуре плавления ) | 9,33 г/см 3 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Теплота плавления | 37,48 кДж/моль | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Теплота испарения | 598 кДж/моль | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Молярная теплоемкость | 24,06 Дж/(моль К) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Давление пара
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Атомные свойства | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Стадии окисления | −4, −2, −1, 0, +1, [ нужна ссылка ] +2, +3, +4 , +5, +6 (сильнокислотный оксид ) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Электроотрицательность | Шкала Полинга: 2,16. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Энергии ионизации |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Атомный радиус | эмпирический: 139 вечера | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ковалентный радиус | 154±17:00 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Другие объекты недвижимости | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Естественное явление | первобытный | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Кристаллическая структура | объемно-центрированная кубическая (bcc) ( cI2 ) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Постоянная решетки | а = 154,71 пм (при 20 °С) [ 3 ] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Тепловое расширение | 5.10 × 10 −6 /К (при 20 °С) [ 3 ] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Теплопроводность | 138 Вт/(м⋅К) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Температуропроводность | 54,3 мм 2 /с (при 300 К) [ 4 ] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Электрическое сопротивление | 53,4 нОм⋅м (при 20 °C) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Магнитный заказ | парамагнитный [ 5 ] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Молярная магнитная восприимчивость | +89.0 × 10 −6 см 3 /mol (298 K) [ 6 ] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Модуль Юнга | 329 ГПа | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Модуль сдвига | 126 ГПа | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Объемный модуль | 230 ГПа | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Скорость звука тонкого стержня | 5400 м/с (при комнатной температуре ) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| коэффициент Пуассона | 0.31 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Твердость по шкале Мооса | 5.5 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Твердость по Виккерсу | 1400–2740 МПа | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Твердость по Бринеллю | 1370–2500 МПа | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Номер CAS | 7439-98-7 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| История | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Открытие | Карл Вильгельм Шееле (1778) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Первая изоляция | Шлем Питера Джейкоба (1781 г.) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Изотопы молибдена | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Молибден — химический элемент ; у него есть символ Мо (от неолатинского молибдена ) и атомный номер 42. Название происходит от древнегреческого Μόλυβδος molybdos , что означает свинец , поскольку его руды путали со свинцовыми рудами. [ 9 ] Минералы молибдена были известны на протяжении всей истории, но этот элемент был открыт (в смысле дифференциации его как нового образования от минеральных солей других металлов) в 1778 году Карлом Вильгельмом Шееле . Металл был впервые выделен в 1781 году Питером Якобом Хьельмом . [ 10 ]
Молибден не встречается в природе в виде свободного металла на Земле; в его минералах он встречается только в окисленном состоянии . Свободный элемент, серебристый металл с серым оттенком, имеет шестую по величине температуру плавления среди всех элементов. Он легко образует твердые стабильные карбиды в сплавах , и по этой причине большая часть мирового производства элемента (около 80%) используется в стальных сплавах, включая высокопрочные сплавы и суперсплавы .
Большинство соединений молибдена плохо растворяются в воде. Нагревание минералов, содержащих молибден, в атмосфере кислорода и воды приводит к образованию молибдат- иона MoO. 2−
4 , образующий хорошо растворимые соли. молибдена В промышленности соединения (около 14% мирового производства элемента) используются в качестве пигментов и катализаторов .
Молибденсодержащие ферменты на сегодняшний день являются наиболее распространенными бактериальными катализаторами разрыва химической связи в молекулярном азоте атмосферы в процессе биологической азотфиксации . В настоящее время у бактерий, растений и животных известно не менее 50 ферментов молибдена, однако в фиксации азота участвуют только бактериальные и цианобактериальные ферменты. Большинство нитрогеназ содержат железомолибденовый кофактор FeMoco , который, как полагают, содержит либо Mo(III), либо Mo(IV). [ 11 ] [ 12 ] Напротив, Mo (VI) и Mo (IV) образуют комплексы с молибдоптерином во всех других молибденсодержащих ферментах. [ 13 ] Молибден является важнейшим элементом для всех высших эукариотных организмов, включая человека. Вид губки известен Theonella conica повышенным накоплением молибдена. [ 14 ]
Характеристики
[ редактировать ]Физические свойства
[ редактировать ]В чистом виде молибден представляет собой серебристо-серый металл с твердостью по шкале Мооса 5,5 и стандартной атомной массой 95,95 г/моль. [ 15 ] [ 16 ] Он имеет температуру плавления 2623 ° C (4753 ° F), что является шестым по величине среди встречающихся в природе элементов; только тантал , осмий , рений , вольфрам и углерод имеют более высокие температуры плавления. [ 9 ] Он имеет один из самых низких коэффициентов теплового расширения среди металлов, используемых в промышленности. [ 17 ]
Химические свойства
[ редактировать ]Молибден — переходный металл с электроотрицательностью 2,16 по шкале Полинга. Он не вступает в видимую реакцию с кислородом или водой при комнатной температуре, но подвергается воздействию галогенов и перекиси водорода. Слабое окисление молибдена начинается при 300 °C (572 °F); объемное окисление происходит при температуре выше 600 °C, в результате чего образуется триоксид молибдена . Как и многие более тяжелые переходные металлы, молибден мало склонен образовывать катионы в водном растворе, хотя Mo 3+ Известно, что катион образуется в тщательно контролируемых условиях. [ 18 ]
Газообразный молибден состоит из двухатомных частиц Mo 2 . Эта молекула представляет собой синглет с двумя неспаренными электронами на связывающих орбиталях в дополнение к пяти обычным связям. В результате возникает шестикратная связь . [ 19 ] [ 20 ]
изотопы
[ редактировать ]Известно 39 изотопов молибдена с атомной массой от 81 до 119, а также 13 метастабильных ядерных изомеров . В природе встречаются семь изотопов с атомными массами 92, 94, 95, 96, 97, 98 и 100. Из этих встречающихся в природе изотопов только молибден-100 нестабильен. [ 7 ]
Молибден-98 является наиболее распространенным изотопом, составляющим 24,14% всего молибдена. Молибден-100 имеет период полураспада около 10 19 y и подвергается двойному бета-распаду с образованием рутения-100. Все нестабильные изотопы молибдена распадаются на изотопы ниобия , технеция и рутения . Из синтетических радиоизотопов наиболее стабильным является 93 Мо, период полураспада 4839 лет. [ 8 ]
Наиболее распространенное применение изотопного молибдена связано с молибденом-99 , который является продуктом деления . Это родительский радиоизотоп короткоживущего дочернего гамма-излучающего радиоизотопа технеция-99m , ядерного изомера, используемого в различных приложениях визуализации в медицине. [ 21 ] В 2008 году Делфтский технологический университет подал заявку на патент на производство молибдена-99 на основе молибдена-98. [ 22 ]
Соединения
[ редактировать ]Молибден образует химические соединения в степенях окисления −4 и от −2 до +6. Более высокие степени окисления более важны для его земного распространения и биологической роли, средние степени окисления часто связаны с металлическими кластерами , а очень низкие степени окисления обычно связаны с молибденорганическими соединениями . Химия молибдена и вольфрама демонстрирует большое сходство. Например, относительная редкость молибдена (III) контрастирует с распространением соединений хрома (III). Наивысшая степень окисления наблюдается у оксида молибдена(VI) (MoO 3 ), тогда как нормальным соединением серы является дисульфид молибдена MoS 2 . [ 23 ]
| Окисление состояние |
Пример [ 24 ] [ 25 ] |
|---|---|
| −4 | Уже 4 [Мо(СО) 4 ] |
| −2 | [Мо(СО) 5 ] 2− [ 26 ] |
| −1 | Уже 2 [Пн. 2 (КО) 10 ] |
| 0 | Мо(СО) 6 |
| +1 | С 55Ч 5Mo (Колорадо) 3 |
| +2 | МоCl 2 |
| +3 | МоБр 3 |
| +4 | нет 2 |
| +5 | МоCl 5 |
| +6 | МФ 6 |

С точки зрения торговли наиболее важными соединениями являются дисульфид молибдена ( MoS
2 ) и триоксид молибдена ( MoO
3 ). Черный дисульфид является основным минералом. Его обжаривают на воздухе, чтобы получить триоксид: [ 23 ]
- 2 месяца жизни
2 + 7 О
2 → 2 МОО
3 + 4 СО
2
Триоксид, летучий при высоких температурах, является предшественником практически всех других соединений молибдена, а также сплавов. Молибден имеет несколько степеней окисления , наиболее стабильными являются +4 и +6 (выделены жирным шрифтом в таблице слева).
Оксид молибдена(VI) растворим в сильнощелочной воде , образуя молибдаты (MoO 4 2− ). Молибдаты являются более слабыми окислителями, чем хроматы . Они имеют тенденцию образовывать структурно сложные оксианионы путем конденсации при более низких значениях pH , такие как [Mo 7 O 24 ] 6− и [Mo 8 O 26 ] 4− . Полимолибдаты могут включать в себя другие ионы, образуя полиоксометаллаты . [ 27 ] Темно-синий фосфорсодержащий гетерополимолибдат P[Mo 12 O 40 ] 3− используется для спектроскопического обнаружения фосфора. [ 28 ]
Широкий диапазон степеней окисления молибдена отражается в различных хлоридах молибдена: [ 23 ]
- Хлорид молибдена(II) MoCl 2 , который существует в виде гексамера Mo 6 Cl 12 и родственного дианиона [Mo 6 Cl 14 ] 2- .
- Хлорид молибдена(III) MoCl 3 , темно-красное твердое вещество, которое превращается в анионный трианионный комплекс [MoCl 6 ] 3- .
- Хлорид молибдена(IV) MoCl 4 , черное твердое вещество, имеющее полимерную структуру.
- Хлорид молибдена(V) MoCl 5 темно-зеленого твердого вещества, имеющего димерную структуру.
- Хлорид молибдена(VI) MoCl 6 представляет собой черное твердое вещество, которое является мономерным и медленно разлагается на MoCl 5 и Cl 2 при комнатной температуре. [ 29 ]
Доступность этих степеней окисления довольно сильно зависит от галогенидного противоиона: хотя фторид молибдена (VI) стабилен, молибден не образует стабильных гексахлорида, пентабромида или тетраиодида. [ 30 ]
Подобно хрому и некоторым другим переходным металлам, молибден образует четверные связи , например, в Mo 2 (CH 3 COO) 4 и [Mo 2 Cl 8 ] 4− . [ 23 ] [ 31 ] кислотных свойствах Льюиса димеров бутирата и перфторбутирата Mo 2 (O 2 CR) 4 и Rh 2 (O 2 CR) 4 . Сообщалось о [ 32 ]
Степень окисления 0 и ниже возможна с монооксидом углерода в качестве лиганда, например, в гексакарбониле молибдена Mo(CO) 6 . [ 23 ] [ 25 ]
История
[ редактировать ]Молибденит — основная руда, из которой сейчас добывают молибден, — ранее был известен как молибден. Молибдену путали с графитом и часто использовали так, как будто это графит . Как и графит, молибденит можно использовать для чернения поверхности или в качестве твердой смазки. [ 33 ] Даже когда молибден можно было отличить от графита, его все равно путали с обычной свинцовой рудой PbS (теперь называемой галенитом ); Название происходит от древнегреческого Μόλυβδος molybdos , что означает свинец . [ 17 ] (Само греческое слово было предложено как заимствованное из анатолийского лувийского и лидийского языков). [ 34 ]
Хотя (как сообщается) молибден был намеренно легирован сталью в одном японском мече XIV века (производство около 1330 г. ), это искусство никогда не применялось широко и позже было утеряно. [ 35 ] [ 36 ] На Западе в 1754 году Бенгт Андерссон Квист исследовал образец молибденита и определил, что он не содержит свинца и, следовательно, не является галенитом. [ 37 ]
К 1778 году шведский химик Карл Вильгельм Шееле твердо заявил, что молибдена (на самом деле) не является ни галенитом, ни графитом. [ 38 ] [ 39 ] Вместо этого Шееле правильно предположил, что молибдена представляет собой руду особого нового элемента, названного молибденом в честь минерала, в котором он находился и из которого его можно было выделить. Питер Якоб Хьельм успешно выделил молибден с помощью угля и льняного масла в 1781 году. [ 17 ] [ 40 ]
В течение следующего столетия молибден не имел промышленного применения. Его было относительно мало, чистый металл было трудно добыть, а необходимые методы металлургии были незрелыми. [ 41 ] [ 42 ] [ 43 ] Ранние молибденовые стальные сплавы показали большие надежды на повышенную твердость, но усилия по производству сплавов в больших масштабах были затруднены из-за противоречивых результатов, склонности к хрупкости и рекристаллизации. В 1906 году Уильям Д. Кулидж подал патент на придание молибдену пластичности , что привело к его применению в качестве нагревательного элемента для высокотемпературных печей и в качестве основы для лампочек с вольфрамовой нитью; Образование и разложение оксидов требуют, чтобы молибден был физически изолирован или удерживался в инертном газе. [ 44 ] В 1913 году Фрэнк Э. Элмор разработал процесс пенной флотации для извлечения молибденита из руд; флотация остается основным процессом изоляции. [ 45 ]
Во время Первой мировой войны спрос на молибден резко возрос; его использовали как в броневой обшивке , так и в качестве заменителя вольфрама в быстрорежущих сталях . Некоторые британские танки были защищены обшивкой из марганцовистой стали толщиной 75 мм (3 дюйма) , но это оказалось неэффективным. Пластины из марганцевой стали были заменены гораздо более легкими пластинами из молибденовой стали толщиной 25 мм (1,0 дюйма), что позволило обеспечить более высокую скорость, большую маневренность и лучшую защиту. [ 17 ] Немцы также использовали сталь , легированную молибденом , для тяжелой артиллерии, как в сверхтяжелой гаубице « Большая Берта» , [ 46 ] потому что традиционная сталь плавится при температурах, создаваемых топливом однотонного снаряда . [ 47 ] После войны спрос резко упал, пока достижения металлургии не позволили широко развивать применение в мирное время. Во время Второй мировой войны молибден снова приобрел стратегическое значение в качестве заменителя вольфрама в стальных сплавах. [ 48 ]
Возникновение и производство
[ редактировать ]
Молибден является 54-м по распространенности элементом в земной коре со средним содержанием 1,5 частей на миллион и 25-м по распространенности элементом в океанах со средним содержанием 10 частей на миллиард; это 42-й по распространенности элемент во Вселенной. [ 17 ] [ 49 ] Советская миссия «Луна-24» обнаружила молибденсодержащее зерно (1×0,6 мкм) во фрагменте пироксена, взятом из Mare Crisium на Луне . [ 50 ] Сравнительная редкость молибдена в земной коре компенсируется его концентрацией в ряде водонерастворимых руд, часто соединенных с серой так же, как с медью, с которой он часто встречается. Хотя молибден содержится в таких минералах, как вульфенит (PbMoO 4 ) и повеллит (CaMoO 4 ), основным промышленным источником является молибденит (Mo S 2 ). Молибден добывается как основная руда, а также извлекается как побочный продукт добычи меди и вольфрама. [ 9 ]
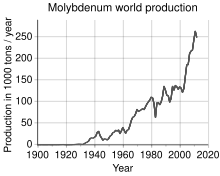
В 2011 году мировое производство молибдена составило 250 000 тонн, крупнейшими производителями были Китай (94 000 тонн), США (64 000 тонн), Чили (38 000 тонн), Перу (18 000 тонн) и Мексика (12 000 тонн). Общие запасы оцениваются в 10 млн тонн и в основном сосредоточены в Китае (4,3 млн тонн), США (2,7 млн тонн) и Чили (1,2 млн тонн). По континентам 93% мирового производства молибдена примерно поровну распределено между Северной Америкой, Южной Америкой (в основном в Чили) и Китаем. Остальную часть производят Европа и остальные страны Азии (в основном Армения, Россия, Иран и Монголия). [ 51 ]
При переработке молибденита руда сначала обжигается на воздухе при температуре 700 °C (1292 °F). В результате этого процесса образуется газообразный диоксид серы и оксид молибдена (VI) : [ 23 ]
Полученный оксид затем обычно экстрагируют водным раствором аммиака с получением молибдата аммония:
Медь, примесь молибденита, на этом этапе отделяется обработкой сероводородом . [ 23 ] Молибдат аммония превращается в димолибдат аммония , который выделяется в виде твердого вещества. Нагревание этого твердого вещества дает триоксид молибдена: [ 52 ]
Сырой триоксид можно дополнительно очистить сублимацией при температуре 1100 ° C (2010 ° F).
Металлический молибден получают восстановлением оксида водородом:
Молибден для производства стали восстанавливается алюминотермической реакцией с добавлением железа для получения ферромолибдена . Обычная форма ферромолибдена содержит 60% молибдена. [ 23 ] [ 53 ]
По состоянию на август 2009 года стоимость молибдена составляла около 30 000 долларов за тонну. С 1997 по 2003 год он поддерживал цену на уровне 10 000 долларов за тонну или около нее и достиг пика в 103 000 долларов за тонну в июне 2005 года. [ 54 ] В 2008 году Лондонская биржа металлов объявила, что молибден будет торговаться как товар. [ 55 ]
Горное дело
[ редактировать ]Рудник Кнабен на юге Норвегии, открытый в 1885 году, был первым специализированным молибденовым рудником. Закрыт в 1973 году, но вновь открыт в 2007 году. [ 56 ] сейчас он производит 100 000 килограммов (98 длинных тонн; 110 коротких тонн) дисульфида молибдена в год. Крупные шахты в Колорадо (такие как шахта Хендерсон и шахта Климакс ) [ 57 ] а в Британской Колумбии в качестве основного продукта добывают молибденит, в то время как многие медно-порфировые месторождения, такие как рудник Бингем-Каньон в штате Юта и рудник Чукикамата на севере Чили, производят молибден как побочный продукт добычи меди.
Приложения
[ редактировать ]Сплавы
[ редактировать ]
Около 86% производимого молибдена используется в металлургии , а остальная часть используется в химической промышленности. По оценкам, глобальное использование составляет 35% конструкционной стали, 25% нержавеющей стали , 14% химикатов, инструментальных и быстрорежущих сталей 9%, чугуна 6%, элементарного металлического молибдена 6% и суперсплавов 5%. [ 58 ]
Молибден может выдерживать экстремальные температуры без значительного расширения или размягчения, что делает его полезным в условиях сильной жары, включая военную броню, детали самолетов, электрические контакты, промышленные двигатели и опоры для нитей в лампочках . [ 17 ] [ 59 ]
Большинство высокопрочных стальных сплавов (например, стали 41хх ) содержат от 0,25% до 8% молибдена. [ 9 ] Даже в этих небольших количествах более 43 000 тонн молибдена ежегодно используется в производстве нержавеющих сталей , инструментальных сталей , чугунов и жаропрочных суперсплавов . [ 49 ]
Молибден также используется в стальных сплавах из-за его высокой коррозионной стойкости и свариваемости . [ 49 ] [ 51 ] Молибден обеспечивает коррозионную стойкость нержавеющих сталей типа 300 (в частности, типа 316) и особенно так называемых супераустенитных нержавеющих сталей (таких как сплавы AL-6XN , 254SMO и 1925hMo). Молибден увеличивает деформацию решетки, тем самым увеличивая энергию, необходимую для растворения атомов железа с поверхности. [ противоречивый ] Молибден также используется для повышения коррозионной стойкости ферритных материалов (например, марки 444). [ 60 ] и мартенситные (например, 1.4122 и 1.4418) нержавеющие стали. [ нужна ссылка ]
Из-за более низкой плотности и более стабильной цены молибден иногда используется вместо вольфрама. [ 49 ] Примером может служить серия быстрорежущих сталей «М», таких как М2, М4 и М42, в качестве замены стали серии «Т», содержащей вольфрам. Молибден также можно использовать в качестве огнестойкого покрытия для других металлов. Хотя его температура плавления составляет 2623 °C (4753 °F), молибден быстро окисляется при температуре выше 760 °C (1400 °F), что делает его более подходящим для использования в вакууме. [ 59 ]
TZM (Mo (~99%), Ti (~0,5%), Zr (~0,08%) и немного C) представляет собой коррозионностойкий молибденовый суперсплав, который устойчив к расплавленным фторидным солям при температурах выше 1300 ° C (2370 ° F). Он имеет примерно в два раза большую прочность, чем чистый Мо, более пластичен и лучше поддается сварке, однако в ходе испытаний он выдержал коррозию стандартной эвтектической соли ( FLiBe ) и паров соли, используемых в реакторах с расплавленными солями, в течение 1100 часов с такой незначительной коррозией, что трудно измерить. [ 61 ] [ 62 ] Благодаря отличным механическим свойствам при высоких температурах и высоких давлениях сплавы ТЗМ широко применяются в военной промышленности. [ 63 ] Его применяют в качестве гидроблока торпедных двигателей, сопел ракет и газопроводов, где он выдерживает экстремальные термические и механические нагрузки. [ 64 ] [ 65 ] Он также используется в качестве радиационной защиты в ядерных приложениях. [ 66 ]
Другие сплавы на основе молибдена, не содержащие железа, имеют лишь ограниченное применение. Например, из-за его устойчивости к расплавленному цинку молибден- вольфрам (70%/30%). для изготовления трубопроводов, мешалок и рабочих колес насосов, контактирующих с расплавленным цинком, используются как чистый молибден, так и сплавы [ 67 ]
Применение чистых элементов
[ редактировать ]- Порошок молибдена используется в качестве удобрения для некоторых растений, например, цветной капусты . [ 49 ]
- Элементарный молибден используется в анализаторах NO, NO 2 , NO x на электростанциях для контроля загрязнения. При 350 °C (662 °F) этот элемент действует как катализатор NO 2 /NO x с образованием молекул NO для обнаружения с помощью инфракрасного света. [ 68 ]
- Молибденовые аноды заменяют вольфрам в некоторых источниках рентгеновского излучения низкого напряжения для специализированных целей, таких как маммография . [ 69 ]
- Радиоактивный изотоп молибден-99 используется для получения технеция-99m , используемого для медицинской визуализации. [ 70 ] С изотопом обращаются и хранят как молибдат. [ 71 ]
Сложные приложения
[ редактировать ]- Дисульфид молибдена (MoS 2 ) используется в качестве твердой смазки и противоизносного средства при высоких давлениях и высоких температурах (HPHT). Он образует прочные пленки на металлических поверхностях и является распространенной добавкой к смазкам HPHT — в случае катастрофического выхода смазки из строя тонкий слой молибдена предотвращает контакт смазываемых деталей. [ 72 ]
- В сочетании с небольшими количествами кобальта MoS 2 также используется в качестве катализатора при гидрообессеривании (HDS) нефти. В присутствии водорода этот катализатор облегчает удаление азота и особенно серы из сырья, которые в противном случае могли бы отравить последующие катализаторы. HDS - одно из крупнейших применений катализа в промышленности. [ 73 ]
- Оксиды молибдена являются важными катализаторами селективного окисления органических соединений. Производство товарных химикатов акрилонитрила и формальдегида основано на катализаторах на основе MoO x . [ 52 ]
- Дисилицид молибдена (MoSi 2 ) — электропроводящая керамика , преимущественно используемая в нагревательных элементах, работающих при температуре выше 1500 °С на воздухе. [ 74 ]
- Триоксид молибдена (MoO 3 ) используется в качестве клея между эмалями и металлами. [ 38 ]
- Молибдат свинца (вульфенит), соосажденный с хроматом и сульфатом свинца, представляет собой ярко-оранжевый пигмент, используемый в керамике и пластмассах. [ 75 ]
- Смешанные оксиды на основе молибдена являются универсальными катализаторами в химической промышленности. Некоторыми примерами являются катализаторы окисления монооксида углерода, пропилена в акролеин и акриловую кислоту, аммоксидирование пропилена в акрилонитрил. [ 76 ] [ 77 ]
- Карбиды, нитриды и фосфиды молибдена могут быть использованы для гидроочистки рапсового масла. [ 78 ]
- Гептамолибдат аммония используется при биологическом окрашивании. [ 79 ]
- Натриево-известковое стекло с молибденовым покрытием используется в CIGS ( селенид меди, индия, галлия ) солнечных элементах , называемых солнечными элементами CIGS .
- Фосфомолибденовая кислота - краситель, используемый в тонкослойной хроматографии. [ 80 ] и трихромное окрашивание в гистохимии . [ 81 ]
Биологическая роль
[ редактировать ]Mo-содержащие ферменты
[ редактировать ]Молибден является важным элементом большинства организмов; В исследовательской работе 2008 года высказывалось предположение, что нехватка молибдена в ранних океанах Земли могла сильно повлиять на эволюцию эукариотической жизни (которая включает в себя все растения и животных). [ 82 ]
Идентифицировано не менее 50 молибденсодержащих ферментов, в основном у бактерий. [ 83 ] [ 84 ] Эти ферменты включают альдегидоксидазу , сульфитоксидазу и ксантиноксидазу . [ 17 ] За одним исключением, Мо в белках связывается молибдоптерином с образованием кофактора молибдена. Единственным известным исключением является нитрогеназа , которая использует кофактор FeMoco , имеющий формулу Fe 7 MoS 9 C. [ 85 ]
С точки зрения функции молибдоферменты катализируют окисление, а иногда и восстановление некоторых небольших молекул в процессе регулирования азота , серы и углерода . [ 86 ] У некоторых животных и у человека окисление ксантина до мочевой кислоты — процесс пуринов катаболизма — катализируется ксантиноксидазой — молибденсодержащим ферментом. Активность ксантиноксидазы прямо пропорциональна количеству молибдена в организме. Чрезвычайно высокая концентрация молибдена меняет эту тенденцию и может ингибировать катаболизм пуринов и другие процессы. Концентрация молибдена также влияет на синтез белка , обмен веществ и рост. [ 87 ]
Мо является компонентом большинства нитрогеназ . Среди молибдоферментов нитрогеназы уникальны тем, что в них отсутствует молибдоптерин. [ 88 ] [ 89 ] Нитрогеназы катализируют образование аммиака из атмосферного азота:
Биосинтез . FeMoco очень активного центра сложен [ 90 ]

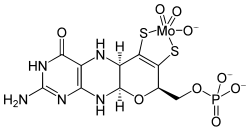
Молибдат транспортируется в организме в виде МоО 4. 2− . [ 87 ]
Человеческий метаболизм и дефицит
[ редактировать ]Молибден является важным микроэлементом в питании . [ 91 ] Известны четыре Mo-зависимых фермента млекопитающих, все они содержат птерина на основе молибденовый кофактор в своем активном центре (Moco): сульфитоксидаза , ксантиноксидоредуктаза , альдегидоксидаза и митохондриальная амидоксимредуктаза . [ 92 ] Люди с серьезным дефицитом молибдена имеют плохо функционирующую сульфитоксидазу и склонны к токсическим реакциям на сульфиты в пищевых продуктах. [ 93 ] [ 94 ] В организме человека содержится около 0,07 мг молибдена на килограмм массы тела. [ 95 ] с более высокими концентрациями в печени и почках и более низкими в позвонках. [ 49 ] Молибден также присутствует в зубной эмали человека и может помочь предотвратить ее разрушение. [ 96 ]
Острая токсичность у людей не наблюдалась, и токсичность сильно зависит от химического состояния. Исследования на крысах показывают, что средняя смертельная доза (LD 50 ) для некоторых соединений Мо составляет всего лишь 180 мг/кг. [ 97 ] Хотя данные о токсичности для человека недоступны, исследования на животных показали, что хроническое употребление молибдена в дозе более 10 мг/день может вызвать диарею, задержку роста, бесплодие , низкий вес при рождении и подагру ; он также может поражать легкие, почки и печень. [ 98 ] [ 99 ] Вольфрамат натрия является конкурентным ингибитором молибдена. Диетический вольфрам снижает концентрацию молибдена в тканях. [ 49 ]
Низкая концентрация молибдена в почве в географическом диапазоне от северного Китая до Ирана приводит к общему дефициту молибдена в рационе и связана с повышенным уровнем заболеваемости раком пищевода . [ 100 ] [ 101 ] [ 102 ] По сравнению с Соединенными Штатами, где запасы молибдена в почве выше, у людей, живущих в этих районах, риск пищевода плоскоклеточного рака примерно в 16 раз выше . [ 103 ]
Сообщалось также о дефиците молибдена как следствие полного парентерального питания (полного внутривенного питания) без добавок молибдена в течение длительных периодов времени. Это приводит к повышению уровня сульфита и уратов в крови , почти так же, как и дефицит кофактора молибдена . Поскольку чистый дефицит молибдена по этой причине возникает преимущественно у взрослых, неврологические последствия не столь выражены, как в случаях врожденного дефицита кофактора. [ 104 ]
Врожденная болезнь дефицита кофактора молибдена , наблюдаемая у младенцев, представляет собой неспособность синтезировать кофактор молибдена , гетероциклическую молекулу, обсуждавшуюся выше, которая связывает молибден в активном центре всех известных человеческих ферментов, использующих молибден. Возникающий в результате дефицит приводит к высокому уровню сульфитов и уратов , а также к неврологическим повреждениям. [ 105 ] [ 106 ]
Экскреция
[ редактировать ]Большая часть молибдена выводится из организма человека в виде молибдата с мочой. Кроме того, выведение молибдена с мочой увеличивается по мере увеличения потребления молибдена с пищей. Небольшие количества молибдена выводятся из организма с калом и желчью; небольшие количества также могут теряться с потом и волосами. [ 107 ] [ 108 ]
Избыток и антагонизм меди
[ редактировать ]организмом Высокий уровень молибдена может препятствовать усвоению меди , вызывая дефицит меди . Молибден предотвращает связывание меди белками плазмы, а также увеличивает количество меди, выводимой с мочой . Жвачные животные , потребляющие большое количество молибдена, страдают от диареи , задержки роста, анемии и ахромотрихии (потеря пигмента шерсти). Эти симптомы можно облегчить с помощью добавок меди, как диетических, так и инъекционных. [ 109 ] Дефицит меди может усугубляться избытком серы . [ 49 ] [ 110 ]
Снижение или дефицит меди также может быть намеренно вызван в терапевтических целях соединением тетратиомолибдата аммония , в котором ярко-красный анион тетратиомолибдат является медь-хелатирующим агентом. Тетратиомолибдат впервые был использован в терапевтических целях при лечении токсикоза меди у животных. Затем его начали использовать для лечения болезни Вильсона — наследственного нарушения обмена меди у человека; он действует как путем конкуренции с абсорбцией меди в кишечнике, так и за счет увеличения выведения. Также было обнаружено, что он оказывает ингибирующее действие на ангиогенез , возможно, за счет ингибирования процесса мембранной транслокации, который зависит от ионов меди. [ 111 ] Это многообещающее направление для исследования методов лечения рака , возрастной дегенерации желтого пятна и других заболеваний, связанных с патологической пролиферацией кровеносных сосудов. [ 112 ] [ 113 ]
У некоторых пасущихся животных, особенно у крупного рогатого скота, избыток молибдена в почве пастбищ может вызвать диарею , если pH почвы от нейтрального до щелочного; см . слезливость .
Диетические рекомендации
[ редактировать ]В 2000 году тогдашний Медицинский институт США (ныне Национальная медицинская академия , NAM) обновил свои расчетные средние потребности (EARS) и рекомендуемые диетические нормы (RDA) для молибдена. Если информации недостаточно для установления EAR и RDA, оценка, обозначенная как Адекватное потребление вместо этого используется (AI).
ДВ в размере 2 микрограммов (мкг) молибдена в день была установлена для детей в возрасте до 6 месяцев и 3 мкг/день в возрасте от 7 до 12 месяцев как для мальчиков, так и для женщин. Для детей старшего возраста и взрослых установлены следующие суточные нормы молибдена: 17 мкг от 1 до 3 лет, 22 мкг от 4 до 8 лет, 34 мкг от 9 до 13 лет, 43 мкг от 14 до 18 лет, и 45 мкг для лиц 19 лет и старше. Все эти RDA действительны для обоих полов. Беременные или кормящие женщины в возрасте от 14 до 50 лет имеют более высокую суточную норму молибдена — 50 мкг.
Что касается безопасности, NAM устанавливает допустимые верхние уровни потребления (ULS) витаминов и минералов, когда доказательства достаточны. В случае молибдена UL составляет 2000 мкг/день. В совокупности EAR, RDA, AI и UL называются эталонными диетическими нормами потребления (DRI). [ 114 ]
Европейское управление по безопасности пищевых продуктов (EFSA) называет совокупный набор информации эталонными диетическими значениями, с эталонным потреблением для населения (PRI) вместо RDA и средней потребностью вместо EAR. AI и UL определяются так же, как и в США. Для женщин и мужчин в возрасте 15 лет и старше ИД устанавливается на уровне 65 мкг/день. Беременные и кормящие женщины имеют одинаковый ИИ. Для детей в возрасте 1–14 лет доза ИА увеличивается с возрастом от 15 до 45 мкг/день. ИИ для взрослых выше, чем RDA в США, [ 115 ] но, с другой стороны, Европейское управление по безопасности пищевых продуктов рассмотрело тот же вопрос безопасности и установило UL на уровне 600 мкг/день, что намного ниже, чем значение в США. [ 116 ]
Маркировка
[ редактировать ]Для целей маркировки пищевых продуктов и пищевых добавок в США количество в порции выражается в процентах от дневной нормы (% ДВ). Для целей маркировки молибдена 100% дневной нормы составляло 75 мкг, но по состоянию на 27 мая 2016 г. она была изменена до 45 мкг. [ 117 ] [ 118 ] Таблица старых и новых дневных норм для взрослых представлена в разделе «Справочная суточная норма» .
Источники пищи
[ редактировать ]Среднесуточное потребление варьируется от 120 до 240 мкг/день, что превышает рекомендации по питанию. [ 98 ] Свинина, баранина и говяжья печень содержат примерно 1,5 части молибдена на миллион. Другие важные пищевые источники включают зеленую фасоль, яйца, семена подсолнечника, пшеничную муку, чечевицу, огурцы и зерновые культуры. [ 17 ]
Меры предосторожности
[ редактировать ]Молибденовая пыль и пары, образующиеся при добыче полезных ископаемых или металлообработке, могут быть токсичными, особенно при проглатывании (включая пыль, попадающую в носовые пазухи и позднее проглатываемую). [ 97 ] Небольшие уровни длительного воздействия могут вызвать раздражение глаз и кожи. Следует избегать прямого вдыхания или проглатывания молибдена и его оксидов. [ 119 ] [ 120 ] В правилах OSHA указано максимально допустимое воздействие молибдена в течение 8-часового рабочего дня как 5 мг/м. 3 . Хроническое воздействие от 60 до 600 мг/м 3 может вызывать такие симптомы, как усталость, головные боли и боли в суставах. [ 121 ] На уровне 5000 мг/м 3 Молибден непосредственно опасен для жизни и здоровья . [ 122 ]
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ «Стандартные атомные массы: молибден» . ЦИАВ . 2013.
- ^ Прохаска, Томас; Ирргехер, Йоханна; Бенефилд, Жаклин; Бёлке, Джон К.; Чессон, Лесли А.; Коплен, Тайлер Б.; Дин, Типинг; Данн, Филип Дж. Х.; Грёнинг, Манфред; Холден, Норман Э.; Мейер, Харро Эй Джей (04 мая 2022 г.). «Стандартные атомные веса элементов 2021 (Технический отчет ИЮПАК)» . Чистая и прикладная химия . дои : 10.1515/pac-2019-0603 . ISSN 1365-3075 .
- ^ Перейти обратно: а б с Арбластер, Джон В. (2018). Некоторые значения кристаллографических свойств элементов . Парк материалов, Огайо: ASM International. ISBN 978-1-62708-155-9 .
- ^ Линдеманн, А.; Блюмм, Дж. (2009). Измерение теплофизических свойств чистого молибдена . Том. 3. 17-й семинар Plansee .
- ^ Лиде, Д.Р., изд. (2005). «Магнитная восприимчивость элементов и неорганических соединений». Справочник CRC по химии и физике (PDF) (86-е изд.). Бока-Ратон (Флорида): CRC Press. ISBN 0-8493-0486-5 .
- ^ Уэст, Роберт (1984). CRC, Справочник по химии и физике . Бока-Ратон, Флорида: Издательство компании Chemical Rubber Company. стр. E110. ISBN 0-8493-0464-4 .
- ^ Перейти обратно: а б с Кондев, ФГ; Ван, М.; Хуанг, WJ; Наими, С.; Ауди, Г. (2021). «Оценка ядерных свойств NUBASE2020» (PDF) . Китайская физика C . 45 (3): 030001. doi : 10.1088/1674-1137/abddae .
- ^ Перейти обратно: а б Каян, И.; Хайниц, С.; Коссерт, К.; Спрунг, П.; Дресслер, Р.; Шуман, Д. (05 октября 2021 г.). «Первое прямое определение 93 Период полураспада Мо» . Научные отчеты . 11 (1). doi : 10.1038/ . ISSN 2045-2322 . PMC 8492754. . PMID 34611245 s41598-021-99253-5
- ^ Перейти обратно: а б с д Лиде, Дэвид Р., изд. (1994). «Молибден». CRC Справочник по химии и физике . Том. 4. Издательство «Химическая резина». п. 18. ISBN 978-0-8493-0474-3 .
- ^ «Это элементарно – элемент молибден» . Научное образование в лаборатории Джефферсона . Архивировано из оригинала 4 июля 2018 г. Проверено 3 июля 2018 г.
- ^ Бьернссон, Рагнар; Низ, Фрэнк; Шрок, Ричард Р.; Эйнсл, Оливер; ДеБир, Серена (2015). «Открытие Mo (III) в FeMoco: воссоединение фермента и модельной химии» . Журнал биологической неорганической химии . 20 (2): 447–460. дои : 10.1007/s00775-014-1230-6 . ISSN 0949-8257 . ПМК 4334110 . ПМИД 25549604 .
- ^ Ван Стаппен, Кейси; Давыдов Роман; Ян, Чжи-Ён; Фань, Жуйси; Го, Исон; Билл, Экхард; Зеефельдт, Лэнс К.; Хоффман, Брайан М.; ДеБир, Серена (16 сентября 2019 г.). «Спектроскопическое описание состояния E1 молибденазы на основе рентгеновского поглощения молибдена и железа и мессбауэровских исследований» . Неорганическая химия . 58 (18): 12365–12376. doi : 10.1021/acs.inorgchem.9b01951 . ISSN 0020-1669 . ПМК 6751781 . ПМИД 31441651 .
- ^ Леймкюлер, Силке (2020). «Биосинтез кофакторов молибдена в Escherichia coli» . Экологическая микробиология . 22 (6): 2007–2026. Бибкод : 2020EnvMi..22.2007L . дои : 10.1111/1462-2920.15003 . ISSN 1462-2920 . ПМИД 32239579 .
- ^ Шохам, Шани; Керен, Рэй; Лави, Ади; Полищук Ирина; Покрой, Вооз; Илан, Миша (19 июля 2024 г.). «Совершенно неожиданно: гипернакопление молибдена в индо-тихоокеанской губке Theonella conica » . Достижения науки . 10 (29). дои : 10.1126/sciadv.adn3923 . ISSN 2375-2548 . ПМК 466961 . ПМИД 39018411 .
- ^ Визер, Мэн; Берглунд, М. (2009). «Атомные веса элементов 2007 (Технический отчет ИЮПАК)» (PDF) . Чистая и прикладная химия . 81 (11): 2131–2156. doi : 10.1351/PAC-REP-09-08-03 . S2CID 98084907 . Архивировано из оригинала (PDF) 11 марта 2012 г. Проверено 13 февраля 2012 г.
- ^ Мейя, Юрис; и др. (2013). «Текущая таблица стандартных атомных весов в алфавитном порядке: Стандартные атомные веса элементов» . Комиссия по изотопному содержанию и атомному весу. Архивировано из оригинала 29 апреля 2014 г.
- ^ Перейти обратно: а б с д и ж г час Эмсли, Джон (2001). Строительные блоки природы . Оксфорд: Издательство Оксфордского университета. стр. 262–266. ISBN 978-0-19-850341-5 .
- ^ Пэриш, Р.В. (1977). Металлические элементы . Нью-Йорк: Лонгман. стр. 112 , 133. ISBN. 978-0-582-44278-8 .
- ^ Мерино, Габриэль; Дональд, Келлинг Дж.; Д'Аккиоли, Джейсон С.; Хоффманн, Роальд (2007). «Множество способов иметь пятерную связь». Дж. Ам. хим. Соц. 129 (49): 15295–15302. дои : 10.1021/ja075454b . ПМИД 18004851 .
- ^ Роос, Бьорн О.; Борин, Антонио К.; Лаура Гальярди (2007). «Достижение максимальной кратности ковалентной химической связи» . Энджью. хим. Межд. Эд. 46 (9): 1469–1472. дои : 10.1002/anie.200603600 . ПМИД 17225237 .
- ^ Армстронг, Джон Т. (2003). «Технеций» . Новости химии и техники . Архивировано из оригинала 6 октября 2008 г. Проверено 7 июля 2009 г.
- ^ Вултербек, Хьюберт Теодор; Боде, Питер «Процесс производства 99Mo без добавок носителей» . Европейский патент EP2301041 (А1) — 30 марта 2011 г. Проверено 27 июня 2012 г.
- ^ Перейти обратно: а б с д и ж г час Холлеман, Арнольд Ф.; Виберг, Эгон; Виберг, Нильс (1985). Учебник неорганической химии (91–100 изд.). Вальтер де Грюйтер. стр. 1096–1104. ISBN 978-3-11-007511-3 .
- ^ Хофманн, Карл А. (1973). «VI. Подгруппа» . В Хофманне, Карл А.; Хофманн, Ульрих; Рюдорф, Вальтер (ред.). Неорганическая химия (на немецком языке). Висбаден: Vieweg+Teubner Verlag. стр. 627–641. дои : 10.1007/978-3-663-14240-9_31 . ISBN 978-3-663-14240-9 .
- ^ Перейти обратно: а б Вернер, Хельмут (2008). Вехи в химии органопереходных металлов: личный взгляд . Springer Science & Business Media. ISBN 978-0-387-09848-7 .
- ^ Эллис, Дж. Э. (2003). «Анионы карбонила металлов: из [Fe(CO) 4 ] 2− [Hf(CO) 6 ] 2− и далее». Металлоорганические соединения . 22 (17): 3322–3338. doi : 10.1021/om030105l .
- ^ Поуп, Майкл Т.; Мюллер, Ахим (1997). «Химия полиоксометаллатов: старая область с новыми измерениями в нескольких дисциплинах». Angewandte Chemie, международное издание . 30 : 34–48. дои : 10.1002/anie.199100341 .
- ^ Ноллет, Лео ML, изд. (2000). Справочник по анализу воды . Нью-Йорк, штат Нью-Йорк: Марсель Деккер. стр. 280–288. ISBN 978-0-8247-8433-1 .
- ^ Тамадон, Фархад; Зеппельт, Конрад (07 января 2013 г.). «Неуловимые галогениды VCl 5, MoCl 6 и ReCl 6». Angewandte Chemie, международное издание . 52 (2): 767–769. дои : 10.1002/anie.201207552 . ПМИД 23172658 .
- ^ Стифель, Эдвард И., «Соединения молибдена», Энциклопедия химической технологии Кирка-Отмера , Нью-Йорк: Джон Уайли, номер документа : 10.1002/0471238961.1315122519200905.a01.pub3 , ISBN 9780471238966
- ^ Уолтон, Ричард А.; Фанвик, Филипп Э.; Джиролами, Грегори С.; Мурильо, Карлос А.; Джонстон, Эрик В. (2014). Джиролами, Грегори С.; Саттельбергер, Альфред П. (ред.). Неорганические синтезы: Том 36 . Джон Уайли и сыновья. стр. 78–81. дои : 10.1002/9781118744994.ch16 . ISBN 978-1118744994 .
- ^ Драго, Рассел С.; Лонг, Джон Р.; Космано, Ричард (1 июня 1982 г.). «Сравнение координационной химии и индуктивного переноса через связь металл-металл в аддуктах карбоксилатов диродия и димолибдена». Неорганическая химия . 21 (6): 2196–2202. дои : 10.1021/ic00136a013 . ISSN 0020-1669 .
- ^ Лэнсдаун, Арканзас (1999). Смазка дисульфид молибдена . Трибология и инженерия интерфейсов. Том. 35. Эльзевир. ISBN 978-0-444-50032-8 .
- ^ Мелчерт, Крейг. «Греческий молибдос как заимствованное из лидийского языка» (PDF) . Университет Северной Каролины в Чапел-Хилл . Архивировано (PDF) из оригинала 31 декабря 2013 г. Проверено 23 апреля 2011 г.
- ^ «История молибдена» . Международная молибденовая ассоциация. Архивировано из оригинала 22 июля 2013 г.
- ^ Случайное использование молибдена в старом мече привело к созданию нового сплава . Американский институт железа и стали. 1948 год.
- ^ Ван дер Крогт, Питер (10 января 2006 г.). «Молибден» . Элементимология и элементы Multidict . Архивировано из оригинала 23 января 2010 г. Проверено 20 мая 2007 г.
- ^ Перейти обратно: а б Ганьон, Стив. «Молибден» . Джефферсон Сайенс Ассошиэйтс, ООО. Архивировано из оригинала 26 апреля 2007 г. Проверено 6 мая 2007 г.
- ^ Шееле, CWK (1779 г.). «Versuche mit Wasserbley; Молибдена» . Шведская наука. Академия. Действия . 40 : 238.
- ^ Хьельм, П.Дж. (1788). «Опыты с молибденом и восстановление одной и той же Земли» . Свенска Ветенск. Академ. Хэндлингар . 49 :268.
- ^ Хойт, Сэмюэл Лесли (1921). Металлография . Том. 2. МакГроу-Хилл.
- ^ Крупп, Альфред; Вильдбергер, Андреас (1888). Металлические сплавы: Практическое руководство по изготовлению всех видов сплавов, амальгам и припоев, используемых металлистами... с приложением по окраске сплавов . HC Baird & Co. с. 60.
- ^ Гупта, СК (1992). Добывающая металлургия молибдена . ЦРК Пресс. ISBN 978-0-8493-4758-0 .
- ^ Райх, Леонард С. (22 августа 2002 г.). Создание американских промышленных исследований: наука и бизнес в Ge and Bell, 1876–1926 гг . Издательство Кембриджского университета. п. 117. ИСБН 978-0521522373 . Архивировано из оригинала 9 июля 2014 г. Проверено 7 апреля 2016 г.
- ^ Воукс, Фрэнк Маркус (1963). Молибденовые месторождения Канады . п. 3.
- ^ Химические свойства молибдена - Влияние молибдена на здоровье - Воздействие молибдена на окружающую среду. Архивировано 20 января 2016 г. в Wayback Machine . lenntech.com
- ^ Кин, Сэм (6 июня 2011 г.). Исчезающая ложка: и другие правдивые истории о безумии, любви и истории мира из периодической таблицы элементов (иллюстрированное издание). Книги Бэк-Бэй. стр. 88–89. ISBN 978-0-316-05163-7 .
- ^ Миллхолланд, Рэй (август 1941 г.). «Битва миллиардов: американская промышленность мобилизует машины, материалы и людей для такой масштабной работы, как рытье 40 Панамских каналов за один год» . Popular Science : 61. Архивировано из оригинала 9 июля 2014 г. Проверено 7 апреля 2016 г.
- ^ Перейти обратно: а б с д и ж г час Консидайн, Гленн Д., изд. (2005). «Молибден». Химическая энциклопедия Ван Ностранда . Нью-Йорк: Wiley-Interscience. стр. 1038–1040. ISBN 978-0-471-61525-5 .
- ^ Джамбор, JL; и др. (2002). «Новые названия минералов» (PDF) . Американский минералог . 87 : 181. Архивировано (PDF) из оригинала 10 июля 2007 г. Проверено 9 апреля 2007 г.
- ^ Перейти обратно: а б «Статистика и информация по молибдену» . Геологическая служба США. 10 мая 2007 г. Архивировано из оригинала 19 мая 2007 г. Проверено 10 мая 2007 г.
- ^ Перейти обратно: а б Себеник, Роджер Ф.; Буркин, А. Ричард; Дорфлер, Роберт Р.; Лаферти, Джон М.; Лейхтфрид, Герхард; Мейер-Грюнов, Хартмут; Митчелл, Филип CH; Вукасович Марк С.; Черч, Дуглас А.; Ван Рипер, Гэри Г.; Гиллиланд, Джеймс С.; Тилке, Стэнли А. (2000). «Молибден и соединения молибдена». Энциклопедия промышленной химии Ульмана . дои : 10.1002/14356007.a16_655 . ISBN 3527306730 . S2CID 98762721 .
- ^ Гупта, СК (1992). Добывающая металлургия молибдена . ЦРК Пресс. стр. 1–2. ISBN 978-0-8493-4758-0 .
- ^ «Динамические цены и графики на молибден» . InfoMine Inc. 2007. Архивировано из оригинала 8 октября 2009 г. Проверено 7 мая 2007 г.
- ^ «LME запустит контракты на второстепенные металлы во втором полугодии 2009 года» . Лондонская биржа металлов. 04 сентября 2008 г. Архивировано из оригинала 22 июля 2012 г. Проверено 28 июля 2009 г.
- ^ Лангедал, М. (1997). «Распространение хвостохранилищ в водосборном бассейне Кнабена-Квина, Норвегия, 1: Оценка береговых отложений как среды отбора проб для регионального геохимического картирования». Журнал геохимических исследований . 58 (2–3): 157–172. Бибкод : 1997JCExp..58..157L . дои : 10.1016/S0375-6742(96)00069-6 .
- ^ Коффман, Пол Б. (1937). «Возникновение нового металла: рост и успех компании Climax Molybdenum». Журнал бизнеса Чикагского университета . 10:30 . дои : 10.1086/232443 .
- ^ «Молибден» . Использование в промышленности . Лондонская биржа металлов. Архивировано из оригинала 10 марта 2012 г.
- ^ Перейти обратно: а б «Молибден» . AZoM.com Pty. Limited. 2007. Архивировано из оригинала 14 июня 2011 г. Проверено 6 мая 2007 г.
- ^ (2023) Марки и свойства нержавеющей стали. Международная молибденовая ассоциация. https://www.imoa.info/molybdenum-uses/molybdenum-grade-stainless-steels/steel-grades.php?m=1683978651&
- ^ Смоллвуд, Роберт Э. (1984). «ТЗМ Моли Сплав» . Специальная техническая публикация ASTM 849: Тугоплавкие металлы и их промышленное применение: симпозиум . АСТМ Интернешнл. п. 9. ISBN 978-0803102033 .
- ^ «Совместимость сплава на основе молибдена ТЗМ с LiF-BeF 2 -ThF 4 -UF 4 » . Отчет Национальной лаборатории Ок-Ридж. Декабрь 1969 г. Архивировано из оригинала 10 июля 2011 г. Проверено 2 сентября 2010 г.
- ^ Леви, М. (1965). «Система защитного покрытия для возвращаемой машины из сплава ТЗМ» (PDF) . Армия США . Проверено 3 июня 2024 г.
- ^ Ян, Чжи; Ху, Кэ (2018). «Диффузионная сварка сплава ТЗМ и сплава WRe методом искрово-плазменного спекания». Журнал сплавов и соединений . 764 : 582–590. дои : 10.1016/j.jallcom.2018.06.111 .
- ^ Патент КНР 109590476B
- ^ Тренто, Чин (27 декабря 2023 г.). «Приготовление и применение сплава ТЗМ» . Стэнфордские продвинутые материалы . Проверено 3 июня 2024 г.
- ^ Кабберли, Вашингтон; Бакерджян, Рамон (1989). Справочник инженера-инженера и инженера-технолога . Общество инженеров-технологов. п. 421. ИСБН 978-0-87263-351-3 .
- ^ Лал, С.; Патил, Р.С. (2001). «Мониторинг атмосферного поведения NO x от автомобильного движения». Экологический мониторинг и оценка . 68 (1): 37–50. дои : 10.1023/А:1010730821844 . ПМИД 11336410 . S2CID 20441999 .
- ^ Ланкастер, Джек Л. «Глава 4: Физические детерминанты контраста» (PDF) . Физика медицинской рентгеновской визуализации . Центр медицинских наук Техасского университета. Архивировано из оригинала (PDF) 10 октября 2015 г.
- ^ Грей, Теодор (2009). Элементы . Черный Пес и Левенталь. стр. 105–107. ISBN 1-57912-814-9 .
- ^ Готшалк, А. (1969). «Технеций-99м в клинической ядерной медицине». Ежегодный обзор медицины . 20 (1): 131–40. дои : 10.1146/annurev.me.20.020169.001023 . ПМИД 4894500 .
- ^ Винер, В. (1967). «Дисульфид молибдена как смазка: обзор фундаментальных знаний» (PDF) . Носить . 10 (6): 422–452. дои : 10.1016/0043-1648(67)90187-1 . hdl : 2027.42/33266 .
- ^ Топсе, Х.; Клаузен, Б.С.; Массот, FE (1996). Катализ гидроочистки, наука и технология . Берлин: Springer-Verlag.
- ^ Моулсон, Эй Джей; Герберт, Дж. М. (2003). Электрокерамика: материалы, свойства, применение . Джон Уайли и сыновья. п. 141. ИСБН 978-0-471-49748-6 .
- ^ Международная молибденовая ассоциация. Архивировано 9 марта 2008 г. в Wayback Machine . imoa.info.
- ^ Фиерро, JGL, изд. (2006). Оксиды металлов, химия и применение . ЦРК Пресс. стр. 414–455.
- ^ Сенти, Г.; Кавани, Ф.; Трифиро, Ф. (2001). Селективное окисление гетерогенным катализом . Издательство Kluwer Academic/Plenum. стр. 363–384.
- ^ Горачек, Ян; Ахметзянова Ульяна; Скухровцова, Ленка; Тишлер, Зденек; де Пас Кармона, Эктор (1 апреля 2020 г.). «Катализаторы MoNx, MoCx и MoPx на оксиде алюминия для гидроочистки рапсового масла» . Прикладной катализ Б: Экология . 263 : 118328. Бибкод : 2020AppCB.26318328H . дои : 10.1016/j.apcatb.2019.118328 . ISSN 0926-3373 . S2CID 208758175 .
- ^ Де Карло, Саша; Харрис, Дж. Робин (2011). «Негативное окрашивание и крионегативное окрашивание макромолекул и вирусов на ТЭМ» . Микрон . 42 (2): 117–131. дои : 10.1016/j.micron.2010.06.003 . ПМЦ 2978762 . ПМИД 20634082 .
- ^ «Краски для проявления пластин ТСХ» (PDF) . Университет Макмастера.
- ^ Эверетт, ММ; Миллер, Вашингтон (1974). «Роль фосфорновольфрамовой и фосфорномолибденовой кислот в окрашивании соединительной ткани I. Гистохимические исследования». Гистохимический журнал . 6 (1): 25–34. дои : 10.1007/BF01011535 . ПМИД 4130630 .
- ^ Скотт, К.; Лайонс, ТВ; Беккер, А.; Шен, Ю.; Поултон, Юго-Запад; Чу, X.; Анбар, AD (2008). «Прослеживание ступенчатой оксигенации протерозойского океана». Природа . 452 (7186): 456–460. Бибкод : 2008Natur.452..456S . дои : 10.1038/nature06811 . ПМИД 18368114 . S2CID 205212619 .
- ^ Энемарк, Джон Х.; Куни, Дж. Джон А.; Ван, Цзюнь-Цзе; Холм, Р.Х. (2004). «Синтетические аналоги и реакционные системы, относящиеся к оксотрансферазам молибдена и вольфрама». хим. Преподобный . 104 (2): 1175–1200. дои : 10.1021/cr020609d . ПМИД 14871153 .
- ^ Мендель, Ральф Р.; Биттнер, Флориан (2006). «Клеточная биология молибдена». Biochimica et Biophysical Acta (BBA) - Исследования молекулярных клеток . 1763 (7): 621–635. дои : 10.1016/j.bbamcr.2006.03.013 . ПМИД 16784786 .
- ^ Расс Хилле; Джеймс Холл; Партха Басу (2014). «Моноядерные молибденовые ферменты» . хим. Преподобный . 114 (7): 3963–4038. дои : 10.1021/cr400443z . ПМК 4080432 . ПМИД 24467397 .
- ^ Кискер, К.; Шинделин, Х.; Баас, Д.; Рети, Дж.; Меккеншток, RU; Кронек, ПМХ (1999). «Структурное сравнение ферментов, содержащих кофактор молибдена» (PDF) . ФЭМС Микробиол. Преподобный . 22 (5): 503–521. дои : 10.1111/j.1574-6976.1998.tb00384.x . ПМИД 9990727 . Архивировано (PDF) из оригинала 10 августа 2017 г. Проверено 25 октября 2017 г.
- ^ Перейти обратно: а б Митчелл, Филипп CH (2003). «Обзор базы данных окружающей среды» . Международная молибденовая ассоциация. Архивировано из оригинала 18 октября 2007 г. Проверено 5 мая 2007 г.
- ^ Мендель, Ральф Р. (2013). «Глава 15 Метаболизм молибдена». В Банки, Люсия (ред.). Металломика и клетка . Ионы металлов в науках о жизни. Том. 12. Спрингер. doi : 10.1007/978-94-007-5561-10_15 (неактивен 31 января 2024 г.). ISBN 978-94-007-5560-4 .
{{cite book}}: CS1 maint: DOI inactive as of January 2024 (link) electronic-book ISBN 978-94-007-5561-1 ISSN 1559-0836 электронный- ISSN 1868-0402 - ^ Чи Чунг, Ли; Маркус В., Риббе; Илинь, Ху (2014). «Биохимия метилкофермента М-редуктазы: никелевый металлофермент, который катализирует заключительный этап синтеза и первый этап анаэробного окисления метана парникового газа». У Питера М.Х. Кронека; Марта Э. Соса Торрес (ред.). Металлозависимая биогеохимия газообразных соединений в окружающей среде . Ионы металлов в науках о жизни. Том. 14. Спрингер. стр. 147–174. дои : 10.1007/978-94-017-9269-1_6 . ISBN 978-94-017-9268-4 . ПМИД 25416393 .
- ^ Дос Сантос, Патрисия К.; Дин, Деннис Р. (2008). «Недавно открытая роль железо-серных кластеров» . ПНАС . 105 (33): 11589–11590. Бибкод : 2008PNAS..10511589D . дои : 10.1073/pnas.0805713105 . ПМЦ 2575256 . ПМИД 18697949 .
- ^ Шварц, Гюнтер; Белаиди, Абдель А. (2013). «Молибден в здоровье и болезнях человека». В Астрид Сигел; Хельмут Сигель; Роланд К.О. Сигел (ред.). Взаимосвязь между ионами незаменимых металлов и заболеваниями человека . Ионы металлов в науках о жизни. Том. 13. Спрингер. стр. 415–450. дои : 10.1007/978-94-007-7500-8_13 . ISBN 978-94-007-7499-5 . ПМИД 24470099 .
- ^ Мендель, Ральф Р. (2009). «Клеточная биология молибдена». Биофакторы . 35 (5): 429–34. дои : 10.1002/биоф.55 . ПМИД 19623604 . S2CID 205487570 .
- ^ Отчет о здоровье Блейлока , февраль 2010 г., стр. 3.
- ^ Коэн, HJ; Дрю, RT; Джонсон, Дж.Л.; Раджагопалан, К.В. (1973). «Молекулярные основы биологической функции молибдена. Связь между сульфитоксидазой и острой токсичностью бисульфита и SO 2 » . Труды Национальной академии наук Соединенных Штатов Америки . 70 (12, ч. 1–2): 3655–3659. Бибкод : 1973PNAS...70.3655C . дои : 10.1073/pnas.70.12.3655 . ПМК 427300 . ПМИД 4519654 .
- ^ Холлеман, Арнольд Ф.; Виберг, Эгон (2001). Неорганическая химия . Академическая пресса. п. 1384. ИСБН 978-0-12-352651-9 .
- ^ Керзон, MEJ; Кубота, Дж.; Бибби, Б.Г. (1971). «Экологическое воздействие молибдена на кариес». Журнал стоматологических исследований . 50 (1): 74–77. дои : 10.1177/00220345710500013401 . S2CID 72386871 .
- ^ Перейти обратно: а б «Информационная система оценки рисков: сводная информация о токсичности молибдена» . Окриджская национальная лаборатория. Архивировано из оригинала 19 сентября 2007 года . Проверено 23 апреля 2008 г.
- ^ Перейти обратно: а б Кофлан, член парламента (1983). «Роль молибдена в биологии человека». Журнал наследственных метаболических заболеваний . 6 (С1): 70–77. дои : 10.1007/BF01811327 . ПМИД 6312191 . S2CID 10114173 .
- ^ Барселу, Дональд Г.; Барселу, Дональд (1999). «Молибден». Клиническая токсикология . 37 (2): 231–237. дои : 10.1081/CLT-100102422 . ПМИД 10382558 .
- ^ Ян, Чунг С. (1980). «Исследование рака пищевода в Китае: обзор» (PDF) . Исследования рака . 40 (8, часть 1): 2633–44. ПМИД 6992989 . Архивировано (PDF) из оригинала 23 ноября 2015 г. Проверено 30 декабря 2011 г.
- ^ Нури, Мохсен; Чалиан, Хамид; Бахман, Атье; Моллахаджян, Хамид; и др. (2008). «Содержание молибдена и цинка в ногтях в группах населения с низкой и средней заболеваемостью раком пищевода» (PDF) . Архивы иранской медицины . 11 (4): 392–6. ПМИД 18588371 . Архивировано из оригинала (PDF) 19 июля 2011 г. Проверено 23 марта 2009 г.
- ^ Чжэн, Лю; и др. (1982). «Географическое распространение почв с дефицитом микроэлементов в Китае» . Акта Пед. Грех . 19 : 209–223. Архивировано из оригинала 05 февраля 2021 г. Проверено 25 июля 2020 г.
- ^ Тейлор, Филип Р.; Ли, Бинг; Доуси, Сэнфорд М.; Ли, Цзюнь-Яо; Ян, Чунг С.; Го, Ванде; Блот, Уильям Дж. (1994). «Профилактика рака пищевода: исследования по изменению питания в Линьсяне, Китай» (PDF) . Исследования рака . 54 (7 дополнений): 2029–2031 гг. ПМИД 8137333 . Архивировано (PDF) из оригинала 17 сентября 2016 г. Проверено 1 июля 2016 г.
- ^ Абумрад, Н. Н. (1984). «Молибден — это важный микроэлемент?» . Бюллетень Нью-Йоркской медицинской академии . 60 (2): 163–71. ПМК 1911702 . ПМИД 6426561 .
- ^ Смолинский, Б; Эйхлер, SA; Бухмайер, С.; Мейер, Дж. К.; Шварц, Г. (2008). «Специфические для сплайсинга функции гефирина в биосинтезе кофактора молибдена» . Журнал биологической химии . 283 (25): 17370–9. дои : 10.1074/jbc.M800985200 . ПМИД 18411266 .
- ^ Рейсс, Дж. (2000). «Генетика дефицита кофактора молибдена». Генетика человека . 106 (2): 157–63. doi : 10.1007/s004390051023 (неактивен 1 февраля 2024 г.). ПМИД 10746556 .
{{cite journal}}: CS1 maint: DOI неактивен по состоянию на февраль 2024 г. ( ссылка ) - ^ Гроппер, Сарин С.; Смит, Джек Л.; Карр, Тимоти П. (05 октября 2016 г.). Продвинутое питание и обмен веществ человека . Cengage Обучение. ISBN 978-1-337-51421-7 .
- ^ Тернлунд, младший; Киз, WR; Пайффер, Г.Л. (октябрь 1995 г.). «Абсорбция, выведение и удержание молибдена изучены с помощью стабильных изотопов у молодых мужчин при пяти приемах молибдена с пищей» . Американский журнал клинического питания . 62 (4): 790–796. дои : 10.1093/ajcn/62.4.790 . ISSN 0002-9165 . ПМИД 7572711 .
- ^ Саттл, Северная Каролина (1974). «Новейшие исследования медно-молибденового антагонизма» . Труды Общества питания . 33 (3): 299–305. дои : 10.1079/PNS19740053 . ПМИД 4617883 .
- ^ Хауэр, Джеральд Дефицит меди у крупного рогатого скота. Архивировано 10 сентября 2011 г. в Wayback Machine . Производители зубров из Альберты. По состоянию на 16 декабря 2010 г.
- ^ Никель, Вт (2003). «Тайна секреции неклассического белка, современный взгляд на грузовые белки и потенциальные маршруты экспорта» . Евро. Дж. Биохим. 270 (10): 2109–2119. дои : 10.1046/j.1432-1033.2003.03577.x . ПМИД 12752430 .
- ^ Брюэр Дж.Дж.; Хедера, П.; Клюин, К.Дж.; Карлсон, М.; Аскари, Ф.; Дик, РБ; Ситтерли, Дж.; Финк, Дж. К. (2003). «Лечение болезни Вильсона тетратиомолибдатом аммония: III. Начальная терапия у 55 пациентов с неврологическими заболеваниями и последующее лечение цинком». Арч Нейрол . 60 (3): 379–85. дои : 10.1001/archneur.60.3.379 . ПМИД 12633149 .
- ^ Брюэр, Дж.Дж.; Дик, РД; Гровер, ДК; Леклер, В.; Ценг, М.; Вича, М.; Пиента, К.; Редман, Б.Г.; Джахан, Т.; Сондак, В.К.; Стродерман, М.; Лекарпантье, Г.; Мерайвер, С.Д. (2000). «Лечение метастатического рака тетратиомолибдатом, антимедным и антиангиогенным агентом: исследование фазы I». Клинические исследования рака . 6 (1): 1–10. PMID 10656425 .
- ^ Медицинский институт (2000). «Молибден» . Рекомендуемая диетическая норма витамина А, витамина К, мышьяка, бора, хрома, меди, йода, железа, марганца, молибдена, никеля, кремния, ванадия и цинка . Вашингтон, округ Колумбия: Издательство национальных академий. стр. 420–441. дои : 10.17226/10026 . ISBN 978-0-309-07279-3 . ПМИД 25057538 . S2CID 44243659 .
- ^ «Обзор диетических эталонных значений для населения ЕС, составленный Группой EFSA по диетическим продуктам, питанию и аллергиям» (PDF) . 2017. Архивировано из оригинала (PDF) 28 августа 2017 г. Проверено 10 сентября 2017 г.
- ^ Допустимые верхние уровни потребления витаминов и минералов (PDF) , Европейское управление по безопасности пищевых продуктов, 2006 г., заархивировано из оригинала (PDF) 16 марта 2016 г. , получено 10 сентября 2017 г.
- ^ «Федеральный реестр, 27 мая 2016 г. Маркировка пищевых продуктов: пересмотренная версия этикеток с информацией о пищевой ценности и пищевых добавках. Страница FR 33982» (PDF) . Архивировано (PDF) из оригинала 8 августа 2016 г. Проверено 10 сентября 2017 г.
- ^ «Справочник по дневной норме базы данных этикеток пищевых добавок (DSLD)» . База данных этикеток пищевых добавок (DSLD) . Архивировано из оригинала 7 апреля 2020 года . Проверено 16 мая 2020 г.
- ^ «Паспорт безопасности материала – Молибден» . Компания REMBAR, Inc. 19 сентября 2000 г. Архивировано из оригинала 23 марта 2007 года . Проверено 13 мая 2007 г.
- ^ «Паспорт безопасности материала – молибденовый порошок» . CERAC, Inc., 23 февраля 1994 г. Архивировано из оригинала 8 июля 2011 г. Проверено 19 октября 2007 г.
- ^ «Документация NIOSH по молибдену IDLH» . Национальный институт охраны труда и здоровья. 16 августа 1996 г. Архивировано из оригинала 7 августа 2007 г. Проверено 31 мая 2007 г.
- ^ «CDC - Карманный справочник NIOSH по химическим опасностям - Молибден» . www.cdc.gov . Архивировано из оригинала 20 ноября 2015 г. Проверено 20 ноября 2015 г.
Библиография
[ редактировать ]- Письмо Джулио Кандиды господину Винченцо Петанье – Об образовании молибдена . Неаполь: Джузеппе Мария Порчелли. 1785.
Внешние ссылки
[ редактировать ]- Молибден в Периодической таблице видео (Ноттингемский университет)
- Минерал и геологоразведка - Карта мировых производителей молибдена, 2009 г.
- "Горное дело" Популярная механика , июль 1935 г., стр. 63–64.
- Сайт глобальной информации о молибдене
- CDC - Карманный справочник NIOSH по химическим опасностям






