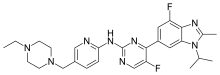
Абемациклиб
 | |
| Клинические данные | |
|---|---|
| Произношение | / ə ˌ b ɛ m ə ˈ s aɪ k l ɪ b / э- БЭМ -э- СИ -зажим |
| Торговые названия | Верзенио, Верзениос, Рамивен и другие |
| Другие имена | LY2835219 |
| AHFS / Drugs.com | Монография |
| Данные лицензии |
|
| Маршруты администрация | Через рот |
| код АТС | |
| Юридический статус | |
| Юридический статус | |
| Фармакокинетические данные | |
| Биодоступность | 45% |
| Связывание с белками | 96.3% |
| Период полувыведения | 18,3 часа |
| Экскреция | 81% через фекалии, 3% через мочу |
| Идентификаторы | |
| Номер CAS | |
| ПабХим CID | |
| Лекарственный Банк | |
| ХимическийПаук | |
| НЕКОТОРЫЙ | |
| КЕГГ | |
| ХЭМБЛ | |
| PDB-лиганд | |
| Панель управления CompTox ( EPA ) | |
| Информационная карта ECHA | 100.233.787 |
| Химические и физические данные | |
| Формула | С 27 Ч 32 Ж 2 Н 8 |
| Молярная масса | 506.606 g·mol −1 |
| 3D model ( JSmol ) | |
Абемациклиб под торговой маркой Verzenio , продаваемый , среди прочего, , представляет собой лекарство для лечения распространенного или метастатического рака молочной железы . Он был разработан компанией Eli Lilly и действует как ингибитор CDK, селективный в отношении CDK4 и CDK6 . [ 4 ]
назвало его прорывной терапией рака молочной железы . В октябре 2015 года Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) [ 5 ]
В сентябре 2017 года FDA одобрило его для использования в США для лечения некоторых видов рака молочной железы. [ 6 ]
Медицинское использование
[ редактировать ]С сентября 2017 года абемациклиб был одобрен в США для «взрослых, у которых диагностирован гормональный рецептор (HR)-положительный и отрицательный по рецептору человеческого эпидермального фактора роста 2 (HER2) распространенный или метастатический рак молочной железы, который прогрессировал после приема терапии, которая изменяет состояние пациента». гормоны». [ 6 ]
В исследованиях, в которых сравнивали фулвестрант в сочетании с абемациклибом с фулвестрантом в сочетании с плацебо у пациентов с раком молочной железы, выживаемость без прогрессирования при терапии абемациклибом составила в среднем 16,4 месяца по сравнению с 9,3 месяца в группе плацебо.
Побочные эффекты
[ редактировать ]Побочными эффектами, которые наблюдались у 20% или более пациентов в исследованиях, были диарея, тошнота и рвота, лейкопения (низкое количество лейкоцитов), включая нейтропению , анемия (низкое количество эритроцитов), тромбоцитопения (низкое количество тромбоцитов), боль в животе, инфекции, усталость , снижение аппетита и головная боль. [ 7 ] [ 8 ]
Взаимодействия
[ редактировать ]Поскольку абемациклиб в основном метаболизируется ферментом печени CYP3A4 ингибиторы этого фермента (такие как кетоконазол , ожидается, что ) повысят его концентрацию в плазме крови . И наоборот, индукторы CYP3A4 снижают концентрацию абемациклиба в плазме, как было показано в исследовании с рифампицином . [ 8 ]
Фармакология
[ редактировать ]Механизм действия
[ редактировать ]Как и родственные препараты палбоциклиб и рибоциклиб , абемациклиб ингибирует ферменты циклинзависимую киназу 4 (CDK4) и циклинзависимую киназу 6 (CDK6). [ 8 ] Эти ферменты ответственны за фосфорилирование и, таким образом, дезактивацию белка ретинобластомы , который играет роль в переходе клеточного цикла от фазы G1 ( первый разрыв ) к фазе S ( синтез ). [ 9 ] Блокирование этого пути предотвращает переход клеток в S-фазу, тем самым вызывая апоптоз (гибель клеток). [ 8 ] Анализ in vitro с использованием линий раковых клеток показал, что абемациклиб индуцирует неапоптотическую гибель клеток, характеризующуюся образованием цитоплазматических вакуолей, происходящих из лизосом. Этот результат предполагает, что может существовать иной механизм действия, чем ингибирование циклин-зависимой киназы. [ 10 ]
Фармакокинетика
[ редактировать ]
После перорального приема абсолютная биодоступность составляет 45%. Наивысшие концентрации в плазме крови достигаются в среднем через 8 часов (диапазон: 4,1–24,0 часа). При попадании в кровообращение 96,3% абемациклиба связывается с белками плазмы . Вещество метаболизируется преимущественно ферментом печени CYP3A4 до N -дезэтилабемациклиба (М2), и в меньшей степени до гидроксипроизводных (М18, М20) и другого окислительного метаболита (М1). Эти метаболиты имеют высокую скорость связывания с белками плазмы, аналогичную исходному веществу. [ 8 ]
Абемациклиб выводится преимущественно с калом (81%) и в незначительной степени с мочой (3%). Период полувыведения составляет в среднем 18,3 часа. [ 8 ]
Клинические испытания
[ редактировать ]В мае 2014 года было объявлено об успешных испытаниях против предварительно леченного метастатического рака молочной железы для фазы I. [ 11 ] II этап в декабре 2014 г. [ 12 ] и этап III в феврале 2017 года. [ 13 ] Абемациклиб был одобрен FDA в сентябре 2017 года либо в сочетании с фулвестрантом, либо в качестве монотерапии для женщин с HR+, HER2-распространенным или метастатическим раком молочной железы, который прогрессировал на фоне приема эндокринной терапии. [ 14 ] Абемациклиб был одобрен для адъювантного лечения HR+, HER2- и адъювантного рака молочной железы с высоким риском рецидива в марте 2023 года. [ 15 ] [ 16 ]
По состоянию на 2023 год абемациклиб участвовал в двух фазы III клинических исследованиях :
- В исследовании SARC041 абемациклиб сравнивают с плацебо у пациентов с поздней стадией дедифференцированной липосаркомы. [ 17 ]
- В исследовании CYCLONE 3 абемациклиб сравнивается с плацебо в сочетании с абиратероном и преднизоном у пациентов с метастатическим гормоночувствительным раком простаты высокого риска. [ 18 ]
Абемациклиб находится в фазе I и II клинических исследований при плоскоклеточном раке головы и шеи . [ 19 ] рак желчевыводящих путей , [ 20 ] опухоли головного мозга , [ 21 ] [ 22 ] [ 23 ] нейрофиброматоз , [ 24 ] саркома Капоши , [ 25 ] метастатический почечно-клеточный рак , [ 26 ] и лимфома мантийных клеток . [ 27 ]
Химия
[ редактировать ]Абемациклиб можно синтезировать в четыре этапа с использованием реакции Сузуки с последующим аминированием Бухвальда-Хартвига , причем последней стадией является восстановительное аминирование с использованием реакции Лейкарта . [ 28 ]
Ссылки
[ редактировать ]- ^ «Верзенио (Eli Lilly Australia Pty Ltd)» . Управление терапевтических товаров (TGA) . 28 сентября 2022 года. Архивировано из оригинала 18 марта 2023 года . Проверено 9 апреля 2023 г.
- ^ «Краткая основа решения (SBD) для Верзенио» . Здоровье Канады . 23 октября 2014 г. Архивировано из оригинала 31 мая 2022 г. Проверено 29 мая 2022 г.
- ^ «ЭПАР Верзениос» . Европейское агентство по лекарственным средствам . 27 сентября 2018 года . Проверено 17 июня 2024 г.
- ^ Лу Дж (август 2015 г.). «Палбоциклиб: первый в своем классе ингибитор CDK4/CDK6 для лечения распространенного рака молочной железы с положительным статусом гормона» . Журнал гематологии и онкологии . 8 (1): 98. дои : 10.1186/s13045-015-0194-5 . ПМЦ 4534142 . ПМИД 26264704 .
- ^ Диджиулио С (8 октября 2015 г.). «Абемациклиб признан FDA революционной терапией при раке молочной железы» . Время онкологии . Журналы LWW. Архивировано из оригинала 4 июня 2021 года . Проверено 30 марта 2016 г.
- ^ Перейти обратно: а б «FDA одобряет новое лечение некоторых распространенных или метастатических видов рака молочной железы» (пресс-релиз). Управление по контролю за продуктами и лекарствами . 28 сентября 2017 года. Архивировано из оригинала 23 апреля 2019 года . Проверено 29 сентября 2017 г.
- ^ Drugs.com : Монография по абемациклибу . По состоянию на 22 ноября 2017 г.
- ^ Перейти обратно: а б с д и ж «Основная информация о назначении Верзенио» (PDF) . Сентябрь 2017 г. Архивировано (PDF) из оригинала 5 сентября 2021 г. Проверено 22 ноября 2017 г. .
- ^ Гудрич Д.В., Ван Н.П., Цянь Ю.В., Ли Э.Ю. , Ли WH (октябрь 1991 г.). «Продукт гена ретинобластомы регулирует развитие фазы G1 клеточного цикла». Клетка . 67 (2): 293–302. дои : 10.1016/0092-8674(91)90181-w . ПМИД 1655277 . S2CID 12990398 .
- ^ Хино Х., Ирияма Н., Кокуба Х. и др. (июнь 2020 г.). «Абемациклиб индуцирует атипичную клеточную гибель раковых клеток, характеризующуюся образованием цитоплазматических вакуолей, происходящих из лизосом» . Наука о раке . 111 (6): 2132–2145. дои : 10.1111/cas.14419 . ПМК 7293084 . ПМИД 32304130 .
- ^ «LY2835219 демонстрирует сильную активность одного агента в предварительном исследовании метастатического рака молочной железы» . Архивировано из оригинала 18 сентября 2015 года . Проверено 8 января 2016 г.
- ^ Диклер М.Н., Толани С.М., Руго Х.С., Кортес Дж., Диерас В., Патт Д. и др. (сентябрь 2017 г.). «MONARCH 1, Исследование фазы II абемациклиба, ингибитора CDK4 и CDK6, в качестве единственного агента у пациентов с рефрактерной HR. + /HER2 - Метастатический рак молочной железы» . Clinical Cancer Research . 23 (17): 5218–5224. doi : -17-0754 . PMC 5581697. 10.1158/ 1078-0432.CCR PMID 28533223 .
{{cite journal}}: CS1 maint: переопределенная настройка ( ссылка ) - ^ Следж Г.В., Той М., Невен П., Зон Дж., Иноуэ К., Пивот X и др. (сентябрь 2017 г.). «МОНАРХ 2: Абемациклиб в сочетании с фулвестрантом у женщин с прогрессирующим раком молочной железы HR + / HER2-, у которых прогрессировало во время приема эндокринной терапии». Журнал клинической онкологии . 35 (25): 2875–2884. дои : 10.1200/JCO.2017.73.7585 . ПМИД 28580882 .
{{cite journal}}: CS1 maint: переопределенная настройка ( ссылка ) - ^ Центр оценки и исследований лекарств (9 февраля 2019 г.). «FDA одобрило абемациклиб для лечения HR-положительного и HER2-негативного рака молочной железы» . FDA .
- ^ Ройс М., Осгуд С., Малки Ф., Блумквист Е., Пирс В.Ф., Рой А. и др. (апрель 2022 г.). «Краткий обзор одобрения FDA: абемациклиб в сочетании с эндокринной терапией раннего рака молочной железы высокого риска» . Журнал клинической онкологии . 40 (11): 1155–1162. дои : 10.1200/JCO.21.02742 . ПМЦ 8987222 . ПМИД 35084948 .
{{cite journal}}: CS1 maint: переопределенная настройка ( ссылка ) - ^ Центр оценки и исследований лекарств (24 марта 2023 г.). «FDA DISCO Burst Edition: одобрение FDA Верзенио (абемациклиба) для эндокринной терапии у пациентов с HR-положительным, HER2-отрицательным, лимфатическим положительным раком молочной железы на ранней стадии» . FDA .
- ^ «SARC041: Исследование абемациклиба по сравнению с плацебо у пациентов с прогрессирующей дедифференцированной липосаркомой» . www.clinicaltrials.gov . Проверено 20 июля 2023 г.
- ^ «Исследование абемациклиба (LY2835219) с абиратероном у мужчин с раком простаты, который распространился на другие части тела и, как ожидается, будет реагировать на гормональное лечение (метастатический гормон-чувствительный рак простаты) (ЦИКЛОН 3)» . www.clinicaltrials.gov . Проверено 20 июля 2023 г.
- ^ «Иммунная модуляция абемациклибом при HNSCC. (Испытание AIM)» . www.clinicaltrials.gov . Проверено 20 июля 2023 г.
- ^ «Исследование по оценке абемациклиба при распространенной карциноме желчных путей» . www.clinicaltrials.gov . Проверено 20 июля 2023 г.
- ^ «Абемациклиб (LY2835219) у пациентов с рецидивирующими первичными опухолями головного мозга» . www.clinicaltrials.gov . Проверено 20 июля 2023 г.
- ^ «Абемациклиб у детей с DIPG или рецидивирующими/рефрактерными солидными опухолями (AflacST1501)» . www.clinicaltrials.gov . Проверено 20 июля 2023 г.
- ^ «Абемациклиб с бевацизумабом у пациентов с рецидивирующим ГБМ с потерей CDKN2A/B или усилением или амплификацией CDK4/6» . www.clinicaltrials.gov . Проверено 20 июля 2023 г.
- ^ «Ингибитор циклин-зависимой киназы (CDK) 4/6 абемациклиб для лечения атипичных нейрофибром, связанных с нейрофиброматозом I типа (NF1)» . www.clinicaltrials.gov . Проверено 20 июля 2023 г.
- ^ «Абемациклиб у пациентов с ВИЧ-ассоциированной и ВИЧ-отрицательной саркомой Капоши» . www.clinicaltrials.gov . Проверено 20 июля 2023 г.
- ^ «Исследование абемациклиба в комбинации с сунитинибом при метастатическом почечно-клеточном раке» . www.clinicaltrials.gov . Проверено 20 июля 2023 г.
- ^ «Исследование LY2835219 при лимфоме из мантийных клеток» . www.clinicaltrials.gov . Проверено 20 июля 2023 г.
- ^ Фредерик М.О., Кьелл Д.П. (февраль 2015 г.). «Синтез абемациклиба с использованием реакции Лейкарта-Валлаха». Буквы тетраэдра . 56 (7): 949–951. дои : 10.1016/j.tetlet.2014.12.082 .