Воспаление
Эта статья нуждается в более надежных медицинских ссылках для проверки или слишком сильно полагается на первоисточники . ( март 2021 г. ) |  |
| Воспаление | |
|---|---|
 | |
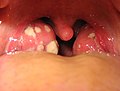
| К основным признакам воспаления относятся: боль, жар, покраснение, отек и потеря функции. Некоторые из этих показателей можно увидеть здесь из-за аллергической реакции. | |
| Специальность | Иммунология , ревматология |
| Symptoms | Heat, pain, redness, swelling |
| Complications | Asthma, pneumonia, autoimmune diseases |
| Duration | Acute: few days Chronic: up to many months, or years |
| Causes | Infection, physical injury, autoimmune disorder |
Воспаление (от латинского патогены inflammatio ) — часть биологического ответа тканей организма на вредные раздражители, такие как , поврежденные клетки или раздражители . [ 1 ] [ 2 ] Пять основных признаков — это жар, боль, покраснение, отек и потеря функции (лат. «calor» , « dolor» , «rubor» , «опухоль » и «functio laesa» ).
Воспаление является общей реакцией и поэтому считается механизмом врожденного иммунитета , тогда как адаптивный иммунитет специфичен для каждого патогена. [ 3 ]
Inflammation is a protective response involving immune cells, blood vessels, and molecular mediators. The function of inflammation is to eliminate the initial cause of cell injury, clear out damaged cells and tissues, and initiate tissue repair. Too little inflammation could lead to progressive tissue destruction by the harmful stimulus (e.g. bacteria) and compromise the survival of the organism. However inflammation can also have negative effects.[4] Слишком сильное воспаление в форме хронического воспаления связано с различными заболеваниями, такими как сенная лихорадка , пародонтоз , атеросклероз и остеоартрит .
Inflammation can be classified as acute or chronic. Acute inflammation is the initial response of the body to harmful stimuli, and is achieved by the increased movement of plasma and leukocytes (in particular granulocytes) from the blood into the injured tissues. A series of biochemical events propagates and matures the inflammatory response, involving the local vascular system, the immune system, and various cells in the injured tissue. Prolonged inflammation, known as chronic inflammation, leads to a progressive shift in the type of cells present at the site of inflammation, such as mononuclear cells, and involves simultaneous destruction and healing of the tissue.
Inflammation has also been classified as Type 1 and Type 2 based on the type of cytokines and helper T cells (Th1 and Th2) involved.[5]
Meaning
[edit]The earliest known reference for the term inflammation is around the early 15th century. The word root comes from Old French inflammation around the 14th century, which then comes from Latin inflammatio or inflammationem. Literally, the term relates to the word "flame", as the property of being "set on fire" or "to burn".[6]
The term inflammation is not a synonym for infection. Infection describes the interaction between the action of microbial invasion and the reaction of the body's inflammatory response—the two components are considered together in discussion of infection, and the word is used to imply a microbial invasive cause for the observed inflammatory reaction. Inflammation, on the other hand, describes just the body's immunovascular response, regardless of cause. But, because of the two are often correlated, words ending in the suffix -itis (which means inflammation) are sometimes informally described as referring to infection: for example, the word urethritis strictly means only "urethral inflammation", but clinical health care providers usually discuss urethritis as a urethral infection because urethral microbial invasion is the most common cause of urethritis. However, the inflammation–infection distinction is crucial in situations in pathology and medical diagnosis that involve inflammation that is not driven by microbial invasion, such as cases of atherosclerosis, trauma, ischemia, and autoimmune diseases (including type III hypersensitivity).
Causes
[edit]- Burns[7]
- Frostbite
- Physical injury, blunt or penetrating[8]
- Foreign bodies, including splinters, dirt and debris
- Trauma[7]
- Ionizing radiation
Biological:
- Infection by pathogens[7]
- Immune reactions due to hypersensitivity
- Stress
Chemical:[7]
Psychological:
- Excitement[9]
Types
[edit]
|
| Acute | Chronic | |
|---|---|---|
| Causative agent | Bacterial pathogens, injured tissues | Persistent acute inflammation due to non-degradable pathogens, viral infection, persistent foreign bodies, or autoimmune reactions |
| Major cells involved | neutrophils (primarily), basophils (inflammatory response), and eosinophils (response to helminth worms and parasites), mononuclear cells (monocytes, macrophages) | Mononuclear cells (monocytes, macrophages, lymphocytes, plasma cells), fibroblasts |
| Primary mediators | Vasoactive amines, eicosanoids | IFN-γ and other cytokines, growth factors, reactive oxygen species, hydrolytic enzymes |
| Onset | Immediate | Delayed |
| Duration | Few days | Up to many months, or years |
| Outcomes | Resolution, abscess formation, chronic inflammation | Tissue destruction, fibrosis, necrosis |
Acute
[edit]Acute inflammation is a short-term process, usually appearing within a few minutes or hours and begins to cease upon the removal of the injurious stimulus.[10] It involves a coordinated and systemic mobilization response locally of various immune, endocrine and neurological mediators of acute inflammation. In a normal healthy response, it becomes activated, clears the pathogen and begins a repair process and then ceases.[11]
Acute inflammation occurs immediately upon injury, lasting only a few days.[12] Cytokines and chemokines promote the migration of neutrophils and macrophages to the site of inflammation.[12] Pathogens, allergens, toxins, burns, and frostbite are some of the typical causes of acute inflammation.[12] Toll-like receptors (TLRs) recognize microbial pathogens.[12] Acute inflammation can be a defensive mechanism to protect tissues against injury.[12] Inflammation lasting 2–6 weeks is designated subacute inflammation.[12][13]
Cardinal signs
[edit]| English | Latin |
|---|---|
| Redness | Rubor |
| Swelling | Tumor |
| Heat | Calor |
| Pain | Dolor |
| Loss of function | Functio laesa[b] |
Inflammation is characterized by five cardinal signs,[16][17] (the traditional names of which come from Latin):
The first four (classical signs) were described by Celsus (c. 30 BC–38 AD).[19]
Pain is due to the release of chemicals such as bradykinin and histamine that stimulate nerve endings.[16] (Acute inflammation of the lung (usually as in response to pneumonia) does not cause pain unless the inflammation involves the parietal pleura, which does have pain-sensitive nerve endings.[16]) Heat and redness are due to increased blood flow at body core temperature to the inflamed site. Swelling is caused by accumulation of fluid.
Loss of function
[edit]The fifth sign, loss of function, is believed to have been added later by Galen,[20] Thomas Sydenham[21] or Rudolf Virchow.[10][16][17] Examples of loss of function include pain that inhibits mobility, severe swelling that prevents movement, having a worse sense of smell during a cold, or having difficulty breathing when bronchitis is present.[22][23] Loss of function has multiple causes.[16]
Acute process
[edit]This section needs more reliable medical references for verification or relies too heavily on primary sources. (April 2023) |  |


The process of acute inflammation is initiated by resident immune cells already present in the involved tissue, mainly resident macrophages, dendritic cells, histiocytes, Kupffer cells and mast cells. These cells possess surface receptors known as pattern recognition receptors (PRRs), which recognize (i.e., bind) two subclasses of molecules: pathogen-associated molecular patterns (PAMPs) and damage-associated molecular patterns (DAMPs). PAMPs are compounds that are associated with various pathogens, but which are distinguishable from host molecules. DAMPs are compounds that are associated with host-related injury and cell damage.
At the onset of an infection, burn, or other injuries, these cells undergo activation (one of the PRRs recognize a PAMP or DAMP) and release inflammatory mediators responsible for the clinical signs of inflammation. Vasodilation and its resulting increased blood flow causes the redness (rubor) and increased heat (calor). Increased permeability of the blood vessels results in an exudation (leakage) of plasma proteins and fluid into the tissue (edema), which manifests itself as swelling (tumor). Some of the released mediators such as bradykinin increase the sensitivity to pain (hyperalgesia, dolor). The mediator molecules also alter the blood vessels to permit the migration of leukocytes, mainly neutrophils and macrophages, to flow out of the blood vessels (extravasation) and into the tissue. The neutrophils migrate along a chemotactic gradient created by the local cells to reach the site of injury.[10] The loss of function (functio laesa) is probably the result of a neurological reflex in response to pain.
In addition to cell-derived mediators, several acellular biochemical cascade systems—consisting of preformed plasma proteins—act in parallel to initiate and propagate the inflammatory response. These include the complement system activated by bacteria and the coagulation and fibrinolysis systems activated by necrosis (e.g., burn, trauma).[10]
Acute inflammation may be regarded as the first line of defense against injury. Acute inflammatory response requires constant stimulation to be sustained. Inflammatory mediators are short-lived and are quickly degraded in the tissue. Hence, acute inflammation begins to cease once the stimulus has been removed.[10]
Chronic
[edit]Chronic inflammation is inflammation that lasts for months or years.[13] Macrophages, lymphocytes, and plasma cells predominate in chronic inflammation, in contrast to the neutrophils that predominate in acute inflammation.[13] Diabetes, cardiovascular disease, allergies, and chronic obstructive pulmonary disease (COPD) are examples of diseases mediated by chronic inflammation.[13] Obesity, smoking, stress and insufficient diet are some of the factors that promote chronic inflammation.[13] A 2014 study reported that 60% of Americans had at least one chronic inflammatory condition, and 42% had more than one.[13]
Cardinal signs
[edit]Common signs and symptoms that develop during chronic inflammation are:[13]
- Body pain, arthralgia, myalgia
- Chronic fatigue and insomnia
- Depression, anxiety and mood disorders
- Gastrointestinal complications such as constipation, diarrhea, and acid reflux
- Weight gain or loss
- Frequent infections
Vascular component
[edit]This section needs more reliable medical references for verification or relies too heavily on primary sources. (March 2021) |  |
Vasodilation and increased permeability
[edit]As defined, acute inflammation is an immunovascular response to inflammatory stimuli, which can include infection or trauma.[25][26] This means acute inflammation can be broadly divided into a vascular phase that occurs first, followed by a cellular phase involving immune cells (more specifically myeloid granulocytes in the acute setting).[25] The vascular component of acute inflammation involves the movement of plasma fluid, containing important proteins such as fibrin and immunoglobulins (antibodies), into inflamed tissue.
Upon contact with PAMPs, tissue macrophages and mastocytes release vasoactive amines such as histamine and serotonin, as well as eicosanoids such as prostaglandin E2 and leukotriene B4 to remodel the local vasculature.[27] Macrophages and endothelial cells release nitric oxide.[28] These mediators vasodilate and permeabilize the blood vessels, which results in the net distribution of blood plasma from the vessel into the tissue space. The increased collection of fluid into the tissue causes it to swell (edema).[27] This exuded tissue fluid contains various antimicrobial mediators from the plasma such as complement, lysozyme, antibodies, which can immediately deal damage to microbes, and opsonise the microbes in preparation for the cellular phase. If the inflammatory stimulus is a lacerating wound, exuded platelets, coagulants, plasmin and kinins can clot the wounded area using vitamin K-dependent mechanisms[29] and provide haemostasis in the first instance. These clotting mediators also provide a structural staging framework at the inflammatory tissue site in the form of a fibrin lattice – as would construction scaffolding at a construction site – for the purpose of aiding phagocytic debridement and wound repair later on. Some of the exuded tissue fluid is also funneled by lymphatics to the regional lymph nodes, flushing bacteria along to start the recognition and attack phase of the adaptive immune system.

Acute inflammation is characterized by marked vascular changes, including vasodilation, increased permeability and increased blood flow, which are induced by the actions of various inflammatory mediators.[27] Vasodilation occurs first at the arteriole level, progressing to the capillary level, and brings about a net increase in the amount of blood present, causing the redness and heat of inflammation. Increased permeability of the vessels results in the movement of plasma into the tissues, with resultant stasis due to the increase in the concentration of the cells within blood – a condition characterized by enlarged vessels packed with cells. Stasis allows leukocytes to marginate (move) along the endothelium, a process critical to their recruitment into the tissues. Normal flowing blood prevents this, as the shearing force along the periphery of the vessels moves cells in the blood into the middle of the vessel.
Plasma cascade systems
[edit]- The complement system, when activated, creates a cascade of chemical reactions that promotes opsonization, chemotaxis, and agglutination, and produces the MAC.
- The kinin system generates proteins capable of sustaining vasodilation and other physical inflammatory effects.
- The coagulation system or clotting cascade, which forms a protective protein mesh over sites of injury.
- The fibrinolysis system, which acts in opposition to the coagulation system, to counterbalance clotting and generate several other inflammatory mediators.
Plasma-derived mediators
[edit]* non-exhaustive list
| Name | Produced by | Description |
|---|---|---|
| Bradykinin | Kinin system | A vasoactive protein that is able to induce vasodilation, increase vascular permeability, cause smooth muscle contraction, and induce pain. |
| C3 | Complement system | Cleaves to produce C3a and C3b. C3a stimulates histamine release by mast cells, thereby producing vasodilation. C3b is able to bind to bacterial cell walls and act as an opsonin, which marks the invader as a target for phagocytosis. |
| C5a | Complement system | Stimulates histamine release by mast cells, thereby producing vasodilation. It is also able to act as a chemoattractant to direct cells via chemotaxis to the site of inflammation. |
| Factor XII (Hageman Factor) | Liver | A protein that circulates inactively, until activated by collagen, platelets, or exposed basement membranes via conformational change. When activated, it in turn is able to activate three plasma systems involved in inflammation: the kinin system, fibrinolysis system, and coagulation system. |
| Membrane attack complex | Complement system | A complex of the complement proteins C5b, C6, C7, C8, and multiple units of C9. The combination and activation of this range of complement proteins forms the membrane attack complex, which is able to insert into bacterial cell walls and causes cell lysis with ensuing bacterial death. |
| Plasmin | Fibrinolysis system | Able to break down fibrin clots, cleave complement protein C3, and activate Factor XII. |
| Thrombin | Coagulation system | Cleaves the soluble plasma protein fibrinogen to produce insoluble fibrin, which aggregates to form a blood clot. Thrombin can also bind to cells via the PAR1 receptor to trigger several other inflammatory responses, such as production of chemokines and nitric oxide. |
Cellular component
[edit]The cellular component involves leukocytes, which normally reside in blood and must move into the inflamed tissue via extravasation to aid in inflammation.[25] Some act as phagocytes, ingesting bacteria, viruses, and cellular debris. Others release enzymatic granules that damage pathogenic invaders. Leukocytes also release inflammatory mediators that develop and maintain the inflammatory response. In general, acute inflammation is mediated by granulocytes, whereas chronic inflammation is mediated by mononuclear cells such as monocytes and lymphocytes.
Leukocyte extravasation
[edit]
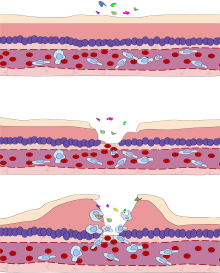
Various leukocytes, particularly neutrophils, are critically involved in the initiation and maintenance of inflammation. These cells must be able to move to the site of injury from their usual location in the blood, therefore mechanisms exist to recruit and direct leukocytes to the appropriate place. The process of leukocyte movement from the blood to the tissues through the blood vessels is known as extravasation and can be broadly divided up into a number of steps:
- Leukocyte margination and endothelial adhesion: The white blood cells within the vessels which are generally centrally located move peripherally towards the walls of the vessels.[30] Activated macrophages in the tissue release cytokines such as IL-1 and TNFα, which in turn leads to production of chemokines that bind to proteoglycans forming gradient in the inflamed tissue and along the endothelial wall.[27] Inflammatory cytokines induce the immediate expression of P-selectin on endothelial cell surfaces and P-selectin binds weakly to carbohydrate ligands on the surface of leukocytes and causes them to "roll" along the endothelial surface as bonds are made and broken. Cytokines released from injured cells induce the expression of E-selectin on endothelial cells, which functions similarly to P-selectin. Cytokines also induce the expression of integrin ligands such as ICAM-1 and VCAM-1 on endothelial cells, which mediate the adhesion and further slow leukocytes down. These weakly bound leukocytes are free to detach if not activated by chemokines produced in injured tissue after signal transduction via respective G protein-coupled receptors that activates integrins on the leukocyte surface for firm adhesion. Such activation increases the affinity of bound integrin receptors for ICAM-1 and VCAM-1 on the endothelial cell surface, firmly binding the leukocytes to the endothelium.
- Migration across the endothelium, known as transmigration, via the process of diapedesis: Chemokine gradients stimulate the adhered leukocytes to move between adjacent endothelial cells. The endothelial cells retract and the leukocytes pass through the basement membrane into the surrounding tissue using adhesion molecules such as ICAM-1.[30]
- Movement of leukocytes within the tissue via chemotaxis: Leukocytes reaching the tissue interstitium bind to extracellular matrix proteins via expressed integrins and CD44 to prevent them from leaving the site. A variety of molecules behave as chemoattractants, for example, C3a or C5a (the anaphylatoxins), and cause the leukocytes to move along a chemotactic gradient towards the source of inflammation.
Phagocytosis
[edit]Extravasated neutrophils in the cellular phase come into contact with microbes at the inflamed tissue. Phagocytes express cell-surface endocytic pattern recognition receptors (PRRs) that have affinity and efficacy against non-specific microbe-associated molecular patterns (PAMPs). Most PAMPs that bind to endocytic PRRs and initiate phagocytosis are cell wall components, including complex carbohydrates such as mannans and β-glucans, lipopolysaccharides (LPS), peptidoglycans, and surface proteins. Endocytic PRRs on phagocytes reflect these molecular patterns, with C-type lectin receptors binding to mannans and β-glucans, and scavenger receptors binding to LPS.
Upon endocytic PRR binding, actin-myosin cytoskeletal rearrangement adjacent to the plasma membrane occurs in a way that endocytoses the plasma membrane containing the PRR-PAMP complex, and the microbe. Phosphatidylinositol and Vps34-Vps15-Beclin1 signalling pathways have been implicated to traffic the endocytosed phagosome to intracellular lysosomes, where fusion of the phagosome and the lysosome produces a phagolysosome. The reactive oxygen species, superoxides and hypochlorite bleach within the phagolysosomes then kill microbes inside the phagocyte.
Phagocytic efficacy can be enhanced by opsonization. Plasma derived complement C3b and antibodies that exude into the inflamed tissue during the vascular phase bind to and coat the microbial antigens. As well as endocytic PRRs, phagocytes also express opsonin receptors Fc receptor and complement receptor 1 (CR1), which bind to antibodies and C3b, respectively. The co-stimulation of endocytic PRR and opsonin receptor increases the efficacy of the phagocytic process, enhancing the lysosomal elimination of the infective agent.
Cell-derived mediators
[edit]* non-exhaustive list
| Name | Type | Source | Description |
|---|---|---|---|
| Lysosome granules | Enzymes | Granulocytes | These cells contain a large variety of enzymes that perform a number of functions. Granules can be classified as either specific or azurophilic depending upon the contents, and are able to break down a number of substances, some of which may be plasma-derived proteins that allow these enzymes to act as inflammatory mediators. |
| GM-CSF | Glycoprotein | Macrophages, monocytes, T-cells, B-cells, and tissue-resident cells | Elevated GM-CSF has been shown to contribute to inflammation in inflammatory arthritis, osteoarthritis, colitis asthma, obesity, and COVID-19. |
| Histamine | Monoamine | Mast cells and basophils | Stored in preformed granules, histamine is released in response to a number of stimuli. It causes arteriole dilation, increased venous permeability, and a wide variety of organ-specific effects. |
| IFN-γ | Cytokine | T-cells, NK cells | Antiviral, immunoregulatory, and anti-tumour properties. This interferon was originally called macrophage-activating factor, and is especially important in the maintenance of chronic inflammation. |
| IL-6 | Cytokine and Myokine | Macrophages, osteoblasts, adipocytes, and smooth muscle cells (cytokine) Skeletal muscle cells (myokine) | Pro-inflammatory cytokine secreted by macrophages in response to pathogen-associated molecular patterns (PAMPs); pro-inflammatory cytokine secreted by adipocytes, especially in obesity; anti-inflammatory myokine secreted by skeletal muscle cells in response to exercise. |
| IL-8 | Chemokine | Primarily macrophages | Activation and chemoattraction of neutrophils, with a weak effect on monocytes and eosinophils. |
| Leukotriene B4 | Eicosanoid | Leukocytes, cancer cells | Able to mediate leukocyte adhesion and activation, allowing them to bind to the endothelium and migrate across it. In neutrophils, it is also a potent chemoattractant, and is able to induce the formation of reactive oxygen species and the release of lysosomal enzymes by these cells. |
| LTC4, LTD4 | Eicosanoid | eosinophils, mast cells, macrophages | These three Cysteine-containing leukotrienes contract lung airways, increase micro-vascular permeability, stimulate mucus secretion, and promote eosinophil-based inflammation in the lung, skin, nose, eye, and other tissues. |
| 5-oxo-eicosatetraenoic acid | Eicosanoid | Leukocytes, cancer cells | Potent stimulator of neutrophil chemotaxis, lysosome enzyme release, and reactive oxygen species formation; monocyte chemotaxis; and with even greater potency eosinophil chemotaxis, lysosome enzyme release, and reactive oxygen species formation. |
| 5-HETE | Eicosanoid | Leukocytes | Metabolic precursor to 5-Oxo-eicosatetraenoic acid, it is a less potent stimulator of neutrophil chemotaxis, lysosome enzyme release, and reactive oxygen species formation; monocyte chemotaxis; and eosinophil chemotaxis, lysosome enzyme release, and reactive oxygen species formation. |
| Prostaglandins | Eicosanoid | Mast cells | A group of lipids that can cause vasodilation, fever, and pain. |
| Nitric oxide | Soluble gas | Macrophages, endothelial cells, some neurons | Potent vasodilator, relaxes smooth muscle, reduces platelet aggregation, aids in leukocyte recruitment, direct antimicrobial activity in high concentrations. |
| TNF-α and IL-1 | Cytokines | В первую очередь макрофаги | Оба влияют на широкий спектр клеток, вызывая множество сходных воспалительных реакций: лихорадку, выработку цитокинов, регуляцию эндотелиальных генов, хемотаксис, адгезию лейкоцитов, активацию фибробластов . Отвечает за системные эффекты воспаления, такие как потеря аппетита и увеличение частоты сердечных сокращений. TNF-α ингибирует дифференцировку остеобластов. |
| Триптаза | Ферменты | Тучные клетки | Считается, что эта сериновая протеаза хранится исключительно в тучных клетках и секретируется вместе с гистамином во время активации тучных клеток. [ 31 ] [ 32 ] [ 33 ] |
Морфологические закономерности
[ редактировать ]Специфические закономерности острого и хронического воспаления наблюдаются в определенных ситуациях, возникающих в организме, например, когда воспаление возникает на поверхности эпителия или когда гноеродные в процесс вовлечены бактерии.
- Гранулематозное воспаление: характеризуется образованием гранулем и является результатом ограниченного, но разнообразного числа заболеваний, в том числе туберкулеза , проказы , саркоидоза и сифилиса .
- Фибринозное воспаление: воспаление, приводящее к значительному увеличению проницаемости сосудов, позволяет фибрину проходить через кровеносные сосуды. соответствующий прокоагуляционный стимул, например раковые клетки, Если присутствует [ 10 ] выпадает фибринозный экссудат. Это обычно наблюдается в серозных полостях , где между серозными оболочками может происходить превращение фибринозного экссудата в рубец, ограничивая их функцию. Отложение иногда образует псевдомембранный лист. При воспалении кишечника ( псевдомембранозном колите ) могут образовываться псевдомембранозные трубки.
- Гнойное воспаление: Воспаление, приводящее к образованию большого количества гноя , состоящего из нейтрофилов, мертвых клеток и жидкости. заражение гноеродными бактериями, такими как стафилококки Для этого вида воспаления характерно . Большие локализованные скопления гноя, окруженные окружающими тканями, называются абсцессами .
- Серозное воспаление: характеризуется обильным излиянием невязкой серозной жидкости, обычно продуцируемой мезотелиальными клетками серозных оболочек , но может происходить и из плазмы крови. Кожные волдыри являются примером такого воспаления.
- Язвенное воспаление. Воспаление, возникающее вблизи эпителия, может привести к некротической потере ткани с поверхности, обнажая нижние слои. Последующее углубление в эпителии известно как язва .
расстройства
[ редактировать ]

Воспалительные нарушения представляют собой большую группу нарушений, лежащих в основе широкого спектра заболеваний человека. Иммунная система часто участвует в воспалительных заболеваниях, о чем свидетельствуют как аллергические реакции , так и некоторые миопатии , причем многие нарушения иммунной системы приводят к аномальному воспалению. К неиммунным заболеваниям, причиной которых являются воспалительные процессы, являются рак, атеросклероз и ишемическая болезнь сердца . [ 10 ]
Примеры нарушений, связанных с воспалением, включают:
- Обыкновенные угри
- Астма
- Аутоиммунные заболевания
- Аутовоспалительные заболевания
- Целиакия
- Хронический простатит
- Колит
- Дивертикулит
- Семейная средиземноморская лихорадка
- Гломерулонефрит
- Гнойный гидраденит
- Гиперчувствительность
- Воспалительные заболевания кишечника
- Интерстициальный цистит
- Плоский лишай
- Синдром активации тучных клеток
- Мастоцитоз
- Отит
- Воспалительные заболевания органов малого таза
- Периферический язвенный кератит
- Пневмония
- Реперфузионное повреждение
- Ревматическая лихорадка
- Ревматоидный артрит
- Ринит
- Саркоидоз
- Отторжение трансплантата
- Васкулит
Атеросклероз
[ редактировать ]Атеросклероз, ранее считавшийся легким заболеванием накопления липидов, на самом деле включает в себя постоянную воспалительную реакцию. Последние достижения фундаментальной науки установили фундаментальную роль воспаления в опосредовании всех стадий атеросклероза от инициации до прогрессирования и, в конечном итоге, тромботических осложнений. Эти новые данные обеспечивают важную связь между факторами риска и механизмами атерогенеза . Клинические исследования показали, что эта новая биология воспаления при атеросклерозе применима непосредственно к пациентам. Повышение маркеров воспаления предсказывает исход пациентов с острым коронарным синдромом независимо от повреждения миокарда. Кроме того, хроническое воспаление низкой степени тяжести, на которое указывают уровни воспалительного маркера С-реактивного белка , проспективно определяет риск атеросклеротических осложнений, тем самым дополняя прогностическую информацию, предоставляемую традиционными факторами риска. Более того, некоторые методы лечения, снижающие коронарный риск, также ограничивают воспаление. В случае снижения уровня липидов с помощью статинов противовоспалительный эффект, по-видимому, не коррелирует со снижением уровня липопротеинов низкой плотности. Эти новые представления о воспалении способствуют этиологии атеросклероза и практическому клиническому применению в стратификации риска и выборе терапии атеросклероза. [ 34 ]
Аллергия
[ редактировать ]Аллергическая реакция, официально известная как гиперчувствительность 1 типа , является результатом неадекватного иммунного ответа, вызывающего воспаление, расширение сосудов и раздражение нервов. Типичным примером является сенная лихорадка , которая вызвана сверхчувствительной реакцией тучных клеток на аллергены . Предварительно сенсибилизированные тучные клетки реагируют дегрануляцией , высвобождая вазоактивные химические вещества, такие как гистамин. Эти химические вещества распространяют чрезмерную воспалительную реакцию, характеризующуюся расширением кровеносных сосудов, выработкой провоспалительных молекул, высвобождением цитокинов и рекрутированием лейкоцитов. [ 10 ] Тяжелая воспалительная реакция может перерасти в системную реакцию, известную как анафилаксия .
Миопатии
[ редактировать ]Воспалительные миопатии возникают из-за того, что иммунная система неадекватно атакует компоненты мышц, что приводит к появлению признаков мышечного воспаления. Они могут возникать в сочетании с другими иммунными нарушениями, такими как системная склеродермия , и включать дерматомиозит , полимиозит и миозит с включенными тельцами . [ 10 ]
Дефекты лейкоцитов
[ редактировать ]Из-за центральной роли лейкоцитов в развитии и распространении воспаления дефекты функциональности лейкоцитов часто приводят к снижению способности к воспалительной защите с последующей уязвимостью к инфекции. [ 10 ] Дисфункциональные лейкоциты могут быть неспособны правильно связываться с кровеносными сосудами из-за мутаций поверхностных рецепторов, переваривать бактерии ( синдром Чедиака-Хигаси ) или вырабатывать микробициды ( хроническая гранулематозная болезнь ). Кроме того, заболевания, поражающие костный мозг, могут привести к аномальному или небольшому количеству лейкоцитов.
Фармакологический
[ редактировать ]Известно, что некоторые лекарства или экзогенные химические соединения влияют на воспаление. Дефицит витамина А , например, вызывает усиление воспалительных реакций, [ 35 ] а противовоспалительные препараты действуют именно путем ингибирования ферментов, вырабатывающих воспалительные эйкозаноиды . Кроме того, некоторые запрещенные наркотики, такие как кокаин и экстази, могут оказывать некоторые из своих вредных эффектов, активируя факторы транскрипции, непосредственно связанные с воспалением (например, NF-κB ). [ 36 ] [ 37 ]
Рак
[ редактировать ]Воспаление управляет микроокружением опухолей, способствуя пролиферации, выживанию и миграции. [ 38 ] Раковые клетки используют селектины , хемокины и их рецепторы для инвазии, миграции и метастазирования. [ 39 ] С другой стороны, многие клетки иммунной системы способствуют иммунизации рака , подавляя рак. [ 40 ] Молекулярное пересечение между рецепторами стероидных гормонов, которые оказывают важное влияние на развитие клеток, и факторами транскрипции, играющими ключевую роль в воспалении, такими как NF-κB , может опосредовать некоторые из наиболее критических эффектов воспалительных стимулов на раковые клетки. [ 41 ] Эта способность медиатора воспаления влиять на действие стероидных гормонов в клетках, скорее всего, влияет на канцерогенез. С другой стороны, из-за модульной природы многих рецепторов стероидных гормонов это взаимодействие может предложить способы препятствовать прогрессированию рака путем нацеливания на определенный белковый домен в определенном типе клеток. Такой подход может ограничить побочные эффекты, не связанные с интересующей опухолью, и помочь сохранить жизненно важные гомеостатические функции и процессы развития в организме.
Согласно обзору 2009 года, недавние данные показывают, что воспаление, связанное с раком (CRI), может привести к накоплению случайных генетических изменений в раковых клетках. [ 42 ]
Роль в раке
[ редактировать ]В 1863 году Рудольф Вирхов выдвинул гипотезу, что рак возникает в местах хронического воспаления. [ 39 ] [ 43 ] По оценкам, по состоянию на 2012 год хроническое воспаление является причиной примерно 15–25% случаев рака у человека. [ 43 ] [ 44 ]
Медиаторы и повреждение ДНК при раке
[ редактировать ]Медиатор воспаления — это посланник, который действует на кровеносные сосуды и/или клетки, вызывая воспалительную реакцию. [ 45 ] Медиаторы воспаления, которые способствуют неоплазии, включают простагландины , воспалительные цитокины, такие как IL-1β , TNF-α , IL-6 и IL-15 , а также хемокины, такие как IL-8 и GRO-альфа . [ 46 ] [ 43 ] Эти и другие медиаторы воспаления создают среду, которая способствует распространению и выживанию. [ 39 ] [ 46 ]
Воспаление также вызывает повреждения ДНК из-за индукции активных форм кислорода (АФК) различными внутриклеточными медиаторами воспаления. [ 39 ] [ 46 ] [ 43 ] Кроме того, лейкоциты и другие фагоцитирующие клетки, привлеченные к месту воспаления, вызывают повреждения ДНК в пролиферирующих клетках за счет генерации АФК и активных форм азота (РНС). АФК и РНС обычно вырабатываются этими клетками для борьбы с инфекцией. [ 39 ] Одни только АФК вызывают более 20 типов повреждений ДНК. [ 47 ] Окислительные повреждения ДНК вызывают обе мутации. [ 48 ] и эпигенетические изменения. [ 49 ] [ 43 ] [ 50 ] РНС также вызывают мутагенные повреждения ДНК. [ 51 ]
Нормальная клетка может подвергнуться канцерогенезу и стать раковой клеткой, если она часто подвергается повреждению ДНК в течение длительных периодов хронического воспаления. Повреждения ДНК могут вызвать генетические мутации из-за неточной репарации . Кроме того, ошибки в процессе репарации ДНК могут вызвать эпигенетические изменения. [ 43 ] [ 46 ] [ 50 ] Мутации и эпигенетические изменения, которые реплицируются и обеспечивают селективное преимущество во время пролиферации соматических клеток, могут быть канцерогенными.
Полногеномный анализ раковых тканей человека показывает, что одна типичная раковая клетка может обладать примерно 100 мутациями в кодирующих областях , 10–20 из которых являются «драйверными мутациями», которые способствуют развитию рака. [ 43 ] Однако хроническое воспаление также вызывает эпигенетические изменения, такие как метилирование ДНК , которые часто встречаются чаще, чем мутации. Обычно в раковой клетке метилируются от нескольких сотен до тысяч генов (см. Метилирование ДНК при раке ). Участки окислительного повреждения хроматина могут рекрутировать комплексы, содержащие ДНК-метилтрансферазы (DNMT), деацетилазу гистонов ( SIRT1 ) и метилтрансферазу гистонов (EZH2) , и, таким образом, индуцировать метилирование ДНК. [ 43 ] [ 52 ] [ 53 ] Метилирование ДНК островка CpG в промоторной области может вызвать замалчивание его нижестоящего гена (см. Сайт CpG и регуляция транскрипции при раке ). Гены репарации ДНК, в частности, часто инактивируются метилированием при различных видах рака (см. гиперметилирование генов репарации ДНК при раке ). Отчет за 2018 год [ 54 ] оценили относительную важность мутаций и эпигенетических изменений в развитии двух разных типов рака. Этот отчет показал, что эпигенетические изменения были гораздо более важными, чем мутации, в возникновении рака желудка (связанного с воспалением). [ 55 ] Однако мутации и эпигенетические изменения имели примерно одинаковое значение в возникновении плоскоклеточного рака пищевода (связанного с химическими веществами табака и ацетальдегидом , продуктом метаболизма алкоголя).
ВИЧ и СПИД
[ редактировать ]Давно признано, что инфекция ВИЧ характеризуется не только развитием глубокого иммунодефицита , но и устойчивым воспалением и иммунной активацией. [ 56 ] [ 57 ] [ 58 ] Значительный объем данных указывает на то, что хроническое воспаление является важнейшим фактором иммунной дисфункции, преждевременного появления заболеваний, связанных со старением, и иммунодефицита. [ 56 ] [ 59 ] Сегодня многие рассматривают ВИЧ-инфекцию не только как развивающийся иммунодефицит, вызванный вирусом, но и как хроническое воспалительное заболевание. [ 60 ] Даже после введения эффективной антиретровирусной терапии (АРТ) и эффективного подавления виремии у ВИЧ-инфицированных лиц хроническое воспаление сохраняется. Исследования на животных также подтверждают взаимосвязь между иммунной активацией и прогрессирующим клеточным иммунодефицитом: заражение SIV sm его естественных хозяев-приматов, не являющихся людьми, сажистого мангабея , вызывает высокий уровень репликации вируса, но ограниченные доказательства заболевания. [ 61 ] [ 62 ] Отсутствие патогенности сопровождается отсутствием воспаления, иммунной активации и клеточной пролиферации. Напротив, экспериментальное SIV заражение sm макака-резуса вызывает активацию иммунной системы и СПИД-подобное заболевание, во многом сходное с ВИЧ-инфекцией человека. [ 63 ]
Определение того, как истощаются Т-клетки CD4 и как индуцируется хроническое воспаление и иммунная активация, лежит в основе понимания патогенеза ВИЧ — одного из главных приоритетов исследований ВИЧ, проводимых Управлением исследований СПИДа Национальных институтов здравоохранения . Недавние исследования показали, что каспазой-1 , опосредованный пироптоз , высоковоспалительная форма запрограммированной гибели клеток, приводит к истощению CD4 Т-клеток и воспалению, вызываемому ВИЧ. [ 64 ] [ 65 ] [ 66 ] Это два характерных события, которые способствуют прогрессированию ВИЧ-инфекции в СПИД . Пироптоз, по-видимому, создает патогенный порочный круг, в котором умирающие Т-клетки CD4 и другие иммунные клетки (включая макрофаги и нейтрофилы) выделяют воспалительные сигналы, которые рекрутируют больше клеток в инфицированные лимфоидные ткани для гибели. Прямой характер этой воспалительной реакции приводит к хроническому воспалению и повреждению тканей. [ 67 ] Идентификация пироптоза как преобладающего механизма, вызывающего истощение CD4 Т-клеток и хроническое воспаление, открывает новые терапевтические возможности, а именно каспазу-1, которая контролирует путь пироптоза. В связи с этим пироптоз CD4 Т-клеток и секреция провоспалительных цитокинов, таких как IL-1β и IL-18, могут быть заблокированы в лимфоидных тканях ВИЧ-инфицированного человека путем добавления ингибитора каспазы-1 VX-765. [ 64 ] который уже доказал свою безопасность и хорошую переносимость в ходе II фазы клинических испытаний на людях. [ 68 ] Эти результаты могут стимулировать разработку совершенно нового класса «анти-СПИД»-терапии, которая воздействует на хозяина, а не на вирус. Такие препараты почти наверняка будут использоваться в сочетании с АРТ. Способствуя «толерантности» к вирусу вместо подавления его репликации, VX-765 или родственные ему лекарства могут имитировать эволюционные решения, возникающие у нескольких обезьян-хозяев (например, сажистый мангабей), инфицированных видоспецифичными лентивирусами, которые привели к отсутствию заболеваний. , отсутствие снижения количества Т-клеток CD4 и отсутствие хронического воспаления.
Разрешение
[ редактировать ]Воспалительную реакцию необходимо активно прекращать, когда она больше не нужна, чтобы предотвратить ненужное «побочное» повреждение тканей. [ 10 ] Несоблюдение этого требования приводит к хроническому воспалению и разрушению клеток. Разрешение воспаления происходит по разным механизмам в разных тканях. Механизмы прекращения воспаления включают: [ 10 ] [ 69 ]
- Короткий период полураспада медиаторов воспаления in vivo .
- Производство и высвобождение трансформирующего фактора роста (TGF) бета из макрофагов. [ 70 ] [ 71 ] [ 72 ]
- Производство и выпуск интерлейкина 10 (IL-10) [ 73 ]
- Производство противовоспалительных специализированных проразрешающих медиаторов : липоксинов , резольвинов , марезинов и нейропротектинов. [ 74 ] [ 75 ]
- Снижение уровня провоспалительных молекул, таких как лейкотриены .
- Повышение регуляции противовоспалительных молекул, таких как антагонист рецептора интерлейкина 1 или рецептор растворимого фактора некроза опухоли (TNFR)
- Апоптоз провоспалительных клеток [ 76 ]
- Десенсибилизация рецепторов.
- Увеличение выживаемости клеток в зонах воспаления за счет их взаимодействия с внеклеточным матриксом (ВКМ). [ 77 ] [ 78 ]
- Снижение активности рецепторов высокими концентрациями лигандов
- Расщепление хемокинов матриксными металлопротеиназами (ММП) может привести к выработке противовоспалительных факторов. [ 79 ]
Острое воспаление обычно разрешается с помощью механизмов, которые до сих пор остаются неясными. Новые данные свидетельствуют о том, что активная, скоординированная программа разрешения начинается в первые несколько часов после начала воспалительной реакции. После проникновения в ткани гранулоциты способствуют переключению арахидоновой кислоты производных простагландинов и лейкотриенов, , на липоксины, которые инициируют последовательность терминации. Таким образом, рекрутирование нейтрофилов запрограммированная гибель путем апоптоза прекращается и запускается . Эти события совпадают с биосинтезом из полиненасыщенных жирных кислот омега-3 резольвинов . и протектинов , которые критически сокращают период инфильтрации нейтрофилов, инициируя апоптоз Как следствие, апоптозные нейтрофилы подвергаются фагоцитозу макрофагов , что приводит к клиренсу нейтрофилов и высвобождению противовоспалительных и репаративных цитокинов, таких как трансформирующий фактор роста-β1. Противовоспалительная программа завершается уходом макрофагов через лимфатические сосуды . [ 80 ]
—Чарльз Н. Серхан
Связь с депрессией
[ редактировать ]Есть доказательства связи между воспалением и депрессией . [ 81 ] Воспалительные процессы могут быть вызваны негативными мыслями или их последствиями, такими как стресс, насилие или депривация. Таким образом, негативное мышление может вызвать воспаление, которое, в свою очередь, может привести к депрессии. [ 82 ] [ 83 ] [ сомнительно – обсудить ] Кроме того, появляется все больше доказательств того, что воспаление может вызвать депрессию из-за повышения уровня цитокинов, переводя мозг в «режим болезни». [ 84 ]
Классические симптомы физического заболевания, такие как вялость, во многом совпадают с поведением, характеризующим депрессию. Уровни цитокинов имеют тенденцию резко возрастать во время депрессивных эпизодов у людей с биполярным расстройством и снижаться во время ремиссии. [ 85 ] Более того, в клинических исследованиях было показано, что противовоспалительные препараты, принимаемые в дополнение к антидепрессантам, не только значительно улучшают симптомы, но и увеличивают долю субъектов, положительно реагирующих на лечение. [ 86 ] Воспаления, которые приводят к серьезной депрессии, могут быть вызваны обычными инфекциями, например, вызванными вирусами, бактериями или даже паразитами. [ 87 ]
Связь с бредом
[ редактировать ]Существуют доказательства связи между воспалением и делирием, основанные на результатах недавнего продольного исследования по изучению СРБ у пациентов с COVID-19. [ 88 ]
Системные эффекты
[ редактировать ]Инфекционный организм может выйти за пределы ближайших тканей через систему кровообращения или лимфатическую систему , откуда он может распространиться на другие части тела. Если организм не сдерживается действием острого воспаления, он может получить доступ к лимфатической системе через близлежащие лимфатические сосуды . Инфекция лимфатических сосудов известна как лимфангит , а инфекция лимфатического узла — лимфаденит . Когда лимфатические узлы не могут уничтожить всех возбудителей, инфекция распространяется дальше. Возбудитель может попасть в кровоток через лимфатический дренаж в систему кровообращения.
Когда воспаление подавляет хозяина, синдром системной воспалительной реакции диагностируется . Когда это вызвано инфекцией, термин «сепсис» применяется , причем термин «бактериемия» применяется конкретно к бактериальному сепсису, а термин «виремия» - конкретно к вирусному сепсису. Расширение сосудов и дисфункция органов являются серьезными проблемами, связанными с широко распространенной инфекцией, которые могут привести к септическому шоку и смерти. [ 89 ]
Белки острой фазы
[ редактировать ]Воспаление также характеризуется высокими системными уровнями белков острой фазы . При остром воспалении эти белки оказываются полезными; однако при хроническом воспалении они могут способствовать развитию амилоидоза . [ 10 ] Эти белки включают С-реактивный белок , сывороточный амилоид А и сывороточный амилоид Р , которые вызывают ряд системных эффектов, включая: [ 10 ]
- Высокая температура
- Повышенное кровяное давление
- Снижение потоотделения
- Недомогание
- Потеря аппетита
- Сонливость
Лейкоциты
[ редактировать ]Воспаление часто влияет на количество лейкоцитов, присутствующих в организме:
- Лейкоцитоз часто наблюдается при воспалении, вызванном инфекцией, что приводит к значительному увеличению количества лейкоцитов в крови, особенно незрелых клеток. Число лейкоцитов обычно увеличивается до 15 000–20 000 клеток на микролитр, но в крайних случаях оно может достигать 100 000 клеток на микролитр. [ 10 ] Бактериальная инфекция обычно приводит к увеличению количества нейтрофилов , создавая нейтрофилию , тогда как такие заболевания, как астма , сенная лихорадка и паразитарные инвазии, приводят к увеличению количества эозинофилов , создавая эозинофилию . [ 10 ]
- Лейкопения может быть вызвана некоторыми инфекциями и заболеваниями, включая вирусную инфекцию, инфекцию риккетсий , некоторые простейшие , туберкулез и некоторые виды рака. [ 10 ]
Интерлейкины и ожирение
[ редактировать ]С открытием интерлейкинов (ИЛ) возникла концепция системного воспаления . Хотя задействованные процессы идентичны воспалению тканей, системное воспаление не ограничивается конкретной тканью, а затрагивает эндотелий и другие системы органов.
Хроническое воспаление широко наблюдается при ожирении . [ 90 ] [ 91 ] У людей с ожирением обычно наблюдается много повышенных маркеров воспаления, в том числе: [ 92 ] [ 93 ]
Хроническое воспаление низкой степени тяжести характеризуется двух-трехкратным увеличением системных концентраций цитокинов, таких как TNF-α, IL-6 и CRP. [ 96 ] Окружность талии значительно коррелирует с системной воспалительной реакцией. [ 97 ]
Потеря белой жировой ткани снижает уровень маркеров воспаления. [ 90 ] По состоянию на 2017 год связь системного воспаления с инсулинорезистентностью и диабетом 2 типа , а также с атеросклерозом находилась в стадии предварительного исследования, хотя строгие клинические исследования для подтверждения такой связи не проводились. [ 98 ]
С-реактивный белок (СРБ) вырабатывается на более высоком уровне у людей с ожирением и может увеличить риск сердечно-сосудистых заболеваний . [ 99 ]
Результаты
[ редактировать ]Исход в конкретных обстоятельствах будет определяться тканью, в которой произошло повреждение, и повреждающим агентом, вызвавшим его. Вот возможные последствия воспаления: [ 10 ]
- Разрешение
Полное восстановление воспаленной ткани до нормального состояния. Воспалительные меры, такие как расширение сосудов, химическая продукция и инфильтрация лейкоцитов, прекращаются, а поврежденные паренхиматозные клетки регенерируют. Таков обычно результат, когда возникает ограниченное или кратковременное воспаление. - Фиброз
Большие объемы разрушения тканей или повреждения тканей, неспособных к регенерации, не могут быть полностью восстановлены организмом. фиброзное рубцевание В этих областях повреждения возникает , образующее рубец, состоящий в основном из коллагена . Рубец не будет содержать каких-либо специализированных структур, таких как паренхиматозные клетки, поэтому могут возникнуть функциональные нарушения. - Образование абсцесса
Образуется полость, содержащая гной, непрозрачную жидкость, содержащую мертвые лейкоциты и бактерии, а также остатки разрушенных клеток. - Хроническое воспаление
При остром воспалении, если повреждающий агент сохраняется, развивается хроническое воспаление. Этот процесс, характеризующийся воспалением, продолжающимся многие дни, месяцы и даже годы, может привести к образованию хронической раны . Хроническое воспаление характеризуется преобладающим присутствием макрофагов в поврежденной ткани. Эти клетки являются мощными защитными агентами организма, но токсины выделяемые ими , включая активные формы кислорода , повреждают как собственные ткани организма, так и вторгающиеся агенты. Как следствие, хроническое воспаление почти всегда сопровождается разрушением тканей.
Примеры
[ редактировать ]Воспаление обычно обозначается добавлением суффикса « итис », как показано ниже. Однако некоторые заболевания, такие как астма и пневмония , не соответствуют этому соглашению. Дополнительные примеры доступны в разделе «Список типов воспалений» .
-
Острый аппендицит
-
Острый дерматит
-
Острый инфекционный менингит
-
Острый тонзиллит
См. также
[ редактировать ]Примечания
[ редактировать ]- ^ Все эти признаки могут наблюдаться в определенных случаях, но ни один из них, конечно, не должен присутствовать. [ 14 ] Это первоначальные, или кардинальные, признаки воспаления. [ 14 ]
- ^ Functio laesa — устаревшее понятие, поскольку оно характерно не только для воспаления и является характеристикой многих болезненных состояний. [ 15 ]
Ссылки
[ редактировать ]- ^ Ферреро-Милиани Л., Нильсен О.Г., Андерсен П.С., Жирарден С.Е. (февраль 2007 г.). «Хроническое воспаление: важность NOD2 и NALP3 в генерации интерлейкина-1бета» . Клиническая и экспериментальная иммунология . 147 (2): 227–235. дои : 10.1111/j.1365-2249.2006.03261.x . ПМК 1810472 . ПМИД 17223962 .
- ^ Чен Л., Дэн Х., Цуй Х., Фанг Дж., Цзо З., Дэн Дж. и др. (январь 2018 г.). «Воспалительные реакции и воспалительные заболевания органов» . Онкотаргет . 9 (6). Impact Journals, LLC: 7204–7218. дои : 10.18632/oncotarget.23208 . ПМЦ 5805548 . ПМИД 29467962 . S2CID 3571245 .
- ^ Аббас А.Б., Лихтман А.Х. (2009). «Гл.2 Врожденный иммунитет». В Сондерсе (Elsevier) (ред.). Основная иммунология. Функции и нарушения иммунной системы (3-е изд.). Сондерс/Эльзевир. ISBN 978-1-4160-4688-2 .
- ^ «Воспаление и ваше здоровье» . Кедры-Синай .
- ^ Бергер А. (август 2000 г.). «Ответы Th1 и Th2: что это такое?» . БМЖ . 321 (7258): 424. doi : 10.1136/bmj.321.7258.424 . ПМК 27457 . ПМИД 10938051 . Архивировано из оригинала 12 июля 2021 года . Проверено 1 июля 2021 г.
- ^ «воспаление» . Этимология воспаления по этимонлину . 28 сентября 2017 г. Проверено 11 августа 2024 г.
- ^ Перейти обратно: а б с д Холл Дж (2011). Учебник Гайтона и Холла по медицинской физиологии (12-е изд.). Филадельфия, Пенсильвания: Сондерс/Эльзевир. п. 428. ИСБН 978-1-4160-4574-8 .
- ^ Грейнджер Д.Н., Сенченкова Е (2010). «Адгезия лейкоцитов и эндотелиальных клеток» . Воспаление и микроциркуляция . Физиология интегрированных систем - от клетки к функции. Том. 2. Морган и Клейпул Науки о жизни. стр. 1–87. дои : 10.4199/C00013ED1V01Y201006ISP008 . ПМИД 21452440 . Архивировано из оригинала 21 января 2021 года . Проверено 1 июля 2017 года .
- ^ Пиира О.П., Миеттинен Я.А., Хаутала А.Дж., Хуйкури Х.В., член Парламента Тулппо (октябрь 2013 г.). «Физиологические реакции на эмоциональное возбуждение у здоровых людей и больных ишемической болезнью сердца». Автономная нейронаука . 177 (2): 280–5. дои : 10.1016/j.autneu.2013.06.001 . ПМИД 23916871 . S2CID 19823098 .
- ^ Перейти обратно: а б с д и ж г час я дж к л м н тот п д р Роббинс С.Л., Котран Р.С., Кумар В., Коллинз Т. (1998). Роббинс Патологическая основа болезней . Филадельфия: Компания WB Saunders. ISBN 978-0-7216-7335-6 .
- ^ Кумар Р., Клермонт Г., Водовоц Ю., Чоу С.С. (сентябрь 2004 г.). «Динамика острого воспаления». Журнал теоретической биологии . 230 (2): 145–55. arXiv : q-bio/0404034 . Бибкод : 2004PhDT.......405K . дои : 10.1016/j.jtbi.2004.04.044 . ПМИД 15321710 . S2CID 16992741 .
- ^ Перейти обратно: а б с д и ж Ханнуди С., Насуруддин Д.Н. (2020). «Острая воспалительная реакция» . СтатПерлс . ПМИД 32310543 . Архивировано из оригинала 15 июня 2022 года . Проверено 28 декабря 2020 г.
- ^ Перейти обратно: а б с д и ж г Пахва Р., Гоял А., Бансал П., Джалал И. (28 сентября 2021 г.). «Хроническое воспаление» . СтатПерлс . Национальные институты здравоохранения – Национальная медицинская библиотека. ПМИД 29630225 . Архивировано из оригинала 19 декабря 2020 года . Проверено 28 декабря 2020 г.
- ^ Перейти обратно: а б Медицинский словарь Стедмана (двадцать пятое изд.). Уильямс и Уилкинс. 1990.
- ^ Скорее ЖЖ (март 1971). «Нарушение функции (functio laesa): легендарный пятый кардинальный признак воспаления, добавленный Клавдием Галеном к четырем кардинальным признакам Цельсия» . Бюллетень Нью-Йоркской медицинской академии . 47 (3): 303–22. ПМК 1749862 . ПМИД 5276838 .
- ^ Перейти обратно: а б с д и Чандрасома П., Тейлор С.Р. (2005). «Часть А. «Общая патология», раздел II. «Реакция организма на травму», глава 3. «Острая воспалительная реакция», подраздел «Основные клинические признаки» » . Краткая патология (3-е изд.). МакГроу-Хилл. ISBN 978-0-8385-1499-3 . OCLC 150148447 . Архивировано из оригинала 5 октября 2008 года . Проверено 5 ноября 2008 г.
- ^ Перейти обратно: а б Скорее ЖЖ (1971). «Нарушение функции (functio laesa): легендарный пятый кардинальный признак воспаления, добавленный Галеном к четырем кардинальным признакам Цельсия. — ПМК» . Бюллетень Нью-Йоркской медицинской академии . 47 (3): 303–322. ПМК 1749862 . ПМИД 5276838 .
- ^ Вернер Р. (2009). Руководство массажиста по патологии (4-е изд.). Уолтерс Клювер. ISBN 978-0-7817-6919-8 . Архивировано из оригинала 21 декабря 2015 года . Проверено 6 октября 2010 г.
- ^ Фогель WH, Берке А (2009). Краткая история зрения и глазной медицины . Публикации Куглера. п. 97. ИСБН 978-90-6299-220-1 .
- ^ Порт С (2007). Основы патофизиологии: концепции измененных состояний здоровья . Хагерстаун, Мэриленд: Липпинкотт Уильямс и Уилкинс. п. 270. ИСБН 978-0-7817-7087-3 .
- ^ Дорманди Т. (2006). Худшее из зол: борьба человека с болью . Нью-Хейвен, Коннектикут: Издательство Йельского университета. стр. 22 . ISBN 978-0-300-11322-8 .
- ^ InformedHealth.org [Интернет] . Институт качества и эффективности здравоохранения (IQWiG). 22 февраля 2018 г. – через www.ncbi.nlm.nih.gov.
- ^ «Воспаление | Определение, симптомы, лечение и факты | Британника» . www.britanica.com . 11 марта 2024 г.
- ^ Роббинс С., Котран Р., Кумар В., Аббас А., Астер Дж. (2020). Патологическая основа заболевания (10-е изд.). Филадельфия, Пенсильвания: Сондерс Эльзевир.
- ^ Перейти обратно: а б с Райтен Д.Д., Сакр Ашур Ф.А., Росс А.С., Мейдани С.Н., Доусон Х.Д., Стивенсен CB и др. (май 2015 г.). «Наука о воспалении и питании для программ/политики и интерпретации данных исследований (INSPIRE)» . Журнал питания . 145 (5): 1039С–1108С. дои : 10.3945/jn.114.194571 . ПМК 4448820 . ПМИД 25833893 .
- ^ Таамс Л.С. (июль 2018 г.). «Воспаление и иммунная резолюция» . Клиническая и экспериментальная иммунология . 193 (1): 1–2. дои : 10.1111/cei.13155 . ПМК 6037995 . ПМИД 29987840 .
- ^ Перейти обратно: а б с д Меджитов Р. (июль 2008 г.). «Происхождение и физиологическая роль воспаления». Природа . 454 (7203): 428–435. Бибкод : 2008Natur.454..428M . дои : 10.1038/nature07201 . ПМИД 18650913 . S2CID 205214291 .
- ^ Мантовани А, Гарланда С (февраль 2023 г.). Лонго Д.Л. (ред.). «Гуморальный врожденный иммунитет и белки острой фазы» . Медицинский журнал Новой Англии . 388 (5): 439–452. дои : 10.1056/NEJMra2206346 . ПМЦ 9912245 . ПМИД 36724330 .
- ^ Ферланд Дж. (2020), «Витамин К» , Современные знания в области питания , Elsevier, стр. 137–153, doi : 10.1016/b978-0-323-66162-1.00008-1 , ISBN 978-0-323-66162-1 , получено 17 февраля 2023 г.
- ^ Перейти обратно: а б Херрингтон С (2014). Учебник патологии Мьюира (15-е изд.). ЦРК Пресс. п. 59. ИСБН 978-1-4441-8499-0 .
- ^ Карстенс Э., Акияма Т., Чевикбас Ф., Кемпкес С., Буль Т., Месс С. и др. (2014). «Роль интерлейкина-31 и онкостатина М в зуде и нейроиммунной коммуникации». В Карстенс М., Акияма Т. (ред.). Зуд: механизмы и лечение . Границы неврологии. Бока-Ратон (Флорида): CRC Press/Тейлор и Фрэнсис. ISBN 978-1-4665-0543-8 . ПМИД 24830021 .
- ^ Коги Г.Х. (июнь 2007 г.). «Триптазы и химазы тучных клеток при воспалении и защите хозяина» . Иммунологические обзоры . 217 (1): 141–54. дои : 10.1111/j.1600-065x.2007.00509.x . ПМК 2275918 . ПМИД 17498057 .
- ^ Коги Г.Х. (май 2016 г.). «Протеазы тучных клеток как фармакологические мишени» . Европейский журнал фармакологии . Фармакологическая модуляция тучных клеток и базофилов. 778 : 44–55. дои : 10.1016/j.ejphar.2015.04.045 . ПМЦ 4636979 . ПМИД 25958181 .
- ^ Либби П. (19–26 декабря 2002 г.). «Воспаление при атеросклерозе». Природа . 420 (6917): 868–74. Бибкод : 2002Natur.420..868L . дои : 10.1038/nature01323 . ПМИД 12490960 . S2CID 407449 .
- ^ Видерманн Ю, Чен XJ, Энербек Л., Хансон Л.А., Каху Х., Дальгрен У.И. (декабрь 1996 г.). «Дефицит витамина А усиливает воспалительные реакции». Скандинавский журнал иммунологии . 44 (6): 578–84. дои : 10.1046/j.1365-3083.1996.d01-351.x . ПМИД 8972739 . S2CID 3079540 .
- ^ Харгрейв БАЙ, Тиангко Д.А., Латтанцио Ф.А., Биб С.Дж. (2003). «Кокаин, а не морфин, вызывает выработку активных форм кислорода и активацию NF-kappaB в временно котрансфицированных клетках сердца». Сердечно-сосудистая токсикология . 3 (2): 141–51. дои : 10.1385/CT:3:2:141 . ПМИД 14501032 . S2CID 35240781 .
- ^ Монтьель-Дуарте С., Ансорена Э., Лопес-Сабальса М.Дж., Сенаррузабеитиа Е., Ирабуру М.Дж. (март 2004 г.). «Роль активных форм кислорода, глутатиона и NF-каппаB в апоптозе, индуцированном 3,4-метилендиоксиметамфетамином («экстази») на звездчатых клетках печени». Биохимическая фармакология . 67 (6): 1025–33. дои : 10.1016/j.bcp.2003.10.020 . ПМИД 15006539 .
- ^ Унгефрорен Х., Себенс С., Зайдль Д., Ленерт Х., Хасс Р. (сентябрь 2011 г.). «Взаимодействие опухолевых клеток с микроокружением» . Сотовая связь и сигнализация . 9:18 . дои : 10.1186/1478-811X-9-18 . ПМК 3180438 . ПМИД 21914164 .
- ^ Перейти обратно: а б с д и Куссенс Л.М., Верб З (2002). «Воспаление и рак» . Природа . 420 (6917): 860–7. Бибкод : 2002Natur.420..860C . дои : 10.1038/nature01322 . ПМК 2803035 . ПМИД 12490959 .
- ^ Ганн Л., Дин С., Лю М., Ма Ю., Ци С., Цай Ю. и др. (сентябрь 2012 г.). «Противоположная роль компонента комплемента C5a в прогрессировании опухоли и микроокружении опухоли» . Журнал иммунологии . 189 (6): 2985–94. doi : 10.4049/jimmunol.1200846 . ПМЦ 3436956 . ПМИД 22914051 .
- ^ Копленд Дж.А., Шеффилд-Мур М., Колджич-Зиванович Н., Джентри С., Лампроу Г., Цорцату-Статопулу Ф. и др. (июнь 2009 г.). «Рецепторы половых стероидов при дифференцировке скелета и эпителиальной неоплазии: возможно ли тканеспецифическое вмешательство?». Биоэссе . 31 (6): 629–41. doi : 10.1002/bies.200800138 . ПМИД 19382224 . S2CID 205469320 .
- ^ Колотта Ф, Аллавена П, Сика А, Гарланда С, Мантовани А (июль 2009 г.). «Воспаление, связанное с раком, седьмой признак рака: связь с генетической нестабильностью» . Канцерогенез (обзор). 30 (7): 1073–81. дои : 10.1093/carcin/bgp127 . ПМИД 19468060 .
- ^ Перейти обратно: а б с д и ж г час Чиба Т., Марусава Х., Ушиджима Т. (сентябрь 2012 г.). «Развитие рака в органах пищеварения, связанное с воспалением: механизмы и роль генетической и эпигенетической модуляции» (PDF) . Гастроэнтерология . 143 (3): 550–563. дои : 10.1053/j.gastro.2012.07.009 . hdl : 2433/160134 . ПМИД 22796521 . S2CID 206226588 . Архивировано (PDF) из оригинала 29 августа 2022 года . Проверено 9 июня 2018 г.
- ^ Мантовани А., Аллавена П., Сика А., Балквилл Ф. (июль 2008 г.). «Раковое воспаление» (PDF) . Природа . 454 (7203): 436–44. Бибкод : 2008Natur.454..436M . дои : 10.1038/nature07205 . hdl : 2434/145688 . ПМИД 18650914 . S2CID 4429118 . Архивировано (PDF) из оригинала 30 октября 2022 года . Проверено 9 июня 2018 г.
- ^ Ларсен Г.Л., Хенсон П.М. (1983). «Медиаторы воспаления». Ежегодный обзор иммунологии . 1 : 335–59. дои : 10.1146/annurev.iy.01.040183.002003 . ПМИД 6399978 .
- ^ Перейти обратно: а б с д Шактер Е, Вайцман С.А. (февраль 2002 г.). «Хроническое воспаление и рак». Онкология . 16 (2): 217–26, 229, обсуждение 230–2. ПМИД 11866137 .
- ^ Ю Ю, Цуй Ю, Нидернхофер Л. Дж., Ван Ю (декабрь 2016 г.). «Происхождение, биологические последствия и значимость для здоровья человека повреждений ДНК, вызванных окислительным стрессом» . Химические исследования в токсикологии . 29 (12): 2008–2039. doi : 10.1021/acs.chemrestox.6b00265 . ПМК 5614522 . ПМИД 27989142 .
- ^ Диздароглу М. (декабрь 2012 г.). «Окислительно-индуцированное повреждение ДНК: механизмы, восстановление и болезни». Письма о раке . 327 (1–2): 26–47. дои : 10.1016/j.canlet.2012.01.016 . ПМИД 22293091 .
- ^ Нисида Н., Кудо М. (2013). «Окислительный стресс и эпигенетическая нестабильность в гепатокарциногенезе человека» . Пищеварительные заболевания . 31 (5–6): 447–53. дои : 10.1159/000355243 . ПМИД 24281019 .
- ^ Перейти обратно: а б Дин Н., Майури А.Р., О'Хаган Х.М. (2017). «Новая роль эпигенетических модификаторов в восстановлении повреждений ДНК, связанных с хроническими воспалительными заболеваниями» . Мутационные исследования . 780 : 69–81. дои : 10.1016/j.mrrev.2017.09.005 . ПМК 6690501 . ПМИД 31395351 .
- ^ Каваниси С., Ониши С., Ма Н., Хираку Ю., Оикава С., Мурата М. (2016). «Нитративное и окислительное повреждение ДНК при инфекционном канцерогенезе в отношении раковых стволовых клеток» . Гены и окружающая среда . 38 (1): 26. Бибкод : 2016GeneE..38...26K . дои : 10.1186/s41021-016-0055-7 . ПМК 5203929 . ПМИД 28050219 .
- ^ О'Хаган Х.М., Ван В., Сен С., Дестефано Шилдс С., Ли С.С., Чжан Ю.В. и др. (ноябрь 2011 г.). «Окислительное повреждение нацелено на комплексы, содержащие ДНК-метилтрансферазы, SIRT1 и члены полисот, на промоторные острова CpG» . Раковая клетка . 20 (5): 606–19. дои : 10.1016/j.ccr.2011.09.012 . ПМК 3220885 . ПМИД 22094255 .
- ^ Майури А.Р., Пэн М., Подичети Р., Шрирамкумар С., Камплейн С.М., Раш Д.Б. и др. (июль 2017 г.). «Белки восстановления несоответствия инициируют эпигенетические изменения во время воспалительного опухолевого процесса» . Исследования рака . 77 (13): 3467–3478. дои : 10.1158/0008-5472.CAN-17-0056 . ПМК 5516887 . ПМИД 28522752 .
- ^ Ямасита С., Кишино Т., Такахаши Т., Симадзу Т., Чарват Х., Какугава Ю. и др. (февраль 2018 г.). «Генетические и эпигенетические изменения в нормальных тканях оказывают различное влияние на риск развития рака в разных тканях» . Труды Национальной академии наук Соединенных Штатов Америки . 115 (6): 1328–1333. Бибкод : 2018PNAS..115.1328Y . дои : 10.1073/pnas.1717340115 . ПМК 5819434 . ПМИД 29358395 .
- ^ Раза Ю., Хан А., Фаруки А., Мубарак М., Фациста А., Ахтар С.С. и др. (октябрь 2014 г.). «Окислительное повреждение ДНК как потенциальный ранний биомаркер канцерогенеза, связанного с Helicobacter pylori». Патологические и онкологические исследования . 20 (4): 839–46. дои : 10.1007/s12253-014-9762-1 . ПМИД 24664859 . S2CID 18727504 .
- ^ Перейти обратно: а б Дикс С.Г. (1 января 2011 г.). «ВИЧ-инфекция, воспаление, старение иммунитета и старение» . Ежегодный обзор медицины . 62 : 141–55. doi : 10.1146/annurev-med-042909-093756 . ПМК 3759035 . ПМИД 21090961 .
- ^ Клатт Н.Р., Чомон Н., Дуек Д.С., Дикс С.Г. (июль 2013 г.). «Иммунная активация и персистенция ВИЧ: последствия для подходов к лечению ВИЧ-инфекции» . Иммунологические обзоры . 254 (1): 326–42. дои : 10.1111/imr.12065 . ПМЦ 3694608 . ПМИД 23772629 .
- ^ Салазар-Гонсалес Дж.Ф., Мартинес-Маза О., Нишанян П., Азиз Н., Шен Л.П., Гроссер С. и др. (август 1998 г.). «Повышенная иммунная активация предшествует точке перегиба CD4 Т-клеток и увеличению вирусной нагрузки в сыворотке крови при инфекции вируса иммунодефицита человека» . Журнал инфекционных болезней . 178 (2): 423–30. дои : 10.1086/515629 . ПМИД 9697722 .
- ^ Ипп Х, Землян А (февраль 2013 г.). «Парадокс иммунного ответа при ВИЧ-инфекции: когда воспаление становится вредным». Клиника Химика Акта; Международный журнал клинической химии . 416 : 96–9. дои : 10.1016/j.cca.2012.11.025 . ПМИД 23228847 .
- ^ Наси М., Пинти М., Муссини С., Коссарица А. (октябрь 2014 г.). «Стойкое воспаление при ВИЧ-инфекции: устоявшиеся концепции, новые перспективы». Письма по иммунологии . 161 (2): 184–8. дои : 10.1016/j.imlet.2014.01.008 . ПМИД 24487059 .
- ^ Милуш Дж.М., Мир К.Д., Сундараварадан В., Гордон С.Н., Энграм Дж., Кано К.А. и др. (март 2011 г.). «Отсутствие клинического СПИДа у инфицированных SIV сажистых мангабеев со значительной потерей CD4+ Т-клеток связано с дважды негативными Т-клетками» . Журнал клинических исследований . 121 (3): 1102–10. дои : 10.1172/JCI44876 . ПМК 3049370 . ПМИД 21317533 .
- ^ Рей-Куйе М.А., Бертье Дж.Л., Бомзель-Демонтой М.К., Чадук И., Монтанье Л., Хованессян А.Г. и др. (май 1998 г.). «Вирус иммунодефицита обезьян реплицируется до высоких уровней в сажистых мангабеях, не вызывая заболевания» . Журнал вирусологии . 72 (5): 3872–86. doi : 10.1128/JVI.72.5.3872-3886.1998 . ПМК 109612 . ПМИД 9557672 .
- ^ Чахруди А., Босингер С.Е., Вандерфорд Т.Х., Пайардини М., Сильвестри Г. (март 2012 г.). «Естественные хозяева ВИО: показывая СПИДу дверь» . Наука . 335 (6073): 1188–93. Бибкод : 2012Sci...335.1188C . дои : 10.1126/science.1217550 . ПМЦ 3822437 . ПМИД 22403383 .
- ^ Перейти обратно: а б Дойтш Г., Галлоуэй Н.Л., Гэн Х, Ян З., Монро К.М., Зепеда О. и др. (январь 2014 г.). «Гибель клеток в результате пироптоза приводит к истощению Т-клеток CD4 при инфекции ВИЧ-1» . Природа . 505 (7484): 509–14. Бибкод : 2014Natur.505..509D . дои : 10.1038/nature12940 . ПМК 4047036 . ПМИД 24356306 .
- ^ Монро К.М., Ян З., Джонсон Дж.Р., Гэн Икс, Дойтш Г., Кроган Н.Дж. и др. (январь 2014 г.). «ДНК-сенсор IFI16 необходим для гибели лимфоидных Т-клеток CD4, абортивно инфицированных ВИЧ» . Наука . 343 (6169): 428–32. Бибкод : 2014Sci...343..428M . дои : 10.1126/science.1243640 . ПМК 3976200 . ПМИД 24356113 .
- ^ Галлоуэй Н.Л., Дойтш Г., Монро К.М., Ян З., Муньос-Ариас И., Леви Д.Н. и др. (сентябрь 2015 г.). «Передача ВИЧ-1 от клетки к клетке необходима для запуска пироптотической гибели CD4 Т-клеток, полученных из лимфоидной ткани» . Отчеты по ячейкам . 12 (10): 1555–1563. дои : 10.1016/j.celrep.2015.08.011 . ПМЦ 4565731 . ПМИД 26321639 .
- ^ Дойтш Дж., Грин WC (март 2016 г.). «Разбираем, как Т-клетки CD4 теряются во время ВИЧ-инфекции» . Клетка-хозяин и микроб . 19 (3): 280–91. дои : 10.1016/j.chom.2016.02.012 . ПМЦ 4835240 . ПМИД 26962940 .
- ^ «Исследование VX-765 у субъектов с резистентной к лечению парциальной эпилепсией – полнотекстовый просмотр – ClinicalTrials.gov» . www.clinicaltrials.gov . 19 декабря 2013 года. Архивировано из оригинала 26 сентября 2022 года . Проверено 21 мая 2016 г.
- ^ Эминг С.А., Криг Т., Дэвидсон Дж.М. (март 2007 г.). «Воспаление при заживлении ран: молекулярные и клеточные механизмы» . Журнал исследовательской дерматологии . 127 (3): 514–25. дои : 10.1038/sj.jid.5700701 . ПМИД 17299434 .
- ^ Эшкрофт Г.С., Ян Х., Глик А.Б., Вайнштейн М., Леттерио Дж.Л., Мизель Д.Е. и др. (сентябрь 1999 г.). «У мышей, лишенных Smad3, наблюдается ускоренное заживление ран и нарушение местной воспалительной реакции». Природная клеточная биология . 1 (5): 260–6. дои : 10.1038/12971 . ПМИД 10559937 . S2CID 37216623 .
- ^ Эшкрофт Г.С. (декабрь 1999 г.). «Двунаправленная регуляция функции макрофагов с помощью TGF-бета» . Микробы и инфекции . 1 (15): 1275–82. дои : 10.1016/S1286-4579(99)00257-9 . ПМИД 10611755 . Архивировано из оригинала 10 января 2020 года . Проверено 11 сентября 2019 г.
- ^ Вернер Ф., Джайн М.К., Фейнберг М.В., Сибинга Н.Е., Пеллакани А., Визель П. и др. (ноябрь 2000 г.). «Ингибирование активации трансформирующего фактора роста-бета 1 опосредовано через Smad3» . Журнал биологической химии . 275 (47): 36653–8. дои : 10.1074/jbc.M004536200 . ПМИД 10973958 .
- ^ Сато Ю, Осима Т, Кондо Т (ноябрь 1999 г.). «Регуляторная роль эндогенного интерлейкина-10 в кожной воспалительной реакции при заживлении ран у мышей». Связь с биохимическими и биофизическими исследованиями . 265 (1): 194–9. дои : 10.1006/bbrc.1999.1455 . ПМИД 10548513 .
- ^ Серхан CN (август 2008 г.). «Контроль разрешения острого воспаления: новый род двойных противовоспалительных и проразрешающих медиаторов». Журнал пародонтологии . 79 (8 дополнений): 1520–6. дои : 10.1902/jop.2008.080231 . ПМИД 18673006 .
- ^ Headland SE, Norling LV (май 2015 г.). «Разрешение воспаления: принципы и проблемы». Семинары по иммунологии . 27 (3): 149–60. дои : 10.1016/j.smim.2015.03.014 . ПМИД 25911383 .
- ^ Гринхал, Д.Г. (сентябрь 1998 г.). «Роль апоптоза в заживлении ран». Международный журнал биохимии и клеточной биологии . 30 (9): 1019–30. дои : 10.1016/S1357-2725(98)00058-2 . ПМИД 9785465 .
- ^ Цзян Д., Лян Дж., Фань Дж., Ю С., Чен С., Луо Ю. и др. (ноябрь 2005 г.). «Регуляция повреждения и восстановления легких с помощью Toll-подобных рецепторов и гиалуронана». Природная медицина . 11 (11): 1173–9. дои : 10.1038/nm1315 . ПМИД 16244651 . S2CID 11765495 .
- ^ Тедер П., Вандивье Р.В., Цзян Д., Лян Дж., Кон Л., Пюре Э. и др. (апрель 2002 г.). «Разрешение воспаления легких с помощью CD44». Наука . 296 (5565): 155–8. Бибкод : 2002Sci...296..155T . дои : 10.1126/science.1069659 . ПМИД 11935029 . S2CID 7905603 .
- ^ МакКиббан Г.А., Гонг Дж.Х., Тэм Э.М., Маккаллох К.А., Кларк-Льюис I, общий CM (август 2000 г.). «Воспаление, ослабленное желатиназой А, расщепляющим хемоаттрактантный белок-3 моноцитов». Наука . 289 (5482): 1202–6. Бибкод : 2000Sci...289.1202M . дои : 10.1126/science.289.5482.1202 . ПМИД 10947989 .
- ^ Серхан К.Н., Сэвилл Дж. (декабрь 2005 г.). «Разрешение воспаления: начало программирует конец». Природная иммунология . 6 (12): 1191–7. дои : 10.1038/ni1276 . ПМИД 16369558 . S2CID 22379843 .
- ^ Берк М., Уильямс Л.Дж., Джека Ф.Н., О'Нил А., Паско Дж.А., Мойлан С. и др. (сентябрь 2013 г.). «Итак, депрессия — это воспалительное заболевание, но откуда берется воспаление?» . БМК Медицина . 11 :200. дои : 10.1186/1741-7015-11-200 . ПМЦ 3846682 . ПМИД 24228900 .
- ^ Кокс В.Т., Абрамсон Л.И., Дивайн П.Г., Холлон С.Д. (сентябрь 2012 г.). «Стереотипы, предрассудки и депрессия: комплексная перспектива». Перспективы психологической науки . 7 (5): 427–49. дои : 10.1177/1745691612455204 . ПМИД 26168502 . S2CID 1512121 .
- ^ Киколт-Глейзер Дж. К., Дерри Х. М., Фагундес С. П. (ноябрь 2015 г.). «Воспаление: депрессия разжигает пламя и наслаждается жарой» . Американский журнал психиатрии . 172 (11): 1075–91. дои : 10.1176/appi.ajp.2015.15020152 . ПМК 6511978 . ПМИД 26357876 .
- ^ Уильямс С (4 января 2015 г.). «Является ли депрессия своего рода аллергической реакцией?» . Хранитель . Архивировано из оригинала 21 октября 2022 года . Проверено 11 декабря 2016 г.
- ^ Брицке Э., Стерц Л., Фернандес Б.С., Кауэр-Сантанна М., Маскаренхас М., Экостеги Варгас А. и др. (август 2009 г.). «Сравнение уровней цитокинов у депрессивных, маниакальных и эутимических пациентов с биполярным расстройством». Журнал аффективных расстройств . 116 (3): 214–7. дои : 10.1016/j.jad.2008.12.001 . ПМИД 19251324 .
- ^ Мюллер Н., Шварц М.Дж., Денинг С., Дуэ А., Церовецкий А., Гольдштейн-Мюллер Б. и др. (июль 2006 г.). «Ингибитор циклооксигеназы-2 целекоксиб оказывает терапевтическое действие при большой депрессии: результаты двойного слепого рандомизированного плацебо-контролируемого дополнительного пилотного исследования к ребоксетину» . Молекулярная психиатрия . 11 (7): 680–4. дои : 10.1038/sj.mp.4001805 . ПМИД 16491133 .
- ^ Канли Т (2014). «Переосмысление большого депрессивного расстройства как инфекционного заболевания» . Биология расстройств настроения и тревожных расстройств . 4:10 . дои : 10.1186/2045-5380-4-10 . ПМЦ 4215336 . ПМИД 25364500 .
- ^ Сайни А., О Т.Х., Ганем Д.А., Кастро М., Батлер М., Син Фай Лам CC и др. (октябрь 2022 г.). «Маркеры воспаления и газов крови при делирии COVID-19 по сравнению с делирием, не связанным с COVID-19: поперечное исследование» . Старение и психическое здоровье . 26 (10): 2054–2061. дои : 10.1080/13607863.2021.1989375 . ПМИД 34651536 . S2CID 238990849 . Архивировано из оригинала 22 октября 2021 года . Проверено 20 февраля 2023 г.
- ^ Раманлал Р., Гупта В. (2021). «Физиология, вазодилатация» . СтатПерлс . Остров сокровищ (Флорида): StatPearls Publishing. ПМИД 32491494 . Архивировано из оригинала 11 мая 2021 года . Проверено 22 сентября 2021 г.
- ^ Перейти обратно: а б Паримисетти А., Дорсеманс А.С., Авада Р., Раванан П., Диотель Н., Лефевр д'Элленкур К. (март 2016 г.). «Секретный разговор между жировой тканью и центральной нервной системой посредством секретируемых факторов – новый рубеж в нейродегенеративных исследованиях» . Журнал нейровоспаления (обзор). 13 (1): 67. дои : 10.1186/s12974-016-0530-x . ПМЦ 4806498 . ПМИД 27012931 .
- ^ Кершоу Э.Э., Флиер Дж.С. (июнь 2004 г.). «Жировая ткань как эндокринный орган» . Журнал клинической эндокринологии и метаболизма . 89 (6): 2548–56. дои : 10.1210/jc.2004-0395 . ПМИД 15181022 .
- ^ Bastard JP, Jardel C, Bruckert E, Blondy P, Capeau J, Laville M и др. (сентябрь 2000 г.). «Повышенные уровни интерлейкина 6 снижаются в сыворотке и подкожной жировой ткани у женщин с ожирением после потери веса» . Журнал клинической эндокринологии и метаболизма . 85 (9): 3338–42. дои : 10.1210/jcem.85.9.6839 . ПМИД 10999830 .
- ^ Мохамед-Али В., Флауэр Л., Сетхи Дж., Хотамислигил Г., Грей Р., Хамфрис С.Э. и др. (декабрь 2001 г.). «Бета-адренергическая регуляция высвобождения IL-6 из жировой ткани: исследования in vivo и in vitro» . Журнал клинической эндокринологии и метаболизма . 86 (12): 5864–9. дои : 10.1210/jcem.86.12.8104 . ПМИД 11739453 . S2CID 73100391 .
- ^ Перейти обратно: а б с д и ж г Лоффреда С., Ян С.К., Лин Х.З., Карп К.Л., Бренгман М.Л., Ван DJ и др. (январь 1998 г.). «Лептин регулирует провоспалительные иммунные реакции» . Журнал ФАСЭБ . 12 (1): 57–65. дои : 10.1096/fasebj.12.1.57 . ПМИД 9438411 .
- ^ Перейти обратно: а б с д и ж г Эспозито К., Наппо Ф., Марфелла Р., Джулиано Дж., Джулиано Ф., Чиотола М. и др. (октябрь 2002 г.). «Концентрация воспалительных цитокинов резко увеличивается при гипергликемии у людей: роль окислительного стресса» . Тираж . 106 (16): 2067–72. doi : 10.1161/01.CIR.0000034509.14906.AE . ПМИД 12379575 .
- ^ Петерсен А.М., Педерсен Б.К. (апрель 2005 г.). «Противовоспалительный эффект физических упражнений». Журнал прикладной физиологии . 98 (4): 1154–62. doi : 10.1152/japplphysicalol.00164.2004 . ПМИД 15772055 . S2CID 4776835 .
- ^ Роговский О., Шапира И., Бассат О.К., Чундадзе Т., Финн Т., Берлинер С. и др. (июль 2010 г.). «Окружность талии как основной фактор, способствующий микровоспалительной реакции при метаболическом синдроме: поперечное исследование» . Журнал воспаления . 7:35 . дои : 10.1186/1476-9255-7-35 . ПМК 2919526 . ПМИД 20659330 .
- ^ Goldfine AB, Shoelson SE (январь 2017 г.). «Терапевтические подходы к воспалению при диабете и связанному с ним сердечно-сосудистому риску» . Журнал клинических исследований . 127 (1): 83–93. дои : 10.1172/jci88884 . ПМК 5199685 . ПМИД 28045401 .
- ^ Чой Дж., Джозеф Л., Пилот Л. (март 2013 г.). «Ожирение и С-реактивный белок в различных популяциях: систематический обзор и метаанализ». Обзоры ожирения . 14 (3): 232–44. дои : 10.1111/обр.12003 . ПМИД 23171381 . S2CID 206227739 .
Внешние ссылки
[ редактировать ]- Воспаление Национальной медицинской библиотеки США по медицинским предметным рубрикам (MeSH)