синдром Каллмана
| синдром Каллмана | |
|---|---|
| Другие имена | Наследственная аносмия Каллмана |
| Специальность | Эндокринология |
| Симптомы | Отсутствие или задержка полового созревания , бесплодие , неспособность обонять. |
| Осложнения | Остеопороз |
| Обычное начало | Присутствует при рождении |
| Продолжительность | Пожизненный |
| Уход | Заместительная гормональная терапия Гонадотропиновая терапия |
| Частота | 1:30 000 (мужчины), 1:125 000 (женщины) |
Синдром Каллмана ( СК ) – генетическое заболевание, которое не позволяет человеку начать или полностью завершить половое созревание . Синдром Каллмана — это форма группы состояний, называемых гипогонадотропным гипогонадизмом . [1] Чтобы отличить его от других форм гипогонадотропного гипогонадизма, синдром Каллмана имеет дополнительный симптом полного отсутствия обоняния (аносмии) или снижения обоняния . [2] [3] [4] Если не лечить, у людей будут плохо выраженные вторичные половые признаки , появятся признаки гипогонадизма , почти всегда бесплодие и повышенный риск развития остеопороза . [2] Также может возникнуть ряд других физических симптомов, затрагивающих лицо, руки и скелет. [3]
Причина и диагноз
[ редактировать ]нарушение правильной выработки или активности гонадотропин-рилизинг гормона гипоталамусом Основной причиной является . Это приводит к снижению уровня половых гормонов тестостерона у мужчин или эстрогена и прогестерона у женщин. Диагноз обычно ставится в подростковом возрасте, когда половое созревание еще не наступило. [4] Диагноз синдрома Каллмана основывается на клиническом обследовании, эндокринном тестировании и генетическом анализе. Уровни гормонов обычно показывают низкие уровни половых стероидов и гонадотропинов. [5]
Уход
[ редактировать ]Обычно требуется пожизненное лечение для обоих полов. Заместительная гормональная терапия (ЗГТ) является основной формой лечения, целью которой является восполнение недостающего тестостерона или эстрогена и прогестерона. Также доступны специализированные методы лечения бесплодия. [6] Заместительная гормональная терапия используется для индукции и поддержания вторичных половых признаков и фертильности. [7]
Эпидемиология и история
[ редактировать ]Заболевание чаще диагностируется у мужчин, чем у женщин. [8] Исследование населения Финляндии, проведенное в 2011 году, показало, что заболеваемость в целом составляет 1 на 48 000 человек, при этом 1 на 30 000 для мужчин и 1 на 125 000 для женщин. [9] Синдром Каллмана был впервые описан по имени в статье, опубликованной в 1944 году Францем Йозефом Каллманном , немецко - американским генетиком . [10] [11] Связь между аносмией и гипогонадизмом была отмечена еще испанским врачом Аурелиано Маэстре де Сан-Хуан в 1856 году. [12] [13]
Этиология
[ редактировать ]Синдром Каллмана вызван мутациями в нескольких генах, участвующих в развитии гипоталамуса и обонятельных луковиц, включая KAL1, FGFR1, FGF8, PROKR2 и PROK2. Эти мутации нарушают миграцию нейронов, продуцирующих ГнРГ, из обонятельной плакоды в гипоталамус во время эмбрионального развития. [14]
Признаки и симптомы
[ редактировать ]

Обычно трудно отличить случай синдрома Каллмана (КС)/гипогонадотропного гипогонадизма (ГГ) от простой конституциональной задержки полового созревания . Однако, если половое созревание не началось ни к 14 годам (девочки), ни к 15 годам (мальчики) и присутствует один или несколько из нерепродуктивных признаков, упомянутых ниже, то направление к репродуктивному эндокринологу . может быть целесообразным [15] [2] [8]
Особенности СК и других форм ГГ можно разделить на две разные категории; «репродуктивный» и «нерепродуктивный». [4] [13] [6] [16] [3]
Репродуктивные особенности
[ редактировать ]- Невозможность начала или полного полового созревания. [2]
- Недостаточное развитие яичек у мужчин (размер < 4 мл, тогда как в норме от 12 до 25 мл). [2]
- Первичная аменорея (нарушение начала менструации ). [8]
- Плохо выраженные вторичные половые признаки. [3]
- Микропенис в 5-10% случаев у мужчин. [2]
- Крипторхизм (неопущение яичек) при рождении. [2]
- Низкий уровень гонадотропинов ЛГ и ФСГ . [3]
- Гипогонадизм из-за низкого уровня тестостерона у мужчин или эстрогена / прогестерона у женщин. [3]
- Бесплодие . [2]
Нерепродуктивные особенности
[ редактировать ]- Полное отсутствие обоняния ( аносмия ) или заметно сниженное обоняние (гипосмия). Это определяющая особенность синдрома Каллмана; в других случаях ГГ он не наблюдается. Примерно 50% случаев ГГ протекают с аносмией и могут быть названы синдромом Каллмана. [3]
- Расщелина неба , расщелина губы или другие черепно-лицевые дефекты срединной линии. [4]
- Нейронные нарушения слуха [3]
- Отсутствие одной из почек (односторонняя агенезия почек) [3]
- Дефекты скелета, включая расщепление кисти/стопы ( эктродактилия ), укорочение среднего пальца (пястной кости) [3] или сколиоз [17]
- Мануальная синкинезия (зеркальные движения рук) [3]
- Отсутствие зубов (гиподонтия) [3]
- Плохой баланс или координация из-за церебральной атаксии . [8]
- Дефекты глаз, такие как колобома или птоз . [13]
- Повышенная заболеваемость дальтонизмом. [18] [19]
Точная генетическая природа каждого конкретного случая СК/ГГ будет определять, какие из нерепродуктивных особенностей возникнут, если таковые имеются. Тяжесть симптомов также будет варьироваться от случая к случаю. Даже у членов семьи не будет такого же диапазона или тяжести симптомов. [3] [8]
KS/HH чаще всего присутствует с рождения, но варианты, возникающие во взрослом возрасте, встречаются как у мужчин, так и у женщин. В этих случаях ось гипоталамус-гипофиз-гонады (ось HPG) функционирует нормально при рождении и в течение всей взрослой жизни, обеспечивая нормальное половое созревание и нормальную репродуктивную функцию. Затем ось HPG либо полностью выходит из строя, либо уровень высвобождения ГнРГ снижается до очень низкого уровня во взрослой жизни без очевидной причины (например, опухоли гипофиза). Это приведет к падению уровня тестостерона или эстрогена и бесплодию. [17] [20]
Функциональная гипоталамическая аменорея наблюдается у женщин, у которых ось HPG подавляется в ответ на физический или психологический стресс или недостаточное питание, но обратима при устранении стрессора. [2]
Некоторые случаи KS/HH, по-видимому, обращаются вспять во взрослой жизни, когда ось HPG возобновляет свою нормальную функцию, а уровни GnRH, LH и FSH возвращаются к нормальным уровням. По оценкам, это происходит примерно у 10–22% людей, в первую очередь в случаях нормосмического врожденного гипогонадотропного гипогонадизма (ВГГ), а не в случаях СК, и встречается только у людей, прошедших ту или иную форму заместительной терапии тестостероном. Обычно это обнаруживается только тогда, когда объем яичек увеличивается во время лечения только тестостероном, а уровень тестостерона возвращается к норме после прекращения лечения. Этот тип KS/HH редко возникает в тех случаях, когда у мужчин в анамнезе наблюдалось неопущение яичек. [8] [4]
Больные СК и другими формами ГГ почти всегда рождаются с нормальной половой дифференциацией; т. е. физически они мужчины или женщины. Это связано с хорионическим гонадотропином человека (ХГЧ), вырабатываемым плацентой примерно на сроке беременности от 12 до 20 недель (беременности), на который обычно не влияют СК или ХГГ. [21]
У людей с СК/ГГ отсутствует всплеск уровня ГнРГ, ЛГ и ФСГ, который обычно происходит в период от рождения до шестимесячного возраста, называемый мини-пубертатным периодом . Этот всплеск особенно важен для мальчиков, поскольку он помогает опустить яички в мошонку. Всплеск ГнРГ/ЛГ/ФСГ у детей без СК/ГГ дает определяемые уровни тестостерона у мальчиков и эстрогена и прогестерона у девочек. Отсутствие этого всплеска иногда можно использовать в качестве диагностического инструмента при подозрении на СК/ГГ у новорожденного мальчика, но обычно он недостаточно выражен для диагностики у девочек. [4]
Остеопороз
[ редактировать ]Одним из возможных побочных эффектов KS/CHH является повышенный риск развития вторичного остеопороза или остеопении . Эстроген (женщины) или тестостерон (мужчины) необходимы для поддержания плотности костей . [22] Дефицит тестостерона или эстрогена может увеличить скорость резорбции кости и в то же время замедлить скорость костеобразования . В целом это может привести к ослаблению и хрупкости костей, которые имеют более высокую склонность к переломам. [ нужна ссылка ]
Даже короткое время с низким уровнем эстрогена или тестостерона, как в случае поздней диагностики KS/CHH, может привести к повышенному риску развития остеопороза, но задействованы и другие факторы риска, такие как курение, поэтому риск его развития будет варьироваться от человека к человеку. человек. Сканирование плотности костной ткани рекомендуется для мониторинга минеральной плотности костной ткани. [17]
Сканирование плотности кости известно как двухэнергетическое рентгеновское абсорбциометрическое сканирование (DEXA или DXA). Это простой тест, выполнение которого займет менее 15 минут. Он включает в себя получение специализированного рентгеновского изображения позвоночника и бедер, измерение минеральной плотности костей и сравнение результата со средним значением для молодого здорового взрослого населения в целом. [23]
Адекватный уровень кальция и, что, возможно, что более важно, уровень витамина D необходимы для здоровой плотности костей. Некоторым людям с KS/CHH проверят уровень витамина D, и им могут быть назначены дополнительные таблетки или инъекции витамина D, чтобы попытаться предотвратить ухудшение состояния. Роль витамина D для общего состояния здоровья в настоящее время находится под пристальным вниманием: некоторые исследователи утверждают, что дефицит витамина D распространен во многих группах населения и может быть связан с другими заболеваниями. [24]
Некоторым людям с тяжелым остеопорозом в дополнение к заместительной гормональной терапии могут быть назначены бисфосфонаты для сохранения костной массы. [25]
Генетика
[ редактировать ]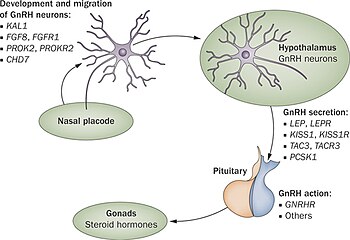
На сегодняшний день по крайней мере 25 различных генов вовлечены в возникновение синдрома Каллмана или других форм гипогонадотропного гипогонадизма вследствие нарушения выработки или активности ГнРГ (37). Эти задействованные гены охватывают все формы наследования , и не было выявлено ни одного генного дефекта, который был бы общим для всех случаев, что затрудняет генетическое тестирование и прогнозирование наследования. [26] [27]
Число генов, которые, как известно, вызывают случаи KS/CHH, все еще увеличивается. [16] Кроме того, считается, что некоторые случаи KS/CHH вызваны двумя отдельными генными дефектами, возникающими одновременно. [8]
Отдельные дефекты генов могут быть связаны с конкретными симптомами, которые могут помочь определить, какие гены следует проверить. [8] [3] От 35 до 45% случаев СК/ХГГ имеют неизвестную генетическую причину. [28]
Дефект гена ANOS1 (ранее известный как KAL-1) был первым обнаруженным и наиболее часто проверяемым. Он вызывает Х-сцепленную форму синдрома Каллмана и связан с дополнительными симптомами аносмии , бимануальной синкинезии и агенезии почек . Считается, что этот дефект является причиной от 5 до 10% всех случаев синдрома Каллмана/CHH. [8] [3]
Патофизиология
[ редактировать ]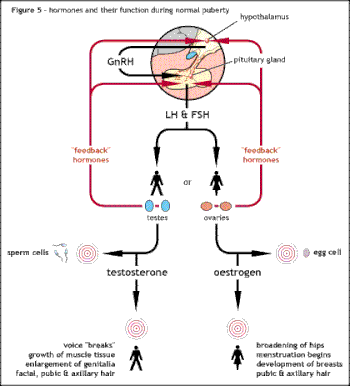
(из PDB : 1YY1 )
Первопричиной синдрома Каллмана или других форм гипогонадотропного гипогонадизма является нарушение правильного действия гипоталамического гормона ГнРГ . Термин «изолированный дефицит ГнРГ» (ИГД) все чаще используется для описания этой группы состояний, поскольку он подчеркивает основную причину этих состояний и отличает их от других состояний, таких как синдром Клайнфельтера или синдром Тернера , которые имеют некоторые схожие симптомы, но имеют другую этиологию. . [29] Термин «гипогонадизм» описывает низкий уровень циркулирующих половых гормонов ; тестостерон у мужчин и эстроген и прогестерон у женщин. Гипогонадизм может возникать по разным механизмам. Использование термина «гипогонадотропный» связано с тем фактом, что гипогонадизм, обнаруженный при ГГ, вызван нарушением выработки гонадотропных гормонов, обычно выделяемых передней долей гипофиза, известных как лютеинизирующий гормон (ЛГ) и фолликулостимулирующий гормон (ФСГ). [16] [28] В противном случае нарушение активности ГнРГ может быть связано с отсутствием нейронов, высвобождающих ГнРГ, внутри гипоталамуса. ГГ может возникать как изолированное состояние, при котором затрагивается только выработка ЛГ и ФСГ, или может возникать при комбинированной недостаточности гипофиза. [ нужна ссылка ]
В первые 10 недель нормального эмбрионального развития нейроны, высвобождающие ГнРГ, мигрируют из своего первоначального источника в носовой области и попадают в гипоталамус. Эти нейроны берут начало в области развивающейся головки, обонятельной плакоде , которая дает начало обонятельному эпителию; затем они проходят через решетчатую пластинку вместе с волокнами обонятельных нервов и попадают в ростральный отдел переднего мозга . Оттуда они мигрируют в то, что станет гипоталамусом. Любые проблемы с развитием волокон обонятельного нерва будут препятствовать продвижению нейронов, высвобождающих ГнРГ, к мозгу. [30]
Диагностика
[ редактировать ]Диагностика СК и других форм ХГГ осложняется трудностями различения между нормальной конституциональной задержкой полового созревания и случаем СК/ХГГ. [31] [6] [32] Диагноз часто является диагнозом исключения, выявляемым при обследовании задержки полового созревания . [33] [34] [35]
У мужчин использование соответствующих возрасту уровней тестостерона может помочь отличить случай KS/CHH от случая задержки полового созревания. Если половое созревание не наблюдается, особенно развитие яичек, может быть целесообразным обратиться к репродуктивному эндокринологу. Если к 16 годам половое созревание не проявляется, человека следует направить на эндокринологическое обследование. [36] Постнатальная диагностика СК/ХГГ иногда возможна в возрасте до 6 месяцев, поскольку у детей с СК/ХГГ отсутствует нормальный постнатальный гормональный всплеск гонадотропинов вместе с тестостероном или эстрогеном. Отсутствие обнаруживаемых гормонов в крови можно использовать в качестве диагностического показателя, особенно у младенцев мужского пола. [37]
У женщин диагноз иногда откладывается, поскольку обычно сначала необходимо исследовать другие причины аменореи , прежде чем рассматривать случай СК/ГКГ. [38]
Диагностика KS/CHH в норме включает ряд клинических, биохимических и радиологических тестов для исключения других состояний, которые могут вызывать аналогичные симптомы. [ нужна ссылка ]
Клинические испытания
[ редактировать ]- Сравнение роста со стандартными диаграммами роста.
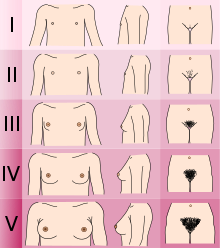
- Определение Таннеровской стадии полового развития. (Мужчины с KS/CHH обычно находятся на стадии I или II с гениталиями, женщины на стадии I с развитием молочных желез и как мужчины, так и женщины на стадии III с развитием лобковых волос). [3]
- Проверка на микропенис и неопущение яичек ( крипторхизм ) у мужчин.
- Измерение объема яичек.
- Проверка развития молочных желез и возраста менархе у женщин.
- Проверка обоняния с помощью панели одорантов или теста идентификации запаха Пенсильванского университета (UPSIT)
- Проверка слуха на предмет нарушения слуха.
- Проверка отсутствия зубов или наличия расщелины губы и/или неба .
- Проверка пигментации кожи и волос.
- Проверка зеркальных движений рук или признаков задержки нервного развития .
Лабораторные тесты
[ редактировать ]- Рано утром гормональный анализ, включая ФСГ , ЛГ , тестостерон , эстроген и пролактин .
- Тест стимуляции ГнРГ и/или ХГЧ для определения активности гипоталамуса и гипофиза .
- Тест спермы
- Функция печени , функция почек и маркеров воспаления . тестирование
- Кариотипирование для выявления хромосомных аномалий.
Медицинская визуализация
[ редактировать ]- Проведение рентгенографии запястья для определения костного возраста.
- головного мозга МРТ , чтобы исключить любые структурные аномалии в гипоталамусе или гипофизе и проверить наличие обонятельных луковиц .
- УЗИ почек для исключения односторонней агенезии почек .
- Сканирование плотности костей ( DXA ) для выявления остеопороза или остеопении .
Уход
[ редактировать ]
Как для мужчин, так и для женщин первоначальной целью лечения является развитие вторичных половых признаков, обычно наблюдаемых в период полового созревания. [3] [39] [34] [35] [40] Как только это будет достигнуто, продолжение заместительной гормональной терапии как мужчинам, так и женщинам потребуется для поддержания сексуальной функции, здоровья костей, либидо и общего благополучия. [4] У мужчин заместительная терапия тестостероном необходима для поддержания нормальной мышечной массы. [3]
Младенцам мужского пола с подозрением на СК/ХГГ иногда требуется раннее лечение для коррекции неопустившихся яичек и микропениса , если таковые имеются, с помощью хирургического вмешательства или гонадотропинами или ДГТ лечения . Женщины с СК/ХГГ обычно не нуждаются в каком-либо лечении до подросткового возраста. В настоящее время не существует лечения отсутствия обоняния, зеркального движения рук или отсутствия одной почки. [4]
Лечение как мужчин, так и женщин с СК/ХГГ обычно состоит из одного из трех вариантов, которые могут использоваться как для заместительной гормональной терапии, так и для лечения бесплодия. [3] [4]
- Заместительная терапия половыми гормонами (тестостероном или эстрогеном и прогестероном).
- Гонадотропиновая терапия (препараты, повторяющие активность ФСГ и ЛГ).
- Пульсирующая терапия ГнРГ.
Заместительная гормональная терапия
[ редактировать ]Метод и доза лечения будут варьироваться в зависимости от человека, которого лечат. Первоначальное лечение обычно проводится более низкими дозами у более молодых пациентов с целью развития вторичных половых признаков до того, как будут достигнуты дозы для взрослых. [3]
Для мужчин с СК/ВГГ способы доставки тестостерона включают ежедневные пластыри, ежедневное использование геля, ежедневные капсулы, подкожные или внутримышечные инъекции или шестимесячные имплантаты. Различные формы тестостерона используются для достижения как анаболического , так и андрогенного эффекта тестостерона. [4] [6] Были разработаны методы назальной доставки тестостерона, но их использование в лечении KS/CHH официально не оценивалось. [3]
Гонадотропиновая терапия в виде инъекций хорионического гонадотропина человека (ХГЧ) с использованием или без использования ФСГ также может использоваться у пациентов мужского пола для индукции развития вторичных половых признаков наряду с возможной индукцией фертильности. [4]
У женщин заместительная гормональная терапия включает использование эстрогена и прогестерона. Сначала эстроген используется в форме таблеток или геля, чтобы максимизировать развитие груди, затем используется комбинация эстрогена и прогестерона. [4] [3] Циклический прогестерон обычно необходим для поддержания здоровья эндометрия (слизистой оболочки матки ). [3]
У мужчин мониторинг лечения обычно требует измерения сывороточного тестостерона, ингибина B , гематокрита и простатспецифического антигена (ПСА). Если используются инъекции, принимаются минимальные уровни, чтобы обеспечить достижение адекватного уровня тестостерона на протяжении всего цикла инъекции. [4]
У женщин мониторинг обычно состоит из измерения уровня эстрогена, ФСГ, ЛГ, ингибина В и антимюллерова гормона (АМГ). [4]
Стандартная заместительная гормональная терапия обычно не вызывает фертильности ни у мужчин, ни у женщин, при этом у мужчин не наблюдается роста яичек. Раннее лечение в подростковом возрасте может помочь улучшить психологическое благополучие людей с СК/ВГГ. [4]
Лечение бесплодия
[ редактировать ]Терапия гонадотропинами может использоваться как у мужчин, так и у женщин для достижения фертильности у некоторых людей. [4] [3]
Пульсирующая ГнРГ-терапия также может использоваться для индуцирования фертильности, особенно у женщин, но ее применение ограничено несколькими специализированными лечебными центрами. [3]
У мужчин с KS/CHH бесплодие обусловлено в первую очередь отсутствием выработки спермы в семенниках . Производство спермы может быть достигнуто либо с помощью ГнРГ, вводимого через микроинфузионную помпу, либо с помощью инъекций гонадотропинов ( ХГЧ , ФСГ, ЧМГ ). Время, необходимое для достижения адекватного производства спермы для естественного зачатия, будет варьироваться от человека к человеку. Если яички до лечения были очень маленькими и в анамнезе наблюдалось неопущение яичек, для достижения производства спермы может потребоваться больше времени. В этих случаях вспомогательные репродуктивные технологии , такие как получение спермы с использованием экстракции сперматозоидов из яичка (TESE) и/или интрацитоплазматической инъекции спермы (ICSI). могут потребоваться [41]
У женщин с СК/ХГГ бесплодие обусловлено прежде всего отсутствием созревания яйцеклеток, расположенных в яичниках . Индукция овуляции может быть достигнута либо с помощью пульсирующей терапии ГнРГ, либо, альтернативно, с помощью инъекций гонадотропинов (ХГЧ, ФСГ, ЧМГ), вводимых через определенные промежутки времени, чтобы вызвать созревание и высвобождение яйцеклетки для естественного зачатия. [41]
Прогноз
[ редактировать ]Об обратном развитии симптомов сообщалось в 10–22% случаев. [42] [3]
Случаи реверсии наблюдались как при СК, так и при нормосмическом ХГГ, но, по-видимому, менее распространены в случаях СК (при котором также поражается обоняние). Реверсирование не всегда является постоянным, и точные генетические причины еще не до конца изучены. [43]
Эпидемиология
[ редактировать ]Эпидемиология синдрома Каллмана недостаточно изучена. Отдельные исследования включают отчет 1986 года, в котором анализируются медицинские записи в сардинской армии, в котором выявлена распространенность 1 на 86 000 мужчин. [44] и отчет из Финляндии за 2011 год, согласно которому распространенность составляет 1:30 000 среди мужчин и 1:125 000 среди женщин. [45]
Синдром Каллмана встречается примерно в 4 раза чаще у мужчин, чем у женщин, но лишь в 2,5 раза чаще встречается среди мужчин в семейных случаях. [44] [45]
История
[ редактировать ]
Синдром Каллмана был впервые описан по имени в статье, опубликованной в 1944 году Францем Йозефом Каллманном , немецко - американским генетиком . [10] [11] Связь между аносмией и гипогонадизмом была отмечена еще испанским врачом Аурелиано Маэстре де Сан-Хуан в 1856 году. [12] В 1950-х годах Де Морсье и Готье сообщили о частичном или полном отсутствии обонятельной луковицы в мозгу мужчин с гипогонадизмом. [46] [13]
Терминология
[ редактировать ]Терминология, используемая при описании случаев ГГ, различается и может включать: [ нужна ссылка ]
- Дефицит ГнРГ
- врожденный гипогонадотропный гипогонадизм (ВГГ) [47]
- идиопатический/ изолированный гипогонадотропный гипогонадизм (ИГГ)
- нормосмический гипогонадотропный гипогонадизм (нГГ)
- гипоталамический гипогонадизм
- обонятельно-генитальный синдром
Исследовать
[ редактировать ]Кисспептин — белок, регулирующий высвобождение ГнРГ из гипоталамуса, который, в свою очередь, регулирует высвобождение ЛГ и, в меньшей степени, ФСГ из передней доли гипофиза. Известно, что кисспептин и связанный с ним рецептор KISS1R участвуют в регуляции полового созревания. Исследования показали, что кисспептин может использоваться для диагностики и лечения некоторых случаев синдрома Каллмана и ВГГ. [48] [49]
Ссылки
[ редактировать ]- ^ Янг, Дж. (1 августа 1999 г.). «Антимюллеров гормон у больных гипогонадотропным гипогонадизмом» . Журнал клинической эндокринологии и метаболизма . 84 (8): 2696–2699. дои : 10.1210/jcem.84.8.5972 . ISSN 0021-972X . ПМИД 10443662 .
- ^ Jump up to: а б с д и ж г час я «Синдром Каллмана» . Домашний справочник по генетике. Медицинская библиотека США . Национальные институты здравоохранения. Информация о генетических и редких заболеваниях. 26 июня 2016 г. Проверено 17 декабря 2017 г.
- ^ Jump up to: а б с д и ж г час я дж к л м н тот п д р с т в v В х и С аа аб и Баласубраманиан Р., Кроули В.Ф. младший (2017). «Изолированный дефицит гонадотропин-рилизинг гормона (ГнРГ)». ИсточникGeneReviews . ПМИД 20301509 .
- ^ Jump up to: а б с д и ж г час я дж к л м н тот п д р с Бем Ю, Булу П.М., Даттани М.Т., де Ру Н., Доде С., Данкель Л., Дуайер А.А., Джакобини П., Харделин Дж.П., Юул А., Магни М., Питтелуд Н., Прево В., Райвио Т., Тена-Семпере М., Куинтон Р. , Янг Дж (сентябрь 2015 г.). «Документ экспертного консенсуса: Заявление Европейского консенсуса по врожденному гипогонадотропному гипогонадизму - патогенез, диагностика и лечение» . Обзоры природы. Эндокринология . 11 (9): 547–64. дои : 10.1038/nrendo.2015.112 . hdl : 11567/821921 . ПМИД 26194704 .
- ^ Гарроса, М. (2024). «Полустолетие со дня основания первой кафедры гистологии в Испании. Аурелиано Маэстре из Сан-Хуана» . Медицинские текущие дела . 109 (818): 7–8. дои : 10.15568/am.2024.818.ed01 . ISSN 2605-2083 .
- ^ Jump up to: а б с д Данкель Л., Куинтон Р. (июнь 2014 г.). «Переход в эндокринологии: индукция полового созревания» . Европейский журнал эндокринологии . 170 (6): 229–39 р. doi : 10.1530/EJE-13-0894 . ПМИД 24836550 .
- ^ Кристиансен, Питер; Скаккебек, Нильс Э. (2002). «Пульсирующее лечение гонадотропин-рилизинг-гормоном у мужчин с идиопатическим гипогонадотропным гипогонадизмом» . Гормональные исследования в педиатрии . 57 (1–2): 32–36. дои : 10.1159/000057944 . ISSN 1663-2818 . ПМИД 12006717 .
- ^ Jump up to: а б с д и ж г час я Лима Амато Л.Г., Латронико АС, Гонтихо Сильвейра Л.Ф. (июнь 2017 г.). «Молекулярные и генетические аспекты врожденного изолированного гипогонадотропного гипогонадизма». Клиники эндокринологии и обмена веществ Северной Америки . 46 (2): 283–303. дои : 10.1016/j.ecl.2017.01.010 . ПМИД 28476224 .
- ^ Лайтинен Э.М., Вааралахти К., Томмиска Дж., Эклунд Э., Терваниеми М., Валанн Л., Райвио Т. (июнь 2011 г.). «Заболеваемость, фенотипические особенности и молекулярная генетика синдрома Каллмана в Финляндии» . Сиротский журнал редких заболеваний . 6 (17 июня): 41. doi : 10.1186/1750-1172-6-41 . ПМК 3143089 . ПМИД 21682876 .
- ^ Jump up to: а б Каллманн Ф.Дж., Шенфельд В.А., Баррера С.Е. (1943–1944). «Генетические аспекты первичного евнухоидизма». Am J Ment Defic . 48 : 203–236.
- ^ Jump up to: а б Synd/2549 на сайте Who Named It?
- ^ Jump up to: а б Магистр Сан-Хуана Аурелиано (1856 г.). «Тератолагия: полное отсутствие обонятельных нервов с аносмией у человека, у которого наблюдалась врожденная атрофия яичек и полового члена». Медицинский век . 3 : 211–221.
- ^ Jump up to: а б с д Ким Ш. (декабрь 2015 г.). «Врожденный гипогонадотропный гипогонадизм и синдром Каллмана: прошлое, настоящее и будущее» . Эндокринология и обмен веществ . 30 (4): 456–66. дои : 10.3803/EnM.2015.30.4.456 . ПМЦ 4722398 . ПМИД 26790381 .
- ^ Доде, К.; Харделин, Ж.-П. (май 2010 г.). «Клиническая генетика синдрома Каллмана» . Анналы эндокринологии . 71 (3): 149–157. дои : 10.1016/j.ando.2010.02.005 . ISSN 0003-4266 .
- ^ Маккейб MJ, Bancalari RE, Dattani MT (февраль 2014 г.). «Диагностика и оценка гипогонадизма». Обзоры детской эндокринологии . 11 Приложение 2 (февраль): 214–29. ПМИД 24683946 .
- ^ Jump up to: а б с Митчелл А.Л., Дуайер А., Питтелуд Н., Куинтон Р. (июль 2011 г.). «Генетическая основа и вариабельное фенотипическое выражение синдрома Каллмана: к объединяющей теории». Тенденции в эндокринологии и обмене веществ . 22 (7): 249–58. дои : 10.1016/j.tem.2011.03.002 . ПМИД 21511493 . S2CID 23578201 .
- ^ Jump up to: а б с «Синдром Каллмана» . Редкие заболевания . Национальная организация редких заболеваний (NORD). 2012 . Проверено 16 декабря 2017 г.
- ^ Чопра Р., Чандер А., Джейкоб Дж.Дж. (май 2012 г.). «Глаз как окно к редким эндокринным заболеваниям» . Индийский журнал эндокринологии и метаболизма . 16 (3): 331–8. дои : 10.4103/2230-8210.95659 . ПМЦ 3354836 . ПМИД 22629495 .
- ^ Яффе М.Дж., Шеринс Р.Дж., де Монастерио Ф. (1989). Недостатки цветового зрения IX . Серия докладов Documenta Ophthalmologica. Дордрехт: Спрингер. стр. 201–207. дои : 10.1007/978-94-009-2695-0_24 . ISBN 9789401077156 .
- ^ «Синдром Каллмана» . Национальные институты здравоохранения. Медицинская библиотека США. Домашний справочник по генетике . Декабрь 2017 года . Проверено 17 декабря 2017 г.
- ^ Сперлинг, Марк (2014). Электронная книга по детской эндокринологии . Elsevier Науки о здоровье. п. 136. ИСБН 9781455759736 .
- ^ Го С.И., Джонс Т.Х., Истелл Р. (февраль 1997 г.). «Лечение изолированного гипогонадотропного гипогонадизма, влияние на минеральную плотность костной ткани и костный обмен» . Журнал клинической эндокринологии и метаболизма . 82 (2): 658–65. дои : 10.1210/jcem.82.2.3758 . ПМИД 9024272 .
- ^ Лайтинен Э.М., Герой М., Вааралахти К., Томмиска Дж., Райвио Т. (август 2012 г.). «Минеральная плотность костной ткани, состав тела и обмен костной ткани у пациентов с врожденным гипогонадотропным гипогонадизмом» . Международный журнал андрологии . 35 (4): 534–40. дои : 10.1111/j.1365-2605.2011.01237.x . ПМИД 22248317 .
- ^ Вималаванса С.Дж., Раззак Д.М., Аль-Дагри Н.М. (декабрь 2017 г.). «Кальций и витамин D для здоровья человека: реклама или реальность?». Журнал биохимии стероидов и молекулярной биологии . 16 декабря: 4–14. дои : 10.1016/j.jsbmb.2017.12.009 . ПМИД 29258769 . S2CID 11467429 .
- ^ Голдс Г., Хоудек Д., Арнасон Т. (2017). «Мужской гипогонадизм и остеопороз: эффекты, клинические последствия и лечение дефицита тестостерона для здоровья костей» . Int J Эндокринол . 2017 : 4602129. doi : 10.1155/2017/4602129 . ПМК 5376477 . ПМИД 28408926 .
- ^ Layman LC (май 2013 г.). «Клинико-генетическое тестирование синдрома Каллмана» . Журнал клинической эндокринологии и метаболизма . 98 (5): 1860–2. дои : 10.1210/jc.2013-1624 . ПМЦ 3644595 . ПМИД 23650337 .
- ^ Вальдес-Сосин Х., Рубио Альманса М., Томе Фернандес-Ладреда М., Дебрэ Ф.Г., Бурс В., Беккерс А. (2014). «Нарушения репродукции, обоняния и развития нервной системы: генетические дефекты при различных гипогонадотропных гипогонадных синдромах» . Границы эндокринологии . 5 (109): 109. дои : 10.3389/fendo.2014.00109 . ПМЦ 4088923 . ПМИД 25071724 .
- ^ Jump up to: а б Веццоли В., Думинуко П., Басси И., Гуиззарди Ф., Персани Л., Бономи М. (июнь 2016 г.). «Сложная генетическая основа врожденного гипогонадотропного гипогонадизма». Минерва Эндокринологическая . 41 (2): 223–39. ПМИД 26934720 .
- ^ Au MG, Кроули WF, Бак CL (октябрь 2011 г.). «Генетическое консультирование при изолированном дефиците ГнРГ» . Молекулярная и клеточная эндокринология . 346 (1–2): 102–9. дои : 10.1016/j.mce.2011.05.041 . ПМК 3185214 . ПМИД 21664415 .
- ^ Тейшейра Л., Гимио Ф., Доде С., Фалле-Бьянко С., Миллар Р.П., Делезойд А.Л., Харделин Дж.П. (октябрь 2010 г.). «Дефектная миграция нейроэндокринных клеток ГнРГ при арринэнцефалических состояниях человека» . Журнал клинических исследований . 120 (10): 3668–72. дои : 10.1172/JCI43699 . ПМЦ 2947242 . ПМИД 20940512 .
- ^ Питтелуд Н. (декабрь 2012 г.). «Управление задержкой или изменением полового созревания у мальчиков». БМЖ . 345 (3 декабря): e7913. дои : 10.1136/bmj.e7913 . ПМИД 23207503 . S2CID 5159169 .
- ^ Янг Джей (март 2012 г.). «Подход к пациенту мужского пола с врожденным гипогонадотропным гипогонадизмом» . Журнал клинической эндокринологии и метаболизма . 97 (3): 707–18. дои : 10.1210/jc.2011-1664 . ПМИД 22392951 .
- ^ Ли П.А., Хоук К.П. (13 августа 2012 г.). «Самый маленький ребенок в школе: оценка задержки полового созревания» . Медскейп Педиатрия .
- ^ Jump up to: а б Джонс Х, изд. (2008). «Глава 9: Половое созревание и фертильность». Дефицит тестостерона у мужчин . Оксфордская эндокринологическая библиотека. ISBN 978-0199545131 .
- ^ Jump up to: а б Йокенховел Ф (2004). «Глава 3: Диагностика гипогонадизма». Мужской гипогонадизм . Uni-Med Science. ISBN 978-3-89599-748-8 .
- ^ Куинтон Р. (апрель 2005 г.). «Развитие подростков: советы «Азбуки подросткового возраста» потенциально вводят в заблуждение» . БМЖ . 330 (7494): 789, ответ автора 789. doi : 10.1136/bmj.330.7494.789 . ПМК 555895 . ПМИД 15802728 .
- ^ Дуайер А.А., Джаясена С.Н., Куинтон Р. (июнь 2016 г.). «Врожденный гипогонадотропный гипогонадизм: последствия отсутствия мини-полового созревания». Минерва Эндокринологическая . 41 (2): 188–95. ПМИД 27213784 .
- ^ Бри-Гайяр Х., Трабадо С., Булиганд Дж., Сарфати Дж., Франку Б., Саленав С., Шансон П., Брайи-Табар С., Гиошон-Мантель А., Янг Дж. (май 2010 г.). «Врожденный гипогонадотропный гипогонадизм у женщин: клинический спектр, оценка и генетика». Анналы эндокринологии . 71 (3): 158–62. дои : 10.1016/j.ando.2010.02.024 . ПМИД 20363464 .
- ^ Буваттье С, Майоне Л, Булиганд Дж, Доде С, Гиошон-Мантель А, Янг Дж (октябрь 2011 г.). «Неонатальная гонадотропная терапия при врожденном гипогонадотропном гипогонадизме у мужчин». Обзоры природы. Эндокринология . 8 (3): 172–82. дои : 10.1038/nrendo.2011.164 . ПМИД 22009162 . S2CID 4564169 .
- ^ Хан Т.С., Булу, премьер-министр (июнь 2010 г.). «Какова оптимальная терапия для молодых мужчин с гипогонадотропным гипогонадизмом?» . Клиническая эндокринология . 72 (6): 731–7. дои : 10.1111/j.1365-2265.2009.03746.x . ПМИД 19912242 .
- ^ Jump up to: а б Майоне Л., Дуайер А.А., Франку Б., Гиошон-Мантель А., Бинар Н., Булиганд Дж., Янг Дж. (март 2018 г.). «ГЕНЕТИКА В ЭНДОКРИНОЛОГИИ: Генетическое консультирование при врожденном гипогонадотропном гипогонадизме и синдроме Каллмана: новые проблемы в эпоху олигогенизма и секвенирования следующего поколения» . Европейский журнал эндокринологии . 178 (3): R55–R80. doi : 10.1530/EJE-17-0749 . ПМИД 29330225 .
- ^ Сидхум В.Ф., Чан Ю.М., Липпинкотт М.Ф., Баласубраманиан Р., Куинтон Р., Пламмер Л., Дуайер А., Питтелуд Н., Хейс Ф.Дж., Холл Дж.Е., Мартин К.А., Боеппл П.А., Семинара С.Б. (март 2014 г.). «Реверс и рецидив гипогонадотропного гипогонадизма: устойчивость и хрупкость репродуктивной нейроэндокринной системы» . Журнал клинической эндокринологии и метаболизма . 99 (3): 861–70. дои : 10.1210/jc.2013-2809 . ПМЦ 3942233 . ПМИД 24423288 .
- ^ Дуайер А.А., Райвио Т., Питтелуд Н. (июнь 2016 г.). «ВЕДЕНИЕ ЭНДОКРИННЫХ ЗАБОЛЕВАНИЙ: Обратимый гипогонадотропный гипогонадизм» . Европейский журнал эндокринологии . 174 (6): R267–74. дои : 10.1530/EJE-15-1033 . ПМИД 26792935 .
- ^ Jump up to: а б Тритос, Николас А. (10 октября 2016 г.). «Синдром Каллмана и идиопатический гипогонадотропный гипогонадизм: предпосылки, патофизиология, эпидемиология» . электронная медицина.
{{cite journal}}: Для цитирования журнала требуется|journal=( помощь ) - ^ Jump up to: а б Баласубраманиан Р., Кроули В.Ф. (2 марта 2017 г.). «Изолированный дефицит гонадотропин-рилизинг гормона (ГнРГ)» . Джин Обзоры . Вашингтонский университет, Сиэтл. ПМИД 20301509 .
- ^ Де Морсье Дж., Готье Дж. (ноябрь 1963 г.). «[Запахно-генитальная дисплазия]». Патология и биология . 11 :1267–72. ПМИД 14099201 .
- ^ Вальдес-Сосин Х., Рубио Альманса М., Томе Фернандес-Ладреда М., Дебрэ Ф.Г., Бурс В., Беккерс А. (2014). «Нарушения репродукции, обоняния и развития нервной системы: генетические дефекты при различных гипогонадотропных гипогонадных синдромах» . Границы эндокринологии . 5 : 109. дои : 10.3389/fendo.2014.00109 . ПМЦ 4088923 . ПМИД 25071724 .
- ^ Скорупскайте К., Джордж Дж.Т., Андерсон Р.А. (2014). «Путь кисспептин-ГнРГ в репродуктивном здоровье и заболеваниях человека» . Обновление репродукции человека . 20 (4): 485–500. дои : 10.1093/humupd/dmu009 . ПМК 4063702 . ПМИД 24615662 .
- ^ Джордж Дж. Т., Семинара SB (ноябрь 2012 г.). «Кисспептин и гипоталамический контроль репродукции: уроки человека» . Эндокринология . 153 (11): 5130–6. дои : 10.1210/en.2012-1429 . ПМК 3473216 . ПМИД 23015291 .