–Ґ–µ—А–∞–њ–Є—П –Љ–Њ–љ–Њ–Ї–ї–Њ–љ–∞–ї—М–љ—Л–Љ–Є –∞–љ—В–Є—В–µ–ї–∞–Љ–Є
–Ь–Њ–љ–Њ–Ї–ї–Њ–љ–∞–ї—М–љ—Л–µ –∞–љ—В–Є—В–µ–ї–∞ (–Љ–Р—В) –Є–Љ–µ—О—В —А–∞–Ј–љ–Њ–Њ–±—А–∞–Ј–љ–Њ–µ —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Њ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ. –Ь–Њ–ґ–љ–Њ —Б–Њ–Ј–і–∞—В—М –Љ–Њ–љ–Њ–Ї–ї–Њ–љ–∞–ї—М–љ–Њ–µ –∞–љ—В–Є—В–µ–ї–Њ, –Ї–Њ—В–Њ—А–Њ–µ —Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Є —Б–≤—П–Ј—Л–≤–∞–µ—В—Б—П –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є —Б –ї—О–±–Њ–є –≤–љ–µ–Ї–ї–µ—В–Њ—З–љ–Њ–є –Љ–Є—И–µ–љ—М—О, —В–∞–Ї–Њ–є –Ї–∞–Ї –±–µ–ї–Ї–Є –Ї–ї–µ—В–Њ—З–љ–Њ–є –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є –Є —Ж–Є—В–Њ–Ї–Є–љ—Л . –Ш—Е –Љ–Њ–ґ–љ–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М –і–ї—П —В–Њ–≥–Њ, —З—В–Њ–±—Л —Б–і–µ–ї–∞—В—М —Б–≤–Њ—О –Љ–Є—И–µ–љ—М –љ–µ—Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ–є (–љ–∞–њ—А–Є–Љ–µ—А, –њ—А–µ–і–Њ—В–≤—А–∞—Й–∞—П —Б–≤—П–Ј—Л–≤–∞–љ–Є–µ —А–µ—Ж–µ–њ—В–Њ—А–∞), [1] –Є–љ–і—Г—Ж–Є—А–Њ–≤–∞—В—М —Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Є–є –Ї–ї–µ—В–Њ—З–љ—Л–є —Б–Є–≥–љ–∞–ї (–њ—Г—В–µ–Љ –∞–Ї—В–Є–≤–∞—Ж–Є–Є —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤), [1] –Ј–∞—Б—В–∞–≤–Є—В—М –Є–Љ–Љ—Г–љ–љ—Г—О —Б–Є—Б—В–µ–Љ—Г –∞—В–∞–Ї–Њ–≤–∞—В—М –Њ–њ—А–µ–і–µ–ї–µ–љ–љ—Л–µ –Ї–ї–µ—В–Ї–Є –Є–ї–Є –і–Њ—Б—В–∞–≤–Є—В—М –ї–µ–Ї–∞—А—Б—В–≤–Њ –Ї –Њ–њ—А–µ–і–µ–ї–µ–љ–љ–Њ–Љ—Г —В–Є–њ—Г –Ї–ї–µ—В–Њ–Ї (–љ–∞–њ—А–Є–Љ–µ—А, –њ—А–Є —А–∞–і–Є–Њ–Є–Љ–Љ—Г–љ–Њ—В–µ—А–∞–њ–Є–Є , –Ї–Њ—В–Њ—А–∞—П –і–Њ—Б—В–∞–≤–ї—П–µ—В —Ж–Є—В–Њ—В–Њ–Ї—Б–Є—З–µ—Б–Ї–Њ–µ –Є–Ј–ї—Г—З–µ–љ–Є–µ).
–Ю—Б–љ–Њ–≤–љ—Л–µ –Њ–±–ї–∞—Б—В–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –≤–Ї–ї—О—З–∞—О—В —А–∞–Ї , –∞—Г—В–Њ–Є–Љ–Љ—Г–љ–љ—Л–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П , –∞—Б—В–Љ—Г , —В—А–∞–љ—Б–њ–ї–∞–љ—В–∞—Ж–Є—О –Њ—А–≥–∞–љ–Њ–≤ , –њ—А–µ–і–Њ—В–≤—А–∞—Й–µ–љ–Є–µ –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П —В—А–Њ–Љ–±–Њ–≤ –Є –љ–µ–Ї–Њ—В–Њ—А—Л–µ –Є–љ—Д–µ–Ї—Ж–Є–Є.
–°—В—А—Г–Ї—В—Г—А–∞ –Є —Д—Г–љ–Ї—Ж–Є—П –∞–љ—В–Є—В–µ–ї
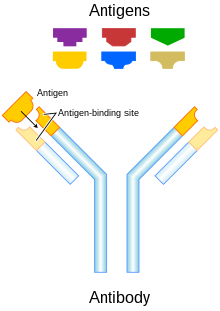
[ —А–µ–і–∞–Ї—В–Є—А–Њ–≤–∞—В—М ]–Р–љ—В–Є—В–µ–ї–∞ –Є–Љ–Љ—Г–љ–Њ–≥–ї–Њ–±—Г–ї–Є–љ–∞ G ( IgG ) –њ—А–µ–і—Б—В–∞–≤–ї—П—О—В —Б–Њ–±–Њ–є –±–Њ–ї—М—И–Є–µ –≥–µ—В–µ—А–Њ–і–Є–Љ–µ—А–љ—Л–µ –Љ–Њ–ї–µ–Ї—Г–ї—Л, –њ—А–Є–Љ–µ—А–љ–Њ 150 –Ї–Ф–∞ –Є —Б–Њ—Б—В–Њ—П—В –Є–Ј –і–≤—Г—Е —В–Є–њ–Њ–≤ –њ–Њ–ї–Є–њ–µ–њ—В–Є–і–љ—Л—Е —Ж–µ–њ–µ–є, –љ–∞–Ј—Л–≤–∞–µ–Љ—Л—Е —В—П–ґ–µ–ї–Њ–є (~ 50 –Ї–Ф–∞) –Є –ї–µ–≥–Ї–Њ–є —Ж–µ–њ—М—О (~ 25 –Ї–Ф–∞). –Ф–≤—Г–Љ—П —В–Є–њ–∞–Љ–Є –ї–µ–≥–Ї–Є—Е —Ж–µ–њ–µ–є —П–≤–ї—П—О—В—Б—П –Ї–∞–њ–њ–∞ (ќЇ) –Є –ї—П–Љ–±–і–∞ (ќї). –Я—Г—В–µ–Љ —А–∞—Б—Й–µ–њ–ї–µ–љ–Є—П —Д–µ—А–Љ–µ–љ—В–Њ–Љ –њ–∞–њ–∞–Є–љ–Њ–Љ —З–∞—Б—В—М Fab ) –Љ–Њ–ґ–µ—В –±—Л—В—М ( —Б–≤—П–Ј—Л–≤–∞—О—Й–Є–є —Д—А–∞–≥–Љ–µ–љ—В-–∞–љ—В–Є–≥–µ–љ –Њ—В–і–µ–ї–µ–љ–∞ –Њ—В —З–∞—Б—В–Є Fc ( –Ї—А–Є—Б—В–∞–ї–ї–Є–Ј—Г–µ–Љ–∞—П –Њ–±–ї–∞—Б—В—М —Д—А–∞–≥–Љ–µ–љ—В–∞ ) –Љ–Њ–ї–µ–Ї—Г–ї—Л. Fab-—Д—А–∞–≥–Љ–µ–љ—В—Л —Б–Њ–і–µ—А–ґ–∞—В –≤–∞—А–Є–∞–±–µ–ї—М–љ—Л–µ –і–Њ–Љ–µ–љ—Л, –Ї–Њ—В–Њ—А—Л–µ —Б–Њ—Б—В–Њ—П—В –Є–Ј —В—А–µ—Е –≥–Є–њ–µ—А–≤–∞—А–Є–∞–±–µ–ї—М–љ—Л—Е –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В–љ—Л—Е –і–Њ–Љ–µ–љ–Њ–≤ –∞–љ—В–Є—В–µ–ї–∞, –Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ—Л—Е –Ј–∞ —Б–њ–µ—Ж–Є—Д–Є—З–љ–Њ—Б—В—М –∞–љ—В–Є—В–µ–ї–∞, –≤—Б—В—А–Њ–µ–љ–љ—Л—Е –≤ –Ї–Њ–љ—Б—В–∞–љ—В–љ—Л–µ –Њ–±–ї–∞—Б—В–Є. –І–µ—В—Л—А–µ –Є–Ј–≤–µ—Б—В–љ—Л—Е –њ–Њ–і–Ї–ї–∞—Б—Б–∞ IgG —Г—З–∞—Б—В–≤—Г—О—В –≤ –∞–љ—В–Є—В–µ–ї–Њ–Ј–∞–≤–Є—Б–Є–Љ–Њ–є –Ї–ї–µ—В–Њ—З–љ–Њ–є —Ж–Є—В–Њ—В–Њ–Ї—Б–Є—З–љ–Њ—Б—В–Є . [2] –Р–љ—В–Є—В–µ–ї–∞ —П–≤–ї—П—О—В—Б—П –Ї–ї—О—З–µ–≤—Л–Љ –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–Њ–Љ –∞–і–∞–њ—В–Є–≤–љ–Њ–≥–Њ –Є–Љ–Љ—Г–љ–љ–Њ–≥–Њ –Њ—В–≤–µ—В–∞ , –Є–≥—А–∞—П —Ж–µ–љ—В—А–∞–ї—М–љ—Г—О —А–Њ–ї—М –Ї–∞–Ї –≤ —А–∞—Б–њ–Њ–Ј–љ–∞–≤–∞–љ–Є–Є —З—Г–ґ–µ—А–Њ–і–љ—Л—Е –∞–љ—В–Є–≥–µ–љ–Њ–≤, —В–∞–Ї –Є –≤ —Б—В–Є–Љ—Г–ї—П—Ж–Є–Є –Є–Љ–Љ—Г–љ–љ–Њ–≥–Њ –Њ—В–≤–µ—В–∞ –љ–∞ –љ–Є—Е. –Я–Њ—П–≤–ї–µ–љ–Є–µ —В–µ—Е–љ–Њ–ї–Њ–≥–Є–Є –Љ–Њ–љ–Њ–Ї–ї–Њ–љ–∞–ї—М–љ—Л—Е –∞–љ—В–Є—В–µ–ї –њ–Њ–Ј–≤–Њ–ї–Є–ї–Њ –њ–Њ–ї—Г—З–Є—В—М –∞–љ—В–Є—В–µ–ї–∞ –њ—А–Њ—В–Є–≤ —Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Є—Е –∞–љ—В–Є–≥–µ–љ–Њ–≤, –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–љ—Л—Е –љ–∞ –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є –Њ–њ—Г—Е–Њ–ї–µ–є. [3] –Ь–Њ–љ–Њ–Ї–ї–Њ–љ–∞–ї—М–љ—Л–µ –∞–љ—В–Є—В–µ–ї–∞ –Љ–Њ–≥—Г—В –њ—А–Є–Њ–±—А–µ—В–∞—В—М—Б—П –Є–Љ–Љ—Г–љ–љ–Њ–є —Б–Є—Б—В–µ–Љ–Њ–є –њ–Њ—Б—А–µ–і—Б—В–≤–Њ–Љ –њ–∞—Б—Б–Є–≤–љ–Њ–≥–Њ –Є–ї–Є –∞–Ї—В–Є–≤–љ–Њ–≥–Њ –Є–Љ–Љ—Г–љ–Є—В–µ—В–∞ . –Я—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–Њ –∞–Ї—В–Є–≤–љ–Њ–є —В–µ—А–∞–њ–Є–Є –Љ–Њ–љ–Њ–Ї–ї–Њ–љ–∞–ї—М–љ—Л–Љ–Є –∞–љ—В–Є—В–µ–ї–∞–Љ–Є –Ј–∞–Ї–ї—О—З–∞–µ—В—Б—П –≤ —В–Њ–Љ, —З—В–Њ –Є–Љ–Љ—Г–љ–љ–∞—П —Б–Є—Б—В–µ–Љ–∞ –±—Г–і–µ—В –≤—Л—А–∞–±–∞—В—Л–≤–∞—В—М –∞–љ—В–Є—В–µ–ї–∞ –≤ —В–µ—З–µ–љ–Є–µ –і–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –≤—А–µ–Љ–µ–љ–Є, –Є —В–Њ–ї—М–Ї–Њ –Ї—А–∞—В–Ї–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–µ –≤–≤–µ–і–µ–љ–Є–µ –ї–µ–Ї–∞—А—Б—В–≤–∞ –Љ–Њ–ґ–µ—В –≤—Л–Ј–≤–∞—В—М —Н—В–Њ—В –Њ—В–≤–µ—В. –Ю–і–љ–∞–Ї–Њ –Є–Љ–Љ—Г–љ–љ—Л–є –Њ—В–≤–µ—В –љ–∞ –Њ–њ—А–µ–і–µ–ї–µ–љ–љ—Л–µ –∞–љ—В–Є–≥–µ–љ—Л –Љ–Њ–ґ–µ—В –±—Л—В—М –љ–µ–∞–і–µ–Ї–≤–∞—В–љ—Л–Љ, –Њ—Б–Њ–±–µ–љ–љ–Њ —Г –њ–Њ–ґ–Є–ї—Л—Е –ї—О–і–µ–є. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –Є–Ј-–Ј–∞ –і–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –Њ—В–≤–µ—В–∞ –љ–∞ –∞–љ—В–Є–≥–µ–љ—Л –Љ–Њ–≥—Г—В –≤–Њ–Ј–љ–Є–Ї–љ—Г—В—М –њ–Њ–±–Њ—З–љ—Л–µ —А–µ–∞–Ї—Ж–Є–Є —Б–Њ —Б—В–Њ—А–Њ–љ—Л —Н—В–Є—Е –∞–љ—В–Є—В–µ–ї. [4] –Ґ–µ—А–∞–њ–Є—П –њ–∞—Б—Б–Є–≤–љ—Л–Љ–Є –Љ–Њ–љ–Њ–Ї–ї–Њ–љ–∞–ї—М–љ—Л–Љ–Є –∞–љ—В–Є—В–µ–ї–∞–Љ–Є –Љ–Њ–ґ–µ—В –Њ–±–µ—Б–њ–µ—З–Є—В—М –њ–Њ—Б—В–Њ—П–љ–љ—Г—О –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—О –∞–љ—В–Є—В–µ–ї –Є –Ї–Њ–љ—В—А–Њ–ї–Є—А–Њ–≤–∞—В—М –њ–Њ–±–Њ—З–љ—Л–µ —А–µ–∞–Ї—Ж–Є–Є –њ—Г—В–µ–Љ –њ—А–µ–Ї—А–∞—Й–µ–љ–Є—П –≤–≤–µ–і–µ–љ–Є—П. –Ю–і–љ–∞–Ї–Њ –њ–Њ–≤—В–Њ—А–љ–Њ–µ –≤–≤–µ–і–µ–љ–Є–µ –Є, –Ї–∞–Ї —Б–ї–µ–і—Б—В–≤–Є–µ, –±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї–∞—П —Б—В–Њ–Є–Љ–Њ—Б—В—М —Н—В–Њ–є —В–µ—А–∞–њ–Є–Є —П–≤–ї—П—О—В—Б—П –Њ—Б–љ–Њ–≤–љ—Л–Љ–Є –љ–µ–і–Њ—Б—В–∞—В–Ї–∞–Љ–Є. [4]
–Ґ–µ—А–∞–њ–Є—П –Љ–Њ–љ–Њ–Ї–ї–Њ–љ–∞–ї—М–љ—Л–Љ–Є –∞–љ—В–Є—В–µ–ї–∞–Љ–Є –Љ–Њ–ґ–µ—В –Њ–Ї–∞–Ј–∞—В—М—Б—П –њ–Њ–ї–µ–Ј–љ–Њ–є –њ—А–Є —А–∞–Ї–µ , –∞—Г—В–Њ–Є–Љ–Љ—Г–љ–љ—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П—Е –Є –љ–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞—Е, –Ї–Њ—В–Њ—А—Л–µ –њ—А–Є–≤–Њ–і—П—В –Ї –і–µ–≥–µ–љ–µ—А–∞—Ж–Є–Є –Ї–ї–µ—В–Њ–Ї –Њ—А–≥–∞–љ–Є–Ј–Љ–∞, —В–∞–Ї–Є—Е –Ї–∞–Ї –±–Њ–ї–µ–Ј–љ—М –Р–ї—М—Ж–≥–µ–є–Љ–µ—А–∞ . –Ґ–µ—А–∞–њ–Є—П –Љ–Њ–љ–Њ–Ї–ї–Њ–љ–∞–ї—М–љ—Л–Љ–Є –∞–љ—В–Є—В–µ–ї–∞–Љ–Є –Љ–Њ–ґ–µ—В –њ–Њ–Љ–Њ—З—М –Є–Љ–Љ—Г–љ–љ–Њ–є —Б–Є—Б—В–µ–Љ–µ, –њ–Њ—Б–Ї–Њ–ї—М–Ї—Г –≤—А–Њ–ґ–і–µ–љ–љ–∞—П –Є–Љ–Љ—Г–љ–љ–∞—П —Б–Є—Б—В–µ–Љ–∞ —А–µ–∞–≥–Є—А—Г–µ—В –љ–∞ —Д–∞–Ї—В–Њ—А—Л –Њ–Ї—А—Г–ґ–∞—О—Й–µ–є —Б—А–µ–і—Л, —Б –Ї–Њ—В–Њ—А—Л–Љ–Є –Њ–љ–∞ —Б—В–∞–ї–Ї–Є–≤–∞–µ—В—Б—П, –Њ—В–ї–Є—З–∞—П —З—Г–ґ–µ—А–Њ–і–љ—Л–µ –Ї–ї–µ—В–Ї–Є –Њ—В –Ї–ї–µ—В–Њ–Ї –Њ—А–≥–∞–љ–Є–Ј–Љ–∞. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –Њ–њ—Г—Е–Њ–ї–µ–≤—Л–µ –Ї–ї–µ—В–Ї–Є , –Ї–Њ—В–Њ—А—Л–µ –њ—А–Њ–ї–Є—Д–µ—А–Є—А—Г—О—В —Б –≤—Л—Б–Њ–Ї–Њ–є —Б–Ї–Њ—А–Њ—Б—В—М—О, –Є–ї–Є –Ї–ї–µ—В–Ї–Є –Њ—А–≥–∞–љ–Є–Ј–Љ–∞, –Ї–Њ—В–Њ—А—Л–µ —Г–Љ–Є—А–∞—О—В, —З—В–Њ –≤–њ–Њ—Б–ї–µ–і—Б—В–≤–Є–Є –≤—Л–Ј—Л–≤–∞–µ—В —Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ –њ—А–Њ–±–ї–µ–Љ—Л, –Ї–∞–Ї –њ—А–∞–≤–Є–ї–Њ, –љ–µ —П–≤–ї—П—О—В—Б—П —Ж–µ–ї–µ–≤–Њ–є –Љ–Є—И–µ–љ—М—О –Є–Љ–Љ—Г–љ–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л, –њ–Њ—Б–Ї–Њ–ї—М–Ї—Г –Њ–њ—Г—Е–Њ–ї–µ–≤—Л–µ –Ї–ї–µ—В–Ї–Є —П–≤–ї—П—О—В—Б—П —Б–Њ–±—Б—В–≤–µ–љ–љ—Л–Љ–Є –Ї–ї–µ—В–Ї–∞–Љ–Є –њ–∞—Ж–Є–µ–љ—В–∞. –Ю–і–љ–∞–Ї–Њ –Њ–њ—Г—Е–Њ–ї–µ–≤—Л–µ –Ї–ї–µ—В–Ї–Є —П–≤–ї—П—О—В—Б—П –≤ –≤—Л—Б—И–µ–є —Б—В–µ–њ–µ–љ–Є –∞–љ–Њ–Љ–∞–ї—М–љ—Л–Љ–Є, –Є –Љ–љ–Њ–≥–Є–µ –Є–Ј –љ–Є—Е —Б–Њ–і–µ—А–ґ–∞—В –љ–µ–Њ–±—Л—З–љ—Л–µ –∞–љ—В–Є–≥–µ–љ—Л . –Э–µ–Ї–Њ—В–Њ—А—Л–µ —В–∞–Ї–Є–µ –Њ–њ—Г—Е–Њ–ї–µ–≤—Л–µ –∞–љ—В–Є–≥–µ–љ—Л –љ–µ –њ–Њ–і—Е–Њ–і—П—В –і–ї—П –і–∞–љ–љ–Њ–≥–Њ —В–Є–њ–∞ –Ї–ї–µ—В–Њ–Ї –Є–ї–Є –Є—Е –Њ–Ї—А—Г–ґ–µ–љ–Є—П. –Ь–Њ–љ–Њ–Ї–ї–Њ–љ–∞–ї—М–љ—Л–µ –∞–љ—В–Є—В–µ–ї–∞ –Љ–Њ–≥—Г—В –љ–∞—Ж–µ–ї–Є–≤–∞—В—М—Б—П –љ–∞ –Њ–њ—Г—Е–Њ–ї–µ–≤—Л–µ –Ї–ї–µ—В–Ї–Є –Є–ї–Є –∞–љ–Њ–Љ–∞–ї—М–љ—Л–µ –Ї–ї–µ—В–Ї–Є –Њ—А–≥–∞–љ–Є–Ј–Љ–∞, –Ї–Њ—В–Њ—А—Л–µ —А–∞—Б–њ–Њ–Ј–љ–∞—О—В—Б—П –Ї–∞–Ї –Ї–ї–µ—В–Ї–Є –Њ—А–≥–∞–љ–Є–Ј–Љ–∞, –љ–Њ –љ–∞–љ–Њ—Б—П—В –≤—А–µ–і –Ј–і–Њ—А–Њ–≤—М—О. [ –љ—Г–ґ–љ–∞ —Б—Б—Л–ї–Ї–∞ ]
–Ш—Б—В–Њ—А–Є—П
[ —А–µ–і–∞–Ї—В–Є—А–Њ–≤–∞—В—М ]
–Ш–Љ–Љ—Г–љ–Њ—В–µ—А–∞–њ–Є—П –њ–Њ–ї—Г—З–Є–ї–∞ —А–∞–Ј–≤–Є—В–Є–µ –≤ 1970-—Е –≥–Њ–і–∞—Е –њ–Њ—Б–ї–µ –Њ—В–Ї—А—Л—В–Є—П —Б—В—А—Г–Ї—В—Г—А—Л –∞–љ—В–Є—В–µ–ї –Є —А–∞–Ј—А–∞–±–Њ—В–Ї–Є –≥–Є–±—А–Є–і–Њ–Љ–љ–Њ–є —В–µ—Е–љ–Њ–ї–Њ–≥–Є–Є, –Ї–Њ—В–Њ—А–∞—П –Њ–±–µ—Б–њ–µ—З–Є–ї–∞ –њ–µ—А–≤—Л–є –љ–∞–і–µ–ґ–љ—Л–є –Є—Б—В–Њ—З–љ–Є–Ї –Љ–Њ–љ–Њ–Ї–ї–Њ–љ–∞–ї—М–љ—Л—Е –∞–љ—В–Є—В–µ–ї . [6] [7] –≠—В–Є –і–Њ—Б—В–Є–ґ–µ–љ–Є—П –њ–Њ–Ј–≤–Њ–ї–Є–ї–Є —Ж–µ–ї–µ–љ–∞–њ—А–∞–≤–ї–µ–љ–љ–Њ –≤–Њ–Ј–і–µ–є—Б—В–≤–Њ–≤–∞—В—М –љ–∞ –Њ–њ—Г—Е–Њ–ї–Є –Ї–∞–Ї in vitro , —В–∞–Ї –Є in vivo . –Я–µ—А–≤–Њ–љ–∞—З–∞–ї—М–љ—Л–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Ј–ї–Њ–Ї–∞—З–µ—Б—В–≤–µ–љ–љ—Л—Е –љ–Њ–≤–Њ–Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–є –њ–Њ–Ї–∞–Ј–∞–ї–Є, —З—В–Њ —В–µ—А–∞–њ–Є—П –Љ–Њ–љ–Њ–Ї–ї–Њ–љ–∞–ї—М–љ—Л–Љ–Є –∞–љ—В–Є—В–µ–ї–∞–Љ–Є –Є–Љ–µ–µ—В –Њ–≥—А–∞–љ–Є—З–µ–љ–љ—Л–є –Є, –Ї–∞–Ї –њ—А–∞–≤–Є–ї–Њ, –Ї—А–∞—В–Ї–Њ–≤—А–µ–Љ–µ–љ–љ—Л–є —Г—Б–њ–µ—Е –њ—А–Є –Ј–ї–Њ–Ї–∞—З–µ—Б—В–≤–µ–љ–љ—Л—Е –љ–Њ–≤–Њ–Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П—Е –Ї—А–Њ–≤–Є. [8] [9] –Ы–µ—З–µ–љ–Є–µ —В–∞–Ї–ґ–µ –і–Њ–ї–ґ–љ–Њ –±—Л–ї–Њ –±—Л—В—М –∞–і–∞–њ—В–Є—А–Њ–≤–∞–љ–Њ –Ї –Ї–∞–ґ–і–Њ–Љ—Г –Њ—В–і–µ–ї—М–љ–Њ–Љ—Г –њ–∞—Ж–Є–µ–љ—В—Г, —З—В–Њ –±—Л–ї–Њ –љ–µ–≤–Њ–Ј–Љ–Њ–ґ–љ–Њ –≤ –Њ–±—Л—З–љ—Л—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е —Г—Б–ї–Њ–≤–Є—П—Е. [ –љ—Г–ґ–љ–∞ —Б—Б—Л–ї–Ї–∞ ]
–†–∞–Ј—А–∞–±–Њ—В–∞–љ—Л —З–µ—В—Л—А–µ –Њ—Б–љ–Њ–≤–љ—Л—Е —В–Є–њ–∞ –∞–љ—В–Є—В–µ–ї: –Љ—Л—И–Є–љ—Л–µ , —Е–Є–Љ–µ—А–љ—Л–µ , –≥—Г–Љ–∞–љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л–µ –Є —З–µ–ї–Њ–≤–µ—З–µ—Б–Ї–Є–µ. –Р–љ—В–Є—В–µ–ї–∞ –Ї–∞–ґ–і–Њ–≥–Њ —В–Є–њ–∞ —А–∞–Ј–ї–Є—З–∞—О—В—Б—П —Б—Г—Д—Д–Є–Ї—Б–∞–Љ–Є –≤ –љ–∞–Ј–≤–∞–љ–Є–Є. [ –љ—Г–ґ–љ–∞ —Б—Б—Л–ї–Ї–∞ ]
–Ь—Л—И–Є–љ—Л–є
[ —А–µ–і–∞–Ї—В–Є—А–Њ–≤–∞—В—М ]–Ш—Б—Е–Њ–і–љ—Л–Љ–Є —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є–Љ–Є –∞–љ—В–Є—В–µ–ї–∞–Љ–Є –±—Л–ї–Є –Љ—Л—И–Є–љ—Л–µ –∞–љ–∞–ї–Њ–≥–Є (—Б—Г—Д—Д–Є–Ї—Б -–Њ–Љ–∞–± ). –≠—В–Є –∞–љ—В–Є—В–µ–ї–∞ –Є–Љ–µ—О—В: –Ї–Њ—А–Њ—В–Ї–Є–є –њ–µ—А–Є–Њ–і –њ–Њ–ї—Г—А–∞—Б–њ–∞–і–∞ in vivo (–Є–Ј-–Ј–∞ –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П –Є–Љ–Љ—Г–љ–љ—Л—Е –Ї–Њ–Љ–њ–ї–µ–Ї—Б–Њ–≤ ), –Њ–≥—А–∞–љ–Є—З–µ–љ–љ–Њ–µ –њ—А–Њ–љ–Є–Ї–љ–Њ–≤–µ–љ–Є–µ –≤ —Г—З–∞—Б—В–Ї–Є –Њ–њ—Г—Е–Њ–ї–Є –Є –љ–µ–∞–і–µ–Ї–≤–∞—В–љ–Њ–µ —А–µ–Ї—А—Г—В–Є—А–Њ–≤–∞–љ–Є–µ —Н—Д—Д–µ–Ї—В–Њ—А–љ—Л—Е —Д—Г–љ–Ї—Ж–Є–є —Е–Њ–Ј—П–Є–љ–∞. [10] –•–Є–Љ–µ—А–љ—Л–µ –Є –≥—Г–Љ–∞–љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л–µ –∞–љ—В–Є—В–µ–ї–∞ –Њ–±—Л—З–љ–Њ –Ј–∞–Љ–µ–љ—П—О—В –Є—Е –≤ —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є—Е —Ж–µ–ї—П—Е. [11] –Я–Њ–љ–Є–Љ–∞–љ–Є–µ –њ—А–Њ—В–µ–Њ–Љ–Є–Ї–Є –Њ–Ї–∞–Ј–∞–ї–Њ—Б—М –≤–∞–ґ–љ—Л–Љ –і–ї—П –≤—Л—П–≤–ї–µ–љ–Є—П –љ–Њ–≤—Л—Е –Љ–Є—И–µ–љ–µ–є –Њ–њ—Г—Е–Њ–ї–µ–є. [ –љ—Г–ґ–љ–∞ —Б—Б—Л–ї–Ї–∞ ]
–Я–µ—А–≤–Њ–љ–∞—З–∞–ї—М–љ–Њ –Љ—Л—И–Є–љ—Л–µ –∞–љ—В–Є—В–µ–ї–∞ –±—Л–ї–Є –њ–Њ–ї—Г—З–µ–љ—Л –≥–Є–±—А–Є–і–Њ–Љ–љ–Њ–є —В–µ—Е–љ–Њ–ї–Њ–≥–Є–µ–є, –Ј–∞ —З—В–Њ –Щ–µ—А–љ–µ, –Ъ—С–ї–µ—А –Є –Ь–Є–ї—М—И—В–µ–є–љ –њ–Њ–ї—Г—З–Є–ї–Є –Э–Њ–±–µ–ї–µ–≤—Б–Ї—Г—О –њ—А–µ–Љ–Є—О. –Ю–і–љ–∞–Ї–Њ –љ–µ—Б—Е–Њ–і—Б—В–≤–Њ –Љ–µ–ґ–і—Г –Є–Љ–Љ—Г–љ–љ–Њ–є —Б–Є—Б—В–µ–Љ–Њ–є –Љ—Л—И–Є –Є —З–µ–ї–Њ–≤–µ–Ї–∞ –њ—А–Є–≤–µ–ї–Њ –Ї –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –љ–µ—Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є —Н—В–Є—Е –∞–љ—В–Є—В–µ–ї, –Ј–∞ –Є—Б–Ї–ї—О—З–µ–љ–Є–µ–Љ –љ–µ–Ї–Њ—В–Њ—А—Л—Е –Ї–Њ–љ–Ї—А–µ—В–љ—Л—Е –Њ–±—Б—В–Њ—П—В–µ–ї—М—Б—В–≤. –Ю—Б–љ–Њ–≤–љ—Л–µ –њ—А–Њ–±–ї–µ–Љ—Л, —Б–≤—П–Ј–∞–љ–љ—Л–µ —Б –Љ—Л—И–Є–љ—Л–Љ–Є –∞–љ—В–Є—В–µ–ї–∞–Љ–Є, –≤–Ї–ї—О—З–∞–ї–Є —Б–љ–Є–ґ–µ–љ–Є–µ —Б—В–Є–Љ—Г–ї—П—Ж–Є–Є —Ж–Є—В–Њ—В–Њ–Ї—Б–Є—З–љ–Њ—Б—В–Є –Є –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–Њ–≤ –њ–Њ—Б–ї–µ –њ–Њ–≤—В–Њ—А–љ–Њ–≥–Њ –≤–≤–µ–і–µ–љ–Є—П, —З—В–Њ –њ—А–Є–≤–Њ–і–Є–ї–Њ –Ї –ї–µ–≥–Ї–Є–Љ –∞–ї–ї–µ—А–≥–Є—З–µ—Б–Ї–Є–Љ —А–µ–∞–Ї—Ж–Є—П–Љ , –∞ –Є–љ–Њ–≥–і–∞ –Є –Ї –∞–љ–∞—Д–Є–ї–∞–Ї—В–Є—З–µ—Б–Ї–Њ–Љ—Г —И–Њ–Ї—Г . [10] –Ґ–µ—Е–љ–Њ–ї–Њ–≥–Є—П –≥–Є–±—А–Є–і–Њ–Љ –±—Л–ї–∞ –Ј–∞–Љ–µ–љ–µ–љ–∞ —В–µ—Е–љ–Њ–ї–Њ–≥–Є–µ–є —А–µ–Ї–Њ–Љ–±–Є–љ–∞–љ—В–љ–Њ–є –Ф–Э–Ъ , —В—А–∞–љ—Б–≥–µ–љ–љ—Л–Љ–Є –Љ—Л—И–∞–Љ–Є –Є —Д–∞–≥–Њ–≤—Л–Љ –і–Є—Б–њ–ї–µ–µ–Љ . [11]
–•–Є–Љ–µ—А–љ—Л–є –Є –≥—Г–Љ–∞–љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л–є
[ —А–µ–і–∞–Ї—В–Є—А–Њ–≤–∞—В—М ]–І—В–Њ–±—Л —Б–љ–Є–Ј–Є—В—М –Є–Љ–Љ—Г–љ–Њ–≥–µ–љ–љ–Њ—Б—В—М –Љ—Л—И–Є–љ—Л—Е –∞–љ—В–Є—В–µ–ї (–∞—В–∞–Ї–Є –Є–Љ–Љ—Г–љ–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л –љ–∞ –∞–љ—В–Є—В–µ–ї–∞), –Љ—Л—И–Є–љ—Л–µ –Љ–Њ–ї–µ–Ї—Г–ї—Л –±—Л–ї–Є —Б–Њ–Ј–і–∞–љ—Л –і–ї—П —Г–і–∞–ї–µ–љ–Є—П –Є–Љ–Љ—Г–љ–Њ–≥–µ–љ–љ–Њ–≥–Њ —Б–Њ–і–µ—А–ґ–Є–Љ–Њ–≥–Њ –Є –њ–Њ–≤—Л—И–µ–љ–Є—П –Є–Љ–Љ—Г–љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є. [10] –Я–µ—А–≤–Њ–љ–∞—З–∞–ї—М–љ–Њ —Н—В–Њ –±—Л–ї–Њ –і–Њ—Б—В–Є–≥–љ—Г—В–Њ –њ—Г—В–µ–Љ –њ—А–Њ–Є–Ј–≤–Њ–і—Б—В–≤–∞ —Е–Є–Љ–µ—А–љ—Л—Е (—Б—Г—Д—Д–Є–Ї—Б -–Ї—Б–Є–Љ–∞–±) –Є –≥—Г–Љ–∞–љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е –∞–љ—В–Є—В–µ–ї (—Б—Г—Д—Д–Є–Ї—Б -–Ј—Г–Љ–∞–± ). –•–Є–Љ–µ—А–љ—Л–µ –∞–љ—В–Є—В–µ–ї–∞ —Б–Њ—Б—В–Њ—П—В –Є–Ј –Љ—Л—И–Є–љ—Л—Е –≤–∞—А–Є–∞–±–µ–ї—М–љ—Л—Е –Њ–±–ї–∞—Б—В–µ–є, —Б–ї–Є—В—Л—Е —Б –Ї–Њ–љ—Б—В–∞–љ—В–љ—Л–Љ–Є –Њ–±–ї–∞—Б—В—П–Љ–Є —З–µ–ї–Њ–≤–µ–Ї–∞. –Т–Ј—П—В–Є–µ –њ–Њ—Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ—Б—В–µ–є –≥–µ–љ–Њ–≤ —З–µ–ї–Њ–≤–µ–Ї–∞ –Є–Ј –ї–µ–≥–Ї–Њ–є –Ї–∞–њ–њ–∞-—Ж–µ–њ–Є –Є —В—П–ґ–µ–ї–Њ–є —Ж–µ–њ–Є IgG1 –њ—А–Є–≤–Њ–і–Є—В –Ї –њ–Њ–ї—Г—З–µ–љ–Є—О –∞–љ—В–Є—В–µ–ї, –Ї–Њ—В–Њ—А—Л–µ –њ—А–Є–Љ–µ—А–љ–Њ –љ–∞ 65% —Б–Њ—Б—В–Њ—П—В –Є–Ј —З–µ–ї–Њ–≤–µ–Ї–∞. –≠—В–Њ —Б–љ–Є–ґ–∞–µ—В –Є–Љ–Љ—Г–љ–Њ–≥–µ–љ–љ–Њ—Б—В—М –Є, —В–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В –Є–Ј —Б—Л–≤–Њ—А–Њ—В–Ї–Є –њ–µ—А–Є–Њ–і –њ–Њ–ї—Г–≤—Л–≤–µ–і–µ–љ–Є—П . [ –љ—Г–ґ–љ–∞ —Б—Б—Л–ї–Ї–∞ ]
–У—Г–Љ–∞–љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л–µ –∞–љ—В–Є—В–µ–ї–∞ –њ–Њ–ї—Г—З–∞—О—В –њ—Г—В–µ–Љ –њ—А–Є–≤–Є–≤–Ї–Є –Љ—Л—И–Є–љ—Л—Е –≥–Є–њ–µ—А–≤–∞—А–Є–∞–±–µ–ї—М–љ—Л—Е –Њ–±–ї–∞—Б—В–µ–є –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В–љ—Л—Е –і–Њ–Љ–µ–љ–Њ–≤ –≤ —З–µ–ї–Њ–≤–µ—З–µ—Б–Ї–Є–µ –∞–љ—В–Є—В–µ–ї–∞. –Т —А–µ–Ј—Г–ї—М—В–∞—В–µ –њ–Њ–ї—Г—З–∞–µ—В—Б—П –Љ–Њ–ї–µ–Ї—Г–ї–∞ –њ—А–Є–Љ–µ—А–љ–Њ –љ–∞ 95% —З–µ–ї–Њ–≤–µ—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Њ–Є—Б—Е–Њ–ґ–і–µ–љ–Є—П. –У—Г–Љ–∞–љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л–µ –∞–љ—В–Є—В–µ–ї–∞ —Б–≤—П–Ј—Л–≤–∞—О—В –∞–љ—В–Є–≥–µ–љ –≥–Њ—А–∞–Ј–і–Њ —Б–ї–∞–±–µ–µ, —З–µ–Љ –Є—Б—Е–Њ–і–љ—Л–µ –Љ—Л—И–Є–љ—Л–µ –Љ–Њ–љ–Њ–Ї–ї–Њ–љ–∞–ї—М–љ—Л–µ –∞–љ—В–Є—В–µ–ї–∞, –њ—А–Є —Н—В–Њ–Љ —Б–Њ–Њ–±—Й–∞–µ—В—Б—П –Њ —Б–љ–Є–ґ–µ–љ–Є–Є –∞—Д—Д–Є–љ–љ–Њ—Б—В–Є –≤ –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ —Б–Њ—В–µ–љ —А–∞–Ј. [12] [13] –£–≤–µ–ї–Є—З–µ–љ–Є–µ —Б–Є–ї—Л —Б–≤—П–Ј—Л–≤–∞–љ–Є—П –∞–љ—В–Є—В–µ–ї–Њ-–∞–љ—В–Є–≥–µ–љ –±—Л–ї–Њ –і–Њ—Б—В–Є–≥–љ—Г—В–Њ –Ј–∞ —Б—З–µ—В –≤–≤–µ–і–µ–љ–Є—П –Љ—Г—В–∞—Ж–Є–є –≤ –Њ–±–ї–∞—Б—В–Є, –Њ–њ—А–µ–і–µ–ї—П—О—Й–Є–µ –Ї–Њ–Љ–њ–ї–µ–Љ–µ–љ—В–∞—А–љ–Њ—Б—В—М (CDR). [14] —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ —В–∞–Ї–Є—Е –Љ–µ—В–Њ–і–Њ–≤, –Ї–∞–Ї –њ–µ—А–µ—В–∞—Б–Њ–≤–Ї–∞ —Ж–µ–њ–µ–є, —А–∞–љ–і–Њ–Љ–Є–Ј–∞—Ж–Є—П –Њ–±–ї–∞—Б—В–µ–є, –Њ–њ—А–µ–і–µ–ї—П—О—Й–Є—Е –Ї–Њ–Љ–њ–ї–µ–Љ–µ–љ—В–∞—А–љ–Њ—Б—В—М, –Є –∞–љ—В–Є—В–µ–ї —Б –Љ—Г—В–∞—Ж–Є—П–Љ–Є –≤ –≤–∞—А–Є–∞–±–µ–ї—М–љ—Л—Е –Њ–±–ї–∞—Б—В—П—Е, –Є–љ–і—Г—Ж–Є—А–Њ–≤–∞–љ–љ—Л—Е –њ–Њ–і–≤–µ—А–ґ–µ–љ–љ–Њ–є –Њ—И–Є–±–Ї–∞–Љ –Я–¶–† , —И—В–∞–Љ–Љ–∞–Љ–Є-–Љ—Г—В–∞—В–Њ—А–∞–Љ–Є E. coli –Є —Б–∞–є—В-—Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Є–Љ –Љ—Г—В–∞–≥–µ–љ–µ–Ј–Њ–Љ . [15]
–І–µ–ї–Њ–≤–µ—З–µ—Б–Ї–Є–µ –Љ–Њ–љ–Њ–Ї–ї–Њ–љ–∞–ї—М–љ—Л–µ –∞–љ—В–Є—В–µ–ї–∞
[ —А–µ–і–∞–Ї—В–Є—А–Њ–≤–∞—В—М ]–І–µ–ї–Њ–≤–µ—З–µ—Б–Ї–Є–µ –Љ–Њ–љ–Њ–Ї–ї–Њ–љ–∞–ї—М–љ—Л–µ –∞–љ—В–Є—В–µ–ї–∞ (—Б—Г—Д—Д–Є–Ї—Б -—Г–Љ–∞–± ) –њ—А–Њ–Є–Ј–≤–Њ–і—П—В—Б—П —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ —В—А–∞–љ—Б–≥–µ–љ–љ—Л—Е –Љ—Л—И–µ–є –Є–ї–Є —Д–∞–≥–Њ–≤–Њ–≥–Њ –і–Є—Б–њ–ї–µ—П –±–Є–±–ї–Є–Њ—В–µ–Ї –њ—Г—В–µ–Љ –њ–µ—А–µ–љ–Њ—Б–∞ –≥–µ–љ–Њ–≤ –Є–Љ–Љ—Г–љ–Њ–≥–ї–Њ–±—Г–ї–Є–љ–Њ–≤ —З–µ–ї–Њ–≤–µ–Ї–∞ –≤ –≥–µ–љ–Њ–Љ –Љ—Л—И–Є –Є –≤–∞–Ї—Ж–Є–љ–∞—Ж–Є–Є —В—А–∞–љ—Б–≥–µ–љ–љ–Њ–є –Љ—Л—И–Є –њ—А–Њ—В–Є–≤ –ґ–µ–ї–∞–µ–Љ–Њ–≥–Њ –∞–љ—В–Є–≥–µ–љ–∞, —З—В–Њ –њ—А–Є–≤–Њ–і–Є—В –Ї –њ—А–Њ–Є–Ј–≤–Њ–і—Б—В–≤—Г —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г—О—Й–Є—Е –Љ–Њ–љ–Њ–Ї–ї–Њ–љ–∞–ї—М–љ—Л—Е –∞–љ—В–Є—В–µ–ї. [11] –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –Љ—Л—И–Є–љ—Л–µ –∞–љ—В–Є—В–µ–ї–∞ in vitro —В—А–∞–љ—Б—Д–Њ—А–Љ–Є—А—Г—О—В—Б—П –≤ –њ–Њ–ї–љ–Њ—Б—В—М—О —З–µ–ї–Њ–≤–µ—З–µ—Б–Ї–Є–µ –∞–љ—В–Є—В–µ–ї–∞. [3]
–Ґ—П–ґ–µ–ї—Л–µ –Є –ї–µ–≥–Ї–Є–µ —Ж–µ–њ–Є –±–µ–ї–Ї–Њ–≤ IgG —З–µ–ї–Њ–≤–µ–Ї–∞ —Н–Ї—Б–њ—А–µ—Б—Б–Є—А—Г—О—В—Б—П –≤ —Б—В—А—Г–Ї—В—Г—А–љ—Л—Е –њ–Њ–ї–Є–Љ–Њ—А—Д–љ—Л—Е (–∞–ї–ї–Њ—В–Є–њ–Є—З–µ—Б–Ї–Є—Е) —Д–Њ—А–Љ–∞—Е. IgG —З–µ–ї–Њ–≤–µ–Ї–∞ –Р–ї–ї–Њ—В–Є–њ —П–≤–ї—П–µ—В—Б—П –Њ–і–љ–Є–Љ –Є–Ј –Љ–љ–Њ–≥–Є—Е —Д–∞–Ї—В–Њ—А–Њ–≤, –Ї–Њ—В–Њ—А—Л–µ –Љ–Њ–≥—Г—В —Б–њ–Њ—Б–Њ–±—Б—В–≤–Њ–≤–∞—В—М –Є–Љ–Љ—Г–љ–Њ–≥–µ–љ–љ–Њ—Б—В–Є. [16] [17]
–¶–µ–ї–µ–≤—Л–µ —Г—Б–ї–Њ–≤–Є—П
[ —А–µ–і–∞–Ї—В–Є—А–Њ–≤–∞—В—М ]–†–∞–Ї
[ —А–µ–і–∞–Ї—В–Є—А–Њ–≤–∞—В—М ]–Я—А–Њ—В–Є–≤–Њ—А–∞–Ї–Њ–≤—Л–µ –Љ–Њ–љ–Њ–Ї–ї–Њ–љ–∞–ї—М–љ—Л–µ –∞–љ—В–Є—В–µ–ї–∞ –Љ–Њ–≥—Г—В –±—Л—В—М –љ–∞–њ—А–∞–≤–ї–µ–љ—Л –њ—А–Њ—В–Є–≤ –Ј–ї–Њ–Ї–∞—З–µ—Б—В–≤–µ–љ–љ—Л—Е –Ї–ї–µ—В–Њ–Ї —Б –њ–Њ–Љ–Њ—Й—М—О –љ–µ—Б–Ї–Њ–ї—М–Ї–Є—Е –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–≤. –†–∞–Љ—Г—Ж–Є—А—Г–Љ–∞–± –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В —Б–Њ–±–Њ–є —А–µ–Ї–Њ–Љ–±–Є–љ–∞–љ—В–љ–Њ–µ —З–µ–ї–Њ–≤–µ—З–µ—Б–Ї–Њ–µ –Љ–Њ–љ–Њ–Ї–ї–Њ–љ–∞–ї—М–љ–Њ–µ –∞–љ—В–Є—В–µ–ї–Њ –Є –Є—Б–њ–Њ–ї—М–Ј—Г–µ—В—Б—П –і–ї—П –ї–µ—З–µ–љ–Є—П –Ј–∞–њ—Г—Й–µ–љ–љ—Л—Е –Ј–ї–Њ–Ї–∞—З–µ—Б—В–≤–µ–љ–љ—Л—Е –Њ–њ—Г—Е–Њ–ї–µ–є. [18] –Я—А–Є –ї–Є–Љ—Д–Њ–Љ–µ —Г –і–µ—В–µ–є –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —Д–∞–Ј—Л I –Є II –Њ–±–љ–∞—А—Г–ґ–Є–ї–Є –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л–є —Н—Д—Д–µ–Ї—В –Њ—В –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П —В–µ—А–∞–њ–Є–Є –∞–љ—В–Є—В–µ–ї–∞–Љ–Є. [19]
–Ь–Њ–љ–Њ–Ї–ї–Њ–љ–∞–ї—М–љ—Л–µ –∞–љ—В–Є—В–µ–ї–∞, –Є—Б–њ–Њ–ї—М–Ј—Г–µ–Љ—Л–µ –і–ї—П —Г—Б–Є–ї–µ–љ–Є—П –њ—А–Њ—В–Є–≤–Њ—А–∞–Ї–Њ–≤–Њ–≥–Њ –Є–Љ–Љ—Г–љ–љ–Њ–≥–Њ –Њ—В–≤–µ—В–∞, —П–≤–ї—П—О—В—Б—П –µ—Й–µ –Њ–і–љ–Њ–є —Б—В—А–∞—В–µ–≥–Є–µ–є –±–Њ—А—М–±—Л —Б —А–∞–Ї–Њ–Љ, –Ї–Њ–≥–і–∞ —А–∞–Ї–Њ–≤—Л–µ –Ї–ї–µ—В–Ї–Є –љ–µ –≤–Њ–Ј–і–µ–є—Б—В–≤—Г—О—В –љ–∞–њ—А—П–Љ—Г—О. –°—В—А–∞—В–µ–≥–Є–Є –≤–Ї–ї—О—З–∞—О—В –∞–љ—В–Є—В–µ–ї–∞, —Б–Њ–Ј–і–∞–љ–љ—Л–µ –і–ї—П –±–ї–Њ–Ї–Є—А–Њ–≤–∞–љ–Є—П –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–≤, –Ї–Њ—В–Њ—А—Л–µ –њ–Њ–і–∞–≤–ї—П—О—В –њ—А–Њ—В–Є–≤–Њ—А–∞–Ї–Њ–≤—Л–µ –Є–Љ–Љ—Г–љ–љ—Л–µ —А–µ–∞–Ї—Ж–Є–Є, –Ї–Њ–љ—В—А–Њ–ї—М–љ—Л–µ —В–Њ—З–Ї–Є, —В–∞–Ї–Є–µ –Ї–∞–Ї PD-1 –Є CTLA-4 ( —В–µ—А–∞–њ–Є—П –Ї–Њ–љ—В—А–Њ–ї—М–љ—Л—Е —В–Њ—З–µ–Ї ), [20] –Є –∞–љ—В–Є—В–µ–ї–∞, –Љ–Њ–і–Є—Д–Є—Ж–Є—А–Њ–≤–∞–љ–љ—Л–µ –і–ї—П —Б—В–Є–Љ—Г–ї—П—Ж–Є–Є –∞–Ї—В–Є–≤–∞—Ж–Є–Є –Є–Љ–Љ—Г–љ–љ—Л—Е –Ї–ї–µ—В–Њ–Ї. [21]
–Р—Г—В–Њ–Є–Љ–Љ—Г–љ–љ—Л–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П
[ —А–µ–і–∞–Ї—В–Є—А–Њ–≤–∞—В—М ]–Ь–Њ–љ–Њ–Ї–ї–Њ–љ–∞–ї—М–љ—Л–µ –∞–љ—В–Є—В–µ–ї–∞, –Є—Б–њ–Њ–ї—М–Ј—Г–µ–Љ—Л–µ –њ—А–Є –∞—Г—В–Њ–Є–Љ–Љ—Г–љ–љ—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П—Е , –≤–Ї–ї—О—З–∞—О—В –Є–љ—Д–ї–Є–Ї—Б–Є–Љ–∞–± –Є –∞–і–∞–ї–Є–Љ—Г–Љ–∞–± , –Ї–Њ—В–Њ—А—Л–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л –њ—А–Є —А–µ–≤–Љ–∞—В–Њ–Є–і–љ–Њ–Љ –∞—А—В—А–Є—В–µ , –±–Њ–ї–µ–Ј–љ–Є –Ъ—А–Њ–љ–∞ –Є —П–Ј–≤–µ–љ–љ–Њ–Љ –Ї–Њ–ї–Є—В–µ –±–ї–∞–≥–Њ–і–∞—А—П —Б–≤–Њ–µ–є —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В–Є —Б–≤—П–Ј—Л–≤–∞—В—М—Б—П –Є –Є–љ–≥–Є–±–Є—А–Њ–≤–∞—В—М TNF-ќ± . [22] –С–∞–Ј–Є–ї–Є–Ї—Б–Є–Љ–∞–± –Є –і–∞–Ї–ї–Є–Ј—Г–Љ–∞–± –Є–љ–≥–Є–±–Є—А—Г—О—В IL-2 –љ–∞ –∞–Ї—В–Є–≤–Є—А–Њ–≤–∞–љ–љ—Л—Е –Ґ-–Ї–ї–µ—В–Ї–∞—Е –Є —В–µ–Љ —Б–∞–Љ—Л–Љ –њ–Њ–Љ–Њ–≥–∞—О—В –њ—А–µ–і–Њ—В–≤—А–∞—В–Є—В—М –Њ—Б—В—А–Њ–µ –Њ—В—В–Њ—А–ґ–µ–љ–Є–µ —В—А–∞–љ—Б–њ–ї–∞–љ—В–∞—В–∞ –њ–Њ—З–Ї–Є. [22] –Ю–Љ–∞–ї–Є–Ј—Г–Љ–∞–± –Є–љ–≥–Є–±–Є—А—Г–µ—В —З–µ–ї–Њ–≤–µ—З–µ—Б–Ї–Є–є –Є–Љ–Љ—Г–љ–Њ–≥–ї–Њ–±—Г–ї–Є–љ –Х (IgE) –Є —Н—Д—Д–µ–Ї—В–Є–≤–µ–љ –њ—А–Є –∞–ї–ї–µ—А–≥–Є—З–µ—Б–Ї–Њ–є –∞—Б—В–Љ–µ —Б—А–µ–і–љ–µ–є –Є —В—П–ґ–µ–ї–Њ–є —Б—В–µ–њ–µ–љ–Є . [ –љ—Г–ґ–љ–∞ —Б—Б—Л–ї–Ї–∞ ]
–±–Њ–ї–µ–Ј–љ—М –Р–ї—М—Ж–≥–µ–є–Љ–µ—А–∞
[ —А–µ–і–∞–Ї—В–Є—А–Њ–≤–∞—В—М ]–С–Њ–ї–µ–Ј–љ—М –Р–ї—М—Ж–≥–µ–є–Љ–µ—А–∞ (–С–Р) –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В —Б–Њ–±–Њ–є –Љ–љ–Њ–≥–Њ–≥—А–∞–љ–љ–Њ–µ, –≤–Њ–Ј—А–∞—Б—В–љ–Њ-–Ј–∞–≤–Є—Б–Є–Љ–Њ–µ, –њ—А–Њ–≥—А–µ—Б—Б–Є—А—Г—О—Й–µ–µ –љ–µ–є—А–Њ–і–µ–≥–µ–љ–µ—А–∞—В–Є–≤–љ–Њ–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–µ –Є —П–≤–ї—П–µ—В—Б—П –Њ—Б–љ–Њ–≤–љ–Њ–є –њ—А–Є—З–Є–љ–Њ–є –і–µ–Љ–µ–љ—Ж–Є–Є. [23] –°–Њ–≥–ї–∞—Б–љ–Њ –≥–Є–њ–Њ—В–µ–Ј–µ –∞–Љ–Є–ї–Њ–Є–і–∞ , –љ–∞–Ї–Њ–њ–ї–µ–љ–Є–µ –≤–љ–µ–Ї–ї–µ—В–Њ—З–љ—Л—Е –±–µ—В–∞-–∞–Љ–Є–ї–Њ–Є–і–љ—Л—Е –њ–µ–њ—В–Є–і–Њ–≤ (Aќ≤) –≤ –±–ї—П—И–Ї–∞—Е –њ–Њ—Б—А–µ–і—Б—В–≤–Њ–Љ –Њ–ї–Є–≥–Њ–Љ–µ—А–Є–Ј–∞—Ж–Є–Є –њ—А–Є–≤–Њ–і–Є—В –Ї —Е–∞—А–∞–Ї—В–µ—А–љ—Л–Љ —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Є–Љ —Б–Њ—Б—В–Њ—П–љ–Є—П–Љ AD —З–µ—А–µ–Ј —Б–Є–љ–∞–њ—В–Є—З–µ—Б–Ї—Г—О –і–Є—Б—Д—Г–љ–Ї—Ж–Є—О –Є –љ–µ–є—А–Њ–і–µ–≥–µ–љ–µ—А–∞—Ж–Є—О. [24] –Ш–Ј–≤–µ—Б—В–љ–Њ, —З—В–Њ –Є–Љ–Љ—Г–љ–Њ—В–µ—А–∞–њ–Є—П —Б –њ–Њ–Љ–Њ—Й—М—О –≤–≤–µ–і–µ–љ–Є—П —Н–Ї–Ј–Њ–≥–µ–љ–љ—Л—Е –Љ–Њ–љ–Њ–Ї–ї–Њ–љ–∞–ї—М–љ—Л—Е –∞–љ—В–Є—В–µ–ї (mAb) –ї–µ—З–Є—В —А–∞–Ј–ї–Є—З–љ—Л–µ —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞ —Ж–µ–љ—В—А–∞–ї—М–љ–Њ–є –љ–µ—А–≤–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л. –°—З–Є—В–∞–µ—В—Б—П, —З—В–Њ –≤ —Б–ї—Г—З–∞–µ AD –Є–Љ–Љ—Г–љ–Њ—В–µ—А–∞–њ–Є—П –Є–љ–≥–Є–±–Є—А—Г–µ—В Aќ≤-–Њ–ї–Є–≥–Њ–Љ–µ—А–Є–Ј–∞—Ж–Є—О –Є–ї–Є –≤—Л–≤–µ–і–µ–љ–Є–µ Aќ≤ –Є–Ј –Љ–Њ–Ј–≥–∞ –Є —В–µ–Љ —Б–∞–Љ—Л–Љ –њ—А–µ–і–Њ—В–≤—А–∞—Й–∞–µ—В –љ–µ–є—А–Њ—В–Њ–Ї—Б–Є—З–љ–Њ—Б—В—М . [25]
–Ю–і–љ–∞–Ї–Њ –Љ–Њ–љ–Њ–Ї–ї–Њ–љ–∞–ї—М–љ—Л–µ –∞–љ—В–Є—В–µ–ї–∞ –њ—А–µ–і—Б—В–∞–≤–ї—П—О—В —Б–Њ–±–Њ–є –±–Њ–ї—М—И–Є–µ –Љ–Њ–ї–µ–Ї—Г–ї—Л, –Є –Є–Ј-–Ј–∞ –≥–µ–Љ–∞—В–Њ—Н–љ—Ж–µ—Д–∞–ї–Є—З–µ—Б–Ї–Њ–≥–Њ –±–∞—А—М–µ—А–∞ –њ—А–Њ–љ–Є–Ї–љ–Њ–≤–µ–љ–Є–µ –Љ–Њ–љ–Њ–Ї–ї–Њ–љ–∞–ї—М–љ—Л—Е –∞–љ—В–Є—В–µ–ї –≤ –Љ–Њ–Ј–≥ –Ї—А–∞–є–љ–µ –Њ–≥—А–∞–љ–Є—З–µ–љ–Њ: –њ–Њ –Њ—Ж–µ–љ–Ї–∞–Љ, –њ—А–Њ—Е–Њ–і–Є—В —В–Њ–ї—М–Ї–Њ –њ—А–Є–Љ–µ—А–љ–Њ 1 –Є–Ј 1000 –Љ–Њ–ї–µ–Ї—Г–ї –Љ–Њ–љ–Њ–Ї–ї–Њ–љ–∞–ї—М–љ—Л—Е –∞–љ—В–Є—В–µ–ї. [25] –Ю–і–љ–∞–Ї–Њ –≥–Є–њ–Њ—В–µ–Ј–∞ –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–≥–Њ —Б—В–Њ–Ї–∞ –њ—А–µ–і–њ–Њ–ї–∞–≥–∞–µ—В –Љ–µ—Е–∞–љ–Є–Ј–Љ, –њ—А–Є –Ї–Њ—В–Њ—А–Њ–Љ –Љ–Њ–љ–Њ–Ї–ї–Њ–љ–∞–ї—М–љ—Л–Љ –∞–љ—В–Є—В–µ–ї–∞–Љ, –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ, –љ–µ –љ—Г–ґ–љ–Њ –њ–µ—А–µ—Б–µ–Ї–∞—В—М –≥–µ–Љ–∞—В–Њ—Н–љ—Ж–µ—Д–∞–ї–Є—З–µ—Б–Ї–Є–є –±–∞—А—М–µ—А. [26] –Я–Њ—Н—В–Њ–Љ—Г –Љ–љ–Њ–≥–Є–µ –љ–∞—Г—З–љ—Л–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ—А–Њ–≤–Њ–і—П—В—Б—П –љ–∞ –Њ—Б–љ–Њ–≤–µ –љ–µ—Г–і–∞—З–љ—Л—Е –њ–Њ–њ—Л—В–Њ–Ї –ї–µ—З–µ–љ–Є—П –С–Р –≤ –њ—А–Њ—И–ї–Њ–Љ. [24]
–Ю–і–љ–∞–Ї–Њ –≤–∞–Ї—Ж–Є–љ—Л –њ—А–Њ—В–Є–≤ Aќ≤ –Љ–Њ–≥—Г—В —Б–њ–Њ—Б–Њ–±—Б—В–≤–Њ–≤–∞—В—М –Њ–њ–Њ—Б—А–µ–і–Њ–≤–∞–љ–љ–Њ–Љ—Г –∞–љ—В–Є—В–µ–ї–∞–Љ–Є –Ї–ї–Є—А–µ–љ—Б—Г –±–ї—П—И–µ–Ї Aќ≤ –љ–∞ –Љ–Њ–і–µ–ї—П—Е —В—А–∞–љ—Б–≥–µ–љ–љ—Л—Е –Љ—Л—И–µ–є —Б –±–µ–ї–Ї–∞–Љ–Є-–њ—А–µ–і—И–µ—Б—В–≤–µ–љ–љ–Є–Ї–∞–Љ–Є –∞–Љ–Є–ї–Њ–Є–і–∞ (APP) –Є –Љ–Њ–≥—Г—В —Г–Љ–µ–љ—М—И–∞—В—М –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л–µ –љ–∞—А—Г—И–µ–љ–Є—П. [23] –Т–∞–Ї—Ж–Є–љ—Л –Љ–Њ–≥—Г—В —Б—В–Є–Љ—Г–ї–Є—А–Њ–≤–∞—В—М –Є–Љ–Љ—Г–љ–љ—Г—О —Б–Є—Б—В–µ–Љ—Г –Ї –≤—Л—А–∞–±–Њ—В–Ї–µ —Б–Њ–±—Б—В–≤–µ–љ–љ—Л—Е –∞–љ—В–Є—В–µ–ї, –≤ —Б–ї—Г—З–∞–µ –±–Њ–ї–µ–Ј–љ–Є –Р–ї—М—Ж–≥–µ–є–Љ–µ—А–∞, –њ—Г—В–µ–Љ –≤–≤–µ–і–µ–љ–Є—П –∞–љ—В–Є–≥–µ–љ–∞ Aќ≤. [27] –≠—В–Њ —В–∞–Ї–ґ–µ –Є–Ј–≤–µ—Б—В–љ–Њ –Ї–∞–Ї –∞–Ї—В–Є–≤–љ–∞—П –Є–Љ–Љ—Г–љ–Њ—В–µ—А–∞–њ–Є—П . –Ф—А—Г–≥–∞—П —Б—В—А–∞—В–µ–≥–Є—П вАУ —В–∞–Ї –љ–∞–Ј—Л–≤–∞–µ–Љ–∞—П –њ–∞—Б—Б–Є–≤–љ–∞—П –Є–Љ–Љ—Г–љ–Њ—В–µ—А–∞–њ–Є—П . –Т —Н—В–Њ–Љ —Б–ї—Г—З–∞–µ –∞–љ—В–Є—В–µ–ї–∞ –≤—Л—А–∞–±–∞—В—Л–≤–∞—О—В—Б—П –Є–Ј–≤–љ–µ –≤ –Ї—Г–ї—М—В–Є–≤–Є—А—Г–µ–Љ—Л—Е –Ї–ї–µ—В–Ї–∞—Е –Є –і–Њ—Б—В–∞–≤–ї—П—О—В—Б—П –њ–∞—Ж–Є–µ–љ—В—Г –≤ –≤–Є–і–µ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ–Њ–≥–Њ —Б—А–µ–і—Б—В–≤–∞. –С—Л–ї–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ —Г –Љ—Л—И–µ–є, —Н–Ї—Б–њ—А–µ—Б—Б–Є—А—Г—О—Й–Є—Е –Р–†–†, –Ї–∞–Ї –∞–Ї—В–Є–≤–љ–∞—П, —В–∞–Ї –Є –њ–∞—Б—Б–Є–≤–љ–∞—П –Є–Љ–Љ—Г–љ–Є–Ј–∞—Ж–Є—П –∞–љ—В–Є—В–µ–ї–∞–Љ–Є –њ—А–Њ—В–Є–≤ Aќ≤ —Н—Д—Д–µ–Ї—В–Є–≤–љ–∞ –≤ –Њ—З–Є—Й–µ–љ–Є–Є –±–ї—П—И–µ–Ї –Є –Љ–Њ–ґ–µ—В —Г–ї—Г—З—И–Є—В—М –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л–µ —Д—Г–љ–Ї—Ж–Є–Є. [24]
–Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П —Б—Г—Й–µ—Б—В–≤—Г–µ—В –і–≤–∞ –Њ–і–Њ–±—А–µ–љ–љ—Л—Е FDA –њ—А–µ–њ–∞—А–∞—В–∞ –і–ї—П –ї–µ—З–µ–љ–Є—П –±–Њ–ї–µ–Ј–љ–Є –Р–ї—М—Ж–≥–µ–є–Љ–µ—А–∞ –љ–∞ –Њ—Б–љ–Њ–≤–µ –∞–љ—В–Є—В–µ–ї: –∞–і—Г–Ї–∞–љ–µ–Љ–∞–± –Є –ї–µ–Ї–∞–љ–µ–Љ–∞–± . –Р–і—Г–Ї–∞–љ–µ–Љ–∞–± –њ–Њ–ї—Г—З–Є–ї —Г—Б–Ї–Њ—А–µ–љ–љ–Њ–µ –Њ–і–Њ–±—А–µ–љ–Є–µ , –∞ –Ы–µ–Ї–∞–љ–µ–Љ–∞–± вАФ –њ–Њ–ї–љ–Њ–µ –Њ–і–Њ–±—А–µ–љ–Є–µ. [25] –С—Л–ї–Њ –њ—А–Њ–≤–µ–і–µ–љ–Њ –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б–њ—Л—В–∞–љ–Є–є —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ –њ–∞—Б—Б–Є–≤–љ–Њ–є –Є –∞–Ї—В–Є–≤–љ–Њ–є –Є–Љ–Љ—Г–љ–Є–Ј–∞—Ж–Є–Є, –Є –љ–µ–Ї–Њ—В–Њ—А—Л–µ –Є–Ј –љ–Є—Е —Г–ґ–µ –≤ –њ—Г—В–Є –Є –њ—А–Є–љ–µ—Б—Г—В –Њ–ґ–Є–і–∞–µ–Љ—Л–µ —А–µ–Ј—Г–ї—М—В–∞—В—Л —З–µ—А–µ–Ј –њ–∞—А—Г –ї–µ—В. [24] [25] –Я—А–Є–Љ–µ–љ–µ–љ–Є–µ —Н—В–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ —З–∞—Б—В–Њ –њ—А–Є—Е–Њ–і–Є—В—Б—П –љ–∞ —А–∞–љ–љ–µ–µ –љ–∞—З–∞–ї–Њ –Р–Ф. –Ф—А—Г–≥–Є–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Є —А–∞–Ј—А–∞–±–Њ—В–Ї–Є –ї–µ–Ї–∞—А—Б—В–≤ –і–ї—П —А–∞–љ–љ–µ–≥–Њ –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤–∞ –Є –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є AD –њ—А–Њ–і–Њ–ї–ґ–∞—О—В—Б—П. –Я—А–Є–Љ–µ—А—Л –≤–∞–ґ–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –Љ–Њ–љ–Њ–Ї–ї–Њ–љ–∞–ї—М–љ—Л—Е –∞–љ—В–Є—В–µ–ї, –Ї–Њ—В–Њ—А—Л–µ –њ—А–Њ—И–ї–Є –Є–ї–Є –њ—А–Њ—Е–Њ–і—П—В –Њ—Ж–µ–љ–Ї—Г –і–ї—П –ї–µ—З–µ–љ–Є—П –С–Р, –≤–Ї–ї—О—З–∞—О—В –±–∞–њ–Є–љ–µ—Г–Ј—Г–Љ–∞–± , —Б–Њ–ї–∞–љ–µ–Ј—Г–Љ–∞–± , –≥–∞—Г—В–µ–љ—Г–Љ–∞–± , –Ї—А–µ–љ–µ–Ј—Г–Љ–∞–± , –∞–і—Г–Ї–∞–љ–µ–Љ–∞–± , –ї–µ–Ї–∞–љ–µ–Љ–∞–± –Є –і–Њ–љ–∞–љ–µ–Љ–∞–± . [25]
–С–∞–њ–Є–љ–µ—Г–Ј—Г–Љ–∞–±
[ —А–µ–і–∞–Ї—В–Є—А–Њ–≤–∞—В—М ]–С–∞–њ–Є–љ–µ—Г–Ј—Г–Љ–∞–± , –≥—Г–Љ–∞–љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–µ –Љ–Њ–љ–Њ–Ї–ї–Њ–љ–∞–ї—М–љ–Њ–µ –∞–љ—В–Є—В–µ–ї–Њ –њ—А–Њ—В–Є–≤ Aќ≤, –љ–∞–њ—А–∞–≤–ї–µ–љ–Њ –њ—А–Њ—В–Є–≤ N-–Ї–Њ–љ—Ж–∞ Aќ≤. –Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —Д–∞–Ј—Л II –±–∞–њ–Є–љ–µ—Г–Ј—Г–Љ–∞–±–∞ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –С–Р –ї–µ–≥–Ї–Њ–є –Є —Б—А–µ–і–љ–µ–є —Б—В–µ–њ–µ–љ–Є —В—П–ґ–µ—Б—В–Є –њ—А–Є–≤–µ–ї–Є –Ї —Б–љ–Є–ґ–µ–љ–Є—О –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є Aќ≤ –≤ –≥–Њ–ї–Њ–≤–љ–Њ–Љ –Љ–Њ–Ј–≥–µ. –Ю–і–љ–∞–Ї–Њ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –њ–Њ–≤—Л—И–µ–љ–љ—Л–Љ –љ–Њ—Б–Є—В–µ–ї—М—Б—В–≤–Њ–Љ –∞–њ–Њ–ї–Є–њ–Њ–њ—А–Њ—В–µ–Є–љ–∞ (–Р–†–Ю–Х) –µ4 –ї–µ—З–µ–љ–Є–µ –±–∞–њ–Є–љ–µ—Г–Ј—Г–Љ–∞–±–Њ–Љ —В–∞–Ї–ґ–µ —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–µ—В—Б—П –≤–∞–Ј–Њ–≥–µ–љ–љ—Л–Љ –Њ—В–µ–Ї–Њ–Љ , [28] –¶–Є—В–Њ—В–Њ–Ї—Б–Є—З–µ—Б–Ї–Њ–µ —Б–Њ—Б—В–Њ—П–љ–Є–µ, –њ—А–Є –Ї–Њ—В–Њ—А–Њ–Љ –≥–µ–Љ–∞—В–Њ—Н–љ—Ж–µ—Д–∞–ї–Є—З–µ—Б–Ї–Є–є –±–∞—А—М–µ—А –љ–∞—А—Г—И–∞–µ—В—Б—П, —З—В–Њ –њ—А–Є–≤–Њ–і–Є—В –Ї –њ–Њ—А–∞–ґ–µ–љ–Є—О –±–µ–ї–Њ–≥–Њ –≤–µ—Й–µ—Б—В–≤–∞ –Є–Ј-–Ј–∞ –Є–Ј–±—Л—В–Њ—З–љ–Њ–≥–Њ –љ–∞–Ї–Њ–њ–ї–µ–љ–Є—П –ґ–Є–і–Ї–Њ—Б—В–Є –Є–Ј –Ї–∞–њ–Є–ї–ї—П—А–Њ–≤ –≤–Њ –≤–љ—Г—В—А–Є–Ї–ї–µ—В–Њ—З–љ—Л—Е –Є –≤–љ–µ–Ї–ї–µ—В–Њ—З–љ—Л—Е –њ—А–Њ—Б—В—А–∞–љ—Б—В–≤–∞—Е –≥–Њ–ї–Њ–≤–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞. [29]
–Т –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е —Д–∞–Ј—Л III –±–∞–њ–Є–љ–µ—Г–Ј—Г–Љ–∞–± –њ—А–Њ–і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–ї –Љ–љ–Њ–≥–Њ–Њ–±–µ—Й–∞—О—Й–µ–µ –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ–µ –≤–ї–Є—П–љ–Є–µ –љ–∞ –±–Є–Њ–Љ–∞—А–Ї–µ—А—Л –С–Р, –љ–Њ –љ–µ –њ—А–Њ–і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–ї –≤–ї–Є—П–љ–Є—П –љ–∞ —Б–љ–Є–ґ–µ–љ–Є–µ –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е —Д—Г–љ–Ї—Ж–Є–є. –Я–Њ—Н—В–Њ–Љ—Г –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –±–∞–њ–Є–љ–µ—Г–Ј—Г–Љ–∞–±–∞ –±—Л–ї–Њ –њ—А–µ–Ї—А–∞—Й–µ–љ–Њ –њ–Њ—Б–ї–µ –љ–µ—Г–і–∞—З–Є –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є —Д–∞–Ј—Л III. [29]
–°–Њ–ї–∞–љ–µ–Ј—Г–Љ–∞–±
[ —А–µ–і–∞–Ї—В–Є—А–Њ–≤–∞—В—М ]–°–Њ–ї–∞–љ–µ–Ј—Г–Љ–∞–± , mAb –њ—А–Њ—В–Є–≤ Aќ≤, –љ–∞—Ж–µ–ї–µ–љ –љ–∞ N-–Ї–Њ–љ–µ—Ж Aќ≤. –Т —Д–∞–Ј–µ I –Є —Д–∞–Ј–µ II –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –ї–µ—З–µ–љ–Є–µ —Б–Њ–ї–∞–љ–µ–Ј—Г–Љ–∞–±–Њ–Љ –њ—А–Є–≤–Њ–і–Є–ї–Њ –Ї –њ–Њ–≤—Л—И–µ–љ–Є—О —Г—А–Њ–≤–љ—П Aќ≤ –≤ —Б–њ–Є–љ–љ–Њ–Љ–Њ–Ј–≥–Њ–≤–Њ–є –ґ–Є–і–Ї–Њ—Б—В–Є , —В–µ–Љ —Б–∞–Љ—Л–Љ –і–µ–Љ–Њ–љ—Б—В—А–Є—А—Г—П —Б–љ–Є–ґ–µ–љ–Є–µ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –±–ї—П—И–µ–Ї Aќ≤. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –Њ—В—Б—Г—В—Б—В–≤—Г—О—В —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–Є–µ –љ–µ–±–ї–∞–≥–Њ–њ—А–Є—П—В–љ—Л–µ –њ–Њ–±–Њ—З–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л. –Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П III —Д–∞–Ј—Л —Б–Њ–ї–∞–љ–µ–Ј—Г–Љ–∞–±–∞ –њ—А–Є–≤–µ–ї–Є –Ї –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–Љ—Г —Б–љ–Є–ґ–µ–љ–Є—О –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –ї–µ–≥–Ї–Њ–є —Д–Њ—А–Љ–Њ–є –С–Р, –љ–Њ –љ–µ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —В—П–ґ–µ–ї–Њ–є —Д–Њ—А–Љ–Њ–є –С–Р. –Ю–і–љ–∞–Ї–Њ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П Aќ≤ —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –љ–µ –Є–Ј–Љ–µ–љ–Є–ї–∞—Б—М, –Ї–∞–Ї –Є –і—А—Г–≥–Є–µ –±–Є–Њ–Љ–∞—А–Ї–µ—А—Л AD, –≤–Ї–ї—О—З–∞—П —Н–Ї—Б–њ—А–µ—Б—Б–Є—О —Д–Њ—Б—Д–Њ-—В–∞—Г –Є –Њ–±—К–µ–Љ –≥–Є–њ–њ–Њ–Ї–∞–Љ–њ–∞. –Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ –Є—Б–њ—Л—В–∞–љ–Є—П III —Д–∞–Ј—Л —Б–Њ–ї–∞–љ–µ–Ј—Г–Љ–∞–±–∞ –љ–µ —Г–≤–µ–љ—З–∞–ї–Є—Б—М —Г—Б–њ–µ—Е–Њ–Љ, –њ–Њ—Б–Ї–Њ–ї—М–Ї—Г –Њ–љ –љ–µ –њ–Њ–Ї–∞–Ј–∞–ї –≤–ї–Є—П–љ–Є—П –љ–∞ —Б–љ–Є–ґ–µ–љ–Є–µ –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е —Д—Г–љ–Ї—Ж–Є–є –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –њ–ї–∞—Ж–µ–±–Њ. [30]
–Ы–µ–Ї–∞–љ–µ–Љ–∞–±
[ —А–µ–і–∞–Ї—В–Є—А–Њ–≤–∞—В—М ]–Ы–µ–Ї–∞–љ–µ–Љ–∞–± (BAN2401) –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В —Б–Њ–±–Њ–є –≥—Г–Љ–∞–љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–µ –Љ–Њ–љ–Њ–Ї–ї–Њ–љ–∞–ї—М–љ–Њ–µ –∞–љ—В–Є—В–µ–ї–Њ, –Є–Ј–±–Є—А–∞—В–µ–ї—М–љ–Њ –≤–Њ–Ј–і–µ–є—Б—В–≤—Г—О—Й–µ–µ –љ–∞ —В–Њ–Ї—Б–Є—З–љ—Л–µ —А–∞—Б—В–≤–Њ—А–Є–Љ—Л–µ –њ—А–Њ—В–Њ—Д–Є–±—А–Є–ї–ї—Л Aќ≤. [31] –Т —В—А–µ—В—М–µ–є —Д–∞–Ј–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б–њ—Л—В–∞–љ–Є–є [32] –Ы–µ–Ї–∞–љ–µ–Љ–∞–± –њ–Њ–Ї–∞–Ј–∞–ї —Б–љ–Є–ґ–µ–љ–Є–µ –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е —Д—Г–љ–Ї—Ж–Є–є –љ–∞ 27% –Љ–µ–і–ї–µ–љ–љ–µ–µ –њ–Њ—Б–ї–µ 18 –Љ–µ—Б—П—Ж–µ–≤ –ї–µ—З–µ–љ–Є—П –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –њ–ї–∞—Ж–µ–±–Њ. [33] [34] –Т –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е —Д–∞–Ј—Л 3 —В–∞–Ї–ґ–µ —Б–Њ–Њ–±—Й–∞–ї–Њ—Б—М –Њ —А–µ–∞–Ї—Ж–Є—П—Е, —Б–≤—П–Ј–∞–љ–љ—Л—Е —Б –Є–љ—Д—Г–Ј–Є–µ–є, –љ–∞—А—Г—И–µ–љ–Є—П—Е –≤–Є–Ј—Г–∞–ї–Є–Ј–∞—Ж–Є–Є, —Б–≤—П–Ј–∞–љ–љ—Л—Е —Б –∞–Љ–Є–ї–Њ–Є–і–Њ–Љ , –Є –≥–Њ–ї–Њ–≤–љ—Л—Е –±–Њ–ї—П—Е –Ї–∞–Ї –Њ –љ–∞–Є–±–Њ–ї–µ–µ —З–∞—Б—В—Л—Е –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–∞—Е –ї–µ–Ї–∞–љ–µ–Љ–∞–±–∞. –Т –Є—О–ї–µ 2023 –≥–Њ–і–∞ FDA –њ–Њ–ї–љ–Њ—Б—В—М—О –Њ–і–Њ–±—А–Є–ї–Њ –Ы–µ–Ї–∞–љ–µ–Љ–∞–± –і–ї—П –ї–µ—З–µ–љ–Є—П –±–Њ–ї–µ–Ј–љ–Є –Р–ї—М—Ж–≥–µ–є–Љ–µ—А–∞. [35] –Є –µ–Љ—Г –±—Л–ї–Њ –њ—А–Є—Б–≤–Њ–µ–љ–Њ –Ї–Њ–Љ–Љ–µ—А—З–µ—Б–Ї–Њ–µ –љ–∞–Ј–≤–∞–љ–Є–µ –Ы–µ–Ї–µ–Љ–±–Є.
–Я—А–Њ—Д–Є–ї–∞–Ї—В–Є—З–µ—Б–Ї–Є–µ –Є—Б–њ—Л—В–∞–љ–Є—П
[ —А–µ–і–∞–Ї—В–Є—А–Њ–≤–∞—В—М ]–Э–µ—Г–і–∞—З–∞ –љ–µ—Б–Ї–Њ–ї—М–Ї–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б–њ—Л—В–∞–љ–Є—П—Е —Д–∞–Ј—Л III –њ—А–Є–≤–µ–ї–∞ –Ї –њ—А–µ–і–Њ—В–≤—А–∞—Й–µ–љ–Є—О –С–Р –Є —А–∞–љ–љ–µ–Љ—Г –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤—Г –і–ї—П –љ–∞—З–∞–ї–∞ –ї–µ—З–µ–љ–Є—П –С–Р. –Я–∞—Б—Б–Є–≤–љ–Њ–µ –ї–µ—З–µ–љ–Є–µ –Љ–Њ–љ–Њ–Ї–ї–Њ–љ–∞–ї—М–љ—Л–Љ–Є –∞–љ—В–Є—В–µ–ї–∞–Љ–Є –Ї Aќ≤ –Љ–Њ–ґ–љ–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М –і–ї—П –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є—З–µ—Б–Ї–Є—Е –њ–Њ–њ—Л—В–Њ–Ї –Є–Ј–Љ–µ–љ–Є—В—М –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є–µ –С–Р –і–Њ —В–Њ–≥–Њ, –Ї–∞–Ї –Њ–љ–Њ –≤—Л–Ј–Њ–≤–µ—В –Њ–±—И–Є—А–љ–Њ–µ –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є–µ –≥–Њ–ї–Њ–≤–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞ –Є —Б–Є–Љ–њ—В–Њ–Љ—Л. –Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –њ—А–Њ–≤–Њ–і—П—В—Б—П –Є—Б–њ—Л—В–∞–љ–Є—П –њ–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—О –ї–µ—З–µ–љ–Є—П –Љ–Њ–љ–Њ–Ї–ї–Њ–љ–∞–ї—М–љ—Л–Љ–Є –∞–љ—В–Є—В–µ–ї–∞–Љ–Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л–Љ–Є –≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є–Љ–Є —Д–∞–Ї—В–Њ—А–∞–Љ–Є —А–Є—Б–Ї–∞ –Є –њ–Њ–ґ–Є–ї—Л—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л–Љ–Є –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П–Љ–Є –С–Р. –°—О–і–∞ –≤—Е–Њ–і–Є—В –∞–љ—В–Є-–Р–С –ї–µ—З–µ–љ–Є–µ –±–µ—Б—Б–Є–Љ–њ—В–Њ–Љ–љ–Њ–є –±–Њ–ї–µ–Ј–љ–Є –Р–ї—М—Ж–≥–µ–є–Љ–µ—А–∞ (–Р4), –Ш–љ–Є—Ж–Є–∞—В–Є–≤–∞ –њ–Њ –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–µ –±–Њ–ї–µ–Ј–љ–Є –Р–ї—М—Ж–≥–µ–є–Љ–µ—А–∞ (API) –Є DIAN-TU. [26] –Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –Р4 –љ–∞ –њ–Њ–ґ–Є–ї—Л—Е –ї—О–і—П—Е, —Г –Ї–Њ—В–Њ—А—Л—Е –µ—Б—В—М –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –С–Р, –љ–Њ –Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ—Л–µ –њ–Њ –≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є–Љ —Д–∞–Ї—В–Њ—А–∞–Љ —А–Є—Б–Ї–∞, —Б–Њ–ї–∞–љ–µ–Ј—Г–Љ–∞–± –±—Г–і–µ—В –њ—А–Њ–≤–µ—А–µ–љ –≤ III —Д–∞–Ј–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –≤ –Ї–∞—З–µ—Б—В–≤–µ –њ—А–Њ–і–Њ–ї–ґ–µ–љ–Є—П –њ—А–µ–і—Л–і—Г—Й–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є —Б–Њ–ї–∞–љ–µ–Ј—Г–Љ–∞–±–∞. [26] –Я—А–Њ–≥—А–∞–Љ–Љ–∞ DIAN-TU, –Ј–∞–њ—Г—Й–µ–љ–љ–∞—П –≤ –і–µ–Ї–∞–±—А–µ 2012 –≥–Њ–і–∞, –Њ—А–Є–µ–љ—В–Є—А–Њ–≤–∞–љ–∞ –љ–∞ –Љ–Њ–ї–Њ–і—Л—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л–Љ–Є –≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є–Љ–Є –Љ—Г—В–∞—Ж–Є—П–Љ–Є, –Ї–Њ—В–Њ—А—Л–µ –њ—А–µ–і—Б—В–∞–≤–ї—П—О—В —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П –С–Р. –Т —Н—В–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –Є—Б–њ–Њ–ї—М–Ј—Г—О—В—Б—П —Б–Њ–ї–∞–љ–µ–Ј—Г–Љ–∞–± –Є –≥–∞—Г—В–µ–љ—Г–Љ–∞–±. –У–∞—Г—В–µ–љ—Г–Љ–∞–±, –њ–µ—А–≤—Л–є –њ–Њ–ї–љ–Њ—Б—В—М—О —З–µ–ї–Њ–≤–µ—З–µ—Б–Ї–Є–є MAB, –Ї–Њ—В–Њ—А—Л–є –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –≤–Ј–∞–Є–Љ–Њ–і–µ–є—Б—В–≤—Г–µ—В —Б –Њ–ї–Є–≥–Њ–Љ–µ—А–Є–Ј–Њ–≤–∞–љ–љ—Л–Љ–Є –±–ї—П—И–Ї–∞–Љ–Є Aќ≤ –≤ –≥–Њ–ї–Њ–≤–љ–Њ–Љ –Љ–Њ–Ј–≥–µ, –≤—Л–Ј—Л–≤–∞–ї –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є Aќ≤ –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е —Д–∞–Ј—Л I, –њ—А–µ–і–Њ—В–≤—А–∞—Й–∞—П –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ –Є –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—О –±–ї—П—И–µ–Ї –±–µ–Ј –Є–Ј–Љ–µ–љ–µ–љ–Є—П –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –≤ –њ–ї–∞–Ј–Љ–µ –Љ–Њ–Ј–≥–∞. –Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –њ—А–Њ–≤–Њ–і—П—В—Б—П –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —Д–∞–Ј—Л II –Є III. [26]
–Т–Є–і—Л —В–µ—А–∞–њ–Є–Є
[ —А–µ–і–∞–Ї—В–Є—А–Њ–≤–∞—В—М ]–†–∞–і–Є–Њ–Є–Љ–Љ—Г–љ–Њ—В–µ—А–∞–њ–Є—П
[ —А–µ–і–∞–Ї—В–Є—А–Њ–≤–∞—В—М ]–†–∞–і–Є–Њ–Є–Љ–Љ—Г–љ–Њ—В–µ—А–∞–њ–Є—П (–†–Ш–Ґ) –њ—А–µ–і–њ–Њ–ї–∞–≥–∞–µ—В –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ —А–∞–і–Є–Њ–∞–Ї—В–Є–≤–љ–Њ –Ї–Њ–љ—К—О–≥–Є—А–Њ–≤–∞–љ–љ—Л—Е –Љ—Л—И–Є–љ—Л—Е –∞–љ—В–Є—В–µ–ї –њ—А–Њ—В–Є–≤ –Ї–ї–µ—В–Њ—З–љ—Л—Е –∞–љ—В–Є–≥–µ–љ–Њ–≤. –С–Њ–ї—М—И–Є–љ—Б—В–≤–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –њ—А–µ–і–њ–Њ–ї–∞–≥–∞–µ—В –Є—Е –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –Ї –ї–Є–Љ—Д–Њ–Љ–∞–Љ , –њ–Њ—Б–Ї–Њ–ї—М–Ї—Г –Њ–љ–Є —П–≤–ї—П—О—В—Б—П –≤—Л—Б–Њ–Ї–Њ—А–∞–і–Є–Њ—З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ—Л–Љ–Є –Ј–ї–Њ–Ї–∞—З–µ—Б—В–≤–µ–љ–љ—Л–Љ–Є –љ–Њ–≤–Њ–Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П–Љ–Є. –Ф–ї—П –Њ–≥—А–∞–љ–Є—З–µ–љ–Є—П —А–∞–і–Є–∞—Ж–Є–Њ–љ–љ–Њ–≥–Њ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є—П –±—Л–ї–Є –≤—Л–±—А–∞–љ—Л –Љ—Л—И–Є–љ—Л–µ –∞–љ—В–Є—В–µ–ї–∞, –њ–Њ—Б–Ї–Њ–ї—М–Ї—Г –Є—Е –≤—Л—Б–Њ–Ї–∞—П –Є–Љ–Љ—Г–љ–Њ–≥–µ–љ–љ–Њ—Б—В—М —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В –±—Л—Б—В—А–Њ–Љ—Г –≤—Л–≤–µ–і–µ–љ–Є—О –Њ–њ—Г—Е–Њ–ї–Є. –Ґ–Њ–Ј–Є—В—Г–Љ–Њ–Љ–∞–± —П–≤–ї—П–µ—В—Б—П –њ—А–Є–Љ–µ—А–Њ–Љ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –њ—А–Є –љ–µ—Е–Њ–і–ґ–Ї–Є–љ—Б–Ї–Њ–є –ї–Є–Љ—Д–Њ–Љ–µ. [ –љ—Г–ґ–љ–∞ —Б—Б—Л–ї–Ї–∞ ]
–Р–љ—В–Є—В–µ–ї–∞-–љ–∞–њ—А–∞–≤–ї–µ–љ–љ–∞—П —Д–µ—А–Љ–µ–љ—В–љ–∞—П –њ—А–Њ–ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ–∞—П —В–µ—А–∞–њ–Є—П
[ —А–µ–і–∞–Ї—В–Є—А–Њ–≤–∞—В—М ]–Я—А–Њ–ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ–∞—П —Д–µ—А–Љ–µ–љ—В–љ–∞—П —В–µ—А–∞–њ–Є—П, –љ–∞–њ—А–∞–≤–ї–µ–љ–љ–∞—П –љ–∞ –∞–љ—В–Є—В–µ–ї–∞ (ADEPT), –≤–Ї–ї—О—З–∞–µ—В –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –∞—Б—Б–Њ—Ж–Є–Є—А–Њ–≤–∞–љ–љ—Л—Е —Б —А–∞–Ї–Њ–Љ –Љ–Њ–љ–Њ–Ї–ї–Њ–љ–∞–ї—М–љ—Л—Е –∞–љ—В–Є—В–µ–ї, –Ї–Њ—В–Њ—А—Л–µ —Б–≤—П–Ј–∞–љ—Л —Б —Д–µ—А–Љ–µ–љ—В–Њ–Љ, –∞–Ї—В–Є–≤–Є—А—Г—О—Й–Є–Љ –ї–µ–Ї–∞—А—Б—В–≤–Њ. –°–Є—Б—В–µ–Љ–љ–Њ–µ –≤–≤–µ–і–µ–љ–Є–µ –љ–µ—В–Њ–Ї—Б–Є—З–љ–Њ–≥–Њ –∞–≥–µ–љ—В–∞ –њ—А–Є–≤–Њ–і–Є—В –Ї –њ—А–µ–≤—А–∞—Й–µ–љ–Є—О –∞–љ—В–Є—В–µ–ї–∞ –≤ —В–Њ–Ї—Б–Є—З–љ–Њ–µ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ–Њ–µ —Б—А–µ–і—Б—В–≤–Њ, —З—В–Њ –њ—А–Є–≤–Њ–і–Є—В –Ї —Ж–Є—В–Њ—В–Њ–Ї—Б–Є—З–µ—Б–Ї–Њ–Љ—Г —Н—Д—Д–µ–Ї—В—Г, –Ї–Њ—В–Њ—А—Л–є –Љ–Њ–ґ–µ—В –±—Л—В—М –љ–∞–њ—А–∞–≤–ї–µ–љ –љ–∞ –Ј–ї–Њ–Ї–∞—З–µ—Б—В–≤–µ–љ–љ—Л–µ –Ї–ї–µ—В–Ї–Є. –Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Є–є —Г—Б–њ–µ—Е –ї–µ—З–µ–љ–Є—П ADEPT –Њ–≥—А–∞–љ–Є—З–µ–љ. [36]
–Ъ–Њ–љ—К—О–≥–∞—В—Л –∞–љ—В–Є—В–µ–ї–Њ-–ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ–Њ–µ —Б—А–µ–і—Б—В–≤–Њ
[ —А–µ–і–∞–Ї—В–Є—А–Њ–≤–∞—В—М ]–Ъ–Њ–љ—К—О–≥–∞—В—Л –∞–љ—В–Є—В–µ–ї–Њ-–ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ–Њ–µ —Б—А–µ–і—Б—В–≤–Њ (ADC) –њ—А–µ–і—Б—В–∞–≤–ї—П—О—В —Б–Њ–±–Њ–є –∞–љ—В–Є—В–µ–ї–∞, —Б–≤—П–Ј–∞–љ–љ—Л–µ —Б –Њ–і–љ–Њ–є –Є–ї–Є –љ–µ—Б–Ї–Њ–ї—М–Ї–Є–Љ–Є –Љ–Њ–ї–µ–Ї—Г–ї–∞–Љ–Є –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ–Њ–≥–Њ —Б—А–µ–і—Б—В–≤–∞. –Ю–±—Л—З–љ–Њ, –Ї–Њ–≥–і–∞ ADC –≤—Б—В—А–µ—З–∞–µ—В –Ї–ї–µ—В–Ї—Г-–Љ–Є—И–µ–љ—М (–љ–∞–њ—А–Є–Љ–µ—А, —А–∞–Ї–Њ–≤—Г—О –Ї–ї–µ—В–Ї—Г), –ї–µ–Ї–∞—А—Б—В–≤–Њ –≤—Л—Б–≤–Њ–±–Њ–ґ–і–∞–µ—В—Б—П, —З—В–Њ–±—Л —Г–±–Є—В—М –µ–µ. –Ь–љ–Њ–≥–Є–µ ADC –љ–∞—Е–Њ–і—П—В—Б—П –≤ —Б—В–∞–і–Є–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є —А–∞–Ј—А–∞–±–Њ—В–Ї–Є. –Я–Њ —Б–Њ—Б—В–Њ—П–љ–Є—О –љ–∞ 2016 –≥–Њ–і [update] –љ–µ–Ї–Њ—В–Њ—А—Л–µ –Є–Ј –љ–Є—Е –±—Л–ї–Є –Њ–і–Њ–±—А–µ–љ—Л. [ –љ—Г–ґ–љ–∞ —Б—Б—Л–ї–Ї–∞ ]
–Ш–Љ–Љ—Г–љ–Њ–ї–Є–њ–Њ—Б–Њ–Љ–љ–∞—П —В–µ—А–∞–њ–Є—П
[ —А–µ–і–∞–Ї—В–Є—А–Њ–≤–∞—В—М ]–Ш–Љ–Љ—Г–љ–Њ–ї–Є–њ–Њ—Б–Њ–Љ—Л –њ—А–µ–і—Б—В–∞–≤–ї—П—О—В —Б–Њ–±–Њ–є –ї–Є–њ–Њ—Б–Њ–Љ—Л , –Ї–Њ–љ—К—О–≥–Є—А–Њ–≤–∞–љ–љ—Л–µ —Б –∞–љ—В–Є—В–µ–ї–∞–Љ–Є . –Ы–Є–њ–Њ—Б–Њ–Љ—Л –Љ–Њ–≥—Г—В –љ–µ—Б—В–Є –ї–µ–Ї–∞—А—Б—В–≤–∞ –Є–ї–Є —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є–µ –љ—Г–Ї–ї–µ–Њ—В–Є–і—Л –Є –њ—А–Є –Ї–Њ–љ—К—О–≥–∞—Ж–Є–Є —Б –Љ–Њ–љ–Њ–Ї–ї–Њ–љ–∞–ї—М–љ—Л–Љ–Є –∞–љ—В–Є—В–µ–ї–∞–Љ–Є –Љ–Њ–≥—Г—В –±—Л—В—М –љ–∞–њ—А–∞–≤–ї–µ–љ—Л –њ—А–Њ—В–Є–≤ –Ј–ї–Њ–Ї–∞—З–µ—Б—В–≤–µ–љ–љ—Л—Е –Ї–ї–µ—В–Њ–Ї. –Ш–Љ–Љ—Г–љ–Њ–ї–Є–њ–Њ—Б–Њ–Љ—Л —Г—Б–њ–µ—И–љ–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї–Є—Б—М in vivo –і–ї—П –њ–µ—А–µ–љ–Њ—Б–∞ –≥–µ–љ–Њ–≤, –њ–Њ–і–∞–≤–ї—П—О—Й–Є—Е –Њ–њ—Г—Е–Њ–ї–Є, –≤ –Њ–њ—Г—Е–Њ–ї–Є —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ —Д—А–∞–≥–Љ–µ–љ—В–∞ –∞–љ—В–Є—В–µ–ї–∞ –њ—А–Њ—В–Є–≤ —А–µ—Ж–µ–њ—В–Њ—А–∞ —В—А–∞–љ—Б—Д–µ—А—А–Є–љ–∞ —З–µ–ї–Њ–≤–µ–Ї–∞ . –Ґ–Ї–∞–љ–µ—Б–њ–µ—Ж–Є—Д–Є—З–љ–∞—П –і–Њ—Б—В–∞–≤–Ї–∞ –≥–µ–љ–Њ–≤ —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ –Є–Љ–Љ—Г–љ–Њ–ї–Є–њ–Њ—Б–Њ–Љ –±—Л–ї–∞ –і–Њ—Б—В–Є–≥–љ—Г—В–∞ –≤ —В–Ї–∞–љ—П—Е —А–∞–Ї–∞ –≥–Њ–ї–Њ–≤–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞ –Є –Љ–Њ–ї–Њ—З–љ–Њ–є –ґ–µ–ї–µ–Ј—Л. [37]
–Ъ–Њ–љ—В—А–Њ–ї—М–љ–Њ-–њ—А–Њ–њ—Г—Б–Ї–љ–∞—П —В–µ—А–∞–њ–Є—П
[ —А–µ–і–∞–Ї—В–Є—А–Њ–≤–∞—В—М ]–Ґ–µ—А–∞–њ–Є—П –Ї–Њ–љ—В—А–Њ–ї—М–љ—Л—Е —В–Њ—З–µ–Ї –Є—Б–њ–Њ–ї—М–Ј—Г–µ—В –∞–љ—В–Є—В–µ–ї–∞ –Є –і—А—Г–≥–Є–µ –Љ–µ—В–Њ–і—Л, —З—В–Њ–±—Л –Њ–±–Њ–є—В–Є –Ј–∞—Й–Є—В—Г, –Ї–Њ—В–Њ—А—Г—О –Њ–њ—Г—Е–Њ–ї–Є –Є—Б–њ–Њ–ї—М–Ј—Г—О—В –і–ї—П –њ–Њ–і–∞–≤–ї–µ–љ–Є—П –Є–Љ–Љ—Г–љ–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л. –Ъ–∞–ґ–і–∞—П –Ј–∞—Й–Є—В–∞ –Є–Ј–≤–µ—Б—В–љ–∞ –Ї–∞–Ї –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ-–њ—А–Њ–њ—Г—Б–Ї–љ–Њ–є –њ—Г–љ–Ї—В. –Ъ–Њ–Љ–њ–ї–µ–Ї—Б–љ–∞—П —В–µ—А–∞–њ–Є—П —Б–Њ—З–µ—В–∞–µ—В –≤ —Б–µ–±–µ –∞–љ—В–Є—В–µ–ї–∞ –і–ї—П –њ–Њ–і–∞–≤–ї–µ–љ–Є—П –љ–µ—Б–Ї–Њ–ї—М–Ї–Є—Е –Ј–∞—Й–Є—В–љ—Л—Е —Б–ї–Њ–µ–≤. –Ш–Ј–≤–µ—Б—В–љ—Л–µ –Ї–Њ–љ—В—А–Њ–ї—М–љ—Л–µ —В–Њ—З–Ї–Є –≤–Ї–ї—О—З–∞—О—В CTLA-4, –љ–∞ –Ї–Њ—В–Њ—А—Л–є –≤–Њ–Ј–і–µ–є—Б—В–≤—Г–µ—В –Є–њ–Є–ї–Є–Љ—Г–Љ–∞–±, PD-1, –љ–∞ –Ї–Њ—В–Њ—А—Л–є –≤–Њ–Ј–і–µ–є—Б—В–≤—Г—О—В –љ–Є–≤–Њ–ї—Г–Љ–∞–± –Є –њ–µ–Љ–±—А–Њ–ї–Є–Ј—Г–Љ–∞–± , –∞ —В–∞–Ї–ґ–µ –Љ–Є–Ї—А–Њ–Њ–Ї—А—Г–ґ–µ–љ–Є–µ –Њ–њ—Г—Е–Њ–ї–Є. [20]
–Ю—Б–Њ–±–µ–љ–љ–Њ—Б—В–Є –Љ–Є–Ї—А–Њ–Њ–Ї—А—Г–ґ–µ–љ–Є—П –Њ–њ—Г—Е–Њ–ї–Є (TME) –њ—А–µ–і–Њ—В–≤—А–∞—Й–∞—О—В –њ—А–Є–≤–ї–µ—З–µ–љ–Є–µ –Ґ-–Ї–ї–µ—В–Њ–Ї –≤ –Њ–њ—Г—Е–Њ–ї—М. –Я—Г—В–Є –≤–Ї–ї—О—З–∞—О—В —Е–µ–Љ–Њ–Ї–Є–љ CCL 2 –љ–Є—В—А–Њ–≤–∞–љ–Є–µ, –Ї–Њ—В–Њ—А–Њ–µ –Ј–∞—Е–≤–∞—В—Л–≤–∞–µ—В –Ґ-–Ї–ї–µ—В–Ї–Є –≤ —Б—В—А–Њ–Љ–µ . -–Ї–ї–µ—В–Ї–Є, —З–∞—Б—В–Є—З–љ–Њ –Ј–∞ —Б—З–µ—В —Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Њ–є –і–ї—П —Н–љ–і–Њ—В–µ–ї–Є–∞–ї—М–љ—Л—Е –Ї–ї–µ—В–Њ–Ї (EC) —Н–Ї—Б–њ—А–µ—Б—Б–Є–Є FasL , ETBR –°–Њ—Б—Г–і–Є—Б—В–∞—П —Б–µ—В—М –Њ–њ—Г—Е–Њ–ї–Є –њ–Њ–Љ–Њ–≥–∞–µ—В –Њ–њ—Г—Е–Њ–ї—П–Љ –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ —А–µ–Ї—А—Г—В–Є—А–Њ–≤–∞—В—М –і—А—Г–≥–Є–µ –Є–Љ–Љ—Г–љ–љ—Л–µ –Ї–ї–µ—В–Ї–Є, –∞ –љ–µ –Ґ –Є B7H3. –Ь–Є–µ–ї–Њ–Љ–Њ–љ–Њ—Ж–Є—В–∞—А–љ—Л–µ –Є –Њ–њ—Г—Е–Њ–ї–µ–≤—Л–µ –Ї–ї–µ—В–Ї–Є –Љ–Њ–≥—Г—В –њ–Њ–≤—Л—И–∞—В—М —Н–Ї—Б–њ—А–µ—Б—Б–Є—О PD-L1 , —З—В–Њ —З–∞—Б—В–Є—З–љ–Њ –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–Њ –≥–Є–њ–Њ–Ї—Б–Є—З–µ—Б–Ї–Є–Љ–Є —Г—Б–ї–Њ–≤–Є—П–Љ–Є –Є –≤—Л—А–∞–±–Њ—В–Ї–Њ–є —Ж–Є—В–Њ–Ї–Є–љ–Њ–≤, —В–∞–Ї–Є—Е –Ї–∞–Ї IFNќ≤. –Р–±–µ—А—А–∞–љ—В–љ–Њ–µ –њ—А–Њ–Є–Ј–≤–Њ–і—Б—В–≤–Њ –Љ–µ—В–∞–±–Њ–ї–Є—В–Њ–≤ –≤ TME, —В–∞–Ї–Њ–µ –Ї–∞–Ї —А–µ–≥—Г–ї—П—Ж–Є—П –њ—Г—В–Є —Б –њ–Њ–Љ–Њ—Й—М—О IDO , –Љ–Њ–ґ–µ—В –≤–ї–Є—П—В—М –љ–∞ —Д—Г–љ–Ї—Ж–Є–Є –Ґ-–Ї–ї–µ—В–Њ–Ї –њ—А—П–Љ–Њ –Є–ї–Є –Ї–Њ—Б–≤–µ–љ–љ–Њ —З–µ—А–µ–Ј –Ї–ї–µ—В–Ї–Є, —В–∞–Ї–Є–µ –Ї–∞–Ї T- reg -–Ї–ї–µ—В–Ї–Є. –Ъ–ї–µ—В–Ї–Є CD8 –Љ–Њ–≥—Г—В –њ–Њ–і–∞–≤–ї—П—В—М—Б—П –Ј–∞ —Б—З–µ—В —А–µ–≥—Г–ї—П—Ж–Є–Є –Т-–Ї–ї–µ—В–Ї–∞–Љ–Є —Д–µ–љ–Њ—В–Є–њ–Њ–≤ –Ґ–Р–Ь. –°–≤—П–Ј–∞–љ–љ—Л–µ —Б —А–∞–Ї–Њ–Љ —Д–Є–±—А–Њ–±–ї–∞—Б—В—Л (CAF) –≤—Л–њ–Њ–ї–љ—П—О—В –Љ–љ–Њ–ґ–µ—Б—В–≤–Њ —Д—Г–љ–Ї—Ж–Є–є TME, –Њ—В—З–∞—Б—В–Є –Ј–∞ —Б—З–µ—В –Ј–∞—Е–≤–∞—В–∞ –Ґ-–Ї–ї–µ—В–Њ–Ї, –Њ–њ–Њ—Б—А–µ–і–Њ–≤–∞–љ–љ–Њ–≥–Њ –≤–љ–µ–Ї–ї–µ—В–Њ—З–љ—Л–Љ –Љ–∞—В—А–Є–Ї—Б–Њ–Љ (ECM), –Є –Є—Б–Ї–ї—О—З–µ–љ–Є—П –Ґ-–Ї–ї–µ—В–Њ–Ї, —А–µ–≥—Г–ї–Є—А—Г–µ–Љ–Њ–≥–Њ CXCL12 . [38]
–Ґ–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є–µ –∞–љ—В–Є—В–µ–ї–∞, –Њ–і–Њ–±—А–µ–љ–љ—Л–µ FDA
[ —А–µ–і–∞–Ї—В–Є—А–Њ–≤–∞—В—М ]–≠—В–Њ—В —А–∞–Ј–і–µ–ї –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –Њ–±–љ–Њ–≤–Є—В—М . ( –Љ–∞–є 2021 –≥. ) |
–Я–µ—А–≤—Л–Љ —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є–Љ –Љ–Њ–љ–Њ–Ї–ї–Њ–љ–∞–ї—М–љ—Л–Љ –∞–љ—В–Є—В–µ–ї–Њ–Љ, –Њ–і–Њ–±—А–µ–љ–љ—Л–Љ FDA, –±—Л–ї–Њ –Љ—Л—И–Є–љ–Њ–µ IgG2a CD3-—Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Њ–µ –ї–µ–Ї–∞—А—Б—В–≤–Њ –Њ—В –Њ—В—В–Њ—А–ґ–µ–љ–Є—П —В—А–∞–љ—Б–њ–ї–∞–љ—В–∞—В–∞ , OKT3 (—В–∞–Ї–ґ–µ –љ–∞–Ј—Л–≤–∞–µ–Љ–Њ–µ –Љ—Г—А–Њ–Љ–Њ–љ–∞–±–Њ–Љ), –≤ 1986 –≥–Њ–і—Г. –≠—В–Њ—В –њ—А–µ–њ–∞—А–∞—В –љ–∞—И–µ–ї –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ —Г —В—А–∞–љ—Б–њ–ї–∞–љ—В–∞—В–Њ–≤ —В–≤–µ—А–і—Л—Е –Њ—А–≥–∞–љ–Њ–≤ —А–µ—Ж–Є–њ–Є–µ–љ—В–Њ–≤ , –Ї–Њ—В–Њ—А—Л–µ —Б—В–∞–ї–Є —Г—Б—В–Њ–є—З–Є–≤—Л–Љ–Є –Ї —Б—В–µ—А–Њ–Є–і–∞–Љ . [39] –°–Њ—В–љ–Є –Љ–µ—В–Њ–і–Њ–≤ –ї–µ—З–µ–љ–Є—П –њ—А–Њ—Е–Њ–і—П—В –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ –Є—Б–њ—Л—В–∞–љ–Є—П . –С–Њ–ї—М—И–Є–љ—Б—В–≤–Њ –Є–Ј –љ–Є—Е –Ї–∞—Б–∞—О—В—Б—П –Є–Љ–Љ—Г–љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –Є –Њ–љ–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е —Ж–µ–ї–µ–є.
–Ґ–Њ–Ј–Є—В—Г–Љ–Њ–Љ–∞–± вАУ –°–њ—А–µ–є вАУ 2003 вАУ CD20
–Ь–Њ–≥–∞–Љ—Г–ї–Є–Ј—Г–Љ–∞–± вАУ –≤ –±—Г—В—Л–ї–Ї–∞—Е вАУ –∞–≤–≥—Г—Б—В 2018 –≥. вАУ CCR4
–Ь–Њ–Ї—Б–µ—В—Г–Љ–Њ–Љ–∞–± –њ–∞—Б—Г–і–Њ—В–Њ–Ї—Б вАУ –Ы—О–Љ–Њ–Ї—Б–Є—В–Є вАУ —Б–µ–љ—В—П–±—А—М 2018 –≥. вАУ CD22
–¶–µ–Љ–Є–њ–ї–Є–Љ–∞–± вАУ –Ы–Є–±—В–∞–є–Њ вАУ —Б–µ–љ—В—П–±—А—М 2018 –≥. вАУ PD-1
–Я–Њ–ї–∞—В—Г–Ј—Г–Љ–∞–± –≤–µ–і–Њ—В–Є–љ вАУ Polivy вАУ –Є—О–љ—М 2019 –≥. вАУ CD79B
–С–Є—Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Є–µ –∞–љ—В–Є—В–µ–ї–∞ –і–∞–ї–Є –Љ–љ–Њ–≥–Њ–Њ–±–µ—Й–∞—О—Й–Є–µ —А–µ–Ј—Г–ї—М—В–∞—В—Л –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б–њ—Л—В–∞–љ–Є—П—Е. –Т –∞–њ—А–µ–ї–µ 2009 –≥–Њ–і–∞ –±–Є—Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Њ–µ –∞–љ—В–Є—В–µ–ї–Њ –Ї–∞—В—Г–Љ–∞–Ї—Б–Њ–Љ–∞–± –±—Л–ї–Њ –Њ–і–Њ–±—А–µ–љ–Њ –≤ –Х–≤—А–Њ–њ–µ–є—Б–Ї–Њ–Љ –°–Њ—О–Ј–µ. [40] [41]
–≠–Ї–Њ–љ–Њ–Љ–Є–Ї–∞
[ —А–µ–і–∞–Ї—В–Є—А–Њ–≤–∞—В—М ]–° 2000 –≥–Њ–і–∞ —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є–є —А—Л–љ–Њ–Ї –Љ–Њ–љ–Њ–Ї–ї–Њ–љ–∞–ї—М–љ—Л—Е –∞–љ—В–Є—В–µ–ї –≤—Л—А–Њ—Б –≤ –≥–µ–Њ–Љ–µ—В—А–Є—З–µ—Б–Ї–Њ–є –њ—А–Њ–≥—А–µ—Б—Б–Є–Є. –Т 2006 –≥–Њ–і—Г ¬Ђ–±–Њ–ї—М—И–∞—П –њ—П—В–µ—А–Ї–∞¬ї —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є—Е –∞–љ—В–Є—В–µ–ї –љ–∞ —А—Л–љ–Ї–µ –≤–Ї–ї—О—З–∞–ї–∞ –±–µ–≤–∞—Ж–Є–Ј—Г–Љ–∞–± , —В—А–∞—Б—В—Г–Ј—Г–Љ–∞–± (–Њ–±–∞ –Њ–љ–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ), –∞–і–∞–ї–Є–Љ—Г–Љ–∞–± , –Є–љ—Д–ї–Є–Ї—Б–Є–Љ–∞–± (–Ї–∞–Ї –∞—Г—В–Њ–Є–Љ–Љ—Г–љ–љ—Л–µ, —В–∞–Ї –Є –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П , ¬Ђ–Р–Т–Ч¬ї) –Є —А–Є—В—Г–Ї—Б–Є–Љ–∞–± (–Њ–љ–Ї–Њ–ї–Њ–≥–Є—П –Є –Ю–Ш–Ш–Ч), –љ–∞ –і–Њ–ї—О –Ї–Њ—В–Њ—А—Л—Е –њ—А–Є—Е–Њ–і–Є–ї–Њ—Б—М 80% –і–Њ—Е–Њ–і–Њ–≤ –≤ 2006 –≥–Њ–і—Г. 2006. –Т 2007 –≥–Њ–і—Г –≤–Њ—Б–µ–Љ—М –Є–Ј 20 —Б–∞–Љ—Л—Е –њ—А–Њ–і–∞–≤–∞–µ–Љ—Л—Е –±–Є–Њ—В–µ—Е–љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –≤ –°–®–Р –њ—А–µ–і—Б—В–∞–≤–ї—П–ї–Є —Б–Њ–±–Њ–є —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є–µ –Љ–Њ–љ–Њ–Ї–ї–Њ–љ–∞–ї—М–љ—Л–µ –∞–љ—В–Є—В–µ–ї–∞. [42] –≠—В–Њ—В –±—Л—Б—В—А—Л–є —А–Њ—Б—В —Б–њ—А–Њ—Б–∞ –љ–∞ –њ—А–Њ–Є–Ј–≤–Њ–і—Б—В–≤–Њ –Љ–Њ–љ–Њ–Ї–ї–Њ–љ–∞–ї—М–љ—Л—Е –∞–љ—В–Є—В–µ–ї —Е–Њ—А–Њ—И–Њ —Б–Њ—З–µ—В–∞–µ—В—Б—П —Б –Є–љ–і—Г—Б—В—А–Є–∞–ї–Є–Ј–∞—Ж–Є–µ–є –њ—А–Њ–Є–Ј–≤–Њ–і—Б—В–≤–∞ –Љ–Њ–љ–Њ–Ї–ї–Њ–љ–∞–ї—М–љ—Л—Е –∞–љ—В–Є—В–µ–ї. [43]
–°—Б—Л–ї–Ї–Є
[ —А–µ–і–∞–Ї—В–Є—А–Њ–≤–∞—В—М ]- ^ –Я–µ—А–µ–є—В–Є –Њ–±—А–∞—В–љ–Њ: –∞ –± –ѓ–Њ –°., –І–ґ—Г –Ѓ, –І–µ–љ –Ы. (—Д–µ–≤—А–∞–ї—М 2013 –≥.). ¬Ђ–Ф–Њ—Б—В–Є–ґ–µ–љ–Є—П –≤ –љ–∞—Ж–µ–ї–Є–≤–∞–љ–Є–Є –љ–∞ —Б–Є–≥–љ–∞–ї—М–љ—Л–µ –Љ–Њ–ї–µ–Ї—Г–ї—Л –Ї–ї–µ—В–Њ—З–љ–Њ–є –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є –і–ї—П –Є–Љ–Љ—Г–љ–љ–Њ–є –Љ–Њ–і—Г–ї—П—Ж–Є–Є¬ї . –Ю–±–Ј–Њ—А—Л –њ—А–Є—А–Њ–і—Л. –Ю—В–Ї—А—Л—В–Є–µ –љ–∞—А–Ї–Њ—В–Є–Ї–Њ–≤ . 12 (2): 130вАУ146. –і–Њ–Є : 10.1038/nrd3877 . –Я–Ь–¶ ¬† 3698571 . –Я–Ь–Ш–Ф ¬† 23370250 .
- ^ –Ф–ґ–µ–є–љ–≤–µ–є, –І–∞—А–ї—М–Ј ; –Я–Њ–ї –Ґ—А—Н–≤–µ—А—Б; –Ь–∞—А–Ї –£–Њ–ї–њ–Њ—А—В; –Ь–∞—А–Ї –®–ї–Њ–Љ—З–Є–Ї (2001). –Ш–Љ–Љ—Г–љ–Њ–±–Є–Њ–ї–Њ–≥–Є—П; –Я—П—В–Њ–µ –Є–Ј–і–∞–љ–Є–µ . –Э—М—О-–Щ–Њ—А–Ї –Є –Ы–Њ–љ–і–Њ–љ: Garland Science. ISBN ¬†978-0-8153-4101-7 .
- ^ –Я–µ—А–µ–є—В–Є –Њ–±—А–∞—В–љ–Њ: –∞ –± –Ф–ґ–µ–є–љ–≤–µ–є –Ъ–∞–ї–Є—Д–Њ—А–љ–Є—П –Љ–ї. ; –Є –і—А. (2005). –Ш–Љ–Љ—Г–љ–Њ–±–Є–Њ–ї–Њ–≥–Є—П (6-–µ –Є–Ј–і.). –У–Є—А–ї—П–љ–і–љ–∞—П –љ–∞—Г–Ї–∞. ISBN ¬†978-0-443-07310-6 .
- ^ –Я–µ—А–µ–є—В–Є –Њ–±—А–∞—В–љ–Њ: –∞ –± –С–∞–Ї—Б—В–µ—А –Ф. (–і–µ–Ї–∞–±—А—М 2007 –≥.). ¬Ђ–Р–Ї—В–Є–≤–љ—Л–є –Є –њ–∞—Б—Б–Є–≤–љ—Л–є –Є–Љ–Љ—Г–љ–Є—В–µ—В, —В–Є–њ—Л –≤–∞–Ї—Ж–Є–љ, –≤—Б–њ–Њ–Љ–Њ–≥–∞—В–µ–ї—М–љ—Л–µ –≤–µ—Й–µ—Б—В–≤–∞ –Є –ї–Є—Ж–µ–љ–Ј–Є—А–Њ–≤–∞–љ–Є–µ¬ї . –Я—А–Њ—Д–µ—Б—Б–Є–Њ–љ–∞–ї—М–љ–∞—П –Љ–µ–і–Є—Ж–Є–љ–∞ . 57 (8): 552вАУ556. doi : 10.1093/ocmed/kqm110 . –Я–Ь–Ш–Ф ¬† 18045976 .
- ^ –Ш–Ј–Љ–µ–љ–µ–љ–Њ –Є–Ј –Ъ–∞—А—В–µ—А –Я. (–љ–Њ—П–±—А—М 2001 –≥.). ¬Ђ–Я–Њ–≤—Л—И–µ–љ–Є–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –ї–µ—З–µ–љ–Є—П —А–∞–Ї–∞ –љ–∞ –Њ—Б–љ–Њ–≤–µ –∞–љ—В–Є—В–µ–ї¬ї. –Ю–±–Ј–Њ—А—Л –њ—А–Є—А–Њ–і—Л. –†–∞–Ї . 1 (2): 118вАУ129. –і–Њ–Є : 10.1038/35101072 . –Я–Ь–Ш–Ф ¬† 11905803 . S2CID ¬† 10169378 .
- ^ –С—А–Є–і–≤–µ–ї–і (—Д–µ–≤—А–∞–ї—М 2000 –≥.). ¬Ђ–Ґ–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є–µ –Љ–Њ–љ–Њ–Ї–ї–Њ–љ–∞–ї—М–љ—Л–µ –∞–љ—В–Є—В–µ–ї–∞¬ї. –Ы–∞–љ—Ж–µ—В . 355 (9205): 735вАУ740. –і–Њ–Є : 10.1016/S0140-6736(00)01034-5 . –Я–Ь–Ш–Ф ¬† 10703815 . S2CID ¬† 43781004 .
- ^ –Ъ—С–ї–µ—А –У., –Ь–Є–ї—М—И—В–µ–є–љ –°. (–∞–≤–≥—Г—Б—В 1975 –≥.). ¬Ђ–Э–µ–њ—А–µ—А—Л–≤–љ—Л–µ –Ї—Г–ї—М—В—Г—А—Л —Б–ї–Є—В—Л—Е –Ї–ї–µ—В–Њ–Ї, —Б–µ–Ї—А–µ—В–Є—А—Г—О—Й–Є—Е –∞–љ—В–Є—В–µ–ї–∞ –Ј–∞–і–∞–љ–љ–Њ–є —Б–њ–µ—Ж–Є—Д–Є—З–љ–Њ—Б—В–Є¬ї. –Я—А–Є—А–Њ–і–∞ . 256 (5517): 495вАУ497. –С–Є–±–Ї–Њ–і : 1975Natur.256..495K . –і–Њ–Є : 10.1038/256495a0 . –Я–Ь–Ш–Ф ¬† 1172191 . S2CID ¬† 4161444 .
- ^ –Э–∞–і–ї–µ—А –Ы.–Ь., –°—В–∞—И–µ–љ–Ї–Њ –Я., –•–∞—А–і–Є –†., –Ъ–∞–њ–ї–∞–љ –Т.–Ф., –С–∞—В—В–Њ–љ –Ы.–Э., –Ъ—Г—Д–µ –Ф.–Т. –Є –і—А. (—Б–µ–љ—В—П–±—А—М 1980 –≥.). ¬Ђ–°–µ—А–Њ—В–µ—А–∞–њ–Є—П –њ–∞—Ж–Є–µ–љ—В–∞ –Љ–Њ–љ–Њ–Ї–ї–Њ–љ–∞–ї—М–љ—Л–Љ –∞–љ—В–Є—В–µ–ї–Њ–Љ, –љ–∞–њ—А–∞–≤–ї–µ–љ–љ—Л–Љ –њ—А–Њ—В–Є–≤ –∞–љ—В–Є–≥–µ–љ–∞, –∞—Б—Б–Њ—Ж–Є–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ —Б –ї–Є–Љ—Д–Њ–Љ–Њ–є —З–µ–ї–Њ–≤–µ–Ї–∞¬ї. –Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —А–∞–Ї–∞ . 40 (9): 3147вАУ3154. –Я–Ь–Ш–Ф ¬† 7427932 .
- ^ –†–Є—В—Ж –Ф–ґ., –®–ї–Њ—Б—Б–Љ–∞–љ –°.–§. (—П–љ–≤–∞—А—М 1982 –≥.). ¬Ђ–Ш—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –Љ–Њ–љ–Њ–Ї–ї–Њ–љ–∞–ї—М–љ—Л—Е –∞–љ—В–Є—В–µ–ї –≤ –ї–µ—З–µ–љ–Є–Є –ї–µ–є–Ї–Њ–Ј–Њ–≤ –Є –ї–Є–Љ—Д–Њ–Љ¬ї . –Ъ—А–Њ–≤—М . 59 (1): 1вАУ11. –і–Њ–Є : 10.1182/blood.V59.1.1.1 . –Я–Ь–Ш–Ф ¬† 7032624 .
- ^ –Я–µ—А–µ–є—В–Є –Њ–±—А–∞—В–љ–Њ: –∞ –± —Б –°—В–µ—А–љ –Ь., –•–µ—А—А–Љ–∞–љ–љ –†. (–∞–њ—А–µ–ї—М 2005 –≥.). ¬Ђ–Ю–±–Ј–Њ—А –Љ–Њ–љ–Њ–Ї–ї–Њ–љ–∞–ї—М–љ—Л—Е –∞–љ—В–Є—В–µ–ї –≤ —В–µ—А–∞–њ–Є–Є —А–∞–Ї–∞: –љ–∞—Б—В–Њ—П—Й–µ–µ –Є –њ–µ—А—Б–њ–µ–Ї—В–Є–≤–љ–Њ–µ¬ї. –Ъ—А–Є—В–Є—З–µ—Б–Ї–Є–µ –Њ–±–Ј–Њ—А—Л –њ–Њ –Њ–љ–Ї–Њ–ї–Њ–≥–Є–Є/–≥–µ–Љ–∞—В–Њ–ї–Њ–≥–Є–Є . 54 (1): 11вАУ29. –і–Њ–Є : 10.1016/j.critrevonc.2004.10.011 . –Я–Ь–Ш–Ф ¬† 15780905 .
- ^ –Я–µ—А–µ–є—В–Є –Њ–±—А–∞—В–љ–Њ: –∞ –± —Б –•–∞–і—Б–Њ–љ –Я.–Ф–ґ., –°—Г—А–Є–Њ –°. (—П–љ–≤–∞—А—М 2003 –≥.). ¬Ђ–Ш–љ–ґ–µ–љ–µ—А–љ—Л–µ –∞–љ—В–Є—В–µ–ї–∞¬ї. –Я—А–Є—А–Њ–і–љ–∞—П –Љ–µ–і–Є—Ж–Є–љ–∞ . 9 (1): 129вАУ134. –і–Њ–Є : 10.1038/nm0103-129 . –Я–Ь–Ш–Ф ¬† 12514726 . S2CID ¬† 19243664 .
- ^ –Ъ–∞—А—В–µ—А –Я., –Я—А–µ—Б—В–∞ –Ы., –У–Њ—А–Љ–∞–љ –°.–Ь., –†–Є–і–ґ—Г—Н–є –Ф–ґ.–С., –•–µ–љ–љ–µ—А –Ф., –Т–Њ–љ–≥ –Т.–Ы. –Є –і—А. (–Љ–∞–є 1992 –≥.). ¬Ђ–У—Г–Љ–∞–љ–Є–Ј–∞—Ж–Є—П –∞–љ—В–Є—В–µ–ї–∞ –њ—А–Њ—В–Є–≤ p185HER2 –і–ї—П —В–µ—А–∞–њ–Є–Є —А–∞–Ї–∞ —З–µ–ї–Њ–≤–µ–Ї–∞¬ї . –Ґ—А—Г–і—Л –Э–∞—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–є –∞–Ї–∞–і–µ–Љ–Є–Є –љ–∞—Г–Ї –°–Њ–µ–і–Є–љ–µ–љ–љ—Л—Е –®—В–∞—В–Њ–≤ –Р–Љ–µ—А–Є–Ї–Є . 89 (10): 4285вАУ4289. –С–Є–±–Ї–Њ–і : 1992PNAS...89.4285C . –і–Њ–Є : 10.1073/pnas.89.10.4285 . –Я–Ь–Ъ ¬† 49066 . –Я–Ь–Ш–Ф ¬† 1350088 .
- ^ –Я—А–µ—Б—В–∞ –Ы.–У., –Ы–∞—А –°.–Ф–ґ., –®–Є–ї–і—Б –†.–Ы., –Я–Њ—А—В–µ—А –Ф–ґ.–Я., –У–Њ—А–Љ–∞–љ –Ъ.–Ь., –§–µ–љ–і–ї–Є –С.–Ь., –Ц–∞—А–і—М–µ –Я.–Ь. (—Б–µ–љ—В—П–±—А—М 1993 –≥.). ¬Ђ–У—Г–Љ–∞–љ–Є–Ј–∞—Ж–Є—П –∞–љ—В–Є—В–µ–ї–∞, –љ–∞–њ—А–∞–≤–ї–µ–љ–љ–Њ–≥–Њ –њ—А–Њ—В–Є–≤ IgE¬ї . –Ц—Г—А–љ–∞–ї –Є–Љ–Љ—Г–љ–Њ–ї–Њ–≥–Є–Є . 151 (5): 2623вАУ2632. –і–Њ–Є : 10.4049/jimmunol.151.5.2623 . –Я–Ь–Ш–Ф ¬† 8360482 . S2CID ¬† 904440 .
- ^ –І–Њ—В–Є—П –°., –Ы–µ—Б–Ї –Р.–Ь., –Ґ—А–∞–Љ–Њ–љ—В–∞–љ–Њ –Р., –Ы–µ–≤–Є—В—В –Ь., –°–Љ–Є—В-–У–Є–ї–ї –°.–Ф–ґ., –≠–є—А –Ф–ґ. –Є –і—А. (1989). ¬Ђ–Ъ–Њ–љ—Д–Њ—А–Љ–∞—Ж–Є–Є –≥–Є–њ–µ—А–≤–∞—А–Є–∞–±–µ–ї—М–љ—Л—Е –Њ–±–ї–∞—Б—В–µ–є –Є–Љ–Љ—Г–љ–Њ–≥–ї–Њ–±—Г–ї–Є–љ–∞¬ї. –Я—А–Є—А–Њ–і–∞ . 342 (6252): 877вАУ883. –С–Є–±–Ї–Њ–і : 1989Natur.342..877C . –і–Њ–Є : 10.1038/342877a0 . –Я–Ь–Ш–Ф ¬† 2687698 . S2CID ¬† 4241051 .
- ^ –Т–∞–ї—М–і–Љ–∞–љ–љ –Ґ.–Р. (–Љ–∞—А—В 2003 –≥.). ¬Ђ–Ш–Љ–Љ—Г–љ–Њ—В–µ—А–∞–њ–Є—П: –њ—А–Њ—И–ї–Њ–µ, –љ–∞—Б—В–Њ—П—Й–µ–µ –Є –±—Г–і—Г—Й–µ–µ¬ї . –Я—А–Є—А–Њ–і–љ–∞—П –Љ–µ–і–Є—Ж–Є–љ–∞ . 9 (3): 269вАУ277. –і–Њ–Є : 10.1038/nm0303-269 . –Я–Ь–Ш–Ф ¬† 12612576 . S2CID ¬† 9745527 .
- ^ –Ф–ґ–µ—Д—Д–µ—А–Є—Б –†., —З–ї–µ–љ –њ–∞—А–ї–∞–Љ–µ–љ—В–∞ –Њ—В –Ы–µ—Д—А–∞–љ–Ї–∞ (–Є—О–ї—М вАУ –∞–≤–≥—Г—Б—В 2009 –≥.). ¬Ђ–Р–ї–ї–Њ—В–Є–њ—Л –Є–Љ–Љ—Г–љ–Њ–≥–ї–Њ–±—Г–ї–Є–љ–Њ–≤ —З–µ–ї–Њ–≤–µ–Ї–∞: –≤–Њ–Ј–Љ–Њ–ґ–љ—Л–µ –њ–Њ—Б–ї–µ–і—Б—В–≤–Є—П –і–ї—П –Є–Љ–Љ—Г–љ–Њ–≥–µ–љ–љ–Њ—Б—В–Є¬ї . –Ь–Р–С . 1 (4): 332вАУ338. –і–Њ–Є : 10.4161/mabs.1.4.9122 . –Я–Ь–Ъ ¬† 2726606 . –Я–Ь–Ш–Ф ¬† 20073133 .
- ^ –І–µ–њ–Љ–µ–љ –Ъ., –Я—Г–ї–ї–µ–љ –Э., –Ъ–Њ–љ–Є –Ы., –Ф–µ–Љ–њ—Б—В–µ—А –Ь., –≠–љ–і—А—О—Б –Ы., –С–∞–є—А–∞–Љ–Њ–≤–Є—З –Ф–ґ. –Є –і—А. (2009). ¬Ђ–Ф–Њ–Ї–ї–Є–љ–Є—З–µ—Б–Ї–∞—П —А–∞–Ј—А–∞–±–Њ—В–Ї–∞ –Љ–Њ–љ–Њ–Ї–ї–Њ–љ–∞–ї—М–љ—Л—Е –∞–љ—В–Є—В–µ–ї: —Б–Њ–Њ–±—А–∞–ґ–µ–љ–Є—П –њ–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—О –њ—А–Є–Љ–∞—В–Њ–≤, –Ї—А–Њ–Љ–µ —З–µ–ї–Њ–≤–µ–Ї–∞¬ї . –Ь–Р–С . 1 (5): 505вАУ516. –і–Њ–Є : 10.4161/mabs.1.5.9676 . –Я–Ь–Ъ ¬† 2759500 . –Я–Ь–Ш–Ф ¬† 20065651 .
- ^ –Т–µ–љ–љ–µ–њ—Г—А–µ–і–і–Є –Р., –°–Є–љ–≥—Е –Я., –†–∞—Б—В–Њ–≥–Є –†., –Р—В–∞–ї–ї–∞—Е –Ф–ґ. –Я., –Ґ–µ—А–і–ґ–∞–љ—П–љ –Ґ. (–Њ–Ї—В—П–±—А—М 2017 –≥.). ¬Ђ–≠–≤–Њ–ї—О—Ж–Є—П —А–∞–Љ—Г—Ж–Є—А—Г–Љ–∞–±–∞ –≤ –ї–µ—З–µ–љ–Є–Є —А–∞–Ї–∞ - –Њ–±–Ј–Њ—А –ї–Є—В–µ—А–∞—В—Г—А—Л¬ї. –Ц—Г—А–љ–∞–ї –Њ–љ–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –∞–њ—В–µ—З–љ–Њ–є –њ—А–∞–Ї—В–Є–Ї–Є . 23 (7): 525вАУ539. –і–Њ–Є : 10.1177/1078155216655474 . –Я–Ь–Ш–Ф ¬† 27306885 . S2CID ¬† 21298489 .
- ^ –і–µ –¶–≤–∞—А—В –Т., –У–Њ—Г –°–Ъ, –Ь–µ–є–µ—А-–Т–µ–љ—В—А—Г–њ –§.–Р. (—П–љ–≤–∞—А—М 2016 –≥.). ¬Ђ–Ґ–µ—А–∞–њ–Є—П –∞–љ—В–Є—В–µ–ї–∞–Љ–Є –њ—А–Є –ї–Є–Љ—Д–Њ–Љ–∞—Е —Г –і–µ—В–µ–є¬ї . –Ъ–Њ–Ї—А–∞–љ–Њ–≤—Б–Ї–∞—П –±–∞–Ј–∞ –і–∞–љ–љ—Л—Е —Б–Є—Б—В–µ–Љ–∞—В–Є—З–µ—Б–Ї–Є—Е –Њ–±–Ј–Њ—А–Њ–≤ . 2016 (1): CD011181. –і–Њ–Є : 10.1002/14651858.cd011181.pub2 . –Я–Ь–Ъ ¬† 8719646 . –Я–Ь–Ш–Ф ¬† 26784573 .
- ^ –Я–µ—А–µ–є—В–Є –Њ–±—А–∞—В–љ–Њ: –∞ –± –®–∞—А–Љ–∞ –Я., –≠–ї–ї–Є—Б–Њ–љ –Ф–ґ.–Я. (–∞–њ—А–µ–ї—М 2015 –≥.). ¬Ђ–С—Г–і—Г—Й–µ–µ —В–µ—А–∞–њ–Є–Є –Є–Љ–Љ—Г–љ–љ—Л—Е –Ї–Њ–љ—В—А–Њ–ї—М–љ—Л—Е —В–Њ—З–µ–Ї¬ї. –Э–∞—Г–Ї–∞ . 348 (6230): 56вАУ61. –С–Є–±–Ї–Њ–і : 2015Sci...348...56S . –і–Њ–Є : 10.1126/science.aaa8172 . –Я–Ь–Ш–Ф ¬† 25838373 . S2CID ¬† 4608450 .
- ^ –Ф–µ–Љ–њ–Ї–µ –Т.–Ъ., –§–µ–љ—З–µ–ї –Ъ., –£—Ж–µ—Е–Њ–≤—Б–Ї–Є –Я., –Ф–µ–є–ї –°.–Я. (–Љ–∞—А—В 2017 –≥.). ¬Ђ–Я—А–µ–њ–∞—А–∞—В—Л –≤—В–Њ—А–Њ–≥–Њ –Є —В—А–µ—В—М–µ–≥–Њ –њ–Њ–Ї–Њ–ї–µ–љ–Є—П –і–ї—П –ї–µ—З–µ–љ–Є—П –Є–Љ–Љ—Г–љ–Њ–Њ–љ–Ї–Њ–ї–Њ–≥–Є–Є. –І–µ–Љ –±–Њ–ї—М—И–µ, —В–µ–Љ –ї—Г—З—И–µ?¬ї. –Х–≤—А–Њ–њ–µ–є—Б–Ї–Є–є –ґ—Г—А–љ–∞–ї —А–∞–Ї–∞ . 74 : 55вАУ72. –і–Њ–Є : 10.1016/j.ejca.2017.01.001 . –Я–Ь–Ш–Ф ¬† 28335888 .
- ^ –Я–µ—А–µ–є—В–Є –Њ–±—А–∞—В–љ–Њ: –∞ –± –†–∞–љ–≥, HP (2003). –§–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є—П . –≠–і–Є–љ–±—Г—А–≥: –І–µ—А—З–Є–ї–ї—М –Ы–Є–≤–Є–љ–≥—Б—В–Њ–љ. –њ. 241. –Ш–°–С–Э ¬†978-0-443-07145-4 .
- ^ –Я–µ—А–µ–є—В–Є –Њ–±—А–∞—В–љ–Њ: –∞ –± –Я—Г–ї –†., –Ф–Њ–і–µ–ї—М –†., –°—В–∞–љ–≥–µ–ї—М –Ь. (–Љ–∞—А—В 2011 –≥.). ¬Ђ–Ґ–µ—А–∞–њ–Є—П –љ–∞ –Њ—Б–љ–Њ–≤–µ –∞–љ—В–Є—В–µ–ї –њ—А–Є –±–Њ–ї–µ–Ј–љ–Є –Р–ї—М—Ж–≥–µ–є–Љ–µ—А–∞¬ї. –≠–Ї—Б–њ–µ—А—В–љ–Њ–µ –Љ–љ–µ–љ–Є–µ –Њ –±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є —В–µ—А–∞–њ–Є–Є . 11 (3): 343вАУ357. –і–Њ–Є : 10.1517/14712598.2011.552884 . –Я–Ь–Ш–Ф ¬† 21261567 . S2CID ¬† 19375883 .
- ^ –Я–µ—А–µ–є—В–Є –Њ–±—А–∞—В–љ–Њ: –∞ –± —Б –і –≤–∞–љ –Ф–µ–є–Ї CH (—Д–µ–≤—А–∞–ї—М 2018 –≥.). ¬Ђ–Ь–Њ–љ–Њ–Ї–ї–Њ–љ–∞–ї—М–љ—Л–µ –∞–љ—В–Є—В–µ–ї–∞ –Ї ќ≤-–∞–Љ–Є–ї–Њ–Є–і—Г –њ—А–Є –±–Њ–ї–µ–Ј–љ–Є –Р–ї—М—Ж–≥–µ–є–Љ–µ—А–∞: –њ–Њ–і–≤–Њ–і–љ—Л–µ –Ї–∞–Љ–љ–Є –Є –њ–µ—А—Б–њ–µ–Ї—В–Є–≤—Л¬ї . –С–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–∞—П –њ—Б–Є—Е–Є–∞—В—А–Є—П . 83 (4): 311вАУ319. doi : 10.1016/j.biopsych.2017.08.010 . –Я–Ь–¶ ¬† 5767539 . –Я–Ь–Ш–Ф ¬† 28967385 .
- ^ –Я–µ—А–µ–є—В–Є –Њ–±—А–∞—В–љ–Њ: –∞ –± —Б –і –Є –У–Њ X, –ѓ–љ –Ы, –І–ґ–∞–љ –Ф, –І–ґ–∞–Њ –Ѓ (—Д–µ–≤—А–∞–ї—М 2024 –≥.). ¬Ђ–Я–∞—Б—Б–Є–≤–љ–∞—П –Є–Љ–Љ—Г–љ–Њ—В–µ—А–∞–њ–Є—П –±–Њ–ї–µ–Ј–љ–Є –Р–ї—М—Ж–≥–µ–є–Љ–µ—А–∞¬ї . –Ю–±–Ј–Њ—А—Л –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є —Б—В–∞—А–µ–љ–Є—П . 94 : 102192. doi : 10.1016/j.arr.2024.102192 . –Я–Ь–Ш–Ф ¬† 38219962 .
- ^ –Я–µ—А–µ–є—В–Є –Њ–±—А–∞—В–љ–Њ: –∞ –± —Б –і –Я–∞–љ—Ж–∞ –§, –°–Њ–ї—Д—А–Є—Ж—Ж–Є –Т, –Ш–Љ–±–Є–Љ–±–Њ –С.–Я., –Ы–Њ–≥—А–Њ—Б—Ж–Є–љ–Њ –У (–Њ–Ї—В—П–±—А—М 2014 –≥.). ¬Ђ–Р–Љ–Є–ї–Њ–Є–і-–љ–∞–њ—А–∞–≤–ї–µ–љ–љ—Л–µ –Љ–Њ–љ–Њ–Ї–ї–Њ–љ–∞–ї—М–љ—Л–µ –∞–љ—В–Є—В–µ–ї–∞ –і–ї—П –ї–µ—З–µ–љ–Є—П –±–Њ–ї–µ–Ј–љ–Є –Р–ї—М—Ж–≥–µ–є–Љ–µ—А–∞: —В–Њ—З–Ї–∞ –љ–µ–≤–Њ–Ј–≤—А–∞—В–∞?¬ї. –≠–Ї—Б–њ–µ—А—В–љ–Њ–µ –Љ–љ–µ–љ–Є–µ –Њ –±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є —В–µ—А–∞–њ–Є–Є . 14 (10): 1465вАУ1476. –і–Њ–Є : 10.1517/14712598.2014.935332 . –Я–Ь–Ш–Ф ¬† 24981190 . S2CID ¬† 26323381 .
- ^ –≤–∞–љ –Ф–µ–є–Ї CH (—Д–µ–≤—А–∞–ї—М 2018 –≥.). ¬Ђ–Ь–Њ–љ–Њ–Ї–ї–Њ–љ–∞–ї—М–љ—Л–µ –∞–љ—В–Є—В–µ–ї–∞ –Ї ќ≤-–∞–Љ–Є–ї–Њ–Є–і—Г –њ—А–Є –±–Њ–ї–µ–Ј–љ–Є –Р–ї—М—Ж–≥–µ–є–Љ–µ—А–∞: –њ–Њ–і–≤–Њ–і–љ—Л–µ –Ї–∞–Љ–љ–Є –Є –њ–µ—А—Б–њ–µ–Ї—В–Є–≤—Л¬ї . –С–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–∞—П –њ—Б–Є—Е–Є–∞—В—А–Є—П . 83 (4): 311вАУ319. doi : 10.1016/j.biopsych.2017.08.010 . –Я–Ь–¶ ¬† 5767539 . –Я–Ь–Ш–Ф ¬† 28967385 .
- ^ –У–Њ—Н–ї, –Р—О—И (20 –∞–≤–≥—Г—Б—В–∞ 2013 –≥.). ¬Ђ–Т–∞–Ј–Њ–≥–µ–љ–љ—Л–є –Њ—В–µ–Ї –≥–Њ–ї–Њ–≤–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞¬ї . Radiopaedia.org . –Я—А–Њ–≤–µ—А–µ–љ–Њ 1 –љ–Њ—П–±—А—П 2017 –≥.
- ^ –Я–µ—А–µ–є—В–Є –Њ–±—А–∞—В–љ–Њ: –∞ –± –Я–∞–љ—Б–∞ –§., –§—А–Є—Б–∞—А–і–Є –Т., –Ш–Љ–±–Є–Љ–±–Њ –С.–Я., –Ф'–Ю–љ–Њ—Д—А–Є–Њ –Ф–ґ., –Я—М–µ—В—А–∞—А–Њ—Б—Б–∞ –Ф–ґ., –°–µ—А–Є–њ–∞ –Ф. –Є –і—А. (–љ–Њ—П–±—А—М 2010 –≥.). ¬Ђ–С–∞–њ–Є–љ–µ–Ј—Г–Љ–∞–±: –Љ–Њ–љ–Њ–Ї–ї–Њ–љ–∞–ї—М–љ—Л–µ –∞–љ—В–Є—В–µ–ї–∞ –њ—А–Њ—В–Є–≤ ќ≤-–∞–Љ–Є–ї–Њ–Є–і–∞ –і–ї—П –ї–µ—З–µ–љ–Є—П –±–Њ–ї–µ–Ј–љ–Є –Р–ї—М—Ж–≥–µ–є–Љ–µ—А–∞¬ї. –Ш–Љ–Љ—Г–љ–Њ—В–µ—А–∞–њ–Є—П . 2 (6): 767вАУ782. –і–Њ–Є : 10.2217/–Є–Љ—В.10.80 . –Я–Ь–Ш–Ф ¬† 21091109 .
- ^ –°–њ–µ—А–ї–Є–љ–≥ –†.–Р., –Ф–Њ–љ–Њ—Е—М—О –Ь.–°., –†–∞–Љ–∞–љ –†., –†–∞—Д–Є–Є –Ь.–°., –Ф–ґ–Њ–љ—Б–Њ–љ –Ъ., –Ь–∞—Б—В–µ—А—Б –Ъ.–Ы. –Є –і—А. (—Б–µ–љ—В—П–±—А—М 2023 –≥.). ¬Ђ–Ш—Б–њ—Л—В–∞–љ–Є–µ —Б–Њ–ї–∞–љ–µ–Ј—Г–Љ–∞–±–∞ –њ—А–Є –і–Њ–Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є —Б—В–∞–і–Є–Є –±–Њ–ї–µ–Ј–љ–Є –Р–ї—М—Ж–≥–µ–є–Љ–µ—А–∞¬ї . –Ь–µ–і–Є—Ж–Є–љ—Б–Ї–Є–є –ґ—Г—А–љ–∞–ї –Э–Њ–≤–Њ–є –Р–љ–≥–ї–Є–Є . 389 (12): 1096вАУ1107. –і–Њ–Є : 10.1056/NEJMoa2305032 . –Я–Ь–Ъ ¬† 10559996 . –Я–Ь–Ш–Ф ¬† 37458272 .
- ^ –Ы–Њ–≥–Њ–≤–Є–љ—Б–Ї–Є–є –Т., –°–∞—В–ї–Є–љ –Р., –Ы–∞–є –†., –°—Г–Њ–љ—Б–Њ–љ –°., –Ъ–∞–њ–ї–Њ–≤ –Ф–ґ., –Ю—Б—Б–≤–∞–ї—М–і –У. –Є –і—А. (–∞–њ—А–µ–ї—М 2016 –≥.). ¬Ђ–С–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В—М –Є –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В—М BAN2401 вАФ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –±–Њ–ї–µ–Ј–љ–Є –Р–ї—М—Ж–≥–µ–є–Љ–µ—А–∞ —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ —Б–µ–ї–µ–Ї—В–Є–≤–љ–Њ–≥–Њ –Ї –њ—А–Њ—В–Њ—Д–Є–±—А–Є–ї–ї–∞–Љ –∞–љ—В–Є—В–µ–ї–∞ Aќ≤¬ї . –Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Є —В–µ—А–∞–њ–Є—П –±–Њ–ї–µ–Ј–љ–Є –Р–ї—М—Ж–≥–µ–є–Љ–µ—А–∞ . 8 (1): 14. –і–Њ–Є : 10.1186/s13195-016-0181-2 . –Я–Ь–¶ ¬† 4822297 . –Я–Ь–Ш–Ф ¬† 27048170 .
- ^ ¬Ђ–Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –і–ї—П –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–Є—П –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В–Є –Є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є BAN2401 —Г —Г—З–∞—Б—В–љ–Є–Ї–Њ–≤ —Б —А–∞–љ–љ–µ–є –±–Њ–ї–µ–Ј–љ—М—О –Р–ї—М—Ж–≥–µ–є–Љ–µ—А–∞¬ї . –Ъ–µ–є—Б-–Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ . 25 –Љ–∞—А—В–∞ 2019 –≥. –і–Њ–Є : 10.31525/ct1-nct03887455 . ISSN ¬† 2643-4652 . S2CID ¬† 242999976 .
- ^ –Т–∞–љ –Ф–∞–є–Ї CH, –°—Г–Њ–љ—Б–Њ–љ CJ, –Р–є—Б–µ–љ –Я., –С–µ–є—В–Љ–∞–љ –†.–Ф–ґ., –І–µ–љ –°., –Ф–ґ–Є –Ь. –Є –і—А. (—П–љ–≤–∞—А—М 2023 –≥.). ¬Ђ–Ы–µ–Ї–∞–љ–µ–Љ–∞–± –њ—А–Є —А–∞–љ–љ–µ–є –±–Њ–ї–µ–Ј–љ–Є –Р–ї—М—Ж–≥–µ–є–Љ–µ—А–∞¬ї. –Ь–µ–і–Є—Ж–Є–љ—Б–Ї–Є–є –ґ—Г—А–љ–∞–ї –Э–Њ–≤–Њ–є –Р–љ–≥–ї–Є–Є . 388 (1): 9вАУ21. –і–Њ–Є : 10.1056/NEJMoa2212948 . –Я–Ь–Ш–Ф ¬† 36449413 .
- ^ "–Ы–µ–Ї–µ–Љ–±–Є | –Р–Ы–¶–§–Ю–†–£–Ь" . www.alzforum.org . –Я—А–Њ–≤–µ—А–µ–љ–Њ 14 —Д–µ–≤—А–∞–ї—П 2024 –≥.
- ^ –Ъ–Њ–Љ–Є—Б—Б–∞—А –£–њ—А–∞–≤–ї–µ–љ–Є—П (07.07.2023). ¬ЂFDA –њ—А–µ–≤—А–∞—Й–∞–µ—В –љ–Њ–≤–Њ–µ –ї–µ—З–µ–љ–Є–µ –±–Њ–ї–µ–Ј–љ–Є –Р–ї—М—Ж–≥–µ–є–Љ–µ—А–∞ –≤ —В—А–∞–і–Є—Ж–Є–Њ–љ–љ–Њ–µ –Њ–і–Њ–±—А–µ–љ–Є–µ¬ї . FDA . –Я—А–Њ–≤–µ—А–µ–љ–Њ 14 —Д–µ–≤—А–∞–ї—П 2024 –≥.
- ^ –§—А—Н–љ—Б–Є—Б –†.–Ф–ґ., –®–∞—А–Љ–∞ –°.–Ъ., –°–њ—А–Є–љ–≥–µ—А –°., –У—А–Є–љ –Р.–Ф–ґ., –•–Њ—Г–њ-–°—В–Њ—Г–љ –Ы.–Ф., –°–µ–љ–∞ –Ы. –Є –і—А. (—Б–µ–љ—В—П–±—А—М 2002 –≥.). ¬Ђ–§–∞–Ј–∞ I –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –∞–љ—В–Є—В–µ–ї–Њ-–љ–∞–њ—А–∞–≤–ї–µ–љ–љ–Њ–є —Д–µ—А–Љ–µ–љ—В–љ–Њ–є –њ—А–Њ–ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ–Њ–є —В–µ—А–∞–њ–Є–Є (ADEPT) —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ—Л–Љ –Ї–Њ–ї–Њ—А–µ–Ї—В–∞–ї—М–љ—Л–Љ —А–∞–Ї–Њ–Љ –Є–ї–Є –і—А—Г–≥–Є–Љ–Є –Њ–њ—Г—Е–Њ–ї—П–Љ–Є, –њ—А–Њ–і—Г—Ж–Є—А—Г—О—Й–Є–Љ–Є –°–Х–Р¬ї . –С—А–Є—В–∞–љ—Б–Ї–Є–є –ґ—Г—А–љ–∞–ї —А–∞–Ї–∞ . 87 (6): 600вАУ607. –і–Њ–Є : 10.1038/sj.bjc.6600517 . –Я–Ь–¶ ¬† 2364249 . –Я–Ь–Ш–Ф ¬† 12237768 .
- ^ –Ъ—А–∞—Г—Б—Б –Т.–Ъ., –Я–∞—А–Ї –Ф–ґ.–Т., –Ъ–Є—А–њ–Њ—В–Є–љ –Ф.–С., –•–Њ–љ–≥ –Ъ., –С–µ–љ—Ж CC (2000). ¬Ђ–Э–Њ–≤—Л–µ –Љ–µ—В–Њ–і—Л –ї–µ—З–µ–љ–Є—П HER2 (ErbB-2/neu) –љ–∞ –Њ—Б–љ–Њ–≤–µ –∞–љ—В–Є—В–µ–ї¬ї. –С–Њ–ї–µ–Ј–љ—М –Љ–Њ–ї–Њ—З–љ–Њ–є –ґ–µ–ї–µ–Ј—Л . 11 : 113вАУ124. –і–Њ–Є : 10.3233/bd-1999-11110 . –Я–Ь–Ш–Ф ¬† 15687597 .
- ^ –Ф–ґ–Њ–є—Б –Ф–ґ. –Р., –§–Є—А–Њ–љ –Ф. –Ґ. (–∞–њ—А–µ–ї—М 2015 –≥.). ¬Ђ–Ш—Б–Ї–ї—О—З–µ–љ–Є–µ –Ґ-–Ї–ї–µ—В–Њ–Ї, –Є–Љ–Љ—Г–љ–љ–∞—П –њ—А–Є–≤–Є–ї–µ–≥–Є—П –Є –Љ–Є–Ї—А–Њ–Њ–Ї—А—Г–ґ–µ–љ–Є–µ –Њ–њ—Г—Е–Њ–ї–Є¬ї . –Э–∞—Г–Ї–∞ . 348 (6230): 74вАУ80. –С–Є–±–Ї–Њ–і : 2015Sci...348...74J . –і–Њ–Є : 10.1126/science.aaa6204 . –Я–Ь–Ш–Ф ¬† 25838376 . S2CID ¬† 11603692 .
- ^ –•—Г–Ї—Б –Ь.–Р., –£—Н–є–і –Ъ.–°., –Ь–Є–ї–ї–Є–Ї–µ–љ –£.–Ф–ґ. (1991). ¬Ђ–Ь—Г—А–Њ–Љ–Њ–љ–∞–± CD-3: –Њ–±–Ј–Њ—А –µ–≥–Њ —Д–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є–Є, —Д–∞—А–Љ–∞–Ї–Њ–Ї–Є–љ–µ—В–Є–Ї–Є –Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –њ—А–Є —В—А–∞–љ—Б–њ–ї–∞–љ—В–∞—Ж–Є–Є¬ї. –§–∞—А–Љ–∞–Ї–Њ—В–µ—А–∞–њ–Є—П . 11 (1): 26вАУ37. –і–Њ–Є : 10.1002/j.1875-9114.1991.tb03595.x . –Я–Ь–Ш–Ф ¬† 1902291 . S2CID ¬† 25271222 .
- ^ –І–µ–є–Љ—Б –Я., –С–∞—В–Є –Ф. (2009). ¬Ђ–С–Є—Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Є–µ –∞–љ—В–Є—В–µ–ї–∞ –і–ї—П –ї–µ—З–µ–љ–Є—П —А–∞–Ї–∞: —Б–≤–µ—В –≤ –Ї–Њ–љ—Ж–µ —В—Г–љ–љ–µ–ї—П?¬ї . –Ь–Р–С . 1 (6): 539вАУ547. –і–Њ–Є : 10.4161/mabs.1.6.10015 . –Я–Ь–¶ ¬† 2791310 . –Я–Ь–Ш–Ф ¬† 20073127 .
- ^ –Ы–Є–љ–Ї–µ –†., –Ъ–ї—П–є–љ –Р., –Ч–µ–є–Љ–µ—Ж –Ф. (2010). ¬Ђ–Ъ–∞—В—Г–Љ–∞–Ї—Б–Њ–Љ–∞–±: –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–µ —А–∞–Ј–≤–Є—В–Є–µ –Є –±—Г–і—Г—Й–Є–µ –љ–∞–њ—А–∞–≤–ї–µ–љ–Є—П¬ї . –Ь–Р–С . 2 (2): 129вАУ136. –і–Њ–Є : 10.4161/mabs.2.2.11221 . –Я–Ь–Ъ ¬† 2840231 . –Я–Ь–Ш–Ф ¬† 20190561 .
- ^ –°–Ї–Њ–ї—М–љ–Є–Ї –Я.–Р. (2009). ¬Ђ–Ь–Р–С: –±–Є–Ј–љ–µ—Б-–њ–µ—А—Б–њ–µ–Ї—В–Є–≤–∞¬ї . –Ь–Р–С . 1 (2): 179вАУ184. –і–Њ–Є : 10.4161/mabs.1.2.7736 . –Я–Ь–¶ ¬† 2725420 . –Я–Ь–Ш–Ф ¬† 20061824 .
- ^ –Ъ–µ–ї–ї–Є –С. (2009). ¬Ђ–Ш–љ–і—Г—Б—В—А–Є–∞–ї–Є–Ј–∞—Ж–Є—П —В–µ—Е–љ–Њ–ї–Њ–≥–Є–Є –њ—А–Њ–Є–Ј–≤–Њ–і—Б—В–≤–∞ –Љ–Њ–љ–Њ–Ї–ї–Њ–љ–∞–ї—М–љ—Л—Е –∞–љ—В–Є—В–µ–ї: –±–Є–Њ–њ–µ—А–µ—А–∞–±–∞—В—Л–≤–∞—О—Й–∞—П –њ—А–Њ–Љ—Л—И–ї–µ–љ–љ–Њ—Б—В—М –љ–∞ –њ–µ—А–µ–њ—Г—В—М–µ¬ї . –Ь–Р–С . 1 (5): 443вАУ452. –і–Њ–Є : 10.4161/mabs.1.5.9448 . –Я–Ь–¶ ¬† 2759494 . –Я–Ь–Ш–Ф ¬† 20065641 .