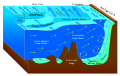
Гидротермальное жерло


Гидротермальные источники — это трещины на морском дне , из которых вытекает геотермально нагретая вода. Они обычно встречаются вблизи вулканически активных мест, областей, где тектонические плиты раздвигаются на срединно-океанических хребтах , океанских котловинах и горячих точках . [ 1 ] Распространение гидротермальных жидкостей по всему мировому океану в местах активных жерл создает гидротермальные шлейфы. Гидротермальные месторождения — это горные породы и месторождения минеральных руд, образовавшиеся под действием гидротермальных источников.
Hydrothermal vents exist because the earth is both geologically active and has large amounts of water on its surface and within its crust. Under the sea, they may form features called black smokers or white smokers, which deliver a wide range of elements to the world's oceans, thus contributing to global marine biogeochemistry. Relative to the majority of the deep sea, the areas around hydrothermal vents are biologically more productive, often hosting complex communities fueled by the chemicals dissolved in the vent fluids. Chemosynthetic bacteria and archaea found around hydrothermal vents form the base of the food chain, supporting diverse organisms including giant tube worms, clams, limpets, and shrimp. Active hydrothermal vents are thought to exist on Jupiter's moon Europa and Saturn's moon Enceladus,[2][3] and it is speculated that ancient hydrothermal vents once existed on Mars.[1][4]
Hydrothermal vents have been hypothesized to have been a significant factor to starting abiogenesis and the survival of primitive life. The conditions of these vents have been shown to support the synthesis of molecules important to life. Some evidence suggests that certain vents such as alkaline hydrothermal vents or those containing supercritical CO2 are more conducive to the formation of these organic molecules. However, the origin of life is a widely debated topic, and there are many conflicting viewpoints.
Physical properties
[edit]Hydrothermal vents in the deep ocean typically form along the mid-ocean ridges, such as the East Pacific Rise and the Mid-Atlantic Ridge. These are locations where two tectonic plates are diverging and new crust is being formed.[5]
The water that issues from seafloor hydrothermal vents consists mostly of seawater drawn into the hydrothermal system close to the volcanic edifice through faults and porous sediments or volcanic strata, plus some magmatic water released by the upwelling magma.[1] In terrestrial[clarification needed] hydrothermal systems, the majority of water circulated within the fumarole and geyser systems, is meteoric water plus ground water that has percolated down into the thermal system from the surface, but also commonly contains some portion of metamorphic water, magmatic water, and sedimentary formational brine that is released by the magma. The proportion of each varies from location to location.[citation needed]
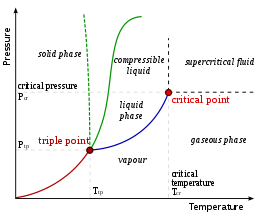
In contrast to the approximately 2 °C (36 °F) ambient water temperature at these depths, water emerges from these vents at temperatures ranging from 60 °C (140 °F)[6] up to as high as 464 °C (867 °F).[7][8] Due to the high hydrostatic pressure at these depths, water may exist in either its liquid form or as a supercritical fluid at such temperatures.[5] The critical point of (pure) water is 375 °C (707 °F) at a pressure of 218 atmospheres.
However, introducing salinity into the fluid raises the critical point to higher temperatures and pressures. The critical point of seawater (3.2 wt. % NaCl) is 407 °C (765 °F) and 298.5 bars,[9] corresponding to a depth of ~2,960 m (9,710 ft) below sea level. Accordingly, if a hydrothermal fluid with a salinity of 3.2 wt. % NaCl vents above 407 °C (765 °F) and 298.5 bars, it is supercritical. Furthermore, the salinity of vent fluids have been shown to vary widely due to phase separation in the crust.[10] The critical point for lower salinity fluids is at lower temperature and pressure conditions than that for seawater, but higher than that for pure water. For example, a vent fluid with a 2.24 wt. % NaCl salinity has the critical point at 400 °C (752 °F) and 280.5 bars. Thus, water emerging from the hottest parts of some hydrothermal vents can be a supercritical fluid, possessing physical properties between those of a gas and those of a liquid.[7][8]
Examples of supercritical venting are found at several sites. Sister Peak (Comfortless Cove Hydrothermal Field, 4°48′S 12°22′W / 4.800°S 12.367°W, depth 2,996 m or 9,829 ft) vents low salinity phase-separated, vapor-type fluids. Sustained venting was not found to be supercritical but a brief injection of 464 °C (867 °F) was well above supercritical conditions. A nearby site, Turtle Pits, was found to vent low salinity fluid at 407 °C (765 °F), which is above the critical point of the fluid at that salinity. A vent site in the Cayman Trough named Beebe, which is the world's deepest known hydrothermal site at ~5,000 m (16,000 ft) below sea level, has shown sustained supercritical venting at 401 °C (754 °F) and 2.3 wt% NaCl.[11]
Although supercritical conditions have been observed at several sites, it is not yet known what significance, if any, supercritical venting has in terms of hydrothermal circulation, mineral deposit formation, geochemical fluxes or biological activity.[citation needed]
The initial stages of a vent chimney begin with the deposition of the mineral anhydrite. Sulfides of copper, iron, and zinc then precipitate in the chimney gaps, making it less porous over the course of time. Vent growths on the order of 30 cm (1 ft) per day have been recorded.[12] An April 2007 exploration of the deep-sea vents off the coast of Fiji found those vents to be a significant source of dissolved iron (see iron cycle).[13]
Black smokers and white smokers
[edit]

Some hydrothermal vents form roughly cylindrical chimney structures. These form from minerals that are dissolved in the vent fluid. When the superheated water contacts the near-freezing sea water, the minerals precipitate out to form particles which add to the height of the stacks. Some of these chimney structures can reach heights of 60 m (200 ft).[14] An example of such a towering vent was "Godzilla", a structure on the Pacific Ocean deep seafloor near Oregon that rose to 40 m (130 ft) before it fell over in 1996.[15]
Black smokers
[edit]
A black smoker or deep-sea vent is a type of hydrothermal vent found on the seabed, typically in the bathyal zone (with largest frequency in depths from 2,500 to 3,000 m (8,200 to 9,800 ft)), but also in lesser depths as well as deeper in the abyssal zone.[1] They appear as black, chimney-like structures that emit a cloud of black material. Black smokers typically emit particles with high levels of sulfur-bearing minerals, or sulfides. Black smokers are formed in fields hundreds of meters wide when superheated water from below Earth's crust comes through the ocean floor (water may attain temperatures above 400 °C (752 °F)).[1] This water is rich in dissolved minerals from the crust, most notably sulfides. When it comes in contact with cold ocean water, many minerals precipitate, forming a black, chimney-like structure around each vent. The deposited metal sulfides can become massive sulfide ore deposits in time. Some black smokers on the Azores portion of the Mid-Atlantic Ridge are extremely rich in metal content, such as Rainbow with 24,000 μM concentrations of iron.[16]
Black smokers were first discovered in 1979 on the East Pacific Rise by scientists from Scripps Institution of Oceanography during the RISE Project.[17] They were observed using the deep submergence vehicle ALVIN from the Woods Hole Oceanographic Institution. Now, black smokers are known to exist in the Atlantic and Pacific Oceans, at an average depth of 2,100 m (6,900 ft). The most northerly black smokers are a cluster of five named Loki's Castle,[18] discovered in 2008 by scientists from the University of Bergen at 73°N, on the Mid-Atlantic Ridge between Greenland and Norway. These black smokers are of interest as they are in a more stable area of the Earth's crust, where tectonic forces are less and consequently fields of hydrothermal vents are less common.[19] The world's deepest known black smokers are located in the Cayman Trough, 5,000 m (3.1 miles) below the ocean's surface.[20]
White smokers
[edit]
White smoker vents emit lighter-hued minerals, such as those containing barium, calcium and silicon. These vents also tend to have lower-temperature plumes probably because they are generally distant from their heat source.[1]
Black and white smokers may coexist in the same hydrothermal field, but they generally represent proximal (close) and distal (distant) vents to the main upflow zone, respectively. However, white smokers correspond mostly to waning stages of such hydrothermal fields, as magmatic heat sources become progressively more distant from the source (due to magma crystallization) and hydrothermal fluids become dominated by seawater instead of magmatic water. Mineralizing fluids from this type of vent are rich in calcium and they form dominantly sulfate-rich (i.e., barite and anhydrite) and carbonate deposits.[1]
Hydrothermal plumes
[edit]Hydrothermal plumes are fluid entities that manifest where hydrothermal fluids are expelled into the overlying water column at active hydrothermal vent sites.[21] As hydrothermal fluids typically harbor physical (e.g., temperature, density) and chemical (e.g., pH, Eh, major ions) properties distinct from seawater, hydrothermal plumes embody physical and chemical gradients that promote several types of chemical reactions, including oxidation-reduction reactions and precipitation reactions.[21] Because of these reactions, hydrothermal plumes are dynamic entities whose physical and chemical properties evolve over both space and time within the ocean.
Hydrothermal vent fluids harbor temperatures (~40 to >400°C) well above that of ocean floor seawater (~4°C), meaning that hydrothermal fluid is less dense than the surrounding seawater and will rise through the water column due to buoyancy, forming a hydrothermal plume; therefore, the phase during which hydrothermal plumes rise through the water column is known as the "buoyant plume" phase.[21] During this phase, shear forces between the hydrothermal plume and surrounding seawater generate turbulent flow that facilitates mixing between the two types of fluids, which progressively dilutes the hydrothermal plume with seawater.[21] Eventually, the coupled effects of dilution and rising into progressively warmer (less dense) overlying seawater will cause the hydrothermal plume to become neutrally buoyant at some height above the seafloor; therefore, this stage of hydrothermal plume evolution is known as the "nonbuoyant plume" phase.[21] Once the plume is neutrally buoyant, it can no longer continue to rise through the water column and instead begins to spread laterally throughout the ocean, potentially over several thousands of kilometers.[22]
Chemical reactions occur concurrently with the physical evolution of hydrothermal plumes. While seawater is a relatively oxidizing fluid, hydrothermal vent fluids are typically reducing in nature.[21] Consequently, reduced chemicals such as hydrogen gas, hydrogen sulfide, methane, Fe2+, and Mn2+ that are common in many vent fluids will react upon mixing with seawater. In fluids with high concentrations of H2S, dissolved metal ions such as Fe2+ and Mn2+ readily precipitate as dark-colored metal sulfide minerals (see "black smokers").[21] Furthermore, Fe2+ and Mn2+ entrained within the hydrothermal plume will eventually oxidize to form insoluble Fe and Mn (oxy)hydroxide minerals.[23] For this reason, the hydrothermal "near field" has been proposed to refer to the hydrothermal plume region undergoing active oxidation of metals while the term "far field" refers to the plume region within which complete metal oxidation has occurred.[22]
Identification and dating
[edit]Several chemical tracers found in hydrothermal plumes are used to locate deep-sea hydrothermal vents during discovery cruises. Useful tracers of hydrothermal activity should be chemically unreactive so that changes in tracer concentration subsequent to venting are due solely to dilution.[21] The noble gas helium fits this criterion and is a particularly useful tracer of hydrothermal activity. This is because hydrothermal venting releases elevated concentrations of helium-3 relative to seawater, a rare, naturally occurring He isotope derived exclusively from the Earth's interior.[21] Thus, the dispersal of 3He throughout the oceans via hydrothermal plumes creates anomalous seawater He isotope compositions that signify hydrothermal venting. Another noble gas that can serve as a tracer of hydrothermal activity is radon. As all naturally occurring isotopes of Rn are radioactive, Rn concentrations in seawater can also provide information on hydrothermal plume ages when combined with He isotope data.[21] The isotope radon-222 is utilized for this purpose as 222Rn has the longest half-life of all naturally occurring radon isotopes of roughly 3.82 days.[24] Dissolved gases, such as H2, H2S, and CH4, and metals, such as Fe and Mn, present at high concentrations in hydrothermal vent fluids relative to seawater may also be diagnostic of hydrothermal plumes and thus active venting; however, these components are reactive and are thus less suitable as tracers of hydrothermal activity.[21]
Ocean biogeochemistry
[edit]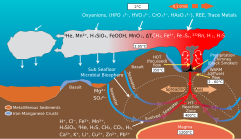
Hydrothermal plumes represent an important mechanism through which hydrothermal systems influence marine biogeochemistry. Hydrothermal vents emit a wide variety of trace metals into the ocean, including Fe, Mn, Cr, Cu, Zn, Co, Ni, Mo, Cd, V, and W,[25] many of which have biological functions.[26] Numerous physical and chemical processes control the fate of these metals once they are expelled into the water column. Based on thermodynamic theory, Fe2+ and Mn2+ should oxidize in seawater to form insoluble metal (oxy)hydroxide precipitates; however, complexation with organic compounds and the formation of colloids and nanoparticles can keep these redox-sensitive elements suspended in solution far from the vent site.[21][23]
Fe and Mn often have the highest concentrations among metals in acidic hydrothermal vent fluids,[25] and both have biological significance, particularly Fe, which is often a limiting nutrient in marine environments.[26] Therefore, far-field transport of Fe and Mn via organic complexation may constitute an important mechanism of ocean metal cycling.[22] Additionally, hydrothermal vents deliver significant concentrations of other biologically important trace metals to the ocean such as Mo, which may have been important in the early chemical evolution of the Earth's oceans and to the origin of life (see "theory of hydrothermal origin of life").[25][27] However, Fe and Mn precipitates can also influence ocean biogeochemistry by removing trace metals from the water column. The charged surfaces of iron (oxy)hydroxide minerals effectively adsorb elements such as phosphorus, vanadium, arsenic, and rare earth metals from seawater; therefore, although hydrothermal plumes may represent a net source of metals such as Fe and Mn to the oceans, they can also scavenge other metals and non-metalliferous nutrients such as P from seawater, representing a net sink of these elements.[23]
Biology of hydrothermal vents
[edit]Life has traditionally been seen as driven by energy from the sun, but deep-sea organisms have no access to sunlight, so biological communities around hydrothermal vents must depend on nutrients found in the dusty chemical deposits and hydrothermal fluids in which they live. Previously, benthic oceanographers assumed that vent organisms were dependent on marine snow, as deep-sea organisms are. This would leave them dependent on plant life and thus the sun. Some hydrothermal vent organisms do consume this "rain", but with only such a system, life forms would be sparse. Compared to the surrounding sea floor, however, hydrothermal vent zones have a density of organisms 10,000 to 100,000 times greater. These organisms include yeti crabs, which have long hairy arms that they reach out over the vent to collect food with.[citation needed]
The hydrothermal vents are recognized as a type of chemosynthetic based ecosystems (CBE) where primary productivity is fuelled by chemical compounds as energy sources instead of light (chemoautotrophy).[28] Hydrothermal vent communities are able to sustain such vast amounts of life because vent organisms depend on chemosynthetic bacteria for food. The water from the hydrothermal vent is rich in dissolved minerals and supports a large population of chemoautotrophic bacteria. These bacteria use sulfur compounds, particularly hydrogen sulfide, a chemical highly toxic to most known organisms, to produce organic material through the process of chemosynthesis.
The vents' impact on the living environment goes beyond the organisms that lives around them, as they act as a significant source of iron in the oceans, providing iron for the phytoplankton.[29]
Biological communities
[edit]
The ecosystem so formed is reliant upon the continued existence of the hydrothermal vent field as the primary source of energy, which differs from most surface life on Earth, which is based on solar energy. However, although it is often said that these communities exist independently of the sun, some of the organisms are actually dependent upon oxygen produced by photosynthetic organisms, while others are anaerobic.

The chemosynthetic bacteria grow into a thick mat which attracts other organisms, such as amphipods and copepods, which graze upon the bacteria directly. Larger organisms, such as snails, shrimp, crabs, tube worms, fish (especially eelpout, cutthroat eel, Ophidiiformes and Symphurus thermophilus), and octopuses (notably Vulcanoctopus hydrothermalis), form a food chain of predator and prey relationships above the primary consumers. The main families of organisms found around seafloor vents are annelids, pogonophorans, gastropods, and crustaceans, with large bivalves, vestimentiferan worms, and "eyeless" shrimp making up the bulk of nonmicrobial organisms.[citation needed]

Siboglinid tube worms, which may grow to over 2 m (6.6 ft) tall in the largest species, often form an important part of the community around a hydrothermal vent. They have no mouth or digestive tract, and like parasitic worms, absorb nutrients produced by the bacteria in their tissues. About 285 billion bacteria are found per ounce of tubeworm tissue. Tubeworms have red plumes which contain hemoglobin. Hemoglobin combines with hydrogen sulfide and transfers it to the bacteria living inside the worm. In return, the bacteria nourish the worm with carbon compounds. Two of the species that inhabit a hydrothermal vent are Tevnia jerichonana, and Riftia pachyptila. One discovered community, dubbed "Eel City", consists predominantly of the eel Dysommina rugosa. Though eels are not uncommon, invertebrates typically dominate hydrothermal vents. Eel City is located near Nafanua volcanic cone, American Samoa.[30]
In 1993, already more than 100 gastropod species were known to occur in hydrothermal vents.[31] Over 300 new species have been discovered at hydrothermal vents,[32] many of them "sister species" to others found in geographically separated vent areas. It has been proposed that before the North American plate overrode the mid-ocean ridge, there was a single biogeographic vent region found in the eastern Pacific.[33] The subsequent barrier to travel began the evolutionary divergence of species in different locations. The examples of convergent evolution seen between distinct hydrothermal vents is seen as major support for the theory of natural selection and of evolution as a whole.

Although life is very sparse at these depths, black smokers are the centers of entire ecosystems. Sunlight is nonexistent, so many organisms, such as archaea and extremophiles, convert the heat, methane, and sulfur compounds provided by black smokers into energy through a process called chemosynthesis. More complex life forms, such as clams and tubeworms, feed on these organisms. The organisms at the base of the food chain also deposit minerals into the base of the black smoker, therefore completing the life cycle.
A species of phototrophic bacterium has been found living near a black smoker off the coast of Mexico at a depth of 2,500 m (8,200 ft). No sunlight penetrates that far into the waters. Instead, the bacteria, part of the Chlorobiaceae family, use the faint glow from the black smoker for photosynthesis. This is the first organism discovered in nature to exclusively use a light other than sunlight for photosynthesis.[34]
New and unusual species are constantly being discovered in the neighborhood of black smokers. The Pompeii worm Alvinella pompejana, which is capable of withstanding temperatures up to 80 °C (176 °F), was found in the 1980s, and a scaly-foot gastropod Chrysomallon squamiferum in 2001 during an expedition to the Indian Ocean's Kairei hydrothermal vent field. The latter uses iron sulfides (pyrite and greigite) for the structure of its dermal sclerites (hardened body parts), instead of calcium carbonate. The extreme pressure of 2,500 m of water (approximately 25 megapascals or 250 atmospheres) is thought to play a role in stabilizing iron sulfide for biological purposes. This armor plating probably serves as a defense against the venomous radula (teeth) of predatory snails in that community.
In March 2017, researchers reported evidence of possibly the oldest forms of life on Earth. Putative fossilized microorganisms were discovered in hydrothermal vent precipitates in the Nuvvuagittuq Belt of Quebec, Canada, that may have lived as early as 4.280 billion years ago, not long after the oceans formed 4.4 billion years ago, and not long after the formation of the Earth 4.54 billion years ago.[35][36][37]


Animal-bacterial symbiosis
[edit]
Hydrothermal vent ecosystems have enormous biomass and productivity, but this rests on the symbiotic relationships that have evolved at vents. Deep-sea hydrothermal vent ecosystems differ from their shallow-water and terrestrial hydrothermal counterparts due to the symbiosis that occurs between macroinvertebrate hosts and chemoautotrophic microbial symbionts in the former.[38] Since sunlight does not reach deep-sea hydrothermal vents, organisms in deep-sea hydrothermal vents cannot obtain energy from the sun to perform photosynthesis. Instead, the microbial life found at hydrothermal vents is chemosynthetic; they fix carbon by using energy from chemicals such as sulfide, as opposed to light energy from the sun. In other words, the symbiont converts inorganic molecules (H2S, CO2, O) to organic molecules that the host then uses as nutrition. However, sulfide is an extremely toxic substance to most life on Earth. For this reason, scientists were astounded when they first found hydrothermal vents teeming with life in 1977. What was discovered was the ubiquitous symbiosis of chemoautotrophs living in (endosymbiosis) the vent animals' gills; the reason why multicellular life is capable to survive the toxicity of vent systems. Scientists are therefore now studying how the microbial symbionts aid in sulfide detoxification (therefore allowing the host to survive the otherwise toxic conditions). Work on microbiome function shows that host-associated microbiomes are also important in host development, nutrition, defense against predators, and detoxification. In return, the host provides the symbiont with chemicals required for chemosynthesis, such as carbon, sulfide, and oxygen.[citation needed]
In the early stages of studying life at hydrothermal vents, there were differing theories regarding the mechanisms by which multicellular organisms were able to acquire nutrients from these environments, and how they were able to survive in such extreme conditions. In 1977, it was hypothesized that the chemoautotrophic bacteria at hydrothermal vents might be responsible for contributing to the diet of suspension-feeding bivalves.[39]
Finally, in 1981, it was understood that giant tubeworm nutrition acquisition occurred as a result of chemoautotrophic bacterial endosymbionts.[40][41][42] As scientists continued to study life at hydrothermal vents, it was understood that symbiotic relationships between chemoautotrophs and macrofauna invertebrate species was ubiquitous. For instance, in 1983, clam gill tissue was confirmed to contain bacterial endosymbionts;[43] in 1984 vent bathymodiolid mussels and vesicomyid clams were also found to carry endosymbionts.[44][45]
However, the mechanisms by which organisms acquire their symbionts differ, as do the metabolic relationships. For instance, tubeworms have no mouth and no gut, but they do have a "trophosome", which is where they deal with nutrition and where their endosymbionts are found. They also have a bright red plume, which they use to uptake compounds such as O, H2S, and CO2, which feed the endosymbionts in their trophosome. Remarkably, the tubeworms hemoglobin (which incidentally is the reason for the bright red color of the plume) is capable of carrying oxygen without interference or inhibition from sulfide, despite the fact that oxygen and sulfide are typically very reactive. In 2005, it was discovered that this is possible due to zinc ions that bind the hydrogen sulfide in the tubeworms hemoglobin, therefore preventing the sulfide from reacting with the oxygen. It also reduces the tubeworms tissue from exposure to the sulfide and provides the bacteria with the sulfide to perform chemoautotrophy.[46] It has also been discovered that tubeworms can metabolize CO2 in two different ways, and can alternate between the two as needed as environmental conditions change.[47]
In 1988, research confirmed thiotrophic (sulfide-oxidizing) bacteria in Alviniconcha hessleri, a large vent mollusk.[48] In order to circumvent the toxicity of sulfide, mussels first convert it to thiosulfate before carrying it over to the symbionts.[49] In the case of motile organisms such as alvinocarid shrimp, they must track oxic (oxygen-rich) / anoxic (oxygen-poor) environments as they fluctuate in the environment.[citation needed]
Organisms living at the edge of hydrothermal vent fields, such as pectinid scallops, also carry endosymbionts in their gills, and as a result their bacterial density is low relative to organisms living nearer to the vent. However, the scallop's dependence on the microbial endosymbiont for obtaining their nutrition is therefore also lessened.[citation needed]
Furthermore, not all host animals have endosymbionts; some have episymbionts—symbionts living on the animal as opposed to inside the animal. Shrimp found at vents in the Mid-Atlantic Ridge were once thought of as an exception to the necessity of symbiosis for macroinvertebrate survival at vents. That changed in 1988 when they were discovered to carry episymbionts.[50] Since then, other organisms at vents have been found to carry episymbionts as well,[51] such as Lepetodrilis fucensis.[52]
Furthermore, while some symbionts reduce sulfur compounds, others are known as "methanotrophs" and reduce carbon compounds, namely methane. Bathmodiolid mussels are an example of a host that contains methanotrophic endosymbionts; however, the latter mostly occur in cold seeps as opposed to hydrothermal vents.[citation needed]
While chemosynthesis occurring at the deep ocean allows organisms to live without sunlight in the immediate sense, they technically still rely on the sun for survival, since oxygen in the ocean is a byproduct of photosynthesis. However, if the sun were to suddenly disappear and photosynthesis ceased to occur on our planet, life at the deep-sea hydrothermal vents could continue for millennia (until the oxygen was depleted).[citation needed]
Theory of hydrothermal origin of life
[edit]The chemical and thermal dynamics in hydrothermal vents makes such environments highly suitable thermodynamically for chemical evolution processes to take place. Therefore, thermal energy flux is a permanent agent and is hypothesized to have contributed to the evolution of the planet, including prebiotic chemistry.[1]
Günter Wächtershäuser proposed the iron-sulfur world theory and suggested that life might have originated at hydrothermal vents. Wächtershäuser proposed that an early form of metabolism predated genetics. By metabolism he meant a cycle of chemical reactions that release energy in a form that can be harnessed by other processes.[53]
It has been proposed that amino acid synthesis could have occurred deep in the Earth's crust and that these amino acids were subsequently shot up along with hydrothermal fluids into cooler waters, where lower temperatures and the presence of clay minerals would have fostered the formation of peptides and protocells.[54] This is an attractive hypothesis because of the abundance of CH4 (methane) and NH3 (ammonia) present in hydrothermal vent regions, a condition that was not provided by the Earth's primitive atmosphere. A major limitation to this hypothesis is the lack of stability of organic molecules at high temperatures, but some have suggested that life would have originated outside of the zones of highest temperature.[55] There are numerous species of extremophiles and other organisms currently living immediately around deep-sea vents, suggesting that this is indeed a possible scenario.[citation needed]
Experimental research and computer modeling indicate that the surfaces of mineral particles inside hydrothermal vents have similar catalytic properties to enzymes and are able to create simple organic molecules, such as methanol (CH3OH) and formic acid (HCO2H), out of the dissolved CO2 in the water.[56][57][58] Additionally, the discovery of supercritical CO2 at some sites has been used to further support the theory of hydrothermal origin of life given that it can increase organic reaction rates. Its high solvation power and diffusion rate allow it to promote amino and formic acid synthesis, as well as the synthesis of other organic compounds, polymers, and the four amino acids: alanine, arginine, aspartic acid, and glycine. In situ experiments have revealed the convergence of high N2 content and supercritical CO2 at some sites, as well as evidence for complex organic material (amino acids) within supercritical CO2 bubbles.[59][60][61] Proponents of this theory for the origin of life also propose the presence of supercritical CO2 as a solution to the “water paradox” that pervades theories on the origin of life in aquatic settings. This paradox encompasses the fact that water is both required for life and will, in abundance, hydrolyze organic molecules and prevent dehydration synthesis reactions necessary to chemical and biological evolution.[62] Supercritical CO2, being hydrophobic, acts as a solvent that facilitates an environment conducive to dehydration synthesis. Therefore it has been hypothesized that the presence of supercritical CO2 in Hadean hydrothermal vents played an important role in the origin of life.[60]
There is some evidence that links the origin of life to alkaline hydrothermal vents in particular. The pH conditions of these vents may have made them more suitable for emerging life.[63][64] One current theory is that the naturally occurring proton gradients at these deep sea vents supplemented the lack of phospholipid bilayer membranes and proton pumps in early organisms, allowing ion gradients to form despite the lack of cellular machinery and components present in modern cells.[65] There is some discourse around this topic.[66][67] It has been argued that the natural pH gradients of these vents playing a role in the origin of life is actually implausible. The counter argument relies, among other points, on what the author describes as the unlikelihood of the formation of machinery which produces energy from the pH gradients found in hydrothermal vents without/before the existence of genetic information.[67] This counterpoint has been responded to by Nick Lane, one of the researchers whose work it focuses on. He argues that the counterpoint largely misinterprets both his work and the work of others.[66]
Another reason that the view of deep sea hydrothermal vents as an ideal environment for the origin of life remains controversial is the absence of wet-dry cycles and exposure to UV light, which promote the formation of membranous vesicles and synthesis of many biomolecules.[68][69][70] The ionic concentrations of hydrothermal vents differs from the intracellular fluid within the majority of life. It has instead been suggested that terrestrial freshwater environments are more likely to be an ideal environment for the formation of early cells.[71][72] Meanwhile, proponents of the deep sea hydrothermal vent hypothesis suggest thermophoresis in mineral cavities to be an alternative compartment for polymerization of biopolymers.[73][74]
How thermophoresis within mineral cavities could promote coding and metabolism is unknown. Nick Lane suggests that nucleotide polymerization at high concentrations of nucleotides within self-replicating protocells, where "Molecular crowding and phosphorylation in such confined, high-energy protocells could potentially promote the polymerization of nucleotides to form RNA".[75] Acetyl phosphate could possibly promote polymerization at mineral surfaces or at low water activity.[76] A computational simulation shows that nucleotide concentration of nucleotide catalysis of "the energy currency pathway is favored, as energy is limiting; favoring this pathway feeds forward into a greater nucleotide synthesis". Fast nucleotide catalysis of CO2 fixation lowers nucleotide concentration as protocell growth and division is rapid which then leads to halving of nucleotide concentration, weak nucleotide catalysis of CO2 fixation promotes little to protocell growth and division.[77]
In biochemistry, reactions with CO2 and H2 produce precursors to biomolecules that are also produced from the acetyl-CoA pathway and Krebs cycle which would support an origin of life at deep sea alkaline vents. Acetyl phosphate produced from the reactions are capable of phosphorylating ADP to ATP,[78] with maximum synthesis occurring at high water activity and low concentrations of ions, the Hadean ocean likely had lower concentrations of ions than modern oceans. The concentrations of Mg2+ and Ca2+ at alkaline hydrothermal systems are lower than the at the ocean.[79] The high concentration of potassium within most life forms could be readily explained that protocells might have evolved sodium-hydrogen antiporters to pump out Na+ as prebiotic lipid membranes are less permeable to Na+ than H+.[80] If cells originated at these environments, they would have been autotrophs with a Wood-Ljungdahl pathway and incomplete reverse Krebs cycle.[81] Mathematical modelling of organic synthesis of carboxylic acids to lipids, nucleotides, amino acids, and sugars, and polymerization reactions are favorable at alkaline hydrothermal vents.[82]
The Deep Hot Biosphere
[edit]At the beginning of his 1992 paper The Deep Hot Biosphere, Thomas Gold referred to ocean vents in support of his theory that the lower levels of the earth are rich in living biological material that finds its way to the surface.[83] He further expanded his ideas in the book The Deep Hot Biosphere.[84]
В статье о добыче абиогенных углеводородов в февральском выпуске журнала Science за 2008 г. использовались данные экспериментов на гидротермальном месторождении Лост-Сити, чтобы сообщить, как абиотический синтез низкомолекулярных углеводородов из углекислого газа, полученного из мантии, может происходить в присутствии ультраосновных пород, воды и умеренное количество тепла. [ 85 ]
Открытия и исследования
[ редактировать ]В 1949 году глубоководные исследования показали аномально горячие рассолы в центральной части Красного моря . Более поздние работы, проведенные в 1960-х годах, подтвердили наличие горячих соленых рассолов с температурой 60 ° C (140 ° F) и связанных с ними металлоносных грязей. Горячие растворы исходили из активного разлома подводного дна . Сильно соленая вода не была благоприятна для живых организмов. [ 86 ] Рассолы и связанные с ними растворы в настоящее время исследуются как источник добываемых драгоценных и цветных металлов.


В июне 1976 года ученые из Океанографического института Скриппса получили первые доказательства существования подводных гидротермальных жерл вдоль Галапагосского разлома, отрога Восточно-Тихоокеанского поднятия , в экспедиции Плеяды II , используя систему визуализации морского дна Deep-Tow. [ 87 ] В 1977 году были опубликованы первые научные статьи о гидротермальных источниках. [ 88 ] ученые из Океанографического института Скриппса ; учёный-исследователь Питер Лонсдейл опубликовал фотографии, сделанные с глубоководных камер, [ 89 ] и аспирантка Кэтлин Крейн опубликовали карты и данные о температурных аномалиях. [ 90 ] Транспондеры были развернуты на участке, получившем прозвище «Клэм-бейк», чтобы дать возможность экспедиции вернуться в следующем году для прямых наблюдений с помощью DSV Alvin .
Хемосинтетические экосистемы, окружающие подводные гидротермальные источники Галапагосского рифта, впервые были непосредственно обнаружены в 1977 году, когда группа морских геологов, финансируемая Национальным научным фондом, вернулась на места Кламбейка. Главным исследователем подводного исследования был Джек Корлисс из Университета штата Орегон . Корлисс и Тьерд ван Андел из Стэнфордского университета наблюдали и брали образцы жерл и их экосистемы 17 февраля 1977 года во время погружения на DSV Alvin , исследовательском подводном аппарате, которым управляет Океанографический институт Вудс-Хоул (WHOI). [ 91 ] Среди других ученых, участвовавших в исследовательском круизе, были Ричард (Дик) фон Герцен и Роберт Баллард из WHOI, Джек Даймонд и Луи Гордон из Университета штата Орегон, Джон Эдмонд и Таня Этуотер из Массачусетского технологического института , Дэйв Уильямс из Геологической службы США и Кэтлин Крейн из Океанографического института Скриппса . [ 91 ] [ 92 ] Эта группа опубликовала свои наблюдения за жерлами, организмами и составом жерловых жидкостей в журнале Science. [ 93 ] В 1979 году группа биологов под руководством Дж. Фредерика Грассла, работавшего в то время в WHOI , вернулась в то же место, чтобы исследовать биологические сообщества, обнаруженные двумя годами ранее.
Высокотемпературные гидротермальные источники, «черные курильщики», были обнаружены весной 1979 года командой Океанографического института Скриппса с помощью подводного аппарата «Элвин» . Экспедиция RISE исследовала Восточно-Тихоокеанское поднятие на 21° северной широты с целью протестировать геофизическое картирование морского дна с помощью « Элвина» и найти еще одно гидротермальное поле за пределами жерл Галапагосского разлома. Экспедицию возглавили Фред Списс и Кен Макдональд , в ее состав вошли участники из США, Мексики и Франции. [ 17 ] Район для погружения был выбран на основании открытия на морском дне насыпей сульфидных минералов французской экспедицией CYAMEX в 1978 году. [ 94 ] Перед погружением участник экспедиции Роберт Баллард обнаружил аномалии температуры придонной воды с помощью глубоко буксируемого набора инструментов. Первое погружение было нацелено на одну из этих аномалий. В пасхальное воскресенье 15 апреля 1979 года во время погружения Элвина на глубину 2600 метров Роджер Ларсон и Брюс Луендик обнаружили гидротермальное жерловое поле с биологическим сообществом, похожим на жерла Галапагосских островов. Во время последующего погружения 21 апреля Уильям Нормарк и Тьерри Жюто обнаружили высокотемпературные источники, испускающие струи черных минеральных частиц из дымоходов; черные курильщики. [ 95 ] датчик температуры, После этого Макдональд и Джим Эйкен установили Элвину чтобы измерять температуру воды в вентиляционных отверстиях для черных курильщиков. При этом наблюдались самые высокие температуры, зарегистрированные на тот момент в глубоководных гидротермальных источниках (380 ± 30 ° C). [ 96 ] Анализ материала черных курильщиков и дымоходов, из которых они питались, показал, что осадки сульфида железа являются обычными минералами в «дыме» и стенках дымоходов. [ 97 ]

В 2005 году компания Neptune Resources NL, занимающаяся разведкой полезных ископаемых, подала заявку и получила право на 35 000 км. 2 прав на разведку дуги Кермадек в Новой Зеландии с исключительной экономической зоне целью разведки месторождений массивных сульфидов на морском дне , потенциального нового источника сульфидов свинца , цинка и меди, образовавшихся на современных гидротермальных жерловых полях. В апреле 2007 года было объявлено об открытии жерла в Тихом океане у побережья Коста-Рики , получившего название гидротермального жерлового поля Медузы (в честь змееволосой Медузы из греческой мифологии ). [ 98 ] Гидротермальное поле Ашадзе (13° с.ш. на Срединно-Атлантическом хребте, высота -4200 м) было самым глубоким из известных высокотемпературных гидротермальных полей до 2010 года, когда гидротермальный шлейф, исходящий из реки Бибе, был самым глубоким из известных высокотемпературных гидротермальных полей. [ 99 ] сайт ( 18 ° 33' с.ш. 81 ° 43' з.д. / 18,550 ° с.ш. 81,717 ° з.д. , высота -5000 м) была обнаружена группой ученых из Лаборатории реактивного движения НАСА и Океанографического института Вудс-Хоул . Этот участок расположен на 110-километровом сверхмедленно расширяющемся возвышении Среднего Каймана в пределах Каймановой впадины . [ 100 ] В начале 2013 года самые глубокие из известных гидротермальных источников были обнаружены в Карибском море на глубине почти 5000 метров (16000 футов). [ 101 ]
Океанографы изучают вулканы и гидротермальные жерла срединно-океанского хребта Хуан-де-Фука , где тектонические плиты отходят друг от друга. [ 102 ]
Гидротермальные источники и другие геотермальные проявления в настоящее время исследуются в Баия-де-Консепсьон, Южная Нижняя Калифорния, Мексика. [ 103 ]
Распределение
[ редактировать ]Гидротермальные жерла распределены вдоль границ земной плиты, хотя их также можно найти во внутриплитных местах, таких как горячие точки вулканов. По состоянию на 2009 год насчитывалось около 500 активных подводных гидротермальных жерловых полей, примерно половина из которых наблюдалась визуально на морском дне, а другая половина подозревалась по индикаторам водной толщи и / или отложениям морского дна. [ 104 ]
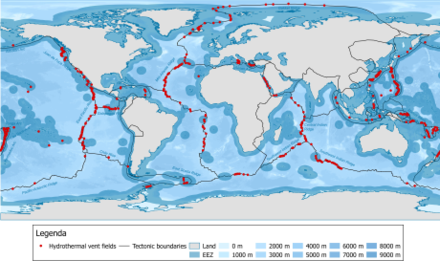
Роджерс и др. (2012) [ 105 ] признали как минимум 11 биогеографических провинций гидротермальных жерловых систем:
- Срединно-Атлантического хребта , Провинция
- Восточная Скотия-Ридж , провинция
- северная провинция Восточно-Тихоокеанского поднятия ,
- центральная провинция Восточно-Тихоокеанского поднятия,
- южная провинция Восточно-Тихоокеанского поднятия,
- к югу от Пасхальной микроплиты ,
- провинция Индийского океана,
- четыре провинции в западной части Тихого океана и многие другие.
Эксплуатация
[ редактировать ]
Гидротермальные жерла в некоторых случаях привели к образованию полезных ископаемых за счет отложения массивных сульфидных отложений на морском дне . Рудное тело Маунт -Айза , расположенное в Квинсленде , Австралия , является прекрасным примером. [ 106 ] Многие гидротермальные источники богаты кобальтом , золотом , медью и редкоземельными металлами, необходимыми для электронных компонентов. [ 107 ] Считается, что гидротермальные выходы на архейское морское дно сформировали типа Алгомы полосчатые железные образования , которые были источником железной руды . [ 108 ]
В последнее время компании, занимающиеся разведкой полезных ископаемых, движимые возросшей ценовой активностью в секторе цветных металлов в середине 2000-х годов, обратили свое внимание на добычу минеральных ресурсов из гидротермальных месторождений на морском дне. Теоретически возможно существенное снижение затрат. [ 109 ]
В таких странах, как Япония , где минеральные ресурсы в основном поступают из международного импорта, [ 110 ] Особое внимание уделяется добыче минеральных ресурсов морского дна. [ 111 ] Первая в мире «крупномасштабная» добыча гидротермальных месторождений полезных ископаемых была осуществлена Японской национальной корпорацией нефти, газа и металлов (JOGMEC) в августе – сентябре 2017 года. JOGMEC провела эту операцию с использованием исследовательского судна «Хакурей» . Эта добыча велась на жерловом поле «Изена/котел» в гидротермально активном задуговом бассейне, известном как Окинавский прогиб , который содержит 15 подтвержденных жерловых полей согласно базе данных InterRidge Vents.
Две компании в настоящее время находятся на поздней стадии начала добычи массивных сульфидов морского дна (SMS). Nautilus Minerals находится на продвинутой стадии начала добычи на своем месторождении Солварра на архипелаге Бисмарка , а Neptune Minerals находится на более ранней стадии со своим месторождением Rumble II West, расположенным на дуге Кермадек , недалеко от островов Кермадек . Обе компании предлагают использовать модифицированную существующую технологию. Nautilus Minerals в партнерстве с Placer Dome (теперь часть Barrick Gold ) в 2006 году впервые в мире сумела вернуть на поверхность более 10 метрических тонн добытых SMS с помощью модифицированных барабанных фрез, установленных на ROV. [ 112 ] В 2007 году компании Neptune Minerals удалось извлечь образцы отложений SMS с помощью модифицированного всасывающего насоса для нефтяной промышленности, установленного на ROV, что также было первым в мире. [ 113 ]
Потенциальная добыча на морском дне оказывает воздействие на окружающую среду, включая шлейфы пыли от горнодобывающего оборудования, влияющие на организмы-фильтраторы, [ 107 ] обрушение или повторное открытие жерл, выброс клатрата метана или даже субокеанические оползни. [ 114 ]

Инструменты, необходимые для добычи полезных ископаемых в этих гидротермальных жерловых экосистемах, также могут оказывать потенциальное воздействие на окружающую среду, включая шумовое загрязнение и антропогенный свет. Разработка гидротермальных жерловых систем потребует использования как погружных горнодобывающих инструментов на морском дне, в том числе подводных аппаратов с дистанционным управлением (ROV), так и надводных вспомогательных судов на поверхности океана. [ 115 ] При работе этих машин неизбежно будет создаваться некоторый уровень шума, что представляет собой проблему для организмов гидротермальных жерл, поскольку, поскольку они находятся на глубине до 12 000 футов ниже поверхности океана, они ощущают очень мало звука. [ 115 ] В результате этого у этих организмов появились высокочувствительные органы слуха, поэтому в случае внезапного увеличения шума, например, создаваемого горнодобывающим оборудованием, существует вероятность повреждения этих органов слуха и вредных организмов, обитающих в жерлах. [ 115 ] Также важно учитывать, что многие исследования смогли показать, что большой процент донных организмов общается, используя очень низкочастотные звуки; следовательно, повышение уровня окружающего шума на морском дне потенциально может замаскировать общение между организмами и изменить модели поведения. [ 115 ] Подобно тому, как глубоководные средства добычи SMS создают шумовое загрязнение, они также создают антропогенные источники света на морском дне (от горнодобывающих инструментов) и на поверхности океана (от надводных судов поддержки). Организмы в этих гидротермальных жерловых системах находятся в афотической зоне океана и адаптировались к условиям очень низкой освещенности. Исследования глубоководных креветок показали, что прожекторы, используемые на морском дне и используемые при изучении вентиляционных систем, могут вызвать необратимое повреждение сетчатки. [ 115 ] гарантируя дальнейшие исследования потенциального риска для других жерловых организмов. Помимо риска для глубоководных организмов, надводные суда обеспечения используют ночное антропогенное освещение. [ 115 ] Исследования показали, что этот тип освещения на поверхности океана может дезориентировать морских птиц и вызывать выпадение осадков, когда они летят навстречу антропогенному свету и утомляются или сталкиваются с искусственными объектами, что приводит к травмам или смерти. [ 115 ] При оценке воздействия добычи гидротермальных источников на окружающую среду учитываются как водные, так и наземные организмы.
Существует три процесса с отходами горнодобывающей промышленности, известные как боковой выброс отложений, процесс обезвоживания и сдвиг или возмущение отложений, которые можно ожидать при процессах глубоководной добычи полезных ископаемых и которые могут привести к накоплению шлейфа или облака отложений, что может имеют существенные экологические последствия. Выброс отложений в сторону — это процесс, который может происходить на морском дне и включать в себя перемещение материала по морскому дну погруженными ROV и, скорее всего, будет способствовать образованию шлейфов отложений на морском дне. [ 115 ] Идея бокового сброса заключается в том, что ROV будет сбрасывать экономически бесценный материал в сторону горного прицела перед транспортировкой сульфидного материала на поддерживающее судно на поверхности. Целью этого процесса является уменьшение количества материала, переносимого на поверхность, и минимизация наземного перемещения. [ 115 ] Процесс обезвоживания – это процесс, связанный с отходами горнодобывающей промышленности, который, скорее всего, будет способствовать образованию шлейфов отложений с поверхности. Метод утилизации шахтных отходов приводит к высвобождению с корабля воды, которая могла быть получена при добыче и транспортировке материала со дна моря на поверхность. Третьим вкладом в формирование шлейфа или облака наносов будет нарушение и выброс наносов. Этот вклад отходов горнодобывающей промышленности в основном связан с горнодобывающей деятельностью на морском дне, связанной с движением ROV и разрушительным нарушением морского дна как частью самого процесса добычи полезных ископаемых. [ 115 ]
Двумя основными экологическими проблемами, возникающими в результате процессов добычи отходов, которые способствуют образованию шлейфа наносов, являются выброс тяжелых металлов и увеличение количества выбрасываемых отложений. Выброс тяжелых металлов в основном связан с процессом обезвоживания, который будет происходить на борту корабля у поверхности воды. [ 115 ] Основная проблема, связанная с обезвоживанием, заключается в том, что это не просто выброс морской воды, повторно попадающей в толщу воды. Тяжелые металлы, такие как медь и кобальт, которые могут быть получены из материалов, добываемых на морском дне, также смешиваются с водой, которая сбрасывается в водную толщу. Первая экологическая проблема, связанная с выбросами тяжелых металлов, заключается в том, что они могут изменить химический состав океана в этой локализованной области водного столба. Вторая проблема заключается в том, что некоторые из тяжелых металлов, которые могут быть выброшены, могут иметь определенный уровень токсичности не только для организмов, населяющих эту территорию, но и для организмов, проходящих через зону добычи. [ 115 ] Опасения, связанные с увеличением выброса отложений, в основном связаны с двумя другими процессами с отходами горнодобывающей промышленности: боковыми выбросами отложений и нарушением отложений морского дна. Основной экологической проблемой будет удушение организмов, находящихся внизу, в результате перераспределения большого количества отложений в другие области морского дна, что потенциально может угрожать популяции организмов, населяющих этот район. Перераспределение большого количества осадков также может повлиять на процессы питания и газообмена между организмами, представляя серьезную угрозу для популяции. Наконец, эти процессы могут также увеличить скорость седиментации на морском дне, в результате чего прогнозируется минимум 500 м на каждые 1–10 км. [ 115 ]
В настоящее время обе вышеупомянутые компании проводят большой объем работы, чтобы обеспечить четкое понимание потенциального воздействия добычи полезных ископаемых на морское дно на окружающую среду и принятие мер контроля до начала эксплуатации. [ 116 ] Однако этому процессу, возможно, препятствует непропорциональное распределение исследовательских усилий между жерловыми экосистемами; наиболее изученные и изученные экосистемы гидротермальных жерл не являются репрезентативными для тех, которые предназначены для добычи полезных ископаемых. [ 117 ]
В прошлом предпринимались попытки добывать полезные ископаемые с морского дна. проводилось большое количество работ (и затрат) по добыче марганцевых конкреций на абиссальных равнинах В 1960-е и 1970-е годы с разной степенью успеха . Однако это демонстрирует, что извлечение полезных ископаемых с морского дна возможно и возможно уже в течение некоторого времени. Добыча марганцевых конкреций послужила прикрытием для тщательно продуманной попытки ЦРУ в 1974 году поднять затонувшую советскую подводную лодку К-129 с помощью корабля «Гломар Эксплорер» , специально построенного для этой задачи Говардом Хьюзом . [ 118 ] Операция была известна как «Проект Азориан» , и легенда о добыче марганцевых конкреций на морском дне, возможно, послужила стимулом для других компаний предпринять эту попытку.
Сохранение
[ редактировать ]Сохранение гидротермальных источников было предметом порой горячих дискуссий в океанографическом сообществе в течение последних 20 лет. [ 119 ] Было отмечено, что, возможно, наибольший ущерб этим довольно редким местам обитания наносят ученые. [ 120 ] [ 121 ] Были попытки договориться о поведении ученых, исследующих жерла, но, хотя и существует согласованный кодекс практики, формального международного и юридически обязывающего соглашения не существует. [ 122 ]
Сохранение экосистем гидротермальных жерл после факта добычи активной системы будет зависеть от реколонизации хемосинтезирующих бактерий и, следовательно, от продолжения существования гидротермальной жерловой жидкости, поскольку она является основным источником гидротермальной энергии . [ 115 ] Очень сложно получить представление о влиянии добычи полезных ископаемых на гидротермальную жидкость, поскольку крупномасштабных исследований не проводилось. [ 115 ] Однако были исследования по повторному заселению этих жерловых экосистем после вулканического разрушения. [ 123 ] Из них мы можем получить представление о потенциальных последствиях разрушения горных работ и узнали, что бактериям потребовалось 3–5 лет, чтобы повторно заселить эту территорию, и около 10 лет, чтобы мегафауна вернулась. [ 123 ] Также было обнаружено изменение видового состава экосистемы по сравнению с тем, что было до разрушения, и наличие видов-иммигрантов. [ 115 ] Хотя необходимы дальнейшие исследования влияния устойчивой добычи SMS на морском дне на реколонизацию видов.
Геохронологическое датирование
[ редактировать ]Обычными методами определения возраста гидротермальных источников являются датирование сульфидных (например, пирита ) и сульфатных минералов (например, барита ). [ 124 ] [ 125 ] [ 126 ] [ 127 ] [ 128 ] Распространенные методы датирования включают радиометрическое датирование. [ 124 ] [ 125 ] и датирование по электронному спиновому резонансу . [ 126 ] [ 127 ] [ 128 ] Различные методы датирования имеют свои ограничения, предположения и проблемы. Общие проблемы включают высокую чистоту извлеченных минералов, необходимую для датирования, возрастной диапазон каждого метода датирования, нагрев выше температуры закрытия, стирающий возраст более старых минералов, а также множественные эпизоды образования минералов, приводящие к смешению возрастов. В средах с несколькими фазами минералообразования , как правило, датирование электронным спиновым резонансом дает средний возраст основного минерала, в то время как радиометрические даты смещены в сторону возраста более молодых фаз из-за распада родительских ядер . Это объясняет, почему разные методы могут дать разный возраст одному и тому же образцу и почему в одном и том же гидротермальном дымоходе могут быть образцы разного возраста. [ 127 ] [ 128 ] [ 129 ]
См. также
[ редактировать ]| Морская среда обитания |
|---|
| Прибрежные места обитания |
| Поверхность океана |
| Открытый океан |
| Морское дно |
- Абиогенез – жизнь, возникающая из неживой материи.
- Бассейн с рассолом - скопление рассола во впадине морского дна.
- Гидротермальные жерла Индевор - группа гидротермальных жерл Тихого океана.
- Экстремофилы – организмы, способные жить в экстремальных условиях.
- Хемосинтез сероводорода - система получения энергии, используемая в гидротермальных источниках.
- Гидротермальное поле Затерянного города
- Волшебная гора (Британская Колумбия) – гидротермальное жерло на Южном хребте Эксплорер, к западу от острова Ванкувер, Британская Колумбия.
- 9 ° северной широты - область гидротермальных источников на Восточно-Тихоокеанском поднятии в Тихом океане.
- Подводная гора Пито - подводная гора в Тихом океане к северо-северо-западу от острова Пасхи.
- Подводный вулкан - подводные отверстия или трещины на поверхности Земли, из которых может извергаться магма.
- Вулканогенное месторождение массивных сульфидных руд , также известное как месторождение ВМС – Месторождение сульфидных руд металлов.
- Глубоководная добыча полезных ископаемых
Ссылки
[ редактировать ]- ^ Перейти обратно: а б с д и ж г час Колин-Гарсия, Мария (2016). «Гидротермальные источники и пребиотическая химия: обзор» . Бюллетень Мексиканского геологического общества . 68 (3): 599–620. дои : 10.18268/BSGM2016v68n3a13 .
- ^ Чанг, Кеннет (13 апреля 2017 г.). «Условия жизни обнаружены на спутнике Сатурна Энцеладе» . Нью-Йорк Таймс . Проверено 14 апреля 2017 г.
- ^ «Данные космического корабля позволяют предположить, что океан спутника Сатурна может быть источником гидротермальной активности» . НАСА . 11 марта 2015 года . Проверено 12 марта 2015 г.
- ^ Пейн, М. (15 мая 2001 г.). «Исследователи Марса получат выгоду от австралийских исследований» . Space.com . Архивировано из оригинала 21 февраля 2006 года.
- ^ Перейти обратно: а б немецкий, ЧР; Сейфрид, WE (2014), «Гидротермальные процессы» , Трактат по геохимии , Elsevier, стр. 191–233, doi : 10.1016/b978-0-08-095975-7.00607-0 , ISBN 978-0-08-098300-4 , получено 8 февраля 2024 г.
- ^ Гарсия, Елена Гихарро; Рагнарссон, Стефан Аки; Штейнгримссон, Зигмар Арнар; Невестад, Даг; Харальдссон, Хоук; Фосса, Ян Хельге; Тендал, Оле Сешер; Эйрикссон, Храфнкелл (2007). Донное траление и дноуглубительные работы в Арктике: воздействие рыболовства на нецелевые виды, уязвимые места обитания и культурное наследие . Совет министров Северных стран. п. 278. ИСБН 978-92-893-1332-2 .
- ^ Перейти обратно: а б Хаазе, К.М.; и др. (2007). «Молодой вулканизм и связанная с ним гидротермальная активность на 5 ° ю.ш. на медленно расширяющемся южном Срединно-Атлантическом хребте» . Геохимия, геофизика, геосистемы . 8 (11): Q11002. Бибкод : 2007GGG.....811002H . дои : 10.1029/2006GC001509 . S2CID 53495818 .
- ^ Перейти обратно: а б Хаазе, К.М.; и др. (2009). «Состав флюидов и минералогия осадков из гидротермальных источников Среднеатлантического хребта на 4 ° 48' ю.ш.». Пангея . дои : 10.1594/PANGAEA.727454 .
- ^ Бишофф, Джеймс Л.; Розенбауэр, Роберт Дж (1988). «Отношения жидкость-пар в критической области системы NaCl-H2O от 380 до 415°C: уточненное определение критической точки и двухфазной границы морской воды» . Geochimica et Cosmochimica Acta (Представленная рукопись). 52 (8): 2121–2126. Бибкод : 1988GeCoA..52.2121B . дои : 10.1016/0016-7037(88)90192-5 .
- ^ Фон Дамм, КЛ (1990). «Гидротермальная активность морского дна: химия черного курильщика и дымоходы» . Ежегодный обзор наук о Земле и планетах (представленная рукопись). 18 (1): 173–204. Бибкод : 1990AREPS..18..173V . doi : 10.1146/annurev.ea.18.050190.001133 .
- ^ Уэббер, АП; Мертон, Б.; Робертс, С.; Ходжкинсон, М. «Сверхкритическое вентилирование и образование VMS на гидротермальном месторождении Бибе, Каймановский центр распространения» . Тезисы докладов Гольдшмидтской конференции 2014 . Геохимическое общество. Архивировано из оригинала 29 июля 2014 года . Проверено 29 июля 2014 г.
- ^ Тайви, МК (1 декабря 1998 г.). «Как построить дымоход для черного курильщика: образование месторождений полезных ископаемых на срединно-океанических хребтах» . Океанографический институт Вудс-Хоул . Проверено 7 июля 2006 г.
- ^ Петкевич, Рэйчел (сентябрь 2008 г.). «Отслеживание океанского железа». Новости химии и техники . 86 (35): 62–63. doi : 10.1021/cen-v086n035.p062 .
- ^ Перкинс, С. (2001). «Новый тип гидротермальных источников выглядит угрожающе». Новости науки . 160 (2): 21. дои : 10.2307/4012715 . JSTOR 4012715 .
- ^ Келли, Дебора С. «Черные курильщики: инкубаторы на морском дне» (PDF) . п. 2.
- ^ Дувиль, Э; Чарлу, Дж.Л.; Олкерс, Э.Х.; Бьенвеню, П; Джоув Колон, CF; Донваль, Япония; Фуке, Ю; Приер, Д; Априу, П. (март 2002 г.). «Радужные жерла (36 ° 14' с.ш., САХ): влияние ультраосновных пород и фазового разделения на содержание микроэлементов в гидротермальных жидкостях Срединно-Атлантического хребта». Химическая геология . 184 (1–2): 37–48. Бибкод : 2002ЧГео.184...37Д . дои : 10.1016/S0009-2541(01)00351-5 .
- ^ Перейти обратно: а б Шписс, ФН; Макдональд, КК; Этуотер, Т.; Баллард, Р.; Карранса, А.; Кордова, Д.; Кокс, К.; Гарсия, ВМД; Франшето, Дж.; Герреро, Дж.; Хокинс, Дж.; Хэймон, Р. ; Хесслер, Р.; Жуто, Т.; Кастнер, М.; Ларсон, Р.; Луендык, Б.; Макдугалл, доктор медицинских наук; Миллер, С.; Нормарк, В.; Оркатт, Дж.; Ранджин, К. (28 марта 1980 г.). «Восточно-Тихоокеанское поднятие: горячие источники и геофизические эксперименты». Наука . 207 (4438): 1421–1433. Бибкод : 1980Sci...207.1421S . дои : 10.1126/science.207.4438.1421 . ПМИД 17779602 . S2CID 28363398 .
- ^ «Кипящая горячая вода найдена в холодном арктическом море» . ЖиваяНаука . 24 июля 2008 года . Проверено 25 июля 2008 г.
- ^ «Ученые побили рекорд, обнаружив самое северное гидротермальное поле» . Наука Дейли . 24 июля 2008 года . Проверено 25 июля 2008 г.
- ^ Кросс, А. (12 апреля 2010 г.). «Самые глубокие в мире подводные источники обнаружены в Карибском бассейне» . Новости Би-би-си . Проверено 13 апреля 2010 г.
- ^ Перейти обратно: а б с д и ж г час я дж к л немецкий, ЧР; Сейфрид, МЫ (01 января 2014 г.), Голландия, Генрих Д.; Турекян, Карл К. (ред.), «8.7 – Гидротермальные процессы» , Трактат по геохимии (второе издание) , Oxford: Elsevier, стр. 191–233, doi : 10.1016/b978-0-08-095975-7.00607-0 , ISBN 978-0-08-098300-4 , получено 25 февраля 2024 г.
- ^ Перейти обратно: а б с Гартман, Эми; Финдли, Алисса Дж. (июнь 2020 г.). «Воздействие процессов гидротермальных шлейфов на океанические циклы и перенос металлов» . Природа Геонауки . 13 (6): 396–402. Бибкод : 2020NatGe..13..396G . дои : 10.1038/s41561-020-0579-0 . ISSN 1752-0908 .
- ^ Перейти обратно: а б с Сандер, СГ; Кощинский А. (2016), Демина Людмила Л.; Галкин, Сергей В. (ред.), «Экспорт железа и других микроэлементов из гидротермальных жерл и влияние на их морской биогеохимический цикл» , Биогеохимия микроэлементов и экология глубоководных гидротермальных жерловых систем , Справочник по химии окружающей среды. , Чам: Springer International Publishing, стр. 9–24, номер документа : 10.1007/698_2016_4. , ISBN 978-3-319-41340-2 , получено 8 марта 2024 г.
- ^ Беллотти, Э.; Брогджини, К.; Ди Карло, Дж.; Лаубенштайн, М.; Менегаццо, Р. (апрель 2015 г.). «Точное измерение периода полураспада 222Rn: зонд для контроля стабильности радиоактивности» . Буквы по физике Б. 743 : 526–530. arXiv : 1501.07757 . doi : 10.1016/j.physletb.2015.03.021 .
- ^ Перейти обратно: а б с Эванс, Гай Н.; Сейфрид, Уильям Э.; Тан, Чуньян (январь 2023 г.). «Питательные переходные металлы во временных рядах гидротермальных жерловых флюидов с месторождения Мейн-Индевор, хребет Хуан-де-Фука, Тихий океан» . Письма о Земле и планетологии . 602 : 117943. Бибкод : 2023E&PSL.60217943E . дои : 10.1016/j.epsl.2022.117943 . ISSN 0012-821X .
- ^ Перейти обратно: а б Бруланд, Кеннет В.; Донат, Джон Р.; Хатчинс, Дэвид А. (декабрь 1991 г.). «Интерактивное влияние биологически активных микроэлементов на биологическую продукцию в океанических водах» . Лимнология и океанография . 36 (8): 1555–1577. Бибкод : 1991LimOc..36.1555B . дои : 10.4319/lo.1991.36.8.1555 .
- ^ Вайс, Мэдлин С.; Соуза, Филиппа Л.; Мрнявац, Наталья; Нойкирхен, Синье; Реттгер, Мэйо; Нельсон-Сати, Шиджулал; Мартин, Уильям Ф. (25 июля 2016 г.). «Физиология и среда обитания последнего всеобщего общего предка» . Природная микробиология . 1 (9): 16116. doi : 10.1038/nmicrobiol.2016.116 . ISSN 2058-5276 . ПМИД 27562259 .
- ^ Рамирес-Льодра, Э; Кейт, окружной прокурор (2020). «M3.7 Экосистемы на основе хемосинтеза (CBE)» . В Ките, округ Колумбия; Феррер-Париж-младший; Николсон, Э.; Кингсфорд, RT (ред.). Типология глобальной экосистемы МСОП 2.0: Описательные профили биомов и функциональных групп экосистем . Гланд, Швейцария: МСОП. doi : 10.2305/IUCN.CH.2020.13.en . ISBN 978-2-8317-2077-7 . S2CID 241360441 .
- ^ Горячие источники на морском дне - важный источник железа в океанах.
- ^
«Крайности города Угря» . Журнал астробиологии . 28 мая 2008 г. Архивировано из оригинала 28 июня 2011 г. Проверено 30 августа 2007 г.
{{cite web}}: CS1 maint: неподходящий URL ( ссылка ) - ^ Сысоев А.В.; Кантор, Ю. И. (1995). «Два новых вида Phymorhynchus (Gastropoda, Conoidea, Conidae) из гидротермальных источников» (PDF) . Рутеница . 5 : 17–26.
- ^ Ботос, С. «Жизнь на гидротермальном источнике» . Гидротермальные жерла .
- ^ Ван Довер, К. Л. «Актуальные темы: биогеография фаун глубоководных гидротермальных жерл» . Океанографический институт Вудс-Хоул.
- ^ Битти, Джей Ти; и др. (2005). «Облигатно фотосинтезирующий бактериальный анаэроб из глубоководных гидротермальных источников» . Труды Национальной академии наук . 102 (26): 9306–10. Бибкод : 2005PNAS..102.9306B . дои : 10.1073/pnas.0503674102 . ПМК 1166624 . ПМИД 15967984 .
- ^ Додд, Мэтью С.; Папино, Доминик; Гренн, Тор; Слэк, Джон Ф.; Риттнер, Мартин; Пирайно, Франко; О'Нил, Джонатан; Литтл, Криспин Т.С. (2 марта 2017 г.). «Доказательства ранней жизни в осадках старейших гидротермальных источников Земли» (PDF) . Природа . 543 (7643): 60–64. Бибкод : 2017Natur.543...60D . дои : 10.1038/nature21377 . ПМИД 28252057 . S2CID 2420384 .
- ^ Циммер, Карл (1 марта 2017 г.). «Ученые говорят, что окаменелости канадских бактерий могут быть древнейшими на Земле» . Нью-Йорк Таймс . Проверено 2 марта 2017 г.
- ^ Гош, Паллаб (1 марта 2017 г.). «Найдены самые ранние свидетельства жизни на Земле » . Новости Би-би-си . Проверено 2 марта 2017 г.
- ^ Из Дувра, 2000 г. [ нужна полная цитата ]
- ^ Лонсдейл, Питер (1977). «Скопление макробентоса, питающегося взвесью, возле глубинных гидротермальных источников в центрах океанического спрединга». Глубоководные исследования . 24 (9): 857–863. Бибкод : 1977DSR....24..857L . дои : 10.1016/0146-6291(77)90478-7 . S2CID 128478123 .
- ^ Кавана и др. 1981 [ нужна полная цитата ]
- ^ Фелбак 1981 [ нужна полная цитата ]
- ^ За 1981 год [ нужна полная цитата ]
- ^ Кавано 1983 [ нужна полная цитата ]
- ^ Фиала-Медиони, А. (1984). «Ультраструктурные доказательства обилия внутриклеточных симбиотических бактерий в жабрах двустворчатых моллюсков глубоких гидротермальных источников». Comptes rendus de l'Académie des Sciences . 298 (17): 487–492.
- ^ Ле Пеннек, М.; Хили, А. (1984). «Анатомия, структура и ультраструктура жабр митилид гидротермальных участков восточной части Тихого океана». Oceanologica Acta (на французском языке). 7 (4): 517–523.
- ^ Флорес, Дж. Ф.; Фишер, ЧР; Карни, СЛ; Грин, Б.Н.; Фрейтаг, Дж. К.; Шеффер, SW; Ройер, МЫ (2005). «Связывание сульфида опосредовано ионами цинка, обнаруженными в кристаллической структуре гемоглобина гидротермальных жерловых червей» . Труды Национальной академии наук . 102 (8): 2713–2718. Бибкод : 2005PNAS..102.2713F . дои : 10.1073/pnas.0407455102 . ПМК 549462 . ПМИД 15710902 .
- ^ Тиль, Вера; Хюглер, Михаэль; Блюмель, Мартина; Бауманн, Хайке И.; Гертнер, Андреа; Шмальйоханн, Рольф; Штраус, Харальд; Гарбе-Шенберг, Дитер; Петерсен, Свен; Коварт, Доминик А.; Фишер, Чарльз Р.; Имхофф, Йоханнес Ф. (2012). «Широкое распространение двух путей фиксации углерода у эндосимбионтов трубчатых червей: уроки, полученные от трубчатых червей, связанных с гидротермальными источниками, из Средиземного моря» . Границы микробиологии . 3 : 423. дои : 10.3389/fmicb.2012.00423 . ПМК 3522073 . ПМИД 23248622 .
- ^ Штейн и др. 1988 г. [ нужна полная цитата ]
- ^ Биология глубокого моря, Питер Херринг [ нужна полная цитата ]
- ^ Ван Довер и др. 1988 г. [ нужна полная цитата ]
- ^ Дебрюйер и др. 1985 г. [ нужна полная цитата ]
- ^ де Бург, Мэн; Сингла, CL (декабрь 1984 г.). «Бактериальная колонизация и эндоцитоз на жабрах нового вида блюдечек из гидротермальных источников». Морская биология . 84 (1): 1–6. Бибкод : 1984МарБи..84....1D . дои : 10.1007/BF00394520 . S2CID 85072202 .
- ^ Вахтерсхаузер, Г. (1 января 1990 г.). «Эволюция первых метаболических циклов» . Труды Национальной академии наук . 87 (1): 200–204. Бибкод : 1990PNAS...87..200W . дои : 10.1073/pnas.87.1.200 . ПМЦ 53229 . ПМИД 2296579 .
- ^ Танниклифф, В. (1991). «Биология гидротермальных источников: экология и эволюция». Океанография и морская биология: Ежегодный обзор . 29 : 319–408.
- ^ Чандру, Кухан; Имаи, ЭйИчи; Канеко, Такео; Обаяси, Юмико; Кобаяши, Кенсей (2013). «Выживаемость и абиотические реакции избранных аминокислот в различных симуляторах гидротермальных систем». Происхождение жизни и биосферы . 43 (2): 99–108. Бибкод : 2013OLEB...43...99C . дои : 10.1007/s11084-013-9330-9 . ПМИД 23625039 . S2CID 15200910 .
- ↑ Химия горячих источников морского дна может объяснить возникновение жизни . Журнал «Астробиология», 27 апреля 2015 г.
- ^ Ролдан, А.; Холлингсворт, Н.; Роффи, А.; Ислам, Х.-У.; Гудолл, JBM; Кэтлоу, CRA; Дарр, Дж.А.; Брас, В.; Санкар, Г.; Холт, КБ; Хогарта, Г.; де Леу, Нью-Хэмпшир (24 марта 2015 г.). «Биологическая конверсия CO 2 с помощью катализаторов на основе сульфида железа в устойчивых условиях» (PDF) . Химические коммуникации . 51 (35): 7501–7504. дои : 10.1039/C5CC02078F . ПМИД 25835242 . S2CID 217970758 .
- ^ Обри, AD; Кливс, HJ; Бада, Дж.Л. (2008). «Роль подводных гидротермальных систем в синтезе аминокислот». Происхождение жизни и биосферы . 39 (2): 91–108. Бибкод : 2009ОЛЕВ...39...91А . дои : 10.1007/s11084-008-9153-2 . ПМИД 19034685 . S2CID 207224268 .
- ^ «Гидроочистка сверхкритических углекислых экстрактов лигноцеллюлозной биосырья гидротермального сжижения» . dx.doi.org . doi : 10.1021/acs.iecr.2c02109.s001 . Проверено 6 апреля 2024 г.
- ^ Перейти обратно: а б Сибуя, Таказо; Такай, Кен (16 ноября 2022 г.). «Жидкий и сверхкритический CO2 как органический растворитель в гидротермальных системах морского дна Гаде: значение для пребиотической химической эволюции» . Прогресс в науке о Земле и планетологии . 9 (1). дои : 10.1186/s40645-022-00510-6 . ISSN 2197-4284 .
- ^ Найт, Ханна; Депанье-Аюб, Эммануэль; Мар Диас-Рекехо, М.; Диас-Родригес, Дон; Гонсалес-Нуньес, Мария Елена; Мелло, Росселла; Муньос, Бьянка К.; Глаз, Вильфрид-Соло; Асенсио, Грегори; Стивен, Майкл; Перес, Питер Дж. (13 мая 2011 г.). «Катализируемое серебром образование связи постоянного тока между метаном и этилдиазоацетатом в сверхкритическом CO 2 » . Наука 332 (6031): 835–838. Бибкод : 2011Sci...332..835C . дои : 10.1126/science.1204131 . hdl : 10272/11557 . ISSN 0036-8075 . ПМИД 21566191 .
- ^ Дил, Александра М.; Рапф, Ребекка Дж.; Вайда, Вероника (12 мая 2021 г.). «Взаимодействие вода-воздух как среда для решения водного парадокса в химии пребиотиков: взгляд на физическую химию» . Журнал физической химии А. 125 (23): 4929–4942. Бибкод : 2021JPCA..125.4929D . doi : 10.1021/acs.jpca.1c02864 . ISSN 1089-5639 . ПМИД 33979519 .
- ↑ Джозеф Ф. Сазерленд: о происхождении бактерий и архей , от 16 августа 2014 г.
- ^ Ник Лейн: Жизненно важный вопрос - энергия, эволюция и происхождение сложной жизни , WW Norton, 20 июля 2015 г., ISBN 978-0-393-08881-6 , PDF, заархивировано 10 сентября 2017 г. в Wayback Machine.
- ^ Лейн, Ник; Аллен, Джон Ф.; Мартин, Уильям (26 марта 2010 г.). «Как LUCA зарабатывала на жизнь? Хемиосмос в зарождении жизни» . Биоэссе . 32 (4): 271–280. дои : 10.1002/bies.200900131 . ISSN 0265-9247 . ПМИД 20108228 .
- ^ Перейти обратно: а б Лейн, Ник (15 мая 2017 г.). «Протонные градиенты в возникновении жизни» . Биоэссе . 39 (6). doi : 10.1002/bies.201600217 . ISSN 0265-9247 . ПМИД 28503790 .
- ^ Перейти обратно: а б Гальперин, Михаил Ю. (17 ноября 2017 г.). «Рекомендации профессорско-преподавательского состава о естественных градиентах pH в гидротермальных щелочных источниках вряд ли сыграли роль в возникновении жизни». дои : 10.3410/f.726652474.793539164 .
{{cite web}}: Отсутствует или пусто|url=( помощь ) - ^ Да Силва, Лаура; Морель, Мари-Кристин; Димер, Дэвид (01 февраля 2015 г.). «Синтез РНК-подобных молекул, стимулируемый солью, в моделируемых гидротермальных условиях» . Журнал молекулярной эволюции . 80 (2): 86–97. Бибкод : 2015JMolE..80...86D . дои : 10.1007/s00239-014-9661-9 . ISSN 1432-1432 . ПМИД 25487518 . S2CID 15603239 .
- ^ Патель, Бхавеш Х.; Персиваль, Клаудия; Ритсон, Дугал Дж.; Даффи, Колм Д.; Сазерленд, Джон Д. (16 марта 2015 г.). «Общее происхождение предшественников РНК, белков и липидов в цианосульфидном протометаболизме» . Природная химия . 7 (4): 301–307. Бибкод : 2015НатЧ...7..301П . дои : 10.1038/nchem.2202 . ISSN 1755-4349 . ПМК 4568310 . ПМИД 25803468 .
- ^ Димер, Дэвид; Дамер, Брюс; Компаниченко Владимир (01.12.2019). «Гидротермальная химия и происхождение клеточной жизни» . Астробиология . 19 (12): 1523–1537. Бибкод : 2019AsBio..19.1523D . doi : 10.1089/ast.2018.1979 . ISSN 1531-1074 . ПМИД 31596608 . S2CID 204029724 .
- ^ Пирс, Бен К.Д.; Пудриц, Ральф Э.; Семенов Дмитрий А.; Хеннинг, Томас К. (24 октября 2017 г.). «Происхождение мира РНК: судьба нуклеиновых оснований в теплых прудах» . Труды Национальной академии наук . 114 (43): 11327–11332. arXiv : 1710.00434 . Бибкод : 2017PNAS..11411327P . дои : 10.1073/pnas.1710339114 . ISSN 0027-8424 . ПМК 5664528 . ПМИД 28973920 .
- ^ Дамер, Брюс; Димер, Дэвид (01 апреля 2020 г.). «Гипотеза происхождения жизни из горячих источников» . Астробиология . 20 (4): 429–452. Бибкод : 2020AsBio..20..429D . дои : 10.1089/ast.2019.2045 . ISSN 1531-1074 . ПМЦ 7133448 . ПМИД 31841362 .
- ^ Рассел, Майкл Дж.; Бардж, Лаура М.; Бхартиа, Рохит; Боканегра, Дилан; Брейчер, Пол Дж.; Бранскомб, Элберт; Кидд, Ричард; МакГлинн, Шон; Мейер, Дэвид Х.; Ничке, Вольфганг; Сибуя, Таказо; Вэнс, Стив; Уайт, Лорен; Каник, Исик (01 апреля 2014 г.). «Путь к жизни во влажных и ледяных мирах» . Астробиология . 14 (4): 308–343. Бибкод : 2014AsBio..14..308R . дои : 10.1089/ast.2013.1110 . ISSN 1531-1074 . ПМЦ 3995032 . ПМИД 24697642 .
- ^ Бааске, Филипп; Вайнерт, Франц М.; Дур, Стефан; Лемке, Коно Х.; Рассел, Майкл Дж.; Браун, Дитер (29 мая 2007 г.). «Чрезвычайное накопление нуклеотидов в смоделированных гидротермальных поровых системах» . Труды Национальной академии наук . 104 (22): 9346–9351. дои : 10.1073/pnas.0609592104 . ISSN 0027-8424 . ПМК 1890497 . ПМИД 17494767 .
- ^ Уэст, Тимоти; Соджо, Виктор; Помянковский, Эндрю; Лейн, Ник (05 декабря 2017 г.). «Происхождение наследственности в протоклетках» . Философские труды Королевского общества B: Биологические науки . 372 (1735): 20160419. doi : 10.1098/rstb.2016.0419 . ISSN 0962-8436 . ПМЦ 5665807 . ПМИД 29061892 .
- ^ Уичер, Александра; Кампруби, Элои; Пинна, Сильвана; Херши, Барри; Лейн, Ник (01 июня 2018 г.). «Ацетилфосфат как первичная энергетическая валюта в зарождении жизни» . Происхождение жизни и эволюция биосфер . 48 (2): 159–179. Бибкод : 2018OLEB...48..159W . дои : 10.1007/s11084-018-9555-8 . ISSN 1573-0875 . ПМК 6061221 . ПМИД 29502283 .
- ^ Нуньес Палмейра, Ракель; Колнаги, Марко; Харрисон, Стюарт А.; Помянковский, Эндрю; Лейн, Ник (9 ноября 2022 г.). «Границы метаболической наследственности в протоклетках» . Труды Королевского общества B: Биологические науки . 289 (1986). дои : 10.1098/rspb.2022.1469 . ISSN 0962-8452 . ПМЦ 9653231 . ПМИД 36350219 .
- ^ Харрисон, Стюарт А.; Лейн, Ник (12 декабря 2018 г.). «Жизнь как руководство к синтезу пребиотических нуклеотидов» . Природные коммуникации . 9 (1): 5176. Бибкод : 2018NatCo...9.5176H . дои : 10.1038/s41467-018-07220-y . ISSN 2041-1723 . ПМК 6289992 . ПМИД 30538225 .
- ^ Пинна, Сильвана; Кунц, Сесилия; Халперн, Аарон; Харрисон, Стюарт А.; Джордан, Шон Ф.; Уорд, Джон; Вернер, Финн; Лейн, Ник (04 октября 2022 г.). «Пребиотическая основа АТФ как универсальной энергетической валюты» . ПЛОС Биология . 20 (10): e3001437. дои : 10.1371/journal.pbio.3001437 . ISSN 1545-7885 . ПМЦ 9531788 . ПМИД 36194581 .
- ^ Соджо, Виктор; Помянковский, Эндрю; Лейн, Ник (12 августа 2014 г.). «Биоэнергетическая основа дивергенции мембран архей и бактерий» . ПЛОС Биология . 12 (8): e1001926. дои : 10.1371/journal.pbio.1001926 . ISSN 1545-7885 . ПМК 4130499 . ПМИД 25116890 .
- ^ Харрисон, Стюарт А.; Палмейра, Ракель Нуньес; Халперн, Аарон; Лейн, Ник (01 ноября 2022 г.). «Биофизическая основа возникновения генетического кода в протоклетках» . Biochimica et Biophysica Acta (BBA) — Биоэнергетика . 1863 (8): 148597. doi : 10.1016/j.bbabio.2022.148597 . ISSN 0005-2728 . PMID 35868450 . S2CID 250707510 .
- ^ Аменд, Ян П.; ЛаРоу, Дуглас Э.; Макколлом, Томас М.; Шок, Эверетт Л. (19 июля 2013 г.). «Энергетика органического синтеза внутри и вне клетки» . Философские труды Королевского общества B: Биологические науки . 368 (1622): 20120255. doi : 10.1098/rstb.2012.0255 . ISSN 0962-8436 . ПМЦ 3685458 . ПМИД 23754809 .
- ^ Голд, Т. (1992). «Глубокая горячая биосфера» . Труды Национальной академии наук . 89 (13): 6045–9. Бибкод : 1992PNAS...89.6045G . дои : 10.1073/pnas.89.13.6045 . ПМЦ 49434 . ПМИД 1631089 .
- ^
Голд, Т. (1992). Глубокая, горячая биосфера . Том. 89. Springer Science+Business Media. стр. 6045–6049. Бибкод : 1992PNAS...89.6045G . дои : 10.1073/pnas.89.13.6045 . ISBN 978-0-387-95253-6 . ПМЦ 49434 . ПМИД 1631089 .
{{cite book}}:|journal=игнорируется ( помогите ) - ^ Проскуровский Г.; Лилли, доктор медицины; Зеевальд, Дж. С.; Фру ч-Грин, GL; Олсон, Э.Дж.; Луптон, Дж. Э.; Сильва, СП; Келли, DS (1 февраля 2008 г.). «Добыча абиогенных углеводородов на гидротермальном месторождении Лост-Сити». Наука . 319 (5863): 604–607. дои : 10.1126/science.1151194 . ПМИД 18239121 . S2CID 22824382 .
- ^ Дегенс, ET (1969). Горячие рассолы и новейшие месторождения тяжелых металлов в Красном море . Спрингер-Верлаг. [ нужна страница ]
- ^ Кэтлин., Крейн (2003). Морские ноги: рассказы женщины-океанографа . Боулдер, Колорадо: Westview Press. ISBN 9780813342856 . OCLC 51553643 . [ нужна страница ]
- ^ «Что такое гидротермальное жерло?» . Национальная океаническая служба . Национальное управление океанических и атмосферных исследований . Проверено 10 апреля 2018 г.
- ^ Лонсдейл, П. (1977). «Скопление макробентоса, питающегося взвесью, возле глубинных гидротермальных источников в центрах океанического распространения». Глубоководные исследования . 24 (9): 857–863. Бибкод : 1977DSR....24..857L . дои : 10.1016/0146-6291(77)90478-7 . S2CID 128478123 .
- ^ Крейн, Кэтлин; Нормарк, Уильям Р. (10 ноября 1977 г.). «Гидротермальная активность и структура гребня Восточно-Тихоокеанского поднятия на 21 ° с.ш.». Журнал геофизических исследований . 82 (33): 5336–5348. Бибкод : 1977JGR....82.5336C . дои : 10.1029/jb082i033p05336 .
- ^ Перейти обратно: а б «Ныряй и открывай: Экспедиции на морское дно» . www.divediscover.whoi.edu . Проверено 4 января 2016 г.
- ^ Дэвис, Ребекка; Джойс, Кристофер (5 декабря 2011 г.). «Глубоководная находка, изменившая биологию» . NPR.org . Проверено 9 апреля 2018 г.
- ^ Корлисс, Джон Б.; Даймонд, Джек; Гордон, Луи И.; Эдмонд, Джон М.; фон Герцен, Ричард П.; Баллард, Роберт Д.; Грин, Кеннет; Уильямс, Дэвид; Бейнбридж, Арнольд; Крейн, Кэти; ван Андел, Тьерд Х. (16 марта 1979 г.). «Подводные термальные источники на Галапагосском разломе». Наука . 203 (4385): 1073–1083. Бибкод : 1979Sci...203.1073C . дои : 10.1126/science.203.4385.1073 . ПМИД 17776033 . S2CID 39869961 .
- ^ Франшето, Дж (1979). «На Восточно-Тихоокеанском поднятии обнаружены массивные глубоководные месторождения сульфидных руд» (PDF) . Природа . 277 (5697): 523. Бибкод : 1979Natur.277..523F . дои : 10.1038/277523a0 . S2CID 4356666 .
- ^ Веб-сайт WHOI
- ^ Макдональд, КК; Беккер, Кейр; Шписс, ФН; Баллард, Р.Д. (1980). «Гидротермальный тепловой поток жерл «черного курильщика» на Восточно-Тихоокеанском поднятии». Письма о Земле и планетологии . 48 (1): 1–7. Бибкод : 1980E&PSL..48....1M . дои : 10.1016/0012-821X(80)90163-6 .
- ^ Хэймон, Рэйчел М .; Кастнер, Мириам (1981). «Отложения горячих источников на Восточно-Тихоокеанском поднятии на 21 ° с.ш.: предварительное описание минералогии и генезиса». Письма о Земле и планетологии . 53 (3): 363–381. Бибкод : 1981E&PSL..53..363H . дои : 10.1016/0012-821X(81)90041-8 .
- ^ «Новое подводное отверстие наводит на мысль о мифологии со змееголовыми» (пресс-релиз). ЭврекАлерт! . 18 апреля 2007 года . Проверено 18 апреля 2007 г.
- ^ «Биби» . База данных межриджских вентиляционных каналов.
- ^ немецкий, ЧР; и др. (2010). «Различные стили подводной вентиляции на сверхмедленно распространяющемся поднятии Среднего Каймана» (PDF) . Труды Национальной академии наук . 107 (32): 14020–5. Бибкод : 2010PNAS..10714020G . дои : 10.1073/pnas.1009205107 . ПМЦ 2922602 . ПМИД 20660317 . Проверено 31 декабря 2010 г.
- «Исследование гидротермальных источников на дне океана — гейзеров, соблазняющих астробиологов» . Научный Гуру . 11 октября 2010 г. Архивировано из оригинала 18 октября 2010 г.
- ^ Шукман, Дэвид (21 февраля 2013 г.). «Самые глубокие подводные источники обнаружены британской командой» . Новости Би-би-си . Проверено 21 февраля 2013 г.
- ^ Броуд, Уильям Дж. (12 января 2016 г.). «Вулкан длиной 40 000 миль» . Нью-Йорк Таймс . ISSN 0362-4331 . Проверено 17 января 2016 г.
- ^ Леаль-Акоста, Мария Луиза; Прол-Ледесма, Роза Мария (2016). «Геохимическая характеристика приливно-отливных термических проявлений залива Консепсьон на полуострове Нижняя Калифорния » . Бюллетень Мексиканского геологического общества (на испанском языке). 68 (3): 395–407. дои : 10.18268/bsgm2016v68n3a2 . JSTOR 24921551 .
- ^ Болье, Стэйс Э.; Бейкер, Эдвард Т.; Герман, Кристофер Р.; Маффеи, Эндрю (ноябрь 2013 г.). «Авторитетная глобальная база данных по активным подводным гидротермальным полям» . Геохимия, геофизика, геосистемы . 14 (11): 4892–4905. Бибкод : 2013GGG....14.4892B . дои : 10.1002/2013GC004998 . hdl : 1912/6496 . S2CID 53604809 .
- ^ Роджерс, Алекс Д.; Тайлер, Пол А.; Коннелли, Дуглас П.; Копли, Джон Т.; Джеймс, Рэйчел; Лартер, Роберт Д.; Линсе, Катрин; Миллс, Рэйчел А.; Гарабато, Альфредо Навейра; Панкост, Ричард Д.; Пирс, Дэвид А.; Полунин, Николай В.К.; Герман, Кристофер Р.; Шанк, Тимоти; Бурш-Супан, Филипп Х.; Алкер, Белинда Дж.; Аквилина, Альфред; Беннетт, Сара А.; Кларк, Эндрю; Динли, Роберт Джей-Джей; Грэм, Аластер Г.К.; Грин, Дэррил Р.Х.; Хоукс, Джеффри А.; Хепберн, Лора; Иларио, Ана; Ювенн, Верле А.И.; Марш, Ли; Рамирес-Льодра, Ева; Рид, Уильям Д.К.; Ротерман, Кристофер Н.; Свитинг, Кристофер Дж.; Татье, Свен; Цвирглмайер, Катрин; Эйзен, Джонатан А. (3 января 2012 г.). «Открытие новых глубоководных гидротермальных сообществ в Южном океане и последствия для биогеографии» . ПЛОС Биология . 10 (1): e1001234. дои : 10.1371/journal.pbio.1001234 . ПМК 3250512 . ПМИД 22235194 .
- ^ Перкинс, WG (1 июля 1984 г.). «Кремнеземные доломиты и медные рудные тела горы Иса; результат системы синтектонических гидротермальных изменений». Экономическая геология . 79 (4): 601–637. Бибкод : 1984EcGeo..79..601P . дои : 10.2113/gsecongeo.79.4.601 .
- ^ Перейти обратно: а б Мы собираемся начать добычу гидротермальных источников на дне океана. Архивировано 17 января 2022 г. на Wayback Machine . Наутилус ; Брэндон Кейм. 12 сентября 2015 г.
- ^ Джинли, С.; Дикруп, Д.; Ханнингтон, М. (2014). «Классификация минералогии и геохимии формации полосчатого железа типа Алгома, Темагами, Онтарио» (PDF) . Проверено 14 ноября 2017 г.
- ^ «Рассвет глубоководной добычи полезных ископаемых в океане» . Все, что мне нужно . 2006. Архивировано из оригинала 03 марта 2021 г. Проверено 21 августа 2008 г.
- ^ Правительство Канады, Министерство международных отношений Канады (23 января 2017 г.). «Обзор рынка горнодобывающей отрасли в 2016 году – Япония» . www.tradecommissioner.gc.ca . Проверено 11 марта 2019 г.
- ^ «Освобождение ресурсов Японии» . Джапан Таймс . 25 июня 2012 г.
- ^ «Наутилус очерчивает сульфидную зону морского дна с высоким содержанием золота и меди» (пресс-релиз). Наутилус Минералс. 25 мая 2006 г. Архивировано из оригинала 29 января 2009 г.
- ^ «Нептун Минералы» . Проверено 2 августа 2012 г.
- ^ Бирни, К.; и др. «Потенциальная глубоководная добыча массивных сульфидов морского дна: пример из Папуа-Новой Гвинеи» (PDF) . Калифорнийский университет, Санта-Барбара, Б. Архивировано из оригинала (PDF) 23 сентября 2015 г. Проверено 22 ноября 2009 г.
- ^ Перейти обратно: а б с д и ж г час я дж к л м н тот п Миллер, Кэтрин А.; Томпсон, Кирстен Ф.; Джонстон, Пол; Сантильо, Дэвид (2018). «Обзор добычи полезных ископаемых на морском дне, включая текущее состояние развития, воздействие на окружающую среду и пробелы в знаниях» . Границы морской науки . 4 . дои : 10.3389/fmars.2017.00418 . hdl : 10871/130175 . ISSN 2296-7745 .
- ^ «Сокровища из глубин» . Химический мир . Январь 2007 года.
- ^ Амон, Дива; Талер, Эндрю Д. (06 августа 2019 г.). «262 путешествия под морем: глобальная оценка биоразнообразия макро- и мегафауны и исследования глубоководных гидротермальных источников» . ПерДж . 7 : е7397. дои : 10.7717/peerj.7397 . ISSN 2167-8359 . ПМК 6688594 . ПМИД 31404427 .
- ^ Тайна на дне океана . Дэвид Шукман, BBC News . 19 февраля 2018 г.
- ^ Деви, CW; Фишер, ЧР; Скотт, С. (2007). «Ответственная наука в гидротермальных источниках» (PDF) . Океанография . 20 (1): 162–72. дои : 10.5670/oceanog.2007.90 . Архивировано из оригинала (PDF) 23 июля 2011 г.
- ^ Джонсон, М. (2005). «Океаны тоже нуждаются в защите со стороны ученых» . Природа . 433 (7022): 105. Бибкод : 2005Natur.433..105J . дои : 10.1038/433105a . ПМИД 15650716 . S2CID 52819654 .
- ^ Джонсон, М. (2005). «Глубоководные жерла должны стать объектами всемирного наследия» . Новости МПА . 6:10 .
- ^ Тайлер, П.; Герман, К.; Танниклифф, В. (2005). «Биологи не представляют угрозы глубоководным жерлам» . Природа . 434 (7029): 18. Бибкод : 2005Natur.434...18T . дои : 10.1038/434018b . ПМИД 15744272 . S2CID 205033213 .
- ^ Перейти обратно: а б Маллино, Лорен С.; Метаксас, Анна; Болье, Стэйс Э.; Ярко, Моника; Голлнер, Сабина; Групе, Бенджамин М.; Эррера, Сантьяго; Келлнер, Джули Б.; Левин, Лиза А.; Митарай, Сатоши; Нойберт, Майкл Г.; Турнгерр, Андреас М.; Танниклифф, Верена; Ватанабэ, Хироми К.; Вон, Ён Джин (21 февраля 2018 г.). «Изучение экологии глубоководных гидротермальных источников в рамках метасообщества» . Границы морской науки . 5 : 49. дои : 10.3389/fmars.2018.00049 . hdl : 1912/10332 . ISSN 2296-7745 .
- ^ Перейти обратно: а б Вы, К.-Ф.; Бикл, MJ (август 1998 г.). «Эволюция активного месторождения массивных сульфидов на морском дне» . Природа . 394 (6694): 668–671. Бибкод : 1998Natur.394..668Y . дои : 10.1038/29279 . ISSN 0028-0836 . S2CID 4379956 .
- ^ Перейти обратно: а б Ногучи, Такуро; Синдзё, Рюичи; Ито, Мичихиро; Такада, Джицуя; Оомори, Тамоцу (2011). «Геохимия барита из гидротермальных труб Окинавского прогиба: понимание формирования труб и взаимодействия жидкости и осадков» . Журнал минералогических и петрологических наук 106 (1): 26–35. Бибкод : 2011JMPeS.106... 26N дои : 10.2465/jmps.090825 . ISSN 1345-6296 . S2CID 129266361 .
- ^ Перейти обратно: а б Такамаса, Асако; Накаи, Шуничи; Сато, Фумихиро; Тойода, Шин; Банерджи, Дебабрата; Исибаши, Дзюнъитиро (февраль 2013 г.). «Радиоактивное неравновесие U – Th и ЭПР-датирование баритсодержащей сульфидной коры Южно-Марианского прогиба» . Четвертичная геохронология . 15 : 38–46. Бибкод : 2013QuGeo..15...38T . дои : 10.1016/j.quageo.2012.12.002 . S2CID 129020357 .
- ^ Перейти обратно: а б с Фудзивара, Тайсей, Учида, Ай; Исибаши, Дзюнъитиро, Такамаса, Асако (2015), Исибаши, Дзюнъитиро; Сунамура, Мичинари (ред.) ЭПР-датирование барита в донных гидротермальных сульфидных отложениях Окинавского прогиба", Подводная биосфера, связанная с гидротермальными системами , Токио: Springer Japan, стр. 369–386, doi : 10.1007/978-4-431-54865-2_29 , ISBN 978-4-431-54864-5
- ^ Перейти обратно: а б с Цанг, Мань-Инь; Тойода, Шин; Томита, Макико; Ямамото, Юдзуру (01 августа 2022 г.). «Термическая стабильность и температура смыкания барита для датирования электронным спиновым резонансом» . Четвертичная геохронология . 71 : 101332. Бибкод : 2022QuGeo..7101332T . дои : 10.1016/j.quageo.2022.101332 . ISSN 1871-1014 . S2CID 248614826 .
- ^ Учида, Ай; Тойода, Шин; Исибаши, Дзюнъитиро; Накаи, Шуничи (2015), Исибаши, Дзюнъитиро; Окино, Кёко; Сунамура, Мичинари (ред.), «Датирование барита по 226Ra-210Pb и 228Ra-228Th в подводных гидротермальных сульфидных отложениях, собранных в Окинавском и Южном Марианском прогибах», Подводная биосфера, связанная с гидротермальными системами: Концепция TAIGA , Токио: Springer Japan , стр. 607–615, doi : 10.1007/978-4-431-54865-2_47 , ISBN. 978-4-431-54865-2 , S2CID 129751032
Дальнейшее чтение
[ редактировать ]- Хэймон, РМ (2014). «Гидротермальные жерла на срединно-океанических хребтах». Справочный модуль по системам Земли и наукам об окружающей среде . дои : 10.1016/b978-0-12-409548-9.09050-3 . ISBN 978-0-12-409548-9 .
- Ван Довер, CL; Хамфрис, ЮВ; Форнари, Д; Кавано, CM; Кольер, Р; Гоффреди, СК; Хашимото, Дж; Лилли, доктор медицины; Рейзенбах, Алабама; Шанк, ТМ; Фон Дамм, КЛ; Банта, А; Галлант, РМ; Готц, Д; Грин, Д; Холл, Дж; Хармер, ТЛ; Уртадо, Луизиана; Джонсон, П; МакКинесс, З.П.; Мередит, К; Олсон, Э; Пан, Иллинойс; Репа, М; Выиграл, Ю; Молодой ЧР, 3-е место; Вриенгук, Р.К. (13 сентября 2001 г.). «Биогеография и экология гидротермальных источников Индийского океана» . Наука . 294 (5543): 818–823. Бибкод : 2001Sci...294..818V . дои : 10.1126/science.1064574 . ПМИД 11557843 . S2CID 543841 .
{{cite journal}}: CS1 maint: числовые имена: список авторов ( ссылка ) - Ван Довер; Синди Ли (2000). Экология глубоководных гидротермальных источников . Издательство Принстонского университета. ISBN 978-0-691-04929-8 .
- Битти, Джей Ти; Оверманн, Дж.; Линс, Монтана; Манске, АК; Ланг, А.С.; Бланкеншип, RE ; Ван Довер, CL; Мартинсон, штат Калифорния; Пламли, ФГ (20 июня 2005 г.). «Облигатно фотосинтезирующий бактериальный анаэроб из глубоководных гидротермальных источников» . Труды Национальной академии наук . 102 (26): 9306–9310. Бибкод : 2005PNAS..102.9306B . дои : 10.1073/pnas.0503674102 . ПМК 1166624 . ПМИД 15967984 .
- Глин Форд и Джонатан Симнетт, Серебро из моря , сентябрь/октябрь 1982 г., том 33, номер 5, мировой доступ Saudi Aramco, 17 октября 2005 г.
- Баллард, Роберт Д., 2000, Вечная тьма , Издательство Принстонского университета.
- Чотони, Дж. Т.; Стакебрандт, Э.; Юрков, В. (4 июля 2006 г.). «Анаэробное дыхание теллурата и других металлоидов у бактерий из гидротермальных жерловых полей в восточной части Тихого океана» . Прикладная и экологическая микробиология . 72 (7): 4950–4956. Бибкод : 2006ApEnM..72.4950C . дои : 10.1128/АЕМ.00223-06 . ПМЦ 1489322 . ПМИД 16820492 .
- Кощинский, Андреа; Гарбе-Шенберг, Дитер; Сандер, Сильвия; Шмидт, Катя; Геннерих, Ганс-Германн; Штраус, Харальд (2008). «Гидротермальная вентиляция в условиях давления и температуры выше критической точки морской воды, 5 ° ю.ш. на Срединно-Атлантическом хребте». Геология . 36 (8): 615. Бибкод : 2008Гео....36..615К . дои : 10.1130/G24726A.1 .
- Екатерина Браич (4 августа 2008 г.). «Найдено: Самая горячая вода на Земле» . Новый учёный . Проверено 18 июня 2010 г.
Внешние ссылки
[ редактировать ]- База данных InterRidge Vents - глобальная база данных о местоположении известных активных подводных гидротермальных полей, размещенная на InterRidge.
- Ocean Explorer - общественный информационный сайт об исследованиях, спонсируемый Управлением по исследованию океана США.
- Видео EV Nautilus
- Видео Оушена Шмидта