Транспортер ионов
В биологии переносчик ионов — это трансмембранный белок , который перемещает ионы (или другие небольшие молекулы) через биологическую мембрану для выполнения множества различных биологических функций, включая клеточную связь, поддержание гомеостаза, производство энергии и т. д. [1] Существуют различные типы транспортеров, включая насосы, унипортеры, антипортеры и симпортеры. Активные переносчики или ионные насосы — это переносчики, которые преобразуют энергию из различных источников, включая аденозинтрифосфат (АТФ), солнечный свет и другие окислительно-восстановительные реакции, в потенциальную энергию путем накачки иона вверх по градиенту концентрации. [2] Эта потенциальная энергия затем может быть использована вторичными переносчиками, включая переносчики ионов и ионные каналы, для управления жизненно важными клеточными процессами, такими как синтез АТФ . [3]
Эта страница посвящена в основном транспортерам ионов, действующим как насосы, но транспортеры также могут перемещать молекулы посредством облегченной диффузии . Облегченная диффузия не требует АТФ и позволяет молекулам, которые не могут быстро диффундировать через мембрану ( пассивная диффузия ), диффундировать вниз по градиенту концентрации через эти белковые переносчики. [4]
Транспортеры ионов необходимы для правильного функционирования клеток, поэтому они в высокой степени регулируются клеткой и изучаются исследователями с использованием различных методов. Будут приведены некоторые примеры клеточной регуляции и методов исследования.

Классификация и устранение неоднозначности
[ редактировать ]Транспортеры ионов классифицируются как суперсемейство транспортеров , которое включает 12 семейств транспортеров. [5] Эти семейства являются частью системы транспортной классификации (TC), которая используется Международным союзом биохимии и молекулярной биологии (IUBMB), и группируются по таким характеристикам, как транспортируемые субстраты, механизм транспорта, используемый источник энергии и также путем сравнения последовательностей ДНК, составляющих каждый белок. Наиболее важным объединяющим фактором является заряженная природа субстрата, которая указывает на транспорт иона, а не нейтрального вещества. [5] Транспортеры ионов существенно отличаются от ионных каналов . Каналы — это поры, проходящие через мембрану, тогда как транспортеры — это белки, которые должны менять форму, чтобы переключиться на ту сторону мембраны, с которой они открыты. Из-за этого транспортеры гораздо медленнее перемещают молекулы, чем каналы.
Электрохимический градиент или градиент концентрации — это разница в концентрации химической молекулы или иона в двух отдельных областях. [6] В состоянии равновесия концентрации ионов в обеих областях будут равны, поэтому, если есть разница в концентрации, ионы будут стремиться течь «вниз» по градиенту концентрации или от высокой концентрации к низкой концентрации. Ионные каналы позволяют определенным ионам, которые попадают в канал, течь по градиенту концентрации, выравнивая концентрации по обе стороны клеточной мембраны. Ионные каналы и переносчики ионов достигают этого посредством облегченной диффузии , которая является разновидностью пассивного транспорта . Однако только переносчики ионов также могут осуществлять активный транспорт, который предполагает перемещение ионов против градиента их концентрации. [7] Используя источники энергии, такие как АТФ, переносчики ионов способны перемещать ионы против градиента их концентрации, которые затем могут использоваться вторичными переносчиками или другими белками в качестве источника энергии. [6]
Источник энергии
[ редактировать ]Первичный транспортер
[ редактировать ]
Первичные переносчики используют энергию для транспортировки ионов, таких как Na. + , К + и Ка 2+ через клеточную мембрану и может создавать градиенты концентрации. [6] Этот транспорт может использовать АТФ в качестве источника энергии или его можно использовать для генерации АТФ с помощью таких методов, как цепь переноса электронов в растениях. [7] [6]
Активный транспортер
[ редактировать ]Активные переносчики используют АТФ для преобразования энергии АТФ в потенциальную энергию в форме градиента концентрации. Они используют АТФ для транспортировки ионов от низкой концентрации к более высокой концентрации. Примерами белков, использующих АТФ, являются АТФазы P-типа , которые переносят Na. + , К + и Ка 2+ ионы путем фосфорилирования, АТФазы А-типа, которые переносят анионы, и транспортеры ABC (транспортеры кассет, связывающих АТФ), которые транспортируют широкий набор молекул. [6] Примеры АТФазы P-типа включают Na + /К + -АТФаза [7] [8] [9] регулируется Янус Киназой-2 [10] а также Ка 2+ АТФаза , проявляющая чувствительность к концентрациям АДФ и АТФ. [3] P-гликопротеин является примером транспортно-связывающего белка ABC в организме человека.
Транспортер, производящий АТФ
[ редактировать ]Транспортеры, производящие АТФ, движутся в противоположном направлении от транспортеров, использующих АТФ. Эти белки переносят ионы от высокой концентрации к низкой с градиентом, но при этом образуется АТФ. Потенциальная энергия в виде градиента концентрации используется для генерации АТФ. [6] У животных синтез АТФ происходит в митохондриях с использованием АТФазы F-типа, иначе известной как АТФ-синтаза . Этот процесс использует цепь переноса электронов в процессе, называемом окислительным фосфорилированием . [11] [2] АТФаза V-типа выполняет функцию, противоположную АТФазе F-типа, и используется в растениях для гидролиза АТФ с целью создания протонного градиента. Примером этого являются лизосомы, которые используют АТФазу V-типа для подкисления пузырьков или вакуолей растений во время процесса фотосинтеза в хлоропластах. [7] Этот процесс можно регулировать с помощью различных методов, таких как pH. [12]
Вторичный транспортер
[ редактировать ]
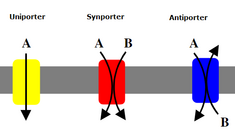
Вторичные переносчики также транспортируют ионы (или небольшие молекулы) против градиента концентрации – от низкой концентрации к высокой концентрации – но в отличие от первичных переносчиков, которые используют АТФ для создания градиента концентрации, вторичные переносчики используют потенциальную энергию градиента концентрации, создаваемого первичными переносчиками. для транспортировки ионов. [6] Например, натрий-зависимый переносчик глюкозы, обнаруженный в тонком кишечнике и почках, использует градиент натрия, создаваемый в клетке натриево-калиевым насосом (как упоминалось выше), для доставки глюкозы в клетку. [13] Это происходит, когда натрий стекает по градиенту концентрации, что обеспечивает достаточно энергии, чтобы вытолкнуть глюкозу вверх по градиенту концентрации обратно в клетку. Это важно для тонкого кишечника и почек, чтобы предотвратить потерю глюкозы. Симпортеры, такие как симпортер натрий-глюкозы, транспортируют ион с градиентом его концентрации и связывают транспорт второй молекулы в том же направлении. Антипортеры также используют градиент концентрации одной молекулы для перемещения другой вверх по градиенту концентрации, но связанная молекула транспортируется в противоположном направлении. [6]
Регулирование
[ редактировать ]Транспортеры ионов можно регулировать различными способами, такими как фосфорилирование, аллостерическое ингибирование или активация, а также чувствительность к концентрации ионов. Использование протеинкиназ для добавления фосфатной группы или фосфатаз для дефосфорилирования белка может изменить активность переносчика. [14] Активируется или ингибируется белок при добавлении фосфатной группы, зависит от конкретного белка. При аллостерическом ингибировании регуляторный лиганд может связываться с регуляторным сайтом и либо ингибировать, либо активировать транспортер. Транспортеры ионов также можно регулировать концентрацией иона (не обязательно иона, который он переносит) в растворе. Например, цепь переноса электронов регулируется наличием H + ионы (pH) в растворе. [6]
Методы исследования переносчиков ионов
[ редактировать ]Патч-зажим
[ редактировать ]Патч-зажим — это электрофизиологический метод, используемый для изучения каналов и транспортеров в клетках путем отслеживания тока, проходящего через них. Эта техника была усовершенствована Ходжкиным и Хаксли еще до того, как стало известно о существовании каналов и транспортеров. [11] [15] Помимо того, что его новаторская работа на ранних этапах разработки патч-зажима, наследие продолжается и широко используется исследователями до сих пор для изучения переносчиков ионов и того, как окружающая среда и лиганды влияют на функцию переносчика. [1] [16]
Рентгеновская кристаллография
[ редактировать ]Рентгеновская кристаллография — невероятный инструмент, позволяющий визуализировать структуру белков, однако это всего лишь снимок одной конформации белка. Структура транспортных белков позволяет исследователям лучше понять, как и что делает транспортер для перемещения молекул через мембрану. [17] [18]
Восстановление флуоресценции после фотообесцвечивания
[ редактировать ]Восстановление флуоресценции после фотообесцвечивания (FRAP) — это метод, используемый для отслеживания диффузии липидов или белков в мембране. Этот метод используется для лучшего понимания подвижности транспортеров в клетке и их взаимодействия с липидными доменами и липидными плотами в клеточной мембране.
Резонансная передача энергии Фёрстера
[ редактировать ]Резонансный перенос энергии Фёрстера (FRET) — это метод, который использует флуоресценцию для отслеживания того, насколько близки два белка друг к другу. Это использовалось при изучении транспортеров, чтобы увидеть, как они взаимодействуют с другими клеточными белками. [1]
Таблица переносчиков ионов
[ редактировать ]См. также
[ редактировать ]- Активный транспорт
- Ионно-транспортное число
- Суперсемейство ионных транспортеров
- Мембранный транспортный белок
- Транспортный белок
Ссылки
[ редактировать ]- ^ Jump up to: а б с Маффео С., Бхаттачарья С., Ю Дж., Уэллс Д., Аксиментьев А. (декабрь 2012 г.). «Моделирование и моделирование ионных каналов» . Химические обзоры . 112 (12): 6250–84. дои : 10.1021/cr3002609 . ПМЦ 3633640 . ПМИД 23035940 .
- ^ Jump up to: а б Первс Д., Августин Г.Дж., Фитцпатрик Д., Кац Л.К., ЛаМантия А.С., Макнамара Д.О., Уильямс С.М., ред. (2001). «Каналы и транспортеры» . Нейронаука (2-е изд.). Сандерленд, Массачусетс: Sinauer Associates. ISBN 0-87893-742-0 .
- ^ Jump up to: а б Хауманн Дж., Даш Р.К., Стоу Д.Ф., Боеленс А.Д., Бирд Д.А., Камара АК (август 2010 г.). «Свободный от митохондрий [Ca2+] увеличивается во время антипорта АТФ/АДФ и фосфорилирования АДФ: исследование механизмов» . Биофизический журнал . 99 (4): 997–1006. Бибкод : 2010BpJ....99..997H . дои : 10.1016/j.bpj.2010.04.069 . ПМЦ 2920628 . ПМИД 20712982 .
- ^ Гэдсби, округ Колумбия (май 2009 г.). «Ионные каналы и ионные насосы: принципиальная разница» . Обзоры природы. Молекулярно-клеточная биология . 10 (5): 344–52. дои : 10.1038/nrm2668 . ПМЦ 2742554 . ПМИД 19339978 .
- ^ Jump up to: а б Пракаш С., Купер Г., Сингхи С., Сайер М.Х. (декабрь 2003 г.). «Суперсемейство ионных транспортеров» . Biochimica et Biophysical Acta (BBA) – Биомембраны . 1618 (1): 79–92. дои : 10.1016/j.bbamem.2003.10.010 . ПМИД 14643936 .
- ^ Jump up to: а б с д и ж г час я Воет Д., Воет В.Г., Пратт CW (29 февраля 2016 г.). Основы биохимии: жизнь на молекулярном уровне . ISBN 9781118918401 . OCLC 910538334 .
- ^ Jump up to: а б с д Шеер БТ (01 января 2014 г.). «Ионный транспорт» . ДоступНаука . дои : 10.1036/1097-8542.352000 .
- ^ Морт Дж.П., Педерсен Б.П., Бух-Педерсен М.Дж., Андерсен Дж.П., Вильсен Б., Палмгрен М.Г., Ниссен П. (январь 2011 г.). «Структурный обзор ионных насосов плазматической мембраны Na +, K + -АТФаза и H + -АТФаза». Обзоры природы. Молекулярно-клеточная биология . 12 (1): 60–70. дои : 10.1038/nrm3031 . ПМИД 21179061 . S2CID 9734181 .
- ^ Такеучи А., Рейес Н., Артигас П., Гадсби, округ Колумбия (ноябрь 2009 г.). «Визуализация картированного пути ионов через насос Na,K-АТФазы» . Каналы . 3 (6): 383–6. дои : 10.4161/chan.3.6.9775 . ПМК 2889157 . ПМИД 19806033 .
- ^ Хоссейнзаде З., Луо Д., Сопджани М., Бхавсар С.К., Ланг Ф. (апрель 2014 г.). «Понижающая регуляция эпителиального Na⁺-канала ENaC с помощью Янус-киназы 2». Журнал мембранной биологии . 247 (4): 331–8. дои : 10.1007/s00232-014-9636-1 . ПМИД 24562791 . S2CID 16015149 .
- ^ Jump up to: а б Преббл Дж. Н. (сентябрь 2010 г.). «Открытие окислительного фосфорилирования: концептуальное ответвление изучения гликолиза». Исследования по истории и философии биологических и биомедицинских наук . 41 (3): 253–62. дои : 10.1016/j.shpsc.2010.07.014 . ПМИД 20934646 .
- ^ Тихонов А.Н. (октябрь 2013). «РН-зависимая регуляция транспорта электронов и синтеза АТФ в хлоропластах». Исследования фотосинтеза . 116 (2–3): 511–34. дои : 10.1007/s11120-013-9845-y . ПМИД 23695653 . S2CID 12903551 .
- ^ Крейн Р.К., Форстнер Г., Эйххольц А. (ноябрь 1965 г.). «Исследования механизма кишечной абсорбции сахаров. X. Влияние концентрации Na + на кажущиеся константы Михаэлиса для кишечного транспорта сахара in vitro». Биохимика и биофизика Acta . 109 (2): 467–77. дои : 10.1016/0926-6585(65)90172-х . ПМИД 5867548 .
- ^ Маршалл В.С., Уоттерс К.Д., Ховдестад Л.Р., Коззи Р.Р., Като Ф. (август 2009 г.). «Функциональная регуляция CFTR Cl-канала путем фосфорилирования киназы фокальной адгезии по тирозину 407 в осмочувствительных ион-транспортирующих богатых митохондриями клетках эвригалинной рыбы-киллифиши» . Журнал экспериментальной биологии . 212 (Часть 15): 2365–77. дои : 10.1242/jeb.030015 . ПМК 2712415 . ПМИД 19617429 .
- ^ Ванденберг Дж.И., Ваксман С.Г. (июнь 2012 г.). «Ходжкин и Хаксли и основы электрической сигнализации: замечательное наследие, которое все еще живо» . Журнал физиологии . 590 (11): 2569–70. дои : 10.1113/jphysicalol.2012.233411 . ПМЦ 3424715 . ПМИД 22787169 .
- ^ Свант Дж., Гудвин Дж.С., Норт А., Али А.А., Гэмбл-Джордж Дж., Чирва С., Хошбуэй Х. (декабрь 2011 г.). «α-Синуклеин стимулирует зависимый от переносчика дофамина хлоридный ток и модулирует активность переносчика» . Журнал биологической химии . 286 (51): 43933–43. дои : 10.1074/jbc.M111.241232 . ПМЦ 3243541 . ПМИД 21990355 .
- ^ Морт Дж.П., Педерсен Б.П., Тоуструп-Йенсен М.С., Соренсен Т.Л., Петерсен Дж., Андерсен Дж.П. и др. (декабрь 2007 г.). «Кристаллическая структура натриево-калиевого насоса». Природа . 450 (7172): 1043–9. Бибкод : 2007Nature.450.1043M . дои : 10.1038/nature06419 . ПМИД 18075585 . S2CID 4344526 .
- ^ Шинода Т., Огава Х., Корнелиус Ф., Тоёсима К. (май 2009 г.). «Кристаллическая структура натрий-калиевого насоса при разрешении 2,4 А». Природа . 459 (7245): 446–50. Бибкод : 2009Natur.459..446S . дои : 10.1038/nature07939 . ПМИД 19458722 . S2CID 205216514 .
Внешние ссылки
[ редактировать ]- Ионные + насосы в Национальной медицинской библиотеке США по медицинским предметным рубрикам (MeSH) D12.776.157.530.450; Д12.776.543.585.450
- База данных подложек Transporter (TSdb)