Бензойная кислота
| |||

| |||
| Имена | |||
|---|---|---|---|
| Предпочтительное название ИЮПАК
Бензойная кислота [ 1 ] | |||
| Систематическое название ИЮПАК
Бензолкарбоновая кислота | |||
Другие имена
| |||
| Идентификаторы | |||
3D model ( JSmol )
|
|||
| 3DMeet | |||
| 636131 | |||
| КЭБ | |||
| ХЭМБЛ | |||
| ХимическийПаук | |||
| Лекарственный Банк | |||
| Информационная карта ECHA | 100.000.562 | ||
| Номер ЕС |
| ||
| номер Е | Е210 (консерванты) | ||
| 2946 | |||
| КЕГГ | |||
| МеШ | бензойная+кислота | ||
ПабХим CID
|
|||
| номер РТЭКС |
| ||
| НЕКОТОРЫЙ | |||
Панель управления CompTox ( EPA )
|
|||
| Характеристики | |||
| C7H6OC7H6O2 | |||
| Молярная масса | 122.123 g/mol | ||
| Появление | Бесцветное кристаллическое вещество | ||
| Запах | Слабый, приятный запах | ||
| Плотность | 1,2659 г/см 3 (15 °С) 1,0749 г/см 3 (130 °С) [ 2 ] | ||
| Температура плавления | 122 ° С (252 ° F; 395 К) [ 7 ] | ||
| Точка кипения | 250 ° С (482 ° F; 523 К) [ 7 ] | ||
| 1,7 г/л (0 °С) 2,7 г/л (18 °С) 3,44 г/л (25 °С) 5,51 г/л (40 °С) 21,45 г/л (75 °С) 56,31 г/л (100 °С) [ 2 ] [ 3 ] | |||
| Растворимость | Растворим в ацетоне , бензоле , CCl 4 , CHCl 3 , спирте , этиловом эфире , гексане , фенилах , жидком аммиаке , ацетатах. | ||
| Растворимость в метаноле | 30 г/100 г (-18 °С) 32,1 г/100 г (-13 °С) 71,5 г/100 г (23 °С) [ 2 ] | ||
| Растворимость в этаноле | 25,4 г/100 г (-18 °С) 47,1 г/100 г (15 °С) 52,4 г/100 г (19,2 °С) 55,9 г/100 г (23 °С) [ 2 ] | ||
| Растворимость в ацетоне | 54,2 г/100 г (20 °С) [ 2 ] | ||
| Растворимость в оливковом масле | 4,22 г/100 г (25 °С) [ 2 ] | ||
| Растворимость в 1,4-диоксане | 55,3 г/100 г (25 °С) [ 2 ] | ||
| войти P | 1.87 | ||
| Давление пара | 0,16 Па (25°С) 0,19 кПа (100 °С) 22,6 кПа (200°С) [ 4 ] | ||
| Кислотность ( pKa ) | |||
| −70.28·10 −6 см 3 /моль | |||
Показатель преломления ( n D )
|
1,5397 (20 °С) 1,504 (132 °С) [ 2 ] | ||
| Вязкость | 1,26 МПа (130 °С) | ||
| Структура | |||
| Моноклиника | |||
| Планарный | |||
| 1,72 Д в диоксане | |||
| Термохимия | |||
Теплоемкость ( С )
|
146.7 J/mol·K [ 4 ] | ||
Стандартный моляр
энтропия ( S ⦵ 298 ) |
167,6 Дж/моль·К [ 2 ] | ||
Стандартная энтальпия
образование (Δ f H ⦵ 298 ) |
−385,2 кДж/моль [ 2 ] | ||
Стандартная энтальпия
горение (Δ c H ⦵ 298 ) |
−3228 кДж/моль [ 4 ] | ||
| Опасности | |||
| Безопасность и гигиена труда (OHS/OSH): | |||
Основные опасности
|
Раздражающий | ||
| СГС Маркировка : | |||
  [ 8 ] [ 8 ]
| |||
| Опасность | |||
| Х318 , Х335 [ 8 ] | |||
| П261 , П280 , П305+П351+П338 [ 8 ] | |||
| NFPA 704 (огненный алмаз) | |||
| точка возгорания | 121,5 ° С (250,7 ° F; 394,6 К) [ 7 ] | ||
| 571 ° C (1060 ° F; 844 К) [ 7 ] | |||
| Летальная доза или концентрация (LD, LC): | |||
ЛД 50 ( средняя доза )
|
1700 мг/кг (крыса, перорально) | ||
| Паспорт безопасности (SDS) | Джей Ти Бейкер | ||
| Родственные соединения | |||
Другие катионы
|
бензоат натрия , Бензоат калия | ||
Родственные карбоновые кислоты
|
Гидроксибензойные кислоты аминобензойные кислоты , нитробензойные кислоты , Фенилуксусная кислота | ||
Родственные соединения
|
Бензальдегид , Бензиловый спирт , Бензоилхлорид , бензиламин , Бензамид , Бензонитрил | ||
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа).
| |||
Бензойная кислота / b ɛ n ˈ z oʊ . ɪ k / — белое (или бесцветное) твердое органическое соединение формулы C 6 H 5 COOH , структура которого состоит из бензольного кольца ( C 6 H 6 ) с карбоксилом ( -C(=O)OH ) заместитель . Бензоильную бензила группу часто обозначают сокращенно «Bz» (не путать с «Bn», которое используется для обозначения ) , поэтому бензойную кислоту также обозначают как BzOH, поскольку бензоильная группа имеет формулу – С 6 Н 5 СО . Это простейшая ароматическая карбоновая кислота. Название происходит от бензоиновой камеди , которая долгое время была его единственным источником.
Бензойная кислота в природе встречается во многих растениях. [ 9 ] и служит промежуточным продуктом в биосинтезе многих вторичных метаболитов . Соли бензойной кислоты используются как консерванты пищевых продуктов . Бензойная кислота является важным предшественником для промышленного синтеза многих других органических веществ. Соли и эфиры бензойной кислоты известны как бензоаты / ˈ b ɛ n z oʊ . еɪ т / .
История
[ редактировать ]Бензойная кислота была открыта в шестнадцатом веке. Сухая перегонка бензойной смолы была впервые описана Нострадамусом (1556 г.), а затем Алексиусом Педемонтаном (1560 г.) и Блезом де Виженером (1596 г.). [ 10 ]
Юстус фон Либих и Фридрих Вёлер определили состав бензойной кислоты. [ 11 ] Последние также исследовали связь гиппуровой кислоты с бензойной кислотой.
В 1875 году Сальковский открыл противогрибковые свойства бензойной кислоты, которую долгое время использовали при консервировании бензоатсодержащих плодов морошки . [ 12 ] [ оспаривается – обсуждаем ]
Производство
[ редактировать ]Промышленные препараты
[ редактировать ]масштабах получают путем частичного окисления толуола промышленных кислородом Бензойную кислоту в . Процесс катализируется кобальта или марганца нафтенатами . В этом процессе используются обильные материалы, и он протекает с высоким выходом. [ 13 ]
Первый промышленный процесс включал реакцию бензотрихлорида (трихлорметилбензола) с гидроксидом кальция в воде с использованием железа или солей железа в качестве катализатора . Полученный бензоат кальция превращают в бензойную кислоту с помощью соляной кислоты . Продукт содержит значительные количества хлорированных производных бензойной кислоты. По этой причине бензойную кислоту для потребления человеком получали путем сухой перегонки бензойной камеди . Пищевая бензойная кислота в настоящее время производится синтетическим путем.
Лабораторный синтез
[ редактировать ]Бензойная кислота дешева и легкодоступна, поэтому лабораторный синтез бензойной кислоты практикуется в основном из-за ее педагогической ценности. Это обычная подготовка к бакалавриату.
Бензойную кислоту можно очистить перекристаллизацией из воды из-за ее высокой растворимости в горячей воде и плохой растворимости в холодной воде. Отсутствие органических растворителей при перекристаллизации делает этот эксперимент особенно безопасным. Этот процесс обычно дает выход около 65%. [ 14 ]
Путем гидролиза
[ редактировать ]Как и другие нитрилы и амиды , бензонитрил и бензамид могут гидролизоваться до бензойной кислоты или сопряженного с ней основания в кислых или основных условиях.
Из реактива Гриньяра
[ редактировать ]Бромбензол можно превратить в бензойную кислоту путем «карбоксилирования» промежуточного фенилмагнийбромида . [ 15 ] Этот синтез предлагает студентам удобное упражнение для проведения реакции Гриньяра , важного класса реакций образования углерод-углеродных связей в органической химии. [ 16 ] [ 17 ] [ 18 ] [ 19 ] [ 20 ]
Окисление бензильных соединений
[ редактировать ]Бензиловый спирт [ 21 ] а бензилхлорид и практически все бензилпроизводные легко окисляются до бензойной кислоты.
Использование
[ редактировать ]Бензойная кислота в основном расходуется на производство фенола путем окислительного декарбоксилирования при 300-400 °С: [ 22 ]
Требуемую температуру можно снизить до 200 °C путем добавления каталитических количеств солей меди (II). Фенол можно превратить в циклогексанол , который является исходным материалом для синтеза нейлона .
Прекурсор пластификаторов
[ редактировать ]Бензоатные пластификаторы и триэтиленгликоля, получают переэтерификацией метилбензоата , такие как эфиры гликоля, диэтиленгликоля соответствующим диолом . [ 22 ] Эти пластификаторы, которые используются аналогично пластификаторам, полученным из эфира терефталевой кислоты , представляют собой альтернативу фталатам . [ 22 ]
Прекурсор бензоата натрия и родственных консервантов.
[ редактировать ]Бензойная кислота и ее соли используются в качестве пищевых консервантов и имеют номера E210 , E211 , E212 и E213 . Бензойная кислота подавляет рост плесени , дрожжей. [ 23 ] и некоторые бактерии . Он либо добавляется напрямую, либо создается в результате реакций с его натриевой , калиевой или кальциевой солью. Механизм начинается с всасывания бензойной кислоты в клетку. Если внутриклеточный pH изменяется до 5 или ниже, анаэробная ферментация глюкозы фосфофруктокиназы посредством . снижается на 95% Таким образом, эффективность бензойной кислоты и бензоата зависит от pH пищи. [ 24 ] Бензойная кислота, бензоаты и их производные используются в качестве консервантов для кислых продуктов и напитков, таких как цитрусовых соки ( лимонная кислота ), газированные напитки ( диоксид углерода ), безалкогольные напитки ( фосфорная кислота ), соленья ( уксус ) и другие подкисленные продукты.
Типичные концентрации бензойной кислоты в качестве консерванта в пищевых продуктах составляют от 0,05 до 0,1%. Продукты питания, в которых может использоваться бензойная кислота, и максимальные уровни ее применения контролируются местными законами о пищевых продуктах. [ 25 ] [ 26 ]
Была выражена обеспокоенность тем, что бензойная кислота и ее соли могут вступать в реакцию с аскорбиновой кислотой (витамином С) в некоторых безалкогольных напитках, образуя небольшие количества канцерогенного бензола . [ 27 ]
Лекарственный
[ редактировать ]Бензойная кислота входит в состав мази Уитфилда , которая используется для лечения грибковых заболеваний кожи, таких как стригущий лишай и микоз . [ 28 ] [ 29 ] Бензойная кислота, являющаяся основным компонентом бензоиновой камеди , также является основным ингредиентом как настойки бензоина, так и бальзама Монаха. Такие продукты имеют долгую историю использования в качестве местных антисептиков и ингаляционных противозастойных средств .
Бензойная кислота использовалась как отхаркивающее , болеутоляющее и антисептическое средство в начале 20 века. [ 30 ]
Нишевое и лабораторное использование
[ редактировать ]В учебных лабораториях бензойная кислота является распространенным стандартом для калибровки бомбового калориметра . [ 31 ]
Биология и влияние на здоровье
[ редактировать ]Бензойная кислота, как и ее эфиры, встречается в природе во многих видах растений и животных. Заметные количества содержатся в большинстве ягод (около 0,05%). Спелые плоды некоторых Vaccinium видов (например, клюквы , V. vitis macrocarpon ; черники , V. myrtillus ) содержат до 0,03–0,13% свободной бензойной кислоты. Бензойная кислота образуется также в яблоках после заражения грибом Nectria Galligena . Среди животных бензойная кислота была идентифицирована преимущественно у всеядных или фитофагов, например, во внутренностях и мышцах каменной куропатки ( Lagopus muta ), а также в секретах желез самцов овцебыка ( Ovibos moschatus ) или азиатских слонов-быков ( Elephas maximus ). . [ 32 ] Камедь бензойная содержит до 20% бензойной кислоты и 40% эфиров бензойной кислоты. [ 33 ]
По биосинтезу бензоат образуется в растениях из коричной кислоты . [ 34 ] Путь был идентифицирован от фенола через 4-гидроксибензоат . [ 35 ]
Реакции
[ редактировать ]Реакции бензойной кислоты могут происходить как по ароматическому кольцу , так и по карбоксильной группе .
Ароматическое кольцо
[ редактировать ]Реакция электрофильного ароматического замещения будет происходить преимущественно в 3-положении из-за электроноакцепторной карбоксильной группы ; т.е. бензойная кислота метанаправляющей является . [ 36 ]
Карбоксильная группа
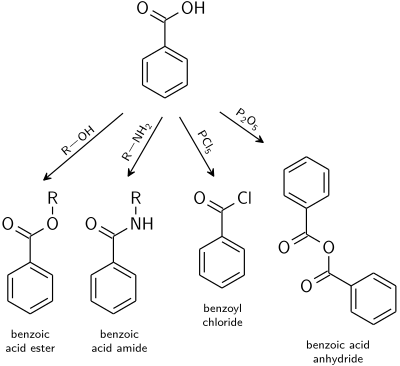
[ редактировать ]Реакции, типичные для карбоновых кислот, применимы и к бензойной кислоте. [ 22 ]
- бензойной кислоты Эфиры являются продуктом кислотно-катализируемой реакции со спиртами .
- бензойной кислоты Амиды обычно получают из бензоилхлорида .
- Дегидратацию до бензойного ангидрида вызывают уксусным ангидридом или пятиокисью фосфора .
- Высокореакционноспособные производные кислот, такие как галогенангидриды, легко получить путем смешивания с галогенирующими агентами, такими как хлориды фосфора или тионилхлорид .
- Ортоэфиры можно получить реакцией спиртов в кислых безводных условиях с бензонитрилом .
- Восстановление до бензальдегида и бензилового спирта возможно с использованием DIBAL-H , LiAlH 4 или боргидрида натрия .
- Декарбоксилирование до бензола можно осуществить нагреванием в хинолине в присутствии солей меди. Декарбоксилирование Хунсдикера можно осуществить путем нагревания соли серебра.
Безопасность и метаболизм млекопитающих
[ редактировать ]Выводится из организма в виде гиппуровой кислоты . [ 37 ] Бензойная кислота метаболизируется бутират-КоА-лигазой с образованием промежуточного продукта бензоил-КоА . [ 38 ] который затем метаболизируется глицин -N -ацилтрансферазой в гиппуровую кислоту. [ 39 ] Люди метаболизируют толуол , который также выводится из организма в виде гиппуровой кислоты. [ 40 ]
(IPCS) предполагает, что для людей здравоохранения Всемирной организации Международная программа по химической безопасности временная допустимая доза составляет 5 мг/кг массы тела в день. [ 32 ] Кошки имеют значительно более низкую толерантность к бензойной кислоте и ее солям , чем крысы и мыши . Смертельная доза для кошек может составлять всего 300 мг/кг массы тела. [ 41 ] Пероральная ЛД 50 для крыс составляет 3040 мг/кг, для мышей — 1940–2263 мг/кг. [ 32 ]
В Тайбэе , Тайвань, городское медицинское обследование, проведенное в 2010 году, показало, что 30% сушеных и маринованных продуктов питания содержат бензойную кислоту. [ 42 ]
См. также
[ редактировать ]- Ниацин – органическое соединение и форма витамина B3.
Ссылки
[ редактировать ]- ^ Номенклатура органической химии: Рекомендации ИЮПАК и предпочтительные названия 2013 (Синяя книга) . Кембридж: Королевское химическое общество . 2014. с. 745. дои : 10.1039/9781849733069-00648 . ISBN 978-0-85404-182-4 .
- ^ Jump up to: а б с д и ж г час я дж «бензойная кислота» . chemister.ru . Проверено 24 октября 2018 г.
- ^ Зейделл, Атертон; Линке, Уильям Ф. (1952). Растворимость неорганических и органических соединений . Ван Ностранд.
- ^ Jump up to: а б с Бензойная кислота — Линстрем, Питер Дж.; Маллард, Уильям Г. (ред.); Интернет-книга NIST по химии , Справочная база данных стандартов NIST № 69 , Национальный институт стандартов и технологий, Гейтерсбург (Мэриленд) (получено 23 мая 2014 г.)
- ^ Харрис, Дэниел (2010). Количественный химический анализ (8-е изд.). Нью-Йорк: WH Freeman and Company. стр. АП12. ISBN 9781429254366 .
- ^ Олмстед, Уильям Н.; Бордвелл, Фредерик Г. (1980). «Константы ассоциации ионных пар в диметилсульфоксиде». Журнал органической химии . 45 (16): 3299–3305. дои : 10.1021/jo01304a033 .
- ^ Jump up to: а б с д Запись в базе данных веществ ГЕСТИС Института охраны труда.
- ^ Jump up to: а б с Sigma-Aldrich Co. , Бензойная кислота . Проверено 23 мая 2014 г.
- ^ «Ученые раскрывают последние шаги по созданию бензойной кислоты в растениях» . Новости сельского хозяйства Purdue.
- ^ Ноймюллер О.А. (1988). Химический словарь Рёмппа (6-е изд.). Штутгарт: Frankh'sche Verlagshandlung. ISBN 978-3-440-04516-9 . OCLC 50969944 .
- ^ Либих Дж .; Вёлер Ф (1832). «Исследования радикала бензойной кислоты». Анналы химии . 3 (3): 249–282. дои : 10.1002/jlac.18320030302 . hdl : 2027/hvd.hxdg3f .
- ^ Салковский Э (1875). Берл Клин Еженедельник . 12 :297-298.
{{cite journal}}: Отсутствует или пусто|title=( помощь ) - ^ Уэйд, Лерой Г. (2014). Органическая химия (новое международное издание Пирсона). Харлоу: Pearson Education Limited. п. 985. ИСБН 978-1-292-02165-2 .
- ^ Д.Д. Перрен; WLF Армарего (1988). Очистка лабораторных химикатов (3-е изд.). Пергамон Пресс. стр. 94 . ISBN 978-0-08-034715-8 .
- ^ Дональд Л. Павиа (2004). Введение в органические лабораторные методы: маломасштабный подход . Томсон Брукс/Коул. стр. 312–314. ISBN 978-0-534-40833-6 .
- ^ Ширли, Д.А. (1954). «Синтез кетонов из галогенангидридов и металлоорганических соединений магния, цинка и кадмия». Орг. Реагировать. 8 : 28–58.
- ^ Гурин, Д.М. (1991). «Карбанионы щелочных и щелочноземельных катионов: (ii) Селективность реакций присоединения карбонила». Трост , BM ; Флеминг, И. (ред.). Комплексный органический синтез, Том 1: Дополнения к π-связям C—X, Часть 1 . Эльзевир Наука . стр. 49–75. дои : 10.1016/B978-0-08-052349-1.00002-0 . ISBN 978-0-08-052349-1 .
- ^ «Реакция Гриньяра. Получение бензойной кислоты» (PDF) . Портлендский общественный колледж. Архивировано из оригинала (PDF) 26 февраля 2015 года . Проверено 12 марта 2015 г. >
- ^ «Эксперимент 9: Синтез бензойной кислоты путем карбонилирования реактива Гриньяра» (PDF) . Университет Висконсин-Мэдисон. Архивировано из оригинала (PDF) 23 сентября 2015 года . Проверено 12 марта 2015 г.
- ^ «Эксперимент 3: Получение бензойной кислоты» (PDF) . Таусонский университет. Архивировано из оригинала (PDF) 13 апреля 2015 года . Проверено 12 марта 2015 г. >
- ^ Сантонастасо, Марко; Фрикли, Саймон Дж.; Медзяк, Питер Дж.; Бретт, Джемма Л.; Эдвардс, Дженнифер К.; Хатчингс, Грэм Дж. (21 ноября 2014 г.). «Окисление бензилового спирта с использованием перекиси водорода, полученной на месте». Исследования и разработки органических процессов . 18 (11): 1455–1460. дои : 10.1021/op500195e . ISSN 1083-6160 .
- ^ Jump up to: а б с д Маки, Такао; Такеда, Кадзуо (2000). «Бензойная кислота и производные». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. дои : 10.1002/14356007.a03_555 . ISBN 978-3527306732 . .
- ^ А.Д. Варт (1 декабря 1991 г.). «Механизм действия бензойной кислоты на Zygosaccharomyces bailii: влияние на уровни гликолитических метаболитов, выработку энергии и внутриклеточный pH» . Appl Environ Microbiol . 57 (12): 3410–4. Бибкод : 1991ApEnM..57.3410W . дои : 10.1128/АЕМ.57.12.3410-3414.1991 . ЧВК 183988 . ПМИД 1785916 .
- ^ Пастророва И., де Костер К.Г., Бум Дж.Дж. (1997). «Аналитическое исследование свободных и сложноэфирных бензойных и коричных кислот камедь-бензоиновых смол с помощью ГХ-МС ВЭЖХ-фритты FAB-MS». Фитохимический анал . 8 (2): 63–73. doi : 10.1002/(SICI)1099-1565(199703)8:2<63::AID-PCA337>3.0.CO;2-Y .
- ^ Подробности онлайн-группы пищевых добавок GSFA: Бензоаты (2006). Архивировано 26 сентября 2007 года в Wayback Machine.
- ^ ДИРЕКТИВА ЕВРОПЕЙСКОГО ПАРЛАМЕНТА И СОВЕТА № 95/2/EC от 20 февраля 1995 г. о пищевых добавках, кроме красителей и подсластителей (версии Consleg не содержат последних изменений в законе). Архивировано 19 апреля 2003 г. на Wayback Machine.
- ^ «Признаки возможного образования бензола из бензойной кислоты в пищевых продуктах, Экспертное заключение BfR № 013/2006» (PDF) . Немецкий федеральный институт оценки рисков. 1 декабря 2005 г. Архивировано (PDF) из оригинала 26 апреля 2006 г. . Проверено 30 марта 2022 г.
- ^ «Мазь Уитфилда» . Архивировано из оригинала 9 октября 2007 года . Проверено 15 октября 2007 г.
- ^ Чарльз Оуэнс Уилсон; Оле Гисволд; Джон Х. Блок (2004). Учебник Уилсона и Гисвольда по органической медицине и фармацевтике . Липпинкотт Уильямс и Уилкинс. стр. 234 . ISBN 978-0-7817-3481-3 .
- ^ Лиллард, Бенджамин (1919). «Пастилки бензойной кислоты» . Практический аптекарь и фармацевтический обзор отзывов .
- ^ Эксперимент 2: Использование бомбовой калориметрии для определения резонансной энергии бензола. Архивировано 9 марта 2012 г. в Wayback Machine.
- ^ Jump up to: а б с «Краткий международный документ химической оценки 26: БЕНЗОЙНАЯ КИСЛОТА И БЕНЗОАТ НАТРИЯ» .
- ^ Томокуни К., Огата М. (1972). «Прямое колориметрическое определение гиппуровой кислоты в моче» . Клин Чем . 18 (4): 349–351. дои : 10.1093/клинчем/18.4.349 . ПМИД 5012256 .
- ^ Фогт, Т. (2010). «Биосинтез фенилпропаноидов» . Молекулярный завод . 3 :2–20. дои : 10.1093/mp/ssp106 . ПМИД 20035037 .
- ^ Жуто, Пьер; Валери Коте; Мари-Франс Дакетт; Режан Боде; Франсуа Лепин; Ричард Виллемур; Жан-Ги Бисайон (январь 2005 г.). «Cryptanaerobacterphenolicus gen. nov., sp. nov., анаэроб, который превращает фенол в бензоат через 4-гидроксибензоат» . Международный журнал систематической и эволюционной микробиологии . 55 (1): 245–250. дои : 10.1099/ijs.0.02914-0 . ПМИД 15653882 .
- ^ Брюстер, RQ; Уильямс, Б.; Филлипс, Р. (1955). «3,5-динитробензойная кислота» . Органические синтезы ; Сборник томов , т. 3, с. 337 .
- ^ Экспертная группа по обзору косметических ингредиентов Бинду Наир (2001). «Заключительный отчет об оценке безопасности бензилового спирта, бензойной кислоты и бензоата натрия». Инт Джей Токс . 20 (Приложение 3): 23–50. дои : 10.1080/10915810152630729 . ПМИД 11766131 . S2CID 13639993 .
- ^ «бутират-КоА-лигаза» . БРЕНДА . Технический университет Брауншвейга . Проверено 7 мая 2014 г. Субстраты/Продукт
- ^ «глицин-N-ацилтрансфераза» . БРЕНДА . Технический университет Брауншвейга . Проверено 7 мая 2014 г. Субстраты/Продукт
- ^ Кребс Х.А., Виггинс Д., Стаббс М. (1983). «Исследование механизма противогрибкового действия бензоата» . Биохим Дж . 214 (3): 657–663. дои : 10.1042/bj2140657 . ПМЦ 1152300 . ПМИД 6226283 .
- ^ Бедфорд П.Г., Кларк Э.Г. (1972). «Экспериментальное отравление бензойной кислотой у кошки». Ветеринарная запись . 90 (3): 53–58. doi : 10.1136/vr.90.3.53 (неактивен 11 сентября 2024 г.). ПМИД 4672555 . S2CID 2553612 .
{{cite journal}}: CS1 maint: DOI неактивен по состоянию на сентябрь 2024 г. ( ссылка ) - ^ Чен, Цзянь; Ю.Л. Као (18 января 2010 г.). «Почти 30% сушеных и маринованных продуктов не проходят проверку безопасности» . Почта Китая .