Фосфатидилэтаноламин
Фосфатидилэтаноламин ( ФЭ ) представляет собой класс фосфолипидов , обнаруженных в биологических мембранах . [ 1 ] Они синтезируются путем присоединения цитидиндифосфата - этаноламина к диглицеридам , высвобождая цитидинмонофосфат . S -Аденозилметионин может впоследствии метилировать амин фосфатидилэтаноламинов с образованием фосфатидилхолинов .
Функция
[ редактировать ]
В клетках
[ редактировать ]Фосфатидилэтаноламины обнаружены во всех живых клетках, составляя 25% всех фосфолипидов. В физиологии человека они обнаруживаются, в частности, в нервной ткани, такой как белое вещество головного мозга , нервы, нервная ткань и спинной мозг , где они составляют 45% всех фосфолипидов. [ 2 ]
Фосфатидилэтаноламины играют роль в слиянии мембран и разборке сократительного кольца во время цитокинеза при делении клеток . [ 3 ] Кроме того, считается, что фосфатидилэтаноламин регулирует кривизну мембраны . Фосфатидилэтаноламин является важным предшественником, субстратом или донором в нескольких биологических путях. [ 2 ]
Как полярная головная группа, фосфатидилэтаноламин создает более вязкую липидную мембрану по сравнению с фосфатидилхолином . Например, температура плавления диолеоилфосфатидилэтаноламина составляет -16 °C, а температура плавления диолеоилфосфатидилхолина составляет -20 °C. Если бы липиды имели две пальмитоильные цепи, фосфатидилэтаноламин плавился бы при 63 °C, а фосфатидилхолин плавился бы уже при 41 °C. [ 4 ] Более низкие температуры плавления, проще говоря, соответствуют более текучим мембранам.
У людей
[ редактировать ]Считается, что у людей метаболизм фосфатидилэтаноламина важен в сердце. Когда приток крови к сердцу ограничен, асимметричное распределение фосфатидилэтаноламина между листками мембраны нарушается, и в результате мембрана разрушается. Кроме того, фосфатидилэтаноламин играет роль в секреции липопротеинов в печени. Это связано с тем, что везикулы, секретирующие липопротеины очень низкой плотности , выходящие из аппарата Гольджи, имеют значительно более высокую концентрацию фосфатидилэтаноламина по сравнению с другими везикулами, содержащими липопротеины очень низкой плотности. [ 5 ] Также было показано, что фосфатидилэтаноламин способен размножать инфекционные прионы без помощи каких-либо белков или нуклеиновых кислот , что является его уникальной характеристикой. [ 6 ] Считается также, что фосфатидилэтаноламин играет роль в свертывании крови, поскольку вместе с фосфатидилсерином он увеличивает скорость образования тромбина , способствуя связыванию с фактором V и фактором X , двумя белками, которые катализируют образование тромбина из протромбина . [ 7 ] Синтез эндоканнабиноида анандамида осуществляется из фосфатидилэтаноламина путем последовательного действия двух ферментов: N - ацетилтрансферазы и фосфолипазы -D. [ 8 ]
У бактерий
[ редактировать ]Если фосфатидилхолин является основным фосфолипидом у животных, то фосфатидилэтаноламин является основным у бактерий . Одной из основных ролей фосфатидилэтаноламина в бактериальных мембранах является распространение отрицательного заряда, вызванного анионными мембранными фосфолипидами . В бактериях E. coli фосфатидилэтаноламин играет роль в поддержке через пермеазы активного транспорта лактозы в клетку лактозы, а также может играть роль в других транспортных системах. Фосфатидилэтаноламин играет роль в сборке пермеазы лактозы и других мембранных белков. Он действует как «сопровождающий», помогая мембранным белкам правильно складывать свои третичные структуры , чтобы они могли правильно функционировать. В отсутствие фосфатидилэтаноламина транспортные белки имеют неправильную третичную структуру и не функционируют правильно. [ 9 ]
Фосфатидилэтаноламин также обеспечивает правильное функционирование бактериальных мультилекарственных переносчиков и образование промежуточных продуктов, необходимых для правильного открытия и закрытия транспортеров. [ 10 ]
Структура
[ редактировать ]
Как лецитин , фосфатидилэтаноламин состоит из комбинации глицерина, этерифицированного двумя жирными кислотами и фосфорной кислотой . В то время как фосфатная группа соединяется с холином в фосфатидилхолине, она соединяется с этаноламином в фосфатидилэтаноламине. Две жирные кислоты могут быть одинаковыми или разными и обычно находятся в положениях 1,2 (реже в положениях 1,3).
Синтез
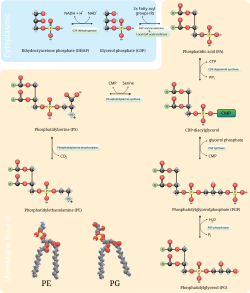
[ редактировать ]фосфатидилсерина . Путь декарбоксилирования и путь цитидиндифосфат-этаноламин используются для синтеза фосфатидилэтаноламина Фосфатидилсериндекарбоксилаза — это фермент, который используется для декарбоксилирования фосфатидилсерина по первому пути. Путь декарбоксилирования фосфатидилсерина является основным источником синтеза фосфатидилэтаноламина в мембранах митохондрий . Фосфатидилэтаноламин, вырабатываемый в митохондриальной мембране, также транспортируется по клетке к другим мембранам для использования. В процессе, который отражает синтез фосфатидилхолина , фосфатидилэтаноламин также образуется по пути цитидиндифосфат-этаноламин с использованием этаноламина в качестве субстрата. Через несколько этапов, происходящих как в цитозоле , так и в эндоплазматическом ретикулуме , путь синтеза дает конечный продукт фосфатидилэтаноламин. [ 11 ] Фосфатидилэтаноламин также в изобилии содержится в соевом или яичном лецитине и производится в промышленных масштабах с использованием хроматографического разделения.
Регулирование
[ редактировать ]Синтез фосфатидилэтаноламина посредством фосфатидилсерина пути декарбоксилирования происходит быстро во внутренней митохондриальной мембране . Однако фосфатидилсерин вырабатывается в эндоплазматическом ретикулуме . Из-за этого транспорт фосфатидилсерина из эндоплазматического ретикулума к мембране митохондрий, а затем к внутренней мембране митохондрий ограничивает скорость синтеза по этому пути. Механизм этого транспорта в настоящее время неизвестен, но может играть роль в регуляции скорости синтеза на этом пути. [ 12 ]
Присутствие в продуктах питания, проблемы со здоровьем
[ редактировать ]Фосфатидилэтаноламины в пищевых продуктах распадаются с образованием связанных с фосфатидилэтаноламином продуктов Амадори в рамках реакции Майяра . [ 13 ] Эти продукты ускоряют мембран липидов перекисное окисление , вызывая окислительный стресс клеток, которые с ними контактируют. [ 14 ] Известно, что окислительный стресс вызывает порчу продуктов питания и ряд заболеваний. Значительные уровни продуктов Амадори-фосфатидилэтаноламина были обнаружены в самых разных пищевых продуктах, таких как шоколад , соевое молоко , детские смеси и другие обработанные пищевые продукты . Уровни продуктов Амадори-фосфатидилэтаноламина выше в продуктах с высоким содержанием липидов и сахара, которые обрабатываются при высоких температурах. [ 13 ] Дополнительные исследования показали, что амадори-фосфатидилэтаноламин может играть роль в сердечно-сосудистых заболеваниях . [ 15 ] действовать как механизм, с помощью которого диабет может увеличить заболеваемость раком , [ 16 ] и потенциально играют роль и в других заболеваниях. Амадори-фосфатидилэтаноламин имеет более высокую в плазме концентрацию у пациентов с диабетом, чем у здоровых людей, что указывает на то, что он может играть роль в развитии заболевания или быть его продуктом. [ 17 ]
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Веллнер, Нильс; Дип, Тхи Ай; Янфельт, Кристиан; Хансен, Харальд Северин (2012). «N-ацилирование фосфатидилэтаноламина и его биологические функции у млекопитающих». Biochimica et Biophysical Acta (BBA) - Молекулярная и клеточная биология липидов . 1831 (3): 652–62. дои : 10.1016/j.bbalip.2012.08.019 . ПМИД 23000428 .
- ^ Перейти обратно: а б Вэнс, Джин Э.; Тассева, Гергана (2012). «Образование и функция фосфатидилсерина и фосфатидилэтаноламина в клетках млекопитающих». Biochimica et Biophysical Acta (BBA) - Молекулярная и клеточная биология липидов . 1831 (3): 543–54. дои : 10.1016/j.bbalip.2012.08.016 . ПМИД 22960354 .
- ^ Эмото, К.; Кобаяши, Т; Ямаджи, А; Айзава, Х; Яхара, я; Иноуэ, К; Умеда, М. (1996). «Перераспределение фосфатидилэтаноламина в борозде расщепления делящихся клеток во время цитокинеза» . Труды Национальной академии наук . 93 (23): 12867–72. Бибкод : 1996PNAS...9312867E . дои : 10.1073/pnas.93.23.12867 . JSTOR 40713 . ПМК 24012 . ПМИД 8917511 .
- ^ См. ссылки в Wan et al. Биохимия 47 2008 г. [ нужна проверка ]
- ^ Вэнс, Дж. Э. (2008). «Серия тематических обзоров: Глицеролипиды. Фосфатидилсерин и фосфатидилэтаноламин в клетках млекопитающих: два метаболически связанных аминофосфолипида» . Журнал исследований липидов . 49 (7): 1377–87. doi : 10.1194/jlr.R700020-JLR200 . ПМИД 18204094 .
- ^ Делео, Северная Каролина; Пиро-младший; Уолш, диджей; Ван, Ф.; Ма, Дж.; Геогеган, Дж. К.; Супаттапоне, С. (2012). «Выделение фосфатидилэтаноламина как единственного кофактора образования прионов в отсутствие нуклеиновых кислот» . Труды Национальной академии наук . 109 (22): 8546–51. Бибкод : 2012PNAS..109.8546D . дои : 10.1073/pnas.1204498109 . ПМЦ 3365173 . ПМИД 22586108 .
- ^ Маджамдер, Р.; Лян, X.; Куинн-Аллен, Массачусетс; Кейн, Вашингтон; Ленц, БР (2011). «Модуляция сборки и активности протромбиназы фосфатидилэтаноламином» . Журнал биологической химии . 286 (41): 35535–42. дои : 10.1074/jbc.M111.260141 . ПМК 3195639 . ПМИД 21859710 .
- ^ Исидро, Ф. (2014). «Каннабиноиды для лечения болезни Альцгеймера: движение к клинике» . Границы в фармакологии . 5 : 37. дои : 10.3389/fphar.2014.00037 . ПМЦ 3942876 . ПМИД 24634659 .
- ^ Кристи, WW (16 апреля 2012 г.). «Фосфатидилэтаноламин и родственные липиды» . Липидная библиотека AOCS. Архивировано из оригинала 21 августа 2012 года . Проверено 3 сентября 2012 г.
- ^ Гбагиди, Б.; Хакизимана, П.; Ванденбуше, Г.; Рюйшерт, Ж.-М. (2007). «Конформационные изменения в бактериальном переносчике нескольких лекарств зависят от фосфатидилэтаноламина» (PDF) . Клеточные и молекулярные науки о жизни . 64 (12): 1571–82. дои : 10.1007/s00018-007-7031-0 . ПМИД 17530171 . S2CID 2078590 .
- ^ Келли, Карен (28 июля 2011 г.). «Биосинтез фосфолипидов» . Липидная библиотека AOCS . Проверено 3 сентября 2012 г.
- ^ Куге, Осаму; Нисидзима, Масахиро (1 апреля 2003 г.). «Биосинтетическая регуляция и внутриклеточный транспорт фосфатидилсерина в клетках млекопитающих» . Журнал биохимии . 133 (4): 397–403. дои : 10.1093/jb/mvg052 . ПМИД 12761285 . Архивировано из оригинала 30 января 2021 года . Проверено 30 января 2021 г.
- ^ Перейти обратно: а б Дуб, Чон-Хо; Накагава, Киётака; Миядзава, Теруо (2002). «УФ-анализ Амадори-гликированного фосфатидилэтаноламина в пищевых продуктах и биологических образцах» . Журнал исследований липидов . 43 (3): 523–9. дои : 10.1016/S0022-2275(20)30158-9 . ПМИД 11893788 .
- ^ Дуб, Чон-Хо; Накагава, Киётака; Миядзава, Теруо (2000). «Синтетически полученный Амадори-гликированный фосфатидилэтаноламин может вызвать перекисное окисление липидов посредством свободнорадикальных реакций» . Письма ФЭБС . 481 (1): 26–30. Бибкод : 2000FEBSL.481...26O . дои : 10.1016/S0014-5793(00)01966-9 . ПМИД 10984609 . S2CID 23265125 .
- ^ Дуб, Чон-Хо; Накагава, Киётака; Оикава, Синъити; Миядзава, Теруо (2003). «Амадори-гликированный фосфатидилэтаноламин индуцирует ангиогенную дифференцировку в культивируемых эндотелиальных клетках пупочной вены человека». Письма ФЭБС . 555 (2): 419–23. Бибкод : 2003FEBSL.555..419O . дои : 10.1016/S0014-5793(03)01237-7 . ПМИД 14644453 . S2CID 33974755 .
- ^ Эйцука, Такахиро; Оно, Юичи, Наото; Курата, Тадао, Наоки; Миядзава, Теруо (2012). «Амадори-гликированный фосфатидилэтаноламин повышает активность теломеразы у человека». PMID . Письма FEBS / 586 : 2542–7 : 2012FEBSL.586.2542E . doi : 10.1016 j.febslet.2012.06.027 . Бибкод 22750441 . . ( 16 )
- ^ Ариизуми, Кен; Койке, Т; Охара, С; Иномата, Ю; Абэ, Ю; Иидзима, К; Иматани, А; Ока, Т; Симосегава, Т. (2008). «Заболеваемость рефлюкс-эзофагитом и инфекцией H. pylori у пациентов с диабетом» . Всемирный журнал гастроэнтерологии . 14 (20): 3212–7. дои : 10.3748/wjg.14.3212 . ПМК 2712855 . ПМИД 18506928 .
Внешние ссылки
[ редактировать ]- Фосфатидилэтаноламины Национальной медицинской библиотеки США в медицинских предметных рубриках (MeSH)
- Фосфатидилэтаноламин в Липидной библиотеке AOCS.