Диффузная крупноклеточная В-клеточная лимфома
| Диффузная крупноклеточная В-клеточная лимфома | |
|---|---|
| Другие имена | ДЛБКЛ или ДЛБЛ |
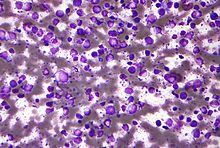 | |
| Микрофотография ( полевая окраска ) диффузной крупноклеточной В-клеточной лимфомы. | |
| Специальность | Гематология , онкология , дерматология |
Диффузная B-крупноклеточная лимфома ( DLBCL ) — это рак B -клеток , типа лимфоцитов , ответственных за выработку антител . Это наиболее распространенная форма неходжкинской лимфомы среди взрослых. [ 1 ] с ежегодной заболеваемостью 7–8 случаев на 100 000 человек в год в США и Великобритании. [ 2 ] [ 3 ] Этот рак встречается преимущественно у пожилых людей, средний возраст диагностики составляет около 70 лет. [ 3 ] хотя это может произойти у молодых людей и, в редких случаях, у детей. [ 4 ] DLBCL может возникнуть практически в любой части тела и, в зависимости от различных факторов, часто является очень агрессивным злокачественным новообразованием. [ 5 ] Первым признаком этого заболевания обычно является наблюдение быстро растущей массы или инфильтрации тканей, что иногда связано с системными симптомами группы В , например лихорадкой , потерей веса и ночной потливостью . [ 6 ]
Причины диффузной крупноклеточной В-клеточной лимфомы недостаточно изучены. Обычно DLBCL возникает из нормальных В-клеток, но может также представлять собой злокачественную трансформацию других типов лимфом (особенно лимфом маргинальной зоны). [ 7 ] ) или, в редких случаях, называемых трансформацией Рихтера , хроническим лимфоцитарным лейкозом . [ 8 ] Основной иммунодефицит является значимым фактором риска развития заболевания. [ 9 ] Инфекции вирусом Эпштейна-Барра (ВЭБ), [ 10 ] [ 11 ] Герпесвирус, ассоциированный с саркомой Капоши , [ 12 ] [ 13 ] вирус иммунодефицита человека (т.е. ВИЧ), [ 12 ] и Helicobacter pylori бактерия [ 7 ] также связаны с развитием некоторых подтипов диффузной крупноклеточной В-клеточной лимфомы. Однако большинство случаев этого заболевания связано с необъяснимым поэтапным приобретением возрастающего количества генных мутаций и изменений в экспрессии генов, которые происходят в определенных типах В-клеток и постепенно способствуют злокачественному поведению. [ 14 ]
Диагноз DLBCL ставится путем удаления части опухоли посредством биопсии и последующего исследования этой ткани с помощью микроскопа. Обычно этот диагноз ставит гематопатолог . [ 15 ] Были идентифицированы многочисленные подтипы DLBCL, которые различаются по своим клиническим проявлениям, результатам биопсии, агрессивным характеристикам, прогнозам и рекомендуемым методам лечения. [ 16 ] Однако обычное лечение большинства подтипов DLBCL представляет собой химиотерапию в сочетании с препаратом моноклональных антител, нацеленным на раковые B-клетки заболевания , обычно ритуксимабом . [ 17 ] Благодаря этому лечению можно вылечить более половины всех пациентов с DLBCL; [ 18 ] общий уровень излечения пожилых людей ниже этого показателя, но их пятилетняя выживаемость составляет около 58%. [ 19 ]
Подтипы диффузной крупноклеточной В-клеточной лимфомы
[ редактировать ]Диффузная крупноклеточная В-клеточная лимфома включает в себя биологически и клинически разнообразный набор подтипов заболевания. [ 20 ] многие из которых трудно отделить друг от друга на основе четко определенных и широко принятых критериев. Система классификации Всемирной организации здравоохранения в 2008 году определила более десятка подтипов. [ 21 ] каждый из которых был идентифицирован на основе местоположения опухоли, присутствия в опухоли других типов клеток, таких как Т-клетки , а также наличия у пациента некоторых других заболеваний, связанных с DLBCL. На основании дальнейших исследований Всемирная организация здравоохранения в 2016 году реклассифицировала DLBCL в наиболее распространенный подтип - диффузную крупноклеточную B-клеточную лимфому, не уточненную иначе (DLBCL, NOS). DLBCL, NOS составляют 80–85% всех DLBCL. [ 22 ] Остальные случаи DLBCL состоят из относительно редких подтипов, которые отличаются морфологией ( т. е. микроскопическим видом), иммунофенотипом (т. е. экспрессией определенных маркерных белков), клиническими проявлениями и/или ассоциацией с определенными патогенными вирусами . [ 12 ] Некоторые случаи DLBCL, БДУ, хотя и не включены в классификацию Всемирной организации здравоохранения 2016 года, явно связаны и вызваны хронической инфекцией бактерией Helicobacter pylori . [ 23 ]
Диффузная крупноклеточная В-клеточная лимфома, не уточненная иначе
[ редактировать ]Случаи DLBCL, которые не соответствуют отличительным клиническим проявлениям, морфологии тканей, фенотипу неопластических клеток и/или патоген-ассоциированным критериям других подтипов DLBCL, называются диффузной крупноклеточной B-клеточной лимфомой, не указанной иначе: DLBCL, NOS, хотя они представляют собой 80–80– 85% всех случаев DLBCL является диагнозом исключения . В целом, DLBCL, NOS представляет собой агрессивное заболевание с общей долгосрочной выживаемостью у пациентов, получавших стандартные схемы химиотерапии, около 65%. Однако это заболевание имеет множество вариантов, различающихся не только только что указанными параметрами, но и агрессивностью и чувствительностью к лечению. [ 24 ]
Представление признаков и симптомов
[ редактировать ]Около 70% случаев DLBCL, NOS проявляются преимущественно поражением лимфатических узлов. В этих случаях наиболее типичным симптомом на момент постановки диагноза является образование, которое быстро увеличивается и располагается в части тела с множественными лимфатическими узлами, например в паху, подмышках или шее. В оставшихся примерно 30% остальных случаев заболевание начинается с экстранодальной лимфомы, чаще всего в желудке. [ 12 ] или, реже, в других местах, таких как яички, молочные железы, матка, яичники, почки, надпочечники , щитовидная железа или кости. [ 25 ] Признаки и симптомы в этих случаях отражают наличие быстро расширяющейся опухоли или инфильтрата, вызывающего симптомы, специфичные для пораженного органа, такие как увеличение размера, боль и/или дисфункция. [ 25 ] У лиц с узловым или экстранодальным заболеванием также наблюдаются: системные симптомы группы В, такие как потеря веса, ночная потливость, лихорадка и/или утомляемость примерно в 33% случаев; в крови необъяснимое повышение уровня дегидрогеназы молочной кислоты и бета-2-микроглобулина во многих случаях ; злокачественные клетки, инфильтрирующие костный мозг , в 10–20% случаев; и/или локализованное заболевание I или II стадии в 50% случаев и диссеминированное заболевание III или IV стадии в остальных случаях. [ 12 ] Вовлечение костного мозга может быть связано с DLBCL, клетками NOS или клетками лимфомы низкой степени злокачественности; только DLBCL, инфильтраты клеток NOS указывают на худший прогноз. [ 22 ] В редких случаях DLBCL может возникнуть как трансформация лимфомы маргинальной зоны (MZL) у лиц, у которых этот вялотекущий рак был диагностирован 4–5 лет (среднее время) назад. [ 26 ]
Прогностические показатели, основанные на клинической картине
[ редактировать ]В Международном прогностическом индексе , а в последнее время и в его скорректированном по возрасту варианте, возраст >60 лет, повышенные уровни лактатдегидрогеназы в сыворотке крови , низкий статус работоспособности и поражение более чем одного экстранодального участка считаются факторами плохого прогноза у пациентов с DLBCL, БДУ. . [ 22 ] Кроме того, заболевание, которое первоначально поражает яички, молочные железы или матку, имеет относительно высокую скорость распространения на центральную нервную систему, в то время как заболевание, первоначально поражающее почки, надпочечники , яичники или костный мозг, имеет высокую скорость распространения на другие органы. , включая центральную нервную систему. Все эти случаи, а также случаи, первоначально поражающие центральную нервную систему, имеют прогноз от относительно плохого до очень плохого. Случаи, первоначально поражающие желудок, щитовидную железу или одиночный участок кости, имеют относительно хороший прогноз. [ 25 ]
Патофизиология
[ редактировать ]Большинство случаев DLBCL, NOS, по-видимому, являются результатом, по крайней мере частично, поэтапного развития генных изменений, таких как мутации , измененная экспрессия , амплификации (т. е. увеличение количества копий определенных генов) и транслокации из нормальных участков в другие. хромосомные участки. Эти изменения часто приводят к увеличению или снижению производства или функции продукта этих генов и, следовательно, к активности клеточных сигнальных путей, которые регулируют созревание , пролиферацию , выживание, распространение, уклонение от иммунной системы и другие злокачественные проявления. клетки, в которых они происходят. Хотя сообщалось об изменении множества генов при DLBCL, NOS, многие из них могут не способствовать DLBCL, NOS. Изменения в следующих генах часто происходят и предположительно способствуют развитию и/или прогрессированию этого заболевания. [ 14 ]
- BCL2 : Этот ген является протоонкогеном , то есть нормальным геном, который может стать причиной рака при мутации или сверхэкспрессии. Его продукт, белок Bcl-2, регулирует клеточный апоптоз путем ингибирования белков, вызывающих апоптоз, Bcl-2-ассоциированного белка X и гомологичного антагониста-киллера Bcl-2 . [ 27 ]
- BCL6 : Продукт этого гена, Bcl-6, является репрессором транскрипции, который регулирует экспрессию других генов, которые контролируют созревание, пролиферацию и выживание клеток. [ 27 ]
- MYC : Продукт этого протоонкогена, Myc, кодирует фактор транскрипции , который регулирует экспрессию других генов, чьи продукты стимулируют пролиферацию клеток и экспансию в экстраузловые ткани. [ 28 ]
- EZH2 : Продукт этого гена, белок EZH2, представляет собой гистон-лизин N-метилтрансферазу . Тем самым он регулирует экспрессию других генов, которые контролируют созревание лимфоцитов. [ 22 ]
- MYD88 : Продукт этого гена представляет собой адаптерный белок, передающий сигнал , необходимый для трансдукции сигнальных путей интерлейкина-1 и toll-подобных рецепторов . Таким образом, он регулирует NF-κB и сигнальные пути MAPK/ERK , которые контролируют пролиферацию и выживание клеток. [ 27 ]
- CREBBP : Продукт этого гена является коактиватором транскрипции ; он активирует многочисленные факторы транскрипции , некоторые из которых контролируют пролиферацию клеток. [ 14 ]
- CD79A и CD79B : продукты этих генов являются важными компонентами рецептора B-клеток . Мутации в любом гене могут вызвать неконтролируемую активацию и пролиферацию клеток. [ 14 ]
- PAX5 : продукт этого гена, Pax-5, является фактором транскрипции, который контролирует развитие, созревание и выживание B-клеток; он также контролирует экспрессию гена MYC в этих клетках. [ 29 ]
В результате этих генных изменений и, возможно, других изменений, которые еще не идентифицированы, неопластические клетки при DLBCL, NOS демонстрируют патологически сверхактивные NF-κB, PI3K/AKT/mTOR , JAK-STAT 0, MAPK/ERK , B-клетки. рецептор , toll-подобный рецептор и сигнальные пути NF-κB и, таким образом, неконтролируемое прозлокачественное поведение. [ 27 ]
Диагностика
[ редактировать ]При микроскопическом исследовании пораженных тканей выявляются крупные неопластические клетки, которые обычно классифицируются как B-клетки на основании экспрессии маркерных белков B-клеток (например, CD20 , CD19 , CD22 , CD79 , PAX5, BOB1 , OCT2 , иммуноглобулина [обычно IgM , но иногда IgG или IgA )], [ 12 ] CD30 и примерно в 20–25% случаев PD-L1 или PD-L2 (PD-L1 и PD-L2 представляют собой трансмембранные белки , которые обычно функционируют для подавления атаки иммунной системы). [ 22 ] Эти клетки располагаются диффузно, стирают структуру тканей и напоминают клетки центробластов (80% случаев), клетки иммунобластов (8–10% случаев) или анапластические клетки (9% случаев; анапластические клетки имеют причудливые ядра). и другие особенности, которые могут имитировать клетки Рида-Штернберга при болезни Ходжкина или неопластические клетки анапластической крупноклеточной лимфомы ). Редко эти неопластические клетки характеризуются наличием ядер в форме кольца или веретена, выраженных цитоплазматических гранул, множественных выступов микроворсинок или, при осмотре с помощью электронной микроскопии , плотных соединений с другими клетками . [ 12 ] Эти инфильтраты неопластической ткани часто сопровождаются небольшими доброкачественными Т-клеточными лимфоцитами и гистиоцитами, имеющими реактивную морфологию. [ 22 ]
Варианты DLBCL, NOS
[ редактировать ]Всемирная организация здравоохранения, 2016 г., требует, чтобы неопластические клетки в DLBCL, NOS были дополнительно определены на основе того, происходят ли они из B-клеток зародышевого центра (т. е. GBC) или активированных B-клеток (т. е. ABC), как это идентифицировано с помощью профилирования экспрессии генов. (GEP) или являются GBC или не-GBC, как идентифицировано с помощью иммуногистохимического (ИГХ) анализа. По данным GEP, который измеряет все клеточные матричные РНК , GBC и ABC составляют около 50 и ~ 35% случаев DLBCL и NOS соответственно, при этом ~ 15% случаев не поддаются классификации. [ 30 ] Анализы ИГХ измеряют клеточную экспрессию конкретных белков с использованием панели флуоресцентных антител, которые связываются и, следовательно, окрашивают набор ключевых белков. Например, одна коммерчески доступная панель использует три антитела для обнаружения белков CD10, BCL6 и MUM1; GBC экспрессируют, тогда как ABC и неопознанные клетки не экспрессируют эти белки; соответственно, эта, а также другие панели IHC классифицируют ABC и неопределенные типы неопластических клеток вместе как не-GBC. [ 27 ] Лица с вариантами ABC, неклассифицируемыми вариантами и вариантами, не относящимися к GBC, имеют значительно худшие прогнозы, чем люди с вариантом GBC: [ 24 ] соответствующие 5-летняя выживаемость без прогрессирования и общая выживаемость Сообщается, что составляют 73–80% для вариантов GBC и 31–56% для вариантов ABC. Клинически, однако, большинство случаев DLBCL, NOS анализируются с помощью ИГХ и, следовательно, классифицируются как варианты GBC или варианты без GBC, причем варианты без GBC имеют показатели без прогрессирования и общую выживаемость, аналогичную таковым для вариантов ABC. [ 22 ]
Генные и белковые маркеры в неопластических клетках DLBCL, NOS, имеющие клиническое значение, включают CD5 , MYC , BCL2 , BCL6, [ 12 ] CD20, CD19, CD22, CD30, PD-L1 и PD-L2. [ 24 ] 5–10% случаев DLBCL, NOS, в которых неопластические клетки экспрессируют CD5, имеют очень плохой прогноз, который не улучшается даже при агрессивных схемах лечения. Случаи, когда флуоресцентный анализ гибридизации in situ показывает, что неопластические клетки при этом заболевании несут транслокации как в генах MYC , так и в BCL2 или в генах MYC и BCL6 (так называемые лимфомы с двойным попаданием) или во всех трех генах (так называемые лимфомы с тройным попаданием) [ 22 ] связаны с запущенным заболеванием, которое распространяется на центральную нервную систему . [ 31 ] Эти лимфомы, называемые В-клеточными лимфомами высокой степени злокачественности с перестройками MYC, BL2 и/или BL6 или, проще говоря, DH/THL, считаются пограничными DLBCL, NOS. [ 22 ] Они составляют 6–14% всех случаев DLBCL, NOS, а долгосрочная выживаемость составляет всего 20–25%. [ 25 ] Другой вариант В-клеточной лимфомы, который также считается пограничным DLBCL, NOS называется В-клеточной лимфомой высокой степени злокачественности, без уточнения иначе (HGBCL, NOS). [ 22 ] Эти две агрессивные пограничные В-клеточные лимфомы ранее были сгруппированы вместе как «В-клеточная лимфома, не поддающаяся классификации, с признаками, промежуточными между DLBCL и лимфомой Беркитта» (т.е. BCLU), но Всемирная организация здравоохранения разделила их на DH/THL и HGBC, NOS. 2016. [ 16 ] Неопластические клетки в родственном варианте, двойной экспрессирующей лимфоме (т.е. DEL), экспрессируют продукты генов MYC и BCL2 , т.е. белки c-Myc и bcl-2 соответственно, но не имеют транслокаций ни в одном из своих генов. DEL, который составляет около одной трети всех случаев DLBCL, NOS, имеет худший прогноз, чем стандартный DLBCL, NOS, но не такой плохой, как случаи DH/THL. [ 22 ] [ 30 ] Случаи, когда в неопластических клетках наблюдаются изменения гена MYC или его экспрессии без изменений BLC2 или BLC6 , также имеют плохой прогноз. [ 22 ] особенно в случаях, когда MYC ген транслоцируется (т.е. перестраивается) с одним из локусов гена иммуноглобулина . DLBCL, начинающаяся в яичках, представляет собой вариант DLBCL, NOS, который, по мнению некоторых авторов, следует классифицировать как отдельный подтип DLBCL. [ 12 ] Этот вариант, называемый первичной диффузной крупноклеточной В-клеточной лимфомой яичек (PT-DLBCL), представляет собой DLBCL, БДУ, которая в >75% случаев включает активированные B-клетки, т.е. ABC. [ 32 ] Эти клетки, которые обычно имеют морфологию, подобную центробластам , инфильтрируют одно или, в ~6% случаев, оба яичка . PT-DLBCL — агрессивное заболевание, которое часто распространяется на центральную нервную систему. [ 32 ] медиана общей выживаемости и выживаемости без прогрессирования составила 96 и 49 месяцев соответственно. [ 12 ]
Неопластические клетки почти во всех случаях DLBCL, NOS экспрессируют CD20. Коммерчески доступные антитела против CD20, такие как ритуксимаб или обинутузумаб (который иногда используется вместо ритуксимаба), убивают клетки, которые экспрессируют высокие уровни CD20, связываясь с этим белком клеточной поверхности и тем самым нацеливая их на атаку адаптивной иммунной системы хозяина. . Добавление одного из этих иммунотерапевтических агентов к протоколам химиотерапии значительно улучшило прогноз большинства вариантов DLBCL и NOS. [ 22 ] Экспрессия CD30 неопластическими клетками, обнаруживаемая в 10–15% случаев DLBCL, NOS, является благоприятным прогностическим показателем. Как указано в следующем разделе «Лечение и прогноз», экспрессия белков CD20 и CD30, а также белков CD19, CD20, CD22, CD30, CD79A, CD79B и D-L1, экспрессия MYC , BCL2 , MYD88nd и CREBBP. генов и экспрессия PI3K/AKT/mTOR, JAK-STAT, B-клеточного рецептора, toll-подобный рецептор и сигнальные пути NF-κB изучаются в качестве потенциальных терапевтических мишеней для индивидуального лечения GBC и случаев ABC/non-GBC DLBCL, NOS. [ 14 ] [ 22 ]
Лечение и прогнозы
[ редактировать ]Терапия первой линии
[ редактировать ]Терапией первой линии для пациентов с GBC-вариантом DLBCL, NOS является R-CHOP . R-CHOP состоит из ритуксимаба, трех химиотерапевтических препаратов ( циклофосфамида , доксорубицина и винкристина ) и глюкокортикоида ( преднизона или преднизолона ). [ 30 ] Режим обеспечивает излечение, рецидив после ремиссии, [ 22 ] и уровень неэффективности 60–70%, 30–40% и <10% соответственно в случаях варианта GBC. [ 33 ] Рецидивы обычно возникают в течение первых 3 лет после постановки диагноза, в некоторых случаях это происходит после 5 лет. Пациенты, которые невосприимчивы к R-CHOP, имеют рецидив в течение 1 года после постановки диагноза до начала лечения, рецидив в течение 6 месяцев после завершения или прогресс в течение 2 лет после начала R-CHOP, имеют худший прогноз. [ 31 ] R-CHOP менее эффективен и не рекомендуется пациентам с реаранжировками MYC, BL2 и/или BL6, независимо от их типа GBC, ABC или не-GBC. Одной из рекомендаций для лечения этих случаев ДГ/ТГЛ является режим DA-R-EPOCH (ритуксимаб с корректированной дозой, этопозид , преднизолон, онковин, циклофосфамид и гидроксидаунорубицин). SR-EPOCH достигает 2-летней выживаемости на уровне 40–67% по сравнению с выживаемостью ~25% для R-CHOP в этих случаях. [ 30 ] DA-R-EPOCH также рекомендован пациентам с двойной экспрессирующей лимфомой. [ 30 ] хотя некоторые эксперты рекомендуют относиться к этому варианту скорее как к типичному DLCBL, NOS. [ 27 ] Терапией первой линии для пациентов с вариантами ABC, неопределенными или не-GBC был режим DA-R-EPOCH. У пациентов с этими вариантами (включая пациентов с лимфомой с двойной экспрессией) показатель излечения при лечении им составил ~ 40%. [ 30 ] Рандомизированное клиническое исследование, проведенное во Франции, показало, что режим химиотерапии R-ACVBP (ритуксимаб, адриамицин , циклофосфамид, виндезин , блеомицин и цитарабин с последующей последовательной консолидирующей терапией системным метотрексатом , ифосфамидом и этопозидом , а затем цитарабином) достиг значительно лучшего ответа. скорости, чем R-CHOP в случаях варианта ABC/NGC лимфома. [ 27 ] При DLBCL, вариантах NOS, которые имеют тенденцию к распространению или поражению центральной нервной системы, рекомендуется добавлять метотрексат к схемам, не содержащим его, для использования в качестве профилактики для снижения частоты этого осложнения. [ 31 ] Роль аутологичной трансплантации стволовых клеток как дополнения к терапии первой линии при лечении DLBCL, БДУ, включая случаи с плохим прогнозом, неясна. [ 14 ]
показало Клиническое исследование фазы I , что добавление леналидомида к схеме R-CHOP дает примерно 80% полного ответа при GBC, а также при вариантах DLBCL без GBC и NOS. [ 14 ] В настоящее время проводятся два клинических исследования фазы III, чтобы подтвердить эти результаты и определить, превосходит ли схема R-CHOP + леналидомид схему R-CHOP при начальном лечении GBC и/или вариантов без GBC. [ 14 ]
Лечение рецидивирующей и рефрактерной DLBCL, БДУ
[ редактировать ]Пациентов с DLBCL, NOS, у которых произошел рецидив или прогрессирование после терапии первой линии, лечили «схемами спасения», состоящими из высоких доз (также называемых высокоинтенсивными) кондиционирующими химиотерапевтическими препаратами с последующей трансплантацией аутологичных стволовых клеток . Этот режим позволил достичь 3-летней выживаемости без прогрессирования на уровне 21–37%. [ 14 ] Рецидив после этого лечения имеет очень плохой прогноз со средней продолжительностью жизни около 10 месяцев. [ 31 ] Пациенты, у которых трансплантация аутологичных стволовых клеток оказалась неудачной или из-за проблем со здоровьем, не имеют права на трансплантацию аутологичных стволовых клеток, лечились низкодозной (т.е. низкоинтенсивной) химиотерапией по кондиционирующим схемам с последующей трансплантацией аллогенных стволовых клеток . Этот режим позволил добиться 3-летней выживаемости без прогрессирования и общей выживаемости 41% и 52% соответственно. [ 33 ] В настоящее время проводятся дальнейшие исследования для определения лучших схем лечения для этих случаев. [ 14 ] [ 33 ] Пациенты, рефрактерные к терапии первой линии или у которых в течение 12 месяцев после получения терапии спасения (включая трансплантацию костного мозга) по поводу рецидивирующего заболевания произошел рецидив, имели плохой прогноз со средней общей выживаемостью 3,3 и 6,3 месяца соответственно. [ 14 ] Прогноз этих пациентов, по-видимому, улучшается при использовании терапии CAR-T.
химерным антигенным рецептором Т-клеток (т.е. CAR-T) Адоптивная клеточная иммунотерапия стала недавним достижением в лечении рефрактерного и рецидивирующего DLBCL, NOS ( тисагенлеклейцел , аксикабтаген цилолеуцел , лизокабтаген маралеуцел ). Т-клетки химерного антигенного рецептора генетически сконструированы для экспрессии: 1) искусственного Т-клеточного рецептора , состоящего из распознающих антиген и прикрепленных шарнирных доменов, экспрессируемых на их поверхностных мембранах ; 2) поверхностный трансмембранный домен; 3) внутриклеточный домен, который, когда домен распознавания антигена связывает целевой антиген, активирует сигнальные пути, которые заставляют Т-клетку атаковать и убивать клетки, несущие распознанный антиген на своих поверхностных мембранах; и 4) в недавно разработанных стратегиях CAR-T второго поколения - ассоциированная внутриклеточная костимулирующая молекула (например, CD28 или 4-1BB ), которая усиливает активацию сигнальных путей, убивающих клетки. CAR-T-терапия, применительно к DLBCL, NOS, убивает неопластические B-клетки пациента, изолируя Т-клетки ; генную инженерию этих клеток для экспрессии искусственного Т-клеточного рецептора, предназначенного для связывания антигена, экспрессируемого на поверхности их неопластических В-клеток; и введение этих клеток обратно пациенту-донору. Целевым антигеном обычно является CD19 , белок поверхностной мембраны, экспрессируемый практически на всех В-клетках, включая неопластические клетки при DLBCL, NOS. [ 31 ] Однако конструкция АВТОМОБИЛЕЙ [ 34 ] а также антигены, выбранные в качестве их мишеней [ 31 ] постоянно изменяются с целью повышения эффективности этой терапевтической стратегии.
CAR-T-терапия при DLBCL, NOS использовалась у пациентов, которые невосприимчивы к схемам лечения первой линии, а также у пациентов с прогрессированием заболевания (включая трансплантацию аутологичных стволовых клеток). Пациентов сначала лечат кондиционирующей химиотерапией, обычно циклофосфамидом и флударабином , а затем вводят их собственные Т-клетки, которые были созданы для атаки клеток, несущих CD19 или, реже, клеток, несущих CD20 . Метаанализ 17 исследований , в которых использовался этот или очень похожие подходы к лечению DLBCL, NOS, показал, что лечение дало полный и частичный ответ в 61% и 43% соответственно. Хотя в этих исследованиях не было контрольных групп, и они были слишком недавними для значимой оценки продолжительности ремиссии, частота ремиссий была выше, чем ожидалось при использовании других подходов к лечению. Значительные и потенциально летальные терапевтические осложнения этой терапии включали развитие синдрома высвобождения цитокинов (21% случаев), нейротоксичности, т.е. синдрома CAR-T-клеточной энцефалопатии (9% случаев), [ 35 ] и гемофагоцитарный лимфогистиоцитоз/синдром активации макрофагов (т.е. форма гемофагоцитарного лимфогистиоцитоза ). [ 36 ] В отдельных исследованиях в рамках этого метаанализа и за его пределами сообщалось о ремиссиях продолжительностью >2 лет, а также о синдроме высвобождения летальных цитокинов и реакциях нейротоксичности на эту терапию. [ 33 ] В результате этих исследований Комитет по передовой терапии и Комитет по лекарственным средствам для использования человеком Европейского агентства по лекарственным средствам рекомендуют выдать регистрационное удостоверение на тисагенлеклейцел (т.е. Т-клетки химерного антигенного рецептора, направленные против CD19) у взрослых пациентов с DLBCL, БДУ. у которых случился рецидив после двух или более линий системной терапии или они рефрактерны к ним. [ 37 ] Комитет по орфанным лекарственным средствам Европейского агентства по лекарственным средствам рекомендует сохранить за тисагенлеклейцелом статус орфанного препарата . [ 37 ] США Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) также одобрило использование этого препарата для лечения рецидивирующей или рефрактерной DLBCL подтипа крупноклеточной B-клеточной лимфомы у пациентов, у которых не было эффекта после двух или более линий системной терапии. [ 38 ] Моноклональные антитела, направленные против CD19, CD22, CD30 и PD-L1, были разработаны для использования в качестве иммунотерапевтических средств при других гематологических злокачественных новообразованиях и проходят или планируются испытания на предмет их полезности при DLBCL, NOS. [ 22 ] В августе 2020 года FDA одобрило гуманизированный Fc-модифицированный цитолитический CD19, нацеленный на моноклональное антитело тафазитамаб, в сочетании с леналидомидом для лечения взрослых пациентов с рецидивирующим или рефрактерным DLBCL. [ 39 ] В апреле 2021 года FDA одобрило направленный на CD19 антитело конъюгат лонкастуксимаба тезирин, , для лечения взрослых пациентов с рецидивирующим или рефрактерным DLBCL после системной терапии. [ 40 ]
Глофитамаб (Колумви) — биспецифическое моноклональное антитело , одобренное для медицинского применения в Канаде в марте 2023 года. [ 41 ]
Новые методы лечения
[ редактировать ]Экспрессия CD30 неопластическими клетками при DLBCL, NOS является благоприятным прогностическим индикатором; в этих случаях брентуксимаб ведотин может быть полезным дополнением к химиотерапии протоколам . Этот агент представляет собой антитело, нацеленное на CD30, которое доставляет токсин монометилауристатин Е к клеткам, экспрессирующим CD30, обладает терапевтической эффективностью против других лимфом, экспрессирующих CD30, и может оказаться полезным при лечении 10–15% случаев DLBCL, экспрессирующих NOS. этот белок. Неопластические клетки в варианте GBC DLBCL, NOS часто имеют мутации в генах EZH2, BCL2 и CREBBP и сверхактивные сигнальные пути PI3K/AKT/mTOR и JAK-STAT, тогда как неопластические клетки в варианте ABC часто имеют мутации в MYD88, CD79A. и гены CD79B ( полатузумаб ведотин ) и сверхактивный B-клеточный рецептор , toll-подобный рецептор и NF-κB . сигнальные пути [ 22 ] Эти различные генные мутации и нарушение регуляции сигнальных путей также изучаются в качестве потенциальных терапевтических мишеней для индивидуального лечения случаев GBC и случаев ABC/не GBC. [ 14 ] CUDC-907 , ингибитор PI3K и деацетилаз гистонов , оценивается в двух отдельных клинических испытаниях. [ 42 ] [ 43 ] для лечения рефрактерного и/или рецидивирующего DLBCL, БДУ, включая случаи с изменениями в гене MYC . [ 44 ] GSK525762 , ингибитор семейства белков BET , подавляет экспрессию гена MYC и проходит I фазу клинических испытаний. [ 45 ] для лечения В-клеточной лимфомы высокой степени злокачественности с реаранжировками MYC, BL2 и/или BL6 (т.е. DH/THL). RO6870810, еще один ингибитор BET, в сочетании с венетоклаксом , ингибитором белка Bcl-2, также находится в I фазе клинических испытаний. [ 46 ] для лечения DH/THL. [ 44 ] Фармакологическое ингибирование BCL-2 эффективно при большинстве В-клеточных лимфом, но часто приводит к приобретенной резистентности из-за экспрессии других основных антиапоптотических белков семейства BCL-2, таких как BCL-XL и MCL-1 . [ 47 ] Решением этой проблемы может стать комбинированная терапия с использованием ингибитора MCL-1 (S63845) или ингибитора BCL-XL (A-1331852) в дополнение к венетоклаксу. [ 48 ]
Подтипы диффузной крупноклеточной В-клеточной лимфомы
[ редактировать ]Подтипы DLBCL были разделены на группы на основе их отличительной морфологии или иммунофенотипа , отличительных клинических проблем и отличительной вирусной этиологии. Прогнозы и лечение этих подтипов варьируются в зависимости от их тяжести. Большинство подтипов являются агрессивными заболеваниями и, следовательно, лечатся так же, как и DLBCL, NOS. Более подробную информацию об этих подтипах, включая способы их лечения, можно найти в соответствующих ссылках на основные статьи. [ нужна ссылка ]
DLBCL с отличительной морфологией или иммунофенотипом
[ редактировать ]Крупноклеточная В-клеточная лимфома, богатая Т-клетками/гистиоцитами
[ редактировать ]Крупноклеточная В-клеточная лимфома, богатая Т-клетками/гистиоцитами (THRLBCL), представляет собой DLBCL, при которой опухоли, содержащие небольшое количество обычно крупных неопластических B-клеток, встроенных в фон реактивных Т-клеток и гистиоцитов. в печени, селезенке, костях развиваются костный мозг и/или, реже, другие участки. У пациентов обычно заболевание развивается на поздних стадиях; их общая трехлетняя выживаемость в различных исследованиях колеблется от 46% до 72%. [ 12 ]
ALK+ крупноклеточная В-клеточная лимфома
[ редактировать ]ALK+ крупноклеточная В-клеточная лимфома (ALK+ LBCL) представляет собой DLBCL, при которой неопластические лимфоциты, экспрессирующие белок рецептора тирозинкиназы ALK, инфильтрируют лимфатические узлы , а также экстранодальные участки, например , средостение , кости, костный мозг , носоглотку, язык, желудок, печень. , селезенка и кожа. Около 60% этих людей имеют позднюю стадию заболевания. ALK+ LBCL имеет общую 5-летнюю выживаемость ~34%. [ 12 ]
Плазмобластная лимфома
[ редактировать ]Плазмобластная лимфома (ПБЛ) представляет собой DLBCL, при которой неопластические иммунобластные или плазмобластные клетки, встроенные в фон других типов клеток, инфильтрируют полость рта/носа или, гораздо реже, желудочно-кишечный тракт. [ 12 ] Около 70% людей с PBL инфицированы EBV. [ 49 ] и/или (особенно при заболеваниях полости рта/носа) вирус иммунодефицита человека (ВИЧ). [ 12 ] PBL — агрессивное заболевание со средней продолжительностью жизни около 15 месяцев. [ 12 ]
Внутрисосудистая крупноклеточная В-клеточная лимфома
[ редактировать ]Внутрисосудистая крупноклеточная В-клеточная лимфома (ИВКЛКЛ) представляет собой ДВКЛКЛ, при которой неопластические В-клетки среднего и крупного размера инфильтрируют мелкие и средние кровеносные сосуды и синусоиды в печени, селезенке и/или костном мозге. IVLBCL может быть связан с гемофагическим синдромом (т.е. с избыточной секрецией цитокинов и системным воспалением). Пациенты с последним синдромом имеют очень короткую продолжительность жизни. [ 12 ] Плохой прогноз этого заболевания был значительно улучшен с помощью ритуксимаба или аналогичных иммунохимиотерапевтических препаратов, но в значительной части случаев, ответивших на лечение, возникает рецидив, часто с поражением центральной нервной системы. [ 50 ]
Крупноклеточная В-клеточная лимфома с реаранжировкой IRF4
[ редактировать ]Крупноклеточная В-клеточная лимфома с перегруппировкой IRF4 (LBCL с перегруппировкой IRF4) представляет собой DLBCL, при которой тканевые инфильтраты, содержащие неопластические B-клетки среднего или большого размера, сильно экспрессируют хромосомную транслокацию с участием гена IRF4 на коротком плече хромосомы 6. Эти клетки образуют фолликулярные , фолликулярно-диффузные или целиком диффузные инфильтраты [ 12 ] в миндалинах Вальдейера или других областях головы и шеи. Заболевание, составляющее ~0,05% всех случаев DLBCL, встречается преимущественно у детей и молодых людей и обычно имеет хороший прогноз. [ 24 ] В случаях с фолликулярным паттерном тканевых инфильтратов заболевание часто протекает вяло, имеет отличный прогноз после иссечения и может не нуждаться в химиотерапии. Напротив, случаи с чисто диффузной тканевой инфильтрацией часто требуют химиотерапии. [ 12 ]
DLBCL с характерными клиническими проблемами
[ редактировать ]Первичная медиастинальная крупноклеточная В-клеточная лимфома
[ редактировать ]Первичная медиастинальная крупноклеточная В-клеточная лимфома (ПМБЛ), также называемая первичной медиастинальной (тимической) В-крупноклеточной лимфомой, представляет собой DLBCL, при которой неопластические инфильтраты В-клеток обычно локализуются в склеротических /фиброзных тканях тимуса и медиастинальных лимфатических узлах. Заболевание составляет 6–10% всех случаев DLBCL, проявляется на ранней стадии заболевания примерно в 80% случаев и имеет общую выживаемость в течение 5 лет 75–85%. [ 12 ]
Первичная кожная диффузная крупноклеточная В-клеточная лимфома, тип ноги
[ редактировать ]Первичная кожная диффузная крупноклеточная В-клеточная лимфома типа ног (PCDLBCL-LT) представляет собой DLBCL, при которой диффузные структуры иммунобластных и/или центробластных B-клеток инфильтрируют дерму и/или подкожную ткань преимущественно, но не исключительно, ног. Общая 5-летняя выживаемость при этом заболевании составляет 50–60%. [ 12 ]
Первичная диффузная крупноклеточная В-клеточная лимфома центральной нервной системы
[ редактировать ]Первичная диффузная крупноклеточная В-клеточная лимфома центральной нервной системы (DLBCL-CNS, также называемая первичной лимфомой центральной нервной системы [PCNSL]) представляет собой DLBCL, при которой инфильтрируются диффузные структуры неопластических B-клеток с центробластными, иммунобластными или плохо дифференцированными признаками. головной, спинной мозг, лептоменинги или глаз. [ 24 ] Заболевание обычно проявляется как единичное поражение со склонностью к супратенториальной области головного мозга, но может поражать глаз в 15–25% случаев, спинномозговую жидкость в 7–42% случаев и спинной мозг примерно в 1% случаев. случаев. Заболевание имеет 5-летнюю общую выживаемость около 30%. [ 12 ]
Диффузная крупноклеточная В-клеточная лимфома, связанная с хроническим воспалением
[ редактировать ]Диффузная В-крупноклеточная лимфома, связанная с хроническим воспалением (DLBCL-CI), представляет собой лимфопролиферативное заболевание, связанное с вирусом Эпштейна-Барр, возникающее у людей с длительным и постоянным анамнезом хронического воспаления. легких Очаги заболевания состоят из крупных, зрелых B-клеток, инфильтрирующих плевру и близлежащие ткани. Большинство случаев наблюдалось у пациентов, которым был назначен пневмоторакс (т. е. терапевтическое введение воздуха в грудную полость для того, чтобы коллапсировать и тем самым «отдохнуть» легкое) для лечения туберкулеза легких , перешедшего в пиоторакс (т. е. гной в плевральной полости). ). Фибрин-ассоциированная крупноклеточная В-клеточная лимфома (FA-DLBCL), часто рассматриваемая как подтип DLBCL-CI, представляет собой инфильтрацию крупных неопластических B-клеток и прикрепление фибрина к протезу (например, сердечному клапану, ортопедическому устройству) или накапливаются в гидроцеле , псевдокисте , сердечной миксоме или хронической субдуральной гематоме . В-клетки в этих поражениях часто, но не всегда, инфицированы вирусом Эпштейна-Барра. [ 12 ] DLBCL-CI, возникающая в случаях эмпиемы плевры (иногда называемой пиоторакс-ассоциированной лимфомой , т.е. PAL), представляет собой агрессивную лимфому с пятилетней общей выживаемостью 20–35%; FA-DLBCL при вовлечении сердца (например, при миксоммах или протезных клапанах) или сосудистых структурах (например, при тромбированных сосудистых трансплантатах) может приводить к опасным для жизни сердечно-сосудистым осложнениям, особенно инсультам. Однако, помимо этих осложнений, DLBCL-CI обычно имеет весьма благоприятный исход. [ 24 ]
Лимфоматоидный гранулематоз
[ редактировать ]Лимфоматоидный гранулематоз (LYG) представляет собой DLBCL, при котором крупные атипичные B-клетки с иммунобластными или симптомами, подобными болезни Ходжкина , инфицированные вирусом Эпштейна-Барра, сосредотачиваются вокруг и разрушают микроциркуляторное русло . Лимфоматоидный гранулематоз почти всегда поражает легкие, но может одновременно поражать мозг, периферическую нервную систему, кожу, почки, печень, желудочно-кишечный тракт и/или верхние дыхательные пути; LYG чаще встречается у людей с синдромом Вискотта-Олдрича или ВИЧ , а также у лиц с иммуносупрессией из-за химиотерапии или трансплантации органов. [ 12 ] Прогноз заболевания сильно варьируется: пациентам с легкой степенью заболевания часто не требуется никакого лечения, кроме бдительного ожидания, в то время как пациентам с высокой степенью заболевания обычно требуется химиотерапия. [ 51 ]
Первичная выпотная лимфома
[ редактировать ]Первичная выпотная лимфома (ПЭЛ) представляет собой DLBCL, при которой неопластические В-клетки, напоминающие иммунобласты, плазмобласты или клетки Рида-Штернберга, инфильтрируют плевральную , перикардиальную или перитонеальную мембраны, окружающие легкие, сердце и органы брюшной полости соответственно. Эта инфильтрация приводит к просачиванию жидкости в полости, окруженные этими оболочками, т. е. к плевральным выпотам , перикардиальным выпотам и абдоминальному асциту . В некоторых случаях ПЭЛ также поражаются желудочно-кишечный тракт и лимфатические узлы. Заболевание возникает преимущественно у людей с ослабленным иммунитетом или у людей с положительным результатом теста на ВИЧ. [ 12 ] а также латентно инфицированы герпесвирусом, ассоциированным с саркомой Капоши ; [ 13 ] ПЭЛ — агрессивное заболевание с общей выживаемостью в течение 1 года ~30%. [ 13 ]
DLBCL, управляемый вирусами
[ редактировать ]Положительная на вирус Эпштейна-Барра диффузная крупноклеточная В-клеточная лимфома, не уточненная иначе
[ редактировать ]Положительная по вирусу Эпштейна-Барр диффузная крупноклеточная В-клеточная лимфома, не уточненная иначе (EBV+ DLBCL, NOS) представляет собой В-клеточную лимфому, при которой неопластические В-клетки, инфицированные вирусом Эпштейна-Барра, вызывают заболевание, не подпадающее под определение вируса Эпштейна-Барра. другие подтипы DLBCL. При EBV+ DLBCL небольшие неопластические B-клетки, другие типы лимфоцитов, плазматические клетки, гистиоциты и эпителиоидные клетки с вкраплениями клеток, подобных Риду-Штернбергу. [ 24 ] инфильтрируют, почти исключительно, лимфатические узлы. [ 11 ] У пожилых пациентов с этим заболеванием медиана выживаемости составляет около 2 лет, тогда как у молодых пациентов наблюдаются длительные ремиссии, связанные с лечением, в> 80% случаев. [ 24 ]
HHV8-положительная диффузная крупноклеточная В-клеточная лимфома, БДУ
[ редактировать ]HHV8-положительная диффузная крупноклеточная B-клеточная лимфома, БДУ (HHV8+DLBCL, NOS; также называемая HHV8-положительная диффузная крупноклеточная B-клеточная лимфома [HHV8+DLBCL]) представляет собой DLBCL, при которой герпесвирус, инфицированный саркомой Капоши , имеет размер от среднего до большого размера. Неопластические B-клетки неопластического размера, напоминающие лимфоциты или иммунобласты, инфильтрируют лимфу. узлы (~80% случаев) и при диссеминированном (20% случаев) печень и селезенку. Эта инфильтрация обычно нарушает нормальную архитектуру пораженных тканей. DLBCL HHV8+ развивается у ВИЧ -инфицированных лиц в ~50% случаев, у лиц с мультицентрической болезнью Кастлемана, плазмоклеточным вариантом в редких случаях и у лиц с саркомой Капоши в редких случаях. DLBCL HHV8+ обычно протекает агрессивно и имеет плохой прогноз. [ 12 ]
Сопутствующие расстройства
[ редактировать ]Helicobacter pylori Диффузная крупноклеточная В-клеточная лимфома, ассоциированная с
[ редактировать ]Редкие случаи DLBCL связаны с присутствием бактерии Helicobacter pylori в неопластических B-клетках. [ 7 ] Хотя гистология ассоциированной с Helicobacter pylori диффузной крупноклеточной В-клеточной лимфомы ( H. pylori + DLBCL) типична для DLBCL, заболевание иногда представляет собой прогрессирование лимфомы из мантийных клеток , часто ограничивается желудком и менее агрессивно, чем большинство DLBCL. случаях и может реагировать на схему приема лекарств, состоящую из антибиотиков и ингибиторов протонной помпы, направленных на уничтожение бактерии. [ 52 ] [ 23 ] Возможно, из-за этих особенностей заболевания H. pylori + DLBCL не была классифицирована Всемирной организацией здравоохранения в 2016 году как DLBCL. [ 23 ]
Недавние исследования показывают, что локализованную раннюю стадию H. pylori + DLBCL, ограниченную желудком, успешно лечат с помощью протоколов эрадикации H. pylori, состоящих из двух или более антибиотиков плюс ингибитор протонной помпы. [ 53 ] [ 52 ] [ 54 ] [ 23 ] Тем не менее, эти исследования также согласны с тем, что за пациентами, получающими одну из этих схем эрадикации H. pylori , необходимо тщательно наблюдать: тех, кто не реагирует на эти схемы или у них ухудшается состояние, следует перевести на схему химиотерапии (например, R-CHOP) и/или , при осложненном обширном заболевании, хирургическом вмешательстве и/или местной лучевой терапии. [ 52 ] [ 23 ]
Слизисто-кожная язва, положительная на вирус Эпштейна-Барра
[ редактировать ]Слизисто-кожная язва, положительная к вирусу Эпштейна-Барра (EBVMCU), была впервые описана как лимфопролиферативное заболевание, при котором инфицированные вирусом Эпштейна-Барра B-клетки пролиферируют и вызывают изъязвления на слизистых оболочках и коже у людей с ослабленным иммунитетом . Его поражения состоят из вирус-положительных атипичных B-клеток различного размера, которые по общепринятым гистопатологическим критериям указывают на то, что поражения являются формой DLBCL. Поскольку эти поражения спонтанно регрессируют без противоракового лечения, ЭБВМК теперь считается псевдозлокачественным заболеванием. [ 55 ] У пожилых людей, у которых имеется заболевание, но нет других причин для иммуносупрессии, может наблюдаться рецидивирующее и ремиттирующее течение, при этом язвы ухудшаются, но затем спонтанно регрессируют. [ 56 ] В персистирующих и/или тяжелых симптоматических случаях наблюдался отличный ответ на ритуксимаб . [ 57 ] У людей, у которых эти язвы развиваются в результате иммуносупрессивной терапии, обычно наблюдается ремиссия после снижения дозировки препаратов, используемых при иммуносупрессивном лечении. У большинства этих пациентов рецидивов не возникает. [ 56 ]
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ «Клиническая оценка классификации неходжкинских лимфом Международной группы по изучению лимфомы. Проект классификации неходжкинских лимфом» . Кровь . 89 (11): 3909–3918. Июнь 1997 г. doi : 10.1182/blood.V89.11.3909 . ПМИД 9166827 .
- ^ Мортон Л.М., Ван С.С., Девеса С.С., Хартге П., Вайзенбургер Д.Д., Линет М.С. (январь 2006 г.). «Схема заболеваемости лимфомой по подтипам ВОЗ в США, 1992–2001 гг.» . Кровь . 107 (1): 265–276. дои : 10.1182/кровь-2005-06-2508 . ЧВК 1895348 . ПМИД 16150940 .
- ^ Jump up to: а б Смит А., Хауэлл Д., Патмор Р., Джек А., Роман Э. (ноябрь 2011 г.). «Заболеваемость гематологическими злокачественными новообразованиями по подтипам: отчет Сети исследований гематологических злокачественных опухолей» . Британский журнал рака . 105 (11): 1684–1692. дои : 10.1038/bjc.2011.450 . ПМК 3242607 . ПМИД 22045184 .
- ^ Смит А., Роман Э., Хауэлл Д., Джонс Р., Патмор Р., Джек А. (март 2010 г.). «Сеть исследований гематологических злокачественных новообразований (HMRN): новая информационная стратегия для популяционной эпидемиологии и исследований в области здравоохранения» . Британский журнал гематологии . 148 (5): 739–753. дои : 10.1111/j.1365-2141.2009.08010.x . ПМК 3066245 . ПМИД 19958356 .
- ^ Кумар В., Аббас А.К., Фауст Н., Астер Дж.К. (28 мая 2009 г.). Роббинс и Котран Патологическая основа болезней . Elsevier Науки о здоровье. п. 607. ИСБН 978-1-4377-2015-0 .
- ^ Фриман А.С., Астер Дж.С. (2012). «Эпидемиология, клинические проявления, патологические особенности и диагностика диффузной крупноклеточной В-клеточной лимфомы» . В Басове Д.С. (ред.). До настоящего времени . Уолтем, Массачусетс: UpToDate.
- ^ Jump up to: а б с Казуло С., Фридберг Дж. (2017). «Трансформация лимфомы маргинальной зоны (и ассоциация с другими лимфомами)». Лучшие практики и исследования. Клиническая гематология . 30 (1–2): 131–138. дои : 10.1016/j.beha.2016.08.029 . ПМИД 28288708 .
- ^ Абуэльгасим К.А., Рехан Х., Алсубайе М., Аль Атви Н., Аль Балви М., Альшиебан С., Альмугайри А. (март 2018 г.). «Сосуществование хронического миелолейкоза и диффузной крупноклеточной В-клеточной лимфомы с предшествующим хроническим лимфоцитарным лейкозом: описание случая и обзор литературы» . Журнал отчетов о медицинских случаях . 12 (1): 64. дои : 10.1186/s13256-018-1612-4 . ПМЦ 5845776 . ПМИД 29524963 .
- ^ Свердлов и др. 2008 , с. 233.
- ^ Кастильо Дж.Дж., Бельтран Б.Е., Миранда Р.Н., Янг К.Х., Чавес Дж.К., Сотомайор Э.М. (июль 2018 г.). «EBV-положительная диффузная крупноклеточная B-клеточная лимфома, не указанная иначе: обновленная информация о диагностике, стратификации риска и лечении за 2018 год» . Американский журнал гематологии . 93 (7): 953–962. дои : 10.1002/ajh.25112 . hdl : 20.500.12727/6261 . ПМИД 29984868 .
- ^ Jump up to: а б Николае А., Питталуга С., Абдулла С., Стейнберг С.М., Фам Т.А., Дэвис-Хилл Т., Си Л., Раффельд М., Джаффе Э.С. (август 2015 г.). «EBV-положительные крупноклеточные B-клеточные лимфомы у молодых пациентов: узловая лимфома с признаками толерогенной иммунной среды» . Кровь . 126 (7): 863–72. doi : 10.1182/blood-2015-02-630632 . ПМЦ 4536540 . ПМИД 25999451 .
- ^ Jump up to: а б с д и ж г час я дж к л м н тот п д р с т в v В х и Суксвай Н., Ляпичев К., Хури Дж.Д., Медейрос Л.Дж. (ноябрь 2019 г.). «Диффузные крупноклеточные варианты В-клеточной лимфомы: обновленная информация». Патология . 52 (1): 53–67. дои : 10.1016/j.pathol.2019.08.013 . PMID 31735345 . S2CID 208142227 .
- ^ Jump up to: а б с Симада К., Хаякава Ф., Кийой Х. (ноябрь 2018 г.). «Биология и лечение первичной выпотной лимфомы» . Кровь . 132 (18): 1879–1888. дои : 10.1182/blood-2018-03-791426 . ПМИД 30154110 .
- ^ Jump up to: а б с д и ж г час я дж к л Лю Ю, Барта СК (май 2019 г.). «Диффузная крупноклеточная В-клеточная лимфома: обновленная информация о диагностике, стратификации риска и лечении за 2019 год» . Американский журнал гематологии . 94 (5): 604–616. дои : 10.1002/ajh.25460 . ПМИД 30859597 .
- ^ Goldman & Schafer 2012 , с. 1222.
- ^ Jump up to: а б Свердлов С.Х., Кампо Э., Пилери С.А., Харрис Н.Л., Стейн Х., Зиберт Р., Адвани Р., Гильмини М., Саллес Г.А., Зеленец А.Д., Яффе Э.С. (май 2016 г.). «Пересмотр классификации лимфоидных новообразований Всемирной организации здравоохранения 2016 г.» . Кровь . 127 (20): 2375–90. дои : 10.1182/blood-2016-01-643569 . ПМЦ 4874220 . ПМИД 26980727 .
- ^ Goldman & Schafer 2012 , с. 1225.
- ^ Акюрек Н., Унер А., Бенекли М., Бариста И. (сентябрь 2012 г.). «Прогностическое значение перестроек MYC, BCL2 и BCL6 у пациентов с диффузной крупноклеточной В-клеточной лимфомой, получавших циклофосфамид, доксорубицин, винкристин и преднизон плюс ритуксимаб» . Рак . 118 (17): 4173–4183. дои : 10.1002/cncr.27396 . ПМИД 22213394 . S2CID 19134744 .
- ^ Фейжер П., Ван Хуф А., Себбан С., Солаль-Селиньи П., Буабдаллах Р., Ферме С. и др. (июнь 2005 г.). «Отдаленные результаты исследования R-CHOP в лечении пожилых пациентов с диффузной крупноклеточной В-клеточной лимфомой: исследование Groupe d'Etude des Lymphomes de l'Adulte» . Журнал клинической онкологии . 23 (18): 4117–4126. дои : 10.1200/JCO.2005.09.131 . ПМИД 15867204 . S2CID 23556248 .
- ^ Ализаде А.А., Эйзен М.Б., Дэвис Р.Э., Ма С., Лоссос И.С., Розенвальд А. и др. (февраль 2000 г.). «Отличные типы диффузной крупноклеточной В-клеточной лимфомы, выявленные с помощью анализа экспрессии генов». Природа . 403 (6769): 503–511. Бибкод : 2000Natur.403..503A . дои : 10.1038/35000501 . ПМИД 10676951 . S2CID 4382833 .
- ^ Свердлов и др. 2008 , стр. 233–7.
- ^ Jump up to: а б с д и ж г час я дж к л м н тот п д Ли С., Янг К.Х., Медейрос Л.Дж. (январь 2018 г.). «Диффузная В-крупноклеточная лимфома» . Патология . 50 (1): 74–87. дои : 10.1016/j.pathol.2017.09.006 . ПМИД 29167021 . S2CID 20839613 . [ постоянная мертвая ссылка ]
- ^ Jump up to: а б с д и Ченг Ю, Сяо Ю, Чжоу Р, Ляо Ю, Чжоу Дж, Ма Х (август 2019 г.). «Прогностическое значение инфекции Helicobacter pylori при диффузной крупноклеточной В-клеточной лимфоме желудка» . БМК Рак . 19 (1): 842. doi : 10.1186/s12885-019-6067-5 . ПМК 6712724 . PMID 31455250 .
- ^ Jump up to: а б с д и ж г час Гримм К.Э., О'Мэлли Д.П. (февраль 2019 г.). «Агрессивные В-клеточные лимфомы в пересмотренной классификации ВОЗ опухолей кроветворной и лимфоидной тканей 2017 года». Анналы диагностической патологии . 38 : 6–10. doi : 10.1016/j.anndiagpath.2018.09.014 . ПМИД 30380402 . S2CID 53196244 .
- ^ Jump up to: а б с д Оллила Т.А., Ольшевский А.Я. (июнь 2018 г.). «Экстранодальная диффузная крупноклеточная В-клеточная лимфома: молекулярные особенности, прогноз и риск рецидива центральной нервной системы» . Современные возможности лечения онкологии . 19 (8): 38. дои : 10.1007/s11864-018-0555-8 . ПМК 6294323 . ПМИД 29931605 .
- ^ Пилери С., Понцони М. (2017). «Патология узловых лимфом маргинальной зоны». Лучшие практики и исследования. Клиническая гематология . 30 (1–2): 50–55. дои : 10.1016/j.beha.2016.11.001 . ПМИД 28288717 .
- ^ Jump up to: а б с д и ж г Абрамсон Дж.С. (сентябрь 2019 г.). «Ответ лимфоме: как современная диагностика выявляет подгруппы диффузных крупных В-клеточных лимфом высокого риска и меняет лечение?» . Рак . 125 (18): 3111–3120. дои : 10.1002/cncr.32145 . ПМИД 31287161 .
- ^ Анупама Р., Чжан Дж. (октябрь 2017 г.). «Генетические и функциональные факторы диффузной крупноклеточной В-клеточной лимфомы» . Клетка . 171 (2): 481–494. дои : 10.1016/j.cell.2017.09.027 . ПМК 5659841 . ПМИД 28985567 .
- ^ Шахджахани М, Норози Ф, Ахмадзаде А, Шахраби С, Таваколи Ф, Аснафи А.А., Саки Н (январь 2015 г.). «Роль Pax5 при лейкемии: значение диагностики и прогноза». Медицинская онкология (Нортвуд, Лондон, Англия) . 32 (1): 360. doi : 10.1007/s12032-014-0360-6 . ПМИД 25428382 . S2CID 7127158 .
- ^ Jump up to: а б с д и ж Кабанильяс Ф, Шах Б (декабрь 2017 г.). «Достижения в диагностике и лечении диффузной крупноклеточной B-клеточной лимфомы». Клиническая лимфома, миелома и лейкемия . 17 (12): 783–796. дои : 10.1016/j.clml.2017.10.007 . ПМИД 29126866 . S2CID 25304758 .
- ^ Jump up to: а б с д и ж Чавес Дж. К., Локк, Флорида (июнь 2018 г.). «CAR Т-клеточная терапия В-клеточных лимфом» . Лучшие практики и исследования. Клиническая гематология . 31 (2): 135–146. дои : 10.1016/j.beha.2018.04.001 . ПМК 6716161 . ПМИД 29909914 .
- ^ Jump up to: а б Тва ДДВ, Мотток А, Сэвидж К.Дж., Стейдл С (май 2018 г.). «Патобиология первичной диффузной В-клеточной лимфомы яичка: значение для новых методов лечения». Обзоры крови . 32 (3): 249–255. дои : 10.1016/j.blre.2017.12.001 . ПМИД 29289361 .
- ^ Jump up to: а б с д Гиссельбрехт К., Ван Ден Несте Э (сентябрь 2018 г.). «Как я веду пациентов с рецидивирующей/рефрактерной диффузной крупноклеточной В-клеточной лимфомой» . Британский журнал гематологии . 182 (5): 633–643. дои : 10.1111/bjh.15412 . ПМК 6175435 . ПМИД 29808921 .
- ^ Ли Ю.Х., Ким Ч.Х. (июль 2019 г.). «Эволюция Т-клеточной терапии химерным антигенным рецептором (CAR): современное состояние и перспективы на будущее». Архивы фармацевтических исследований . 42 (7): 607–616. дои : 10.1007/s12272-019-01136-x . ПМИД 30830661 . S2CID 73475110 .
- ^ Чжэн XH, Чжан XY, Донг QQ, Чен Ф, Ян СБ, Ли ВБ (январь 2020 г.). «Эффективность и безопасность Т-клеток химерного антигенного рецептора при лечении В-клеточной лимфомы: систематический обзор и метаанализ» . Китайский медицинский журнал . 133 (1): 74–85. дои : 10.1097/CM9.0000000000000568 . ПМК 7028209 . ПМИД 31923107 .
- ^ Хопфингер Г., Ягер У., Ворел Н. (апрель 2019 г.). «CAR-T-клеточная терапия при диффузной крупноклеточной B-клеточной лимфоме: шумиха и надежда» . Гемасфера . 3 (2): е185. дои : 10.1097/HS9.0000000000000185 . ПМК 6746029 . ПМИД 31723824 .
- ^ Jump up to: а б Али С, Кьекен Р, Нидерлендер С, Марки Дж, Сондерс Т.С., Опсата М, Молту К, Бремнес Б, Грёневик Е, Муусс М, Хоконсен Г.Д., Скибели В, Калланд М.Э., Ван И, Буахордет И, Урбаниак А, Джонстон Дж. 2000, Рантелл К., Керваш Э., Шюсслер-Ленц М., Салмонсон Т., Берг Дж., Гиссельбрехт К., Цогани К., Пападули И., Пиньятти Ф. (октябрь 2019 г.). «Обзор Европейского агентства по лекарственным средствам Кимрии (Тисагенлеклейцел) для лечения острого лимфобластного лейкоза и диффузной крупноклеточной В-клеточной лимфомы» . Онколог 25 (2): теонколог.2019–0233. doi : 10.1634/теонколог.2019-0233 . ПМК 7011647 . ПМИД 31619548 .
- ^ Бушку Н., Касамон Ю.Л., де Кларо Р.А., Джордж Б., Лин Х, Ли С., Блюменталь Г.М., Брайан В., Макки А.Э., Паздур Р. (март 2019 г.). «Краткий обзор одобрения FDA: аксикабтаген цилолеуцел для лечения рецидивирующей или рефрактерной крупноклеточной B-клеточной лимфомы». Клинические исследования рака . 25 (6): 1702–1708. дои : 10.1158/1078-0432.CCR-18-2743 . ПМИД 30413526 . S2CID 53249281 .
- ^ «Монджуви: препараты, одобренные FDA» . FDA США . Проверено 20 августа 2020 г.
- ^ «FDA выдает ускоренное одобрение лонкастуксимаба тезирин-липила для лечения крупноклеточной В-клеточной лимфомы» . FDA . 11 июня 2021 г.
- ^ «Колумви (глофитамаб для инъекций) получает разрешение Министерства здравоохранения Канады с условиями для взрослых пациентов с рецидивирующей или рефрактерной диффузной крупноклеточной B-клеточной лимфомой» (пресс-релиз). Рош Канада. 25 марта 2023 г. Проверено 24 апреля 2023 г. - через Cision Canada.
- ^ «Исследование по оценке эффективности и безопасности CUDC-907 у пациентов с RR DLBCL, включая пациентов с изменениями MYC» . ClinicalTrials.gov . 30 августа 2019 г.
- ^ «Исследование по оценке безопасности, переносимости и фармакокинетики фимепиностата (CUDC-907) у пациентов с лимфомой» . ClinicalTrials.gov . 5 мая 2021 г.
- ^ Jump up to: а б Хорошо, CY, Медейрос LJ (январь 2020 г.). «В-клеточная лимфома высокой степени злокачественности: термин, измененный в пересмотренной классификации ВОЗ». Патология . 52 (1): 68–77. дои : 10.1016/j.pathol.2019.09.008 . ПМИД 31735344 . S2CID 208144461 .
- ^ «Испытание новой комбинации противораковых препаратов, энтиностата и GSK525762C, для лечения распространенных и рефрактерных солидных опухолей и лимфом» . ClinicalTrials.gov . 25 сентября 2020 г.
- ^ «Исследование по оценке безопасности, фармакокинетики и клинической активности комбинации RO6870810 и венетоклакса с ритуксимабом или без него у участников с рецидивирующей/рефрактерной DLBCL и/или B-клеточной лимфомой высокой степени и/или B-клеточной лимфомой высокой степени злокачественности» С MYC и/или BCL2 и/или BCL6" . ClinicalTrials.gov . 27 января 2021 г.
- ^ Чжао X, Рен Ю, Лоулор М, Шах Б.Д., Парк П.М., Лвин Т. и др. (май 2019 г.). «Потеря ампликона BCL2 и ремоделирование транскрипции приводят к устойчивости ABT-199 в моделях B-клеточной лимфомы» . Раковая клетка . 35 (5): 752–766.е9. doi : 10.1016/j.ccell.2019.04.005 . ПМЦ 6945775 . ПМИД 31085176 .
- ^ Денглер М.А., Тех К.Э., Тийссен Р., Гангода Л., Лан П., Херольд М.Дж. и др. (февраль 2020 г.). «Мощная эффективность терапии на основе ингибиторов MCL-1 в доклинических моделях лимфомы мантийных клеток». Онкоген . 39 (9): 2009–2023. дои : 10.1038/s41388-019-1122-x . ПМИД 31772331 . S2CID 208302779 .
- ^ Резк С.А., Чжао X, Вайс Л.М. (июнь 2018 г.). «Лимфоидная пролиферация, связанная с вирусом Эпштейна-Барра, обновленная информация за 2018 год». Патология человека . 79 : 18–41. дои : 10.1016/j.humpath.2018.05.020 . ПМИД 29885408 . S2CID 47010934 .
- ^ Понцони М., Кампо Э., Накамура С. (октябрь 2018 г.). «Внутрисосудистая крупноклеточная В-клеточная лимфома: хамелеон с множеством лиц и множеством масок» . Кровь . 132 (15): 1561–1567. дои : 10.1182/blood-2017-04-737445 . ПМИД 30111607 .
- ^ Чавес Х.К., Сандовал-Сус Дж., Хорна П., Далия С., Белло С., Чеверник П., Сотомайор Э.М., Сокол Л., Шах Б. (август 2016 г.). «Лимфоматоидный гранулематоз: опыт одного учреждения и обзор литературы». Клиническая лимфома, миелома и лейкемия . 16 (Приложение): S170–4. дои : 10.1016/j.clml.2016.02.024 . ПМИД 27521314 .
- ^ Jump up to: а б с Куо Ш., Йе К.Х., Чен Л.Т., Линь К.В., Сюй П.Н., Сюй С., Ву М.С., Цзэн Ю.С., Цай Х.Дж., Ван Х.П., Ченг А.Л. (июнь 2014 г.). «Диффузная крупноклеточная В-клеточная лимфома желудка, связанная с Helicobacter pylori: отдельное заболевание с меньшей агрессивностью и более высокой химиочувствительностью» . Журнал рака крови . 4 (6): е220. дои : 10.1038/bcj.2014.40 . ПМК 4080211 . ПМИД 24949857 .
- ^ Пайдас С (апрель 2015 г.). «Эрадикация Helicobacter pylori при диффузной крупноклеточной В-клеточной лимфоме желудка» . Всемирный журнал гастроэнтерологии . 21 (13): 3773–6. дои : 10.3748/wjg.v21.i13.3773 . ПМЦ 4385524 . ПМИД 25852262 .
- ^ Цай HJ, Тай JJ, Чен LT, Ву М.С., Йе К.Х., Линь CW, Ван ТЭ, Ван Х.П., Ю Ф.Дж., Лю Дж.М., Сяо К.Ф., Ченг TY, Йе HJ, Ко CW, Чен MJ, Ло GH, Сюй ПИ , Чанг К.С., Хван В.С., Чуанг СС, Ли Х.В., Шун К.Т., Чиу К.Ф., Ван В.М., Се С.И., Лю Т.В., Линь Дж.Т., Куо Ш., Ченг А.Л. (ноябрь 2019 г.). «Многоцентровое проспективное исследование антибиотикотерапии первой линии при лимфоме лимфоидной ткани, ассоциированной со слизистой оболочкой желудка, на ранней стадии и диффузной крупноклеточной В-клеточной лимфоме с гистологическими признаками лимфоидной ткани, ассоциированной со слизистой оболочкой» . Гематологическая . 105 (7): е349–е354. doi : 10.3324/haematol.2019.228775 . ПМЦ 7327622 . ПМИД 31727764 .
- ^ Икеда Т., Гион Ю., Ёсино Т., Сато Ю. (2019). «Обзор EBV-положительных слизисто-кожных язв с акцентом на клинические и патологические аспекты» . Журнал клинической и экспериментальной гематопатологии . 59 (2): 64–71. дои : 10.3960/jslrt.18039 . ПМК 6661964 . ПМИД 31257347 .
- ^ Jump up to: а б Гудлад-младший (июнь 2017 г.). «Лимфопролиферативные заболевания кожи, связанные с вирусом Эпштейна-Барр». Клиники хирургической патологии . 10 (2): 429–453. дои : 10.1016/j.path.2017.01.001 . ПМИД 28477890 .
- ^ Дойчинов С.Д., Фенд Ф., Кинтанилья-Мартинес Л. (март 2018 г.). «EBV-положительная лимфопролиферация производных B-T- и NK-клеток у хозяев без ослабленного иммунитета» . Патогены (Базель, Швейцария) . 7 (1): 28. doi : 10.3390/pathogens7010028 . ПМК 5874754 . ПМИД 29518976 .
Источники
[ редактировать ]- Свердлов С.Х., Кампо Э., Яффе Е.С., Пилери С.А., ред. (2008). Классификация ВОЗ опухолей кроветворной и лимфоидной тканей . Лион: МАИР. ISBN 978-92-832-2431-0 .
- Гольдман Л., Шафер А.И. (2012). Cecil Medicine от Goldman (24-е изд.). ISBN 978-1-4377-1604-7 .
- Турджен М.Л. (2005). Клиническая гематология: теория и методика . Хагерстаун, Мэриленд: Липпинкотт Уильямс и Уилкинс. ISBN 978-0-7817-5007-3 .