Фторид водорода
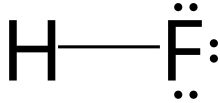
| |||
| |||
| Имена | |||
|---|---|---|---|
| Другие имена
Флуор
| |||
| Идентификаторы | |||
3D model ( JSmol )
|
|||
| Чеби | |||
| Chemspider | |||
| Echa Infocard | 100.028.759 | ||
| Кегг | |||
PubChem CID
|
|||
| Rtecs номер |
| ||
| НЕКОТОРЫЙ | |||
| Номер | 1052 | ||
Comptox Dashboard ( EPA )
|
|||
| Характеристики | |||
| Hf | |||
| Молярная масса | 20.006 g·mol −1 | ||
| Появление | бесцветный газ или бесцветная жидкость (ниже 19,5 ° C) | ||
| Запах | неприятный | ||
| Плотность | 1,15 г/л, газ (25 ° C) 0,99 г/мл, жидкость (19,5 ° C) 1,663 г/мл, твердое вещество (–125 ° C) | ||
| Точка плавления | −83,6 ° C (-118,5 ° F; 189,6 К) | ||
| Точка кипения | 19,5 ° C (67,1 ° F; 292,6 K) | ||
| смешиваемое (жидкость) | |||
| Давление паров | 783 мм рт. Ст. (20 ° C) [ 1 ] | ||
| Кислотность (p k a ) | 3.17 (в воде),
15 (в ДМСО) [ 2 ] | ||
| Сопряженная кислота | Флуороний | ||
| Сопряженная база | Фторид | ||
Показатель преломления ( N D )
|
1.00001 | ||
| Структура | |||
| Линейный | |||
| 1,86 г | |||
| Термохимия | |||
Std Molar
энтропия ( с ⦵ 298 ) |
8.687 J/g K (газ) | ||
Энтальпия STD
образование (Δ f h ⦵ 298 ) |
−13,66 кДж/г (газ) −14,99 кДж/г (жидкость) | ||
| Опасности | |||
| Безопасность и гигиена труда (OHS/OSH): | |||
Основные опасности
|
Высокотоксичный, коррозийный, раздражающий | ||
| GHS Маркировка : | |||
  
| |||
| Опасность | |||
| H300+H310+H330 , H314 | |||
| P260 , P262 , P264 , P270 , P271 , P280 , P284 , P301+P310 , P301+P330+P331 , P302 +P350 , P303+P361+P353 , P304+P340 , P305+P351+P338 , P310 , P320, P320, P320, P320, P320, P320, P320, P320, P320 , P320 , стр. P322 , P330 , P361 , P363 , P403+P233 , P405 , P501 | |||
| NFPA 704 (Огненная бриллиант) | |||
| точка возгорания | никто | ||
| Смертельная доза или концентрация (LD, LC): | |||
Ld 50 ( средняя доза )
|
17 ч / млн (крыса, устное) | ||
LC 50 ( медианная концентрация )
|
1276 м.д. (крыса, 1 час) 1774 ч / млн (обезьяна, 1 час) 4327 м.д. (морская свинка, 15 мин) [ 3 ] | ||
LC LO ( самый низкий опубликован )
|
313 ч / млн (кролик, 7 часов) [ 3 ] | ||
| Niosh (пределы воздействия на здоровье США): | |||
Пел (допустимый)
|
TWA 3 PPM [ 1 ] | ||
Rel (рекомендуется)
|
TWA 3 PPM (2,5 мг/м 3 ) C 6 ч/млн (5 мг/м 3 ) [15 минут] [ 1 ] | ||
IDLH (немедленная опасность)
|
30 ч / млн [ 1 ] | ||
| Связанные соединения | |||
Другие анионы
|
Хлорид водорода Водород Бромид Йодид водорода Водород астатид | ||
Другие катионы
|
Фторид натрия Калиевый фторид Фторид рубидиума Цезий фторид | ||
Связанные соединения
|
Вода Аммиак | ||
За исключением случаев, когда отмечены, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа).
| |||
Фторид водорода (флуор) является неорганическим соединением с химической формулой H f . Это очень ядовитый, бесцветный газ или жидкость, которая растворяется в воде, чтобы получить водный раствор, называемый гидрофторической кислотой . Он является основным промышленным источником фтора , часто в форме гидрофлуорической кислоты, и является важным сырью при приготовлении многих важных соединений, включая фармацевтические препараты и полимеры , EG политетрафторээтилен (PTFE). HF также широко используется в нефтехимической промышленности в качестве компонента супероидов . Из -за сильной и обширной водородной связи он кипит при почти комнатной температуре, намного выше, чем у других галогенидов водорода .
Фторид водорода является чрезвычайно опасным газом, образующим коррозию и проникающую гидрофторическую кислоту при контакте с влажностью . Газ также может вызвать слепоту путем быстрого разрушения роговицы .
История
[ редактировать ]В 1771 году Карл Вильгельм Шеле приготовил водный раствор, гидрофлуорическую кислоту была известна гидрофлуорическая кислота в больших количествах, хотя в стеклянной промышленности . Французский химик Эдмонду Фреми (1814–1894) приписывают обнаружение фторида водорода (HF) при попытке изолировать фторин .
Структура и реакции
[ редактировать ]
HF диатомный в газовой фазе. Как жидкость, HF образует относительно сильные водородные связи , следовательно, его относительно высокая температура кипения. Твердый HF состоит из зигзагообразных цепей молекул HF. Молекулы HF с короткой ковалентной связью H - F длиной 95 вечера связаны с соседними молекулами межмолекулярными расстояниями H - F 155 ч. [ 4 ] Жидкий HF также состоит из цепей молекул HF, но цепи короче, состоящие в среднем только пять или шесть молекул. [ 5 ]
Сравнение с другими галогенами водорода
[ редактировать ]Фторид водорода не кипит до 20 ° C в отличие от более тяжелых галогенидов водорода, которые кипят между -85 ° C (-120 ° F) и -35 ° C (-30 ° F). [ 6 ] [ 7 ] [ 8 ] Эта водородная связь между молекулами HF приводит к высокой вязкости в жидкой фазе и ниже ожидаемого давления в газовой фазе.
Водные решения
[ редактировать ]HF недоступен с водой (растворяется в любой пропорции). Напротив, другие галогениды водорода демонстрируют ограничивающие растворимость в воде. Фторид водорода образует моногидратный HF . H 2 O с температурой плавления -40 ° C (-40 ° F), которая составляет 44 ° C (79 ° F) выше температуры плавления чистого HF. [ 9 ]
| HF и H 2 O сходства | |

|

|
| Точки кипения галогенидов водорода (синий) и водородных халкогенидов HF и H 2 (красный): тенденции O. | Точка замерзания смесей HF/ H 2 O: стрелки указывают соединения в твердом состоянии. |
Водные растворы HF называются гидрофторической кислотой . При разбавлении гидрофлуорическая кислота ведет себя как слабая кислота, в отличие от других гидрогальных кислот, из-за образования ионных паров , связанных с водородом [ H 3 o + · F − ] Однако концентрированные растворы представляют собой сильные кислоты, потому что бифторидные преобладают анионы, а не ионные пар. При жидком безводном HF самоонизация : происходит [ 10 ] [ 11 ]
- 3 HF ⇌ H 2 F + + Hf - 2
которая образует чрезвычайно кислую жидкость ( H 0 = -15.1 ).
Реакции с кислотами Льюиса
[ редактировать ]Как и вода, HF может действовать как слабое основание, реагируя с кислотами Льюиса , чтобы дать супецид . Функция кислотности Хамметт ( H 0 ) -21 получена с помощью сурьмы пентафторида (SBF 5 ), образуя фторантоновую кислоту . [ 12 ] [ 13 ]
Производство
[ редактировать ]Фторид водорода обычно продуцируется реакцией между серной кислотой и чистыми классами минерального флуорита : [ 14 ]
- CAF 2 + H 2 SO 4 → 2 HF + CASO 4
Около 20% промышленного HF является побочным продуктом производства удобрений, который генерирует гексафторосилическую кислоту . Эту кислоту можно ухудшить для высвобождения HF термически и гидролизом:
- H 2 SIF 6 → 2 HF + SIF 4
- SIF 4 + 2 H 2 O → 4 HF + SIO 2
Использовать
[ редактировать ]В целом, безводный фторид водорода более распространен в промышленности, чем его водный раствор, гидрофторическая кислота . Основное использование, на тоннаже, является предшественником органических соединений и предшественника криолита для электролиза алюминия. [ 14 ]
Предшественник органофлюориновых соединений
[ редактировать ]HF реагирует с хлорокубенными, чтобы дать фторуглероды. Важным применением этой реакции является производство тетрафторэтилена (TFE), предшественника тефлона . Хлороформ фторирован HF для получения хлордифторметана (R-22): [ 14 ]
- CHCL 3 + 2 HF → CHCLF 2 + 2 HCL
Пиролиз хлордифторметана (при 550-750 ° C) дает TFE.
HF является реактивным растворителем в электрохимическом фторировании органических соединений. При таком подходе HF окисляется в присутствии углеводорода , а фторин заменяет связи C - H на связи C - F. перфторированные карбоновые кислоты и сульфоновые кислоты . Таким образом, [ 15 ]
1,1-дифторуэтан производится путем добавления HF в ацетилен с использованием ртути в качестве катализатора. [ 15 ]
- Hc≡CH + 2 Hf → CH 3 CHF 2
Промежуточным соединением в этом процессе является виниловый фторид или фторэтилен, мономерный предшественник поливинил фторида .
Предшественник металлических фторидов и фтора
[ редактировать ]Электровининг алюминия опирается на электролиз алюминиевого фторида у расплавленного криолита. Несколько килограммов HF потребляются на тонну производимого AL. Другие металлические фториды вырабатываются с использованием HF, включая тетрафлюрид урана . [ 14 ]
HF является предшественником элементарного фтора , F 2 путем электролиза раствора HF и бифлуорида калия . Требуется бифлюорид калия, потому что безводная СН не проводит электричество. Несколько тысяч тонн F 2 производятся ежегодно. [ 16 ]
Катализатор
[ редактировать ]HF служит катализатором в процессах алкилирования на нефтеперерабатывающих заводах. Он используется в большинстве установленных линейных производственных объектов алкилбензола в мире. Процесс включает в себя дегидрирование N -параффинов на олефины и последующую реакцию с бензолом с использованием HF в качестве катализатора. Например, в нефтеперерабатывающих заводах «алкилат», компонент высококтанового бензина ( бензин ), генерируется в алкилиционных единицах, которые объединяют C 3 и C 4 Olefins и ISO -Бутан . [ 14 ]
Растворитель
[ редактировать ]Фторид водорода является отличным растворителем. Отражая способность HF участвовать в водородной связи, даже белки и углеводы растворяются в HF и могут быть извлечены из нее. Напротив, большинство неорганических химических веществ не фторида реагируют с HF, а не растворяются. [ 17 ]
Последствия для здоровья
[ редактировать ]
Фторид водорода очень коррозий и мощный контактный яд. Воздействие требует немедленной медицинской помощи. [ 18 ] Это может вызвать слепоту путем быстрого разрушения роговицы . Вдыхание фторида водорода на высоких уровнях или в сочетании с контактом кожи может вызвать смерть от нерегулярного сердцебиения или от отека легких (накопление жидкости в легких). [ 18 ]
Ссылки
[ редактировать ]- ^ Jump up to: а беременный в дюймовый Niosh Pocket Guide к химическим опасностям. "#0334" . Национальный институт безопасности и гигиены труда (NIOSH).
- ^ Эванс, да "ПКА неорганических и оксокидов" (PDF) . Получено 19 июня 2020 года .
- ^ Jump up to: а беременный «Фторид водорода» . Немедленно опасно для жизни или концентрации в области здоровья (IDLH) . Национальный институт безопасности и гигиены труда (NIOSH).
- ^ Джонсон, MW; Sándor, E.; Арзи Э. (1975). «Кристаллическая структура фторида детериума». Crystalliphica Acta . B31 (8): 1998–2003. Doi : 10.1107/s0567740875006711 .
- ^ McLain, Sylvia E.; Бенмор, CJ; Размер, когда -либо; Urquidi, j .; Тернер, JF (2004). «О структуре жидкого водорода фторида». Ingraded Chemistry International Edition . 43 (15): 1952-55. DOO : 10.1002 / anie.200353289 . PMID 15065271 .
- ^ Полинг, Линус А. (1960). Природа химической связи и структура молекул и кристаллов: введение в современную структурную химию . Издательство Корнелльского университета. С. 454 –464. ISBN 978-0-8014-0333-0 .
- ^ Аткинс, Питер; Джонс, Лоретта (2008). Химические принципы: стремление к пониманию . WH Freeman & Co. с. 184–185. ISBN 978-1097774678 .
- ^ Эмсли, Джон (1981). «Скрытая сила водорода» . Новый ученый . 91 (1264): 291–292. Архивировано из оригинала 22 июля 2023 года . Получено 25 декабря 2012 года .
- ^ Гринвуд, NN; Эрншоу А. (1998). Химия элементов (2 -е изд.). Оксфорд: Баттерворт Хейнеманн. С. 812–816. ISBN 0-7506-3365-4 .
- ^ C. E. Housecroft и A. G. Sharpe неорганическая химия , с. 221
- ^ F. A. Cotton и G. Wilkinson Advanced Inorganic Chemistry , p. 111.
- ^ W. L. Jolly "Modern неорганическая химия" (McGraw-Hill 1984), с. 203. ISBN 0-07-032768-8 .
- ^ FA Cotton и G. Wilkinson, Advanced неорганическая химия (5 -е изд.) Джон Вили и сыновья: Нью -Йорк, 1988. ISBN 0-471-84997-9 . п. 109
- ^ Jump up to: а беременный в дюймовый и J. Aiuerse, P. Mollarard, D. Devilliers, R. Chemla, R. Неорганический. Энциклопедия Вейнхайм: Wiley-VCH doi : 10.1002/ 14366007.a11_ ISBN 3527306730 .
{{cite encyclopedia}}: Cs1 maint: несколько имен: список авторов ( ссылка ) - ^ Jump up to: а беременный G. Siegemund, W. Schwertfeger, A. Feering, B. Smart, F. Behr, H. Vogel, B. McKusick (2005). «Фториновые соединения, органические». Энциклопедия промышленной химии Уллмана . Вейнхайм: Wiley-VCH. Doi : 10.1002/14356007.a11_349 . ISBN 978-3527306732 .
{{cite encyclopedia}}: Cs1 maint: несколько имен: список авторов ( ссылка ) - ^ М. Джако, Р. Фарон, Д. Девиллиерс, Р. Роман (2005). "Фтор" Энциклопедия Вейнхайм: Wiley-VCH doi : 10.1002/ 1436000 ISBN 978-3527306732 .
{{cite encyclopedia}}: Cs1 maint: несколько имен: список авторов ( ссылка ) . - ^ Гринвуд и Эрншоу, «Химия элементов», с. 816–819.
- ^ Jump up to: а беременный Факты о фториде водорода (гидрофлуорическая кислота)
Внешние ссылки
[ редактировать ]- Фториды, фторид водорода и фтор при ATSDR . Получено 30 сентября 2019 г.
- CDC - Pocket Guide niosh к химической опасности
- Информационный бюллетень водорода [ мертвая ссылка ] в Институте сокращения использования токсиков



