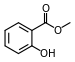
Эфир
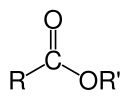
В химии эфир полученную представляет собой функциональную группу, из кислоты (органической или неорганической), в которой атом водорода (H) по крайней мере одной кислой гидроксильной группы ( -OH ) этой кислоты заменяется органической группой (r ′ ). Аналоги, полученные из кислорода , замененные другими халкогенами, также относятся к категории сложных эфиров. [ 1 ] По мнению некоторых авторов, органические производные кислого водорода других кислот также являются сложными эфирами (например, амиды ), но не в соответствии с IUPAC . [ 1 ]
Глицериды представляют собой эфиры жирных кислот глицерина сложные ; Они важны в биологии, являются одним из основных классов липидов и содержат основную часть животных жиров и растительных масел . Лактоны - это циклические карбоновые эфиры; Природные лактоны в основном являются 5- и 6-членными кольцевыми лактонами. Лактоны способствуют аромату фруктов, масла, сыра, овощей , таких как сельдерей и другие продукты.
Эфиры могут образовываться из оксоцидов (например, эфиры уксусной кислоты , углекислота , серной кислоты , фосфорной кислоты , азотной кислоты , ксантоической кислоты ), но также из кислот, которые не содержат кислорода (например, эфир тиоциановой кислоты и тритиокарбонической кислоты ). Примером образования сложного эфира является реакция замещения между карбоновой кислотой ( R - C (= O) −OH ) и алкоголь ( R' -Oh ), образуя эфир ( R - C (= O) -O -R ' ), где R обозначает любую группу (обычно водород или организм), а R ' обозначает органирующую группу.
Органиловые эфиры карбоновых кислот обычно имеют приятный запах; Те, кто низкомолекулярно, обычно используются в качестве ароматов и встречаются в эфирных маслах и феромонах . Они работают в качестве высококлассных растворителей для широкого спектра пластмассы , пластификаторов , смол и лаков , [ 2 ] и являются одним из крупнейших классов синтетических смазок на коммерческом рынке. [ 3 ] Полиэфиры являются важными пластмассами, с мономерами, связанными эфирными фрагментами . Эфиры фосфорной кислоты образуют основную цепь молекул ДНК . Эфиры азотной кислоты , такие как нитроглицерин , известны своими взрывными свойствами.
Существуют соединения, в которых кислотный водород кислот, упомянутых в этой статье, не заменяется организом, а какой -то другой группой. По мнению некоторых авторов, эти соединения также являются сложными эфирами, особенно когда первый атом углерода органической группы, заменяющий кислотный водород, заменяется другим атом из элементов группы 14 ( Si , Ge , SN , PB ); Например, в соответствии с ними, триметилстанилацетат (или ацетат триметилтина) CH 3 COOSN (CH 3 ) 3 - триметилстаниловый эфир уксусной кислоты , а дибутилтин дилаврат (CH 3 (Ch 2 ) 10 COO) 2 SN ((CH 2 ) 3 CH 3 ) 2 - дибутилстанилена эфир лауриновой кислоты , а Phillips катализатор Phillips CRO 2 (OSI (OCH 3 ) 3 ) 2 - это триметоксисилильный сложный эфир хромовой кислоты ( H 2 Cro 4 ). [ 4 ] [ 5 ]
Номенклатура
[ редактировать ]Этимология
[ редактировать ]Слово эфир было придуман в 1848 году немецким химиком Леопольдом Гмелин , [ 6 ] Вероятно, как сокращение немецкого Essigäther , « Укесенный эфир ».
IUPAC NOMENCLATURE
[ редактировать ]Названия эфиров, которые образуются из спирта и кислоты, получены из родительского спирта и родительской кислоты, где последняя может быть органическим или неорганическим. Эфиры, полученные из самых простых карбоновых кислот , обычно названы в соответствии с более традиционными, так называемыми « тривиальными именами », например, как формиата, ацетата, пропионата и бутирата, в отличие от метаноата IUPAC, этаноата, пропаноата и бутаноата. Эфиры, полученные из более сложных карбоновых кислот, с другой стороны, чаще называются с использованием систематического имени IUPAC, основываясь на названии кислоты, за которой следует суффикс -оат . Например, эфир гексиль -октаноат, также известный под тривиальным именем hexyl caprylate , имеет формулу Ch 3 (Ch 2 ) 6 CO 2 (Ch 2 ) 5 Ch 3 .

Химические формулы органических эфиров, образованных из карбоновых кислот и спиртов, обычно принимают форму RCO 2 R ' или RCOOR', где R и R 'являются органическими частями карбоновой кислоты и спирта, соответственно, и R могут быть водородом в случае сложных эфиров муравьиной кислоты . Например, бутилацетат (систематически бутилотаноат), полученный из бутанола и уксусной кислоты (систематически этановая кислота) будет написана CH 3 CO 2 (Ch 2 ) 3 Ch 3 . Альтернативные презентации распространены, включая Buoac и CH 3 CO (Ch 2 ) 3 Ch 3 .
Циклические эфиры называются лактонами , независимо от того, являются ли они из органической или неорганической кислоты. Одним из примеров органического лактона является γ-валеролактон .
Ортоэфиры
[ редактировать ]Необычный класс сложных эфиров - ортоэфиры . Одним из них являются сложные эфиры ортокарбоновых кислот. У этих эфиров есть формула RC (или ′) 3 , где R обозначает любую группу (органическую или неорганическую), а R ' обозначает органическую группу. Например, триэтилортоформат ( HC (OCH 2 CH 3 ) 3 ) получен с точки зрения его названия (но не его синтеза) из этерификации ортоформической кислоты ( HC (OH) 3 ) с этанолом .
Эфиры неорганических кислот
[ редактировать ]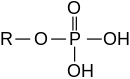
Эфиры также могут быть получены из неорганических кислот.
- Перхловая кислота образует эфиры перхлората , например, метил перхлорат ( CH 3 -O - Cl (= O) 3 )
- Серная кислота образует сульфатные эфиры , например, диметилсульфат ( (Ch 3 -O-) 2 S (= O) 2 ) и метил бисульфат ( CH 3 -O - (= O) 2 -Oh )
- Азотная кислота образует эфиры нитратов , например, метил -нитрат ( CH 3 -O -NO 2 ) и нитроглицерин ( CH (-O -NO 2 ) ( - CH 2 -O -NO 2 ) 2 )
- Фосфорная кислота образует фосфатные эфиры , например , трифенилфосфат ( O = P (-O -C 6 H 5 ) 3 ) и метилдигидрофосфат ( O = P ( - -Ch 3 ) ( - - OH) 2 )
- Пирофосфорная образует пирофосфатные эфиры тетраэтилпирофосфат , ADP , DADP , ADPR , CADPR , CDP , DCDP , GDP , DGDP Mecp DTDP , ) , например ( , , дифхосфорная кислотная UDP кислота , , NAD , NADP .
- Трихосфорная кислота образует трифосфатные эфиры, например , ATP , DATP , CTP , DCTP , GTP , DGTP , UTP , DTTP , ITP , XTP , THTP , Athtp .
- Углекислота образует карбонатные сложные эфиры , например, диметилбонат ( (CH 3 -O-) 2 C = O ) и 5-участник циклического этилен-карбоната ( (−ch 2 -o-) 2 c = O ) (если один классифицирует углекислоту как неорганическое соединение)
- Тритиокарбоновая кислота образует тритиокарбонатные эфиры , например, диметилритиокарбонат ( (Ch 3 −S-) 2 C = S ) (если один классифицирует тритиокарбоновую кислоту как неорганическое соединение)
- Хлороформическая кислота образует хлороформатные сложные эфиры, например, метилхлороформа ( CL - C (= O) -O -CH 3 ) (если один классифицирует хлороформическую кислоту как неорганическое соединение)
- Борная кислота образует борат эфиры , например, триметил борат ( B ( --Sch 3 ) 3 )
- Хромовая кислота диперт -бутиловый ( хромат образует ((D 3 ) 3 C -O - 2 Cr (= O) 2 )
Неорганические кислоты, которые существуют в качестве таутомеров, образуют два или более типов сложных эфиров.
- Тиозольфурическая кислота образует два типа эфиров тиосульфата , например O , ( -диметил тиосульфат (CH 3 -O-) 2 S (= O) (= S) ) и O , S -диметил тиосульфат ( (Ch 3 -O -) (Ch 3 −S-) s (= O) 2 )
- Тиоциановая кислота образует эфиры тиоцианата , например, метилтиоцианат ( CH 3 -S -C≡N ) (если кто -то классифицирует тиоциановую кислоту как неорганическое соединение), но образует изотиоцианат также «сложные эфиры», например, метил изотиоцианат ( CH 3 -n = C = S ), хотя органические изотиоцианаты не классифицируются как эфиры IUPAC
- Фосфорная кислота образует два типа сложных эфиров: фосфитные эфиры , например, триэтилофосфит ( P (-O -ch 2 ch 3 ) 3 ) и фосфонатные эфиры , например, диэтилфосфонат ( H - P (= O) ( - O - ch 2 ch 3 ) 2 )
Некоторые неорганические кислоты, которые являются нестабильными или неуловимыми стабильными эфирами.
- Серная кислота , которая нестабильна, образует стабильный диметилсульфит ( (Ch 3 -S -) 2 S = O )
- Дикарбоновая кислота , которая является нестабильной, образует стабильный диметилдикарбонат ( CH 3 -O - C (= O) −o - c (= O) −o - ch 3 )
В принципе, часть металлоидных алкоксидов , из которых известны многие сотни, можно было бы классифицировать как сложные эфиры соответствующих кислот (например, алюминиевый триэтоксид ( Al (OCH 2 CH 3 ) 3 ) может быть классифицирован как сложный эфир алюминовой кислоты, которая представляет собой гидроксид алюминия , тетраэтил -ортосиликат ( Si (OCH 2 CH 3 ) 4 ) может быть классифицирован как сложный эфир ортосилической кислоты и титанового оксида ( Ti (OCH 2 CH 3 ) 4 ) может быть классифицирован как сложный эфир ортотитановой кислоты ).
Структура и связь
[ редактировать ]Эфиры, полученные из карбоновых кислот и спиртов, содержат карбонильную группу C = O, которая является двухвалентной группой при атом C , которая приводит к увеличению 120 ° C - C - O и O - C - O. В отличие от амидов , эфиры карбоновой кислоты являются структурно гибкими функциональными группами, потому что вращение вокруг связей C -O -C имеет низкий барьер. Их гибкость и низкая полярность проявляются в их физических свойствах; Они имеют тенденцию быть менее жесткими (более низкая температура плавления) и более летучими (более низкая точка кипения), чем соответствующие амиды . [ 7 ] P карбонильной k a альфа-гидрогенов на сложных эфирах карбоновых кислот составляет около 25 (альфа-гидроген представляет собой водород, связанный с углеродом, прилегающим к группе (C = O) эфиров карбоксилат). [ 8 ]
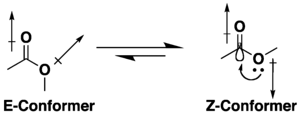
Многие эфиры карбоновой кислоты имеют потенциал для конформационной изомерии , но они, как правило, применяют конформацию S - CI (или Z ), а не альтернативу S - Trans (или E ) из -за комбинации дипольной минимизации гиперконъюгации и эффектов . На предпочтение конформации Z влияет природа заместителей и растворителя, если они присутствуют. [ 9 ] [ 10 ] Лактоны с небольшими кольцами ограничены конформацией S -Trans (т. Е. E ) из -за их циклической структуры.

Физические свойства и характеристика
[ редактировать ]Эфиры, полученные из карбоновых кислот и спиртов, являются более полярными, чем эфиры , но менее полярные, чем спирты. Они участвуют в водородных связях в качестве акцепторов водородных связей, но не могут выступать в качестве доноров водородных связей, в отличие от их родительских спиртов. Эта способность участвовать в водородной связи обеспечивает некоторую воду. Из-за отсутствия способности к водородным связям, сложные эфиры не самостоятельно не ассоциируются. Следовательно, сложные эфиры являются более летучими, чем карбоновые кислоты сходной молекулярной массы. [ 7 ]
Характеристика и анализ
[ редактировать ]Эфиры обычно идентифицируются по газовой хроматографии, используя их волатильность. ИК -спектры для эфиров имеют интенсивную острую полосу в диапазоне 1730–1750 см. −1 назначено ν c = o . Этот пик меняется в зависимости от функциональных групп, прикрепленных к карбонилу. Например, бензоловое кольцо или двойная связь в сочетании с карбонилом снизит волновое число около 30 см. −1 .
Приложения и появление
[ редактировать ]Эфиры широко распространены по своей природе и широко используются в промышленности. В природе жиры , как правило, являются триестами, полученными из глицерина и жирных кислот . [ 12 ] Эфиры несут ответственность за аромат многих фруктов, включая яблоки , дурицы , груши , бананы , ананасы и клубника . [ 13 ] Несколько миллиардов килограммов полиэфиров производится в промышленности ежегодно, важными продуктами являются полиэтилентерефталат , акрилатные эфиры и ацетат целлюлозы . [ 14 ]
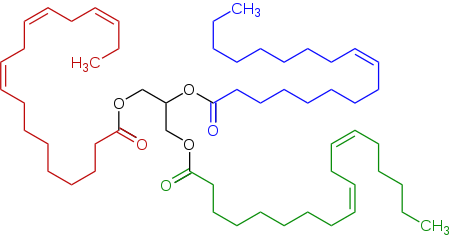
Репрезентативный триглицерид, обнаруженный в льняном масле, триэстер глицерина (центра, черный), полученный из линолевой кислоты (нижний справа, зеленый), альфалиноленовой кислоты (слева, красная) и олеиновая кислота (сверху вверху, синий).
Подготовка
[ редактировать ]Этерификация является общим названием для химической реакции , в которой два реагента (обычно спирт и кислота) образуют эфир в качестве продукта реакции . Эфиры распространены в органической химии и биологических материалах и часто имеют приятный характерный, фруктовый запах. Это приводит к их широкому использованию в ароматизационной и ароматической индустрии. Эфирные связи также встречаются во многих полимерах .
Этерификация карбоновых кислот с спиртами
[ редактировать ]Классическим синтезом является этерификация фишера , которая включает в себя лечение карбоновой кислоты с помощью спирта в присутствии обезвоживающего агента:
- RCO 2 H + R'OH ⇌ RCO 2 R ' + H 2 O
Константа равновесия для таких реакций составляет около 5 для типичных сложных эфиров, например, этилацетат. [ 15 ] Реакция медленно в отсутствие катализатора. Серная кислота является типичным катализатором для этой реакции. Также используются многие другие кислоты, такие как полимерные сульфоновые кислоты . Поскольку этерификация очень обратима, урожайность эфира может быть улучшена с помощью принципа Le Chatelier :
- Использование алкоголя в большом избытке (т.е. в качестве растворителя).
- Использование обезвоживающего агента: серная кислота не только катализирует реакцию, но и секвестирует воду (продукт реакции). Другие сушильные агенты, такие как молекулярные сита, также эффективны.
- Удаление воды физическими средствами, такими как дистилляция с низким содержанием куковления в качестве азеотропа с толуолом , в сочетании с аппаратом-декан-звездой .
Известно, что реагенты стимулируют обезвоживание смесей спиртов и карбоновых кислот. Одним из примеров является этерификация Steglich , которая является методом формирования сложных эфиров в мягких условиях. Метод популярен в синтезе пептидов , где субстраты чувствительны к суровым условиям, таким как высокая температура. DCC ( dicyclogexyxylcarbodiimide ) используется для активации карбоновой кислоты для дальнейшей реакции. 4-диметиламинопиридин (DMAP) используется в качестве катализатора ацил-переноса . [ 16 ]
Другим методом обезвоживания смесей спиртов и карбоновых кислот является реакция Mitsunobu :
- RCO 2 H + R'OH + P (C 6 H 5 ) 3 + R 2 N 2 → RCO 2 R ' + OP (C 6 H 5 ) 3 + R 2 N 2 H 2
Карбоновые кислоты могут быть этерифицированы с использованием диазометана :
- RCO 2 H + CH 2 N 2 → RCO 2 CH 3 + N 2
Используя этот диазометан, смеси карбоновых кислот могут быть преобразованы в их метиловые эфиры в почти количественных выходах, например, для анализа с помощью газовой хроматографии . Метод полезен в специализированных органических синтетических операциях, но считается слишком опасным и дорогим для крупномасштабных применений.
Этерификация карбоновых кислот с эпоксидами
[ редактировать ]Карбоновые кислоты этерифицируются путем обработки эпоксидами , давая β-гидроксисторы:
- RCO 2 H + RCHCH 2 O → RCO 2 CH 2 CH (OH) R
Эта реакция используется в производстве виниловой эфирной смолы из акриловой кислоты .
Алкоголь ацилхлоридов и кислотных ангидридов
[ редактировать ]Спирты реагируют с ацилхлоридами и кислотными ангидридами с получением сложных эфиров:
- Rcocl + r'oh → rco 2 r ' + hcl
- (RCO) 2 O + R'OH → RCO 2 R ' + RCO 2 H
Реакции-необратимая упрощающая работа . Поскольку ацилхлориды и кислотные ангидриды также реагируют с водой, предпочтительны безводные условия. Аналогичные ацилирования аминов с получением амидов менее чувствительны, поскольку амины являются более сильными нуклеофилами и реагируют быстрее, чем вода. Этот метод используется только для лабораторных процедур, так как он дорого.
Алкилирование карбоновых кислот и их солей
[ редактировать ]Теттрафлюороборат триметилоксоний может использоваться для этерификации карбоновых кислот в условиях, где кислотные катализируемые реакции невозможно: [ 17 ]
- RCO 2 H + (Ch 3 ) 3 OBF 4 → RCO 2 CH 3 + (Ch 3 ) 2 O + HBF 4
Несмотря на то, что редко используются для эмификаций, карбоксилатные соли (часто генерируемые in situ ) реагируют с электрофильными алкилирующими агентами , такими как алкил галогенид , с получением сложных эфиров. [ 14 ] [ 18 ] Доступность анионов может ингибировать эту реакцию, которая соответственно выигрывает от катализаторов фазового переноса или таких высокополярных аплодистских растворителей, как DMF . Дополнительная йодидная соль может, через реакцию Финкельштейна , катализировать реакцию непокорного алкилгалогенида. Альтернативно, соли координирующего металла, такого как серебро, могут улучшить скорость реакции за счет облегчения устранения галогенидов.
Переэтерификация
[ редактировать ]Трансэтерификация , которая включает в себя изменение одного эфира в другой, широко практикуется:
- RCO 2 R ' + CH 3 OH → RCO 2 CH 3 + R'OH
Как и гидролизация, переэтерификация катализируется кислотами и основаниями. Реакция широко используется для разложения триглицеридов , например, в производстве сложных эфиров и спиртов жирных кислот. Поли (этилентерефталат) продуцируется путем переэтерификации диметилтерефталата и этиленгликоля: [ 14 ]
- N (C 6 H 4 ) (CO 2 CH 3 ) 2 + 2 N C 2 H 4 (OH) 2 → ((C 6 H 4 ) (CO 2 ) 2 (C 2 H 4 )] N + 2 N CH 3 Ох
Подгруппой переэтерификации является алкоголь дикетена . Эта реакция дает 2-кетоэфиры. [ 14 ]
- (CH 2 CO) 2 + ROH → CH 3 C (O) CH 2 CO 2 R
Карбонилирование
[ редактировать ]Алкены подвергаются углеводу в присутствии металлических карбонильных катализаторов. Эфирные эфиры пропановой кислоты производится в коммерческом виде этим методом:
- H 2 C = CH 2 + ROH + CO → CH 3 CH 2 CO 2 R
Приготовление метилового пропионата является одним из иллюстративных примеров.
- H 2 C = CH 2 + CO + CH 3 OH → CH 3 CH 2 CO 2 CH 3
Карбонилирование метанола дает формиат метила , который является основным коммерческим источником муравьиной кислоты . Реакция катализируется метоксидом натрия :
- CH 3 OH + CO → HCO 2 CH 3
Добавление карбоновых кислот в алкены и алкины
[ редактировать ]В гидротерификации алкены и алкины вставляют в O -H связь карбоновых кислот. Винилацетат производится в промышленности путем добавления уксусной кислоты к ацетилену в присутствии катализаторов цинка ацетата : [ 19 ]
- Hc≡CH + CH 3 CO 2 H → CH 3 CO 2 CH = CH 2
Винилацетат также может быть продуцирован с помощью катализируемой палладий реакции этилена, уксусной кислоты и кислорода :
- 2 H 2 C = CH 2 + 2 CH 3 CO 2 H + O 2 → 2 CH 3 CO 2 CH = CH 2 + 2 H 2 O
Силикотунгстическая кислота используется для изготовления этилацетата путем алкилирования уксусной кислоты этиленом:
- H 2 C = CH 2 + CH 3 CO 2 H → CH 3 CO 2 CH 2 CH 3
От альдегидов
[ редактировать ]Реакция Тишхенко включает в себя диспропорционирование альдегида . в присутствии безводного основания, чтобы получить сложный эфир Катализаторами являются алюминиевые алкоксиды или алкоксиды натрия. Бензальдегид реагирует с бензилоксидом натрия (генерируемый натрием и бензиловым спиртом ) на генерацию бензилбензоата . [ 20 ] Метод используется в производстве этилацетата из ацетальдегида . [ 14 ]
Другие методы
[ редактировать ]- присутствии Перегруппировка α-халокетонов в присутствии основания в
- Байер -Виллигер Окисление кетонов с пероксидами
- Пиннер -реакция нитрилов с спиртом
- Нуклеофильная абстракция металлического комплекса
- Гидролиз ортоэфиров в водной кислоте
- Целлюлолиз через этерификацию [ 21 ]
- Озонолиз алкенов и с использованием работы в присутствии соляной кислоты различных спиртов . [ 22 ]
- Анодное окисление метилкетонов , . приводящих к метиловым эфирам [ 23 ]
- Производительность обменивается групп жирных кислот разных эфиров.
Реакция
[ редактировать ]Эфиры менее реактивны, чем кислотные галогениды и ангидриды. Как и в случае с более реактивными ацильными производными, они могут реагировать с аммиаком и первичными и вторичными аминами с получением амидов, хотя этот тип реакции не часто используется, поскольку кислотные галогениды дают лучшие урожаи.
Переэтерификация
[ редактировать ]Эфиры могут быть преобразованы в другие сложные эфиры в процессе, известном как переэтерификация . Переэтерификация может быть катализирована кислотой или основанием и включает реакцию эфира с спиртом. К сожалению, поскольку уходная группа также является алкоголем, прямые и обратные реакции часто встречаются с одинаковыми скоростями. Использование большого избытка реактивного спирта или удаление уходного группы алкоголя (например, через дистилляцию ) будет стимулировать прямую реакцию на завершение в соответствии с принципом Le Chatelier . [ 24 ]
Гидролиз и омыление
[ редактировать ]Кислотно-катализируемый гидролиз сложных эфиров также является равновесным процессом-по сути, обратной реакцией эфирификации фишера . Поскольку алкоголь (который действует как оставшаяся группа) и вода (которая действует как нуклеофил) имеют одинаковые значения p a A , прямые и обратные реакции конкурируют друг с другом. Как при переэтерификации, использование большого избытка реагента (воды) или удаление одного из продуктов (спирт) может способствовать прямой реакции.
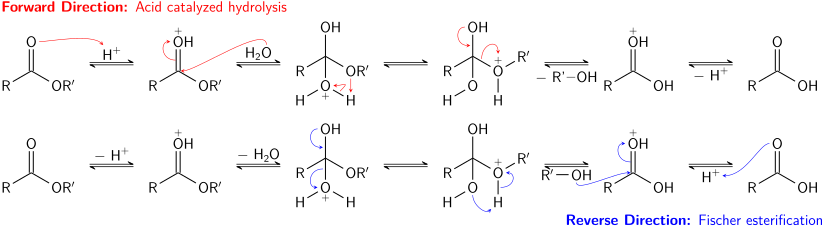
Основной гидролиз сложных эфиров, известный как опонирование , не является равновесным процессом; Полный эквивалент основания потребляется в реакции, которая производит один эквивалент спирта и один эквивалент карбоксилатной соли. Опонирование сложных эфиров жирных кислот является промышленно важным процессом, используемым при производстве мыла. [ 24 ]
Этерификация является обратимой реакцией. Эфиры подвергаются гидролизу в кислых и основных условиях. В кислых условиях реакция является обратной реакцией этерификации фишера . В основных условиях гидроксид действует как нуклеофил, в то время как алкоксид является уходной группой. Эта реакция, опонирование , является основой для изготовления мыла.
Алкоксидная группа также может быть смещена более сильными нуклеофилами, такими как аммиак или первичные или вторичные амины, давая амиды (реакция аммонолиза):
- Rco 2 r ' + nh 2 r ″ → rconhr ″ + r'oh
Эта реакция обычно не является обратимой. Гидразины и гидроксиламин могут использоваться вместо аминов. Эфиры могут быть преобразованы в изоцианаты посредством промежуточных гидроксамовых кислот в перестройке проигравшей .
Источники углеродных нуклеофилов, например, реагенты Grignard и органические соединения, легко добавляют карбонил.
Снижение
[ редактировать ]По сравнению с кетонами и альдегидами, сложные эфиры относительно устойчивы к снижению . Введение каталитического гидрирования в начале 20 -го века было прорывом; Эфиры жирных кислот являются гидрогенизированными до жировых спиртов .
- RCO 2 R ' + 2 H 2 → RCH 2 OH + R'OH
Типичным катализатором является медный хромит . До развития каталитического гидрирования эфиры были снижены в больших масштабах, используя снижение Bouveault -Blanc . Этот метод, который в значительной степени устарел, использует натрий в присутствии источников протонов.
Особенно для синтеза из тонкого химического вещества, гидрид алюминия лития используется для уменьшения эфиров до двух первичных спиртов. Связанный борогидрид натрия в реагенте медленно в этой реакции. Диба сводит эфиры в альдегиды. [ 25 ]
Прямое восстановление с получением соответствующего эфира затруднено, так как промежуточный гемиацетальный, как правило, разлагается с получением спирта и альдегида (который быстро снижается, чтобы дать второй алкоголь). Реакция может быть достигнута с использованием триэтилсилана с различными кислотами Льюиса. [ 26 ] [ 27 ]
Claisen Condensation и связанные с ними реакции
[ редактировать ]Эфиры могут подвергаться разнообразным реакциям с углеродными нуклеофилами. Они реагируют с избытком реагента Grignard, чтобы дать третичные спирты. Эфиры также легко реагируют на inolates . В конденсации CLAISEN енолят одного сложного ( 1 ) атакует карбонильную группу другого сложного эфира ( 2 ), чтобы дать тетраэдрический промежуточный 3 . Промежуточный падение, вынуждая алкоксид (r'o − ) и продуцируя β-кето-эфир 4 .

Скрещенные конденсации CLAISEN, в которых энолят и нуклеофил являются разными эфирами, также возможны. Внутримолекулярная или конденсация Claisen называется конденсацией Dieckmann циклизацией Dieckmann, поскольку ее можно использовать для формирования колец. Эфиры также могут подвергаться конденсациям с кетоновыми и альдегидными энолатами с получением β-дикарбонильных соединений. [ 28 ] Конкретным примером этого является перестройка пекаря -венкатарамана , в которой ароматический орто -ацидокси кетон подвергается интрамолекулярной нуклеофильной ацильной замене и последующей перестройке с образованием ароматического β -дикетона. [ 29 ] Перестановка Чана является еще одним примером перестройки, возникающей в результате внутримолекулярной реакции нуклеофильного замены ацила.
Другие эфирные реактивность
[ редактировать ]Эфиры реагируют с нуклеофилами в карбонильном углероде. Карбонил слабо электрофильный, но подвергается воздействию сильных нуклеофилов (амины, алкоксиды, источники гидридов, соединения организма и т. Д.). Связывание C - H, примыкающие к карбониле, слабо кислы, но подвергаются депротонированию сильным основанием. Этот процесс - тот, который обычно инициирует реакции конденсации. Карбонильный кислород в сложных эфирах слабо прост, что менее, чем карбонильный кислород в амидах из -за резонансного донорства электронной пары из азота в амидах, но образует аддукты .
Что касается альдегидов , атомы водорода на соседних углеродах («α к») карбоксильная группа в эфирах достаточно кисла для депротонирования, что, в свою очередь, приводит к различным полезным реакциям. Депротонирование требует относительно сильных оснований, таких как алкоксиды . Депротонирование дает нуклеофильный энулат , который может дополнительно реагировать, например, конденсация CLAISEN и его внутримолекулярный эквивалент, конденсация Dieckmann . Это преобразование используется в синтезе малонического эфира , в котором диэстер малоновой кислоты реагирует с помощью электрофила (например, алкилгалогенид ) и впоследствии декарбоксилируется. Другим вариантом является алкилирование Fráter -Seebach .
Другие реакции
[ редактировать ]В этом разделе нужны дополнительные цитаты для проверки . ( Сентябрь 2024 г. ) |
- Эфиры могут быть непосредственно преобразованы в нитрилы . [ 30 ] [ Необходимый источник необходимы ]]
- Метиловые эфиры часто подвержены декарбоксилированию в декарбоксилировании Krapcho .
- Фениловые эфиры реагируют на гидроксиарилкеты в перестройке фри .
- Специфические сложные эфиры функционируются с α-гидроксильной группой в перестройке Чана .
- Эфиры с атомами β-гидрогена могут быть преобразованы в алкены в эфирном пиролизе .
- Пары эфиров связаны для получения α-гидроксикетонов в конденсации ацилоина
Защита групп
[ редактировать ]Как класс, сложные эфиры служат защитой групп для карбоновых кислот . Защита карбоновой кислоты полезна при синтезе пептидов, чтобы предотвратить самооценку бифункциональных аминокислот . Метил и этиловые эфиры обычно доступны для многих аминокислот; Т -бутиловый эфир имеет тенденцию быть дороже. Тем не менее, Т -бутиловые эфиры особенно полезны, потому что в сильно кислых условиях Т -бутиловые эфиры подвергаются элиминации, чтобы получить карбоновую кислоту и изобутилен , упрощая работу.
Список эфирных одоранов
[ редактировать ]Многие сложные эфиры имеют отличительные фруктовые запахи, и многие встречаются естественным образом в эфирных маслах растений. Это также привело к их общему использованию в искусственных ароматизациях и ароматах, которые направлены на имитацию этих запахов.
Смотрите также
[ редактировать ]- Список сложных эфиров
- Амид
- Тиоамид
- Углексидат
- Карбамат
- Ксантат
- Амидина
- Цианат
- Тиоцианат
- Селеноцианат
- Теллуроцианат
- Полиэфир , пластмассы, изготовленные из полимерного эфира
- Олигоэфир , полимерный сложный эфир из небольшого числа эфирных мономеров
- Polyolester , сложный эфир, который является синтетическим маслом, используемым в охлажденных компрессорах
- Тиоэстер
- Переэтерификация
- Эфирный липид , эфир, который является липидом и эфиром
- Ацилальный (Р 1 −c (= o) −o -) (r 2 −c (= o) −o-) CH - R 3 )
- Орто -эфир , сложный эфир орто -кислоты (например, сложные эфиры ортокарбоновых кислот , ортокарбоновой кислоты , ортосилической кислоты , ортотеллуриновой кислоты , ортофосфорной кислоты , ортоборовой кислоты , ...)
- Depside , полимерный эфир, тип полифенольного соединения, состоящий из двух или более моноциклических ароматических единиц, связанных группой сложных эфиров
- Депсипептид , тип сложного эфира, который представляет собой пептид , в котором одна или несколько его амидных групп ( −c (= o) −nh- ) заменяются соответствующими группами эфиров ( −c (= o) −o- ) [ 31 ]
- Глицерид ( (Р 1 −c (= o) −o - ch 2 -) (r 2 −c (= o) −o - ch 2 -) (r 3 −c (= O) -O-) CH ), эфир жирных кислот и глицерина
- Лактон , циклический карбоновый эфир
- Лактид , тип эфира лактона
- Витамин С (аскорбиновая кислота), эфир лактона, незаменимое питательное вещество для людей и других животных
- Фталид , тип эфира лактона
- Кумарин , тип эфира лактона
- Макролид , класс естественных сложных эфиров, состоящих из большого макроциклического лактонового кольца, к которому один или несколько дезоксси сахара может быть прикреплен
- Форматы
- Хлороформат
Ссылки
[ редактировать ]- ^ Jump up to: а беременный IUPAC , сборник химической терминологии , 2 -е изд. («Золотая книга») (1997). Онлайн -исправленная версия: (2006–) « Эфирные эфиры ». doi : 10.1351/goldbook.e02219
- ^ Кэмерон Райт (1986). Руководство работника по опасностям растворителя . Группа. п. 48. ISBN 9780969054542 .
- ^ Э. Ричард Бузер (21 декабря 1993 г.). Справочник по смазке и трибологии CRC, том III: мониторинг, материалы, синтетические смазочные материалы и применение . CRC. п. 237. ISBN 978-1-4200-5045-5 .
- ^ «Ацетокситриметилтин» .
- ^ "Триметилтин ацетат | C5H12O2SN | chemspider" .
- ^ Леопольд Гмелин, Справочник по химии , вып. 4: Справочник по органической химии (том 1) (Гейдельберг, Баден (Германия): Карл Винтер, 1848), стр. 182 .
Оригинальный текст:
Перевод:беременный Эфир или кислородная кислота.
Эфиры третьего вида.
Многие минеральные и органические кислородные кислоты собираются вместе с типом спирта с выделением воды к нейтральному, мимолетному, мимолетному незаменимым соединениям, которые можно рассматривать как парные связи спиртовой и кислотной воды или, согласно теории радикалов, в которой кислота с кислотой с кислотой с кислотой с кислотой с кислотой с кислотой один подключен.беременный Эфир или окси-кислотные эфиры.
Эфиры третьего типа.
Многие минеральные и органические кислоты, содержащие кислород, в сочетании с спиртом при удалении воды в [формы] нейтральных, летучих эфирных соединений, которые можно рассматривать как связанные соединения спирта и кислотной воды, или, согласно теории радикалов, как соли в котором кислота связана с эфиром. - ^ Jump up to: а беременный Март, J. Advanced Organic Chemistry 4th Ed. J. Wiley and Sons, 1992: Нью -Йорк. ISBN 0-471-60180-2 .
- ^ «Химия энолей и енолятов-кислотность альфа-гидрогенов» . 13 февраля 2011 года.
- ^ Дивакар М. Павар; Абдельназер А. Халил; Дениз Р. Хукс; Кеннет Коллинз; Тихуана Эллиотт; Джеффорей Стаффорд; Люсиль Смит; Эрик А. Ноэ (1998). " E и Z Конформации сложных эфиров, эфиров тиола и амидов". Журнал Американского химического общества . 120 (9): 2108–2112. doi : 10.1021/ja9723848 .
- ^ Кристоф Дугав; Люк Деманж (2003). «Изомеризация цис -транс -транс органических молекул и биомолекул: последствия и применения». Химические обзоры . 103 (7): 2475–2932. doi : 10.1021/cr0104375 . PMID 12848578 .
- ^ А.А. Яковенко; JH Gallegos; М. Ю. Антипин; А. Масунов; ТВ -Тимофева (2011). «Морфология кристаллов как доказательство супрамолекулярной организации в аддуктах 1,2-бис (хлормеркурио) тетрафторубензола с органическими эфирами». Кристаллический рост и дизайн . 11 (9): 3964–3978. doi : 10.1021/cg200547k .
- ^ Выделение триглицерида из мускатного ореха: GD Beal "Trimiristen" органические синтезы, Coll. Тол. 1, с.538 (1941). Связь
- ^ МакГи, Гарольд. О еде и приготовлении пищи . 2003, Скрибнер, Нью -Йорк.
- ^ Jump up to: а беременный в дюймовый и Riemenschneider, Wilhelm; Болт, Герман М. "Эфиры, органические". Энциклопедия промышленной химии Уллмана . Вейнхайм: Wiley-VCH. Doi : 10.1002/14356007.a09_565.pub2 . ISBN 978-3527306732 .
- ^ Уильямс, Роджер Дж.; Габриэль, Альтон; Эндрюс, Рой С. (1928). «Соотношение между гидролизом равновесие постоянной эфиров и сильной стороны соответствующих кислот». Журнал Американского химического общества . 50 (5): 1267–1271. doi : 10.1021/ja01392a005 .
- ^ Б. Нойзс и В. Стеглих. «Этерификация карбоновых кислот с помощью дициклогексилкарбодиимида/4 -диметиламинопиридина: трет -бутиловый этиловый фумарат» . Органические синтезы ; Собранные объемы , вып. 7, с. 93 .
- ^ Рабер, Дуглас Дж.; Гариано -младший, Патрик; Брод, Альберт О.; Gariano, Anne L.; Guida, Wayne C. (1977). «Этерификация карбоновых кислот с солями из пробных килоксоний: этил и метил 4-ацетоксибензоаты». Органические синтезы . 56 : 59. doi : 10.15227/orgsyn.056.0059 .
- ^ Мацумото, Коучи; Шимазаки, Хаято; Миямото, Юу; Шимада, Казуакаки; Сумма, fumi; Ямада, Юки; Миязава, Хироцугу; Нишиваки, Кейджи; Кашимура, Шигенори (2014). «Простой и удобный синтез эссейстов из карбоновых кислот и алкилгалогенидов с использованием фторида тетрабутиламмония » Журнал науки Oleo 63 (5): 539–544. Doi : 10.5650/ jos.esss1 ISSN 1345-8 24770480PMID
- ^ Bienewald, Frank; Лейбольд, Эдгар; Тужина, Павел; Рошер, Гюнтер (2019). «Виниловые эфиры». Энциклопедия промышленной химии Уллмана . Вейнхайм: Wiley-VCH. С. 1–16. doi : 10.1002/14356007.a27_419.pub2 . ISBN 9783527303854 .
- ^ Камм, О.; Камм, WF (1922). "Бензил -бензоат" . Органические синтезы . 2 : 5. doi : 10.15227/orgsyn.002.0005 ; Собранные объемы , вып. 1, с. 104
- ^ Игнатьев, Игорь; Чарли Ван Усула; Паскаль Гн Мертен; Известные; Третий. E. The Vost (2011). «Синтез или глюкоза Эссис флоглеоз в ионных жидких жидкостях» . Хольцфоршонг . 66 (4): 417–425. doi : 10 1515/hf.2011.161 . S2CID 1017591 .
- ^ Neumeister, Joachim; Кюл, Хельмут; Пратап Саксена, Махендра; Грисбаум, Карл (1978). «Озоновое расщепление олефинов с образованием фрагментов сложных эфиров». Applied Chemistry International Edition на английском языке . 17 (12): 939–940. Doi : 10.1002/ani.197809392 .
- ^ Махова, Ирина В.; Элинсон, Михайл Н.; Nikishin, Gennady I. (1991). «Электрохимическое окисление кетонов в метаноле в присутствии щелочных металлических бромидов». Тетраэдр . 47 (4–5): 895–905. doi : 10.1016/s0040-4020 (01) 87078-2 .
- ^ Jump up to: а беременный Wade 2010, с. 1005–1009.
- ^ W. Reusch. «Реакционная способность карбоксильного производного» . Виртуальный учебник по органической химии . Архивировано с оригинала 2016-05-16.
- ^ Ято, Мичихиса; Хомма, Коичи; Ишида, Акихико (июнь 2001 г.). «Сокращение карбоновых эфиров на эфиры с триэтилоланом в комбинированном использовании тетрахлорида титана и трифриллиллил трифторуорометанесульфонат». Тетраэдр . 57 (25): 5353–5359. doi : 10.1016/s0040-4020 (01) 00420-3 .
- ^ Сакай, Норо; Мория, Тосимицу; Конакахара, Такео (июль 2007 г.). «Эффективный синтез единоличных эфиров с одним POT: непосредственная восстановительная дезоксигенация сложных эфиров с использованием каталитической системы InBr3/ET3SIH». Журнал органической химии . 72 (15): 5920–5922. doi : 10.1021/jo070814z . PMID 17602594 .
- ^ Carey 2006, с. 919–924.
- ^ Kürti and Czakó 2005, p. 30
- ^ Вуд, JL; Хатри, На; Weinreb, SM (1979). «Прямое преобразование сложных эфиров в нитрилы». Тетраэдр буквы . 20 (51): 4907. DOI : 10.1016/S0040-4039 (01) 86746-0 .
- ^ Iupac , сборник химической терминологии , 2 -е изд. («Золотая книга») (1997). Онлайн -исправленная версия: (2006–) « Депсипептиды ». doi : 10.1351/goldbook.d01604