Алкин

В органической химии алкин содержащий — ненасыщенный углеводород, по крайней мере одну углерод —углерод тройную связь . [1] Простейшие ациклические алкины, имеющие только одну тройную связь и не имеющие других функциональных групп, образуют гомологический ряд с общей химической формулой. C п ЧАС 2 п -2 . Алкины традиционно известны как ацетилены, хотя название ацетилен также относится конкретно к C 2 H 2 , формально известный как этин по номенклатуре IUPAC . Как и другие углеводороды, алкины обычно гидрофобны . [2]
Структура и связь
[ редактировать ]В ацетилене валентные углы H–C≡C составляют 180°. Благодаря такому валентному углу алкины имеют стержнеобразную форму. Соответственно, циклические алкины встречаются редко. Бензин не может быть изолирован. Расстояние связи C≡C в 118 пикометров (для C 2 H 2 ) значительно короче, чем расстояние C=C в алкенах (132 пм, для C 2 H 4 ) или связь C–C в алканах (153 пм). [3]

Иллюстративные алкины: а — ацетилен, б — два изображения пропина, в — 1-бутин, г — 2-бутин , д — природный 1-фенилгепта-1,3,5-триин и е — напряженный циклогептин. Тройные связи выделены синим цветом .
Тройная связь очень прочная: сила связи составляет 839 кДж/моль. Сигма -связь дает вклад 369 кДж/моль, первая пи-связь - 268 кДж/моль. и вторая пи-связь 202 кДж/моль. Связь обычно обсуждается в контексте теории молекулярных орбиталей , которая признает, что тройная связь возникает в результате перекрытия s- и p-орбиталей. На языке теории валентных связей атомы углерода в алкиновой связи являются sp-гибридизованными : каждый из них имеет две негибридизированные p-орбитали и две sp-гибридные орбитали . Перекрытие sp-орбиталей каждого атома образует одну sp-sp- сигма-связь . Каждая p-орбиталь одного атома перекрывается друг с другом, образуя две пи-связи, что дает в общей сложности три связи. Оставшаяся sp-орбиталь каждого атома может образовывать сигма-связь с другим атомом, например с атомами водорода в исходном ацетилене. Две sp-орбитали выступают на противоположных сторонах атома углерода.
Терминальные и внутренние алкины
[ редактировать ]Внутренние алкины содержат углеродные заместители на каждом ацетиленовом углероде. Симметричные примеры включают дифенилацетилен и 3-гексин . Они также могут быть асимметричными, как, например, у 2-пентина .
Терминальные алкины имеют формулу РЦ 2 Н . Примером является метилацетилен (пропин по номенклатуре ИЮПАК). Их часто получают алкилированием ацетилида натрия . [4] Концевые алкины, как и сам ацетилен , являются умеренно кислотными, со pKa значениями около 25. Они гораздо более кислые, чем алкены и алканы, значения pKa которых составляют 40 около и 50 соответственно. Кислый водород на концевых алкинах может быть заменен различными группами, в результате чего образуются галоген-, силил- и алкоксоалкины. Карбанионы , образующиеся при депротонировании концевых алкинов, называются ацетилидами . [5]
Именование алкинов
[ редактировать ]В систематической химической номенклатуре алкины обозначаются греческой префиксной системой без каких-либо дополнительных букв. Примеры включают этин или октин. В материнских цепях с четырьмя и более атомами углерода необходимо сказать, где находится тройная связь. Для октина можно написать либо 3-октин, либо окт-3-ин, если связь начинается с третьего атома углерода. Наименьшее возможное число присвоено тройной связи . Когда нет высших функциональных групп, родительская цепь должна включать тройную связь, даже если это не самая длинная возможная углеродная цепь в молекуле. Этин обычно называют тривиальным названием ацетилен.
В химии суффикс -ин используется для обозначения наличия тройной связи. В органической химии суффикс часто следует за номенклатурой ИЮПАК . Однако неорганические соединения, имеющие ненасыщенность в виде тройных связей, могут быть обозначены по номенклатуре заместителей теми же методами, что и для алкинов (т.е. название соответствующего насыщенного соединения модифицируется путем замены « -ана » на «-ин»). . «-дийн» используется, когда есть две тройные связи и так далее. Положение ненасыщенности обозначается числовым локантом, непосредственно предшествующим суффиксу «-yne», или «локантами» в случае нескольких тройных связей. Локанты выбираются так, чтобы их численность была как можно меньшей. «-yne» также используется в качестве суффикса для обозначения групп заместителей, которые трижды связаны с исходным соединением.
число между дефисами, Иногда перед ним ставится указывающее, между какими атомами находится тройная связь. Этот суффикс возник как свернутая форма окончания слова « ацетилен ». Конечный «-e» исчезает, если за ним следует другой суффикс, начинающийся с гласной. [6]
Структурная изомерия
[ редактировать ]Алкины, имеющие четыре или более атомов углерода , могут образовывать различные структурные изомеры , поскольку тройная связь находится в разных положениях или некоторые атомы углерода являются заместителями, а не частью исходной цепи. Возможны также другие неалкиновые структурные изомеры.
- C 2 H 2 : ацетилен только
- C 3 H 4 : пропин только
- C 4 H 6 : 2 изомера: 1-бутин и 2-бутин.
- C 5 H 8 :3 изомера: 1-пентин , 2-пентин и 3-метил-1-бутин.
- C 6 H 10 :7 изомеров: 1-гексин , 2-гексин , 3-гексин , 4-метил-1-пентин , 4-метил-2-пентин , 3-метил-1-пентин , 3,3-диметил- 1-бутин
Синтез
[ редактировать ]Крекинг
[ редактировать ]В коммерческом отношении преобладающим алкином является сам ацетилен, который используется в качестве топлива и предшественника других соединений, например акрилатов . сотни миллионов килограммов Ежегодно в результате частичного окисления производятся природного газа : [7]
Пропин, также полезный в промышленности, также получают термическим крекингом углеводородов.
Дегидрогалогенирование и родственные реакции
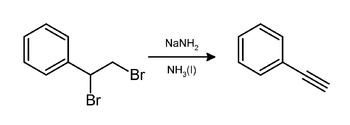
[ редактировать ]Алкины получают из 1,1- и 1,2- дигалогеналканов двойным дегидрогалогенированием . Реакция позволяет получать алкины из алкенов, которые сначала галогенируются , а затем дегидрогалогенируются. Например, фенилацетилен получить из стирола бромированием в с последующей обработкой полученного дибромида стирола амидом натрия можно аммиаке : [8] [9]
посредством перегруппировки Фрича-Буттенберга-Вичелла Алкины получают из винилбромидов . Алкины можно получить из альдегидов по реакции Кори-Фукса, а также из альдегидов или кетонов по реакции Сейферта-Гилберта .
Винилгалогениды чувствительны к дегидрогалогенированию.
Реакции, включая заявки
[ редактировать ]Обладая реакционноспособной функциональной группой , алкины участвуют во многих органических реакциях . Впервые такое использование было предложено Ральфом Рафаэлем , который в 1955 году написал первую книгу, описывающую их универсальность в качестве промежуточных продуктов синтеза . [10]
гидрирование
[ редактировать ]Будучи более ненасыщенными, чем алкены, алкины обычно вступают в реакции, которые показывают, что они «дважды ненасыщены». Алкины способны присоединять два эквивалента H 2 , тогда как алкен добавляет только один эквивалент. [11] В зависимости от катализаторов и условий к алкинам добавляют один или два эквивалента водорода. Частичное гидрирование , прекращающееся после добавления только одного эквивалента с образованием алкена , обычно более желательно, поскольку алканы менее полезны:

Наиболее масштабное применение этой технологии — конверсия ацетилена в этилен на нефтеперерабатывающих заводах (паровой крекинг алканов дает несколько процентов ацетилена, который селективно гидрируется в присутствии палладиевого / серебряного катализатора). Для более сложных алкинов широко рекомендуется использовать катализатор Линдлара , чтобы избежать образования алкана, например, при превращении фенилацетилена в стирол . [12] Точно так же галогенирование алкинов дает алкендигалогениды или алкилтетрагалогениды:
Добавление одного эквивалента H 2 к внутренним алкинам дает цис-алкены.
Добавление галогенов и родственных реагентов
[ редактировать ]Алкины характерно способны присоединять два эквивалента галогенов и галогеноводородов.
Добавление неполярных E-H связи через C≡C является общим для силанов, боранов и родственных гидридов. Гидроборирование алкинов дает виниловые бораны, которые окисляются до соответствующего альдегида или кетона. В тиол-иновой реакции субстратом является тиол.
Добавление галогеноводородов вызывает интерес уже давно. В присутствии хлорида сулемы в качестве катализатора ацетилен и хлористый водород реагируют с образованием винилхлорида . Хотя на Западе от этого метода отказались, он остается основным методом производства в Китае. [13]
Увлажнение
[ редактировать ]Реакция гидратации ацетилена дает ацетальдегид . Реакция протекает с образованием винилового спирта , который таутомеризуется с образованием альдегида. Эта реакция когда-то была основным промышленным процессом, но ее заменил процесс Вакера . Эта реакция происходит в природе, катализатором является ацетиленгидратаза .
Гидратация фенилацетилена дает ацетофенон : [14]
(Ph 3 P)AuCH 3 катализирует гидратацию 1,8-нонадиина в 2,8-нонандион: [15]
Таутомерия
[ редактировать ]Концевые алкилалкины обладают таутомерией. Пропин находится в равновесии с пропадиеном :
Циклоприсоединения и окисление
[ редактировать ]Алкины вступают в разнообразные реакции циклоприсоединения . Реакция Дильса -Альдера с 1,3- диенами дает 1,4-циклогексадиены . Эта общая реакция получила широкое развитие. являются электрофильные алкины Особенно эффективными диенофилами . «Циклоаддукт», полученный в результате добавления алкинов к 2-пирону, удаляет углекислый газ с образованием ароматического соединения. Другие специализированные циклоприсоединения включают многокомпонентные реакции, такие как тримеризация алкинов с образованием ароматических соединений и [2+2+1]-циклоприсоединение алкина, алкена и монооксида углерода в реакции Паусона-Ханда . Неуглеродные реагенты также подвергаются циклизации, например азидалкиновому циклоприсоединению Хейсгена с образованием триазолов . Процессы циклоприсоединения с участием алкинов часто катализируются металлами, например метатезис енинов и метатезис алкинов , что позволяет перемешивать карбиновые (RC) центры:
Окислительное расщепление алкинов протекает путем циклоприсоединения к оксидам металлов. Самый известный способ — перманганат калия превращает алкины в пару карбоновых кислот .
Реакции, специфичные для терминальных алкинов
[ редактировать ]Концевые алкины легко превращаются во многие производные, например, посредством реакций сочетания и конденсации. Конденсацией с формальдегидом и ацетиленом получают бутиндиол : [7] [16]
В реакции Соногаширы концевые алкины соединяются с арил- или винилгалогенидами:
Эта реакционная способность основана на том факте, что концевые алкины являются слабыми кислотами, типичные значения p K a которых составляют около 25, что ставит их между значениями аммиака (35) и этанола (16):
где MX = NaNH 2 , LiBu или RMgX .
Реакции алкинов с катионами некоторых металлов, например В + и С + также дает ацетилиды. Так, несколько капель гидроксида диамминсеребра(I) ( Ag(NH 3 ) 2 OH ) реагирует с концевыми алкинами, о чем свидетельствует образование белого осадка ацетилида серебра. Эта реакционная способность лежит в основе реакций сочетания алкинов , включая сочетание Кадио-Ходкевича , сочетание Глейзера и сочетание Эглинтона , показанное ниже: [17]
В реакции Фаворского и при алкинилировании в целом концевые алкины присоединяются к карбонильным соединениям с образованием гидроксиалкина .
Металлические комплексы
[ редактировать ]Алкины образуют комплексы с переходными металлами. Такие комплексы возникают также в катализируемых металлами реакциях алкинов, таких как тримеризация алкинов . Концевые алкины, включая сам ацетилен, реагируют с водой с образованием альдегидов. Для получения результата антимарковниковского присоединения для превращения обычно требуются металлические катализаторы. [18]
Алкины в природе и медицине
[ редактировать ]По словам Фердинанда Больмана , первое встречающееся в природе ацетиленовое соединение, эфир дегидроматрикарии, было выделено из вида Artemisia в 1826 году. За последующие почти два столетия было обнаружено и зарегистрировано более тысячи встречающихся в природе ацетиленов. Полиины , подмножество этого класса натуральных продуктов, были выделены из самых разных видов растений, культур высших грибов, бактерий, морских губок и кораллов. [19] Некоторые кислоты, такие как таририновая кислота, содержат алкиновую группу. Диины и триины, виды со связью RC≡C-C≡CR' и RC≡C-C≡C-C≡CR' соответственно, встречаются у некоторых растений ( ихтиотерий , хризантема , цикута , энанта и другие представители сложноцветных и семейства Зонтичные ). Некоторыми примерами являются цикутоксин , оэнантотоксин и фалькаринол . Эти соединения обладают высокой биоактивностью, например, являются нематоцидами . [20] 1-Фенилгепта-1,3,5-триин является иллюстрацией встречающегося в природе триина.
Алкины встречаются в некоторых фармацевтических препаратах, включая противозачаточный норэтинодрел . Тройная связь углерод-углерод также присутствует в имеющихся на рынке лекарствах, таких как антиретровирусный препарат Эфавиренц и противогрибковый препарат Тербинафин . Молекулы, называемые ен-диинами, имеют кольцо, содержащее алкен («ен») между двумя алкиновыми группами («диин»). Эти соединения, например калихеамицин , являются одними из наиболее агрессивных известных противоопухолевых препаратов, настолько, что субъединицу ендиин иногда называют «боеголовкой». Эне-диины подвергаются перегруппировке посредством циклизации Бергмана , генерируя высокореактивные радикальные промежуточные соединения, которые атакуют ДНК внутри опухоли. [21]
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Алкин . Британская энциклопедия
- ^ Сол Патай, изд. (1978). Тройная связь углерод-углерод . Том. 1. Джон Уайли и сыновья. ISBN 9780470771563 .
- ^ Смит, Майкл Б.; Марш, Джерри (2006). Продвинутая органическая химия марта: реакции, механизмы и структура . п. 24. дои : 10.1002/0470084960 . ISBN 9780470084960 .
- ^ К. Н. Кэмпбелл, Б. К. Кэмпбелл (1950). « Н -Бутилацетилен». Органические синтезы . 30:15 . дои : 10.15227/orgsyn.030.0015 .
- ^ Блох, Дэниел Р. (2012). Органическая химия демистифицирована (2-е изд.). МакГроу-Хилл. п. 57. ИСБН 978-0-07-176797-2 .
- ^ Комиссия по номенклатуре органической химии (1971) [1958 (A: Углеводороды и B: Фундаментальные гетероциклические системы), 1965 (C: Характеристические группы)]. Номенклатура органической химии (3-е изд.). Лондон: Баттервортс. ISBN 0-408-70144-7 .
- ^ Jump up to: а б Графье, Хайнц; Кёрниг, Вольфганг; Вайц, Ханс Мартин; Рейсс, Вольфганг; Стеффан, Гвидо; Диль, Герберт; Боше, Хорст; Шнайдер, Курт; Кечка, Хайнц (2000). «Бутандиолы, бутендиол и бутинедиол». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. дои : 10.1002/14356007.a04_455 . ISBN 978-3527306732 .
- ^ Кеннет Н. Кэмпбелл, Барбара К. Кэмпбелл (1950). «Фенилацетилен». Органические синтезы . 30:72 . дои : 10.15227/orgsyn.030.0072 .
- ^ А. Ле Кок и А. Горг (1979). «Алкичность посредством дегидрогалогенирования, катализируемого фазовым переносом: диэтилацеталь пропиолальдегида». Органические синтезы . 59 : 10. дои : 10.15227/orgsyn.059.0010 .
- ^ Рафаэль, Ральф Александр (1955). Ацетиленовые соединения в органическом синтезе . Лондон: Научные публикации Баттерворта. ОСЛК 3134811 .
- ^ Россер и Уильямс (1977). Современная органическая химия для A-level . Великобритания: Коллинз. п. 82. ИСБН 0003277402 .
- ^ Х. Линдлар; Р. Дюбюи (1973). «Палладиевый катализатор частичного восстановления ацетиленов» . Органические синтезы ; Сборник томов , т. 5, с. 880 ..
- ^ Дреер, Эберхард-Людвиг; Торкельсон, Теодор Р.; Сумка, Клаус К. (2011). «Хлорэтаны и хлорэтилены». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. дои : 10.1002/14356007.o06_o01 . ISBN 978-3527306732 .
- ^ Фукуда, Ю.; Утимото, К. (1991). «Эффективное преобразование неактивированных алкинов в кетоны или ацетали с помощью катализатора золото (III)». Дж. Орг. хим. 56 (11): 3729. doi : 10.1021/jo00011a058 .
- ^ Мидзушима, Э.; Кюи, Д.-М.; Нат, округ Колумбия; Хаяши, Т.; Танака, М. (2005). «Au(I)-Катализируемая гидратация алкинов: 2,8-нонандиона» . Органические синтезы . 83:55 .
- ^ Питер Пэсслер; Вернер Хефнер; Клаус Бакл; Хельмут Мейнасс; Андреас Мейсвинкель; Ханс-Юрген Вернике; Гюнтер Эберсберг; Рихард Мюллер; Юрген Бесслер; Хартмут Берингер; Дитер Майер (2008). "Ацетилен". Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. дои : 10.1002/14356007.a01_097.pub3 . ISBN 978-3527306732 .
- ^ К. Штёкель и Ф. Сондхаймер (1974). «[18]Аннулен». Органический синтез . 54 : 1. дои : 10.15227/orgsyn.054.0001 .
- ^ Хинтерманн, Лукас; Лабонн, Орели (2007). «Каталитическая гидратация алкинов и ее применение в синтезе». Синтез . 2007 (8): 1121–1150. дои : 10.1055/s-2007-966002 . S2CID 95666091 .
- ^ Аннабель Л.К. Ши Шунь; Рик Р. Тыквински (2006). «Синтез встречающихся в природе полиинов». Энджью. хим. Межд. Эд . 45 (7): 1034–1057. дои : 10.1002/anie.200502071 . ПМИД 16447152 .
- ^ Лам, Йорген (1988). Химия и биология природных ацетиленов и родственных соединений (NOARC): материалы конференции по химии и биологии природных ацетиленов и родственных соединений (NOARC) . Амстердам: Эльзевир. ISBN 0-444-87115-2 .
- ^ С. Уокер; Р. Ландовиц; В. Д. Дин; Г.А. Эллестад; Д. Кан (1992). «Поведение расщепления калихеамицина гамма 1 и калихеамицина Т» . Proc Natl Acad Sci США . 89 (10): 4608–12. Бибкод : 1992PNAS...89.4608W . дои : 10.1073/pnas.89.10.4608 . ПМЦ 49132 . ПМИД 1584797 .














![{\displaystyle {\ce {2R-\!{\equiv }\!-H->[{\ce {Cu(OAc)2}}][{\ce {пиридин}}]R-\!{\equiv }\!-\!{\эквив }\!-R}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/8fe5690544a4da60b118164e70291e6eae02f82e)