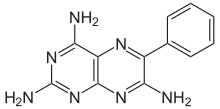
Триамтерен
Этот раздел нуждается в дополнительных цитатах для проверки . ( июнь 2012 г. ) |
 | |
 | |
| Клинические данные | |
|---|---|
| Торговые названия | Дирениум, другие |
| AHFS / Drugs.com | Монография |
| Медлайн Плюс | а682337 |
| Беременность категория |
|
| Маршруты администрация | Через рот |
| код АТС | |
| Юридический статус | |
| Юридический статус |
|
| Фармакокинетические данные | |
| Биодоступность | 30-70% |
| Связывание с белками | 67% |
| Метаболизм | гидроксилирование до парагидрокситриамтерена |
| Период полувыведения | 1-2 часа, активный метаболит 3 часа |
| Экскреция | почки <50%, 21% без изменений |
| Идентификаторы | |
| Номер CAS | |
| ПабХим CID | |
| ИЮФАР/БПС | |
| Лекарственный Банк | |
| ХимическийПаук | |
| НЕКОТОРЫЙ | |
| КЕГГ | |
| ЧЕМБЛ | |
| Панель управления CompTox ( EPA ) | |
| Информационная карта ECHA | 100.006.278 |
| Химические и физические данные | |
| Формула | С 12 Ч 11 Н 7 |
| Молярная масса | 253.269 g·mol −1 |
| | |
Триамтерен (продаваемый под такими названиями, как Dyrenium и Dytac) представляет собой калийсберегающий диуретик , часто используемый в сочетании с тиазидными диуретиками для лечения высокого кровяного давления или отеков . Комбинация с гидрохлоротиазидом известна как гидрохлоротиазид/триамтерен .
Побочные эффекты
[ редактировать ]Общие побочные эффекты могут включать истощение запасов натрия , фолиевой кислоты и кальция , тошноту, рвоту, диарею, головную боль, головокружение, усталость и сухость во рту. Серьезные побочные эффекты могут включать учащенное сердцебиение, покалывание/онемение, лихорадку, озноб, боль в горле, сыпь и боль в спине. Триамтерен также может вызывать образование камней в почках путем прямой кристаллизации или путем посева камней из оксалата кальция . Триамтерен лучше избегать пациентам с хронической болезнью почек из-за возможности гиперкалиемии . Людям, принимающим этот препарат, следует с осторожностью использовать заменитель соли . [2]
Триамтерен может придавать моче синий флуоресцентный цвет.
Осторожность при определенных болезненных состояниях
[ редактировать ]Диабет : применять с осторожностью людям с преддиабетом или сахарным диабетом, поскольку могут наблюдаться изменения в контроле уровня глюкозы.
Нарушение функции печени : применять с осторожностью людям с тяжелыми нарушениями функции печени; при циррозе печени избегайте электролитного и кислотно-щелочного дисбаланса, который может привести к печеночной энцефалопатии .
Почечная недостаточность : комбинированная терапия триамтереном и индометацином вызывала обратимое острое повреждение почек . у некоторых людей [3]
Камни в почках : применять с осторожностью людям с камнями в почках.
Следует избегать применения, если клиренс креатинина менее 10 мл/мин.
Механизм действия
[ редактировать ]Триамтерен напрямую блокирует эпителиальные натриевые каналы. [4] почки (ENaC) на просветной стороне собирательных трубочек . [5] : 127 Другие диуретики вызывают снижение концентрации натрия в формирующейся моче за счет поступления натрия в клетку через ENaC и сопутствующего выхода калия из основной клетки в формирующуюся мочу. Блокировка ENaC предотвращает это. Амилорид действует таким же образом. Блокаторы натриевых каналов непосредственно ингибируют поступление натрия в натриевые каналы.
С гидрохлоротиазидом
[ редактировать ]Триамтерен обычно готовят в сочетании с гидрохлоротиазидом для лечения гипертонии (высокого кровяного давления) и отеков (задержки воды). Эта комбинация относится к классу лекарств, называемых диуретиками или «водными таблетками», и заставляет почки избавляться от ненужной организму воды и натрия через мочу . [6]
История
[ редактировать ]Кольцевая система триамтерена встречается во многих встречающихся в природе соединениях, таких как фолиевая кислота и рибофлавин. Наблюдение того, что встречающееся в природе соединение ксантоптерин оказывает влияние на почки, побудило ученых из Smith Kline и French Laboratories в Филадельфии начать кампанию по медицинской химии для открытия потенциальных лекарств в рамках программы по поиску калийсберегающих диуретиков. [5] : 125 Первые клинические исследования были опубликованы в 1961 году, а первые испытания по сочетанию его с гидрохлоротиазидом были опубликованы в следующем году. [5] : 126 [7] [8]
Smith Kline & French запустила его как единого агента под брендом Dyrenium в 1964 году. [9] : 83 Комбинированный препарат с гидрохлоротиазидом, Диазид, был впервые одобрен в США в 1965 году, а первый дженерик, выпущенный компанией Bolar Pharmaceutical Co., был одобрен в 1987 году. [10] [11] В 1986 году Диазид был самым прописываемым препаратом в США, его объем продаж составил 325 миллионов долларов, что сделало его вторым по величине продаваемым препаратом компании SmithKline Beckman после Тагамета . [11]
Срок действия патентов на Диазид истек в 1980 году, но с появлением дженериков возникли сложности, поскольку в результате рецептуры Диазида использовались различные партии, из-за которых производители дженериков не могли продемонстрировать, что их версии биоэквивалентны. [12] [13]
Компания Bolar Pharmaceutical претендовала на то, чтобы первой представить дженерик, но ее применение было отложено из-за опасений по поводу того, обеспечивает ли ее рецептура одинаковое количество каждого препарата; они были осложнены обвинениями в том, что Болар обманным путем заменил Диазид своей собственной версией для проведения исследований, которые были представлены в FDA. [11] Вскоре после того, как дженерик Болара был одобрен, возникли дополнительные опасения по поводу применения Болара на рынке дженериков в более широком смысле; Эти результаты, среди прочего, вызвали широкую обеспокоенность среди врачей и общественности по поводу того, действительно ли дженерики совпадают с фирменными лекарствами. [14] [15] В конечном итоге Болар отозвал свою непатентованную форму Диазида и прекратил выпуск продукта в 1990 году. [16] В 1991 году Министерство юстиции США от имени FDA возбудило против Болара 20 уголовных обвинений за мошенничество. [17] а в начале следующего года Болар признал себя виновным и согласился выплатить штраф в размере 10 миллионов долларов. [18] Обеспокоенность общественности по поводу безопасности непатентованных лекарств еще больше усугубилась расследованием Конгресса по факту взяточничества в FDA со стороны компаний-производителей дженериков, которое обнаружило широко распространенную коррупцию; Расследование было инициировано компанией-производителем дженериков Mylan , которая наняла частных детективов, поскольку считала, что конкуренты получают несправедливые преимущества при одобрении своих дженериков. [19]
Сама компания Mylan разработала версию комбинированного препарата триамтерен/гидрохлоротиазид после истечения срока действия патента на диазид и использовала другую, более стабильную рецептуру. [13] а также разные дозировки каждого активного ингредиента (50 мг гидрохлоротиазида и 75 мг триамтерена по сравнению с 25 мг гидрохлоротиазида и 50 мг триамтерена у Dyazide), поэтому он должен был получить одобрение как новый препарат, а не как дженерик; их продукт назывался Maxzide и был одобрен в 1984 году. [20] [21] Более высокая доза позволяла принимать препарат один раз в день, что, по мнению Mylan и его маркетингового партнера Lederle, помогло бы ему конкурировать с Dyazide, объем продаж которого в 1983 году составил 210 миллионов долларов. [21]
Патенты Милана на препарат были признаны недействительными в суде, а его эксклюзивность на рынке истекла в 1987 году, что вызвало всплеск конкуренции со стороны дженериков и судебные разбирательства между двумя из них, American Therapeutics Inc. и Vitarine Pharmaceuticals, с FDA. [22] Vitarine, наряду с Par Pharmaceutical , были двумя компаниями, на которые Mylan нацелился в своем расследовании коррупции, и выяснилось, что Par и Vitarine использовали Maxzide Mylan для получения данных о его биоэквивалентности, что привело к тому, что обе компании отозвали своего конкурента-генерика в пользу Mylan. продукт. [19] [23] Дженерики в конечном итоге вышли на рынок. [24]
Исследовать
[ редактировать ]Несмотря на отсутствие рандомизированных контролируемых исследований по оценке использования триамтерена в лечении болезни Меньера , типичное лечение составляет 37,5 мг триамтерена с 25 мг гидрохлоротиазида по 1–2 капсулы в день. [25] [26] Этой рекомендации был присвоен класс таксономии «Сила рекомендации» (SORT) — C. [ нужна ссылка ]
Ссылки
[ редактировать ]- ^ «Список всех лекарств с предупреждениями о черном ящике, полученный FDA (используйте ссылки «Загрузить полные результаты» и «Просмотреть запрос»)» . nctr-crs.fda.gov . FDA . Проверено 22 октября 2023 г.
- ^ «Консультативное заявление» (PDF) . ЛоСоль . Архивировано из оригинала (PDF) 10 декабря 2005 г.
- ^ Фавр Л., Глассон П., Валлоттон М.Б. (март 1982 г.). «Обратимая острая почечная недостаточность при комбинированном применении триамтерена и индометацина: исследование на здоровых добровольцах». Анналы внутренней медицины . 96 (3): 317–320. дои : 10.7326/0003-4819-96-3-317 . ПМИД 6949485 .
- ^ Буш А.Е., Зюссбрих Х., Кунцельманн К., Хиппер А., Грегер Р., Вальдеггер С. и др. (сентябрь 1996 г.). «Блокада эпителиальных каналов Na+ триамтеренами - основные механизмы и молекулярные основы». Архив Пфлюгерса . 432 (5): 760–766. дои : 10.1007/s004240050196 . ПМИД 8772124 . S2CID 10489391 .
- ^ Jump up to: а б с Финк К.А., Маккенна Дж.М., Вернер Л.Х. (2003). «Мочегонные и урикозурические средства». В Аврааме DJ (ред.). Медицинская химия Бургера и открытие лекарств. Том 3: Сердечно-сосудистые агенты и эндокринная система (6-е изд.). Уайли. стр. 55–154. ISBN 978-0471370291 .
- ^ «Триамтерен и гидрохлоротиазид» . МедлайнПлюс . Национальная медицинская библиотека США . Национальные институты здравоохранения . 1 сентября 2008 г.
- ^ Кросли А.П., Ронкильо Л.М., Стрикленд У.Х., Александр Ф. (февраль 1962 г.). «Триамтерен, новый натруретик. Предварительные наблюдения на человеке». Анналы внутренней медицины . 56 (2): 241–251. дои : 10.7326/0003-4819-56-2-241 . ПМИД 13882367 .
- ^ Хит У.К., Фрейс Э.Д. (октябрь 1963 г.). «Триамтерен с гидрохлоротиазидом в лечении гипертонии». ДЖАМА . 186 (2): 119–122. дои : 10.1001/jama.1963.03710020039012 . ПМИД 14056525 .
- ^ Ландау Р., Ахилладелис Б., Скрябин А. (1999). Фармацевтические инновации: революция в здравоохранении человека . Серия Фонда химического наследия, посвященная инновациям и предпринимательству. Том. 2. Фонд химического наследия. ISBN 9780941901215 .
- ^ FDA «История одобрения NDA 016042: Диазид» . Управление по контролю за продуктами и лекарствами США . Проверено 8 сентября 2016 г.
- ^ Jump up to: а б с Вольф Р. (22 августа 1987 г.). Smithkline теряет исключительные права на наркотики .
{{cite book}}:|work=игнорируется ( помогите ) - ^ Бём Г., Яо Л., Хан Л., Чжэн Ц. (сентябрь 2013 г.). «Развитие индустрии непатентованных лекарств в США после Закона Хэтча-Ваксмана 1984 года» . Акта Фармацевтика Синика Б. 3 (5): 297–311. дои : 10.1016/j.apsb.2013.07.004 .
- ^ Jump up to: а б Моряк Дж., Лэндри Дж.Т. (2011). Милан 50 лет нетрадиционного успеха . Университетское издательство Новой Англии. п. 50. ISBN 9781611682700 .
- ^ Стрикленд С. (15 октября 1989 г.). «Болар: фармацевтическая компания в осаде» . Нью-Йорк Таймс .
- ^ Саймонс М. (29 августа 1989 г.). «FDA отменяет одобрение последней генерической версии диазида» . Лос-Анджелес Таймс .
- ^ «Болар вспоминает непатентованную версию диазида и фенитоина пролонгированного действия, заявляя, что «биоэквивалентность не может быть гарантирована»; продукты составляют 52% продаж» . Розовый лист . 5 февраля 1990 г.
- ^ Шоу Д. (27 февраля 1991 г.). «США обвиняют Bolar Pharmaceutical в искажении информации о своей продукции» . Филадельфийский исследователь .
- ^ Фройденхайм М (28 февраля 1991 г.). «Болар планирует признать себя виновным в отношении дженериков» . Нью-Йорк Таймс .
- ^ Jump up to: а б Фройденхайм М (10 сентября 1989 г.). «Разоблачение FDA» The New York Times .
- ^ «История одобрения NDA 019129: Максзид» . Управление по контролю за продуктами и лекарствами США . Проверено 8 сентября 2016 г.
- ^ Jump up to: а б «Максид Mylan «одобрен» FDA: Lederle будет конкурировать с брендом Smithkline, занявшим третье место в рейтинге Dyazide; окончательное одобрение ожидается «немедленно» » . Розовый лист . 22 октября 1984 г.
- ^ Рид К. (17 ноября 1987 г.). «Судья США вынесет решение по делу о маркетинге наркотиков» . Журнал коммерции.
- ^ Эндрюс Э.Л. (31 июля 1989 г.). «Расследование FDA по непатентованным лекарствам сосредоточено на изменениях в ингредиентах» . Нью-Йорк Таймс .
- ^ «Дженерик Максзид» . Наркотики.com . Проверено 8 сентября 2016 г.
- ^ Шварц Р., Лонгвелл П. (март 2005 г.). «Лечение головокружения» (PDF) . Американский семейный врач . 71 (6): 1115–1122. ПМИД 15791890 .
- ^ Слоан П.Д., Коейто Р.Р., Бек Р.С., Даллара Дж. (май 2001 г.). «Головокружение: состояние науки». Анналы внутренней медицины . 134 (9, часть 2): 823–832. doi : 10.7326/0003-4819-134-9_Part_2-200105011-00005 . ПМИД 11346317 . S2CID 6762911 .