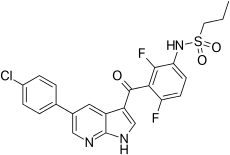
Вемурафениб
 | |
 | |
| Клинические данные | |
|---|---|
| Произношение | / ˌ v ɛ m ə ˈ r æ f ə n ɪ b / VEM -ə- RAF -ə-nib |
| Торговые названия | Зельбораф |
| Другие имена | PLX4032, RG7204, PLX4720, RO5185426 |
| AHFS / Drugs.com | Монография |
| МедлайнПлюс | а612009 |
| Данные лицензии |
|
| Беременность категория |
|
| Маршруты администрация | Через рот |
| код АТС | |
| Юридический статус | |
| Юридический статус | |
| Идентификаторы | |
| Номер CAS | |
| ПабХим CID | |
| ИЮФАР/БПС | |
| Лекарственный Банк | |
| ХимическийПаук | |
| НЕКОТОРЫЙ | |
| КЕГГ | |
| ХЭМБЛ | |
| PDB-лиганд | |
| Панель управления CompTox ( EPA ) | |
| Информационная карта ECHA | 100.287.801 |
| Химические и физические данные | |
| Формула | С 23 Н 18 Cl F 2 Н 3 О 3 С |
| Молярная масса | 489.92 g·mol −1 |
| 3D model ( JSmol ) | |
| (проверять) | |
| вемурафениб | |
|---|---|
| Лекарственный механизм | |
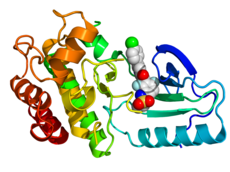 Кристаллографическая структура B-Raf (цвет радуги, N-конец = синий, C-конец = красный) в комплексе с вемурафенибом (сферы, углерод = белый, кислород = красный, азот = синий, хлор = зеленый, фтор = голубой, сера = желтый). [ 2 ] | |
| Терапевтическое использование | меланома |
| Биологическая цель | БРАФ |
| Механизм действия | ингибитор протеинкиназы |
| Внешние ссылки | |
| PDB Идентификатор лиганда | 032: PDBe , RCSB PDB |
| РАСПОЛОЖЕНИЕ УЧАСТОК | 3og7 |
Вемурафениб ( МНН ), продаваемый под торговой маркой Зелбораф , представляет собой препарат, используемый для лечения поздней стадии меланомы . [ 2 ] Он является ингибитором фермента -Raf B и был разработан компанией Plexxikon . [ 2 ]
Механизм действия
[ редактировать ]Вемурафениб вызывает запрограммированную гибель клеток в меланомы . клеточных линиях [ 3 ] Вемурафениб прерывает этап B-Raf/MEK на пути B-Raf/MEK/ERK – если B-Raf имеет общую мутацию V600E.
Вемурафениб работает только у пациентов с меланомой, у которых рак имеет мутацию V600E BRAF (то есть в положении аминокислоты под номером 600 в белке B-Raf нормальный валин заменяется глутаминовой кислотой ). [ 4 ] Около 60% меланом имеют эту мутацию. Он также эффективен против более редкой мутации BRAF V600K. Клетки меланомы без этих мутаций не ингибируются вемурафенибом; препарат парадоксальным образом стимулирует нормальный BRAF и в таких случаях может способствовать росту опухоли. [ 5 ] [ 6 ]
Сопротивление
[ редактировать ]Обнаружены три механизма резистентности к вемурафенибу (охватывающие 40% случаев):
- Раковые клетки начинают сверхэкспрессировать белок клеточной поверхности PDGFRB , создавая альтернативный путь выживания.
- Второй онкоген , называемый NRAS , мутирует, реактивируя нормальный путь выживания BRAF. [ 7 ]
- стромальными клетками Секреция фактора роста гепатоцитов (HGF). [ 8 ] [ 9 ]
Побочные эффекты
[ редактировать ]При максимально переносимой дозе (МПД) 960 мг два раза в день у 31% пациентов возникают поражения кожи, которые могут потребовать хирургического удаления. [ 2 ] В исследовании BRIM-2 приняли участие 132 пациента; наиболее частыми нежелательными явлениями были артралгия у 58% пациентов, кожная сыпь у 52% и фотосенсибилизация у 52%. Чтобы лучше контролировать побочные эффекты, у 45% пациентов потребовалась некоторая модификация дозы. Средняя суточная доза составила 1750 мг, 91% от MTD. [ 10 ]
История
[ редактировать ]В ходе I фазы клинического исследования вемурафениб (тогда известный как PLX4032) смог уменьшить количество раковых клеток более чем у половины группы из 16 пациентов с поздней стадией меланомы. В группе, получавшей лечение, медианное время выживания увеличилось на 6 месяцев по сравнению с контрольной группой. [ 11 ] [ 12 ] [ 13 ] [ 14 ]
Исследование второй фазы I у пациентов с мутацией V600E в B-Raf примерно в 80% случаев показало частичную или полную регрессию. Регресс длился от 2 до 18 месяцев. [ 15 ]
В начале 2010 года фазы I. испытание [ 16 ] для солидных опухолей (включая колоректальный рак ), а также исследование фазы II (для метастатической меланомы). [ 17 ]
Исследование III фазы (по сравнению с дакарбазином ) у пациентов с ранее не леченной метастатической меланомой показало улучшение показателей общей выживаемости и выживаемости без прогрессирования. [ 18 ]
В июне 2011 года были получены положительные результаты исследования меланомы с мутацией BRIM3 фазы III. [ 19 ] В 2012 году в исследовании BRIM3 были получены хорошие обновленные результаты. [ 20 ]
Запланированы дальнейшие испытания, включая исследование вемурафениба, назначаемого одновременно с GDC-0973 ( кобиметинибом ), ингибитором МЕК . [ 19 ] После хороших результатов в 2014 году комбинация была представлена в Европейское медицинское агентство и Управление по контролю за продуктами и лекарствами США для одобрения маркетинга. [ 21 ]
В январе 2015 года результаты исследования сравнивали вемурафениб с комбинацией дабрафениба и траметиниба при метастатической меланоме. [ 22 ]
Общество и культура
[ редактировать ]Юридический статус
[ редактировать ]Вемурафениб был одобрен в США для лечения поздней стадии меланомы в августе 2011 года. [ 23 ] что сделало его первым препаратом, разработанным с использованием открытия свинца на основе фрагментов и получившим одобрение регулирующих органов. [ 24 ]
Вемурафениб был одобрен для применения в Канаде в феврале 2012 года. [ 25 ]
В феврале 2012 года Европейская комиссия одобрила вемурафениб в качестве монотерапии для лечения взрослых с BRAF V600E с положительной мутацией неоперабельной или метастатической меланомой , наиболее агрессивной формой рака кожи. [ 26 ]
США В ноябре 2017 года Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) одобрило вемурафениб для лечения людей с болезнью Эрдгейма-Честера (ECD), редким типом гистиоцитарного новообразования. [ 27 ] [ 28 ]
Исследовать
[ редактировать ]Испытание комбинации вемурафениба и ипилимумаба было остановлено в апреле 2013 года из-за признаков токсичности для печени . [ 29 ]
Лечение волосатоклеточного лейкоза
[ редактировать ]В 2012 году грант Фонда волосатоклеточного лейкоза поддержал открытие мутации BRAF в классическом HCL. Это открытие открыло новый путь вперед для многих пациентов. Это улучшило диагностику и открыло возможности для использования дополнительных методов лечения HCL. [ 30 ] В рамках II фазы клинических исследований компания Memorial Sloan Kettering тестирует вемурафениб в сочетании с обинутузумабом на пациентах с ранее не леченным классическим волосатоклеточным лейкозом. [ 31 ] Отдельное клиническое исследование лечения только вемурафенибом (или монотерапией) продемонстрировало высокие показатели ответа при рецидивирующем/рефрактерном (R/R) волосатоклеточном лейкозе (HCL), достигнув общего уровня ответа 86%, включая 33% полного ответа (CR) и 53% частичный ответ. Однако после медианы наблюдения в течение 40 месяцев у 21 из 31 участника, ответившего на лечение (68%), развился рецидив, при этом медиана безрецидивной выживаемости (БВР) составила 19 месяцев (диапазон 12,5–53,9 месяцев). [ 32 ]
Ссылки
[ редактировать ]- ^ Перейти обратно: а б «Информация об австралийском продукте: Зелбораф® (вемурафениб)» . Roche Products Pty Limited . 25 марта 2020 г.
- ^ Перейти обратно: а б с д ВВП : 3ОГ7 ; Боллаг Г., Хирт П., Цай Дж., Чжан Дж., Ибрагим П.Н., Чо Х. и др. (сентябрь 2010 г.). «Клиническая эффективность ингибитора RAF требует широкой целевой блокады при меланоме с мутацией BRAF» . Природа . 467 (7315): 596–599. Бибкод : 2010Natur.467..596B . дои : 10.1038/nature09454 . ПМК 2948082 . ПМИД 20823850 .
- ^ Сала Э., Молоньи Л., Труффа С., Гаэтано С., Боллаг Г.Е., Гамбакорти-Пассерини С. (май 2008 г.). «Замалчивание BRAF с помощью короткой шпильковой РНК или химическая блокада PLX4032 приводит к различным реакциям в клетках меланомы и рака щитовидной железы». Молекулярные исследования рака . 6 (5): 751–759. doi : 10.1158/1541-7786.MCR-07-2001 . ПМИД 18458053 . S2CID 16031942 .
- ^ Маверакис Э., Корнелиус Л.А., Боуэн Г.М., Фан Т., Патель Ф.Б., Фицморис С. и др. (май 2015 г.). «Метастатическая меланома – обзор текущих и будущих вариантов лечения» . Acta Dermato-Venereologica . 95 (5): 516–524. дои : 10.2340/00015555-2035 . ПМИД 25520039 .
- ^ Хацивассилиу Г., Сонг К., Йен И., Брандхубер Б.Дж., Андерсон Дж.Д., Альварадо Р. и др. (март 2010 г.). «Ингибиторы RAF стимулируют RAF дикого типа для активации пути MAPK и усиления роста» . Природа . 464 (7287): 431–435. Бибкод : 2010Natur.464..431H . дои : 10.1038/nature08833 . ПМИД 20130576 .
- ^ Халабан Р., Чжан В., Баччиокки А., Ченг Э., Паризи Ф., Ариян С. и др. (апрель 2010 г.). «PLX4032, селективный ингибитор киназы BRAF(V600E), активирует путь ERK и усиливает миграцию клеток и пролиферацию клеток меланомы BRAF» . Исследование пигментных клеток и меланомы . 23 (2): 190–200. дои : 10.1111/j.1755-148X.2010.00685.x . ПМЦ 2848976 . ПМИД 20149136 .
- ^ Назарян Р., Ши Х., Ван К., Конг Х., Коя Р.К., Ли Х. и др. (декабрь 2010 г.). «Меланомы приобретают устойчивость к ингибированию B-RAF (V600E) за счет активации RTK или N-RAS» . Природа . 468 (7326): 973–977. Бибкод : 2010Natur.468..973N . дои : 10.1038/nature09626 . ПМК 3143360 . ПМИД 21107323 .
- «Исследователи раскрывают механизмы лекарственной устойчивости меланомы BRAF» . Новости генной инженерии и биотехнологии . 25 ноября 2010 г.
- ^ Штраусман Р., Морикава Т., Ши К., Барзили-Рокни М., Цянь З.Р., Ду Дж. и др. (июль 2012 г.). «Микроокружение опухоли вызывает врожденную устойчивость к ингибиторам RAF посредством секреции HGF» . Природа . 487 (7408): 500–504. Бибкод : 2012Natur.487..500S . дои : 10.1038/nature11183 . ПМЦ 3711467 . ПМИД 22763439 .
- ^ Уилсон Т.Р., Фридлянд Дж., Ян Ю., Пенуэль Э., Бертон Л., Чан Э. и др. (июль 2012 г.). «Широко распространенный потенциал устойчивости факторов роста к ингибиторам противораковых киназ» . Природа . 487 (7408): 505–509. Бибкод : 2012Natur.487..505W . дои : 10.1038/nature11249 . ПМЦ 3724525 . ПМИД 22763448 .
- ^ «BRIM-2 подтверждает преимущества вемурафениба при меланоме» . Новости онкологии и биотехнологий . 5 (7). Июль 2011.
- ^ «Лекарственная надежда на прогрессирующую меланому» . Новости Би-би-си. 2009-06-02 . Проверено 7 июня 2009 г.
- ^ Хармон А (21 февраля 2010 г.). «Погоня за лекарством на американских горках» . Нью-Йорк Таймс .
- ^ Гарбер К. (декабрь 2009 г.). «Исследование рака. Лекарство от меланомы оправдывает целенаправленный подход». Наука . 326 (5960): 1619. Бибкод : 2009Sci...326.1619G . дои : 10.1126/science.326.5960.1619 . ПМИД 20019269 .
- ^ Флаэрти К. «Фаза I исследования PLX4032: подтверждение концепции мутации V600E BRAF как терапевтической мишени при раке человека» . Аннотация к ежегодному собранию ASCO 2009 г., J Clin Oncol 27:15s, 2009 г. (дополнение; абстракт 9000) . Архивировано из оригинала 27 января 2013 г. Проверено 10 сентября 2010 г.
- ^ Флаэрти К.Т., Пузанов И., Ким К.Б., Рибас А., Макартур Г.А., Сосман Дж.А. и др. (август 2010 г.). «Ингибирование мутированного активированного BRAF при метастатической меланоме» . Медицинский журнал Новой Англии . 363 (9): 809–819. дои : 10.1056/NEJMoa1002011 . ПМЦ 3724529 . ПМИД 20818844 .
- Лоу Д. (9 сентября 2010 г.). «PLX4032: хорошие новости и плохие новости» . В Трубопроводе. Коранте . Архивировано из оригинала 11 сентября 2010 г.
- ^ Номер клинического исследования NCT00405587 «Исследование безопасности PLX4032 у пациентов с солидными опухолями» на сайте ClinicalTrials.gov.
- ^ Номер клинического исследования NCT00949702 «Исследование RO5185426 у ранее леченных пациентов с метастатической меланомой» на сайте ClinicalTrials.gov.
- ^ «Plexxikon объявляет о первом пациенте, получившем дозу PLX4032 (RG7204) в рамках третьей фазы исследования при метастатической меланоме» (пресс-релиз). Плексксикон. 08.01.2010. Архивировано из оригинала 01 декабря 2020 г. Проверено 3 февраля 2011 г.
- ^ Перейти обратно: а б «Plexxikon и Roche сообщают о положительных данных исследования меланомы с мутацией BRAF III фазы» . Новости генной инженерии и биотехнологии . Издательство Мэри Энн Либерт. 6 июня 2011 г.
- ^ «Вемурафениб улучшает общую выживаемость пациентов с метастатической меланомой» . Архивировано из оригинала 11 января 2022 г. Проверено 17 декабря 2012 г.
- ^ «Кобиметиниб на exelixis.com» . Архивировано из оригинала 4 февраля 2015 г. Проверено 4 февраля 2015 г.
- ^ «Комбинация ингибиторов MEK/BRAF снижает смертность от меланомы на одну треть» . 2015.
- ^ «FDA одобрило Зелбораф (Вемурафениб) и сопутствующий диагностический препарат для метастатической меланомы с положительной мутацией BRAF, смертельной формы рака кожи» (пресс-релиз). Генентек . Проверено 17 августа 2011 г.
- ^ Боллаг Г., Цай Дж., Чжан Дж., Чжан С., Ибрагим П., Нолоп К., Хирт П. (ноябрь 2012 г.). «Вемурафениб: первый препарат, одобренный для лечения рака с мутацией BRAF». Обзоры природы. Открытие наркотиков . 11 (11): 873–886. дои : 10.1038/nrd3847 . ПМИД 23060265 . S2CID 9337155 .
- ^ «Уведомление о решении ZELBORAF» . Здоровье Канады . 11 марта 2012 г. Архивировано из оригинала 2 мая 2012 г. . Проверено 21 апреля 2012 г.
- ^ Хофланд П. (20 февраля 2012 г.). «Первое персонализированное лекарство от рака позволяет пациентам со смертельной формой метастатической меланомы жить значительно дольше» . Онко'Зин . Международная онкологическая сеть. Архивировано из оригинала 11 апреля 2012 года . Проверено 18 февраля 2013 г.
- ^ «FDA одобряет первое лечение для некоторых пациентов с болезнью Эрдгейма-Честера, редким раком крови» . США Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) (пресс-релиз) . Проверено 20 мая 2018 г.
- ^ Даймонд Э.Л., Суббия В., Локхарт А.С., Блей Дж.Ю., Пузанов И., Чау И. и др. (март 2018 г.). «Вемурафениб при мутантной болезни Эрдгейма-Честера BRAF V600 и гистиоцитозе клеток Лангерганса: анализ данных независимого от гистологии открытого исследования VE-BASKET фазы 2» . JAMA Онкология . 4 (3): 384–388. дои : 10.1001/jamaoncol.2017.5029 . ПМЦ 5844839 . ПМИД 29188284 .
- ^ «Близкое и личное» . Экономист . 4 января 2014 г. ISSN 0013-0613 . Проверено 15 апреля 2016 г.
- ^ «Волосатоклеточный лейкоз: празднование прогресса?» . Блог ХКФ . 29 июля 2022 г. . Проверено 25 июля 2022 г.
- ^ Номер клинического исследования NCT03410875 «Волосатоклеточный лейкоз с вемурафебибом» на сайте ClinicalTrials.gov.
- ^ Ханда С., Ли Дж.О., Деркач А., Стоун Р.М., Савен А., Альтман Дж.К. и др. (декабрь 2022 г.). «Отдаленные результаты у пациентов с рецидивирующим или рефрактерным волосатоклеточным лейкозом, получавших монотерапию вемурафенибом» . Кровь . 140 (25): 2663–2671. дои : 10.1182/blood.2022016183 . ПМЦ 9935554 . ПМИД 35930750 .
Дальнейшее чтение
[ редактировать ]- Дин Л. (2017). «Терапия вемурафенибом и генотип BRAF и NRAS» . В Пратт В.М., МакЛеод Х.Л., Рубинштейн В.С. и др. (ред.). Краткое изложение медицинской генетики . Национальный центр биотехнологической информации (NCBI). ПМИД 28809522 . Идентификатор книжной полки: NBK447416.