Мускариновый рецептор ацетилхолина


Мускариновые рецепторы ацетилхолина , или mAChR , представляют собой рецепторы ацетилхолина , которые образуют рецепторные комплексы, связанные с G-белком, в клеточных мембранах определенных нейронов. [1] и другие клетки . Они играют несколько ролей, в том числе действуют как основные концевые рецепторы, стимулируемые ацетилхолином, высвобождаемым из постганглионарных волокон . Они в основном обнаруживаются в парасимпатической нервной системе , но также играют роль в симпатической нервной системе в контроле над потовыми железами . [2]
Мускариновые рецепторы названы так потому, что они более чувствительны к мускарину, чем к никотину . [3] Их аналогами являются никотиновые ацетилхолиновые рецепторы (нАХР), рецепторные ионные каналы, которые также важны в вегетативной нервной системе . Многие лекарства и другие вещества (например, пилокарпин и скополамин ) манипулируют этими двумя отдельными рецепторами, действуя как селективные агонисты или антагонисты . [4]
Функция
[ редактировать ]Ацетилхолин (АХ) — нейромедиатор , обнаруженный в головном мозге , нервно-мышечных соединениях и вегетативных ганглиях .Мускариновые рецепторы используются в следующих ролях:
Рецепторы восстановления
[ редактировать ]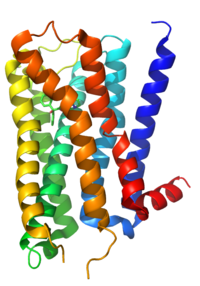
АХ всегда используется в качестве нейромедиатора в вегетативном ганглии . Никотиновые рецепторы постганглионарного нейрона ответственны за начальную быструю деполяризацию (быстрый ВПСП ) этого нейрона. Вследствие этого никотиновые рецепторы часто называют рецепторами постганглионарных нейронов ганглия . Однако последующая гиперполяризация ( IPSP ) и медленная деполяризация (Slow EPSP), которые представляют собой восстановление постганглионарных нейронов после стимуляции, на самом деле опосредуются мускариновыми рецепторами типов M 2 и M 1 соответственно (обсуждается ниже). [ нужна ссылка ]
Периферические вегетативные волокна (симпатические и парасимпатические волокна) анатомически классифицируются как преганглионарные или постганглионарные волокна , а затем далее обобщаются как адренергические волокна, выделяющие норадреналин, или холинергические волокна, одновременно высвобождающие ацетилхолин и экспрессирующие ацетилхолиновые рецепторы. Как преганглионарные симпатические волокна, так и преганглионарные парасимпатические волокна являются холинергическими. Большинство постганглионарных симпатических волокон являются адренергическими: их нейромедиатором является норадреналин, за исключением постганглионарных симпатических волокон, идущих к потовым железам, пилоэректильным мышцам волосков тела и артериолам скелетных мышц, которые не используют адреналин/норадреналин.
Мозговое вещество надпочечников считается симпатическим ганглием и, как и другие симпатические ганглии, снабжается холинергическими преганглионарными симпатическими волокнами: ацетилхолин является нейромедиатором, используемым в этом синапсе. Хромаффинные клетки мозгового вещества надпочечников действуют как «модифицированные нейроны», выделяя адреналин и норадреналин в кровоток в виде гормонов, а не нейромедиаторов. Остальные постганглионарные волокна периферической вегетативной системы относятся к парасимпатическому отделу; все они являются холинергическими волокнами и используют ацетилхолин в качестве нейромедиатора.
Постганглионарные нейроны
[ редактировать ]Другая роль этих рецепторов заключается в соединении иннервируемых тканей и постганглионарных нейронов парасимпатического отдела вегетативной нервной системы. Здесь ацетилхолин снова используется в качестве нейромедиатора, а мускариновые рецепторы образуют основные рецепторы иннервируемой ткани.
Иннервированная ткань
[ редактировать ]Очень немногие части симпатической системы используют холинергические рецепторы. В потовых железах рецепторы мускаринового типа. Симпатическая нервная система также имеет несколько преганглионарных нервов, оканчивающихся у хромаффинных клеток , мозгового вещества надпочечников которые секретируют адреналин и норадреналин в кровоток. Некоторый [ ВОЗ? ] считают, что хромаффинные клетки представляют собой модифицированные постганглионарные волокна ЦНС. В мозговом веществе надпочечников в качестве нейромедиатора используется ацетилхолин, а рецептор никотинового типа .
Соматическая нервная система использует никотиновый рецептор ацетилхолина в нервно-мышечном соединении.
Высшая центральная нервная система
[ редактировать ]Мускариновые рецепторы ацетилхолина также присутствуют и распределены по всей местной нервной системе, в постсинаптических и пресинаптических позициях. Есть также некоторые свидетельства того, что постсинаптические рецепторы на симпатических нейронах позволяют парасимпатической нервной системе ингибировать симпатические эффекты.
Пресинаптическая мембрана нервно-мышечного соединения
[ редактировать ]Известно, что мускариновые рецепторы ацетилхолина появляются также на пресинаптической мембране соматических нейронов нервно-мышечного соединения, где они участвуют в регуляции высвобождения ацетилхолина.
Форма мускариновых рецепторов
[ редактировать ]Мускариновые рецепторы ацетилхолина относятся к классу метаботропных рецепторов , которые используют G-белки в качестве сигнального механизма. В таких рецепторах сигнальная молекула (лиганд ) связывается с мономерным рецептором , имеющим семь трансмембранных областей ; в данном случае лигандом является АХ. Этот рецептор связан с внутриклеточными белками, известными как G-белки, которые запускают информационный каскад внутри клетки. [5]
Напротив, никотиновые рецепторы образуют пентамерные комплексы и используют для передачи сигналов механизм лиганд-управляемых ионных каналов . В этом случае связывание лигандов с рецептором вызывает открытие ионного канала , пропуская один или несколько конкретных типов ионов (например, K + , уже + , Как 2+ ) диффундировать в клетку или из нее.
Изоформы рецептора
[ редактировать ]Классификация
[ редактировать ]С помощью селективных радиоактивно меченных агонистов и антагонистов были определены пять подтипов мускариновых рецепторов, названных М 1 –М 5 (с использованием заглавной буквы М и нижнего индекса). [6] Рецепторы М 1 , М 3 , М 5 связаны с Gq белками , а рецепторы М 2 и М 4 связаны с белками G i/o . [5] Существуют и другие системы классификации. Например, препарат пирензепин является мускариновым антагонистом (снижает эффект АХ), который гораздо более эффективен в отношении рецепторов М 1 , чем в отношении других подтипов. Принятие различных подтипов происходило в числовом порядке, поэтому более ранние источники могут признавать только М 1 и М 2 , подтипы [ нужна ссылка ] в то время как более поздние исследования признают M 3 , M 4 , [1] и совсем недавно M 5 . подтипы [ нужна ссылка ]
Генетические различия
[ редактировать ]Тем временем генетики и молекулярные биологи охарактеризовали пять генов, которые, по-видимому, кодируют мускариновые рецепторы, названные m1-m5 (строчная буква m, без индекса). Они кодируют фармакологические типы М 1 -М 5 . Рецепторы m1 и m2 определяли на основе частичного секвенирования белков рецепторов M1 и M2 . Остальные были найдены путем поиска гомологии с использованием биоинформатических методов.
Разница в G-белках
[ редактировать ]G-белки содержат альфа-субъединицу, которая имеет решающее значение для функционирования рецепторов. Эти субъединицы могут принимать различные формы. Существует четыре широких класса форм G-белка: G s , G i , G q и G 12/13 . [7] Мускариновые рецепторы различаются по G-белку, с которым они связаны, с некоторой корреляцией в зависимости от типа рецептора. G-белки также классифицируются в зависимости от их чувствительности к холерному токсину (СТХ) и коклюшному токсину (ПТХ, коклюшный токсин). G s и некоторые подтипы Gi ( G αt и G αg ) чувствительны к CTX. Только Gi восприимчив к PTX, за исключением одного подтипа Gi ( Gαz ) , который обладает иммунитетом. Кроме того, только при связывании с агонистом те G-белки, которые обычно чувствительны к PTX, также становятся чувствительными к CTX. [8]
Различные субъединицы G-белка по-разному действуют на вторичные мессенджеры, повышая активность фосфолипаз, подавляя цАМФ и так далее.
Из-за сильной корреляции с типом мускариновых рецепторов CTX и PTX являются полезными экспериментальными инструментами для изучения этих рецепторов.
М 1 рецептор
[ редактировать ]Обнаружено, что этот рецептор обеспечивает медленное ВПСП в ганглии постганглионарного нерва. [ нужна ссылка ] , часто встречается в экзокринных железах и в ЦНС. [24] [25]
Преимущественно он обнаруживается связанным с G-белками класса G q , [26] которые используют активацию фосфолипазы C и, следовательно, инозитолтрифосфата и внутриклеточного кальция в качестве сигнального пути. Связанный таким образом рецептор не будет восприимчив к CTX или PTX. Однако было показано, что G i (вызывающий снижение цАМФ ) и G s (вызывающий увеличение цАМФ) участвуют во взаимодействиях в определенных тканях и поэтому могут быть чувствительны к PTX и CTX соответственно.
М 2 рецептор
[ редактировать ]Мускариновые рецепторы М 2 расположены в сердце и легких. В сердце они замедляют частоту сердечных сокращений ниже нормального синусового ритма , замедляя скорость деполяризации . У человека в условиях покоя активность блуждающего нерва доминирует над симпатической активностью. Следовательно, ингибирование рецепторов М 2 (например, атропином) приведет к увеличению частоты сердечных сокращений. Они также умеренно снижают сократительную силу предсердной сердечной мышцы и снижают скорость проводимости атриовентрикулярного узла (АВ-узла). Он также служит для незначительного уменьшения сократительной силы желудочковой мышцы.
Мускариновые рецепторы М 2 действуют через рецептор G i типа, что вызывает снижение цАМФ в клетке, ингибирование потенциалзависимого Са 2+ каналы и увеличение оттока K + , как правило, приводит к эффектам тормозного типа.
М 3 рецептор
[ редактировать ]Мускариновые рецепторы М 3 расположены во многих местах тела. Они расположены в гладких мышцах сосудов, а также в легких. М 3 Поскольку рецептор связан с Gq и опосредует увеличение внутриклеточного кальция, он обычно вызывает сокращение гладких мышц, например, наблюдаемое во время бронхоспазма и мочеиспускания . [27] Однако, что касается сосудистой сети, активация М 3 на эндотелиальных клетках сосудов вызывает повышенный синтез оксида азота , который диффундирует к соседним гладкомышечным клеткам сосудов и вызывает их расслабление , тем самым объясняя парадоксальное влияние парасимпатомиметиков на тонус сосудов и тонус бронхиол. Действительно, прямая стимуляция гладких мышц сосудов М 3 опосредует вазоконстрикцию при заболеваниях, при которых нарушается эндотелий сосудов. [28] Рецепторы М 3 также расположены во многих железах, которые помогают стимулировать секрецию, например, в слюнных железах, а также в других железах организма.
Подобно мускариновому рецептору М1 , рецепторы М3 представляют белки класса Gq собой G - , которые активируют фосфолипазу С и, следовательно, инозитолтрифосфат и внутриклеточный кальций в качестве сигнального пути. [5]
М 4 рецептор
[ редактировать ]Рецепторы М 4 обнаружены в ЦНС.
Рецепторы М 4 действуют через рецепторы Gi , снижая уровень цАМФ в клетке и, таким образом, оказывая в целом ингибирующее действие. Возможен бронхоспазм при стимуляции мускариновыми агонистами.
М 5 рецептор
[ редактировать ]Местоположение рецепторов М 5 недостаточно известно.
Подобно мускариновым рецепторам М1 и М3 , рецепторы М5 связаны с G-белками класса , Gq которые активируют фосфолипазу С и, следовательно, инозитолтрифосфат и внутриклеточный кальций в качестве сигнального пути. [ нужна ссылка ]
Фармакологическое применение
[ редактировать ]Лиганды , нацеленные на mAChR, которые в настоящее время одобрены для клинического использования, включают неселективные антагонисты для лечения болезни Паркинсона . [29] атропин (для расширения зрачка ), скополамин (используется для предотвращения укачивания ) и ипратропий (используется при лечении ХОБЛ ). [4] [30]
См. также
[ редактировать ]- Мускариновый агонист
- Мускариновый антагонист
- Рецептор ацетилхолина (холинергический рецептор)
Ссылки
[ редактировать ]- ^ Эглен Р.М. (июль 2006 г.). «Подтипы мускариновых рецепторов в нейрональных и ненейрональных холинергических функциях». Автономная и аутакоидная фармакология . 26 (3): 219–33. дои : 10.1111/j.1474-8673.2006.00368.x . ПМИД 16879488 .
- ^ Кудлак, Меган; Тади, Прасанна (2024 г.), «Физиология, мускариновые рецепторы» , StatPearls , Остров сокровищ (Флорида): StatPearls Publishing, PMID 32310369 , получено 7 июня 2024 г.
- ^ Исии М., Курачи Ю. (2006). «Мускариновые ацетилхолиновые рецепторы» . Текущий фармацевтический дизайн . 12 (28): 3573–81. дои : 10.2174/138161206778522056 . ПМИД 17073660 . Архивировано из оригинала 5 февраля 2009 г. Проверено 10 апреля 2020 г.
- ^ Перейти обратно: а б Первс, Дейл, Джордж Дж. Августин, Дэвид Фицпатрик, Уильям К. Холл, Энтони-Сэмюэл ЛаМантиа, Джеймс О. Макнамара и Леонард Э. Уайт (2008). Нейронаука. 4-е изд . Синауэр Ассошиэйтс. стр. 122–6. ISBN 978-0-87893-697-7 .
{{cite book}}: CS1 maint: несколько имен: список авторов ( ссылка ) - ^ Перейти обратно: а б с д и ж Цинь К., Донг С., Ву Г, Ламберт Н.А. (август 2011 г.). «Предварительная сборка G(q)-сопряженных рецепторов и G(q)-гетеротримеров» в неактивном состоянии» . Химическая биология природы . 7 (10): 740–7. дои : 10.1038/nchembio.642 . ПМК 3177959 . ПМИД 21873996 .
- ^ Член парламента Колфилда, Бердсолл, штат Нью-Джерси (июнь 1998 г.). «Международный союз фармакологии. XVII. Классификация мускариновых ацетилхолиновых рецепторов» . Фармакологические обзоры . 50 (2): 279–90. ПМИД 9647869 .
- ^ Саймон М.И., член парламента Стратманна, Гаутам Н. (май 1991 г.). «Разнообразие G-белков в передаче сигнала». Наука . 252 (5007): 802–8. Бибкод : 1991Sci...252..802S . дои : 10.1126/science.1902986 . ПМИД 1902986 . S2CID 19110329 .
- ^ Делл'Аква М.Л., Кэрролл Р.К., Перальта Э.Г. (март 1993 г.). «Трансфицированные мускариновые ацетилхолиновые рецепторы m2 соединяются с G альфа i2 и G альфа i3 в клетках яичника китайского хомячка. Активация и десенсибилизация сигнального пути фосфолипазы C» . Журнал биологической химии . 268 (8): 5676–85. дои : 10.1016/S0021-9258(18)53372-X . ПМИД 8449930 .
- ^ Перейти обратно: а б Трипати К.Д. (2004). Основы медицинской фармакологии (5-е изд.). Индия: Jaypee Brothers, медицинские издательства. стр. 890 страниц. ISBN 978-81-8061-187-2 . если в таблице больше ничего не указано
- ^ Смит Р.С., Аранеда Р.К. (декабрь 2010 г.). «Холинергическая модуляция возбудимости нейронов добавочной обонятельной луковицы» . Журнал нейрофизиологии . 104 (6): 2963–74. дои : 10.1152/jn.00446.2010 . ПМК 3007668 . ПМИД 20861438 .
- ^ Егоров А.В., Хамам Б.Н., Франсен Э., Хассельмо М.Е., Алонсо А.А. (ноябрь 2002 г.). «Градуированная постоянная активность нейронов энторинальной коры». Природа . 420 (6912): 173–8. Бибкод : 2002Natur.420..173E . дои : 10.1038/nature01171 . ПМИД 12432392 . S2CID 4302881 .
- ^ Перейти обратно: а б с д и ж г час я дж к л м н тот п д р с т в v В х и С аа аб и объявление но из в ах есть также и аль являюсь а к ап ак с как в В из Позвонил Х.П., Дейл М.М., Риттер Дж.М., Мур П.К. (2003). «Гл. 10». Фармакология (5-е изд.). Эльзевир Черчилль Ливингстон. п. 139. ИСБН 978-0-443-07145-4 .
- ^ Перейти обратно: а б с д и Карлсон, AB; Краус, GP (2019), «статья-19473», Физиология, холинергические рецепторы , Остров сокровищ (Флорида): StatPearls Publishing, PMID 30252390 , получено 7 января 2020 г.
- ^ Перейти обратно: а б Абрамс П., Андерссон К.Е., Буккафуско Дж.Дж., Чаппл С., де Гроат В.К., Фрайер А.Д. и др. (июль 2006 г.). «Мускариновые рецепторы: их распределение и функции в системах организма, а также значение для лечения гиперактивного мочевого пузыря» . Британский журнал фармакологии . 148 (5). Уайли: 565–78. дои : 10.1038/sj.bjp.0706780 . ПМЦ 1751864 . ПМИД 16751797 .
- ^ Перейти обратно: а б Гелардини С., Галеотти Н., Лелли С., Бартолини А. (2001). «Активация рецептора М1 является необходимым условием для аналгезии ареколином». Лекарство . 56 (5–7): 383–5. дои : 10.1016/s0014-827x(01)01091-6 . HDL : 2158/327019 . ПМИД 11482763 .
- ^ Учимура Н., Северная Армения (март 1990 г.). «Мускарин снижает внутреннюю выпрямляющую калиевую проводимость в нейронах прилежащего ядра крысы» . Журнал физиологии . 422 (1): 369–80. doi : 10.1113/jphysicalol.1990.sp017989 . ПМК 1190137 . ПМИД 1693682 . Архивировано из оригинала 30 января 2009 г. Проверено 25 февраля 2008 г.
- ^ Китамура Ю., Канеда Т., Номура Ю. (январь 1991 г.). «Эффекты небрацетама (WEB 1881 FU), нового ноотропа, в качестве мускаринового агониста М1» . Японский журнал фармакологии . 55 (1): 177–80. дои : 10.1254/jjp.55.177 . ПМИД 2041225 .
- ^ Ламех Дж., Бурштейн Э.С., Тейлор Э., Вайнер Д.М., Вановер К.Е., Бонхаус Д.В. (август 2007 г.). «Фармакология N-десметилклозапина». Фармакология и терапия . 115 (2): 223–31. doi : 10.1016/j.pharmthera.2007.05.004 . ПМИД 17583355 .
- ^ Перейти обратно: а б с Эдвардс Фармасьютикалс, Инк.; Belcher Pharmaceuticals, Inc. (май 2010 г.). «ДейлиМед» . Национальная медицинская библиотека США . Проверено 13 января 2013 г.
{{cite journal}}: Для цитирования журнала требуется|journal=( помощь ) - ^ Перейти обратно: а б Сервент Д., Бланше Дж., Мурье Дж., Маркер С., Маркон Э., Фрюшар-Гайяр С. (ноябрь 2011 г.). «Мускариновые токсины». Токсикон . 58 (6–7): 455–63. дои : 10.1016/j.токсикон.2011.08.004 . ПМИД 21906611 .
- ^ Перейти обратно: а б Карлссон Э., Йолкконен М., Мулугета Э., Онали П., Адем А. (сентябрь 2000 г.). «Змеиные токсины с высокой селективностью к подтипам мускариновых рецепторов ацетилхолина». Биохимия . 82 (9–10): 793–806. дои : 10.1016/S0300-9084(00)01176-7 . ПМИД 11086210 .
- ^ Перейти обратно: а б с Уишарт, Дэвид С.; Го, Ань Чи; Олер, Эпонина; Ван, Фел; Анджум, Афия; Питерс, Харрисон; Дизон, Рейнард; Сайида, Зинат; Тянь, Сыян; Ли, Брайан Л.; Бержанский, Марк; Ма, Роберт; Ямамото, Май; Ховел Кастильо, Хуан; Торрес Кальсада, Клаудия; Хиберт Гисбрехт, Микель; Луи, Вики В.; Варшави, Дорна; Варшави, Дорса; Аллен, Дана; Арндт, Дэвид; Кетарпал, Нитья; Сивакумаран, Адхавья; Харфорд, Карксена; Сэнфорд, Селена; Да, Кристен; Цао, Сюань; Будинский, Закари; Лийганд, Янус; Чжан, Лунь; Чжэн, Цзямин; Мандал, Рупасри; Кару, Наама; Дамброва, Майя; Шиот, Хельги Б.; Гаутам, Васук. «Показана метабокарта для ареколина (HMDB0030353)» . База данных метаболомов человека, HMDB . 5.0.
- ^ Мельчиорре С., Анджели П., Ламбрехт Г., Мучлер Э., Пиккио М.Т., Весс Дж. (декабрь 1987 г.). «Антимускариновое действие метоктрамина, нового кардиоселективного антагониста мускариновых рецепторов М-2, отдельно и в сочетании с атропином и галламином». Европейский журнал фармакологии . 144 (2): 117–24. дои : 10.1016/0014-2999(87)90509-7 . ПМИД 3436364 .
- ^ Джонсон, Гордон (2002). PDQ Фармакология (2-е изд.). Гамильтон, Онтарио: BC Decker Inc., стр. 311 страниц. ISBN 978-1-55009-109-0 .
- ^ Ришельсон, Эллиотт (2000). «Холинергическая трансдукция, психофармакология – четвертое поколение прогресса» . Американский колледж нейропсихофармакологии . Проверено 27 октября 2007 г.
- ^ Берфорд Н.Т., Нагорски С.Р. (май 1996 г.). «Активность аденилатциклазы, стимулируемая мускариновым рецептором m1, в клетках яичника китайского хомячка опосредована Gs-альфа и не является следствием активации фосфоинозитидазы C» . Биохимический журнал . 315 (3): 883–8. дои : 10.1042/bj3150883 . ПМЦ 1217289 . ПМИД 8645172 .
- ^ Моро С., Утияма Дж., Чесс-Уильямс Р. (декабрь 2011 г.). «Спонтанная активность уротелия/собственной пластинки уротелия и роль мускариновых рецепторов М3 в опосредовании скорости реакции на растяжение и карбахол». Урология . 78 (6): 1442.e9–15. дои : 10.1016/j.urology.2011.08.039 . ПМИД 22001099 .
- ^ Кейт Паркер; Лоуренс Брантон; Гудман, Луи Сэнфорд; Лазо, Джон С.; Гилман, Альфред (2006). Фармакологическая основа терапии Гудмана и Гилмана (11-е изд.). Нью-Йорк: МакГроу-Хилл. стр. 185 . ISBN 978-0-07-142280-2 .
- ^ Лэнгмид С.Дж., Уотсон Дж., Ривилл С. (февраль 2008 г.). «Мускариновые рецепторы ацетилхолина как мишени лекарств для ЦНС». Фармакология и терапия . 117 (2): 232–43. doi : 10.1016/j.pharmthera.2007.09.009 . ПМИД 18082893 .
- ^ Матера С, Тата AM (2014). «Фармакологические подходы к воздействию на мускариновые рецепторы ацетилхолина». Недавние патенты на открытие лекарств для ЦНС . 9 (2): 85–100. дои : 10.2174/1574889809666141120131238 . ПМИД 25413004 .
Внешние ссылки
[ редактировать ]- Ацетилхолиновые рецепторы (мускариновые)
- Рецепторы + мускариновые в Национальной медицинской библиотеке США по медицинским предметным рубрикам (MeSH)