COVID-19 вакцина
| Описание вакцины | |
|---|---|
| Цель | SARS-CoV-2 |
| Тип вакцины | мРНК, вирусная, инактивированная, белковая |
| Клинические данные | |
| Маршруты администрация | Внутримышечный |
| код АТС | |
| Идентификаторы | |
| ХимическийПаук |
|
| Часть серии о |
| COVID-19 пандемия |
|---|
 |
|
|
|
Вакцина от COVID‑19 — это вакцина, предназначенная для обеспечения приобретенного иммунитета против тяжелого острого респираторного синдрома коронавируса 2 ( SARS-CoV-2 ), вируса, вызывающего коронавирусную болезнь 2019 года ( COVID‑19 ).
До пандемии COVID-19 существовал устоявшийся массив знаний о структуре и функциях коронавирусов, вызывающих такие заболевания, как тяжелый острый респираторный синдром ( ТОРС ) и ближневосточный респираторный синдром ( БВРС ). Эти знания ускорили разработку различных платформ вакцин в начале 2020 года. [ 1 ] Первоначально вакцины против SARS-CoV-2 были направлены на предотвращение симптоматических, часто тяжелых заболеваний. [ 2 ] В 2020 году были разработаны первые вакцины против COVID-19, которые стали доступны населению посредством экстренных разрешений. [ 3 ] и условное одобрение. [ 4 ] [ 5 ] Первоначально большинство вакцин против COVID-19 представляли собой двухдозовые вакцины, за исключением однодозовых вакцин Convidecia [ 6 ] и вакцина «Янссен» от COVID‑19 , [ 3 ] и вакцины с трехдозовым графиком, Рази Ков Парс [ 7 ] и Суверен . [ 8 ] Однако было обнаружено, что иммунитет к вакцинам со временем ослабевает, и людям приходится получать бустерные дозы вакцины для поддержания защиты от COVID-19. [ 3 ]
Вакцины против COVID-19 получили широкое признание за свою роль в уменьшении распространения COVID-19 и уменьшении тяжести и смертности, вызванных COVID-19. [ 3 ] [ 9 ] Согласно исследованию, проведенному в июне 2022 года, вакцины против COVID-19 предотвратили дополнительно от 14,4 до 19,8 миллионов смертей в 185 странах и территориях с 8 декабря 2020 года по 8 декабря 2021 года. [ 10 ] [ 11 ] Многие страны реализовали планы поэтапного распределения, в которых приоритет отдается тем, кто подвергается наибольшему риску осложнений, например, пожилым людям, и тем, кто подвержен высокому риску заражения и передачи, например, медицинским работникам. [ 12 ] [ 13 ]
К частым побочным эффектам вакцин от COVID-19 относятся болезненность, покраснение, сыпь, воспаление в месте инъекции, усталость, головная боль, миалгия (мышечная боль) и артралгия (боль в суставах), которые проходят без медицинского лечения в течение нескольких дней. [ 14 ] [ 15 ] Вакцинация против COVID-19 безопасна для беременных и кормящих грудью людей. [ 16 ]
По состоянию на 1 мая 2024 г. [update] 13,58 , во всем мире было введено По данным официальных отчетов национальных агентств общественного здравоохранения миллиарда доз вакцины против COVID-19 . [ 17 ] К декабрю 2020 года страны предварительно заказали более 10 миллиардов доз вакцины. [ 18 ] при этом около половины доз закупают страны с высоким уровнем дохода, в которых проживает 14% населения мира. [ 19 ]
Несмотря на чрезвычайно быструю разработку эффективных мРНК и вирусных векторных вакцин , мировая справедливость в отношении вакцин не достигнута. разработать и использовать вакцины на основе цельного инактивированного вируса Также рекомендовано (WIV) и белка, особенно для использования в развивающихся странах . [ 20 ] [ 21 ]
2023 года Нобелевская премия по физиологии и медицине была присуждена Каталин Карико и Дрю Вайсману за разработку эффективных мРНК-вакцин против COVID-19. [ 22 ] [ 23 ] [ 24 ]
Фон
-
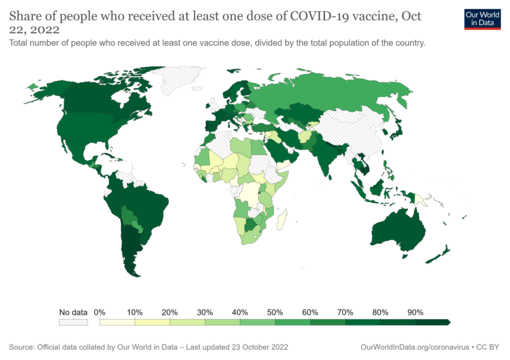
Дозы вакцины против COVID-19, введенные по континентам по состоянию на 11 октября 2021 г. Для вакцин, требующих нескольких доз, учитывается каждая отдельная доза. Поскольку один и тот же человек может получить более одной дозы, количество доз может превышать количество людей в популяции.
-
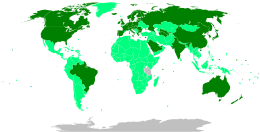
Карта, показывающая долю населения, полностью вакцинированного против COVID-19, по отношению к общей численности населения страны [ примечание 1 ]

До появления COVID-19 вакцина от инфекционного заболевания никогда не производилась менее чем за несколько лет – и не существовало вакцины для предотвращения коронавирусной инфекции у людей. [ 25 ] Однако были произведены вакцины против нескольких болезней животных, вызываемых коронавирусами, включая (по состоянию на 2003 год) вирус инфекционного бронхита птиц, коронавирус собак и коронавирус кошек . [ 26 ] Предыдущие проекты по разработке вакцин против вирусов семейства Coronaviridae , поражающих человека, были направлены на борьбу с тяжелым острым респираторным синдромом (ТОРС) и ближневосточным респираторным синдромом (БВРС). Вакцины против ОРВИ [ 27 ] и БВРС [ 28 ] были протестированы на животных, кроме человека .
Согласно исследованиям, опубликованным в 2005 и 2006 годах, выявление и разработка новых вакцин и лекарств для лечения атипичной пневмонии было в то время приоритетом для правительств и агентств общественного здравоохранения во всем мире. [ 29 ] [ 30 ] [ 31 ] Не существует лекарства или защитной вакцины, доказавшей свою безопасность и эффективность против атипичной пневмонии у людей. [ 32 ] [ 33 ] Также не существует проверенной вакцины против MERS. [ 34 ] Когда БВРС стал широко распространенным, считалось, что существующие исследования атипичной пневмонии могут стать полезной основой для разработки вакцин и терапевтических средств против инфекции БВРС-КоВ. [ 32 ] [ 35 ] По состоянию на март 2020 года существовала одна вакцина против MERS (на основе ДНК), завершившая фазу I клинических испытаний на людях. [ 36 ] и еще три находятся в стадии разработки, причем все они представляют собой вакцины с вектором вируса: две вакцины с аденовирусным вектором (ChAdOx1-MERS, BVRS-GamVac) и одна с вектором MVA (MVA-MERS-S). [ 37 ]
На разработку вакцин, в которых используется неактивный или ослабленный вирус, выращенный в яйцах, обычно уходит более десяти лет. [ 38 ] [ 39 ] Напротив, мРНК — это молекула, которую можно создать быстро, а исследования мРНК для борьбы с болезнями были начаты за десятилетия до пандемии COVID-19 такими учеными, как Дрю Вайсман и Каталин Карико , проводившими испытания на мышах. Компания Moderna начала испытания мРНК-вакцины на людях в 2015 году. [ 38 ] Вирусные векторные вакцины были также разработаны для борьбы с пандемией COVID-19 после того, как ранее технология была одобрена для Эболы. [ 38 ]
Поскольку несколько вакцин против COVID-19 были разрешены или лицензированы для использования, реальная эффективность вакцин (RWE) оценивается с помощью исследований «случай-контроль» и наблюдательных исследований. [ 40 ] [ 41 ] Исследование изучает долговременную защиту от SARS-CoV-2, обеспечиваемую мРНК-вакцинами. [ 42 ] [ 43 ]
Вакцинные технологии
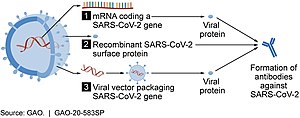
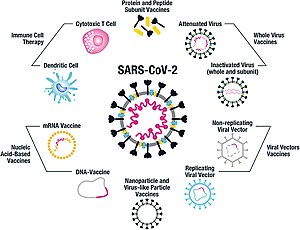
По состоянию на июль 2021 года как минимум девять различных технологических платформ находились в стадии исследований и разработок для создания эффективной вакцины против COVID-19. [ 45 ] [ 46 ] Большинство платформ вакцин-кандидатов в клинических испытаниях ориентированы на белок-шип коронавируса (белок S) и его варианты в качестве первичного антигена инфекции COVID-19. [ 45 ] поскольку белок S вызывает сильный иммунный ответ В-клеток и Т-клеток. [ 47 ] [ 48 ] , также исследуются для разработки вакцин, Однако другие белки коронавируса, такие как нуклеокапсид поскольку они также вызывают устойчивый Т-клеточный ответ, а их гены более консервативны и реже рекомбинируют (по сравнению со Спайком). [ 48 ] [ 49 ] [ 50 ] Будущие поколения вакцин против COVID-19, которые могут быть нацелены на более консервативные области генома, также будут выступать в качестве страховки от проявления катастрофических сценариев, касающихся будущего эволюционного пути SARS-CoV-2, или любой подобной эпидемии/пандемии коронавируса. [ 51 ]
Платформы, разработанные в 2020 году, включали нуклеиновых кислот технологии ( модифицированные нуклеозидами матричную РНК и ДНК ), нереплицирующиеся вирусные векторы , пептиды , рекомбинантные белки , живые аттенуированные вирусы и инактивированные вирусы . [ 25 ] [ 45 ] [ 52 ] [ 53 ]
Многие технологии вакцин, разрабатываемые для лечения COVID-19, не похожи на вакцины против гриппа , а скорее используют стратегии «следующего поколения» для точного воздействия на механизмы заражения COVID-19. [ 45 ] [ 52 ] [ 53 ] В некоторых синтетических вакцинах используется мутация 2P, чтобы зафиксировать белок-шип в его префузионной конфигурации, стимулируя адаптивный иммунный ответ на вирус до того, как он прикрепится к клетке человека. [ 54 ] Разрабатываемые платформы вакцин могут повысить гибкость манипулирования антигенами и эффективность воздействия на механизмы заражения COVID-19 в восприимчивых подгруппах населения, таких как работники здравоохранения, пожилые люди, дети, беременные женщины и люди с ослабленной иммунной системой . [ 45 ] [ 52 ]
мРНК-вакцины

В некоторых вакцинах против COVID-19, таких как вакцины Pfizer–BioNTech и Moderna , используется РНК для стимуляции иммунного ответа . При введении в ткани человека вакцина содержит либо самореплицирующуюся РНК, либо информационную РНК (мРНК), которые заставляют клетки экспрессировать шиповый белок SARS-CoV-2 . Это учит организм тому, как идентифицировать и уничтожить соответствующий патоген. В РНК-вакцинах часто используют модифицированную нуклеозидами информационную РНК . Доставка , которые мРНК достигается путем объединения молекулы в липидные наночастицы защищают цепи РНК и помогают их всасыванию в клетки. [ 55 ] [ 56 ] [ 57 ] [ 58 ]
РНК-вакцины — первые вакцины против COVID-19, разрешенные в Великобритании, США и Европейском Союзе. [ 59 ] [ 60 ] Авторизованными вакцинами этого типа являются Pfizer–BioNTech.
Тяжелые аллергические реакции наблюдаются редко. В декабре 2020 года введение 1 893 360 первых доз вакцины Pfizer–BioNTech против COVID-19 привело к 175 случаям тяжелых аллергических реакций, из которых 21 был анафилаксией . [ 67 ] Из 4 041 396 доз вакцины Moderna против COVID-19 в декабре 2020 г. и январе 2021 г. было зарегистрировано только десять случаев анафилаксии. [ 67 ] Липидные наночастицы (ЛНЧ), скорее всего, были ответственны за аллергические реакции. [ 67 ]
Аденовирусные векторные вакцины
Эти вакцины являются примерами нереплицирующихся вирусных векторных вакцин, использующих оболочку аденовируса , содержащую ДНК, кодирующую белок SARS-CoV-2. [ 68 ] [ 69 ] Вакцины против COVID-19 на основе вирусных векторов нереплицируются, то есть они не создают новых вирусных частиц, а производят только антиген, вызывающий системный иммунный ответ. [ 68 ]
Разрешенными вакцинами этого типа являются вакцина Oxford-AstraZeneca от COVID-19 ,
Convidecia и Janssen представляют собой одноразовые вакцины, которые требуют менее сложной логистики и могут храниться в обычном холодильнике в течение нескольких месяцев. [ 76 ] [ 77 ]
Спутник V использует Ad26 для своей первой дозы, которая такая же, как единственная доза Янссена, и Ad5 для второй дозы, которая такая же, как единственная доза Конвидеции. [ 78 ]
В августе 2021 года разработчики «Спутника V» предложили компании Pfizer протестировать компонент Ad26 (названный его «облегченной» версией), учитывая резкий рост числа случаев Delta. [ 79 ] в качестве стартового выстрела. [ 80 ]
Инактивированные вирусные вакцины
Инактивированные вакцины состоят из вирусных частиц, которые выращиваются в культуре , а затем уничтожаются с помощью таких методов, как нагревание или формальдегид, чтобы потерять способность вызывать заболевания, сохраняя при этом стимуляцию иммунного ответа. [ 81 ]
Инактивированные вирусные вакцины, разрешенные в Китае, включают китайскую вакцину CoronaVac. [ 82 ] [ 83 ] [ 84 ] и Sinopharm BIBP
Субъединичные вакцины
Субъединичные вакцины содержат один или несколько антигенов без введения целых частиц патогена. Вовлеченные антигены часто представляют собой белковые субъединицы , но они могут представлять собой любой фрагмент молекулы возбудителя. [ 91 ]
Разрешенными вакцинами этого типа являются пептидная вакцина EpiVacCorona ,
Вакцина V451 проходила клинические испытания, которые были прекращены после того, как было обнаружено, что вакцина потенциально может привести к неверным результатам последующего тестирования на ВИЧ.
Вакцины на основе вирусоподобных частиц
К разрешенным вакцинам этого типа относится вакцина Novavax COVID‑19 . [ 20 ] [ 104 ]
Другие типы
Дополнительные типы вакцин, которые проходят клинические испытания, включают множественные ДНК-плазмидные вакцины , [ 105 ]
Ученые исследовали, могут ли существующие вакцины от несвязанных заболеваний усилить иммунную систему и снизить тяжесть инфекций COVID-19. [ 114 ] Имеются экспериментальные данные о том, что вакцина БЦЖ от туберкулеза оказывает неспецифическое воздействие на иммунную систему, но нет доказательств эффективности этой вакцины против COVID‑19. [ 115 ]
Список разрешенных вакцин
| Общее имя | Тип (технология) | Страна происхождения | Первая авторизация | Примечания |
|---|---|---|---|---|
| Авторизован более чем в 10 странах. | ||||
| Оксфорд – АстраЗенека | Аденовирусный вектор | Великобритания, Швеция | декабрь 2020 г. | |
| Пфайзер – БиоНТек | РНК | Германия, Соединенные Штаты |
декабрь 2020 г. | Как оригинальные так и варианты Omicron. версии, |
| Янссен (Джонсон и Джонсон) | Аденовирусный вектор | Соединенные Штаты, Нидерланды |
февраль 2021 г. | |
| Современный | РНК | Соединенные Штаты | декабрь 2020 г. | Как оригинальные версии, так и варианты Omicron. |
| Синофарм БИБП | Деактивирован | Китай | июль 2020 г. | |
| Sputnik V | Аденовирусный вектор | Россия | август 2020 г. | |
| КоронаВак | Деактивирован | Китай | август 2020 г. | Низкая эффективность в повторных исследованиях и с некоторыми вариантами. |
| Новавакс | Субъединица / вирусоподобная частица | Соединенные Штаты | декабрь 2021 г. | «Рекомбинантная вакцина наночастиц» [ 116 ] |
| Коваксин | Деактивирован | Индия | январь 2021 г. | |
| Вальнева | Деактивирован | Франция, Австрия | апрель 2022 г. | |
| Санофи–ГСК | Субъединица | Франция, Великобритания |
ноябрь 2022 г. | На основе бета-версии |
| Спутник Лайт | Аденовирусный вектор | Россия | май 2021 г. | |
| Авторизован в 2–10 странах | ||||
| Приглашать | Аденовирусный вектор | Китай | июнь 2020 г. | |
| Синофарм ВИБП | Деактивирован | Китай | февраль 2021 г. | Более низкая эффективность |
| Скорее | Субъединица | Куба | июль 2021 г. | |
| ЭпиВакКорона |
Субъединица | Россия | октябрь 2020 г. | |
| Зифивакс | Субъединица | Китай | март 2021 г. | |
| Суверен 02 | Субъединица | Куба, Иран | июнь 2021 г. | |
| КовиВак | Деактивирован | Россия | февраль 2021 г. | |
| Лекарство | Субъединица | Тайвань | июль 2021 г. | |
| QazCovid-ин | Деактивирован | Казахстан | апрель 2021 г. | |
| Минхай | Деактивирован | Китай | май 2021 г. | Проходит клинические испытания |
| КОВИран Барекат | Деактивирован | Иран | июнь 2021 г. | |
| Суверен Плюс | Субъединица | Куба | август 2021 г. | |
| Корбевакс |
Субъединица | Индия, США | декабрь 2021 г. | |
| Авторизован в 1 стране | ||||
| Китайская академия медицинских наук | Деактивирован | Китай | июнь 2021 г. | |
| ЗиКоВ-Д |
ДНК | Индия | август 2021 г. | |
| ФАХРАВАЦ | Деактивирован | Иран | сентябрь 2021 г. | |
| КОВАКС-19 | Субъединица | Австралия, Иран | октябрь 2021 г. | |
| Рази Ков Парс | Субъединица | Иран | октябрь 2021 г. | |
| Турковац | Деактивирован | Турция | декабрь 2021 г. | |
| Синофарм CNBG | Субъединица | Китай | декабрь 2021 г. | На основе оригинального, бета- и каппа- вариантов. |
| КоВЛП | Вирусоподобная частица | Канада, Великобритания |
февраль 2022 г. | |
| Нора | Субъединица | Иран | март 2022 г. | |
| Скиковионе | Субъединица | Южная Корея | июнь 2022 г. | |
| Вальвакс | РНК | Китай | сентябрь 2022 г. | Получено разрешение на использование в экстренных ситуациях в Индонезии в сентябре 2022 г. |
| iNCOVACC | Аденовирусный вектор | Индия | сентябрь 2022 г. | Назальная вакцина |
| V-01 | Субъединица | Китай | сентябрь 2022 г. | |
| Гемковац | РНК | Индия | Октябрь 2022 г. | Самоамплифицирующаяся РНК-вакцина |
| ИндоВак | Субъединица | Индонезия | Октябрь 2022 г. | |
| ЛУННЫЙ-COV19 | РНК | США, Сингапур | ноябрь 2023 г. | Самоамплифицирующаяся РНК-вакцина |
Способы доставки
Большинство вакцин против коронавируса вводятся инъекционно, при этом изучаются дополнительные методы доставки вакцин для будущих вакцин против коронавируса.
Интраназальный
Интраназальные вакцины воздействуют на иммунитет слизистой оболочки носа , которая является воротами для проникновения вируса в организм. [ 117 ] [ 118 ] Эти вакцины предназначены для стимуляции назальных иммунных факторов , таких как IgA . [ 117 ] Помимо ингибирования вируса, назальные вакцины обеспечивают простоту введения, поскольку при этом не иглы (или боязнь игл ). используются [ 118 ] [ 119 ]
В настоящее время проходят клинические испытания различные интраназальные вакцины против COVID-19. Первой разрешенной интраназальной вакциной была вакцина Рази Ков Парс в Иране в конце октября 2021 года. [ 120 ] Первый вирусный компонент вакцины «Спутник V» был разрешен в России под названием «Спутник Назальный» в апреле 2022 года. [ 121 ] В сентябре 2022 года Индия и Китай одобрили две назальные вакцины против COVID-19 ( iNCOVACC и Convidecia ), которые могут (в качестве ревакцинации) [ 122 ] также уменьшить передачу [ 123 ] [ 124 ] (потенциально через стерилизующий иммунитет). [ 123 ] В декабре 2022 года Китай одобрил вторую интраназальную вакцину в качестве ревакцинации под торговым названием Pneucolin . [ 125 ]
Аутологичный
Aivita Biomedical разрабатывает экспериментальный набор вакцины против COVID-19 на основе аутологичных дендритных клеток , в котором вакцина готовится и инкубируется в месте оказания медицинской помощи с использованием клеток предполагаемого реципиента. [ 126 ] Вакцина проходит небольшие клинические исследования фазы I и фазы II. [ 126 ] [ 127 ] [ 128 ]
Универсальная вакцина
Универсальная вакцина от коронавируса будет эффективна против всех коронавирусов и, возможно, других вирусов. [ 129 ] [ 130 ] Концепция была публично одобрена NIAID директором Энтони Фаучи , вирусологом Джеффри К. Таубенбергером и Дэвидом М. Моренсом. [ 131 ] В марте 2022 года Белый дом опубликовал «Национальный план готовности к COVID-19», в котором рекомендовалось ускорить разработку универсальной вакцины от коронавируса. [ 132 ]
Одна из попыток создания такой вакцины разрабатывается в Армейском исследовательском институте Уолтера Рида . Он использует наночастицы на основе шипового ферритина (SpFN). Клинические испытания этой вакцины начались в апреле 2022 года. [ 133 ] Результаты этого исследования были опубликованы в мае 2024 года. [ 134 ]
Другая стратегия — прикрепить фрагменты вакцины из нескольких штаммов к каркасу из наночастиц . Одна из теорий заключается в том, что против более широкого спектра штаммов можно вакцинировать, нацеливаясь на рецептор-связывающий домен, а не на весь шиповидный белок . [ 135 ]
Формулировка
По состоянию на сентябрь 2020 г. [update]Одиннадцать вакцин-кандидатов, находящихся в стадии клинической разработки, используют адъюванты для повышения иммуногенности. [ 45 ] Иммунологический адъювант — это вещество, приготовленное вместе с вакциной для усиления иммунного ответа на антиген , такой как вирус COVID-19 или вирус гриппа. [ 136 ] В частности, адъювант может использоваться при разработке вакцины-кандидата от COVID-19 для повышения ее иммуногенности и эффективности с целью снижения или предотвращения заражения COVID-19 у вакцинированных лиц. [ 136 ] [ 137 ] Адъюванты, используемые в составе вакцины против COVID-19, могут быть особенно эффективными для технологий, использующих инактивированный вирус COVID-19 и вакцины на основе рекомбинантных белков или векторов. [ 137 ] Соли алюминия, известные как « квасцы », были первым адъювантом, использованным в лицензированных вакцинах, и являются предпочтительным адъювантом примерно в 80% адъювантных вакцин. [ 137 ] Адъювант квасцов инициирует разнообразные молекулярные и клеточные механизмы повышения иммуногенности, включая высвобождение провоспалительных цитокинов. [ 136 ] [ 137 ]
США В июне 2024 года Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) сообщило производителям лицензированных и разрешенных вакцин против COVID-19, что вакцины против COVID-19 (формула 2024–2025 годов), которые будут использоваться в США начиная с осени 2024 года, должны быть моновалентными. Вакцины JN.1. [ 138 ]
Планирование и развитие
С января 2020 года разработка вакцины ускорилась благодаря беспрецедентному сотрудничеству в многонациональной фармацевтической промышленности и между правительствами. [ 45 ]
Оцениваются многочисленные этапы на всем пути разработки, в том числе: [ 25 ] [ 139 ]
- уровень приемлемой токсичности вакцины (ее безопасность),
- нацеленность на уязвимые группы населения,
- необходимость прорыва в эффективности вакцин,
- продолжительность вакцинационной защиты,
- специальные системы доставки (например, перорально или назально, а не путем инъекции),
- режим дозирования,
- стабильность и характеристики хранения,
- разрешение на экстренное использование до официального лицензирования,
- оптимальное производство для масштабирования до миллиардов доз и
- распространение лицензированной вакцины.
Проблемы
При разработке вакцины против COVID-19 возникло несколько уникальных проблем.
Программы общественного здравоохранения [ ВОЗ? ] были описаны как «гонка за вакцинацию людей» вакцинами ранней волны. [ 140 ]
Сроки проведения клинических исследований – обычно это последовательный процесс, занимающий годы – сжимаются до испытаний безопасности, эффективности и дозирования, проводимых одновременно в течение нескольких месяцев, что потенциально ставит под угрозу обеспечение безопасности. [ 141 ] [ 142 ] Например, китайские разработчики вакцин и Китайский центр по контролю и профилактике заболеваний начали свою работу в январе 2020 года. [ 143 ] и к марту они преследовали многочисленных кандидатов в сжатые сроки. [ 141 ] [ 144 ]
Ожидалось, что быстрая разработка и срочность производства вакцины против пандемии COVID-19 повысят риски и частоту неудач в создании безопасной и эффективной вакцины. [ 52 ] [ 53 ] [ 145 ] Кроме того, исследованиям в университетах препятствуют физическое дистанцирование и закрытие лабораторий. [ 146 ] [ 147 ]
Вакцины должны пройти несколько этапов клинических испытаний, чтобы проверить безопасность, иммуногенность , эффективность, уровни доз и побочные эффекты вакцины-кандидата. [ 148 ] [ 149 ] Разработчикам вакцин приходится инвестировать ресурсы на международном уровне, чтобы найти достаточное количество участников для клинических испытаний фазы II–III, когда вирус оказался « движущейся мишенью » изменения скорости передачи внутри страны и внутри страны, что вынуждает компании конкурировать за участников испытаний. [ 150 ]
Организаторы клинических испытаний также могут столкнуться с людьми, не желающими проходить вакцинацию из-за нерешительности в отношении вакцинации. [ 151 ] или неверие в научные данные о технологии вакцин и ее способности предотвращать инфекцию. [ 152 ] Поскольку во время пандемии COVID-19 разрабатываются новые вакцины, лицензирование кандидатов на вакцину против COVID-19 [ ВОЗ? ] требует предоставления полного досье информации о разработке и качестве производства. [ 153 ] [ 154 ] [ 155 ]
Организации
На международном уровне Ускоритель доступа к инструментам борьбы с COVID-19 — это инициатива «Большой двадцатки» и Всемирной организации здравоохранения (ВОЗ), о которой было объявлено в апреле 2020 года. [ 156 ] [ 157 ] Это междисциплинарная структура поддержки, позволяющая партнерам обмениваться ресурсами и знаниями. Он состоит из четырех основных направлений, каждый из которых управляется двумя-тремя сотрудничающими партнерами: вакцины (также называемые « COVAX »), диагностика, терапия и соединитель систем здравоохранения. [ 158 ] В «Плане исследований и разработок (для) нового коронавируса» ВОЗ от апреля 2020 года задокументировано «крупное международное многоцентровое индивидуально рандомизированное контролируемое клиническое исследование», позволяющее «одновременно оценить преимущества и риски каждой многообещающей вакцины-кандидата в течение 3– 6 месяцев из этого времени будут доступны для судебного разбирательства». Коалиция ВОЗ по вакцинам определит приоритеты того, какие вакцины должны пройти клинические испытания фазы II и III, и определит гармонизированные протоколы фазы III для всех вакцин, достигших ключевой стадии испытаний . [ 159 ]
Национальные правительства также принимали участие в разработке вакцины. Канада объявила о финансировании 96 проектов по разработке и производству вакцин в канадских компаниях и университетах, планируя создать «банк вакцин», который можно было бы использовать в случае возникновения новой вспышки коронавируса. [ 160 ] поддерживать клинические испытания и развивать производство и цепочки поставок вакцин. [ 161 ]
Китай предоставил кредиты по низким ставкам одному разработчику вакцины через свой центральный банк и «быстро предоставил компании землю» для строительства производственных предприятий. [ 142 ] Три китайские компании по производству вакцин и научно-исследовательские институты получают поддержку правительства в финансировании исследований, проведении клинических испытаний и производстве. [ 162 ]
В апреле 2020 года правительство Соединенного Королевства сформировало целевую группу по вакцине против COVID-19 , чтобы стимулировать местные усилия по ускоренной разработке вакцины посредством сотрудничества между промышленностью, университетами и государственными учреждениями. Британская целевая группа по вакцинам внесла свой вклад на каждом этапе разработки, от исследований до производства. [ 163 ]
В Соединенных Штатах Управление перспективных биомедицинских исследований и разработок (BARDA), федеральное агентство, финансирующее технологии борьбы с болезнями, объявило об инвестициях в поддержку разработки американской вакцины против COVID-19 и производства наиболее перспективных кандидатов. [ 142 ] [ 164 ] В мае 2020 года правительство объявило о финансировании ускоренной программы под названием Operation Warp Speed . [ 165 ] [ 166 ] К марту 2021 года BARDA профинансировала разработку вакцины против COVID-19 на сумму около 19,3 миллиарда долларов. [ 167 ]
Крупные фармацевтические компании, имеющие опыт масштабного производства вакцин, в том числе Johnson & Johnson , AstraZeneca и GlaxoSmithKline (GSK), сформировали альянсы с биотехнологическими компаниями, правительствами и университетами, чтобы ускорить прогресс в создании эффективных вакцин. [ 142 ] [ 141 ]
Клинические исследования
Клинические исследования вакцин против COVID-19 используют клинические исследования для установления характеристик вакцин против COVID-19. Эти характеристики включают эффективность , результативность и безопасность. По состоянию на ноябрь 2022 г. [update]40 вакцин разрешены как минимум одним национальным регулирующим органом для общественного использования: [ 168 ] [ 169 ]
По состоянию на июнь 2022 г. [update]353 вакцины-кандидата находятся на различных стадиях разработки, из них 135 находятся в стадии клинических исследований , в том числе 38 — в фазе I испытаний , 32 — в фазе I–II испытаний , 39 — в фазе III испытаний и 9 — в фазе IV разработки . [ 168 ]Поствакцинальные осложнения
Поствакцинальные эмболические и тромботические явления, называемые вакцин-индуцированной иммунной тромботической тромбоцитопенией (ВИТТ), [ 170 ] [ 171 ] [ 172 ] [ 173 ] [ 174 ] вакцино-индуцированная протромботическая иммунная тромбоцитопения (ВИПИТ), [ 175 ] тромбоз с синдромом тромбоцитопении (ТТС), [ 176 ] [ 173 ] [ 174 ] вакцино-индуцированная иммунная тромбоцитопения и тромбоз (ВИТТ), [ 174 ] или вакциноассоциированная тромботическая тромбоцитопения (ВАТТ), [ 174 ] — редкие типы синдромов свертывания крови , которые первоначально наблюдались у ряда людей, ранее получивших вакцину Oxford-AstraZeneca от COVID-19 (AZD1222) [ а ] во время пандемии COVID‑19 . [ 175 ] [ 181 ] Впоследствии он был также описан в вакцине Janssen против COVID-19 (Johnson & Johnson), что привело к приостановке ее использования до тех пор, пока не будет проведена повторная оценка ее безопасности. [ 182 ] 5 мая 2022 года FDA опубликовало бюллетень, ограничивающий использование вакцины Янссена очень конкретными случаями из-за дальнейшей переоценки рисков TTS, хотя FDA также заявило в том же бюллетене, что польза от вакцины перевешивает риски. [ 183 ]
В апреле 2021 года компания AstraZeneca и Европейское агентство лекарственных средств (EMA) обновили информацию для медицинских работников об AZD1222, заявив, что «считается правдоподобным» наличие причинно-следственной связи между вакцинацией и возникновением тромбозов в сочетании с тромбоцитопенией и что, «Хотя такие побочные реакции очень редки, они превысили ожидаемые для населения в целом». [ 181 ] [ 184 ] [ 185 ] [ 186 ] AstraZeneca первоначально опровергла эту связь, заявив, что «мы не согласны с тем, что TTS вызван вакциной на общем уровне». Однако в юридических документах, поданных в феврале 2024 года, AstraZeneca наконец признала, что ее вакцина «может в очень редких случаях вызывать СТШ». [ 187 ] [ 188 ]История

SARS-CoV-2 (коронавирус тяжелого острого респираторного синдрома 2), вирус, вызывающий COVID-19 , был выделен в конце 2019 года. [ 189 ] Его генетическая последовательность была опубликована 11 января 2020 года, что вызвало срочные международные меры реагирования, направленные на подготовку к вспышке и ускорение разработки профилактической вакцины против COVID-19. [ 190 ] [ 191 ] [ 192 ] С 2020 года разработка вакцины ускорилась благодаря беспрецедентному сотрудничеству в многонациональной фармацевтической промышленности и между правительствами. [ 193 ] К июню 2020 года корпорации, правительства, международные организации здравоохранения и университетские исследовательские группы вложили десятки миллиардов долларов в разработку десятков кандидатов на вакцины и подготовку к глобальным программам вакцинации для иммунизации против инфекции COVID-19. [ 191 ] [ 194 ] [ 195 ] [ 196 ] По данным Коалиции за инновации в области готовности к эпидемиям (CEPI), географическое распределение разработки вакцины против COVID-19 показывает, что на североамериканские предприятия приходится около 40% активности по сравнению с 30% в Азии и Австралии, 26% в Европе и несколько проектов в Южной Америке и Африке. [ 190 ] [ 193 ]
В феврале 2020 года Всемирная организация здравоохранения (ВОЗ) заявила, что не ожидает, что вакцина против SARS-CoV-2 станет доступной менее чем через 18 месяцев. [ 197 ] Вирусолог Пол Оффит прокомментировал, что, оглядываясь назад, можно сказать, что разработка безопасной и эффективной вакцины за 11 месяцев была выдающимся достижением. [ 198 ] Быстро растущий уровень заражения COVID-19 во всем мире в 2020 году стимулировал международные альянсы и усилия правительств по срочной мобилизации ресурсов для производства нескольких вакцин в сокращенные сроки. [ 199 ] четыре кандидата на вакцину пройдут оценку на людях в марте (см. § Статус испытаний и разрешения на вакцину против COVID-19 ). [ 190 ] [ 200 ]
24 июня 2020 года Китай одобрил вакцину CanSino для ограниченного использования в армии и две инактивированные вирусные вакцины для экстренного использования на профессиях повышенного риска. [ 201 ] 11 августа 2020 года Россия объявила об одобрении своей вакцины «Спутник V» для экстренного использования, хотя месяц спустя лишь небольшое количество вакцины было распространено для использования за пределами третьей фазы испытаний. [ 202 ]
Партнерство Pfizer-BioNTech подало запрос на разрешение на экстренное использование (EUA) в Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) для мРНК-вакцины BNT162b2 (активный ингредиент тозинамеран ) 20 ноября 2020 года. [ 203 ] [ 204 ] Соединенного Королевства 2 декабря 2020 года Агентство по регулированию лекарственных средств и товаров медицинского назначения (MHRA) выдало временное одобрение регулирующих органов на вакцину Pfizer-BioNTech . [ 205 ] [ 206 ] став первой страной, одобрившей вакцину, и первой страной в западном мире, одобрившей использование любой вакцины против COVID-19. [ 207 ] [ 208 ] [ 209 ] По состоянию на 21 декабря 2020 года многие страны и Европейский Союз [ 210 ] разрешил или одобрил вакцину Pfizer-BioNTech от COVID-19. Бахрейн и Объединенные Арабские Эмираты выдали разрешение на экстренный маркетинг вакцины Sinopharm BIBP . [ 211 ] [ 212 ] 11 декабря 2020 г. FDA выдало EUA вакцине Pfizer-BioNTech против COVID-19. [ 213 ] Неделю спустя они выдали EUA для мРНК-1273 (активный ингредиент элазомеран ), вакцины Moderna. [ 214 ] [ 215 ] [ 216 ] [ 217 ]
31 марта 2021 года правительство России объявило, что зарегистрировало первую вакцину от COVID-19 для животных. [ 218 ] Названная Carnivac-Cov , это инактивированная вакцина для плотоядных животных, включая домашних животных, направленная на предотвращение мутаций, возникающих при межвидовой передаче SARS-CoV-2. [ 219 ]
В октябре 2022 года в Китае началось введение пероральной вакцины, разработанной CanSino Biologics с использованием ее модели аденовируса. [ 220 ]
Несмотря на наличие мРНК и вирусных векторных вакцин , мировая справедливость в отношении вакцин не достигнута. продолжать разработку и использование цельноинактивированных вирусных (WIV) и белковых было рекомендовано вакцин, особенно для использования в развивающихся странах . Для смягчения дальнейших волн пандемии [ 221 ] [ 222 ]В ноябре 2021 года Полные нуклеотидные последовательности вакцин AstraZeneca и Pfizer/BioNTech были опубликованы Агентством по регулированию лекарственных средств и товаров медицинского назначения Великобритании в ответ на запрос о свободе информации . [ 223 ] [ 224 ]
Эффективность

Данные об использовании вакцин во время пандемии показывают, что вакцинация может снизить инфекцию и наиболее эффективна для предотвращения тяжелых симптомов и смерти от COVID-19, но менее эффективна для предотвращения легкой формы COVID-19. Эффективность со временем снижается, но ее можно поддерживать с помощью бустеров. [ 226 ] В 2021 году CDC сообщил, что у непривитых людей вероятность госпитализации в 10 раз выше, а вероятность смерти — в 11 раз выше, чем у полностью вакцинированных людей. [ 227 ] [ 228 ]
CDC сообщил, что эффективность вакцины упала с 91% против Альфа до 66% против Дельты. [ 229 ] Один эксперт заявил, что «те, кто заразился после вакцинации, по-прежнему не болеют и не умирают, как это происходило до вакцинации». [ 230 ] К концу августа 2021 года на вариант Дельта приходилось 99 процентов случаев заболевания в США, и было обнаружено, что он удваивает риск тяжелого заболевания и госпитализации для тех, кто еще не был вакцинирован. [ 231 ]
По данным исследования ECDC , проведенного в ноябре 2021 года, с момента начала внедрения вакцинации в европейском регионе было спасено 470 000 жизней в возрасте старше 60 лет. [ 232 ]
10 декабря 2021 года Агентство безопасности здравоохранения Великобритании сообщило, что предварительные данные указывают на 20–40-кратное снижение нейтрализующей активности Омикрона сыворотками пациентов, получивших 2 дозы вакцины Pfizer, по сравнению с более ранними штаммами. После бустерной дозы (обычно мРНК-вакцины) [ 233 ] Эффективность вакцины против симптоматических заболеваний составляла 70–75% , а эффективность против тяжелых заболеваний ожидалась выше. [ 234 ]
По данным CDC на начало декабря 2021 года, «у непривитых взрослых вероятность умереть от COVID-19 была примерно в 97 раз выше, чем у полностью вакцинированных людей, получивших ревакцинацию». [ 235 ]
Метаанализ, изучающий различия в вакцинах против COVID-19 у людей с ослабленным иммунитетом, показал, что люди с ослабленной иммунной системой менее способны вырабатывать нейтрализующие антитела. Например, реципиентам трансплантатов органов необходимо три вакцины для достижения сероконверсии . [ 236 ] Исследование серологического ответа на мРНК-вакцины среди пациентов с лимфомой, лейкемией и миеломой показало, что у четверти пациентов не вырабатываются измеримые антитела, что зависит от типа рака. [ 237 ]
В феврале 2023 года систематический обзор, опубликованный в The Lancet, показал, что защита, обеспечиваемая инфекцией, сравнима с защитой от вакцинации, хотя и с повышенным риском тяжелого заболевания и смерти от заболевания, возникшего в результате первоначального заражения. [ 238 ]
Исследование, проведенное CDC в январе 2024 года, показало, что своевременное применение вакцин может снизить риск инсультов, тромбов и сердечных приступов, связанных с COVID-19, у людей в возрасте 65 лет и старше или с состоянием, которое делает их более уязвимыми к вирусу. указанные условия. [ 239 ] [ 240 ]Анализ с участием более 20 миллионов взрослых показал, что у вакцинированных людей был меньший риск длительного заболевания COVID по сравнению с теми, кто не получил вакцину от COVID-19. [ 241 ] [ 242 ]
Продолжительность иммунитета
По состоянию на 2021 год имеющиеся данные показывают, что полностью вакцинированные люди и лица, ранее инфицированные SARS-CoV-2, имеют низкий риск последующего заражения в течение как минимум шести месяцев. [ 243 ] [ 244 ] [ 245 ] Недостаточно данных для определения порога титра антител, который указывает на то, что человек защищен от инфекции. [ 243 ] Многочисленные исследования показывают, что титры антител связаны с защитой на популяционном уровне, но индивидуальные титры защиты остаются неизвестными. [ 243 ] Для некоторых групп населения, таких как пожилые люди и люди с ослабленным иммунитетом , уровень защиты может снизиться как после вакцинации, так и после заражения. [ 243 ] Имеющиеся данные указывают на то, что уровень защиты может не быть одинаковым для всех вариантов вируса . [ 243 ]
По состоянию на декабрь 2021 года не существует одобренных или одобренных FDA тестов, которые поставщики медицинских услуг или общественность могли бы использовать для определения надежной защиты человека от инфекции. [ 243 ]
По состоянию на март 2022 года защита пожилых жителей от тяжелых заболеваний, госпитализации и смерти в английских домах престарелых была высокой сразу после вакцинации, но защита значительно снизилась в течение нескольких месяцев после вакцинации. [ 246 ] Защита среди более молодого персонала домов престарелых снижалась гораздо медленнее. [ 246 ] Регулярные прививки рекомендуются пожилым людям, а прививки для жителей домов престарелых каждые шесть месяцев кажутся разумными. [ 246 ]
Центры США по контролю и профилактике заболеваний (CDC) рекомендуют ввести четвертую дозу мРНК-вакцины Pfizer с марта 2022 года. [update] для «некоторых лиц с ослабленным иммунитетом и людей старше 50 лет». [ 247 ] [ 248 ]
Уклонение от иммунитета по вариантам
В отличие от других исследованных ранее вариантов, вариант SARS-CoV-2 Omicron [ 249 ] [ 250 ] [ 251 ] [ 252 ] [ 253 ] и его подварианты BA.4/5 [ 254 ] избежали иммунитета, вызванного вакцинами, что может привести к прорывным инфекциям, несмотря на недавнюю вакцинацию. Тем не менее считается, что вакцины обеспечивают защиту от тяжелых заболеваний, госпитализаций и смертей из-за Омикрона. [ 255 ]
Корректировка вакцинации
В июне 2022 года компании Pfizer и Moderna разработали бивалентные вакцины для защиты от дикого типа SARS-CoV-2 и варианта Omicron. Бивалентные вакцины хорошо переносятся и обеспечивают иммунитет к Омикрону, превосходящий предыдущие мРНК-вакцины. [ 256 ] США В сентябре 2022 года Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) разрешило использование бивалентных вакцин в США. [ 257 ] [ 258 ] [ 259 ]
В июне 2023 года FDA рекомендовало производителям обновить состав вакцин против COVID-19 для использования в США на 2023–2024 годы, сделав его моновалентной вакциной против COVID-19 с использованием линии XBB.1.5 варианта Омикрон. [ 260 ] [ 261 ] В июне 2024 года FDA рекомендовало производителям обновить состав вакцин против COVID-19 для использования в США на 2024–2025 годы, сделав его моновалентной вакциной против COVID-19 с использованием линии JN.1. [ 262 ]Эффективность против передачи
По состоянию на 2022 год полностью вакцинированные лица с прорывной инфекцией дельта-вариантом SARS-CoV-2 (B.1.617.2) будут иметь пиковую вирусную нагрузку, аналогичную невакцинированным случаям, и могут передавать инфекцию в домашних условиях. [ 263 ]
Смешивайте и сочетайте
Согласно исследованиям, комбинация двух разных вакцин против COVID-19, также называемая перекрестной вакцинацией или методом «смешай и сопоставь», обеспечивает защиту, эквивалентную защите мРНК-вакцин, включая защиту от варианта Дельта . У людей, получающих комбинацию двух разных вакцин, возникает сильная иммунная реакция с побочными эффектами, не хуже, чем те, которые вызываются стандартными схемами вакцинации. [ 264 ] [ 265 ]
Побочные эффекты
Для большинства людей побочные эффекты вакцин против COVID-19, также называемые побочными эффектами , легкие, и их можно контролировать в домашних условиях. Побочные эффекты вакцинации против COVID-19 аналогичны побочным эффектам других вакцин, а тяжелые побочные эффекты встречаются редко. [ 266 ] [ 267 ] Побочные эффекты вакцины выше, чем у плацебо, но в группах плацебо испытаний вакцины по-прежнему сообщалось о побочных эффектах, которые можно объяснить эффектом ноцебо . [ 268 ]
Все вакцины, которые вводятся внутримышечно , включая вакцины от COVID-19, имеют побочные эффекты, связанные с легкой травмой, связанной с процедурой, и попаданием в организм инородного вещества. [ 269 ] К ним относятся болезненность, покраснение, сыпь и воспаление в месте инъекции. Другие распространенные побочные эффекты включают усталость, головную боль, миалгию (мышечные боли) и артралгию (боль в суставах), которые обычно проходят без медицинского лечения в течение нескольких дней. [ 14 ] [ 15 ] Как и в случае любой другой вакцины, у некоторых людей имеется аллергия на один или несколько ингредиентов вакцины против COVID-19. Типичные побочные эффекты сильнее и чаще встречаются у молодых людей и при последующих дозах, и до 20% людей сообщают о разрушительном уровне побочных эффектов после второй дозы мРНК-вакцины. [ 270 ] Эти побочные эффекты встречаются реже или слабее у инактивированных вакцин . [ 270 ] связанное с вакцинацией против COVID-19, Увеличение лимфатических узлов, происходит у 11,6% тех, кто получил одну дозу вакцины, и у 16% тех, кто получил две дозы. [ 271 ]
Эксперименты на мышах показывают, что внутримышечные инъекции наночастиц липидного наполнителя (неактивного вещества, служащего носителем или средой) вызывают попадание частиц в плазму крови и многие органы, причем более высокие концентрации обнаруживаются в печени, а более низкие концентрации - в селезенке, надпочечниках. и яичники. Самая высокая концентрация наночастиц была обнаружена в самом месте инъекции. [ 272 ]
Вакцинация против COVID-19 безопасна для кормящих грудью людей. [ 16 ] временных изменениях менструального цикла Сообщалось о у молодых женщин. Однако эти изменения «невелики по сравнению с естественными изменениями и быстро обращаются вспять». [ 273 ] В одном исследовании у женщин, получивших обе дозы двухдозовой вакцины в течение одного и того же менструального цикла (атипичная ситуация), следующая менструация может начаться на пару дней позже. У них примерно в два раза выше обычный риск клинически значимой задержки (около 10% этих женщин по сравнению с примерно 4% непривитых женщин). [ 273 ] Продолжительность цикла возвращается к норме после двух менструальных циклов после вакцинации. [ 273 ] Женщины, получившие дозы в отдельных циклах, имели примерно такое же естественное изменение продолжительности цикла, как и непривитые женщины. [ 273 ] Сообщалось о других временных менструальных эффектах, таких как более сильное, чем обычно, менструальное кровотечение после вакцинации. [ 273 ]
Серьезные побочные эффекты, связанные с вакцинами против COVID-19, как правило, редки, но представляют большой интерес для общественности. [ 274 ] Официальные базы данных о зарегистрированных нежелательных явлениях включают:
- Всемирной здравоохранения организации VigiBase ;
- США Система отчетности о побочных эффектах вакцин (VAERS);
- Соединенного Королевства Схема желтой карточки ;
- Европейского по лекарственным средствам агентства Система EudraVigilance , которая обеспечивает регулярную передачу данных о предполагаемых побочных реакциях на лекарства, возникающих в ЕС, в Центр мониторинга ВОЗ в Уппсале . [ 275 ]
Повышенная осведомленность общественности об этих системах отчетности и дополнительные требования к отчетности в соответствии с правилами разрешения на экстренное использование FDA США привели к увеличению количества сообщений о побочных эффектах. [ 276 ] Серьезные побочные эффекты являются постоянной областью изучения, и были выделены ресурсы, чтобы попытаться лучше понять их. [ 277 ] [ 278 ] [ 279 ] Исследования в настоящее время показывают, что частота и тип побочных эффектов менее опасны, чем инфекция. Например, хотя вакцинация может вызвать некоторые побочные эффекты, последствия инфекции могут быть еще хуже. Неврологические побочные эффекты от заражения COVID-19 в сотни раз более вероятны, чем от вакцинации. [ 280 ]
Документированные редкие серьезные эффекты включают:
- анафилаксия , тяжелый тип аллергической реакции . [ 281 ] Анафилаксия поражает одного человека на 250 000–400 000 введенных доз. [ 270 ] [ 282 ]
- тромбы ( тромбоз ). [ 281 ] Эти вызванные вакциной иммунные тромбоцитопении и тромбозы связаны с вакцинами, использующими аденовирусную систему (Janssen и Oxford-AstraZeneca). [ 281 ] Они затрагивают примерно одного человека на 100 000 человек. [ 270 ]
- миокардит и перикардит или воспаление сердца. [ 281 ] Существует редкий риск развития миокардита (воспаления сердечной мышцы) или перикардита (воспаления оболочки, покрывающей сердце) после введения мРНК вакцины против COVID-19 (Moderna или Pfizer-BioNTech). Риск развития миокардита после вакцинации от COVID-19 оценивается в 0,3–5 случаев на 100 000 человек, причем самый высокий риск приходится на молодых мужчин. [ 283 ] В израильском общенациональном популяционном исследовании (в котором применялась исключительно вакцина Pfizer-BioNTech) уровень заболеваемости миокардитом составил 54 случая на 2,5 миллиона получателей вакцины, при общем показателе заболеваемости 2 случая на 100 000 человек. при этом наибольшая заболеваемость наблюдается у молодых мужчин (в возрасте от 16 до 29 лет) — 10 случаев на 100 000 получателей вакцины. Из наблюдаемых случаев миокардита 76% были легкой степени тяжести, при этом в течение 83-дневного периода наблюдения было зарегистрировано один случай кардиогенного шока (сердечная недостаточность) и один случай смерти (у человека с ранее существовавшим заболеванием сердца). [ 284 ] Вакцины против COVID-19 могут защитить от миокардита, вызванного последующей инфекцией COVID-19. [ 285 ] Риск развития миокардита и перикардита значительно выше (до 11 раз выше по сравнению с миокардитом) после заражения COVID-19 по сравнению с вакцинацией против COVID-19, за исключением, возможно, молодых мужчин (менее 40 лет), у которых может быть более высокий риск миокардита после второй мРНК-вакцины Moderna (дополнительно 97 случаев миокардита на 1 миллион привитых). [ 285 ]
- тромботическая тромбоцитопения и другие аутоиммунные заболевания, о которых сообщалось как о нежелательных явлениях после вакцины COVID-19. [ 286 ]
Имеются редкие сообщения о субъективных изменениях слуха, включая шум в ушах , после вакцинации. [ 282 ] [ 287 ] [ 288 ] [ 289 ]
Общество и культура
Распределение
Примечание к таблице в этом разделе: количество и процент людей, получивших хотя бы одну дозу вакцины от COVID-19 (если не указано иное). Может включать вакцинацию неграждан, что может привести к тому, что общая численность местного населения превысит 100%. Таблица обновляется ежедневно ботом. [ примечание 2 ]
По состоянию на 3 января 2024 г. [update]Во всем мире было введено 13,53 миллиарда доз вакцины против COVID-19, при этом 70,6 процента населения планеты получили хотя бы одну дозу. [ 291 ] [ 292 ] 4,19 Хотя тогда ежедневно вводилось миллиона вакцин, только 22,3 процента людей в странах с низкими доходами получили хотя бы первую вакцину к сентябрю 2022 года, согласно официальным отчетам национальных агентств здравоохранения, которые сопоставляются журналом «Наш мир в данных» . [ 293 ]
Во время пандемии с быстрыми темпами и масштабами случаев заболевания COVID-19 в 2020 году международные организации, такие как Всемирная организация здравоохранения (ВОЗ) и Коалиция за инновации в области готовности к эпидемиям (CEPI), разработчики вакцин, правительства и промышленность оценили распространение возможного заражения. вакцина). [ 294 ] Отдельные страны, производящие вакцину, можно убедить отдать предпочтение тому, кто предложит самую высокую цену за ее производство, или предоставить первоклассный сервис своей стране. [ 295 ] [ 296 ] [ 297 ] Эксперты подчеркивают, что лицензированные вакцины должны быть доступны и доступны по цене для людей, находящихся на переднем крае здравоохранения и наиболее нуждающихся в них. [ 295 ] [ 297 ]
В апреле 2020 года сообщалось, что Великобритания согласилась работать с 20 другими странами и глобальными организациями, включая Францию, Германию и Италию, чтобы найти вакцину и поделиться результатами, и что граждане Великобритании не получат преференциального доступа к каким-либо новым вакцинам. Вакцины против COVID-19 разработаны британскими университетами, финансируемыми налогоплательщиками. [ 298 ] Несколько компаний планировали сначала производить вакцину по искусственно заниженным ценам , а затем повышать цены для повышения прибыльности позже, если потребуются ежегодные вакцинации и по мере того, как страны будут создавать запасы для будущих нужд. [ 297 ]
ВОЗ поставила цель вакцинировать 40% населения всех стран к концу 2021 года и 70% к середине 2022 года. [ 299 ] но многие страны не достигли цели в 40% к концу 2021 года. [ 300 ] [ 301 ]-
Доля людей, получивших хотя бы одну дозу вакцины против COVID-19, по отношению к общей численности населения страны. Дата указана на карте. Источник общего доступа .
-
Дозы вакцины против COVID-19, введённые на 100 человек по странам. Дата указана на карте. Источник общего доступа .
Доступ
Страны имеют крайне неравный доступ к вакцине от COVID-19. Справедливость вакцин не была достигнута или даже приблизительна. Неравенство нанесло вред как странам с плохим доступом, так и странам с хорошим доступом. [ 20 ] [ 21 ] [ 302 ]
Страны обязались закупить дозы вакцины против COVID-19 до того, как они станут доступны. Хотя страны с высоким уровнем дохода составляют лишь 14% мирового населения, по состоянию на 15 ноября 2020 года они заключили контракт на покупку 51% всех предварительно проданных доз. Некоторые страны с высоким уровнем дохода закупили больше доз, чем необходимо для вакцинации всего населения. [ 19 ]

В январе 2021 года генеральный директор ВОЗ Тедрос Адханом Гебрейесус предупредил о проблемах со справедливым распределением: «Более 39 миллионов доз вакцины в настоящее время введено как минимум в 49 странах с более высоким доходом. Всего 25 доз было введено в одной стране с самым низким доходом». страна. Не 25 миллионов; не 25 тысяч, а всего 25». [ 303 ]

В марте 2021 года выяснилось, что США пытались убедить Бразилию не закупать вакцину от COVID-19 «Спутник V» , опасаясь «российского влияния» в Латинской Америке. [ 304 ] Сообщается, что некоторым странам, вовлеченным в давние территориальные споры, доступ к вакцинам был заблокирован конкурирующими странами; Палестина обвинила Израиль в блокировании поставок вакцины в сектор Газа , а Тайвань предположил, что Китай препятствовал его усилиям по закупке доз вакцины. [ 305 ] [ 306 ] [ 307 ]
Одна доза вакцины против COVID-19 от AstraZeneca будет стоить 47 египетских фунтов (EGP), а власти продают их по цене от 100 до 200 египетских фунтов. В отчете Фонда Карнеги за международный мир указывается, что уровень бедности в Египте составляет около 29,7 процента, что составляет примерно 30,5 миллиона человек, и утверждается, что около 15 миллионов египтян не смогут получить доступ к такой роскоши, как вакцинация. Адвокат по правам человека Халед Али подал иск против правительства, заставив его предоставить бесплатную вакцинацию всем представителям общественности. [ 308 ]
По словам иммунолога Энтони Фаучи , мутантные штаммы вируса и ограниченное распространение вакцин создают постоянные риски, и он сказал: «Мы должны вакцинировать весь мир, а не только нашу собственную страну». [ 309 ] Эдвард Бергмарк и Арик Виерсон призывают к глобальным усилиям по вакцинации и пишут, что менталитет более богатых стран «я прежде всего» может в конечном итоге иметь неприятные последствия, поскольку распространение вируса в более бедных странах приведет к появлению большего количества вариантов, против которых вакцин может быть меньше. эффективен. [ 310 ]
В марте 2021 года США, Великобритания, государства-члены Европейского Союза и некоторые другие члены Всемирной торговой организации (ВТО) заблокировали попытку более чем восьмидесяти развивающихся стран отказаться от патентных прав на вакцину против COVID-19 в попытке увеличить производство. вакцин для бедных стран. [ 311 ] 5 мая 2021 года правительство США под руководством президента Джо Байдена объявило, что поддерживает отказ от защиты интеллектуальной собственности на вакцины против COVID-19. [ 312 ] Члены Европейского парламента поддержали предложение, требующее временной отмены прав интеллектуальной собственности на вакцины против COVID-19. [ 313 ]

На заседании в апреле 2021 года комитет по чрезвычайным ситуациям Всемирной организации здравоохранения рассмотрел обеспокоенность по поводу сохраняющегося неравенства в глобальном распределении вакцин. [ 314 ] Хотя 9 процентов населения мира проживает в 29 беднейших странах, по состоянию на май 2021 года эти страны получили лишь 0,3% всех вакцин. [ 315 ] В марте 2021 года бразильское журналистское агентство Agência Pública сообщило, что в стране вакцинировано примерно вдвое больше людей, объявивших себя белыми, чем чернокожих, и отметило, что смертность от COVID-19 выше среди чернокожего населения. [ 316 ]
В мае 2021 года ЮНИСЕФ обратился к промышленно развитым странам с призывом объединить свои избыточные мощности по производству вакцины против COVID-19, чтобы восполнить дефицит в 125 миллионов доз в программе COVAX . Программа в основном опиралась на вакцину Oxford-AstraZeneca против COVID-19 , произведенную Индийским институтом сывороток , который столкнулся с серьезными проблемами с поставками из-за возросшей внутренней потребности в вакцинах в Индии в период с марта по июнь 2021 года. Лишь ограниченное количество вакцин может быть эффективно распределено. а нехватка вакцин в Южной Америке и некоторых частях Азии вызвана отсутствием целесообразных пожертвований со стороны более богатых стран. Международные организации по оказанию помощи назвали Непал, Шри-Ланку и Мальдивы, а также Аргентину, Бразилию и некоторые части Карибского бассейна проблемными областями, где не хватает вакцин. В середине мая 2021 года ЮНИСЕФ также раскритиковал тот факт, что большинство предложенных пожертвований вакцин Moderna и Pfizer не планировалось доставить до второй половины 2021 года или начала 2022 года. [ 317 ]

В июле 2021 года главы Группы Всемирного банка, Международного валютного фонда, Всемирной организации здравоохранения и Всемирной торговой организации заявили в совместном заявлении: «Поскольку многие страны борются с новыми вариантами и третьей волной COVID-19, инфекций, ускорение доступа к вакцинам становится еще более важным для повсеместного прекращения пандемии и достижения широкого экономического роста. Мы глубоко обеспокоены ограниченностью вакцин, терапевтических средств, диагностики и поддержки поставок, доступных для развивающихся стран». [ 318 ] [ 319 ] В июле 2021 года издание BMJ сообщило, что страны выбросили более 250 000 доз вакцины, поскольку предложение превысило спрос, а строгие законы не позволяли совместно использовать вакцины. [ 320 ] Опрос, проведенный The New York Times, показал, что более миллиона доз вакцины были выброшены в десяти штатах США, потому что федеральные правила запрещают их отзыв, предотвращая их перераспределение за границу. [ 321 ] Кроме того, страны-получатели часто не могут вводить дозы достаточно быстро, и в конечном итоге их приходится выбрасывать. [ 322 ] Чтобы помочь решить эту проблему, премьер-министр Индии Нарендра Моди объявил, что они сделают свою платформу управления цифровой вакцинацией CoWIN открытой для мирового сообщества. Он также объявил, что Индия также выпустит исходный код приложения для отслеживания контактов Aarogya Setu для разработчиков по всему миру. Около 142 стран, в том числе Афганистан, Бангладеш, Бутан, Мальдивы, Гайана, Антигуа и Барбуда, Сент-Китс и Невис и Замбия, выразили заинтересованность в приложении для управления COVID. [ 323 ] [ 324 ]
Amnesty International и Oxfam International раскритиковали поддержку монополий на вакцины правительствами стран-производителей, отметив, что это резко увеличивает цену дозы в пять раз, а зачастую и намного больше, создавая экономический барьер для доступа к вакцинам для бедных стран. [ 325 ] [ 326 ] « Врачи без границ» также критиковали монополии на вакцины и неоднократно призывали к их приостановке, поддерживая отказ от ТРИПС . Отказ был впервые предложен в октябре 2020 года и получил поддержку большинства стран, но был отложен из-за противодействия ЕС (особенно Германии; крупные страны ЕС, такие как Франция, Италия и Испания, поддерживают исключение). [ 327 ] Великобритания, Норвегия и Швейцария и другие. MSF призвала провести День действий в сентябре 2021 года, чтобы оказать давление на ВТО ноябрьскую встречу министров , на которой, как ожидается, будет обсуждаться отказ от прав на интеллектуальную собственность по ТРИПС . [ 328 ] [ 329 ] [ 330 ]

В августе 2021 года, чтобы уменьшить неравномерное распределение между богатыми и бедными странами, ВОЗ призвала ввести мораторий на ревакцинацию как минимум до конца сентября. Однако в августе правительство США объявило о планах предложить ревакцинацию через восемь месяцев после первоначального курса населению в целом, начиная с приоритетных групп. Перед объявлением ВОЗ резко раскритиковала такое решение, сославшись на отсутствие доказательств необходимости ревакцинации, за исключением пациентов с особыми заболеваниями. В то время охват вакцинацией хотя бы одной дозой составлял 58% в странах с высоким уровнем дохода и только 1,3% в странах с низким доходом, а 1,14 миллиона американцев уже получили несанкционированную ревакцинацию. Официальные лица США утверждали, что снижение эффективности против легких и среднетяжелых заболеваний может указывать на снижение защиты от тяжелых заболеваний в ближайшие месяцы. Израиль, Франция, Германия и Великобритания также начали планировать бустеры для конкретных групп. [ 331 ] [ 332 ] [ 333 ] более 140 бывших мировых лидеров и нобелевских лауреатов, в том числе бывший президент Франции Франсуа Олланд , бывший премьер-министр Великобритании Гордон Браун , бывший премьер-министр Новой Зеландии Хелен Кларк и профессор Джозеф Стиглиц В сентябре 2021 года к кандидатам обратились . стать следующим канцлером Германии, который выступит за отмену правил интеллектуальной собственности на вакцины от COVID-19 и передачу вакцинных технологий. [ 334 ] В ноябре 2021 года профсоюзы медсестер в 28 странах подали официальную апелляцию в Организацию Объединенных Наций по поводу отказа Великобритании, ЕС, Норвегии, Швейцарии и Сингапура временно отказаться от патентов на вакцины против COVID-19. [ 335 ]
Во время своей первой международной поездки президент Перу выступил Педро Кастильо на семьдесят шестой сессии Генеральной Ассамблеи Организации Объединенных Наций 21 сентября 2021 года, предложив создать международный договор, подписанный мировыми лидерами и фармацевтическими компаниями, гарантирующий универсальную вакцину. доступ, утверждая, что «Борьба с пандемией показала нам неспособность международного сообщества сотрудничать в соответствии с принципом солидарности». [ 336 ] [ 337 ]
Оптимизация общественной пользы от вакцинации может выиграть от стратегии, адаптированной к состоянию пандемии, демографии страны, возрасту реципиентов, доступности вакцин и индивидуальному риску тяжелого заболевания. [ 13 ] В Великобритании интервал между основной и ревакцинационной дозами был увеличен, чтобы вакцинировать как можно больше людей как можно раньше. [ 338 ] Многие страны начинают делать дополнительную прививку людям с ослабленным иммунитетом. [ 339 ] [ 340 ] и пожилые люди, [ 341 ] и исследования предсказывают дополнительную выгоду от персонализации доз вакцины в условиях ограниченной доступности вакцины, когда волна вирусных вариантов вируса поражает страну. [ 342 ]
Несмотря на чрезвычайно быструю разработку эффективных вакцин на основе мРНК и вирусных векторов , равноправие по вакцинам не было достигнуто. [ 20 ] Всемирная организация здравоохранения призвала к середине 2022 года вакцинировать 70 процентов населения планеты, однако по состоянию на март 2022 года, по оценкам, только один процент из 10 миллиардов доз, введенных во всем мире, был введен в странах с низким уровнем дохода. [ 343 ] Для заполнения пробелов в доступе к вакцинам могут потребоваться дополнительные 6 миллиардов прививок, особенно в развивающихся странах. Учитывая прогнозируемую доступность новых вакцин, цельного инактивированного вируса рекомендуется также разработать и использовать вакцины на основе (WIV) и белков. Такие организации, как Сеть производителей вакцин в развивающихся странах, могли бы помочь поддержать производство таких вакцин в развивающихся странах с более низкими производственными затратами и большей легкостью внедрения. [ 20 ] [ 344 ]
Хотя вакцины существенно снижают вероятность и тяжесть инфекции, полностью вакцинированные люди по-прежнему могут заразиться и распространить COVID-19. [ 345 ] Агентства общественного здравоохранения рекомендовали вакцинированным людям продолжать использовать профилактические меры (носить маски, соблюдать социальную дистанцию, мыть руки), чтобы избежать заражения других, особенно уязвимых людей, особенно в районах с высокой распространенностью среди населения. Правительства указали, что такие рекомендации будут сокращены по мере увеличения уровня вакцинации и снижения распространения среди населения. [ 346 ]
Экономика
Более того, неравное распределение вакцин приведет к углублению неравенства и увеличению разрыва между богатыми и бедными, а также обратит вспять десятилетия с таким трудом достигнутого прогресса в области человеческого развития.
— Организация Объединенных Наций, Вакцины против COVID: рост неравенства и уязвимость миллионов людей [ 347 ]
Неравенство в отношении вакцин наносит ущерб мировой экономике, нарушая глобальную цепочку поставок . [ 302 ] Большинство вакцин предназначалось для богатых стран; по состоянию на сентябрь 2021 г. [update], [ 347 ] в некоторых странах имеется больше вакцин, чем необходимо для полной вакцинации населения. [ 19 ] Когда люди недостаточно привиты, напрасно умирают, становятся инвалидами и живут в условиях карантина, они не могут предоставлять те же товары и услуги. Это наносит ущерб экономике как недостаточно вакцинированных, так и избыточно вакцинированных стран. Поскольку у богатых стран более крупная экономика, богатые страны могут потерять больше денег из-за неравенства в вакцинах, чем бедные. [ 302 ] хотя бедные страны потеряют более высокий процент ВВП и испытают более долгосрочные последствия. [ 348 ] Страны с высокими доходами получат примерно 4,80 доллара США на каждый доллар, потраченный на вакцинацию стран с низкими доходами. [ 302 ]
Международный валютный фонд рассматривает разрыв в вакцинах между богатыми и бедными странами как серьезное препятствие на пути восстановления мировой экономики. [ 349 ] Неравенство в отношении вакцин непропорционально сильно влияет на государства, предоставляющие убежище, поскольку они, как правило, беднее, а беженцы и перемещенные лица экономически более уязвимы даже в этих штатах с низкими доходами, поэтому они больше страдают экономически от неравенства в отношении вакцин. [ 350 ] [ 20 ]
Обязанность
Правительства нескольких стран согласились оградить фармацевтические компании, такие как Pfizer и Moderna, от претензий по халатности , связанных с вакцинами (и лечением) COVID-19, как и во время предыдущих пандемий , когда правительства также взяли на себя ответственность по таким претензиям.
В США эти меры защиты ответственности вступили в силу 4 февраля 2020 года, когда министр здравоохранения и социальных служб США Алекс Азар опубликовал уведомление о декларации в соответствии с Законом о общественной готовности и готовности к чрезвычайным ситуациям (Закон PREP) о медицинских контрмерах против COVID-19. 19, охватывающий «любую вакцину, используемую для лечения, диагностики, предотвращения или смягчения последствий COVID-19 или передачи SARS-CoV-2 или мутирующего на его основе вируса». Декларация исключает «претензии об ответственности за халатность производителя при создании вакцины или халатность поставщика медицинских услуг при назначении неправильной дозы, за исключением умышленных неправомерных действий». Другими словами, в отсутствие «умышленного неправомерного поведения» на эти компании не могут быть предъявлены иски о возмещении денежного ущерба за любые травмы, возникшие в период с 2020 по 2024 год в результате применения вакцин и методов лечения, связанных с COVID‑19. [ 351 ] Декларация действительна в США до 1 октября 2024 года. [ 351 ]
В декабре 2020 года правительство Великобритании предоставило компании Pfizer юридическое возмещение за ее вакцину от COVID-19. [ 352 ]
В Европейском Союзе вакцинам от COVID-19 было выдано условное разрешение на продажу, которое не освобождает производителей от исков о гражданской и административной ответственности. [ 353 ] Условные регистрационные удостоверения ЕС были заменены на стандартные разрешения в сентябре 2022 года. [ 354 ] Хотя контракты на закупку с производителями вакцин остаются секретными, они не содержат освобождений от ответственности, даже в отношении побочных эффектов, не известных на момент лицензирования. [ 355 ]
Некоммерческая новостная организация « Бюро журналистских расследований» сообщила в ходе расследования, что неназванные должностные лица в некоторых странах, таких как Аргентина и Бразилия, заявили, что Pfizer потребовала гарантий покрытия расходов на судебные дела из-за неблагоприятных последствий в виде отказа от ответственности и суверенных обязательств. активы, такие как резервы федеральных банков, здания посольств или военные базы, выходят за рамки того, что ожидалось от других стран, таких как США. [ 356 ] Во время парламентского расследования пандемии в Бразилии представитель Pfizer заявил, что ее условия для Бразилии такие же, как и для всех других стран, с которыми она подписала соглашения. [ 357 ]
13 декабря 2022 года губернатор Флориды Рон ДеСантис заявил, что подаст прошение в Верховный суд штата о созыве большого жюри для расследования возможных нарушений в отношении вакцин против COVID-19. [ 358 ] и заявил, что его правительство сможет получить «данные независимо от того, хотят они [компании] их предоставить или нет». [ 359 ]
Споры
В июне 2021 года в отчете выяснилось, что вакцина UB-612 , разработанная американской компанией Covaxx, была коммерческим предприятием, инициированным основателем Blackwater Эриком Принсом . В серии текстовых сообщений Полу Берендсу, близкому соратнику, привлеченному для проекта Covaxx, Принс описал возможности получения прибыли от продажи вакцин против COVID-19. Компания Covaxx не предоставила данных о клинических исследованиях безопасности и эффективности, проведенных на Тайване. Ответственность за создание дистрибьюторских сетей была возложена на базирующуюся в Абу-Даби компанию, которая на фирменном бланке Covaxx упоминалась как «Windward Capital», но на самом деле называлась Windward Holdings. Единственным акционером фирмы, занимавшимся «профессиональной, научной и технической деятельностью», был Эрик Принс. В марте 2021 года Covaxx привлек $1,35 млрд в ходе частного размещения. [ 360 ]
Дезинформация и нерешительность

разнообразные необоснованные теории заговора и другая дезинформация Во многих странах распространились о вакцинах против COVID-19, основанная на неправильно понятых или неверно представленных научных, религиозных и юридических законах. К ним относятся преувеличенные заявления о побочных эффектах, искажения информации о том, как работает иммунная система, а также когда и как производятся вакцины против COVID-19, история о распространении COVID-19 через 5G и другая ложная или искаженная информация. Эта дезинформация, частично созданная активистами, выступающими против вакцинации , получила широкое распространение и, возможно, заставила многих людей отказаться от вакцинации. [ 362 ] Это привело к тому, что правительства и частные организации по всему миру ввели меры по стимулированию или принуждению к вакцинации, такие как лотереи, [ 363 ] мандаты, [ 364 ] и бесплатный вход на мероприятия, [ 365 ] что, в свою очередь, привело к дальнейшей дезинформации о законности и эффекте самих этих мер. [ 366 ]
В США некоторые видные ученые-биомедики, публично выступающие за вакцинацию, подверглись нападкам и угрозам в электронных письмах и социальных сетях со стороны активистов, выступающих против вакцинации. [ 367 ]Министерство обороны США (МО) провело кампанию дезинформации на Филиппинах, а затем распространило ее на Центральную Азию и Ближний Восток, стремясь дискредитировать Китай, в частности его вакцину Sinovac , распространяя хэштеги #ChinaIsTheVirus и сообщения, утверждающие, что Sinovac вакцина содержала желатин из свинины и поэтому была харамом или запрещена с точки зрения исламского права. [ 368 ]
См. также
Примечания
- ^ «(OWID) Карты вакцинации» . Наш мир в данных . Архивировано из оригинала 21 декабря 2021 года. Матье Э., Ричи Х., Родес-Гуйрао Л., Аппель С., Джаттино С., Хаселл Дж. и др. (5 марта 2020 г.). «Часто задаваемые вопросы по данным» . Наш мир в данных . Архивировано из оригинала 10 марта 2021 года.
- ^ Данные таблицы автоматически обновляются ботом ежедневно; см . в разделе «Шаблон: данные о COVID-19» дополнительную информацию . Прокрутите таблицу вниз, чтобы найти документацию и основную ссылку. См. также: Категория:Автоматически обновляемые шаблоны таблиц пандемии COVID-19 .
Ссылки
- ^ Ли Ю.Д., Чи Вайоминг, Су Дж.Х., Феррал Л., Хунг К.Ф., Ву ТС (декабрь 2020 г.). «Разработка вакцины против коронавируса: от SARS и MERS до COVID-19» . Журнал биомедицинской науки . 27 (1): 104. дои : 10.1186/s12929-020-00695-2 . ПМЦ 7749790 . ПМИД 33341119 .
- ^ Суббарао К. (июль 2021 г.). «Успех вакцин против SARS-CoV-2 и предстоящие проблемы» . Клетка-хозяин и микроб . 29 (7): 1111–1123. дои : 10.1016/j.chom.2021.06.016 . ПМЦ 8279572 . PMID 34265245 .
- ^ Перейти обратно: а б с д Роджерс К. (11 мая 2022 г.). "COVID-19 вакцина" . Британская энциклопедия . Архивировано из оригинала 12 июня 2022 года . Проверено 12 июня 2022 г.
- ^ «Swissmedic выдает разрешение на производство первой вакцины против COVID-19 в Швейцарии» (пресс-релиз). Швейцарское агентство по терапевтической продукции (Swissmedic) . 18 декабря 2020 года. Архивировано из оригинала 2 мая 2021 года . Проверено 5 июля 2022 г.
- ^ «EMA рекомендует первую вакцину против COVID-19 для авторизации в ЕС» . Европейское агентство лекарственных средств (EMA) (пресс-релиз). 21 декабря 2020 года. Архивировано из оригинала 30 января 2021 года . Проверено 21 декабря 2020 г. .
- ^ «Вакцина CanSino Biologics Ad5-nCoV-S [рекомбинантная] против COVID-19: что вам нужно знать» . www.who.int . Проверено 12 июля 2024 г.
- ^ Додаран М.С., Банихашеми С.Р., Эс-хаги А., Мехрабади М.Х., Нофели М., Мокаррам А.Р. и др. (16 февраля 2023 г.). «Иммуногенность и безопасность комбинированной внутримышечной/интраназальной рекомбинантной белковой вакцины против COVID-19 (RCP) у здоровых взрослых в возрасте от 18 до 55 лет: рандомизированное двойное слепое плацебо-контролируемое исследование фазы I» . Вакцина . 11 (2): 455. doi : 10.3390/vaccines11020455 . ПМЦ 9961243 . ПМИД 36851334 .
- ^ Пуга-Гомес Р., Рикардо-Дельгадо Ю., Рохас-Ириарте С., Сеспедес-Энрикес Л., Пьедра-Белло М., Вега-Мендоса Д. и др. (январь 2023 г.). «Открытое клиническое исследование фазы I/II конъюгированной вакцины с рецептор-связывающим доменом SARS-CoV-2 и столбнячным анатоксином (FINLAY-FR-2) в сочетании с вакциной с рецептор-связывающим доменом и белком (FINLAY-FR-1A) у детей» . Международный журнал инфекционных заболеваний . 126 : 164–173. дои : 10.1016/j.ijid.2022.11.016 . ПМЦ 9673084 . ПМИД 36403819 . Проверено 28 июня 2024 г.
- ^ Маллапати С., Каллауэй Э., Козлов М., Ледфорд Х., Пикрелл Дж., Ван Ноорден Р. (декабрь 2021 г.). «Как вакцины против COVID повлияли на 2021 год в восьми ярких диаграммах» . Природа . 600 (7890): 580–583. Бибкод : 2021Природа.600..580М . дои : 10.1038/d41586-021-03686-x . ПМИД 34916666 . S2CID 245262732 .
- ^ Уотсон О.Дж., Барнсли Дж., Тур Дж., Хоган А.Б., Уинскилл П., Гани А.С. (июнь 2022 г.). «Глобальное влияние первого года вакцинации против COVID-19: исследование с помощью математического моделирования» . Ланцет инфекционных заболеваний . 22 (9): 1293–1302. дои : 10.1016/s1473-3099(22)00320-6 . ПМЦ 9225255 . ПМИД 35753318 .
- ^ «Вакцины против COVID-19 спасли почти 20 миллионов жизней за год, говорится в исследовании» . Новости CBS . 24 июня 2022 года. Архивировано из оригинала 29 июня 2022 года . Проверено 27 июня 2022 г.
- ^ Бомонт П. (18 ноября 2020 г.). «Вакцина против Covid-19: какие страны отдают приоритет при получении первых доз?» . Хранитель . ISSN 0261-3077 . Архивировано из оригинала 18 января 2021 года . Проверено 26 декабря 2020 г.
- ^ Перейти обратно: а б Ван Х, Сюй Р, Цюй С, Шварц М, Адамс А, Чен X (октябрь 2021 г.). «Неравноправие в отношении вакцинации против COVID-19 среди пожилых людей: случай Коннектикута» . Журнал инфекций и общественного здравоохранения . 14 (10): 1563–1565. дои : 10.1016/j.jiph.2021.07.013 . ПМЦ 8491089 . ПМИД 34326008 . S2CID 236515442 .
- ^ Перейти обратно: а б Справочный документ по вакцине мРНК-1273 (Moderna) против COVID-19 (Отчет). Всемирная организация здравоохранения (ВОЗ). Февраль 2021 г. HDL : 10665/339218 . ВОЗ/2019-nCoV/vaccines/SAGE_recommendation/mRNA-1273/background/2021.1. Архивировано из оригинала 13 июня 2021 года . Проверено 24 июля 2021 г.
- ^ Перейти обратно: а б «Справочный документ по вакцине мРНК-1273 (Moderna) против COVID-19» . Всемирная организация здравоохранения (ВОЗ). Архивировано из оригинала 26 января 2022 года . Проверено 23 января 2022 г.
- ^ Перейти обратно: а б «Беременность, грудное вскармливание, фертильность и вакцинация от коронавируса (COVID-19)» . Национальная служба здравоохранения. 5 октября 2022 года. Архивировано из оригинала 15 октября 2022 года . Проверено 15 октября 2022 г.
- ^ Ричи Х., Ортис-Оспина Э., Бельтекян Д., Метье Э., Хаселл Дж., Макдональд Б. и др. (март 2020 г.). «Прививки от коронавируса (COVID-19) – статистика и исследования» . Наш мир в данных . Архивировано из оригинала 10 марта 2021 года . Проверено 7 февраля 2021 г.
- ^ Маллард А. (ноябрь 2020 г.). «Как вакцины против COVID делятся во всем мире». Природа . дои : 10.1038/d41586-020-03370-6 . ПМИД 33257891 . S2CID 227246811 .
- ^ Перейти обратно: а б с Итак, AD, У Джей (декабрь 2020 г.). «Резервирование вакцин против коронавирусной болезни 2019 года для глобального доступа: перекрестный анализ» . БМЖ . 371 : м4750. дои : 10.1136/bmj.m4750 . ПМЦ 7735431 . ПМИД 33323376 .
- ^ Перейти обратно: а б с д и ж Хотез П.Дж., Боттацци М.Э. (январь 2022 г.). «Цельноинактивированные вирусные и белковые вакцины против COVID-19» . Ежегодный обзор медицины . 73 (1): 55–64. doi : 10.1146/annurev-med-042420-113212 . ISSN 0066-4219 . ПМИД 34637324 . S2CID 238747462 .
- ^ Перейти обратно: а б Е Ю, Чжан Ц, Вэй Икс, Цао З, Юань ХИ, Цзэн ДД (февраль 2022 г.). «Справедливый доступ к вакцинам против COVID-19 имеет жизненно важное значение для всех стран» . Природа человеческого поведения . 6 (2): 207–216. дои : 10.1038/s41562-022-01289-8 . ПМЦ 8873023 . ПМИД 35102361 .
- ^ «Нобелевская премия по физиологии и медицине 2023 года» . NobelPrize.org . Архивировано из оригинала 4 октября 2023 года . Проверено 3 октября 2023 г.
- ^ «Венгерские и американские учёные получили Нобелевскую премию за открытие вакцины против COVID-19» . Рейтер . 2 октября 2023 года. Архивировано из оригинала 8 октября 2023 года . Проверено 3 октября 2023 г.
- ^ «Нобелевская премия по физиологии и медицине 2023 года» . NobelPrize.org . Архивировано из оригинала 4 февраля 2024 года . Проверено 3 октября 2023 г.
- ^ Перейти обратно: а б с Ворота Б (30 апреля 2020 г.). «Гонка вакцин объяснила: что нужно знать о вакцине от COVID-19» . Заметки Гейтса. Архивировано из оригинала 14 мая 2020 года . Проверено 2 мая 2020 г.
- ^ Кавана Д. (декабрь 2003 г.). «Разработка вакцины против тяжелого острого респираторного синдрома: опыт вакцинации против коронавируса инфекционного бронхита птиц» . Птичья патология . 32 (6): 567–582. дои : 10.1080/03079450310001621198 . ПМК 7154303 . ПМИД 14676007 .
- ^ Гао В., Тамин А., Солофф А., Д'Айуто Л., Нванегбо Е., Роббинс П.Д. и др. (декабрь 2003 г.). «Эффекты вакцины против SARS-ассоциированного коронавируса на обезьянах» . Ланцет . 362 (9399): 1895–1896. дои : 10.1016/S0140-6736(03) 14962-8 ПМЦ 7112457 . ПМИД 14667748 .
- ^ Ким Э., Окада К., Кеннистон Т., Радж В.С., АльХаджри М.М., Фараг Э.А. и др. (октябрь 2014 г.). «Иммуногенность аденовирусной вакцины против коронавируса ближневосточного респираторного синдрома у мышей BALB/c» . Вакцина . 32 (45): 5975–5982. doi : 10.1016/j.vaccine.2014.08.058 . ПМЦ 7115510 . ПМИД 25192975 .
- ^ Гриноф Т.С., Бэбкок Г.Дж., Робертс А., Эрнандес Х.Дж., Томас В.Д., Кочча Дж.А. и др. (февраль 2005 г.). «Разработка и характеристика человеческого моноклонального антитела, нейтрализующего коронавирус, связанного с тяжелым острым респираторным синдромом, которое обеспечивает эффективную иммунопрофилактику у мышей» . Журнал инфекционных болезней . 191 (4): 507–514. дои : 10.1086/427242 . ПМК 7110081 . ПМИД 15655773 .
- ^ Трипп Р.А., Хейнс Л.М., Мур Д., Андерсон Б., Тамин А., Харкорт Б.Х. и др. (сентябрь 2005 г.). «Моноклональные антитела к SARS-ассоциированному коронавирусу (SARS-CoV): идентификация нейтрализующих и антител, реактивных к вирусным белкам S, N, M и E» . Журнал вирусологических методов . 128 (1–2): 21–28. doi : 10.1016/j.jviromet.2005.03.021 . ПМЦ 7112802 . ПМИД 15885812 .
- ^ Робертс А., Томас В.Д., Гуарнер Дж., Ламиранд Э.В., Бэбкок Г.Дж., Гриноф Т.С. и др. (март 2006 г.). «Терапия человеческими моноклональными антителами, нейтрализующими коронавирус, связанный с тяжелым острым респираторным синдромом, снижает тяжесть заболевания и вирусную нагрузку у золотистых сирийских хомячков» . Журнал инфекционных болезней . 193 (5): 685–692. дои : 10.1086/500143 . ПМК 7109703 . ПМИД 16453264 .
- ^ Перейти обратно: а б Цзян С., Лу Л, Ду Л (январь 2013 г.). «Разработка вакцин и средств лечения атипичной пневмонии все еще необходима» . Будущая вирусология . 8 (1): 1–2. дои : 10.2217/fvl.12.126 . ПМК 7079997 . ПМИД 32201503 .
- ^ «ТОРС (тяжелый острый респираторный синдром)» . Национальная служба здравоохранения. 5 марта 2020 года. Архивировано из оригинала 9 марта 2020 года . Проверено 31 января 2020 г.
- ^ Шехата М.М., Гомаа М.Р., Али М.А., Каяли Г. (июнь 2016 г.). «Коронавирус ближневосточного респираторного синдрома: комплексный обзор» . Границы медицины . 10 (2): 120–136. дои : 10.1007/s11684-016-0430-6 . ПМК 7089261 . ПМИД 26791756 .
- ^ Батлер Д. (октябрь 2012 г.). «Ветераны атипичной пневмонии борются с коронавирусом» . Природа . 490 (7418): 20. Бибкод : 2012Natur.490...20B . дои : 10.1038/490020a . ПМИД 23038444 .
- ^ Моджаррад К., Робертс К.С., Миллс К.Т., Кастеллано А.Р., Паолино К., Мутумани К. и др. (сентябрь 2019 г.). «Безопасность и иммуногенность ДНК-вакцины против коронавируса ближневосточного респираторного синдрома: открытое одногрупповое исследование фазы 1 с увеличением дозы» . «Ланцет». Инфекционные болезни . 19 (9): 1013–1022. дои : 10.1016/S1473-3099(19)30266-X . ПМЦ 7185789 . ПМИД 31351922 .
- ^ Ён Сай, Онг ХК, Йип С.К., Хо К.Л., Тан В.С. (2019). «Последние достижения в разработке вакцины против ближневосточного респираторного синдрома – коронавируса» . Границы микробиологии . 10 : 1781. дои : 10.3389/fmicb.2019.01781 . ПМК 6688523 . ПМИД 31428074 .
- ^ Перейти обратно: а б с Лофтус П., Хопкинс Дж.С., Панчевски Б. (17 ноября 2020 г.). «Moderna и Pfizer заново изобретают вакцины, начиная с Covid» . Уолл Стрит Джорнал . Архивировано из оригинала 6 ноября 2021 года . Проверено 4 октября 2021 г.
- ^ Шарма О, Султан А.А., Дин Х, Триггл ЧР (14 октября 2020 г.). «Обзор прогресса и проблем разработки вакцины от COVID-19» . Границы в иммунологии . 11 : 585354. дои : 10.3389/fimmu.2020.585354 . ПМЦ 7591699 . ПМИД 33163000 .
- ^ Бок К., Ситар С., Грэм Б.С., Маскола-младший (август 2021 г.). «Ускоренная разработка вакцины против COVID-19: основные этапы, уроки и перспективы» . Иммунитет . 54 (8): 1636–1651. doi : 10.1016/j.immuni.2021.07.017 . ПМЦ 8328682 . ПМИД 34348117 .
- ^ Льюис Т. «Новая прививка от COVID-19 может спасти вашу жизнь; сделайте ее сейчас, говорит эксперт FDA» . Научный американец . Архивировано из оригинала 7 ноября 2022 года . Проверено 8 ноября 2022 г.
- ^ Тернер Дж.С., О'Халлоран Дж.А., Калайдина Э., Ким В., Шмитц А.Дж., Чжоу Дж.К. и др. (август 2021 г.). «Вакцины мРНК SARS-CoV-2 вызывают стойкие реакции зародышевого центра человека» . Природа . 596 (7870): 109–113. Бибкод : 2021Natur.596..109T . дои : 10.1038/s41586-021-03738-2 . ПМЦ 8935394 . ПМИД 34182569 .
- ^ «Вакцины Pfizer и Moderna, вероятно, обеспечат стойкий иммунитет, результаты исследования» . Нью-Йорк Таймс . 28 июня 2021 года. Архивировано из оригинала 28 июня 2021 года . Проверено 23 января 2022 г.
- ^ Фланаган К.Л., Бест Э., Кроуфорд Н.В., Джайлз М., Койрала А., Макартни К. и др. (2020). «Прогресс и подводные камни в поисках эффективных вакцин против SARS-CoV-2 (COVID-19)» . Границы в иммунологии . 11 : 579250. дои : 10.3389/fimmu.2020.579250 . ПМЦ 7566192 . ПМИД 33123165 .
- ^ Перейти обратно: а б с д и ж г Ле Т.Т., Крамер Дж.П., Чен Р., Мэйхью С. (октябрь 2020 г.). «Эволюция ландшафта разработки вакцин против COVID-19» . Обзоры природы. Открытие наркотиков . 19 (10): 667–68. дои : 10.1038/d41573-020-00151-8 . ПМИД 32887942 . S2CID 221503034 .
- ^ Перейти обратно: а б «Отслеживание вакцины против COVID-19 (обновите URL-адрес, чтобы обновить)» . Лондонская школа гигиены и тропической медицины . 12 июля 2021 года. Архивировано из оригинала 11 октября 2020 года . Проверено 10 марта 2021 г.
- ^ Арбайтман Ч.Р., Рохас П., Охеда-Мэй П., Гарсия М.Э. (сентябрь 2021 г.). «Белок-шип SARS-CoV-2 уязвим к умеренным электрическим полям» . Природные коммуникации . 12 (1): 5407. arXiv : 2103.12733 . Бибкод : 2021NatCo..12.5407A . дои : 10.1038/s41467-021-25478-7 . ПМЦ 8437970 . ПМИД 34518528 .
- ^ Перейти обратно: а б Грифони А., Вайскопф Д., Рамирес С.И., Матеус Дж., Дэн Дж.М., Модербахер С.Р. и др. (июнь 2020 г.). «Цели Т-клеточного ответа на коронавирус SARS-CoV-2 у людей с заболеванием COVID-19 и лиц, не подвергавшихся воздействию» . Клетка . 181 (7): 1489–1501.e15. дои : 10.1016/j.cell.2020.05.015 . ПМЦ 7237901 . ПМИД 32473127 .
- ^ Дутта Н.К., Мазумдар К., Горди Дж.Т. (июнь 2020 г.). Голландский RE (ред.). «Нуклеокапсидный белок SARS-CoV-2: цель для разработки вакцины» . Журнал вирусологии . 94 (13). дои : 10.1128/JVI.00647-20 . ПМК 7307180 . ПМИД 32546606 .
- ^ Николаидис М., Маркулатос П., Ван де Пер Ю., Оливер С.Г., Амуциас Г.Д. (октябрь 2021 г.). Хепп С. (ред.). «Район гена Spike является горячей точкой для модульной межтипической гомологичной и негомологической рекомбинации в геномах коронавируса» . Молекулярная биология и эволюция . 39 : мсаб292. дои : 10.1093/molbev/msab292 . ПМЦ 8549283 . ПМИД 34638137 .
- ^ Амуциас Г.Д., Николаидис М., Трифонопулу Э., Хлихлия К., Маркулатос П., Оливер С.Г. (январь 2022 г.). «Удивительная эволюционная пластичность коронавирусов посредством мутации и рекомбинации: выводы о пандемии COVID-19 и будущих эволюционных путях SARS-CoV-2» . Вирусы . 14 (1): 78. дои : 10.3390/v14010078 . ПМЦ 8778387 . ПМИД 35062282 .
- ^ Перейти обратно: а б с д Тхань Ле Т., Андредакис З., Кумар А., Гомес Роман Р., Толлефсен С., Сэвилл М. и др. (май 2020 г.). «Ситуация разработки вакцины против COVID-19» . Обзоры природы. Открытие наркотиков . 19 (5): 305–06. дои : 10.1038/d41573-020-00073-5 . ПМИД 32273591 .
- ^ Перейти обратно: а б с Даймонд М.С., Пирсон Т.К. (май 2020 г.). «Проблемы разработки вакцины против нового вируса во время пандемии» . Клетка-хозяин и микроб . 27 (5): 699–703. дои : 10.1016/j.chom.2020.04.021 . ПМЦ 7219397 . ПМИД 32407708 .
- ^ Кросс Р (29 сентября 2020 г.). «Маленькая поправка к вакцинам против COVID-19» . Новости химии и техники . Том. 98, нет. 38. Архивировано из оригинала 16 февраля 2021 года . Проверено 15 апреля 2021 г.
- ^ Краммер Ф. (октябрь 2020 г.). «Вакцина против SARS-CoV-2 находится в разработке» . Природа . 586 (7830): 516–527. Бибкод : 2020Natur.586..516K . дои : 10.1038/s41586-020-2798-3 . ПМИД 32967006 . S2CID 221887746 .
- ^ Пак К.С., Сан Х, Эйкинс М.Э., Мун Дж.Дж. (февраль 2021 г.). «Системы доставки невирусной вакцины против COVID-19» . Обзоры расширенной доставки лекарств . 169 : 137–151. дои : 10.1016/j.addr.2020.12.008 . ISSN 0169-409X . ПМЦ 7744276 . ПМИД 33340620 .
- ^ Ковальски П.С., Рудра А., Мяо Л., Андерсон Д.Г. (апрель 2019 г.). «Доставка посланника: достижения в области технологий терапевтической доставки мРНК» . Молекулярная терапия . 27 (4): 710–728. дои : 10.1016/j.ymthe.2019.02.012 . ПМК 6453548 . ПМИД 30846391 .
- ^ Вербеке Р., Лентакер И., Де Смедт СК, Девитте Х (октябрь 2019 г.). «Три десятилетия разработки вакцины с информационной РНК» . Нано сегодня . 28 : 100766. doi : 10.1016/j.nantod.2019.100766 . hdl : 1854/LU-8628303 . S2CID 202221207 . Архивировано из оригинала 9 октября 2021 года . Проверено 17 января 2021 г.
- ^ «Рекомендации по вакцине ACIP против COVID-19» . Центры США по контролю и профилактике заболеваний (CDC) . Архивировано из оригинала 3 ноября 2021 года . Проверено 18 февраля 2021 г.
- ^ «Безопасные вакцины против COVID-19 для европейцев» . Европейская комиссия . Архивировано из оригинала 4 ноября 2021 года . Проверено 19 февраля 2021 г.
- ^ «Краткий обзор нормативных решений – вакцина Pfizer–BioNTech против COVID-19» . Министерство здравоохранения Канады, Правительство Канады. 9 декабря 2020 года. Архивировано из оригинала 30 января 2021 года . Проверено 9 декабря 2020 г.
- ^ «Исследование по описанию безопасности, переносимости, иммуногенности и эффективности кандидатов на РНК-вакцины против COVID-19 у здоровых взрослых» . ClinicalTrials.gov . 30 апреля 2020 г. NCT04368728. Архивировано из оригинала 11 октября 2020 года . Проверено 14 июля 2020 г.
- ^ «Многоцентровое исследование фазы I/II, состоящее из 2 частей, с увеличением дозы, изучающее безопасность и иммуногенность четырех профилактических РНК-вакцин SARS-CoV-2 против COVID-19 с использованием различных режимов дозирования у здоровых взрослых» . Реестр клинических исследований ЕС . 14 апреля 2020 г. EudraCT 2020-001038-36. Архивировано из оригинала 22 апреля 2020 года . Проверено 22 апреля 2020 г.
- ^ «Исследование по оценке эффективности, безопасности и иммуногенности вакцины мРНК-1273 у взрослых в возрасте 18 лет и старше для профилактики COVID-19» . ClinicalTrials.gov . 14 июля 2020 г. NCT04470427. Архивировано из оригинала 11 октября 2020 года . Проверено 27 июля 2020 г.
- ^ Палка Дж. (27 июля 2020 г.). «Кандидат на вакцину против COVID-19 готовится к широкомасштабным испытаниям в США» NPR. Архивировано из оригинала 11 октября 2020 года . Проверено 27 июля 2020 г.
- ^ «Окончательные данные CureVac фазы 2b/3 испытания кандидатной вакцины против COVID-19 первого поколения, CVnCoV, демонстрируют защиту в возрастной группе от 18 до 60 лет» . CureVac (Пресс-релиз). 30 июня 2021 года. Архивировано из оригинала 12 октября 2021 года . Проверено 2 июля 2021 г.
- ^ Перейти обратно: а б с Могими С.М. (март 2021 г.). «Аллергические реакции и анафилаксия на вакцины против COVID-19 на основе ЛНП» . Молекулярная терапия . 29 (3): 898–900. дои : 10.1016/j.ymthe.2021.01.030 . ПМК 7862013 . ПМИД 33571463 .
- ^ Перейти обратно: а б «Что такое вакцины на основе вирусных векторов и как их можно использовать против COVID-19?» . Гави, Альянс по вакцинам (ГАВИ). 2020. Архивировано из оригинала 11 ноября 2021 года . Проверено 26 января 2021 г.
- ^ «Понимание вирусных векторных вакцин против COVID-19» . Центры США по контролю и профилактике заболеваний (CDC) . 13 апреля 2021 года. Архивировано из оригинала 13 ноября 2021 года . Проверено 19 апреля 2021 г.
- ^ «Исследование вакцины против COVID-19» . ClinicalTrials.gov . 26 мая 2020 г. NCT04400838. Архивировано из оригинала 11 октября 2020 года . Проверено 14 июля 2020 г.
- ^ «Исследование фазы 2/3 для определения эффективности, безопасности и иммуногенности вакцины-кандидата против коронавируса (COVID-19) ChAdOx1 nCoV-19» . Реестр клинических исследований ЕС . 21 апреля 2020 г. EudraCT 2020-001228-32. Архивировано из оригинала 5 октября 2020 года . Проверено 3 августа 2020 г.
- ^ О'Рейли П. (май 2020 г.). «Исследование фазы III по изучению вакцины против COVID-19» . Реестр ISRCTN . дои : 10.1186/ISRCTN89951424 .
- ^ Корум Дж., Карл З. (8 января 2021 г.). «Как действует вакцина Гамалеи» . Нью-Йорк Таймс . Архивировано из оригинала 20 апреля 2021 года . Проверено 27 января 2021 г.
- ^ «Исследование Ad26.COV2.S у взрослых» . 4 августа 2020 г. Архивировано из оригинала 16 сентября 2020 г. . Проверено 23 августа 2020 г. .
- ^ «Исследование Ad26.COV2.S для профилактики COVID-19, опосредованного SARS-CoV-2, у взрослых участников» . Национальная медицинская библиотека США. Архивировано из оригинала 26 сентября 2020 года.
- ^ Джонсон С., МакГинли Л. «Джонсон и Джонсон запрашивают экстренное разрешение FDA на однократную вакцину против коронавируса» . Вашингтон Пост . Архивировано из оригинала 5 февраля 2021 года . Проверено 10 февраля 2021 г.
- ^ «Дело не только в Johnson & Johnson: в Китае есть однократная вакцина против COVID-19, эффективность которой составляет 65%» . Удача . Архивировано из оригинала 8 августа 2021 года . Проверено 28 февраля 2021 г.
- ^ Ву С., Чжун Г., Чжан Дж., Шуай Л., Чжан З., Вэнь З. и др. (август 2020 г.). «Одна доза аденовирусной векторной вакцины обеспечивает защиту от заражения SARS-CoV-2» . Нат Коммун . 11 (1): 4081. Бибкод : 2020NatCo..11.4081W . дои : 10.1038/s41467-020-17972-1 . ПМЦ 7427994 . ПМИД 32796842 .
- ^ «Вакцина однократная «Спутник Лайт», разрешенная к применению в России» . Спутник V (Пресс-релиз). Архивировано из оригинала 14 ноября 2021 года . Проверено 12 августа 2021 г.
- ^ Спутник В [@sputnikvaccine] (6 мая 2021 г.). «Представляем нового члена семейства «Спутник» — однократную дозу «Спутник Лайт»! Это революционная однократная вакцина против COVID-19 с эффективностью 80% — выше, чем у многих двухкратных вакцин. «Спутник Лайт» удвоит уровень вакцинации и поможет справиться с ситуацией. пики эпидемии https://t.co/BCybe8yYWU» ( твит ). Архивировано из оригинала 8 мая 2022 года . Проверено 8 декабря 2022 г. - через Twitter .
- ^ Петровский Н., Агилар Дж.К. (октябрь 2004 г.). «Вакцинные адъюванты: современное состояние и будущие тенденции». Иммунология и клеточная биология . 82 (5): 488–496. дои : 10.1111/j.0818-9641.2004.01272.x . ПМИД 15479434 . S2CID 154670 .
- ^ «Исследование безопасности и иммуногенности инактивированной вакцины для профилактики инфекции SARS-CoV-2 (COVID-19) (Жэньцю)» . ClinicalTrials.gov . 12 мая 2020 г. NCT04383574. Архивировано из оригинала 11 октября 2020 года . Проверено 14 июля 2020 г.
- ^ «Клиническое исследование эффективности и безопасности адсорбированной (инактивированной) вакцины Sinovac против COVID-19 среди медицинских работников (PROFISCOV)» . ClinicalTrials.gov . 2 июля 2020 г. NCT04456595. Архивировано из оригинала 11 октября 2020 года . Проверено 3 августа 2020 г.
- ^ ПТ. Био Фарма (август 2020 г.). «Фаза III, слепое для наблюдателей, рандомизированное, плацебо-контролируемое исследование эффективности, безопасности и иммуногенности инактивированной вакцины против SARS-COV-2 у здоровых взрослых в возрасте 18–59 лет в Индонезии» . Регистр Пеньякит Индонезия . Архивировано из оригинала 11 октября 2020 года . Проверено 15 августа 2020 г. .
- ^ Чен В., Аль Кааби Н. (июль 2020 г.). «Клиническое исследование фазы III инактивированной вакцины против новой коронавирусной пневмонии (COVID-19) (клетки Vero)» . Китайский реестр клинических исследований . Архивировано из оригинала 11 октября 2020 года . Проверено 15 августа 2020 г. .
- ^ Иванова П. (20 февраля 2021 г.). «В России одобрена третья вакцина от COVID-19 — CoviVac» . Рейтер . Архивировано из оригинала 28 февраля 2021 года . Проверено 11 апреля 2021 г.
- ^ «Казахстан выводит собственную вакцину от COVID-19» . Рейтер . 27 апреля 2021 года. Архивировано из оригинала 4 ноября 2021 года . Проверено 2 июля 2021 г.
- ^ «Агентство FarsNews Иран лицензирует экстренную инъекцию домашней противокоронавирусной вакцины» . Информационное агентство «Фарс» . 14 июня 2021 года. Архивировано из оригинала 9 октября 2021 года . Проверено 25 августа 2021 г.
- ^ «Вакцина против COVID-19 VLA2001» . Точные прививки . 31 декабря 2020 года. Архивировано из оригинала 13 января 2021 года . Проверено 11 января 2021 г.
- ^ «Исследование по подбору дозы для оценки безопасности, переносимости и иммуногенности инактивированной адъювантной вакцины-кандидата против вируса Sars-Cov-2 против Covid-19 у здоровых взрослых» . Национальная медицинская библиотека США. 30 декабря 2020 года. Архивировано из оригинала 14 февраля 2021 года . Проверено 11 января 2021 г.
- ^ «Модуль 2 – Субъединичные вакцины» . Основы безопасности вакцин ВОЗ . Архивировано из оригинала 8 августа 2021 года . Проверено 17 января 2021 г.
- ^ «Исследование безопасности, реактогенности и иммуногенности вакцины «ЭпиВакКорона» для профилактики COVID-19 (ЭпиВакКорона)» . ClinicalTrials.gov . 22 сентября 2020 г. NCT04368988. Архивировано из оригинала 29 июня 2021 года . Проверено 16 ноября 2020 г.
- ^ «Вакцина MVC против COVID-19 получила одобрение Тайваня EUA» . Биологические препараты вакцины Медиген . Архивировано из оригинала 27 ноября 2021 года . Проверено 7 августа 2021 г.
- ^ Ахом Д. (28 декабря 2021 г.). «Индия очищает две новые вакцины и таблетку от Covid от Merck: 10 баллов» . NDTV.com . Архивировано из оригинала 28 декабря 2021 года . Проверено 19 января 2022 г.
- ^ Боттацци М.Э., Хотез П.Дж. (30 декабря 2021 г.). «Вакцина от COVID для всех» . Научный американец . Архивировано из оригинала 30 декабря 2021 года . Проверено 19 января 2022 г.
- ^ «ВидПревтин Бета» . Европейское агентство лекарственных средств (EMA) . 4 ноября 2022 года. Архивировано из оригинала 11 ноября 2022 года . Проверено 12 ноября 2022 г. Текст скопирован из источника, права на который принадлежат Европейскому агентству по лекарственным средствам. Воспроизведение разрешено при условии указания источника.
- ^ «EMA рекомендует одобрить ВидПревтин Бета в качестве бустерной вакцины против COVID-19» . Европейское агентство лекарственных средств (EMA) (пресс-релиз). 10 ноября 2022 года. Архивировано из оригинала 12 ноября 2022 года . Проверено 12 ноября 2022 г. Текст скопирован из источника, права на который принадлежат Европейскому агентству по лекарственным средствам. Воспроизведение разрешено при условии указания источника.
- ^ «Ирано-кубинская вакцина вступает в третью фазу клинических испытаний» . Тегеран Таймс . 26 апреля 2021 года. Архивировано из оригинала 19 июля 2021 года . Проверено 7 сентября 2021 г.
- ^ Барри Р. (31 марта 2023 г.). «Бустерная вакцина Hipra Covid-19 получила одобрение EMA и вступила в неопределенную ситуацию» . Фармацевтическая технология . Архивировано из оригинала 10 апреля 2023 года . Проверено 9 апреля 2023 г.
- ^ «Бимервакс ЭПАР» . Европейское агентство по лекарственным средствам . 5 апреля 2023 года. Архивировано из оригинала 8 апреля 2023 года . Проверено 9 апреля 2023 г.
- ^ «Исследование безопасности, переносимости и иммунного ответа вакцины против SARS-CoV-2 (COVID-19) у здоровых взрослых» . ClinicalTrials.gov . 3 августа 2020 г. NCT04495933. Архивировано из оригинала 11 октября 2020 года . Проверено 4 августа 2020 г.
- ^ «Испытания австралийской вакцины прекращены из-за ложноположительных результатов на ВИЧ» . Немецкая волна . 11 декабря 2020 года. Архивировано из оригинала 26 января 2021 года . Проверено 9 января 2023 г.
- ^ «Covid: от австралийской вакцины отказались из-за ложной реакции на ВИЧ» . Новости BBC онлайн . 11 декабря 2020 года. Архивировано из оригинала 16 января 2021 года . Проверено 9 апреля 2023 г.
- ^ «Оценка безопасности и иммуногенности вакцины наночастиц SARS-CoV-2 rS (COVID-19) с адъювантом Matrix-M или без него» . ClinicalTrials.gov . 30 апреля 2020 г. NCT04368988. Архивировано из оригинала 14 июля 2020 года . Проверено 14 июля 2020 г.
- ^ «Проспективное рандомизированное адаптивное клиническое исследование фазы I/II для оценки безопасности и иммуногенности кандидатной вакцины против нового вируса короны -2019-nCov от M/s Cadila Healthcare Limited для внутрикожного введения здоровым субъектам» . Индия: Реестр клинических исследований. 15 декабря 2020 г. CTRI/2020/07/026352. Архивировано из оригинала 22 ноября 2020 года.
- ^ «Безопасность, переносимость и иммуногенность INO-4800 при COVID-19 у здоровых добровольцев» . ClinicalTrials.gov . 7 апреля 2020 г. NCT04336410. Архивировано из оригинала 11 октября 2020 года . Проверено 14 июля 2020 г.
- ^ «IVI, INOVIO и KNIH будут сотрудничать с CEPI в клинических испытаниях фазы I/II ДНК-вакцины INOVIO от COVID-19 в Южной Корее» . Международный институт вакцин. 16 апреля 2020 года. Архивировано из оригинала 24 сентября 2020 года . Проверено 23 апреля 2020 г.
- ^ «Исследование ДНК-вакцины против COVID-19 (AG0301-COVID19)» . ClinicalTrials.gov . 9 июля 2020 г. NCT04463472. Архивировано из оригинала 11 октября 2020 года . Проверено 14 июля 2020 г.
- ^ «Исследование безопасности и иммуногенности GX-19, профилактической ДНК-вакцины против COVID-19, у здоровых взрослых» . ClinicalTrials.gov . 24 июня 2020 г. NCT04445389. Архивировано из оригинала 11 октября 2020 года . Проверено 14 июля 2020 г.
- ^ «Южнокорейская компания Genexine начинает испытания вакцины против коронавируса на людях» . Рейтер. 19 июня 2020 года. Архивировано из оригинала 11 октября 2020 года . Проверено 25 июня 2020 г.
- ^ Чанг Эл Джей (март 2020 г.). «Безопасность и иммунитет вакцины aAPC Covid-19» . ClinicalTrials.gov . NCT04299724. Архивировано из оригинала 11 октября 2020 года . Проверено 14 июля 2020 г.
- ^ «Иммунитет и безопасность синтетической минигенной вакцины против Covid-19» . ClinicalTrials.gov . Февраль 2020 г. NCT04276896. Архивировано из оригинала 11 октября 2020 года . Проверено 14 июля 2020 г.
- ^ «Рандомизированное многоцентровое плацебо-контролируемое исследование фазы I/II с повышением дозы для оценки безопасности, иммуногенности и потенциальной эффективности вакцины rVSV-SARS-CoV-2-S (IIBR-100) у взрослых» . ClinicalTrials.gov . Ноябрь 2020 г. NCT04608305. Архивировано из оригинала 3 мая 2021 года . Проверено 2 января 2021 г.
- ^ Джонсон С.А., Мафсон С. (11 июня 2020 г.). «Могут ли старые вакцины из научной аптечки защитить от коронавируса?» . Вашингтон Пост . ISSN 0190-8286 . Архивировано из оригинала 11 июня 2020 года . Проверено 31 декабря 2020 г.
- ^ «Вакцинация против бациллы Кальметта-Герена (БЦЖ) и COVID-19» . Всемирная организация здравоохранения (ВОЗ) . 12 апреля 2020 года. Архивировано из оригинала 30 апреля 2020 года . Проверено 1 мая 2020 г.
- ^ «Срочные глобальные потребности здравоохранения, удовлетворяемые Novavax» . Новавакс. Архивировано из оригинала 12 мая 2021 года . Проверено 30 января 2021 г.
- ^ Перейти обратно: а б Мудгал Р., Нехул С., Томар С. (декабрь 2020 г.). «Перспективы мукозальной вакцины: закрываем дверь перед SARS-CoV-2» . Человеческие вакцины и иммунотерапия . 16 (12): 2921–2931. дои : 10.1080/21645515.2020.1805992 . ПМЦ 7544966 . ПМИД 32931361 .
- ^ Перейти обратно: а б Ри Дж.Х. (2020). «Современные и новые подходы к доставке вакцин через слизистую оболочку». Слизистые вакцины . Эльзевир. стр. 325–356. дои : 10.1016/b978-0-12-811924-2.00019-5 . ISBN 9780128119242 . ПМК 7149853 .
- ^ «Живая аттенуированная вакцина против гриппа [LAIV] (вакцина против гриппа в виде назального спрея)» . Центры США по контролю и профилактике заболеваний (CDC). 3 августа 2021 года. Архивировано из оригинала 14 октября 2019 года . Проверено 8 сентября 2021 г.
- ^ «Две отечественные вакцины получили лицензию на экстренное использование» . Тегеран Таймс . 1 ноября 2021 г. Проверено 5 июня 2024 г.
- ^ Максимова К. «Ученый Центра Гамалеи рассказал о пользе назальной вакцины от коронавируса» . sibmeda.ru . Проверено 5 июня 2024 г.
- ^ «Одобрены две ингаляционные вакцины против коронавируса, но мы пока не знаем, насколько они хороши» . Обзор технологий Массачусетского технологического института . Архивировано из оригинала 21 октября 2022 года . Проверено 21 октября 2022 г.
- ^ Перейти обратно: а б Вальс Е (сентябрь 2022 г.). «Китай и Индия одобрили назальные вакцины против COVID – меняют ли они правила игры?» . Природа . 609 (7927): 450. Бибкод : 2022Natur.609..450W . дои : 10.1038/d41586-022-02851-0 . ПМИД 36071228 . S2CID 252121594 .
- ^ Дхама К., Дхаван М., Тивари Р., Эмран Т.Б., Митра С., Рабан А.А. и др. (ноябрь 2022 г.). «Интраназальные вакцины против COVID-19: современный прогресс, преимущества, перспективы и проблемы » Человеческие вакцины и иммунотерапия . 18 (5):2045853 дои : 10.1080/21645515.2022.2045853 . ПМЦ 8935456 . ПМИД 35258416 .
- ^ «Уведомление о выпуске плана реализации второй дозы ревакцинации новой коронавирусной вакцины» ) (на китайском языке 14 декабря 2022 г. Проверено 14 декабря 2022 г.
- ^ Перейти обратно: а б Нистор Г.И., Диллман Р.О., Роблес Р.М., Лэнгфорд Дж.Л., Пул А.Дж., Софро М.А. и др. (август 2022 г.). «Персональная дендритно-клеточная вакцина против COVID-19, изготовленная на месте: осуществимость, безопасность и антигенспецифический клеточный иммунный ответ» . Человеческие вакцины и иммунотерапия . 18 (6): 2100189. doi : 10.1080/21645515.2022.2100189 . ПМЦ 9746383 . ПМИД 36018753 .
- ^ «Дендритоклеточная вакцина AV-COVID-19 для предотвращения инфекции COVID-19» . ClinicalTrials.gov . 30 декабря 2020 года. Архивировано из оригинала 13 мая 2022 года . Проверено 5 сентября 2022 г.
- ^ «Профилактическая дендритно-клеточная вакцина AV-COVID-19 для субъектов, не активно инфицированных COVID-19» . ClinicalTrials.gov . 16 августа 2021 года. Архивировано из оригинала 18 июня 2022 года . Проверено 5 сентября 2022 г.
- ^ Маллин Э. (9 июня 2021 г.). «Универсальная» коронавирусная вакцина для предотвращения следующей пандемии . Научный американец . Архивировано из оригинала 20 декабря 2021 года . Проверено 20 декабря 2021 г.
- ^ Джой П. (13 июля 2021 г.). «Может ли универсальная вакцина от коронавируса вскоре стать реальностью?» . ГАВИ . Архивировано из оригинала 20 декабря 2021 года . Проверено 20 декабря 2021 г.
- ^ Буш Э. (15 декабря 2021 г.). «Фаучи настаивает на универсальной вакцине от коронавируса» . NBCNews . Архивировано из оригинала 20 декабря 2021 года . Проверено 20 декабря 2021 г.
- ^ «Национальный план готовности к COVID-19» (PDF) . Белый дом. Март 2022 г., стр. 9, 21, 29. Архивировано из оригинала (PDF) 26 марта 2022 г. . Проверено 29 марта 2022 г.
- ^ «Начинается первая фаза клинических испытаний вакцины против COVID-19, разработанной WRAIR» . 5 апреля 2022 года. Архивировано из оригинала 11 июля 2022 года . Проверено 11 июля 2022 г.
- ^ Обер Шепард Б.Л., Скотт П.Т., Хаттер Дж.Н., Ли С., МакКоли М.Д., Гузман И. и др. (Исследовательская группа EID-030) (июнь 2024 г.). «Вакцина на основе рекомбинантных спайков ферритина против SARS-CoV-2 с адъювантом армейского липосомального состава, содержащего монофосфориллипид A и QS-21: рандомизированное двойное слепое плацебо-контролируемое клиническое исследование фазы 1 на людях». «Ланцет». Микроб . 5 (6): е581–е593. дои : 10.1016/S2666-5247(23)00410-X . ПМЦ 11192176. ПМИД 38761816 .
- ^ Хариди Р. (7 июля 2022 г.). «Еще одна универсальная вакцина от коронавируса готова к испытаниям на людях» . Новый Атлас . Архивировано из оригинала 11 июля 2022 года . Проверено 11 июля 2022 г.
- ^ Перейти обратно: а б с Трегонинг Дж.С., Рассел Р.Ф., Киннер Э. (март 2018 г.). «Адъювантные вакцины против гриппа» . Человеческие вакцины и иммунотерапия . 14 (3): 550–564. дои : 10.1080/21645515.2017.1415684 . ПМЦ 5861793 . ПМИД 29232151 .
- ^ Перейти обратно: а б с д Ван Дж, Пэн Ю, Сюй Х, Цуй З, Уильямс Р.О. (август 2020 г.). «Гонка вакцин против COVID-19: проблемы и возможности в разработке вакцин» . AAPS PharmSciTech . 21 (6): 225. дои : 10.1208/s12249-020-01744-7 . ПМЦ 7405756 . ПМИД 32761294 .
- ^ «Обновленные вакцины против COVID-19 для использования в США, начиная с осени 2024 года» . США Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) . 5 июня 2024 г. Проверено 19 июня 2024 г.
 В данную статью включен текст из этого источника, находящегося в свободном доступе .
В данную статью включен текст из этого источника, находящегося в свободном доступе .
- ^ Симпсон С., Кауфманн М.К., Глозман В., Чакрабарти А. (май 2020 г.). «Болезнь X: ускорение разработки медицинских мер противодействия следующей пандемии» . «Ланцет». Инфекционные болезни . 20 (5): е108–15. дои : 10.1016/S1473-3099(20)30123-7 . ПМЦ 7158580 . ПМИД 32197097 .
- ^ Забалета Н., Дай В., Бхатт У., Херат С., Мезоннасс П., Чичестер Дж.А. и др. (август 2021 г.). «Однодозовая вакцина против COVID-19 на основе AAV, стабильная при комнатной температуре, обеспечивает длительную иммуногенность и защиту у приматов, кроме человека» . Клетка-хозяин и микроб . 29 (9): 1437–1453.e8. дои : 10.1016/j.chom.2021.08.002 . ПМЦ 8346325 . ПМИД 34428428 . S2CID 231676030 .
- ^ Перейти обратно: а б с Сэнгер Д.Э., Киркпатрик Д.Д., Циммер С., Томас К., Ви С.Л. (2 мая 2020 г.). «С ростом давления усиливается глобальная гонка за вакциной» . Нью-Йорк Таймс . ISSN 0362-4331 . Архивировано из оригинала 11 мая 2020 года . Проверено 2 мая 2020 г.
- ^ Перейти обратно: а б с д Стинхейсен Дж., Эйслер П., Мартелл А., Небехай С. (27 апреля 2020 г.). «Специальный отчет: страны и компании рискуют миллиардами в гонке за вакциной от коронавируса» . Рейтер. Архивировано из оригинала 15 мая 2020 года . Проверено 2 мая 2020 г.
- ^ Чон Хо Л., Чжэн В., Чжоу Л. (26 января 2020 г.). «Китайские учёные спешат разработать вакцину, поскольку число смертей от коронавируса резко возрастает» . Южно-Китайская Морнинг Пост . Архивировано из оригинала 26 января 2020 года . Проверено 28 января 2020 г.
- ^ Wee SL (4 мая 2020 г.). «Китайская кампания по вакцинации от коронавируса расширяет возможности проблемной отрасли» . Нью-Йорк Таймс . ISSN 0362-4331 . Архивировано из оригинала 4 мая 2020 года . Проверено 4 мая 2020 г.
- ^ Торп Х.Х. (март 2020 г.). «Недообещать, перевыполнить» . Наука . 367 (6485): 1405. Бибкод : 2020Sci...367.1405T . дои : 10.1126/science.abb8492 . ПМИД 32205459 . S2CID 214628067 .
- ^ Блэквелл Т. (20 апреля 2020 г.). «Исследователи вакцины против COVID-19 заявляют, что пандемический карантин создает множество серьезных препятствий в их работе» . Национальная почта . Архивировано из оригинала 24 апреля 2020 года . Проверено 3 мая 2020 г.
- ^ Чен Дж (4 мая 2020 г.). «Из-за Covid-19 закрылись лаборатории. Это может подвергнуть риску целое поколение исследователей» . Стат . Архивировано из оригинала 6 мая 2020 года . Проверено 4 мая 2020 г.
- ^ «Безопасность вакцин – вакцины» . Министерство здравоохранения и социальных служб США. Архивировано из оригинала 22 апреля 2020 года . Проверено 13 апреля 2020 г. .
- ^ «Процесс разработки лекарств» . США Управление по контролю за продуктами и лекарствами (FDA). 4 января 2018 г. Архивировано из оригинала 22 февраля 2020 г. . Проверено 12 апреля 2020 г.
- ^ Коэн Дж. (июнь 2020 г.). «Пандемическим вакцинам предстоит настоящее испытание» . Наука . 368 (6497): 1295–96. Бибкод : 2020Sci...368.1295C . дои : 10.1126/science.368.6497.1295 . ПМИД 32554572 . S2CID 219911109 .
- ^ Дюбе Э., Лаберж К., Гуай М., Брамадат П., Рой Р., Беттингер Дж. (август 2013 г.). «Нерешительность в отношении вакцинации: обзор» . Человеческие вакцины и иммунотерапия . 9 (8): 1763–73. дои : 10.4161/hv.24657 . ПМЦ 3906279 . ПМИД 23584253 .
- ^ Ховард Дж., Стракуалурси V (18 июня 2020 г.). «Фаучи предупреждает, что «антинаучная предвзятость» является проблемой в США» . CNN . Архивировано из оригинала 21 июня 2020 года . Проверено 21 июня 2020 г.
- ^ «Вакцины: процедура экстренной авторизации» . Европейское агентство лекарственных средств (EMA). 2020. Архивировано из оригинала 24 сентября 2020 года . Проверено 21 августа 2020 г.
- ^ Бирн Дж. (19 октября 2020 г.). «Современная вакцина против COVID-19 находится в стадии непрерывного рассмотрения в Канаде и ЕС» . BioPharma-Reporter.com, William Reed Business Media Ltd. Архивировано из оригинала 25 февраля 2021 года . Проверено 25 ноября 2020 г.
- ^ Дэнджерфилд К. (20 ноября 2020 г.). «Pfizer подает заявку на экстренное использование вакцины от коронавируса в США, а как насчет Канады?» . Глобальные новости . Архивировано из оригинала 25 января 2021 года . Проверено 25 ноября 2020 г.
- ^ «G20 запускает инициативу по инструментам здравоохранения, необходимым для борьбы с коронавирусом» . Глобус и почта . 25 апреля 2020 г. Архивировано из оригинала 27 апреля 2020 г. . Проверено 1 февраля 2021 г.
- ^ «Ускоритель доступа к инструментам борьбы с COVID-19 (ACT)» (PDF) . Всемирная организация здравоохранения (ВОЗ). 24 апреля 2020 г. Архивировано (PDF) из оригинала 25 апреля 2020 г. . Проверено 1 февраля 2021 г.
- ^ «ACT-Акселератор: часто задаваемые вопросы (FAQ)» . Всемирная организация здравоохранения (ВОЗ). 2020. Архивировано из оригинала 4 мая 2021 года . Проверено 16 декабря 2020 г.
- ^ «Обновленная информация об испытании солидарности ВОЗ: ускорение создания безопасной и эффективной вакцины против COVID-19» . Всемирная организация здравоохранения (ВОЗ). 27 апреля 2020 г. Архивировано из оригинала 30 апреля 2020 г. . Проверено 2 мая 2020 г.
Крайне важно оценить как можно больше вакцин, поскольку мы не можем предсказать, сколько из них окажутся жизнеспособными. Чтобы увеличить шансы на успех (учитывая высокий уровень сокращения числа вакцин в процессе разработки), мы должны тестировать все вакцины-кандидаты до тех пор, пока они не потерпят неудачу. [] ВОЗ работает над тем, чтобы все они имели возможность пройти тестирование на начальном этапе разработки. Результаты эффективности каждой вакцины ожидаются в течение трех-шести месяцев, и эти доказательства в сочетании с данными о безопасности послужат основой для принятия решений о том, можно ли ее использовать в более широком масштабе.
- ^ Абеди М (23 марта 2020 г.). «Канада потратит 192 миллиона долларов на разработку вакцины против COVID-19» . Глобальные новости . Архивировано из оригинала 9 апреля 2020 года . Проверено 24 марта 2020 г.
- ^ «Исследовательский ответ правительства Канады на COVID-19» . Правительство Канады. 23 апреля 2020 г. Архивировано из оригинала 13 мая 2020 г. . Проверено 4 мая 2020 г.
- ^ Такада Н., Сатаке М. (2 мая 2020 г.). «США и Китай развязывают кошельки в гонке за вакциной от коронавируса» . Азиатский обзор Nikkei . Архивировано из оригинала 10 мая 2020 года . Проверено 3 мая 2020 г.
- ^ Моррисс Э. (22 апреля 2020 г.). «Правительство создает рабочую группу по вакцине от коронавируса, когда начинаются клинические испытания на людях» . Фармафилд. Архивировано из оригинала 26 июня 2020 года . Проверено 3 мая 2020 г.
- ^ Кузня Р., Полглас К., Меццофиоре Дж. (1 мая 2020 г.). «В поисках вакцины США делают «большую ставку» на компании с непроверенными технологиями» . CNN . Архивировано из оригинала 13 мая 2020 года . Проверено 2 мая 2020 г.
- ^ Коэн Дж. (май 2020 г.). «Усилия США по созданию вакцины Warp Speed выходят из тени» . Наука . 368 (6492): 692–93. Бибкод : 2020Sci...368..692C . дои : 10.1126/science.368.6492.692 . ПМИД 32409451 .
- ^ Синк Дж., Фабиан Дж., Гриффин Р. (15 мая 2020 г.). «Трамп представляет лидеров «варп-скорости», чтобы ускорить вакцинацию от COVID-19» . Блумберг. Архивировано из оригинала 21 мая 2020 года . Проверено 15 мая 2020 г.
- ^ ЛаХусик К. (17 июня 2021 г.). «США вкладывают более 3 миллиардов долларов в исследования по борьбе с COVID-19, чтобы в течение года разработать противовирусную таблетку» . Жестокие биотехнологии . Архивировано из оригинала 9 октября 2021 года . Проверено 11 июля 2021 г.
- ^ Перейти обратно: а б «Отслеживание вакцины против COVID-19 (обновите URL-адрес, чтобы обновить)» . vac-lshtm.shinyapps.io . Лондонская школа гигиены и тропической медицины . 12 июля 2021 г. Проверено 10 марта 2021 г.
- ^ «Одобренные вакцины» . Программа отслеживания вакцин против COVID 19, Университет Макгилла. 12 июля 2021 г.
- ^ Грейнахер А., Тиле Т., Варкентин Т.Е., Вайссер К., Кирле П.А., Эйхингер С. (июнь 2021 г.). «Тромботическая тромбоцитопения после вакцинации ChAdOx1 nCov-19» . Медицинский журнал Новой Англии . 384 (22): 2092–101. дои : 10.1056/NEJMoa2104840 . ПМЦ 8095372 . ПМИД 33835769 .
- ^ Cines DB, Bussel JB (июнь 2021 г.). «Иммунная тромботическая тромбоцитопения, индуцированная вакциной SARS-CoV-2» . Медицинский журнал Новой Англии . 384 (23): 2254–2256. дои : 10.1056/NEJMe2106315 . ПМК 8063912 . ПМИД 33861524 .
- ^ Лю Ю, Шао З, Ван Х (декабрь 2021 г.). «Иммунная тромботическая тромбоцитопения, вызванная вакциной SARS-CoV-2» . Исследование тромбоза . 209 : 75–79. doi : 10.1016/j.thromres.2021.12.002 . ПМЦ 8647389 . ПМИД 34894531 .
- ^ Перейти обратно: а б Клок Ф.А., Пай М., Хейсман М.В., Макрис М. (ноябрь 2021 г.). «Вакцино-индуцированная иммунная тромботическая тромбоцитопения» . «Ланцет». Гематология . 9 (1): е73–е80. дои : 10.1016/S2352-3026(21)00306-9 . ПМЦ 8585488 . ПМИД 34774202 .
Хотя первоначально для описания синдрома использовалось несколько терминов… термин, получивший широкое распространение, — это вакцино-индуцированная иммунная тромботическая тромбоцитопения (ВИТТ). Также использовался тромбоз с синдромом тромбоцитопении, но это более общий термин, который может быть вызван другими состояниями.
- ^ Перейти обратно: а б с д Варкентин Т.Э., Пай М. (октябрь 2021 г.). «Редакционная статья о долгосрочном наблюдении Талера и др. после успешного лечения вакцин-индуцированной протромботической иммунной тромбоцитопении. Thromb Res 2021 в печати». Исследование тромбоза . 207 : 158–160. doi : 10.1016/j.thromres.2021.10.007 . ПМИД 34757250 . S2CID 239574011 .
Мы считаем, что название «ВИТТ» хорошо работает… этот термин четко обозначает ключевые особенности расстройства… обеспечивает полезную мнемонику для распознавания заболевания в обычной последовательности событий… не требует обязательного наличия тромбоза… «ТТС»… имеет ограниченное клиническое значение полезность, поскольку многие состояния... сопровождаются сочетанием тромбоза и тромбоцитопении.
- ^ Перейти обратно: а б «Использование вакцины AstraZeneca против COVID-19 у молодых людей» (пресс-релиз). Здоровье Канады. 29 марта 2021 года. Архивировано из оригинала 11 октября 2021 года . Проверено 2 апреля 2021 г.
- ^ Лонг Б., Бридвелл Р., Готлиб М. (ноябрь 2021 г.). «Тромбоз с синдромом тромбоцитопении, связанный с вакцинами против COVID-19» . Американский журнал неотложной медицины . 49 : 58–61. дои : 10.1016/j.ajem.2021.05.054 . ПМЦ 8143907 . ПМИД 34062319 .
- ^ «Вакцина AstraZeneca против COVID-19 (AZD1222)» (PDF) . Экстренное совещание ACIP по COVID-19 . АстраЗенека. 27 января 2021 г. Архивировано (PDF) из оригинала 27 января 2021 г. . Проверено 16 апреля 2021 г.
- ^ «Вакзеврия (ранее вакцина против COVID-19 AstraZeneca) EPAR» . Европейское агентство лекарственных средств (EMA) . 25 января 2021 года. Архивировано из оригинала 21 апреля 2021 года . Проверено 16 апреля 2021 г.
Название вакцины было изменено на Vaxzevria 25 марта 2021 года.
Vaxzevria (Вакцина против COVID-19 (рекомбинантная ChAdOx1-S) EMA/182334/2021. Архивировано 15 апреля 2021 года в Wayback Machine. Текст скопирован из этого источника, права на который принадлежат European Medicines. Агентство. Воспроизведение разрешено при условии указания источника. - ^ «Вакцина против коронного вируса ChAdOx1 nCoV-19 (рекомбинантная) — Ковишилд» . Индийский институт сывороток . Архивировано из оригинала 19 апреля 2021 года . Проверено 16 апреля 2021 г.
- ^ «AstraZeneca ChAdOx1-S/nCoV-19 [рекомбинантная] вакцина против COVID-19» . Всемирная организация здравоохранения (ВОЗ) . Архивировано из оригинала 28 ноября 2021 года . Проверено 28 ноября 2021 г.
- ^ Перейти обратно: а б «Обновление безопасности вакцины против COVID-19: Вакзеврия» (PDF) . Европейское агентство лекарственных средств (EMA). 28 марта 2021 г. Архивировано (PDF) из оригинала 13 апреля 2021 г. . Проверено 31 марта 2021 г.
- ^ Маркс П. «Совместное заявление CDC и FDA о вакцине Johnson & Johnson против COVID-19» . Архивировано из оригинала 20 мая 2021 года . Проверено 13 апреля 2021 г.
- ^ «Обновление о коронавирусе (COVID-19): FDA ограничивает использование вакцины Janssen против COVID-19 определенными лицами» . Управление по контролю за продуктами и лекарствами США . 5 мая 2022 года. Архивировано из оригинала 7 мая 2022 года . Проверено 7 мая 2022 г.
- ^ Медицинский директор AstraZeneca AB (13 апреля 2021 г.). «Прямое общение с медицинским работником (DHPC): Вакзеврия (ранее вакцина против COVID-19 AstraZeneca): связь между вакциной и возникновением тромбоза в сочетании с тромбоцитопенией» (PDF) . Европейское агентство лекарственных средств (EMA). Архивировано (PDF) из оригинала 18 июля 2022 года . Проверено 13 апреля 2021 г.
- ^ «Исследования и анализ — Вакцина от коронавируса — еженедельная сводка отчетов по желтой карточке» . Агентство по регулированию лекарственных средств и товаров медицинского назначения (MHRA). 1 апреля 2021 года. Архивировано из оригинала 20 мая 2021 года . Проверено 3 апреля 2020 г. .
- ^ EMA (7 апреля 2021 г.). Пресс-конференция EMA 7 апреля — Заключение оценки Комитета по оценке риска фармаконадзора (PRAC) вакцины против COVID-19 AstraZeneca и тромбоэмболических событий . Европейское агентство лекарственных средств (EMA) . Архивировано из оригинала 7 апреля 2021 года . Получено 7 апреля 2021 г. - через Youtube.
- ^ Агентства (29 апреля 2024 г.). «Отчет: AstraZeneca признала в судебном документе, что вакцина против Covid может вызвать редкий побочный эффект [NSTTV] | New Straits Times» . НСТ Онлайн . Архивировано из оригинала 30 апреля 2024 года . Проверено 29 апреля 2024 г.
- ^ «Во-первых, AstraZeneca признает, что ее вакцина против Covid может вызывать редкие тромбы» . Независимый . 30 апреля 2024 года. Архивировано из оригинала 30 апреля 2024 года . Проверено 30 апреля 2024 г.
- ^ «Хронология Всемирной организации здравоохранения – COVID-19» . Всемирная организация здравоохранения (ВОЗ). 27 апреля 2020 г. Архивировано из оригинала 29 апреля 2020 г. . Проверено 2 мая 2020 г.
- ^ Перейти обратно: а б с Тхань Ле Т., Андредакис З., Кумар А., Гомес Роман Р., Толлефсен С., Сэвилл М. и др. (май 2020 г.). «Ситуация разработки вакцины против COVID-19» . Обзоры природы. Открытие наркотиков . 19 (5): 305–306. дои : 10.1038/d41573-020-00073-5 . ПМИД 32273591 .
- ^ Перейти обратно: а б Ворота Б (февраль 2020 г.). «Реакция на Covid-19: пандемия, которая случается раз в столетие?» . Медицинский журнал Новой Англии . 382 (18): 1677–79. дои : 10.1056/nejmp2003762 . ПМИД 32109012 .
- ^ Фаучи А.С., Лейн ХК, Редфилд Р.Р. (март 2020 г.). «Covid-19: путешествие по неизведанному» . Медицинский журнал Новой Англии . 382 (13): 1268–69. дои : 10.1056/nejme2002387 . ПМЦ 7121221 . ПМИД 32109011 .
- ^ Перейти обратно: а б Ле Т.Т., Крамер Дж.П., Чен Р., Мэйхью С. (октябрь 2020 г.). «Эволюция ландшафта разработки вакцин против COVID-19» . Обзоры природы. Открытие наркотиков . 19 (10): 667–668. дои : 10.1038/d41573-020-00151-8 . ПМИД 32887942 . S2CID 221503034 .
- ^ Вайнтрауб Р., Ядав П., Беркли С. (2 апреля 2020 г.). «Вакцина против COVID-19 потребует справедливого глобального распространения» . Гарвардское деловое обозрение . ISSN 0017-8012 . Архивировано из оригинала 9 июня 2020 года . Проверено 9 июня 2020 г.
- ^ «Пандемия COVID-19 обнажает риски, связанные с использованием частного сектора в производстве жизненно важных вакцин, — говорит эксперт» . Радио Си-Би-Си . 8 мая 2020 г. Архивировано из оригинала 13 мая 2020 г. . Проверено 8 июня 2020 г.
- ^ Ахмед Д.Д. (4 июня 2020 г.). «Сделка Оксфорда и AstraZeneca по борьбе с COVID-19 укрепляет «суверенитет вакцин» » . Стат . Архивировано из оригинала 12 июня 2020 года . Проверено 8 июня 2020 г.
- ^ Гренфелл Р., Дрю Т. (14 февраля 2020 г.). «Вот почему ВОЗ заявляет, что до создания вакцины от коронавируса осталось 18 месяцев» . Бизнес-инсайдер . Архивировано из оригинала 5 декабря 2020 года . Проверено 11 ноября 2020 г.
- ^ Оффит П (13 февраля 2021 г.). «TWiV 720: Оффит занимается вакцинами» . Подкаст «Эта неделя вирусологии» . Канал Винсента Раканьелло на YouTube. Архивировано из оригинала 25 мая 2021 года . Проверено 14 июля 2021 г.
- ^ «Обновленная информация об испытании солидарности ВОЗ: ускорение создания безопасной и эффективной вакцины против COVID-19» . Всемирная организация здравоохранения (ВОЗ). 27 апреля 2020 г. Архивировано из оригинала 30 апреля 2020 г. . Проверено 2 мая 2020 г.
Крайне важно оценить как можно больше вакцин, поскольку мы не можем предсказать, сколько из них окажутся жизнеспособными. Чтобы увеличить шансы на успех (учитывая высокий уровень сокращения числа вакцин в процессе разработки), мы должны тестировать все вакцины-кандидаты до тех пор, пока они не потерпят неудачу. [] ВОЗ работает над тем, чтобы все они имели возможность пройти тестирование на начальном этапе разработки. Результаты эффективности каждой вакцины ожидаются в течение трех-шести месяцев, и эти доказательства в сочетании с данными о безопасности послужат основой для принятия решений о том, можно ли ее использовать в более широком масштабе.
- ^ Ями Дж., Шеферхофф М., Хэтчетт Р., Пейт М., Чжао Ф., МакДейд К.К. (май 2020 г.). «Обеспечение глобального доступа к вакцинам против COVID‑19» . Ланцет . 395 (10234): 1405–06. дои : 10.1016/S0140-6736(20)30763-7 . ПМЦ 7271264 . ПМИД 32243778 .
По оценкам CEPI, разработка до трех вакцин в ближайшие 12–18 месяцев потребует инвестиций в размере не менее 2 миллиардов долларов США . Эта оценка включает в себя клинические испытания фазы 1 восьми вакцин-кандидатов, продвижение до шести кандидатов через испытания фазы 2 и 3, выполнение нормативных требований и требований к качеству как минимум для трех вакцин, а также расширение глобальных производственных мощностей для трех вакцин.
- ^ «ВОЗ поддержала экстренное использование Китаем экспериментальных вакцин против Covid-19» . Южно-Китайская Морнинг Пост . 25 сентября 2020 года. Архивировано из оригинала 26 сентября 2020 года . Проверено 26 сентября 2020 г.
- ^ Крамер А.Е. (19 сентября 2020 г.). «Россия медленно вводит вакцину от вируса, несмотря на одобрение Кремля» . Нью-Йорк Таймс . ISSN 0362-4331 . Архивировано из оригинала 27 сентября 2020 года . Проверено 28 сентября 2020 г.
- ^ «Pfizer и BioNTech сегодня подадут в FDA США запрос на разрешение на экстренное использование вакцины против COVID-19» . Pfizer (пресс-релиз). 20 ноября 2020 года. Архивировано из оригинала 29 января 2021 года . Проверено 20 ноября 2020 г.
- ^ Парк А (20 ноября 2020 г.). «Эксклюзив: генеральный директор Pfizer обсуждает подачу первого запроса на одобрение вакцины против COVID-19 в FDA» . Время . Архивировано из оригинала 29 января 2021 года . Проверено 20 ноября 2020 г.
- ^ «Информация для медицинских работников о вакцине Pfizer/BioNTech против COVID-19» . Агентство по регулированию лекарственных средств и товаров медицинского назначения (MHRA) . 8 декабря 2020 года. Архивировано из оригинала 15 марта 2021 года . Проверено 13 декабря 2020 г.
- ^ «Условия авторизации вакцины Pfizer/BioNTech против COVID-19» . Агентство по регулированию лекарственных средств и товаров медицинского назначения (MHRA) . 3 декабря 2020 года. Архивировано из оригинала 26 февраля 2021 года . Проверено 19 декабря 2020 г.
- ^ «Регулятор лекарственных средств Великобритании одобрил первую вакцину против COVID-19 в Великобритании» . Агентство по регулированию лекарственных средств и товаров медицинского назначения, Правительство Великобритании. 2 декабря 2020 года. Архивировано из оригинала 17 марта 2021 года . Проверено 2 декабря 2020 г.
- ^ Мюллер Б. (2 декабря 2020 г.). «Великобритания впервые на Западе одобрила вакцину от коронавируса Pfizer» . Нью-Йорк Таймс . Архивировано из оригинала 28 января 2021 года . Проверено 2 декабря 2020 г.
- ^ Робертс М. (2 декабря 2020 г.). «Вакцина Covid Pfizer одобрена для использования на следующей неделе в Великобритании» . Новости BBC онлайн . Архивировано из оригинала 2 декабря 2020 года . Проверено 2 декабря 2020 г.
- ^ «Вопросы и ответы: вакцинация против COVID-19 в ЕС» . Европейская комиссия . 21 декабря 2020 года. Архивировано из оригинала 29 января 2021 года . Проверено 21 декабря 2020 г. .
- ^ «Бахрейн вторым в мире одобрил вакцину Pfizer/BioNTech Covid-19» . Агентство новостей Бахрейна. 4 декабря 2020 года. Архивировано из оригинала 17 декабря 2020 года . Проверено 9 декабря 2020 г.
- ^ «ОАЭ: Министерство здравоохранения заявляет о 86-процентной эффективности вакцины» . Новости Персидского залива . Архивировано из оригинала 24 декабря 2020 года . Проверено 9 декабря 2020 г.
- ^ Томас К., Лафраньер С., Вейланд Н., Гудноу А., Хаберман М. (12 декабря 2020 г.). «FDA одобрило вакцину Pfizer, и миллионы доз будут немедленно отправлены» . Нью-Йорк Таймс . Архивировано из оригинала 12 декабря 2020 года . Проверено 12 декабря 2020 г. .
- ^ «FDA принимает дополнительные меры в борьбе с COVID-19, выдавая разрешение на экстренное использование второй вакцины против COVID-19» . США Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) (пресс-релиз). Архивировано из оригинала 17 марта 2021 года . Проверено 18 декабря 2020 г.
- ^ Оливер С.Е., Гаргано Дж.В., Марин М., Уоллес М., Карран К.Г., Чемберленд М. и др. (январь 2021 г.). «Временная рекомендация Консультативного комитета по практике иммунизации по использованию вакцины Moderna против COVID-19 — США, декабрь 2020 г.» (PDF) . ММВР. Еженедельный отчет о заболеваемости и смертности . 69 (5152): 1653–56. doi : 10.15585/mmwr.mm695152e1 . ПМК 9191904 . ПМИД 33382675 . S2CID 229945697 . Архивировано (PDF) из оригинала 9 февраля 2021 года . Проверено 18 января 2021 г.
- ^ Лавлейс-младший Б. (19 декабря 2020 г.). «FDA одобряет вторую вакцину от Covid для экстренного использования, поскольку она разрешает распространение вакцины Moderna в США» . CNBC. Архивировано из оригинала 26 января 2021 года . Проверено 19 декабря 2020 г.
- ^ Корум Дж., Циммер С. (17 декабря 2020 г.). «Как действует вакцина Оксфорд-АстраЗенека» . Нью-Йорк Таймс . Архивировано из оригинала 5 января 2022 года . Проверено 2 мая 2021 г.
- ^ Тетро-Фарбер М., Васильева Г. (31 марта 2021 г.). «В России зарегистрирована первая в мире вакцина для животных от COVID-19» . Рейтер . Архивировано из оригинала 17 декабря 2021 года . Проверено 4 апреля 2021 г.
- ^ "В России зарегистрировали первую в мире вакцину против COVID-19 для животных" [The world's first COVID-19 vaccine for animals was registered in Russia]. TASS (in Russian). Moscow. 31 March 2021. Archived from the original on 19 May 2021 . Retrieved 19 May 2021 .
- ^ МОРИЦУГУ К. (26 октября 2022 г.). «Боишься игл? Китай использует ингаляционную вакцину против COVID-19» . АП НОВОСТИ . Проверено 2 ноября 2022 г.
- ^ Хотез П.Дж., Боттацци М.Э. (январь 2022 г.). «Цельноинактивированные вирусные и белковые вакцины против COVID-19» . Ежегодный обзор медицины . 73 (1): 55–64. doi : 10.1146/annurev-med-042420-113212 . ПМИД 34637324 . S2CID 238747462 .
- ^ Е Ю, Чжан Ц, Вэй Икс, Цао З, Юань ХИ, Цзэн ДД (февраль 2022 г.). «Справедливый доступ к вакцинам против COVID-19 имеет жизненно важное значение для всех стран» . Природа человеческого поведения . 6 (2): 207–216. дои : 10.1038/s41562-022-01289-8 . ПМЦ 8873023 . ПМИД 35102361 .
- ^ Ли Проктор, Полные последовательности нуклеотидных оснований для всех вакцин против COVID, одобренных MRHA , WhatDo TheyKnow , Wikidata Q109371097
- ^ Тейлор Р. (2 ноября 2021 г.). «Последовательности вакцин против Covid-19, опубликованные через WhatDo TheyKnow» . мое общество . Архивировано из оригинала 5 ноября 2021 года . Проверено 2 ноября 2021 г.
- ^ «Данные о смертности от COVID-19 в зависимости от прививочного статуса» . Наш мир в данных (данные CDC). Апрель 2023 г. Архивировано из оригинала 16 октября 2023 г.
Источник данных: Центры по контролю и профилактике заболеваний, Группа по разработке вакцин/надзору и аналитике.
- ^ Ян З.Р., Цзян Ю.В., Ли Ф.К., Лю Д., Линь Т.Ф., Чжао З.И. и др. (апрель 2023 г.). «Эффективность вакцин против SARS-CoV-2 и взаимосвязь доза-реакция с тремя основными антителами: систематический обзор и метаанализ рандомизированных контролируемых исследований» . «Ланцет». Микроб . 4 (4): е236–е246. дои : 10.1016/S2666-5247(22)00390-1 . ПМЦ 9974155 . ПМИД 36868258 .
- ^ Холкомб М., Уолдроп Т. (11 сентября 2021 г.). «Исследование CDC: у непривитых в 11 раз больше шансов умереть от Covid-19» . CNN . Проверено 11 сентября 2021 г.
- ^ Скоби Х.М., Джонсон А.Г., Сутар А.Б., Северсон Р., Олден Н.Б., Балтер С. и др. (сентябрь 2021 г.). «Мониторинг заболеваемости, госпитализаций и смертей от COVID-19 в зависимости от статуса вакцинации – 13 юрисдикций США, 4 апреля – 17 июля 2021 г.» (PDF) . ММВР. Еженедельный отчет о заболеваемости и смертности . 70 (37): 1284–1290. doi : 10.15585/mmwr.mm7037e1 . ПМЦ 8445374 . ПМИД 34529637 .
- ^ Фаулкс А., Гаглани М., Грувер К., Тиз М.С., Тайнер Х., Эллингсон К. (август 2021 г.). «Эффективность вакцин против COVID-19 в предотвращении заражения SARS-CoV-2 среди работников первой линии до и во время преобладания варианта B.1.617.2 (Дельта) – восемь регионов США, декабрь 2020 г. – август 2021 г.» (PDF) . ММВР. Еженедельный отчет о заболеваемости и смертности . 70 (34): 1167–1169. дои : 10.15585/mmwr.mm7034e4 . ПМЦ 8389394 . ПМИД 34437521 .
- ^ Шрайбер М., Чайка К., Чайка К., Бейерштейн Л., Бейерштейн Л., Уилсон Дж. и др. (1 июля 2021 г.). «Срочное послание для Америки о варианте Delta Covid» . Новая Республика . ISSN 0028-6583 . Архивировано из оригинала 28 августа 2021 года . Проверено 28 октября 2021 г.
- ^ «Среди непривитых вариант Дельта увеличивает риск госпитализации более чем в два раза» . Лос-Анджелес Таймс . 28 августа 2021 года. Архивировано из оригинала 8 ноября 2021 года.
- ^ «ВОЗ/ECDC: Почти полмиллиона жизней спасены благодаря вакцинации против COVID-19 менее чем за год» . 25 ноября 2021 г.
- ^ «Бустер-вакцина от коронавируса (COVID-19)» . Национальная служба здравоохранения . Государственная цифровая служба. 17 сентября 2021 г. Проверено 11 декабря 2021 г.
- ^ Варианты SARS-CoV-2, вызывающие обеспокоенность, и варианты, находящиеся на стадии расследования в Англии, технический брифинг 31 (PDF) (Брифинг). Общественное здравоохранение Англии. 10 декабря 2021 г. стр. 3–5, 20–22. ГОВ-10645. Архивировано (PDF) из оригинала 18 декабря 2021 года . Проверено 10 декабря 2021 г.
- ^ Гор Д. (9 февраля 2022 г.). «Последние данные CDC: у непривитых взрослых в 97 раз больше шансов умереть от COVID-19, чем у привитых взрослых» . FactCheck.org . Проверено 11 февраля 2022 г.
- ^ Ли А.Р., Вонг С.Ю., Чай Л.И., Ли С.К., Ли М.Х., Мутиа М.Д. и др. (март 2022 г.). «Эффективность вакцин против Covid-19 у пациентов с ослабленным иммунитетом: систематический обзор и метаанализ» . БМЖ . 376 : e068632. дои : 10.1136/bmj-2021-068632 . ПМЦ 8889026 . ПМИД 35236664 .
- ^ Гринбергер Л.М., Зальцман Л.А., Сенефельд Дж.В., Джонсон П.В., ДеДженнаро Л.Дж., Николс Г.Л. (август 2021 г.). «Реакция антител на вакцины SARS-CoV-2 у пациентов с гематологическими злокачественными новообразованиями» . Раковая клетка . 39 (8): 1031–1033. doi : 10.1016/j.ccell.2021.07.012 . ПМЦ 8295014 . ПМИД 34331856 .
- ^ Штейн С., Нассерельдин Х., Соренсен Р.Дж., Амлаг Дж.О., Бисиньяно С., Бирн С. и др. (февраль 2023 г.). «Защита от прошлой инфекции SARS-CoV-2 от повторного заражения: систематический обзор и метаанализ» . Ланцет . 401 (10379): 833–842. дои : 10.1016/S0140-6736(22)02465-5 . ISSN 0140-6736 . ПМЦ 9998097 . ПМИД 36930674 .
- ^ Пейн AB (2024). «Эффективность вакцин против COVID-19 с бивалентной мРНК в предотвращении тромбоэмболических событий, связанных с COVID-19, среди участников программы Medicare в возрасте ≥65 лет и лиц с терминальной стадией заболевания почек — США, сентябрь 2022 г. – март 2023 г.» . ММВР. Еженедельный отчет о заболеваемости и смертности . 73 (1): 16–23. дои : 10.15585/mmwr.mm7301a4 . ISSN 0149-2195 . ПМЦ 10794061 . ПМИД 38206877 . Архивировано из оригинала 14 января 2024 года . Проверено 14 января 2024 г.
- ^ Крот Б (12 января 2024 г.). «Прививки от COVID защищают от инсультов и сердечных приступов, связанных с COVID, — результаты исследования» . Арс Техника . Архивировано из оригинала 14 января 2024 года . Проверено 14 января 2024 г.
- ^ Катала М., Меркаде-Бесора Н., Кольде Р., Трин Н.Т., Роэль Э., Берн Э. и др. (март 2024 г.). «Эффективность вакцин против COVID-19 для предотвращения длительных симптомов COVID: поэтапное когортное исследование данных из Великобритании, Испании и Эстонии» . «Ланцет». Респираторная медицина . 12 (3): 225–236. дои : 10.1016/s2213-2600(23)00414-9 . ПМИД 38219763 .
- ^ «Вакцины снижают риск длительного заболевания COVID» . Доказательства НИХР . 2024. doi : 10.3310/nihrevidence_63203 .
- ^ Перейти обратно: а б с д и ж «Краткий научный обзор: иммунитет, вызванный инфекцией и вакцинацией SARS-CoV-2» . Центры по контролю и профилактике заболеваний (CDC) . 29 октября 2021 года. Архивировано из оригинала 4 декабря 2021 года . Проверено 4 декабря 2021 г.
 В данную статью включен текст из этого источника, находящегося в свободном доступе .
В данную статью включен текст из этого источника, находящегося в свободном доступе .
- ^ Левин Э.Г., Люстиг Ю., Коэн С., Флусс Р., Инденбаум В., Амит С. и др. (декабрь 2021 г.). «Снижение иммунно-гуморального ответа на вакцину BNT162b2 Covid-19 в течение 6 месяцев» . Медицинский журнал Новой Англии . 385 (24): е84. дои : 10.1056/NEJMoa2114583 . ПМЦ 8522797 . ПМИД 34614326 .
- ^ «Бустер-инъекция COVID-19» . Центры по контролю и профилактике заболеваний . 29 ноября 2021 года. Архивировано из оригинала 21 августа 2021 года . Проверено 4 декабря 2021 г.
- ^ Перейти обратно: а б с Девлин Х (18 марта 2022 г.). «У жителей домов престарелых в Англии резко снижается иммунитет к Covid – исследование» . Хранитель . Архивировано из оригинала 23 марта 2022 года . Проверено 12 мая 2022 г.
- ^ Кимбалл С. «CDC рекомендует четвертую дозу вакцины Pfizer и Moderna Covid для людей в возрасте 50 лет и старше» . CNBC . Архивировано из оригинала 3 сентября 2022 года . Проверено 22 августа 2022 г.
- ^ "Коронавирус заболевание 2019" . Центры по контролю и профилактике заболеваний (пресс-релиз). 29 марта 2022 года. Архивировано из оригинала 1 сентября 2022 года . Проверено 22 августа 2022 г.
- ^ Ван Р., Чен Дж., Вэй Г.В. (декабрь 2021 г.). «Механизмы эволюции SARS-CoV-2, выявляющие мутации, устойчивые к вакцинам, в Европе и Америке» (PDF) . Журнал физической химии . 12 (49): 11850–11857. doi : 10.1021/acs.jpclett.1c03380 . ПМЦ 8672435 . ПМИД 34873910 . Архивировано (PDF) из оригинала 18 декабря 2021 года . Проверено 27 января 2022 г.
- ^ «Результаты исследования показывают, что распространение Омикрона можно объяснить уклончивостью иммунитета, а не увеличением заразности» . Новости-Medical.net . 5 января 2022 года. Архивировано из оригинала 21 января 2022 года . Проверено 17 января 2022 г.
- ^ Цао Ю, Ван Дж, Цзянь Ф, Сяо Т, Сун В, Исимайи А и др. (февраль 2022 г.). «Омикрон ускользает от большинства существующих антител, нейтрализующих SARS-CoV-2» . Природа . 602 (7898): 657–663. дои : 10.1038/d41586-021-03796-6 . ПМЦ 8866119 . ПМИД 35016194 . S2CID 245455422 .
- ^ Лю Л., Икетани С., Го Й., Чан Дж.Ф., Ван М., Лю Л. и др. (февраль 2022 г.). «Поразительное уклонение от антител, проявленное вариантом Омикрон SARS-CoV-2» . Природа . 602 (7898): 676–681. дои : 10.1038/d41586-021-03826-3 . ПМИД 35016198 . S2CID 245462866 .
- ^ Мохсин М., Махмуд С. (май 2022 г.). «Вызывающий обеспокоенность вариант Omicron SARS-CoV-2: обзор его заразности, уклонения от иммунитета, повторного заражения и тяжести» . Лекарство . 101 (19): e29165. дои : 10.1097/MD.0000000000029165 . ПМЦ 9276130 . ПМИД 35583528 . S2CID 248858919 .
- ^ «Как скоро после заражения COVID-19 вы сможете заразиться снова?» . Новости АВС . 2 мая 2022 года. Архивировано из оригинала 9 июля 2022 года . Проверено 24 июня 2022 г.
- ^ «Вариант Омикрон: что нужно знать» . Центры по контролю и профилактике заболеваний . 20 декабря 2021 года. Архивировано из оригинала 27 января 2022 года . Проверено 27 января 2022 г.
- ^ Шин Д.Х., Смит Д.М., Чой Дж.Ю. (2022). «Вариант Омикрона SARS-CoV-2, вызывающий беспокойство: все, что вы хотели знать об Омикроне, но боялись спросить» . Медицинский журнал Йонсей . 63 (11): 977–983. дои : 10.3349/ymj.2022.0383 . ПМЦ 9629902 . ПМИД 36303305 .
- ^ «Бустерная вакцина против COVID-19» . США Управление по контролю за продуктами и лекарствами (FDA). 27 сентября 2022 года. Архивировано из оригинала 8 октября 2022 года . Проверено 8 октября 2022 г.
- ^ «Современные вакцины против COVID-19» . Управление по контролю за продуктами и лекарствами США . 7 октября 2022 года. Архивировано из оригинала 7 октября 2022 года . Проверено 8 октября 2022 г.
- ^ «Вакцины Pfizer-BioNTech против COVID-19» . Управление по контролю за продуктами и лекарствами США . 3 октября 2022 года. Архивировано из оригинала 8 октября 2022 года . Проверено 8 октября 2022 г.
- ^ «Обновленные вакцины против COVID-19 для использования в США, начиная с осени 2023 года» . США Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) . 15 июня 2023 года. Архивировано из оригинала 17 июня 2023 года . Проверено 16 июня 2023 г.
 В данную статью включен текст из этого источника, находящегося в свободном доступе .
В данную статью включен текст из этого источника, находящегося в свободном доступе .
- ^ Рекомендации по формуле вакцин против COVID-19 на 2023–2024 годы в США (PDF) (Отчет). США Управление по контролю за продуктами и лекарствами (FDA). 16 июня 2023 года. Архивировано из оригинала 16 июня 2023 года . Проверено 16 июня 2023 г.
- ^ «Обновленные вакцины против COVID-19 для использования в США, начиная с осени 2024 года» . США Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) . 5 июня 2024 года. Архивировано из оригинала 18 июня 2024 года . Проверено 19 июня 2024 г.
 В данную статью включен текст из этого источника, находящегося в свободном доступе .
В данную статью включен текст из этого источника, находящегося в свободном доступе .
- ^ Синганаягам А., Хакки С., Даннинг Дж., Мэдон К.Дж., Кроун М.А., Койчева А. и др. (февраль 2022 г.). «Передача среди населения и кинетика вирусной нагрузки дельта-варианта SARS-CoV-2 (B.1.617.2) у вакцинированных и невакцинированных лиц в Великобритании: проспективное продольное когортное исследование» . «Ланцет». Инфекционные болезни . 22 (2): 183–195. дои : 10.1016/S1473-3099(21)00648-4 . ПМЦ 8554486 . ПМИД 34756186 .
- ^ Каллауэй Э (октябрь 2021 г.). «Комбинированные вакцины против COVID проходят проверку на эффективность». Природа . дои : 10.1038/d41586-021-02853-4 . PMID 34675430 . S2CID 239455075 .
- ^ Рашеди Р., Самифар Н., Масуми Н., Мохсени С., Резаи Н. (апрель 2022 г.). «Смешивание вакцин против COVID-19: концепция, эффективность и сомнения» . Журнал медицинской вирусологии . 94 (4): 1294–1299. дои : 10.1002/jmv.27463 . ПМЦ 8661746 . ПМИД 34796525 .
- ^ Купайе Х., Ансари Х. (август 2022 г.). «Неблагоприятные явления после вакцинации против COVID-19: систематический обзор и метаанализ» . Международная иммунофармакология . 109 : 108906. doi : 10.1016/j.intimp.2022.108906 . ПМЦ 9148928 . ПМИД 35671640 .
- ^ Гранья С., Гон Л., Евреноглу Т., Харде А., Миноцци С., Бергман Х. и др. (декабрь 2022 г.). «Эффективность и безопасность вакцин против COVID-19» . Кокрановская база данных систематических обзоров . 12 (12): CD015477. дои : 10.1002/14651858.CD015477 . ПМЦ 9726273 . ПМИД 36473651 .
- ^ Хаас Дж.В., Бендер Ф.Л., Баллоу С., Келли Дж.М., Вильгельм М., Миллер Ф.Г. и др. (январь 2022 г.). «Частота нежелательных явлений в группах плацебо в испытаниях вакцины против COVID-19: систематический обзор и метаанализ» . Открытая сеть JAMA . 5 (1): e2143955. doi : 10.1001/jamanetworkopen.2021.43955 . ПМЦ 8767431 . ПМИД 35040967 .
- ^ Полания Гутьеррес Дж. Джей, Мунакоми С (январь 2020 г.). «Внутримышечная инъекция» . СтатПерлс . Остров сокровищ (Флорида): StatPearls Publishing. ПМИД 32310581 . Архивировано из оригинала 8 декабря 2020 года . Проверено 24 июля 2021 г.
- ^ Перейти обратно: а б с д Хуан Цзы, Су Ю, Чжан Т, Ся Н (февраль 2022 г.). «Обзор безопасности и эффективности существующих вакцин против COVID-19» . Границы медицины . 16 (1): 39–55. дои : 10.1007/s11684-021-0893-y . ПМЦ 8815389 . ПМИД 35122210 .
- ^ Ту В., Джерада Д.С., Джо Б.Н. (май 2021 г.). «Лимфаденопатия, связанная с вакцинацией COVID-19: что следует знать» . Радиология. Изображение рака . 3 (3): e210038. дои : 10.1148/rycan.2021210038 . ПМК 8049171 . ПМИД 33874733 .
- ^ «Отчет о доклинической оценке: вакцина BNT162b2 [мРНК] против COVID-19» (PDF) . Министерство здравоохранения Австралии: Управление терапевтических товаров . Архивировано (PDF) из оригинала 28 марта 2023 года . Проверено 25 марта 2023 г.
- ^ Перейти обратно: а б с д и Мале V (январь 2022 г.). «Менструация и вакцинация против covid-19» . БМЖ . 376 :о142. дои : 10.1136/bmj.o142 . hdl : 10044/1/94577 . ПМИД 35082132 . S2CID 246287912 .
- ^ Монтгомери Дж., Райан М., Энглер Р., Хоффман Д., МакКленатан Б., Коллинз Л. и др. (октябрь 2021 г.). «Миокардит после иммунизации мРНК вакциной против COVID-19 у военнослужащих США» . JAMA Кардиология . 6 (10): 1202–06. дои : 10.1001/jamacardio.2021.2833 . ПМЦ 8243257 . ПМИД 34185045 .
- ^ «Всемирная организация здравоохранения (ВОЗ)» . 17 сентября 2018 года. Архивировано из оригинала 4 октября 2023 года . Проверено 19 сентября 2023 г.
- ^ Макдональд Дж. (23 декабря 2021 г.). «Увеличение количества отчетов VAERS о COVID-19 из-за требований к отчетности и тщательного изучения широко применяемых вакцин» . FactCheck.org . Архивировано из оригинала 20 мая 2022 года . Проверено 20 мая 2022 г.
- ^ «Лечение поствакцинального синдрома» . Немецкая волна . 11 октября 2022 года. Архивировано из оригинала 17 апреля 2023 года.
- ^ «Час специальных консультаций Post-Vax» [Специальная консультация после вакцинации]. Университетская больница Гиссена и Марбурга (UKGM) (на немецком языке). Архивировано из оригинала 4 мая 2023 года.
- ^ «Ущерб от вакцины от короны: Университетская больница Марбурга открывает собственную амбулаторию» [Ущерб от вакцины от короны: Университетская больница Марбурга открывает собственную амбулаторию]. Frankfurter Allgemeine Zeitung GmbH (на немецком языке). 3 апреля 2023 г. Архивировано из оригинала 8 марта 2024 г.
- ^ Фронтера Дж.А., Тамборска А.А., Дохейм М.Ф., Гарсия-Азорин Д., Гезеген Х., Гехт А. и др. (март 2022 г.). «Неврологические явления, зарегистрированные после вакцинации против COVID-19: анализ VAERS» . Анналы неврологии . 91 (6): 756–771. дои : 10.1002/ana.26339 . ПМЦ 9082459 . ПМИД 35233819 .
- ^ Перейти обратно: а б с д Альтманн Д.М., Бойтон Р.Дж. (март 2022 г.). «Вакцинация против COVID-19: путь вперед». Наука . 375 (6585): 1127–1132. Бибкод : 2022Sci...375.1127A . дои : 10.1126/science.abn1755 . ПМИД 35271316 . S2CID 247384207 .
- ^ Перейти обратно: а б Обновленная информация о безопасности вакцин против COVID-19 (PDF) (Отчет). Архивировано (PDF) из оригинала 3 августа 2022 года . Проверено 6 сентября 2022 г.
- ^ Бассо С. (октябрь 2022 г.). "Миокардит". Медицинский журнал Новой Англии . 387 (16): 1488–1500. дои : 10.1056/NEJMra2114478 . hdl : 11577/3479721 . ПМИД 36260793 . S2CID 240234869 .
- ^ Витберг Г., Барда Н., Хосс С., Рихтер И., Виссман М., Авив Ю. и др. (декабрь 2021 г.). «Миокардит после вакцинации против Covid-19 в крупной организации здравоохранения» . Медицинский журнал Новой Англии . 385 (23): 2132–2139. дои : 10.1056/NEJMoa2110737 . ПМК 8531986 . ПМИД 34614329 . S2CID 238421512 .
- ^ Перейти обратно: а б Патоне М., Мей XW, Хандунетти Л., Диксон С., Заккарди Ф., Шанкар-Хари М. и др. (сентябрь 2022 г.). «Риск развития миокардита после последовательного введения вакцины против COVID-19 и заражения SARS-CoV-2 в зависимости от возраста и пола» . Тираж . 146 (10): 743–754. doi : 10.1161/CIRCULATIONAHA.122.059970 . ПМЦ 9439633 . ПМИД 35993236 .
- ^ Чэнь Ю, Сюй Z, Ван П, Ли XM, Шуай ZW, Йе DQ и др. (апрель 2022 г.). «Новые аутоиммунные явления после вакцинации против COVID-19» . Иммунология . 165 (4): 386–401. дои : 10.1111/imm.13443 . ПМИД 34957554 . S2CID 245522029 .
- ^ Джафари З., Колб Б.Е., Мохаджерани М.Х. (март 2022 г.). «Потеря слуха, шум в ушах и головокружение при COVID-19: систематический обзор и метаанализ» . Канадский журнал неврологических наук . 49 (2): 184–195. дои : 10.1017/cjn.2021.63 . ПМЦ 8267343 . ПМИД 33843530 .
- ^ Сломский А. (май 2022 г.). «Исследования изучают риск потери слуха после вакцинации от COVID-19» . ДЖАМА . 327 (17): 1641. doi : 10.1001/jama.2022.6719 . ПМИД 35503358 . S2CID 248502943 .
- ^ Дорни И., Бобак Л., Оттесон Т., Кельбер, округ Колумбия (сентябрь 2022 г.). «Распространенность впервые возникшего шума в ушах после вакцинации против COVID-19 в сравнении с другими прививками» . Ларингоскоп . 133 (7): 1722–1725. дои : 10.1002/lary.30395 . ПМЦ 9539087 . ПМИД 36098476 .
- ^ Ричи Х. , Матье Э., Родес-Гуйрао Л., Аппель С., Джаттино С., Ортис-Оспина Е. и др. (2020–2022 гг.). «Пандемия коронавируса (COVID-19)» . Наш мир в данных . Проверено 9 августа 2024 г.
- ^ Матье Э., Ричи Х., Родес-Гуйрао Л., Аппель С., Джаттино С., Хаселл Дж. и др. (2020). «Пандемия коронавируса (COVID-19)» . Наш мир в данных . Проверено 14 ноября 2023 г.
- ^ Матье Э., Ричи Х., Ортис-Оспина Э., Розер М., Хаселл Дж., Аппель С. и др. (2021). «Глобальная база данных прививок от COVID-19» . Природа человеческого поведения . 5 (7): 947–953. дои : 10.1038/s41562-021-01122-8 . ПМИД 33972767 .
- ^ Ричи Х., Ортис-Оспина Э., Бельтекян Д., Метье Э., Хаселл Дж., Макдональд Б. и др. (1 сентября 2021 г.). «Прививки от коронавируса (COVID-19) – статистика и исследования» . Наш мир в данных . Архивировано из оригинала 10 марта 2021 года . Проверено 26 января 2021 г.
- ^ «Обновленная информация об испытании солидарности ВОЗ: ускорение создания безопасной и эффективной вакцины против COVID-19» . Всемирная организация здравоохранения (ВОЗ). 27 апреля 2020 г. Архивировано из оригинала 30 апреля 2020 г. . Проверено 2 мая 2020 г.
Крайне важно оценить как можно больше вакцин, поскольку мы не можем предсказать, сколько из них окажутся жизнеспособными. Чтобы увеличить шансы на успех (учитывая высокий уровень сокращения числа вакцин в процессе разработки), мы должны тестировать все вакцины-кандидаты до тех пор, пока они не потерпят неудачу. Всемирная организация здравоохранения (ВОЗ) работает над тем, чтобы все они имели возможность пройти тестирование на начальном этапе разработки. Результаты эффективности каждой вакцины ожидаются в течение трех-шести месяцев, и эти доказательства в сочетании с данными о безопасности послужат основой для принятия решений о том, можно ли ее использовать в более широком масштабе.
- ^ Перейти обратно: а б Ворота Б (апрель 2020 г.). «Реакция на Covid-19: пандемия, которая случается раз в столетие?» . Медицинский журнал Новой Англии . 382 (18): 1677–1679. дои : 10.1056/nejmp2003762 . ПМИД 32109012 .
- ^ Вайнтрауб Р., Ядав П., Беркли С. (2 апреля 2020 г.). «Вакцина против COVID-19 потребует справедливого глобального распространения» . Гарвардское деловое обозрение . ISSN 0017-8012 . Архивировано из оригинала 9 июня 2020 года . Проверено 9 июня 2020 г.
- ^ Перейти обратно: а б с Стинхейсен Дж., Эйслер П., Мартелл А., Небехай С. (27 апреля 2020 г.). «Специальный отчет: страны и компании рискуют миллиардами в гонке за вакциной от коронавируса» . Рейтер. Архивировано из оригинала 15 мая 2020 года . Проверено 2 мая 2020 г.
- ^ Гартнер А., Робертс Л. (3 мая 2020 г.). «Насколько мы близки к созданию вакцины от коронавируса? Последние новости об испытаниях в Великобритании» . Телеграф . ISSN 0307-1235 . Архивировано из оригинала 4 мая 2020 года . Проверено 3 мая 2020 г.
- ^ «ВОЗ и ООН определили шаги для достижения мировых целей вакцинации против COVID» . Всемирная организация здравоохранения (ВОЗ). 7 октября 2021 года. Архивировано из оригинала 31 декабря 2021 года . Проверено 31 декабря 2021 г.
- ^ «COVID-19: ВОЗ призывает страны вакцинировать 70% своего населения к середине 2022 года» . 29 декабря 2021 года. Архивировано из оригинала 31 декабря 2021 года . Проверено 31 декабря 2021 г.
- ^ «Вакцинация против Covid-19: африканские страны не достигают цели ВОЗ» . Би-би-си . 31 декабря 2021 года. Архивировано из оригинала 31 декабря 2021 года . Проверено 31 декабря 2021 г.
- ^ Перейти обратно: а б с д Редакторы журнала Lancet по инфекционным заболеваниям (сентябрь 2021 г.). «Справедливость вакцины против COVID-19 и бустерные дозы» . Ланцет инфекционных заболеваний . 21 (9): 1193. doi : 10.1016/S1473-3099(21)00486-2 . ПМЦ 8360703 . ПМИД 34391506 .
- ^ Адханом Гебрейесус Т (18 января 2021 г.). «Вступительное слово Генерального директора ВОЗ на 148-й сессии Исполнительного комитета» . Всемирная организация здравоохранения (ВОЗ) . Архивировано из оригинала 12 ноября 2021 года . Проверено 25 января 2021 г.
- ^ «США оказали давление на Бразилию, чтобы та отказалась от российской вакцины «Спутник V»» . Бразильский отчет . 15 марта 2021 года. Архивировано из оригинала 15 марта 2021 года . Проверено 21 марта 2021 г.
- ^ Холмс О. (16 февраля 2021 г.). «Израиль заблокировал ввоз вакцин против Covid в сектор Газа, — говорят палестинцы» . Хранитель . Архивировано из оригинала 16 февраля 2021 года . Проверено 17 февраля 2021 г.
- ^ Расгон А (4 февраля 2021 г.). «Успех Израиля в создании вакцины порождает дебаты о неравенстве в Палестине» . Нью-Йорк Таймс . Архивировано из оригинала 28 декабря 2021 года . Проверено 17 февраля 2021 г.
- ^ Хортон С. (17 февраля 2021 г.). «Тайвань обеспокоен тем, что Китай, возможно, заблокировал закупку вакцины» . Блумберг . Архивировано из оригинала 17 февраля 2021 года . Проверено 17 февраля 2021 г.
- ^ «Игра в политику с бедностью: стратегия Сиси в отношении вакцины против COVID-19» . Фонд Карнеги за международный мир . Архивировано из оригинала 28 февраля 2021 года . Проверено 25 февраля 2021 г.
- ^ Стражевский Л. (9 февраля 2021 г.). «Доктор Фаучи: Варианты показывают, что вакцинация против COVID-19 является глобальной задачей» . Американская медицинская ассоциация . Архивировано из оригинала 10 октября 2021 года . Проверено 4 марта 2021 г.
- ^ Бергмарк Э., Вирсон А (26 февраля 2021 г.). «Мнение: Без глобального плана вакцинации варианты коронавируса могут привести к неисчислимому числу смертей» . CNN . Архивировано из оригинала 19 октября 2021 года . Проверено 4 марта 2021 г.
- ^ Бленкинсоп П., Маклин В., Эллис А. (10 марта 2021 г.). «Богатые и развивающиеся страны спорят из-за патентов на вакцины против COVID» . Рейтер . Архивировано из оригинала 11 марта 2021 года . Проверено 19 июня 2021 г.
- ^ Масиас А.М., Бройнингер К., Франк (5 мая 2021 г.). «США поддерживают отказ от патентной защиты вакцин против Covid, ссылаясь на глобальный кризис в области здравоохранения» . CNBC . Архивировано из оригинала 5 мая 2021 года . Проверено 5 мая 2021 г.
- ^ Санчес Николас Э (11 июня 2021 г.). «На ЕС нарастает давление с целью поддержать отказ ВТО от патентов на вакцины» . EUobserver . Архивировано из оригинала 19 октября 2021 года . Проверено 14 июня 2021 г.
- ^ «ВОЗ выступает против доказательства вакцинации против Covid-19 при международных поездках» . Южно-Китайская Морнинг Пост . 20 апреля 2021 года. Архивировано из оригинала 3 мая 2021 года . Проверено 17 мая 2021 г.
- ^ Гудман П.С., Мандавилли А., Роббинс Р., Стевис-Гриднефф М. (15 мая 2021 г.). «Что нужно, чтобы вакцинировать мир от Covid?» . Нью-Йорк Таймс . ISSN 0362-4331 . Архивировано из оригинала 15 мая 2021 года . Проверено 17 мая 2021 г.
- ^ Мунис Б., Фонсека Б., Фернандес Л., Пина Р. (15 марта 2021 г.). « В Бразилии регистрируется в два раза больше вакцинированных белых людей, чем чернокожих» . Agência Pública (на бразильском португальском языке). Архивировано из оригинала 15 марта 2021 года . Проверено 28 мая 2021 г.
- ^ Шнирринг Л. (17 мая 2021 г.). «Агентства ООН срочно призывают предоставить дозы вакцины COVAX» . ЦИДРАП . Архивировано из оригинала 31 октября 2021 года . Проверено 15 июня 2021 г.
- ^ «Первое заседание Целевой группы по вакцинам, терапии и диагностике COVID-19 для развивающихся стран» . Всемирная организация здравоохранения (ВОЗ) . 30 июня 2021 года. Архивировано из оригинала 19 октября 2021 года . Проверено 5 июля 2021 г.
- ^ Таппер Дж., Маккай Р. (3 июля 2021 г.). «Вакцины «опередлены вариантами», предупреждает ВОЗ, поскольку «Дельта» сейчас присутствует в 98 странах» . Хранитель . Архивировано из оригинала 21 октября 2021 года . Проверено 5 июля 2021 г.
- ^ Махасе Э (июль 2021 г.). «Covid-19: страны отказываются от вакцин, поскольку спрос падает, и обмен вакцинами становится затруднительным» . БМЖ . 374 : n1893. дои : 10.1136/bmj.n1893 . ПМИД 34315725 . S2CID 236457553 .
- ^ Левин Д. (1 августа 2021 г.). «США растрачивают дозы вакцины, даже несмотря на то, что число случаев заболевания растет, а другие страны страдают от нехватки вакцины» . Нью-Йорк Таймс . Архивировано из оригинала 9 августа 2021 года . Проверено 10 августа 2021 г.
- ^ «Вакцины против Covid-19: почему некоторые африканские государства не могут использовать свои вакцины» . Новости Би-би-си . 8 июня 2021 года. Архивировано из оригинала 14 ноября 2021 года . Проверено 20 августа 2021 г.
- ^ Дас С (5 июля 2021 г.). «CoWIN выходит на глобальный уровень: Индия делает технологии открытыми, 142 страны проявляют интерес» . Бизнес-стандарт Индии . Архивировано из оригинала 25 марта 2022 года . Проверено 25 марта 2022 г.
- ^ «Aarogya Setu теперь с открытым исходным кодом» . pib.gov.in (пресс-релиз). 26 мая 2020 года. Архивировано из оригинала 26 июня 2020 года . Проверено 18 июля 2023 г.
- ^ «Поддержка фармацевтических монополий G7 подвергает риску миллионы жизней» (пресс-релиз). Международная амнистия. 10 июня 2021 года. Архивировано из оригинала 19 октября 2021 года . Проверено 20 августа 2021 г.
- ^ «Вакцинные монополии делают мировую вакцинацию против COVID как минимум в 5 раз дороже, чем она могла бы быть» (пресс-релиз). Оксфам Интернэшнл. 29 июля 2021 года. Архивировано из оригинала 10 января 2022 года . Проверено 20 августа 2021 г.
- ^ Стиглиц Дж. (15 декабря 2021 г.). «Если Олаф Шольц серьезно настроен на прогресс, он должен поддержать отказ от патентов на вакцины против Covid» . Хранитель . Архивировано из оригинала 15 декабря 2021 года . Проверено 15 декабря 2021 г.
- ^ «Страны не должны упустить еще одну возможность продвинуть глобальный отказ от преодоления монополий в области медицинских инструментов COVID-19» . «Врачи без границ» (MSF)/Врачи без границ . 13 сентября 2021 г. Архивировано из оригинала 10 октября 2021 г. Проверено 23 сентября 2021 г.
- ^ «Врачи без границ» призывают отказаться от патентов и спекуляции на лекарствах и вакцинах против COVID-19 . Международная организация «Врачи без границ» (MSF) . Архивировано из оригинала 26 ноября 2021 года . Проверено 23 сентября 2021 г.
- ^ «Правительства должны действовать быстро, добиваясь консенсуса в поддержку исторического шага по приостановке монополий во время пандемии/COVID-19: правительства должны достичь консенсуса в отношении отказа от прав» . Международная организация «Врачи без границ» (MSF) . Архивировано из оригинала 23 октября 2021 года . Проверено 23 сентября 2021 г.
- ^ «ВОЗ права, призывая к временной остановке бустеров вакцины против COVID» . Природа . 596 (7872): 317. Август 2021 г. Бибкод : 2021Natur.596..317. . дои : 10.1038/d41586-021-02219-w . ПМИД 34404945 . S2CID 237199262 .
- ^ «ВОЗ осуждает стремление богатых стран сделать прививку от Covid, в то время как миллионам людей во всем мире не хватает первой прививки» . Франция 24 . Агентство Франс-Пресс. 18 августа 2021 года. Архивировано из оригинала 2 ноября 2021 года . Проверено 21 августа 2021 г.
- ^ Крамер Дж. (18 августа 2021 г.). «США планируют разрешить ревакцинацию, но многие уже получили третью дозу» . Нэшнл Географик . Архивировано из оригинала 10 октября 2021 года . Проверено 21 августа 2021 г.
- ^ «Более 140 бывших глав государств и нобелевских лауреатов призывают кандидатов на пост канцлера Германии отказаться от правил интеллектуальной собственности для вакцин против COVID-19» . Oxfam International (пресс-релиз). 14 сентября 2021 года. Архивировано из оригинала 19 октября 2021 года . Проверено 22 сентября 2021 г.
- ^ Уокер П. (29 ноября 2021 г.). «Профсоюзы медсестер по всему миру призывают ООН принять меры в отношении патентов на вакцины против Covid» . Хранитель . Архивировано из оригинала 29 ноября 2021 года . Проверено 29 ноября 2021 г.
- ^ Псаледакис Д. (22 сентября 2021 г.). «Обращение развивающихся стран к богатым людям мира в ООН: прекратить накопление вакцин» . Рейтер . Архивировано из оригинала 10 ноября 2021 года . Проверено 29 сентября 2021 г.
- ^ Empresa Peruana de Servicios Editoriales SA EDITORA PERÚ (21 сентября 2021 г.). «Перу: Президент предлагает глобальное соглашение в ООН, предусматривающее всеобщий доступ к вакцинам» . Андина (на испанском языке). Архивировано из оригинала 30 октября 2021 года . Проверено 29 сентября 2021 г.
- ^ Баранюк С (февраль 2021 г.). «Covid-19: как внедрение вакцины в Великобритании на данный момент привело к успеху» . БМЖ . 372 : n421. дои : 10.1136/bmj.n421 . ПМИД 33602672 . S2CID 231946710 .
- ^ «Дополнительная доза мРНК вакцины против COVID-19 для пациентов с ослабленным иммунитетом» . Центры США по контролю и профилактике заболеваний (CDC) . 13 августа 2021 года. Архивировано из оригинала 7 октября 2021 года . Проверено 16 августа 2021 г.
- ^ «Франция планирует внедрить повторную прививку вакцины против Covid – но только для уязвимых слоев населения» . Франция 24 . 4 августа 2021 года. Архивировано из оригинала 22 октября 2021 года . Проверено 16 августа 2021 г.
- ^ «Израиль предложит пожилым гражданам третью прививку от COVID» . Ассошиэйтед Пресс . 29 июля 2021 года. Архивировано из оригинала 31 октября 2021 года . Проверено 16 августа 2021 г.
- ^ Хунцикер П. (июль 2021 г.). «Вакцинация против Covid-19 с персонализированной дозой на волне вируса. Варианты, вызывающие обеспокоенность: обмен индивидуальной эффективностью на общественную пользу» . Прецизионная наномедицина . 4 (3): 805–820. дои : 10.33218/001c.26101 . Архивировано из оригинала 9 октября 2021 года . Проверено 16 августа 2021 г.
- ^ «Анализ ООН показывает связь между отсутствием справедливости в отношении вакцин и увеличением разрыва в бедности» . Новости ООН . 28 марта 2022 года. Архивировано из оригинала 12 апреля 2022 года . Проверено 14 апреля 2022 г.
- ^ «ДЦВМН» . Сеть производителей вакцин в развивающихся странах . Архивировано из оригинала 26 апреля 2022 года . Проверено 26 апреля 2022 г.
- ^ Томпсон М.Г., Берджесс Дж.Л., Нэйлуэй А.Л., Тайнер Х.Л., Юн С.К., Мис Дж. и др. (апрель 2021 г.). «Промежуточные оценки эффективности вакцин BNT162b2 и мРНК-1273 против COVID-19 в предотвращении заражения SARS-CoV-2 среди медицинского персонала, лиц, оказывающих первую помощь, и других основных и передовых работников - восемь мест в США, декабрь 2020 г. – март 2021 г.» ( PDF) . MMWR Morb Mortal Wkly Rep . 70 (13): 495–500. дои : 10.15585/mmwr.mm7013e3 . ПМЦ 8022879 . ПМИД 33793460 . Архивировано (PDF) из оригинала 28 августа 2021 года . Проверено 9 июня 2021 г.
- ^ «Когда ты полностью вакцинирован» . Центры США по контролю и профилактике заболеваний (CDC) . 11 февраля 2020 года. Архивировано из оригинала 28 июля 2021 года . Проверено 29 апреля 2021 г.
- ^ Перейти обратно: а б «Вакцины против COVID: расширение неравенства и уязвимость миллионов» . Объединенные Нации. 19 сентября 2021 года. Архивировано из оригинала 31 декабря 2021 года . Проверено 30 октября 2021 г.
- ^ «Влияние неравенства в отношении вакцин на восстановление экономики» . Программа развития ООН. Архивировано из оригинала 3 ноября 2021 года . Проверено 30 октября 2021 г.
- ^ Эллиот Л. (5 октября 2021 г.). «МВФ снижает глобальный экономический прогноз, поскольку пандемия «сдерживает» рост» . Хранитель . Архивировано из оригинала 27 октября 2021 года . Проверено 6 октября 2021 г.
- ^ «Беженцы сталкиваются с тяжелыми последствиями недостаточного финансирования Covid-19, предупреждает УВКБ ООН» . Объединенные Нации. 17 сентября 2021 г. Архивировано из оригинала 30 октября 2021 г. Проверено 30 октября 2021 г.
- ^ Перейти обратно: а б Азар А (4 февраля 2020 г.). «Уведомление о декларации в соответствии с Законом о общественной готовности и готовности к чрезвычайным ситуациям для медицинских контрмер против COVID-19» . Архивировано из оригинала 25 апреля 2020 года . Проверено 22 апреля 2020 г.
- ^ Линтерн С (2 декабря 2020 г.). «Правительство Великобритании предоставило компании Pfizer защиту от судебных исков по поводу вакцины против коронавируса» . Независимый . Архивировано из оригинала 5 мая 2021 года . Проверено 8 мая 2021 г.
- ^ «Вопросы и ответы: условное разрешение на продажу вакцин против COVID-19 в ЕС» . Европейская комиссия . 11 декабря 2020 г. Вопрос: В чем разница в ответственности между условным разрешением на маркетинг ЕС и разрешением на экстренное использование? Архивировано из оригинала 4 октября 2021 года . Проверено 29 декабря 2020 г. .
- ^ «EMA рекомендует стандартные регистрационные удостоверения для вакцин Comirnaty и Spikevax против COVID-19» . Европейское агентство по лекарственным средствам . 16 сентября 2022 года. Архивировано из оригинала 16 сентября 2022 года . Проверено 7 октября 2022 г.
- ^ Хаар Т (7 сентября 2020 г.). «COVID-19: Депутаты Европарламента хотят безопасных вакцин, полной прозрачности и ответственности для компаний» . Европейский парламент . Г-жа Галлина подчеркнула, что переговоры с компаниями были трудными, но подчеркнула, что те компании, которые разрабатывают и производят вакцины против COVID-19, действительно будут нести ответственность в соответствии с действующим законодательством, и если что-то пойдет не так, они могут быть привлечены к суду. Это касается и компенсации скрытых дефектов. Архивировано из оригинала 13 октября 2021 года . Проверено 29 декабря 2020 г. .
- ^ «Расследование: производитель лекарств «запугивал» латиноамериканские страны» . Аль Джазира . 11 марта 2021 года. Архивировано из оригинала 31 октября 2021 года . Проверено 15 июня 2021 г.
- ^ Барселлос Р. (13 мая 2021 г.). «Карлос Мурильо говорит, что положения, критикуемые Бразилией, действительны в 110 странах» [Карлос Мурильо говорит, что критические положения для Бразилии действительны в 110 странах] . CNN Brasil (на португальском языке). Архивировано из оригинала 28 июня 2021 года . Проверено 15 июня 2021 г.
- ^ «Губернатор Рон ДеСантис подает петицию в Верховный суд Флориды о создании большого жюри штата по вакцинам от COVID-19 и объявляет о создании Комитета по добросовестности общественного здравоохранения» . www.flgov.com . Архивировано из оригинала 14 декабря 2022 года . Проверено 14 декабря 2022 г.
- ^ «Губернатор Флориды требует от большого жюри расследования вакцин против Covid» . www.theguardian.com . 13 декабря 2022 года. Архивировано из оригинала 13 декабря 2022 года . Проверено 14 декабря 2022 г.
- ^ «Основатель Blackwater Принс принимает участие в проекте по созданию вакцины от COVID» . Рейтер . 4 июня 2021 года. Архивировано из оригинала 9 октября 2021 года . Проверено 4 июня 2021 г.
- ^ Перейти обратно: а б Леонхардт Д. (11 марта 2024 г.). «Четвертая годовщина пандемии Covid» . Нью-Йорк Таймс . Архивировано из оригинала 11 марта 2024 года. «Данные не включают Аляску. Источники: CDC Wonder; Edison Research. (Диаграмма) The New York Times . Таблица с указанием источников: Эшли Ву.
- ^ Линас М (20 апреля 2020 г.). «COVID: Топ-10 современных теорий заговора» . Альянс за науку . Проверено 4 октября 2021 г.
- ^ Бураковский А (28 августа 2021 г.). «Реакция России на Covid-19 замедлилась из-за нежелания населения принимать отечественную вакцину» . КРКЕ . Проверено 20 сентября 2021 г.
- ^ «Проход Covid покоряет Францию» . Новости ВЛФИ . Архивировано из оригинала 20 сентября 2021 года . Проверено 20 сентября 2021 г.
- ^ «MLB предлагает бесплатные билеты на прививки от COVID-19» . Крон4. 4 июня 2021 г. Проверено 4 октября 2021 г.
- ^ Гор Д. (10 мая 2021 г.). «Изучение законности требований по вакцинации против COVID-19» . сайт factcheck.org . Проверено 4 октября 2021 г.
- ^ Хотез Пи Джей (2023). Смертоносный рост антинауки: предупреждение учёного . Издательство Университета Джонса Хопкинса. ISBN 978-1421447223 .
- ^ Бинг С., Шехтман Дж. (14 июня 2024 г.). «Пентагон провел секретную кампанию против вакцинации, чтобы подорвать позиции Китая во время пандемии» . Рейтер .
Дальнейшее чтение
- Копаеску А.М., Роза Дуке Дж.С., Филлипс Э.Дж. (июль 2022 г.). «Что мы узнали об аллергенности и побочных реакциях, связанных с вакцинами против тяжелого острого респираторного синдрома от коронавируса 2: год спустя» . Анналы аллергии, астмы и иммунологии . 129 (1): 40–51. дои : 10.1016/j.anai.2022.03.030 . ПМЦ 8979618 . ПМИД 35390476 .
- Краузе П.Р., Флеминг Т.Р., Лонгини И.М., Пето Р., Бриан С., Хейманн Д.Л. и др. (июль 2021 г.). «Варианты и вакцины против SARS-CoV-2» . N Engl J Med . 385 (2): 179–186. дои : 10.1056/NEJMsr2105280 . ПМЦ 8262623 . ПМИД 34161052 .
- Кириакидис Н.К., Лопес-Кортес А., Гонсалес Е.В., Гримальдос А.Б., Прадо Э.О. (февраль 2021 г.). «Стратегии вакцинации против SARS-CoV-2: всесторонний обзор кандидатов фазы 3» . НПЖ Вакцины . 6 (1): 28. дои : 10.1038/s41541-021-00292-w . ПМК 7900244 . ПМИД 33619260 .
- Рамзи М., изд. (2020). «COVID-19: Зеленая книга, глава 14а» . Иммунизация против инфекционных заболеваний . Лондон: Общественное здравоохранение Англии.
- Разработка и лицензирование вакцин для профилактики COVID-19: Руководство для промышленности (PDF) (Отчет). США Управление по контролю за продуктами и лекарствами (FDA). Июнь 2020.
Протоколы вакцинации
- «Протокол мРНК-1273-P301» (PDF) . Модерна . Архивировано из оригинала (PDF) 28 сентября 2020 года . Проверено 21 сентября 2020 г.
- «Протокол C4591001 PF-07302048 (Вакцины против COVID-19 на основе РНК BNT162)» (PDF) . Пфайзер . Архивировано из оригинала (PDF) 6 декабря 2021 года . Проверено 6 августа 2022 г.
- «Протокол AZD1222 – D8110C00001» (PDF) . АстраЗенека .
- «Протокол VAC31518COV3001; Фаза 3 (ансамбль)» (PDF) . Янссен Вакцины и профилактика .
- «Протокол VAC31518COV3009; Фаза 3 (Ансамбль 2)» (PDF) . Янссен Вакцины и профилактика .
- «Протокол НДС00008 – Протокол исследования моновалентных и бивалентных рекомбинантных белковых вакцин против COVID-19 у взрослых в возрасте 18 лет и старше» (PDF) . Санофи Пастер . Архивировано из оригинала (PDF) 23 июля 2021 года . Проверено 30 июля 2021 г.
- «Протокол 2019nCoV-301» . Новавакс .
Внешние ссылки
- «Отслеживание вакцины против COVID-19 и ландшафт» . Всемирная организация здравоохранения (ВОЗ).
- Лекция 10 Массачусетского технологического института: Кизмекия Корбетт, Вакцины на YouTube
- Лекция 12 Массачусетского технологического института: Дэн Баруш, Разработка вакцины против Covid-19 на YouTube
- «5 этапов разработки вакцины против COVID-19: что нужно знать о том, как проходят клинические испытания» . Джонсон и Джонсон. Сентябрь 2020.
- «Вакцина от коронавируса – еженедельная сводка отчетности по желтой карточке» . Великобритании Агентство по регулированию лекарственных средств и товаров медицинского назначения (MHRA).
- «Отчет о безопасности вакцины против COVID-19 – 10.05.2023» . Управление терапевтических товаров (TGA) . 4 октября 2023 г.
- Колата Г., Мюллер Б. (15 января 2022 г.). «Остановка прогресса и счастливые случайности: как были созданы мРНК-вакцины» . Нью-Йорк Таймс . Архивировано из оригинала 15 января 2022 года.

![Карта, показывающая долю населения, полностью вакцинированного против COVID-19, по отношению к общей численности населения страны[примечание 1]](http://upload.wikimedia.org/wikipedia/commons/thumb/b/b4/World_map_of_share_of_people_who_received_all_doses_prescribed_by_the_initial_COVID-19_vaccination_protocol.png/510px-World_map_of_share_of_people_who_received_all_doses_prescribed_by_the_initial_COVID-19_vaccination_protocol.png)