Кетон
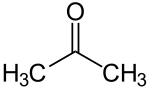
В органической химии кетон n / ˈ k iː t oʊ / является органическим соединением со структурой R -C (= O) −r ' , где R и R' могут быть разнообразными углеродами, содержащими заместители . Кетоны содержат карбонильную группу −c (= o)- углерода-кислорода ( двойная связь C = O). Самый простой кетон - ацетон (где r и r ' - метил ), с формулой (Ch 3 ) 2 co . Многие кетоны имеют большое значение в биологии и промышленности. Примеры включают в себя множество сахаров ( кетозы ), много стероидов (например, тестостерон ) и растворителя ацетон . [ 1 ]
Номенклатура и этимология
[ редактировать ]Слово кетон происходит от Акетона , старого немецкого слова для ацетона . [ 2 ] [ 3 ]
Согласно правилам номенклатуры IUPAC , кетоновые имена получены путем изменения суффикса -эн родительского алкане на -анона . Как правило, позиция карбонильной группы обозначается числом, но традиционные неинсистемные названия по -прежнему обычно используются для наиболее важных кетонов, например, ацетона и бензофенона . Эти несистематические имена считаются сохраненными именами IUPAC, [ 4 ] Хотя некоторые вводные учебники по химии используют систематические имена, такие как «2-пропанон» или «propan-2-one» для простейшего кетона ( C H 3 -C (= O ) −CH 3 ) вместо «ацетона».
Полученные названия кетонов получают отдельно написанием имен двух алкильных групп, прикрепленных к карбонильной группе, за которыми следует «кетоне» в качестве отдельного слова. Традиционно названия алкильных групп были написаны в порядке увеличения сложности, например, метилового этилкетона . Однако, согласно правилам номенклатуры IUPAC , алкильные группы написаны в алфавитном порядке, например, этилмеилкетон . Когда две алкильные группы одинаковы, префикс «di-» добавляется перед именем алкильной группы. Положения других групп обозначены греческими буквами , α-углерод является атом, прилегающим к карбонильной группе.
Несмотря на то, что он использовался редко, Oxo является номенклатурой IUPAC для группы Oxo (= O) и используется в качестве префикса, когда кетон не имеет наивысшего приоритета. Другие префиксы, однако, также используются. Для некоторых распространенных химических веществ (в основном в биохимии) Кето относится к функциональной группе кетона .
Структура и связь
[ редактировать ]
Кетоновый углерод часто описывается как sp 2 Гибридизованный , описание, которое включает в себя как их электронную, так и молекулярную структуру. Кетоны - это тригональный плоский вокруг кетонического углерода, с углеками C -C - O и C - C - C приблизительно 120 °. Кетоны отличаются от альдегидов тем, что карбонильная группа (C = O) связана с двумя углеродами в углеродном скелете . В альдегидах карбонил связан с одним углеродом и одним водородом и расположен на концах углеродных цепей. карбонилсодержащих Кетоны также отличаются от других функциональных групп , таких как карбоновые кислоты , сложные эфиры и амиды . [ 5 ]
Карбонильная группа является полярной , потому что электроотрицательность кислорода больше, чем для углерода. Таким образом, кетоны являются нуклеофильными при кислороде и электрофильном при углероде. Поскольку карбонильная группа взаимодействует с водой путем водородной связи , кетоны обычно более растворимы в воде, чем связанные метиленовые соединения. Кетоны являются акцепторами водорода. Кетоны обычно не являются донорами водородных связей и не могут сами водородных связей. Из-за их неспособности служить как донорами и акцепторами водородных связей, кетоны, как правило, не «самооценка» и являются более летучими, чем спирты и карбоновые кислоты сопоставимых молекулярных весов . Эти факторы связаны с распространенностью кетонов в парфюмерии и в качестве растворителей.
Классы кетонов
[ редактировать ]Кетоны классифицируются на основе их заместителей. Одна широкая классификация подразделяет кетоны в симметричные и несимметричные производные, в зависимости от эквивалентности двух органических заместителей, прикрепленных к центру карбонила. Ацетон и бензофенон ( (C 6 H 5 ) 2 CO ) являются симметричными кетонами. Ацетофенон (C 6 H 5 C (O) CH 3 ) является несимметричным кетоном.
Тетонеты
[ редактировать ]Многие виды дикетонов известны, некоторые с необычными свойствами. Самый простой - диацетил (CH 3 C (O) C (O) CH 3 ) , когда-то используется в качестве масляного алеализации в попкорне . Ацетилацетон (пентатан-2,4-дион) является практически неправильным (неподходящим названием), потому что этот вид существует в основном как моноэенол CH 3 C (O) CH = C (OH) CH 3 . Его эулят является общим лигандом в координационной химии .
Ненасыщенные кетоны
[ редактировать ]Кетоны, содержащие алкинские и алкинские подразделения, часто называют ненасыщенными кетонами. Широко используемым элементом этого класса соединений является метилвинил кетон , CH 3 C (O) CH = CH 2 , A α, β-безсыщенное карбонильное соединение .
Циклические кетоны
[ редактировать ]Многие кетоны циклические. Самый простой класс имеет формулу (CH 2 ) N CO , где N варьируется от 2 для циклопропанона ( (Ch 2 ) 2 CO ) до десятков. Существуют большие производные. Циклогексанон ( (CH 2 ) 5 CO ), симметричный циклический кетон, является важным промежуточным звеном в производстве нейлона . Изофорон , полученный из ацетона, является ненасыщенным, асимметричным кетоном, который является предшественником других полимеров . Мускон животного , 3-метилпентадеканон, является феромоном . Другим циклическим кетоном является циклобутанон , имея формулу (Ch 2 ) 3 CO .
Характеристика
[ редактировать ]Альдегид отличается от кетона тем, что он имеет атом водорода, прикрепленный к его карбонильной группе, что облегчает окисление альдегидов. Кетоны не имеют атома водорода, связанного с карбонильной группой, и, следовательно, более устойчивы к окислению. Они окисляются только мощными окисливными агентами , которые способны расщеплять углерод -углеродные связи.
Спектроскопия
[ редактировать ]Кетоны (и альдегиды) сильно поглощаются в инфракрасном спектре около 1750 см. −1 , который присваивается ν C = O («частота растяжения карбонила»). Энергия пика ниже для арила и ненасыщенных кетонов. [ 6 ]
Тогда как 1 H ЯМР -спектроскопия, как правило, не полезна для установления присутствия кетона, 13 Спектры C ЯМР демонстрируют сигналы несколько внизу поля 200 ч / млн в зависимости от структуры. Такие сигналы, как правило, слабы из -за отсутствия ядерного ремонта . Поскольку альдегиды резонируют при аналогичных химических сдвигах , используются множественные резонансные эксперименты для окончательного различения альдегидов и кетонов.
Качественные органические тесты
[ редактировать ]Кетоны дают положительные результаты в тесте Брэди , реакции с 2,4-динитрофенилгидразином с получением соответствующего гидразона. Кетоны можно отличить от альдегидов, давая отрицательный результат с реагентом Толленса или с решением Фелинга . Метилкетоны дают положительные результаты для теста йодоформ . [ 7 ] Кетоны также дают положительные результаты при обработке м -динитробензолом в присутствии разбавленного гидроксида натрия с получением фиолетовой окраски.
Синтез
[ редактировать ]Существует много методов для подготовки кетонов в промышленных масштабах и академических лабораториях. Кетоны также производятся различными способами организмами; См. Раздел о биохимии ниже.
В промышленности наиболее важный метод, вероятно, включает , часто окисление углеводородов с воздухом. Например, миллиард килограммов циклогексанона производятся ежегодно путем аэробного окисления циклогексана . Ацетон готовится путем окисления кумола .
Для специализированных или мелкомасштабных органических синтетических применений кетоны часто готовятся путем окисления вторичных спиртов :
- R 2 CH (OH) + "O" → R 2 C = O + H 2 O
Типичные сильные окислители (источник «O» в вышеуказанной реакции) включают перманганат калия или соединение Cr (VI) . Более мягкие условия используют методы Dess -Martin или методы Moffatt -Swern .
Было разработано много других методов, примеры включают в себя: [ 8 ]
- Гидролизом гидролиза геминального галогенира . [ 9 ]
- Путем гидратации алкинов . [ 10 ] Такие процессы происходят через enols и требуют наличия кислотного и ртутного (II) сульфата ( HGSO 4 ). Последующая таутомеризация enol -кето дает кетон. Эта реакция всегда производит кетон, даже с терминальным алкином, единственным исключением является гидратация ацетилена , которая производит ацетальдегид .
- От амидов Вайнреба с использованием стехиометрических органометаллических реагентов.
- арилкетоны могут быть приготовлены в ацилировании фриделя -крафтов , [ 11 ] Связанная реакция Houben - Hoesch , [ 12 ] и перестройка фри . [ 10 ]
- Озонолиз и связанные с ними дигидроксилирование/окислительные последовательности, расщепляют алкены с получением альдегидов или кетонов, в зависимости от паттерны замены алкена. [ 13 ]
- От пероксидов ( перестройка Kornblum - Delamare ).
- Циклизация дикарбоновых кислот ( циклизация Ruzicka )
- гидролиз солей вторичных нитро -соединений ( реакция NEF [ 14 ] )
- Алкилирование тиоэфира с помощью соединений организма ( муфта Fukuyama ).
- Алкилирование хлорида кислоты с помощью органокадмийных соединений или органокоппера .
- Реакция Дакин -Запада обеспечивает эффективный метод для приготовления определенных метилкетонов из карбоновых кислот. [ 15 ]
- Кетоны могут быть приготовлены реакцией реагентов Grignard с нитрилами с последующим гидролизом. [ 16 ]
- Декарбоксилированием карбонового ангидрида .
- Кетоны могут быть приготовлены из галокетонов в восстановительном дегалогении кетонов гало .
- В кетоническом декарбоксилировании симметричные кетоны приготовлены из карбоновых кислот. [ 10 ] [ 17 ]
- Гидролиз ненасыщенных вторичных , амидов [ 18 ] β - эфиры кето кислоты , [ 10 ] или β- дикетоны ( синтез ацетоуксомного эфира ).
- Кислотная перегруппировка 1,2 -диола , [ 10 ] или критерии окисления того же самого.
Реакция
[ редактировать ]Кето-Энол Таутомеризация
[ редактировать ]
Кетоны, которые имеют по крайней мере один альфа-гидроген , подвергаются тавтомеризации кето-эенол ; Таутомер - это enol . Таутомеризация катализируется как кислотами, так и основаниями. Обычно форма кето более стабильна, чем enol. готовить кетоны с помощью гидратации алкинов Это равновесие позволяет .
Кислотные/базовые свойства кетонов
[ редактировать ]C - H связи, прилегающие к карбониле в кетонах, более кислыми p k a ≈ 20), чем C -H связи в алкане (P k a ≈ 50). Это различие отражает резонансную стабилизацию иона еноляции , который образуется при депротонировании . Относительная кислотность α-гидрогена важна в реакциях энолизации кетонов и других карбонильных соединений. Кислотность α-гидрогена также позволяет кетонам и другим карбонильным соединениям реагировать как нуклеофилы в этом положении, с либо стехиометрическим , так и каталитическим основанием. Используя очень сильные основания, такие как литий-диизопропиламид (LDA, P k a из конъюгатной кислоты ~ 36) в невравной, в условиях (–78 ° C, 1,1 эквивалентный LDA в THF, кетон добавляется в основание), менее обозначенный кинетический энтезиат генерируется . избирательно, в то время как условия, которые позволяют уравновешивать (более высокая температура, основание добавлено к ктону, используя слабые или нерастворимые основания, например, CH 3 CH 2 ONA в CH 3 CH 2 OH , или NAH ) обеспечивает более замещенную термодинамическую эулят .
Кетоны также являются слабыми основаниями, подвергающимися протонации на карбонильном кислороде в присутствии кислот Бренстеда . Ионы кетония (то есть протонированные кетоны) представляют собой сильные кислоты, причем значения p a значения , по оценкам, находятся где -то между –5 и –7. [ 19 ] [ 20 ] Хотя кислоты, встречающиеся в органической химии, редко бывают достаточно сильными для полного протонирования кетонов, образование равновесных концентраций протонированных кетонов, тем не менее, является важным шагом в механизмах многих общих органических реакций, таких как образование ацетала. Кислоты, такие как слабые, как катион пиридиния (как обнаружено в пиридинии тозилат) с AP K A 5,2, способны служить катализаторами в этом контексте, несмотря на очень неблагоприятное равновесное равновесие для протонирования ( k < 10 −10 ).
Нуклеофильные дополнения
[ редактировать ]Важный набор реакций вытекает из восприимчивости карбонильного углерода к нуклеофильному добавлению и тенденции к увеличению енолятов к электрофилам. Нуклеофильные дополнения включают в приблизительный порядок их общности: [ 8 ]
- С водой (гидратацией) дает геминовые диолы , которые обычно не образуются в заметных (или наблюдаемых) количествах
- С ацетилидом, чтобы получить α- гидроксиалкин
- С аммиаком или первичным амином дает имин
- С вторичным амином дает эман
- С Grignard и реагентами органолита , чтобы дать после водного обучения третичный алкоголь
- С спиртами или алкоксидами, дает гемикетал или его сопряженное основание. С диолом к кеталу . Эта реакция используется для защиты кетонов.
- С амидом натрия, приводящим к расщеплению связей C - C с образованием амида RConh 2 и алкане или арен -r'h, реакцией, называемой реакцией Халлера -Бауэра. [ 21 ]
Окисление
[ редактировать ]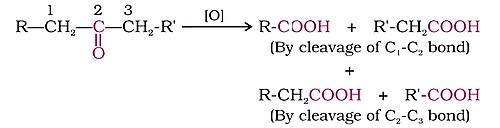
Кетоны расщепляются сильными окислителями и при повышенных температурах. Их окисление включает в себя расщепление углерод -углеродных связей с получением смеси карбоновых кислот, имеющих меньшее количество атомов углерода, чем родительский кетон.
Другие реакции
[ редактировать ]- Электрофильное добавление , реакция с электрофилом дает резонансный стабилизированный катион
- С фосфонием илидидом в реакции Wittig, чтобы дать алкены
- С тиолами, чтобы дать тиоацеталию
- С гидразином или 1-расселенным производными гидразина с получением гидразонов .
- С металлическим гидридом дает металлическую алкоксидную соль, гидролиз которого дает спирт, пример восстановления кетона
- С галогенами с образованием α- галокетона , реакция, которая проходит через ENOL (см. Реакцию ореоформа )
- С тяжелой водой , чтобы дать α- дейтерированный кетон
- Фрагментация в фотохимической норришской реакции
- Реакция 1,4-аминодикетонов на оксазолы путем дегидратации в синтезе Робинсона-Габриэль
- В случае арил -алкилкетонов, с серной и амином дают амиды в реакции Уилгеродта
- С гидроксиламином для производства оксимов
- С уменьшением агентов для образования вторичных спиртов
- С перекисными кислотами для образования эфиров при окислении Baeyer -Villiger
Биохимия
[ редактировать ]Кетоны не появляются ни на стандартных аминокислотах , нуклеиновых кислотах и липидах. Образование органических соединений в фотосинтезе происходит через кетоновую рибулозу-1,5-бисфосфат . Многие сахара являются кетонами, известными как кетозы . Самая известная кетоза - фруктоза ; В основном это существует как циклический гемикетал , который маскирует функциональную группу кетона. Синтез жирных кислот проходит через кетоны. Ацетоацетат является промежуточным в цикле Кребса , который высвобождает энергию из сахаров и углеводов. [ 22 ]
В медицине ацетон , ацетоацетат и бета-гидроксибутират коллективно называются кетоновыми телами , генерируемыми из углеводов , жирных кислот и аминокислот у большинства позвоночных , включая людей. Кетоновые тела повышены в крови ( кетоз ) после поста, включая ночь сна; как в крови, так и в моче в голодании ; В гипогликемии из -за причин, отличных от гиперинсулинизма ; в различных врожденных ошибках метаболизма и преднамеренно индуцированной через кетогенную диету и при кетоацидозе (обычно из -за сахарного диабета). Хотя кетоацидоз характерен для декомпенсированного или необработанного диабета 1 типа могут возникать при диабете 2 типа , кетоз или даже кетоацидоз также при некоторых обстоятельствах.
Приложения
[ редактировать ]Кетоны вырабатываются в масштабных масштабах в промышленности в качестве растворителей, полимерных предшественников и фармацевтических препаратов. С точки зрения масштаба, наиболее важными кетонами являются ацетон , метилатилкетон и циклогексанон . [ 23 ] Они также распространены в биохимии, но меньше, чем в органической химии в целом. Сжигание углеводородов - это неконтролируемый процесс окисления, который дает кетоны , а также многие другие типы соединений.
Токсичность
[ редактировать ]Хотя трудно обобщить токсичность такого широкого класса соединений, простые кетоны, как правило, не очень токсичны. Эта характеристика является одной из причин их популярности как растворителей. Исключениями из этого правила являются ненасыщенные кетоны, такие как метилвинил кетон, с LD 50 из 7 мг/кг (оральный). [ 23 ]
Смотрите также
[ редактировать ]Ссылки
[ редактировать ]- ^ Раймонд, Кеннет В. (2010). Общая органическая и биологическая химия (3 -е изд.). Уайли. п. 297
- ^ Харпер, Дуглас. "Кетон" . Онлайн этимологический словарь .
- ^ Слово «кетон» было придумано в 1848 году немецким химиком Леопольдом Гмелин . См.: Leopold Gmelin, ed., Handbuch der Organischen Chemie: Organische Chemie Im Allgemeinen … (Справочник по органической химии: органическая химия в целом…), 4 -е изд., (Гейдельберг, (Германия): Карл Винтер, 1848), том 1. , с. 4 . также принадлежат, которые обозначены как ацетоны в целом ( кетоны? ). ») (Для этих синдидов*, эти соединения также , кажется , Новые классы соединений были «синдидами», которые были соединены, образованные комбинацией из двух или более простых органических молекул (от греческого σύνΔεσμος ( Syndesmos , Union) + -IDE (указывая на группу родственных соединений)) может быть сформировано сухой дистилляцией ацетатов металлов, поэтому ацетон был синдидесмидом двух ацетатных ионов. «Химическая классификация», Отчеты , 19 : 1089–1100; Смотрите особенно р. 1097.
- ^ Список сохраняемых имен IUPAC, оставленных имена IUPAC, Архивирована 9 июля 2023 года на машине Wayback
- ^ McMurry, John E. (1992), Organic Chemistry (3 -е изд.), Belmont: Wadsworth, ISBN 0-534-16218-5
- ^ Смит, Брайан (ноябрь 2018 г.). "C = O BOND, Часть VIII: обзор" . Спектроскопия . Ноябрь 2018. 33 : 24–29. Архивировано из оригинала 13 февраля 2024 года . Получено 12 февраля 2024 года .
- ^ Mendham, J.; Денни, RC; Барнс, JD; Thomas, MJK (2000), Количественный химический анализ Фогеля (6 -е изд.), Нью -Йорк: Prentice Hall, ISBN 0-582-22628-7
- ^ Jump up to: а беременный Смит, Майкл Б.; Март, Джерри (2007), Advanced Organic Chemistry: реакции, механизмы и структура (6-е изд.), Нью-Йорк: Wiley-Interscience, ISBN 978-0-471-72091-1
- ^ Marvel, CS; Сперри, Wm (1928). "Бензофенон". Органические синтезы . 8 : 26. doi : 10.15227/orgsyn.008.0026 .
- ^ Jump up to: а беременный в дюймовый и Фурнисс, Брайан; Ханнафорд, Энтони; Смит, Питер; Tatchell, Austin (1996). Учебник Фогеля практической органической химии (5 -е изд.). Лондон: Longman Science & Technical. С. 612–623, 976–977, 982–983. ISBN 9780582462366 .
- ^ Аллен, CFH; Баркер, мы (1932). «ДеСоксибензоин». Органические синтезы . 12 : 16. doi : 10.15227/orgsyn.012.0016 .
- ^ Гулати, KC; Сет, ср; Венкатараман, К. (1935). «Флороацетофенон». Органические синтезы . 15 : 70. DOI : 10.15227/Orgsyn.015.0070 .
- ^ Tietze, Lutz F.; Братц, Матиас (1993). «Диалкил -мезоксалаты путем озонолиза диалкилбензалмалонатов: диметил мезоксалат». Органические синтезы . 71 : 214. doi : 10.15227/orgsyn.071.0214 .
- ^ Heinzelman, RV (1955). «О-метоксифенилацетон». Органические синтезы . 35 : 74. doi : 10.15227/orgsyn.035.0074 .
- ^ Wiley, Richard H.; Бум, Огайо (1953). "3-Acetamude-2-но" Органические синтезии . 33 : DOI : 1.
- ^ Моффетт, РБ; Шрайнер, Р.Л. (1941). "ω-метоксиацетофенон". Органические синтезы . 21 : 79. doi : 10.15227/orgsyn.021.0079 .
- ^ Торп, JF; Кон, Гар (1925). «Циклопентанон». Органические синтезы . 5 : 37. doi : 10.15227/orgsyn.005.0037 .
- ^ Хербст, RM; Shemin, D. (1939). «Фенилпирувиновая кислота». Органические синтезы . 19 : 77. doi : 10.15227/orgsyn.019.0077 .
- ^ Эванс, Дэвид А. (4 ноября 2005 г.). «Эванс ПКА таблица» (PDF) . Веб -сайт Evans Group . Архивировано из оригинала (PDF) 19 июня 2018 года . Получено 14 июня 2018 года .
- ^ Смит, Майкл Б. (2013). Мартовская передовая органическая химия (7 -е изд.). Хобокен, Нью -Джерси: Уайли. С. 314–315. ISBN 978-0-470-46259-1 .
- ^ Халлер -Бауэр Реакция . homeip.net
- ^ Нельсон, DL; Cox, MM (2000) Lehninger, Принципы биохимии . 3 -е изд. Стоит публиковать: Нью -Йорк. ISBN 1-57259-153-6 .
- ^ Jump up to: а беременный Сито, хардо; Engrsorfer, Manfred (2000). "Кононы" Энциклопедия doi : 10.1002/1436000 . ISBN 9783527306732 .
{{cite book}}: CS1 Maint: doi неактивен по состоянию на сентябрь 2024 года ( ссылка )
Внешние ссылки
[ редактировать ] СМИ, связанные с кетонами в Wikimedia Commons
СМИ, связанные с кетонами в Wikimedia Commons