Хлор
 | ||||||||||||||||||||||||||||
| Хлор | ||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Произношение | / K l ɔː ːr iː n , - aɪ n / | |||||||||||||||||||||||||||
| Появление | бледно-желтый-зеленый газ | |||||||||||||||||||||||||||
| Стандартный атомный вес A r ° (cl) | ||||||||||||||||||||||||||||
| Хлор в периодической таблице | ||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||
| Атомное число ( z ) | 17 | |||||||||||||||||||||||||||
| Группа | Группа 17 (галогены) | |||||||||||||||||||||||||||
| Период | период 3 | |||||||||||||||||||||||||||
| Блокировать | P-Block | |||||||||||||||||||||||||||
| Электронная конфигурация | [ Ne ] 3S 2 3 с 5 | |||||||||||||||||||||||||||
| Электроны на оболочку | 2, 8, 7 | |||||||||||||||||||||||||||
| Физические свойства | ||||||||||||||||||||||||||||
| Фаза в STP | газ | |||||||||||||||||||||||||||
| Точка плавления | (CL 2 ) 171,6 K (-101,5 ° C, -150,7 ° F) | |||||||||||||||||||||||||||
| Точка кипения | (CL 2 ) 239,11 K (-34,04 ° C, -29,27 ° F) | |||||||||||||||||||||||||||
| Плотность (при STP) | 3,2 г/л | |||||||||||||||||||||||||||
| Когда жидкость (при BP ) | 1,5625 г/см 3 [ 3 ] | |||||||||||||||||||||||||||
| Тройная точка | 172,22 К, 1392 К [ 4 ] | |||||||||||||||||||||||||||
| Критическая точка | 416,9 К, 7,991 МПа | |||||||||||||||||||||||||||
| Теплоте слияния | (CL 2 ) 6,406 кДж/моль | |||||||||||||||||||||||||||
| Тепло испарения | (CL 2 ) 20,41 кДж/моль | |||||||||||||||||||||||||||
| Молярная теплоемкость | (CL 2 ) 33,949 J/(моль · к) | |||||||||||||||||||||||||||
Давление паров
| ||||||||||||||||||||||||||||
| Атомные свойства | ||||||||||||||||||||||||||||
| Состояния окисления | −1 , 0, +1 , +2, +3 , +4, +5 , +6, +7 (сильно кислый оксид) | |||||||||||||||||||||||||||
| Электроотрицательность | Масштаб Полинга: 3.16 | |||||||||||||||||||||||||||
| Энергии ионизации |
| |||||||||||||||||||||||||||
| Ковалентный радиус | 102 ± 16:00 | |||||||||||||||||||||||||||
| Радиус ван дер -ваальса | 175 вечера | |||||||||||||||||||||||||||
| Другие свойства | ||||||||||||||||||||||||||||
| Естественное явление | изначальный | |||||||||||||||||||||||||||
| Кристаллическая структура | Орторомбический ( OS8 ) | |||||||||||||||||||||||||||
| Константы решетки | A = 630,80 вечера B = 455,83 вечера C = 815,49 вечера (в тройной точке) [ 5 ] | |||||||||||||||||||||||||||
| Теплопроводность | 8.9 × 10 −3 W/(Mtak) | |||||||||||||||||||||||||||
| Электрическое удельное сопротивление | > 10 Ом (при 20 ° С) | |||||||||||||||||||||||||||
| Магнитное упорядочение | Диамагнитный [ 6 ] | |||||||||||||||||||||||||||
| Молярная магнитная восприимчивость | −40.5 × 10 −6 см 3 /мол [ 7 ] | |||||||||||||||||||||||||||
| Скорость звука | 206 м/с (газ, при 0 ° C) | |||||||||||||||||||||||||||
| Номер CAS | CL 2 : 7782-50-5 | |||||||||||||||||||||||||||
| История | ||||||||||||||||||||||||||||
| Открытие и первая изоляция | Карл Вильгельм Шил (1774) | |||||||||||||||||||||||||||
| Распознается элемент как | Хамфри Дэви (1808) | |||||||||||||||||||||||||||
| Изотопы хлора | ||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||
Хлор является химическим элементом ; Он имеет символ CL и атомный номер 17. Второй светлый из галогенов , он появляется между фторином и бромом в периодической таблице, и его свойства в основном промежуточные между ними. Хлор-это желто-зеленый газ при комнатной температуре. Это чрезвычайно реактивный элемент и сильный окислительный агент : среди элементов он имеет наибольшее сродство электронов и третью по величине электроотрицательность в пересмотренной шкале Полингинга , за только кислород и фторином.
Хлор сыграл важную роль в экспериментах, проведенных средневековыми алхимиками , которые обычно включают нагрев хлоридных солей, таких как хлорид аммония ( саль -аммиак ) и хлорид натрия ( общая соль ), продуцируя различные химические вещества, содержащие хлор, такие как хлорид водорода , ртуть (II) ) хлорид (коррозийный сублимат) и аква -реглас . Тем не менее, природа свободного газа хлора как отдельного вещества была признана только около 1630 года баптистом Яна Ван Хельмонт . Карл Вильгельм Шил написал описание газа хлора в 1774 году, предполагая, что он является оксидом нового элемента. В 1809 году химики предположили, что газ может быть чистым элементом, и это было подтверждено сэром Хамфри Дэви в 1810 году, который назвал его в честь древнегреческого χλωρός ( хлорос , «бледно -зеленый») из -за его цвета.
Из -за своей великой реакционной способности весь хлор в коре Земли в форме ионных хлоридных соединений, который включает в себя столовую соль. Это второй самый обильный галоген (после фтора) и 20-й самый распространенный элемент в коре Земли. Эти кристаллические отложения, тем не менее, затмеваются огромными запасами хлорида в морской воде.
Элементный хлор коммерчески производится из рассола путем электролиза , преимущественно в процессе хлоралкали . Высокий окислительный потенциал элементарного хлора привел к развитию коммерческих отбеливателей и дезинфицирующих средств , а также реагента для многих процессов в химической промышленности. Хлор используется при изготовлении широкого спектра потребительских товаров, около двух третей из них органических химикатов, таких как поливинилхлорид (ПВХ), многие промежуточные продукты для производства пластмассы и другие конечные продукты, которые не содержат элемента. В качестве общего дезинфицирующего средства, элементарные хлоры игенерирующие хлоры используются более непосредственно в бассейнах, чтобы сохранить их санитарные . Элементный хлор при высокой концентрации чрезвычайно опасен и ядовителен для большинства живых организмов. Как агент по химической войне , хлор впервые использовался в Первой мировой войне в качестве оружия ядовитого газа .
В форме хлоридных ионов хлор необходим для всех известных видов жизни. Другие виды соединений хлора редки в живых организмах, а искусственно продуцируемые хлорированные органики варьируются от инертных до токсичных. В верхней атмосфере , содержащие хлор, содержащие органические молекулы, такие как хлорфторуглероды, были вовлечены в истощение озона . Небольшие количества элементарного хлора генерируются путем окисления хлоридных ионов в нейтрофилах в рамках ответа иммунной системы против бактерий.
История
Наиболее распространенное соединение хлора, хлорид натрия, известно с древних времен; Археологи обнаружили доказательства того, что каменная соль использовалась еще в 3000 г. до н.э. и рассол уже в 6000 г. до н.э. [ 9 ]
Ранние открытия
Около 900 авторы арабских сочинений, приписанных Джабиру Ибн Хайяну (латынь: Гебер) и персидскому врачу и алхимику Абу Бакр аль-Рази ( ок. 865–925, латинские: раза) экспериментировали с сэли-аммиаком ( хлорид аммония ) , который, когда он был дистиллирован вместе с купоросом (гидратированные сульфаты различных металлов) продуцировал хлорид водорода . [ 10 ] Тем не менее, представляется, что в этих ранних экспериментах с хлоридными солями были отброшены газообразные продукты, а хлорид водорода мог быть получен много раз, прежде чем было обнаружено, что его можно использовать в химическом использовании. [ 11 ] Одним из первых таких применений был синтез хлорида ртути (II) (коррозийный сублимам), чье производство из нагрева ртути либо с помощью квасцов , и хлорида аммония, либо с витриолом и хлоридом натрия была впервые описана в De Aluminibus et salibus (»(» На выпускниках и солях »арабский текст одиннадцатого или двенадцатого века ложно приписывается Абу Бакру аль-Рази и переведен на латынь во второй половине двенадцатого века Джерардом Кремона , 1144–11187). [ 12 ] Другим важным развитием было открытие псевдогебера (в De Inventione Veritatis , «об открытии истины», после c. 1300), что, добавив хлорид аммония в азотную кислоту , сильный растворитель, способный растворять золото (т.е., аква Regia ) может быть произведена. [ 13 ] Хотя Aqua Regia является нестабильной смесью, которая постоянно испускает пары, содержащие свободный газ хлора, этот газ хлора, по -видимому, был игнорируется до c. 1630 год, когда его природа как отдельное газообразное вещество было признано бродютным химиком и врачом Яном Баптистом Ван Хельмонтом . [ 14 ] [ в 1 ]

Изоляция
Элемент был впервые подробно изучен в 1774 году шведским химиком Карлом Вильгельмом Шилом , и ему приписывают открытие. [ 15 ] [ 16 ] Scheele производил хлор, реагируя MNO 2 (как минеральный пиролузит ) с HCl: [ 14 ]
- 4 HCl + Mno 2 → Mncl 2 + 2 H 2 O + Cl 2
Шеле наблюдал несколько свойств хлора: отбеливающее влияние на лакмус , смертельное воздействие на насекомых, желто-зеленый цвет и запах, аналогичный аква-режиме . [ 17 ] Он назвал это « дефлогистированным ячеечным воздухом », так как это газ (затем называемый «воздух»), и он поступил из соляной кислоты (затем известной как «сочекалады»). [ 16 ] Он не смог установить хлор как элемент. [ 16 ]
Общая химическая теория в то время считала, что кислота - это соединение, которое содержит кислород (остатки этого выживают в немецких и голландских названиях кислорода : Sauerstoff или Zuurstof , оба переводятся на английский как кислотный вещество ), так что ряд химиков, включая химиков, включая химиков, в том числе химики, в том числе химики, в том числе химики, в том числе химики, в том числе химики, в том числе химики, в том числе химики, в том числе химики, в том числе химики, в том числе химики, в том числе химики, в том числе химики, в том числе химики. Клод Бертолле Шеле , предположил, что дефлогистированный воздух сориальной кислоты должен быть комбинацией кислорода и еще не обнаруженного элемента Muriaticum . [ 18 ] [ 19 ]
В 1809 году Джозеф Луи Гей-Луссак и Луи-Жак Тенард попытались разложить дефлогистированную сочекающую кислоту свободного элемента , реагируя его с помощью древесного угля, чтобы высвободить сочетание (и углекислый газ). [ 16 ] Они не преуспели и опубликовали отчет, в котором они рассмотрели возможность того, что дефлогистированный воздух соляной кислоты является элементом, но не были убеждены. [ 20 ]
В 1810 году сэр Хамфри Дэви снова попробовал тот же эксперимент и пришел к выводу, что это вещество было элементом, а не соединением. [ 16 ] Он объявил о своих результатах Королевскому обществу 15 ноября того же года. [ 14 ] В то время он назвал этот новый элемент «хлор» из греческого слова χλωρος ( Chlōros , «зелено-желтый»), в отношении его цвета. [ 21 ] Название « Галоген », что означает «производитель соли», первоначально использовалось для хлора в 1811 году Иоганном Саломо Кристофом Швегером . [ 22 ] Этот термин был позже использован в качестве общего термина для описания всех элементов в семействе хлор (фтор, бром, йод), после предложения Йенса Якоба Берцелиуса в 1826 году. [ 23 ] [ 24 ] В 1823 году Майкл Фарадей сжимался хлор впервые, [ 25 ] [ 26 ] [ 27 ] и продемонстрировал, что то, что тогда было известно как «твердый хлор», имело структуру гидрата хлора (CL 2 · H 2 O). [ 14 ]
Позже использует
Хлорный газ впервые использовался французским химиком Клодом Бертоллетом для отбеливания текстиля в 1785 году. [ 28 ] [ 29 ] Современные отбеливатели были получены в результате дальнейшей работы Бертолета, который впервые произвел гипохлорит натрия городе в 1789 году в своей лаборатории в Горном (ныне часть Парижа , Франция), проходя из газа хлора через раствор карбоната натрия. Полученная жидкость, известная как « eau de Javel » (« вода вода »), была слабым раствором гипохлорита натрия . Этот процесс был не очень эффективным, и были запрошены альтернативные методы производства. Шотландский химик и промышленник Чарльз Теннант сначала произвел раствор гипохлорита кальция («хлорированная извести»), затем твердый гипохлорит кальция (отбеливающий порошок). [ 28 ] Эти соединения давали низкие уровни элементарного хлора и могли быть более эффективно транспортируются, чем гипохлорит натрия, который оставался в качестве разбавленных растворов, потому что при очистке для устранения воды он стал опасно мощным и нестабильным окислителем. Ближе к концу девятнадцатого века ES Smith запатентовал метод выработки гипохлорита натрия, включающего электролиз рассола с образованием гидроксида натрия и газа хлора, который затем смешивал с образованием гипохлорита натрия. [ 30 ] Это известно как процесс Chloralkali , впервые введенный в промышленном масштабе в 1892 году, а теперь и источник большинства элементарных хлора и гидроксида натрия. [ 31 ] В 1884 году Chemischen Fabrik Griesheim из Германии разработал еще один процесс Chloralkali , который вступил в коммерческое производство в 1888 году. [ 32 ]
Элементные растворы хлора, растворенные в химически основной воде ( гипохлорит натрия и кальция ), были сначала использованы в качестве анти- гнойновых средств и дезинфицирующих веществ в 1820-х годах, во Франции, задолго до установления теории зародышевой теории заболевания . Эта практика была впервые привлечена Антуан-Жермен Лабарраке , который адаптировал отбеливатель Бертолета и другие препараты хлора. [ 33 ] С тех пор элементарный хлор выполнял постоянную функцию в актуальном антисепсе (растворные растворы орошения и тому подобное) и общественную санитарию, особенно в плавании и питьевой воде. [ 17 ]
Газ хлора был впервые использован в качестве оружия 22 апреля 1915 года во Ипресе второй битве при немецкой армией . [ 34 ] [ 35 ] Влияние на союзников было разрушительным, потому что существующие газовые маски были трудно развернуть и не были широко распространены. [ 36 ] [ 37 ]
Характеристики



Хлор является вторым галогеном , являющимся несеталью в группе 17 периодической таблицы. Таким образом, его свойства аналогичны фторину , бромам и йоду , и в значительной степени промежуточные между свойствами первых двух. Хлор имеет конфигурацию электрона [NE] 3S 2 3 с 5 , с семью электронами в третьей и внешней оболочке, действуя как валентные электроны . Как и все галогены, он, таким образом, является одним электроном, не так ли, что он является полным октетом и, следовательно, является сильным окислительным агентом, реагирующим со многими элементами, чтобы завершить его внешнюю оболочку. [ 38 ] В соответствии с периодическими тенденциями , он является промежуточным по электроотрицательности между фторином и бромом (F: 3,98, CL: 3,16, BR: 2,96, I: 2,66) и менее реактивно, чем фтор и более реактивный, чем бромин. Это также более слабый окислительный агент, чем фторин, но более сильный, чем бром. И наоборот, ион хлорида является более слабым восстановительным агентом, чем бромид, но более сильный, чем фторид. [ 38 ] Он является промежуточным по атомному радиусу между фторином и бромом, и это приводит ко многим его атомным свойствам, аналогично продолжая тенденцию от йода до брома вверх, такие как энергия первой ионизации , сродство к электрону , энтальпию диссоциации молекулы x 2 (x = x = x = x = x = x = x = x = x = Cl, Br, I), ионный радиус и длина связи x - x. (Фтор является аномальным из -за его небольшого размера.) [ 38 ]
Все четыре стабильных галогенов испытывают межмолекулярные силы притяжения Ван -дер -Ваальса , и их сила увеличивается вместе с количеством электронов среди всех гомонуклеарных диатомических молекул галогена. Таким образом, точки плавления и кипения хлора являются промежуточными между точками фтора и брома: хлор плавится при -101,0 ° C и кипит при -34,0 ° C. В результате увеличения молекулярной массы галогенов вниз по группе, плотность и нагрев слияния и испарение хлора снова промежуточные между плотностью брома и фтора, хотя все их тепла испарения довольно низкие (приводят к высокой нестабильности). Благодаря их диатомной молекулярной структуре. [ 38 ] Галогенов темнеют по цвету, когда группа спускается: Таким образом, в то время как фтор является бледно-желтым газом, хлор отчетливо желто-зеленый. Эта тенденция возникает потому, что длина волн видимого света, поглощаемого галогенами, увеличивает группу. [ 38 ] В частности, цвет галогена, такой как хлор, является результатом перехода электронного перехода между самым высоким антиспендиционным π G -молекулярной орбитальной орбиталью и самой низкой вакантной антиверсинговой σ -U -молекулярной орбиталью. [ 39 ] Цвет исчезает при низких температурах, так что твердый хлор при -195 ° С является почти бесцветным. [ 38 ]
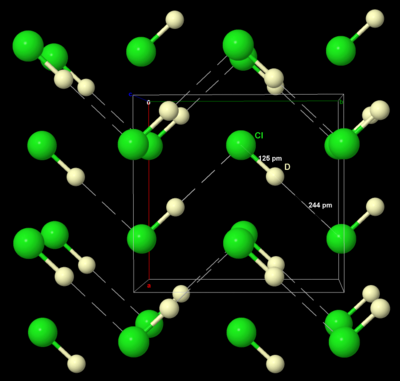
Как и твердый бром и йод, твердые кристаллизы хлора в орторомбической кристаллической системе , в слоистой решетке молекул Cl 2 . Расстояние CL -CL составляет 198 вечера (близко к газообразному расстоянию CL -CL 199 PM), а расстояние Cl · · · Cl между молекулами составляет 332 вечера в слое и 382 вечера между слоями (сравните радиус ван -дер -ваальса Хлор, 180 вечера). Эта структура означает, что хлор является очень плохим проводником электроэнергии, и, действительно, его проводимость настолько низкая, что является практически неизмеримым. [ 38 ]
Изотопы
Хлор имеет два стабильных изотопа, 35 Cl и 37 Калькуляция Это только два натуральных изотопа, встречающихся в количестве, с 35 CL составляет 76% натурального хлора и 37 CL, составляющий оставшиеся 24%. Оба синтезируются в звездах в процессах сжигания кислорода и сжигания кремния . [ 40 ] Оба имеют ядерный спин 3/2+ и, следовательно, могут использоваться для ядерного магнитного резонанса , хотя величина спина превышает 1/2 приводит к не сферическому распределению ядерного заряда и следовательно , Результирующая квадруполярная релаксация. Другие изотопы хлора являются радиоактивными, с полураспадами, слишком короткими, чтобы возникнуть в природе , изначально . Из них наиболее часто используются в лаборатории 36 150 ( T 1/2 = 3,0 × 10 5 y) и 38 CL ( T 1/2 = 37,2 мин), который может быть получен из активации нейтронов природного хлора. [ 38 ]
Самый стабильный радиоизотоп хлора - это 36 Калькуляция Основной режим распада изотопов легче, чем 35 CL - это электронный захват на изотопы серы ; из изотопов тяжелее, чем 37 CL - бета -распад на изотопы аргона ; и 36 CL может разлагаться на любой режим до стабильного 36 S или 36 С. [ 41 ] 36 CL встречается в следовых количествах в природе в виде космогенного нуклида в соотношении около (7–10) × 10 −13 до 1 с стабильными изотопами хлора: он производится в атмосфере размаскивания путем 36 AR по взаимодействию с Cosmic Ray Protons . В верхнем метре литосферы , 36 CL генерируется главным образом тепловой нейтронной активацией 35 CL и разбрызгивание 39 K и 40 Калифорнийский В подповерхностной среде Muon захватывает 40 CA становится более важным как способ генерировать 36 Калькуляция [ 42 ] [ 43 ]
Химия и соединения
| Х | XX | HX | BX 3 | ALX 3 | CX 4 |
|---|---|---|---|---|---|
| Фон | 159 | 574 | 645 | 582 | 456 |
| Калькуляция | 243 | 428 | 444 | 427 | 327 |
| Бренд | 193 | 363 | 368 | 360 | 272 |
| я | 151 | 294 | 272 | 285 | 239 |
Хлор является промежуточным по реактивности между фторином и бромом и является одним из наиболее реактивных элементов. Хлор является более слабым окислительным агентом, чем фторином, но более сильным, чем бром или йод. Это можно увидеть из стандартных потенциалов электродов x 2 /x − Пары (F, +2,866 V; Cl, +1.395 V; Br, +1.087 V; I, +0,615 V; At , приблизительно +0,3 В). Тем не менее, эта тенденция не показана в энергиях связи, потому что фтор является единственным числом из -за его небольшого размера, низкой полярируемости и неспособности показать гипервалентность . В качестве другого отличия, хлор имеет значительную химию в положительных состояниях окисления, а фтор - нет. Хлорирование часто приводит к более высоким состояниям окисления, чем бромирование или йодирование, но более низкие состояния окисления, чем фторирование. Хлор имеет тенденцию реагировать с соединениями, включая связи M - M, M - H или M - C, с образованием связей M - CL. [ 39 ]
Учитывая, что e ° ( 1/2 O) = +1,229 В, что меньше +1,395 O 2 / H 2 В, можно ожидать, что хлор должен иметь возможность окислить воду до кислорода и соляной кислоты. Тем не менее, кинетика этой реакции является неблагоприятной, и существует также пузырьковое воздействие , которое следует учитывать, так что электролиз растворов водного хлорида развивает газовый газ хлора, а не газовый кислород, что очень полезен для промышленного производства хлора. [ 44 ]
Хлорид водорода
Самым простым содержанием хлора является хлорид водорода , HCl, основной химический веществ в промышленности, а также в лаборатории, как в виде газа, так и растворенных в воде в качестве соляной кислоты . Он часто производится сжиганием газа водорода в газе хлора или как побочный продукт хлорирующих углеводородов . Другой подход состоит в том, чтобы лечить хлорид натрия концентрированной серной кислотой с образованием соляной кислоты, также известной как процесс «соленой корпус»: [ 45 ]
- NaCl + h 2 so 4 nahso 4 + hcl
- NaCl + nahso 4 na 2 so 4 + hcl
В лаборатории можно изготовить газ хлористого водорода, высушивая кислоту концентрированной серной кислотой. Хлорид дейтерия, DCL, может быть получен путем реагирования бензоилхлорида с тяжелой водой (D 2 O). [ 45 ]
При комнатной температуре хлорид водорода представляет собой бесцветный газ, как и все галогениды водорода, кроме фторида водорода , поскольку водород не может образовывать сильные водородные связи с более крупным электроотрицательным атомом хлора; Тем не менее, слабая водородная связь присутствует в твердом кристаллическом хлориде водорода при низких температурах, аналогично структуре фторида водорода, до того, как начнут преобладать расстройство при повышении температуры. [ 45 ] Соляная кислота является сильной кислотой (P k a = −7), потому что водородные связи с хлором слишком слабы, чтобы ингибировать диссоциацию. Система HCl/H 2 O имеет много гидратов HCl · N H 2 O Для n = 1, 2, 3, 4 и 6. За пределами смеси 1: 1 HCl и H 2 O Система полностью разделяется на две отдельные жидкие фазы. Соляная кислота образует азеотроп с точкой кипения 108,58 ° C при 20,22 г HCl на 100 г раствора; Таким образом, соляная кислота не может быть сосредоточена за этой точкой дистилляцией. [ 46 ]
В отличие от фторида водорода, с растворителем трудно работать с бельемдрятным жидким водородом, поскольку его температура кипения низкая, он имеет небольшую диапазон жидкости, его диэлектрическая постоянная низкая и не диссоциации заметно в H 2 Cl. + и Hcl −
2 ионы - последний, в любом случае, гораздо менее стабильны, чем ионы бифлуорида ( HF −
2 ) Из -за очень слабой водородной связи между водородом и хлором, хотя его соли с очень большими и слабо поляризующими катионами, такими как CS + и nr +
4 (r я , и пить = не ) все еще может быть изолирован. Безводный хлорид водорода представляет собой плохой растворитель, способный растворить только мелкие молекулярные соединения, такие как нитрозилхлорид и фенол , или соли с очень низкими энергиями решетки, такими как галогениды тетраалкиламмония. Он легко протонирует электрофилы, содержащие одинокие пары или π-связи. Сольволиз , реакции замены лиганда и окисление хорошо охарактеризованы в растворе хлорида водорода: [ 47 ]
- PH 3 SNCL + HCl ⟶ PH 2 SNCL 2 + PHH (сольволиз)
- PH 3 COH + 3 HCl ⟶ PH
3 c +
Hcl −
2 + h 3 o + Калькуляция − (Солволиз) - Мне
4 н +
Hcl −
2 + bcl 3 ⟶ меня
4 н +
Блайт −
4 + HCl (замена лиганда) - PCL 3 + CL 2 + HCl ⟶ PCL +
4 HCl −
2 (окисление)
Другие бинарные хлориды

Почти все элементы в периодической таблице образуют двоичные хлориды. Исключения определенно находятся в меньшинстве и в каждом случае по одной из трех причин: экстремальная инертность и нежелание участвовать в химических реакциях ( благородные газы , за исключением ксенона в очень нестабильном XECL 2 и XECL 4 ); Экстремальная ядерная нестабильность, затрудняющая химическое исследование перед распадом и трансмутацией (многие из самых тяжелых элементов за пределами висмута ); и наличие электроотрицательности выше, чем хлор ( кислород и фтор ), так что результирующие бинарные соединения формально не являются хлоридами, а скорее оксидами или фторидами хлора. [ 48 ] Несмотря на то, что азот в NCL 3 несет отрицательный заряд, соединение обычно называется азотом трихлорида .
Хлорирование металлов с CL 2 обычно приводит к более высокого уровня окисления, чем бромирование с BR 2 , когда доступно множественные состояния окисления, например, в MOCL 5 и MOBR 3 . Хлориды могут быть изготовлены путем реакции элемента или его оксида, гидроксида или карбоната с соляной кислотой, а затем дегидратируются мягкими высокими температурами в сочетании с низким давлением или безводом водорода. Эти методы работают лучше всего, когда хлоридный продукт стабилен гидролизу; В противном случае возможности включают высокотемпературное окислительное хлорирование элемента с хлорином или хлоридом водорода, высокотемпературное хлорирование оксида металла или другого галогенида с помощью хлора, летучего металлического хлорида, тетрахлорида углерода или органического хлорида. Например, диоксид циркония реагирует с хлором в стандартных условиях с образованием тетрахлорида циркония , а урановый триоксид реагирует с гексахлорпропеном при нагревании при рефлюксе, чтобы получить тетрахлорид урана . Второй пример также включает в себя сокращение в Состояние окисления , которое также может быть достигнуто путем уменьшения более высокого хлорида с использованием водорода или металла в качестве восстановительного агента. Это также может быть достигнуто путем термического разложения или диспропорции следующим образом: [ 48 ]
- EUCL 3 + 1/2 + 2 H Eucl ⟶ 2 HCl
- Recl 5 recl 3 + cl 2
- Aucl 3 Aucl + Cl 2
Большинство хлоридов металлов с металлом в низких состояниях окисления (+1 до +3) являются ионными. Нематалы, как правило, образуют ковалентные молекулярные хлориды, как и металлы в высоких состояниях окисления от +3 и выше. Как ионные, так и ковалентные хлориды известны металлами в состоянии окисления +3 (например, хлорид скандала в основном ионный, но хлорид алюминия не является). Хлорид серебра очень нерастворим в воде и, таким образом, часто используется в качестве качественного теста для хлора. [ 48 ]
Полихлорные соединения
Хотя дихлор является сильным окислительным агентом с высокой первой энергией ионизации, он может быть окислен в экстремальных условиях для формирования [CL 2 ] + катион Это очень нестабильно и характеризуется его электронным спектром полос только при получении в пробирке с низким давлением. Желтый [CL 3 ] + катион более стабилен и может быть получен следующим образом: [ 49 ]
- CL 2 + CLF + ASF 5 [CL 3 ] + [ASF 6 ] −
Эта реакция проводится в пентафториде окисляющего растворителя . Анион трихлорида, [CL 3 ] − , также был охарактеризован; Это аналогично трийодиду . [ 50 ]
Хлор фторидов
Три фторида хлора образуют подмножество межгогенных соединений, все из которых являются диамагнитными . [ 50 ] Известны некоторые катионные и анионные производные, такие как CLF −
2 , clf −
4 , clf +
2 , и Cl 2 F + . [ 51 ] Также известны некоторые псевдохалиды хлора, такие как хлорид цианогена (CLCN, линейный), циановый хлора хлор (CLNCO), теоцианат (CLSCN, в отличие от его кислорода) и азида хлора (CLN 3 ). [ 50 ]
Монофлуорид хлора (CLF) чрезвычайно термически стабилен и продается в коммерческом виде в 500-граммовых стальных бутылках. Это бесцветный газ, который тает при -155,6 ° C и кипит при -100,1 ° C. Он может быть получен путем реакции его элементов при 225 ° C, хотя затем он должен быть отделен и очищен от трифторида хлора и его реагентов. Его свойства в основном промежуточные между свойствами хлора и фтора. Он будет реагировать со многими металлами и неметалами по комнатной температуре и выше, флуация их и освобождает хлор. Он также будет выступать в качестве хлорфтоорирующего агента, добавляя хлор и фтор через множественную связь или путем окисления: например, он будет атаковать угарный газ, образуя карбонил хлорфлуорид, COFCL. Он будет аналогично реагировать с гексафторуацетоном , (CF 3 ) 2 CO, с калиевым фторидом катализатором для получения гепптоафторзопропильного гипохлорита, (CF 3 ) 2 CFOCL; с нитрилами RCN для получения RCF 2 NCL 2 ; и с оксидами серы So 2 и So 3 для получения CLSO 2 F и Closo 2 F соответственно. Он также будет реагировать экзотермически с помощью соединений, содержащих –OH и nh группы, таких как вода: [ 50 ]
- H 2 O + 2 Clf ⟶ 2 Hf + Cl 2 O
Хлор трифторид (CLF 3 ) представляет собой летучую бесцветную молекулярную жидкость, которая плавится при -76,3 ° C и кипит при 11,8 ° C. Он может быть образован непосредственно фторирующим газообразным хлором или монофторидом хлора при 200–300 ° C. которые он поджигает, водород , калий , фосфор , мышьяк , сурьма известных, список элементов , серная , селен , теллур , бромин , йодин и порошковый , разнообразным содержащий Одно из наиболее реактивных химических соединений , , является и железо . Он также зажигает воду, наряду со многими веществами, которые в обычных обстоятельствах будут считаться химически инертными, такими как асбест , бетон, стекло и песок. При нагревании он даже будет коррозировать благородные металлы в качестве палладий , платины и золота , и даже благородных газов ксенон и радон не избегают фторирования. Несоответствующий фторидный слой образуется с помощью натрия , магния , алюминия , цинка , олова и серебра , которые могут быть удалены путем нагрева. Никелевые , медные и стальные контейнеры обычно используются из -за их великой устойчивости к атаке хлором трифторида, вытекающим из образования нереактивного слоя фторида металла. Его реакция с Гидразин с образованием фторида водорода, азота и хлора использовали в экспериментальном ракетном двигателе, но у него были проблемы, в значительной степени связанные с его экстремальной гиперголичностью, приводящей к воспламенению без какой -либо измеримой задержки. Сегодня он в основном используется в обработке ядерного топлива, для окисления урана до уранового гексафторида для его обогащения и отделения его от плутония , а также в полупроводниковой промышленности, где он используется для очистки химических камер осаждения пара. [ 52 ] Он может выступать в качестве донора или акцептора фторида (основание Льюиса или кислота), хотя он не рассекается заметно в CLF +
2 и Clf −
4 ионы. [ 53 ]
Хлор пентафторид (CLF 5 ) изготавливается в больших масштабах путем прямого фтора хлора с избыточным фториновым газом при 350 ° C и 250 атм и в небольшом масштабе, реагируя хлориды металлов с фториновым газом при 100–300 ° C. Он плавится при -103 ° C и кипит при -13,1 ° C. Это очень сильный фторирующий агент, хотя он все еще не так эффективен, как трифторид хлора. Было охарактеризовано лишь несколько специфических стехиометрических реакций. Мышьяк пентафторид и сурьма пентафторид формы ионных аддуктов формы [CLF 4 ] + [MF 6 ] − (M = as, sb) и вода энергично реагирует следующим образом: [ 54 ]
- 2 H 2 O + CLF 5 ⟶ 4 HF + FCLO 2
Продукт, фторид хрорила , является одним из пяти известных фторидов оксида хлора. Они варьируются от термически нестабильного FCLO до химически нереактивного фторида перхлорила (FCLO 3 ), остальные три - FCLO 2 , F 3 Clo и F 3 Clo 2 . Все пять ведут себя аналогично фторидам хлора, как структурно, так и химически, и могут действовать как кислоты или основания Льюиса, получая или теряя фторидные ионы соответственно или как очень сильные окислительные и фторирующие агенты. [ 55 ]
Оксиды хлора


Оксиды хлора хорошо изучены, несмотря на их нестабильность (все они являются эндотермическими соединениями). Они важны, потому что они производятся, когда хлорфторуглероды подвергаются фотолизу в верхней атмосфере и вызывают разрушение озонового слоя. Ни один из них не может быть сделан из непосредственного реагирования на элементы. [ 56 ]
Дихлор моноксида (CL 2 O) представляет собой коричневато-желтый газ (красный коричневый, когда твердый или жидкость), который может быть получен путем реагирования газа хлора с помощью желтого ртутного оксида (II) . Он очень растворим в воде, в которой она находится в равновесии с гипохлористой кислотой (HOCL), из которой он является ангидридом. Таким образом, это эффективный отбеливатель и в основном используется для изготовления гипохлоритов . Он взрывается на нагревании или появлении или в присутствии газа аммиака. [ 56 ]
Диоксид хлора (CLO 2 ) был первым оксидом хлора, который был обнаружен в 1811 году Хамфри Дэви . Это желтый парамагнитный газ (глубокий красный как твердый или жидкость), как и ожидалось от нечетного количества электронов: он стабилен к димеризации из-за делокализации непарного электрона. Он взрывается выше -40 ° C в качестве жидкости и под давлением в качестве газа и, следовательно, должен быть получен при низких концентрациях для отбеливания древесной пульпы и очистки воды. Обычно он готовится путем уменьшения хлората следующим образом: [ 56 ]
- Clo −
3 + cl − + 2 часа + ⟶ Clo 2 + 1/2 2 Cl 2 H O +
Таким образом, его производство тесно связано с окислительно -восстановительными реакциями хлорных оксоцидов. Это сильный окислительный агент, реагирующий с серной , фосфором , фосфором и калиевым борогидридом . Он растворяет экзотермически в воде, образуя темно-зеленые растворы, которые очень медленно разлагаются в темноте. Кристаллический клатрат гидраты Clo 2 · N H 2 O ( N ≈ 6–10) разделяются при низких температурах. Однако при наличии света эти растворы быстро фотодекомпалируют, образуя смесь хлорной и соляной кислоты. Фотолиз отдельных молекул Clo 2 приводит к радикалам Clo и Cloo, в то время как при комнатной температуре в основном хлор, кислород и некоторые Clo 3 и Cl 2 O 6 получены. CL 2 O 3 также образуется при фотолизировании твердого вещества при -78 ° C: это темно -коричневое твердое вещество, которое взрывается ниже 0 ° C. Радикал CLO приводит к истощению атмосферного озона и, таким образом, является экологически важным следующим образом: [ 56 ]
- Cl • + o 3 ⟶ clo • + o 2
- Clo • + o • ⟶ cl • + o 2
Хлор перхлорат (Cloclo 3 ) представляет собой бледно -желтую жидкость, которая менее стабильна, чем Clo 2 и разлагается при комнатной температуре, образуя хлор, кислород и гексоксид дихлорина (Cl 2 O 6 ). [ 56 ] Хлор перхлорат также может считаться производным хлора перхловой кислоты (Hoclo 3 ), аналогично термически нестабильным производным хлора других оксоцидов: примеры включают нитрат хлора (Clono 2 , энергично реактивные и взрывоопасные), а также флорозольфульф (Clono 2 F, более стабильный, но все еще чувствительный к влаге и очень реактивная). [ 57 ] Дихлориновый гексоксид представляет собой темно-красную жидкость, которая замораживает, образуя твердое вещество, которое становится желтым при -180 ° C: его обычно производится реакцией диоксида хлора с кислородом. Несмотря на попытки рационализировать его как димер CLO 3 , он реагирует больше, как будто это было хрорил перхлорат, [CLO 2 ] + [CLO 4 ] − , который был подтвержден правильной структурой твердого вещества. Он гидролизуется в воде, чтобы получить смесь хлорной и перхловой кислоты: аналогичная реакция с безводным фторидом водорода не доходит до завершения. [ 56 ]
Дихлориновый гептоксид (CL 2 O 7 ) представляет собой ангидрид перхловой кислоты (HCLO 4 ) и может быть легко получен из нее путем обезвоживания ее фосфорной кислотой при -10 ° C, а затем перегоняет продукт при -35 ° C и 1 мм рт. Это чувствительная к шоку, бесцветную маслянистую жидкость. Это наименее реактивное для оксидов хлора, будучи единственным, кто не устанавливает органические материалы на огне при комнатной температуре. Он может быть растворен в воде для регенерации перхловой кислоты или в водных щелочках для регенерации перхлоратов. Тем не менее, он термически разлагается взрывоопасно, разбивая одну из центральных связей CL -O, производя радикалы CLO 3 и CLO 4 , которые немедленно разлагаются на элементы через промежуточные оксиды. [ 56 ]
Хлор оксоцидки и оксинионы
| E ° (пара) | а (ч + ) = 1 (кислота) |
E ° (пара) | о ( − ) = 1 (база) |
|---|---|---|---|
| Cl 2 /Cl − | +1.358 | Cl 2 /Cl − | +1.358 |
| Hocl/cl − | +1.484 | Clo − /Cl − | +0.890 |
| Clo − 3 /кл − |
+1.459 | ||
| Hocl/Cl 2 | +1.630 | Clo − /Cl 2 | +0.421 |
| HCLO 2 /CL 2 | +1.659 | ||
| Clo − 3 /cl 2 |
+1.468 | ||
| Clo − 4 /cl 2 |
+1.277 | ||
| Hclo 2 /Hocl | +1.701 | Clo − 2 /clo − |
+0.681 |
| Clo − 3 /clo − |
+0.488 | ||
| Clo − 3 /HCLO 2 |
+1.181 | Clo − 3 / clo − 2 |
+0.295 |
| Clo − 4 / clo − 3 |
+1.201 | Clo − 4 / clo − 3 |
+0.374 |
Хлор образует четыре оксоцида: гипохлористую кислоту (hocl), хлорию кислоту (Hoclo), хлорная кислота (Hoclo 2 ) и перхловая кислота (Hoclo 3 ). Как видно из окислительно -восстановительных потенциалов, приведенных в соседней таблице, хлор гораздо более стабилен к смазопоставлению в кислых растворах, чем в щелочных растворах: [ 44 ]
CL 2 + H 2 O ⇌ hocl + h + + Cl − K ac = 4,2 × 10 −4 мол 2 л −2 Cl 2 + 2 Ох − ⇌ OCL − + H 2 o + cl − K alk = 7,5 × 10 15 мол −1 л
Ионы гипохлорита также еще раз непропорционаруются для производства хлорида и хлората (3 Clo − ⇌ 2 кл − + Clo −
3 ) Но эта реакция довольно медленная при температуре ниже 70 ° C, несмотря на очень благоприятную константу равновесия 10 27 Полем Ионы хлората могут сами непропорционально формировать хлорид и перхлорат (4 Clo −
3 ⇌ cl − + 3 Clo −
4 ) Но это все еще очень медленно даже при 100 ° С, несмотря на очень благоприятную константу равновесия 10 20 Полем Скорости реакции на хлорные оксианионы увеличиваются по мере уменьшения уровня окисления хлора. Сильные стороны хлора оксицидов очень быстро увеличиваются, поскольку состояние окисления хлора увеличивается из -за увеличения делокализации заряда в течение все большего и большего количества атомов кислорода в их конъюгатных основаниях. [ 44 ]
Большинство оксоцидов хлора могут быть получены путем использования этих реакций диспропорционирования. Гипохларистая кислота (HOCL) очень реактивная и довольно нестабильная; Его соли в основном используются для их отбеливающих и стерилизационных способностей. Они являются очень сильными окислителями, передающими атом кислорода в большинство неорганических видов. Хлорная кислота (hoclo) еще более нестабильна и не может быть выделена или концентрированной без разложения: она известна из разложения диоксида хлора водного хлора. Тем не менее, хлорит натрия является стабильной солью и полезен для отбеливания и снятия текстиля, как окислительный агент и в качестве источника диоксида хлора. Хлорово -кислота (Hoclo 2 ) представляет собой сильную кислоту, которая довольно стабильна в концентрации холодной воды до 30%, но при потеплении дает хлор и диоксид хлора. Испарение под пониженным давлением позволяет его сосредоточиться примерно до 40%, но затем оно разлагается до перхловой кислоты, хлора, кислорода, воды и диоксида хлора. Его самая важная соль - это Хлорат натрия , в основном используемый для изготовления диоксида хлора в мякоть от отбеливающей бумаги. Разложение хлората к хлориду и кислороду является распространенным способом продуцировать кислород в лаборатории в небольшом масштабе. Хлорид и хлорат могут контролировать хлор следующим образом: [ 58 ]
- Clo −
3 + 5 кл − + 6 ч + ⟶ 3 Cl 2 + 3 H 2 O
Перхлораты и перхловая кислота (Hoclo 3 ) являются наиболее стабильными оксо-компонентами хлора, в соответствии с тем фактом, что хлорные соединения наиболее стабильны, когда атом хлора находится в самом низком (-1) или самых высоких (+7) возможных состояниях окисления Полем Пархлорновая кислота и водные перхлораты являются энергичными, а иногда и сильными окислителями при нагревании, резко контрастируя с их в основном неактивной природой при комнатной температуре из -за высоких энергий активации этих реакций по кинетическим причинам. Перхлораты изготавливаются путем электролитически окисляющего хлората натрия, а перхловая кислота изготовлена путем реагирования безводного перхлората натрия или перхлората бария с концентрированной соляной кислотой, фильтрации от хлорида осажденного и переживания фильтрата, чтобы сконцентрировать его. Безводная перхловая кислота - это бесцветная подвижная жидкость, которая чувствительна к шоку, которая взрывается при контакте с большинством органических соединений, устанавливает йодид водорода и тионилхлорид в огне и даже окисляет серебро и золото. Хотя это слабый лиганд, слабее, чем вода, несколько соединений с участием скоординированных Clo −
4 известны. [ 58 ] В таблице ниже представлены типичные состояния окисления для элемента хлора, как указано в средних школах или колледжах. В любом случае на курсах химии в университете следует отметить, что существуют более сложные химические соединения, структуру которых можно объяснить только с использованием современных квантовых химических методов, например, кластерного технеция хлорид [(CH 3 ) 4 N] 3 [TC 6 CL 14 ], в котором 6 из 14 атомов хлора являются формально двухвалентными, а состояния окисления являются фракционными [1] . [ 59 ] Кроме того, все вышеперечисленные химические закономерности действительны для «нормальных» или близких к нормальным условиям, в то время как при сверхвысоких давлениях (например, в ядрах больших планет), хлор может проявлять состояние окисления -3, образуя NA3CL соединение с натрием, которое не вписывается в традиционные концепции химии. [ 60 ]
| Современное состояние окисления хлора | −1 | +1 | +3 | +5 | +7 |
|---|---|---|---|---|---|
| Имя | хлористый | гипохлорит | хлорит | Хлорат | перхлорат |
| Формула | Калькуляция − | Clo − | Clo − 2 |
Clo − 3 |
Clo − 4 |
| Структура | 
|

|

|
Соединения органохлора

Как и другие углеродистые связи, связь C -CL является общей функциональной группой, которая является частью основной органической химии . Формально соединения с этой функциональной группой могут считаться органическими производными хлоридного аниона. Из-за разницы электроотрицательности между хлором (3,16) и углеродом (2,55) углерод в связке C-CL является электронным дефицитом и, следовательно, электрофильным . Хлорирование изменяет физические свойства углеводородов несколькими способами: хлорокарбоны, как правило, плотнее, чем вода из -за более высокого атомного веса хлора по сравнению с водородом, а алифатические органохлориды являются алкилирующими агентами , потому что хлорид является уходной группой . [ 61 ]
Алканы и арил алканы могут быть хлорированы в условиях свободного радикала с ультрафиолетовым светом. Тем не менее, степень хлорирования трудно контролировать: реакция не является региоселективной и часто приводит к смесью различных изомеров с различными степенями хлорирования, хотя это может быть допустимо, если продукты легко разделяются. Арилхлориды могут быть приготовлены с помощью галогенирования Фриделя , используя хлор и кислотный катализатор Льюиса . [ 61 ] Реакция галоформ с использованием хлора и гидроксида натрия также способна генерировать алкилгалогениды из метилкетонов и родственные соединения. Хлор добавляет к множеству связей на алкенах и алкинах , давая ди- или тетрахлорные соединения. Однако из -за затрат и реакционной способности хлора органохлорные соединения чаще продуцируются с использованием хлорида водорода или с хлорирующими агентами, такими как пентахлорид фосфора (PCL 5 ) или тионилхлорид (SOCL 2 ). Последнее очень удобно в лаборатории, потому что все боковые продукты являются газообразными и не должны быть дистиллированы. [ 61 ]
Многие органохлорные соединения были изолированы из природных источников от бактерий до людей. [ 62 ] [ 63 ] Хлорированные органические соединения обнаруживаются практически в каждом классе биомолекул, включая алкалоиды , терпены , аминокислоты , флавоноиды , стероиды и жирные кислоты . [ 62 ] [ 64 ] Органохлориды, в том числе диоксины , производятся в высокотемпературной среде лесных пожаров, а диоксины были обнаружены в сохранившемся пепел, загрязненных молнией, которые предшествуют синтетическим диоксинам. [ 65 ] Кроме того, различные простые хлорированные углеводороды, включая дихлорметан, хлороформ и тетрахлорид углерода , были выделены из морских водорослей. [ 66 ] Большая часть хлорметана в окружающей среде вырабатывается естественным путем биологического разложения, лесных пожаров и вулканов. [ 67 ]
Некоторые виды органохлоридов, хотя и не все, имеют значительную токсичность для растений или животных, включая людей. Диоксины, полученные, когда органическое вещество сжигается в присутствии хлора, а некоторые инсектициды, такие как ДДТ , являются постоянными органическими загрязнителями , которые представляют опасности, когда они выпускаются в окружающую среду. Например, ДДТ, который широко использовался для контроля насекомых в середине 20 -го века, также накапливается в пищевых цепях и вызывает репродуктивные проблемы (например, истончение яичной скорлупы) у определенных видов птиц. [ 68 ] Из -за готового гомолитического деления связей C -CL для создания хлорных радикалов в верхней атмосфере, хлорфторуглероды были сняты из -за вреда, который они наносят на слой озона. [ 56 ]
Возникновение

Хлор слишком реактивен, чтобы возникнуть как свободный элемент в природе, но очень распространен в форме его хлоридных солей. Это 20 -й самый распространенный элемент [ 69 ] В коре Земли и составляют 126 частей на миллион из нее, через большие отложения хлоридных минералов, особенно хлорид натрия , которые были испарены из водоемов. Все эти бледные по сравнению с запасами хлоридных ионов в морской воде: меньшие количества при более высоких концентрациях встречаются в некоторых внутренних морях и подземных бухгах для соленой косой , таких как Великое Соленое озеро в штате Юта и Мертвое море в Израиле. [ 70 ]
Небольшие партии хлорного газа готовятся в лаборатории путем комбинирования соляной кислоты и диоксида марганца , но необходимость редко возникает из -за его готовой доступности. В промышленности элементарный хлор обычно производится электролизом хлорида натрия, растворенного в воде. Этот метод, процесс Chloralkali , промышленный в 1892 году, теперь предоставляет большинство промышленного газа хлора. [ 31 ] Наряду с хлором, метод дает водород и гидроксид натрия , который является наиболее ценным продуктом. Процесс продолжается в соответствии со следующим химическим уравнением : [ 71 ]
- 2 NaCl + 2 H → Cl 2 + H 2 + 2 + 2 + 2 + 2 + 2 + 2 + 2 + s
Производство
Хлор в первую очередь вырабатывается процессом Chloralkali , хотя существуют нехлоральные процессы. Глобальное производство в 2006 году оценивалось в 65 миллионов коротких тонн. [ 72 ] Наиболее заметное использование хлора в дезинфекции воды . 35-40 % продуцируемого хлора используется для изготовления поли (винилового хлорида) через этилендихлорид и винилхлорид . [ 73 ] Производимый хлор доступен в цилиндрах из размеров от 450 г до 70 кг, а также на барабанах (865 кг), вагонах танков (15 тонн на дорогах; 27–90 тонн по железной дороге) и баржи (600–1200 тонн) Полем [ 74 ] Из -за сложности транспортировки элементарного хлора производство обычно расположено рядом с тем местом, где он потребляется. В качестве примеров производители винилахлорида, такие как Westlake Chemical [ 75 ] и Formosa Plastics [ 76 ] интегрируют активы Chloralkali.
Процессы хлоралкали
Электролиз растворов хлорида продолжается в соответствии со следующими уравнениями:
- Катод: 2 H 2 O + 2 E − → H 2 + 2 OH −
- Анод: 2 кл − → CL 2 + 2 и −
В обычном случае, когда хлорид натрия электролизован, гидроксид натрия и хлор являются копродуками.
В промышленности есть три процесса хлоралкали:
- Процесс Кастнер -Келлнер , который использует ртутный электрод
- Процесс ячейки диафрагма, который использует диафрагму асбеста, которая отделяет катод и анод
- Процесс мембранной ячейки, который использует ионную обменную мембрану вместо диафрагмы
Процесс Кастнер -Кельнера был первым методом, используемым в конце девятнадцатого века для производства хлора в промышленном масштабе. [ 77 ] [ 78 ] Ртуть (токсичный) использовали в качестве электрода для объединения продукта натрия, предотвращая нежелательные боковые реакции.
В электролизе ячейки диафрагма диафрагма асбеста (или полимер-волокна) отделяет катод и анод , предотвращая образующее хлор в аноде от переосмысления с гидроксидом натрия и водородом, образованным в катоде. [ 79 ] Соляный раствор (рассол) непрерывно подается в анодное отделение и течет через диафрагму в катодное компартмент, где образуется каустический щелочи и частично истощается. Методы диафрагмы продуцируют разбавленную и слегка нечистую щелочи, но они не обременены проблемой утилизации ртути , и они более энергоэффективны. [ 31 ]
Электролиз мембранной ячейки использует проницаемую мембрану в качестве ионного обменника . Раствор хлорида насыщенного натрия (или калия) пропускается через анодное компартмент, оставляя при более низкой концентрации . Этот метод также производит очень чистый гидроксид натрия (или калия), но имеет недостаток в том, что требует очень чистого рассола при высоких концентрациях. [ 80 ]
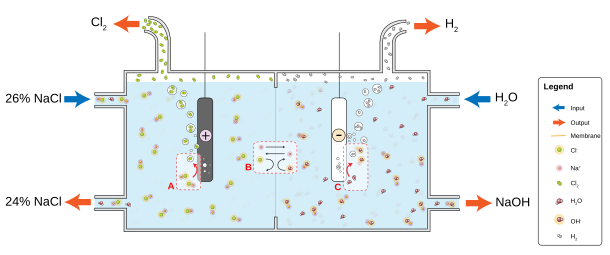
Не-хлоралкали процессы
В процессе дьякона хлорид водорода, извлеченного из производства органохлорных соединений, восстанавливается в виде хлора. Процесс опирается на окисление с использованием кислорода:
- 4 HCl + O 2 → 2 Cl 2 + 2 H 2 O
Реакция требует катализатора. Как представлена Дьяконом, ранние катализаторы были основаны на меди. Коммерческие процессы, такие как процесс MT-хлор Mitsui, переключились на катализаторы на основе хрома и рутения. [ 81 ]
Приложения

Хлорид натрия является наиболее распространенным соединением хлора и является основным источником хлора для спроса химической промышленностью. Около 15000 хлорсодержащих соединений коммерчески торгуются, в том числе такие разнообразные соединения, как хлорированный метан , этаны , винилхлорид , поливинилхлорид (ПВХ), алюминиевый трихлорид для катализа , хлориды магния, титана, циркония и приколы, которые являются прошюрами для магния , , титаном , цирконом и титана, циркония и покрова, которые являются прошюрмиями покровом. создавая чистую форму этих элементов. [ 17 ]
Количественно, из всего производимого элементарного хлора, около 63% используется при изготовлении органических соединений и 18% в производстве неорганических соединений хлора. [ 83 ] Около 15 000 соединений хлора используются в коммерческих целях. [ 84 ] Оставшиеся 19% произведенного хлора используются для отбеливателей и продуктов дезинфекции. [ 74 ] Наиболее значимыми из органических соединений с точки зрения объема производства являются 1,2-дихлорэтан и винилхлорид , промежуточные продукты в производстве ПВХ . Другими особенно важными органохлоринами являются метилхлорид , метиленхлорид , хлороформ , винилиденхлорид , трихлорэтилен , перхлорэтилен , аллилхлорид , эпихлоргидрин , хлорбензол , дихлорбензоны и трихлорбензен . Основные неорганические соединения включают HCl, Cl 2 O, Hocl, NaClo 3 , Alcl 3 , SICL 4 , SNCL 4 , PCL 3 , PCL 5 , POCL 3 , ASCL 3 , SBCL 3 , SBCL 5 , BICL 3 и ZnCl 2 . [ 74 ]
Санитария, дезинфекция и антисепсис
Борьба с гнилом
Во Франции (как и везде) кишечник животных был обработан для изготовления музыкальных инструментов, кожи Goldbeater и других продуктов. Это было сделано на «кишечных фабриках» ( Бойолди ), и это был многонациональный и нездоровый процесс. В 1820 году Société d'Upement Pourlie Nationale предложила приз за обнаружение метода, химического или механического, за отделение брюшной мембраны кишечника животных без гниения . [ 85 ] [ 86 ] Приз был выигран Антуан-Жермен Лабарраке , 44-летний французский химик и фармацевт, который обнаружил, что хлорированные растворы отбеливания Бертолета (« Eau de Javel ») не только разрушили запах гниения разложения тканей животных, но и на самом деле на самом деле, но и на самом деле на самом деле замедлил разложение. [ 86 ] [ 33 ]
Исследование Лабаррака привело к использованию хлоридов и гипохлоритов извести ( гипохлорит кальция ) и натрия ( гипохлорит натрия ) в богоудах. Было обнаружено, что те же химические вещества полезны при обычной дезинфекции и дезодоризация уборных , канализации , рынков, скотобусов , анатомических театров и Morgues. [ 87 ] Они добились успеха в больницах , лазаретах , тюрьмах , лазареях (как на суше, так и на море), нагрузки , конюшни , крупного рогатого скота и т. Д.; и они были полезны во время эксгумаций , [ 88 ] Бальзамирование , вспышки эпидемического заболевания, лихорадки и Blackleg у крупного рогатого скота. [ 85 ]
Дезинфекция
С 1828 года выступали хлорированные растворы извести и газировки Лабаррака для предотвращения инфекции (называемой «заразительной инфекцией», предположительно передаваемой « Миасмами »), и для лечения гниения существующих ран, включая септические раны. [ 89 ] В своей работе в 1828 году Лабаррак рекомендовал врачам дышать хлором, вымыл руки в хлорированную известь и даже посыпать хлорированную лайм о плащах пациентов в случаях «заразной инфекции». В 1828 году заражение инфекций было хорошо известно, хотя агентство микроба не было обнаружено более чем через полвека.
Во время парижской вспышки холеры в 1832 году большие количества так называемого хлорида извести были использованы для дезинфекции капитала. Это был не просто современный хлорид кальция , но газовый газ, растворенный в известком (разбавленный гидроксид кальция ), с образованием гипохлорита кальция (хлорированная извести). Открытие Лабаррака помогло убрать ужасное зловоние распада из больниц и рассеивать комнаты, и, по сути, эффективно дезодорировал латинский квартал Парижа. [ 90 ] Эти «гниловые миасмы» считали многими, чтобы вызвать распространение «заражения» и «инфекции» - оба слова, используемые до теории зародышей инфекции. Хлорид извести использовался для разрушения запахов и «гнилостического вещества». Один источник утверждает, что хлорид извести использовался доктором Джоном Сноу для дезинфекции воды из скважины, загрязненной холерой, которая кормила насос Брод-стрит в 1854 году в Лондоне, [ 91 ] Хотя три других авторитетных источника, которые описывают эту известную эпидемию холеры, не упоминают об инциденте. [ 92 ] [ 93 ] [ 94 ] Одна ссылка дает понять, что хлорид извести использовался для дезинфекции офтала и грязи на улицах, окружающих насос Брод-стрит-обычная практика в Англии в середине девятнадцатого века. [ 92 ] : 296
Semmelweis и эксперименты с антисепсом

растворов Лабаррака Возможно, самое известное применение растворов хлора и химических базовых было в 1847 году, когда Игназ Семмельвейс использовал хлорную воду (хлор, растворенный в чистой воде, который был дешевле, чем хлорированные растворы извести), чтобы дезинфицировать руки австрийских докторов, которые Семмелвей все еще заметил извести) переносил зловоние разложения из комнат для рассечений в комнаты для осмотра пациента. Задолго до теории зародышей болезни, Semmelweis предположил, что «трупные частицы» передавали распад от свежих медицинских трупов на живых пациентов, и он использовал хорошо известные «растворы лабаррака» в качестве единственного известного метода для удаления запаха и ткани. разложение (которое он обнаружил, что мыло не было). Решения оказались гораздо более эффективными антисептиками, чем SOAP (Semmelweis также знал о своей большей эффективности, но не причине), и это привело к празднованию успеха Semmelweis в прекращении передачи лихорадки от детей («пуэрюральная лихорадка») в беременности. Приходы Венская больница общего профиля в Австрии в 1847 году. [ 95 ]
Гораздо позже, во время Первой мировой войны в 1916 году стандартизированная и разбавленная модификация раствора Лабаррака, содержащего гипохлорит (0,5%) и борную кислоту в качестве кислого стабилизатора Генри Дрисдейл Дакин (который дал полную должность предыдущей работе Лабаррака в этой области) Полем Называемый раствором Дакина , метод ирригации раны с помощью хлорированных растворов позволял антисептическому лечению широкого спектра открытых ран задолго до современной эпохи антибиотиков. Модифицированная версия этого решения по -прежнему используется в ирригации раны в наше время, где она остается эффективной против бактерий, которые устойчивы к множественным антибиотикам (см. Century Pharmaceuticals ). [ 96 ]
Общественная санитария


Первое непрерывное применение хлорирования к употреблению воды в США было установлено в Джерси -Сити , штат Нью -Джерси, в 1908 году. [ 97 ] К 1918 году Министерство казначейства США призвало дезинфицировать всю питьевую воду с хлором. Хлор в настоящее время является важным химическим веществом для очистки воды (например, в водоочистных сооружениях), в дезинфицирующих средствах и в отбеливателе . Даже небольшие водоснабжения теперь обычно хлорируются. [ 98 ]
Обычно используется хлор (в форме гипохлористой кислоты ) для убийства бактерий и других микробов в расходных материалах для питьевой воды и общественных бассейнах. В большинстве частных бассейнов сама хлор не используется, а скорее гипохлорит натрия хлора и , образующийся из гидроксида натрия , или твердых таблеток хлорированных изоциануратов. Недостаток использования хлора в бассейнах состоит в том, что хлор реагирует с аминокислотами в белках в волосах и коже человека. Вопреки распространенному мнению, характерный «аромат хлора», связанный с бассейнами, является не результатом самого элементарного хлора, а хлорам , химического соединения, полученного в результате реакции свободного растворенного хлора с аминами в органических веществах, включая мочи и пота Полем [ 99 ] В качестве дезинфицирующего средства в воде хлор более чем в три раза выше, чем в Escherichia coli , чем Bromine , и более чем в шесть раз эффективнее йода . [ 100 ] Все чаще сам монохлорам напрямую добавляется к питьевой воде для целей дезинфекции, процесса, известного как хлораминация . [ 101 ]
Часто нецелесообразно хранить и использовать ядовитый газ хлора для очистки воды, поэтому используются альтернативные методы добавления хлора. К ним относятся растворы гипохлорита , которые постепенно высвобождают хлор в воду, и такие соединения, как дихлор-s-триазинетрион (дигидрат или безводный), иногда называемые «дихлор», а трихлор-s-триазинетрион, иногда называемый «Трихлор», и трихлор-s-триазинетрион, который иногда называют «Трихлор», а трихлор-s-триазинетер , иногда называемый «Трихлор», а трихлор-s-триазинетер. Полем Эти соединения стабильны, находясь твердыми и могут использоваться в порошковой, гранулированной или таблетке. При добавлении в небольших количествах для объединения водных или промышленных водных систем, атомы хлора гидролизуются из остальной части молекулы, образуя гипохлористую кислоту (HOCL), которая действует как общий биоцид , убивая зародышевые зародыши, микроорганизмы, водоросли и так далее. [ 102 ] [ 103 ]
Использовать как оружие
Первая мировая война
Хлор газ, также известный как Бертолит, впервые использовался в качестве оружия в Первой мировой войне Германией 22 апреля 1915 года во второй битве при Ипресе . [ 104 ] [ 105 ] Как описано солдатами, он имел характерный запах смесью перца и ананаса. [ 106 ] Это также попробовал металлик и загнал заднюю часть горла и груди. Хлор реагирует с водой в слизистой оболочке легких с образованием соляной кислоты , разрушительной для живой ткани и потенциально летальной. Респираторные системы человека могут быть защищены от газа хлора газовыми масками с активированным древесным углем или другими фильтрами, что делает газ хлора гораздо менее летальным, чем другое химическое оружие. Позже немецкий ученый стал нобелевским лауреатом, Фриц Хабером из Института Кайзера Вильгельма в Берлине, в сотрудничестве с немецким химическим конгломератом IG Farben , который разработал методы для сброса газа хлора против укоренившегося врага. [ 107 ] После его первого использования обе стороны в конфликте использовали хлор в качестве химического оружия, но вскоре его заменили более смертоносным фосгеном и горчичным газом . [ 108 ]
Средний Восток
Хлор газ также использовался во время войны в Ираке в провинции Анбар в 2007 году, когда повстанцы упаковывали бомбы грузовиков с растворными раковинами и танками хлора. В результате нападений погибли двух человек из взрывчатых веществ и тошнотворно более 350 лет. Большая часть смертей была вызвана силой взрывов, а не воздействием хлора, поскольку токсичный газ легко рассеивается и разбавляется в атмосфере в результате взрыва. В некоторых взрыве более ста гражданских лиц были госпитализированы из -за трудностей с дыханием. Иракские власти ужесточили безопасность для элементарного хлора, что важно для обеспечения безопасной питьевой воды населению. [ 109 ] [ 110 ]
23 октября 2014 года сообщалось, что Исламское государство Ирак и Левант использовали газ хлора в городе Дулуйя, Ирак . [ 111 ] Лабораторный анализ образцов одежды и почвы подтвердил использование газа хлора против курдских сил пешмерга в импровизированной атаке взрывчатых устройств, передаваемой транспортным средством, 23 января 2015 года на шоссе 47 Kiske Jounct возле Мосула. [ 112 ]
Другая страна на Ближнем Востоке, Сирия , использовала хлор в качестве химического оружия [ 113 ] Доставлено из бочковых бомб и ракет. [ 114 ] [ 115 ] В 2016 году механизм расследования OPCW-UN пришел к выводу, что сирийское правительство использовало хлор в качестве химического оружия в трех отдельных атаках. [ 116 ] Позднее расследования группы по расследованию и идентификации OPCW пришли к выводу, что сирийские ВВС были ответственны за атаки хлора в 2017 и 2018 годах. [ 117 ]
Биологическая роль
является Анион хлорида важным питательным веществом для метаболизма. Хлор необходим для производства соляной кислоты в желудке и в функциях клеточного насоса. [ 118 ] Основным диетическим источником является столовая соль или хлорид натрия. Чрезмерно низкие или высокие концентрации хлорида в крови являются примерами нарушений электролитов . Гипохлоремия (имеющая слишком мало хлорида) редко встречается в отсутствие других нарушений. Иногда это связано с гиповентиляцией . [ 119 ] Это может быть связано с хроническим респираторным ацидозом . [ 120 ] Гиперхлоремия (имеющая слишком много хлорида) обычно не создает симптомов. Когда возникают симптомы, они имеют тенденцию напоминать символы гипернатриемии (имея слишком много натрия ). Снижение хлорида крови приводит к дегидратации церебральной; Симптомы чаще всего вызваны быстрой регидратацией, что приводит к отеку головного мозга . Гиперхлоремия может влиять на транспорт кислорода. [ 121 ]
Опасности
| Опасности | |
|---|---|
| GHS Маркировка : [ 122 ] | |
  
| |
| Опасность | |
| H270 , H315 , H319 , H330 , H335 , H400 | |
| P220 , P233 , P244 , P261 , P304 , P312 , P340 , P403 , P410 | |
| NFPA 704 (Огненная бриллиант) | |
Хлор - это токсичный газ, который атакует дыхательную систему, глаза и кожу. [ 124 ] Поскольку он плотно, чем воздух, он имеет тенденцию накапливаться на дне плохо вентилируемых пространств. Хлорный газ является сильным окислителем, который может реагировать с помощью легковоспламеняющихся материалов. [ 125 ] [ 126 ]
Хлор обнаруживается с помощью измерительных устройств в концентрациях всего 0,2 частей на миллион (ppm) и по запаху при 3 ppm. Кашель и рвота могут возникнуть при 30 ч / млн и повреждение легких при 60 ч / млн. Около 1000 ч / млн может быть смертельным после нескольких глубоких вдохов газа. [ 17 ] Концентрация IDLH . (сразу же опасна для жизни и здоровья) составляет 10 ч / млн [ 127 ] Дыхание более низкие концентрации могут усугубить дыхательную систему, а воздействие газа может раздражать глаза. [ 128 ] Когда хлор вдыхается в концентрациях более 30 ч / млн, он реагирует с водой в легких, продуцируя соляную кислоту (HCl) и гипохларистую кислоту (HOCL).
При использовании на указанных уровнях дезинфекции воды реакция хлора с водой не является серьезной проблемой для здоровья человека. Другие материалы, присутствующие в воде, могут генерировать побочные продукты дезинфекции , которые связаны с негативным воздействием на здоровье человека. [ 129 ] [ 130 ]
В Соединенных Штатах Управление по безопасности и гигиене труда (OSHA) установило допустимый предел экспозиции для элементарного хлора при 1 ч/млн или 3 мг/м 3 Полем Национальный институт безопасности и гигиены труда определил рекомендуемый лимит воздействия 0,5 ч / млн в течение 15 минут. [ 127 ]
В доме происходят несчастные случаи, когда растворы отбеливателя гипохлорита вступают в контакт с определенными кислыми утечками для производства газа хлора. [ 131 ] Отбеливатель гипохлорита (популярная добавка для белья ) в сочетании с аммиаком (еще одна популярная добавка для белья) производит хлорам , еще одну токсичную группу химических веществ. [ 132 ]
Индуцированное хлором растрескивание в структурных материалах

Хлор широко используется для очистки воды, особенно питьевой воды и воды, используемой в бассейнах. Несколько катастрофических коллапсов потолков бассейна произошли из-за индуцированного хлором, вызванного стрессовым коррозионным растрескиванием стержней суспензии из нержавеющей стали . [ 133 ] Некоторые полимеры также чувствительны к атаке, включая ацетальную смолу и полибутен . Оба материала использовались в домашней сантехнике горячей и холодной воды, а растрескивание коррозии напряжения вызывало широкие неудачи в США в 1980 -х и 1990 -х годах. [ 134 ]
Хлор-железный огонь
Элемент железа может сочетаться с хлором при высоких температурах в сильной экзотермической реакции, создавая хлор-железный огонь . [ 135 ] [ 136 ] Огня хлора-железа представляет собой риск на заводах химических процессов, где большая часть трубопровода, которая несет хлор, изготовлена из стали. [ 135 ] [ 136 ]
Смотрите также
- Цикл хлора
- Отравление газом хлора
- Промышленное газ
- Деградация полимера
- Восстановительное дехлорирование
Примечания
- ^ Ван Хельмонт, Джон Крестителя (1682). Опера [все работает] (на латыни). Франкфурт-Ам-Мейн, (Германия): Иоганн просто Эритрополь. Из «Комплекса и элементализации mistiones». (Формирование комбинаций и смесей элементов), §37, p. 105: Архивировано 2023-12-30 на машине Wayback «Возьмите соленую петра, купороз , Alembico, по цементу (от воска, колофония и стекла Pulverre) горячо, Firmatus; (Возьмите равные части соленой петры [т.е., нитрат натрия], купорол [т.е., концентрированная серная кислота] и квасцы: сушьте каждый и комбинируйтесь одновременно; отключить воду [то есть жидкость]. Летучая соль [то есть дух соды, азотная кислота]. (Сделано] из воска, канифона и порошкообразного стекла) [который был] залит очень жарко; "De Flatibus" (на газах), с. 408 Архивированный 2023-12-30 в The Wayback Machine : «Sal Armeniacus Enim, & Aqua Chrysulca, Quae Singula, Se Se Distillari, Pospunt, & Pati Calorem: Sin Autem Jungantur, & Intepescant, Non Offint Non, Quin Statis в Gas Sylvestre, sive incoercibilem flatum transmutentur. " (Поистине армянская соль [то есть, хлорид аммония] и азотная кислота, каждая из которых может быть перегоняет само по себе, и подчиняться жару; но если, с другой стороны, они будут объединены и становятся теплыми, они не могут не измениться сразу в углекислый газ [Примечание: идентификация газа Ван Хельмонта ошибочно ошибочна] или неконсилируемый газ.)
Смотрите также:- Helmont, Johannes (Джоан) Baptista Van, Encyclopedia.com Архивировал 2021-12-18 на машине Wayback : «Другие были газом хлора из реакции азотной кислоты и аммиака SAL;…»
- Wisniak, Jaime (2009) «Карл Вильгельм Шил», Revista Cenic Ciencias Químicas , 40 (3): 165–73; Смотрите с. 168: «В начале семнадцатого века Йоханнес Баптист Ван Хельмонт (1579–1644) упомянул, что, когда соленник (хлорид натрия) или соль аммиакус и аква-хрисулька (азотная кислота) смешивались вместе, уточняемый конец (неконтентируемый газ) были развивался ".
Ссылки
- ^ «Стандартные атомные веса: хлор» . Ciaaw . 2009
- ^ Прохаска, Томас; Irrgeher, Johanna; Благосостояние, Жаклин; Böhlke, John K.; Чессон, Лесли А.; Коплен, Тайлер Б.; Ding, наконечник; Данн, Филипп Дж.Х.; Грёнинг, Манфред; Холден, Норман Э.; Meijer, Harro AJ (2022-05-04). «Стандартные атомные веса элементов 2021 (технический отчет IUPAC)» . Чистая и прикладная химия . doi : 10.1515/pac-2019-0603 . ISSN 1365-3075 .
- ^ Хлор , газовая энциклопедия, воздушная жидкость
- ^ Амброуз, D; Холл, диджей; Ли, да; Льюис, ГБ; Mash, CJ (1979). «Давление паров хлора». Журнал химической термодинамики . 11 : 1089–1094. doi : 10.1016/0021-9614 (79) 90139-3 .
- ^ Arblaster, John W. (2018). Выбранные значения кристаллографических свойств элементов . Материал Парк, штат Огайо: ASM International. ISBN 978-1-62708-155-9 .
- ^ Магнитная восприимчивость элементов и неорганических соединений , в Lide, Dr, ed. (2005). Справочник по химии и физике CRC (86 -е изд.). Boca Raton (FL): CRC Press. ISBN 0-8493-0486-5 .
- ^ Weast, Robert (1984). CRC, Справочник по химии и физике . Boca Raton, Florida: Publishing Company Chemical Rubber Company. с. E110. ISBN 0-8493-0464-4 .
- ^ Kondev, FG; Ван, М.; Хуан, WJ; Naimi, S.; Audi, G. (2021). «Оценка ядерных свойств Nubase2020» (PDF) . Китайская физика c . 45 (3): 030001. DOI : 10.1088/1674-1137/Abddae .
- ^ «Самое раннее производство соли в мире: ранняя неолитическая эксплуатация в Poiana Slatinei-Lunca, Румыния» . Архивировано из оригинала 30 апреля 2011 года . Получено 2008-07-10 .
- ^ Краус, Павел (1942–1943). Джабир ибн Хеййн: вклад в историю научных идей в исламе. I. Корпус писаний Джабириенса. II Джабир и греческая наука . Каир: Французский институт восточной археологии . ISBN 978-3487091150 Полем OCLC 468740510 . тол. II, с. 41–42; Малтхауф, Роберт П. (1966). Происхождение химии . Лондон: Oldbourne. С. 141–42.
- ^ Малтхауф 1966 , с. 142, примечание 79.
- ^ Multhauf 1966 , с. 160–163.
- ^ Карпенко, Владимир; Норрис, Джон А. (2002). «Пробись в истории химии» . Chemiche Listy . 96 (12): 997–1005. Архивировано из оригинала 2021-12-18 . Получено 2021-02-09 . п. 1002
- ^ Jump up to: а беременный в дюймовый Greenwood & Earnshaw 1997 , pp. 789–92
- ^ Шил, Карл Вильгельм (1774). и ее свойства] « OM Brunsten, Eller Magnesia, Och Dess Egenskaper» [On Braunstein [IE, пиролузит, диоксид марганца], или магнезия, . Kongliga Vetenskaps Academiens Hastlingar [Труды Королевской научной академии] (на шведском языке). 35 : 89–116, 177–94. Архивировано из оригинала 2020-04-23 . Получено 2018-02-19 . В разделе 6 на стр. 93–94 его бумаги, заархивированной 2021-12-18 на машине Wayback , Шиле описал, как хлор получали, когда смесь соляной кислоты и диоксида марганца ( Brunsten ) была нагрета: «6) (A) På 1/2 UNS FINT RIFVEN BRUNSTEN SLOGES 1 UNS REN SURPICUS SALIS. (6) (а) На одну половину унции тонко молотого браунштейна [пиролузит] выливали одну унцию чистого спирта -салиса [дух соли, хлорид водорода]. После того, как эта смесь стояла на холоде в течение одного часа, кислота предположила темно -коричневый цвет. Одна часть этого раствора была вылита в стакан, который был помещен над огнем. Решение испускало запах, как теплый Aqua Regia , и через четверть часа он был таким же ясным и бесцветным, как вода, и запах исчез.) Для английского перевода соответствующих отрывков этой статьи см . (1774), CL Berthollet (1785), Guyton de Morveau (1787), JL Gay-Lussac и LJ Thenard (1809) (Эдинбург, Шотландия: Alembic Club, 1912), с. 5–10. Архивировано 2021-12-18 на машине Wayback
- ^ Jump up to: а беременный в дюймовый и "17 хлор" . Elements.vanderkrogt.net. Архивировано из оригинала 2010-01-23 . Получено 2008-09-12 .
- ^ Jump up to: а беременный в дюймовый Greenwood & Earnshaw 1997 , pp. 792–93
- ^ Ихде, Аарон Джон (1984). Развитие современной химии . Публикации курьера. п. 158. ISBN 978-0-486-64235-2 Полем Архивировано из оригинала в 2023-12-30 . Получено 2020-05-06 .
- ^ Недели, Мэри Эльвира (1932). «Открытие элементов. XVII. Семейство галогенов». Журнал химического образования . 9 (11): 1915. Bibcode : 1932JCHED ... 9.1915W . doi : 10.1021/ed009p1915 .
- ^ Гей-Луссак; Тогдард (1809). «Extrait des mémoires lus à l'Antitut National, Depuis le 7 Mars 1808 Jusqu'au 27 Février 1809» [Выдержки из мемуаров читаются в Национальном институте, с 7 марта 1808 года по 27 февраля 1809 года]. Mémoires de Physicique et de Chimie de la Société d'Arcueil . 2 : 295–358. Архивировано из оригинала 30 декабря 2023 года . Получено 24 февраля 2018 года . Видеть: § De la Nature et des Propriétés de l'cide muriatique et de l'acide muriatique oxigéné (о природе и свойствах соляной кислоты и окисленной соляной кислоты), с. 339–58. От стр. 357–58: «Le Gaz muriatique oxigéné n'est pas, en effect, décomposé… Comme un composé». («Фактически, оксигенированная соляная кислота не разлагается углями, и можно предположить, из этого факта и тех, которые сообщаются в этом мемуаре, что этот газ является простым телом. Явления, которые он представляет, могут быть достаточно хорошо объяснены достаточно хорошо Однако по этой гипотезе; Джозеф Луи Гей-Луссак и Луи Жак Тенард, «о природе и свойствах соляной кислоты и оксигенированной соляной кислоты» (Колледж Лемун, Сиракузы, Нью-Йорк) Архивировали 2008-07-25 на машине.
- ^ Дэви, Хамфри (1811). «Бейкерская лекция. О некоторых комбинациях оксимуриатического газа и оксигена, а также о химических отношениях этих принципов с целостными телами» . Философские транзакции Королевского общества Лондона . 101 : 1–35. Bibcode : 1811rspt..101 .... 1d . doi : 10.1098/rstl.1811.0001 . Архивировано из оригинала 2020-04-23 . Получено 2018-02-19 . Дэви назвал хлор на р. 32: Архивировано 2021-12-18 на The Wayback Machine «После консультации с некоторыми из самых выдающихся химических философов в этой стране было признано наиболее правильным, чтобы предложить название, основанное на одном из его очевидных и характерных свойств-его цвет Называть это хлором , или хлорным газом. * * из χλωρος. "
- ^ Schweigger, JSC (1811). «Напишите редактору, который относится к новой номенклатуре» [Postscript Редактора в отношении новой номенклатуры]. Журнал по химии и физике (на немецком языке). 3 (2): 249–55. Архивировано из оригинала 2020-04-23 . Получено 2018-02-19 . На р. »: «Вы предпочитаете сказать, что формирование слов с судьей 251, Швеигр предложил слово « галоген (поскольку в минералогии семейством Вернера это слово не является незнакомцем ) из αλς соль и старого γενειν (Дориш γενεν) свидетельствует ». (Вместо этого следует сказать, с правильной морфологией «галоген» (это слово не странно, поскольку [оно] уже в минералогии через «галитские» виды Вернера) из αλς [как] «соль» и старый γενειν [ген] γενεν)) «Чтобы породить».)
- ^ В 1826 году Берзелиус придумал термины Saltbildare (соленой формации) и Corpora Halogenia (солевые вещества) для элементов хлора, йода и фтора. Видеть: Берцелиус, Джейкоб (1826). «Годовые отчеты о прогрессе Physik и Chemie» [Годовой отчет о прогрессе в области физики и химии]. ARSB. Наука. Прогресс (на шведском языке). 6 Стокгольм, Швеция: PA NORSTEDT & Söner: 187. Архивировано из оригинала 2020-04-23 . Получено 2018-02-19 . . "De förre af dessa, d. ä. От р (Первые из них [т.е. элементы], то есть электроотрицательные [один], делятся на три класса: 1) Первые включают вещества, которые, когда] объединены с электропозитивными [элементами], немедленно производит соль -имя. -МИФРЕРЫ »(солевые вещества). Это хлор, йод и фтор *).).)
- ^ Снелдерс, Хэм (1971). «JSC Schweigger: его романтизм и его хрустальная электрическая теория материи». ИГИЛ . 62 (3): 328–38. doi : 10.1086/350763 . JSTOR 229946 . S2CID 170337569 .
- ^ Фарадей, М. (1823). «На жидкости хлор» . Философские транзакции Королевского общества Лондона . 113 : 160–64. Bibcode : 1823rspt..113..160f . doi : 10.1098/rstl.1823.0016 . Архивировано из оригинала 2020-04-23 . Получено 2018-02-19 .
- ^ Чодос, Алан (ред.). «В этом месяце в истории физики 4 сентября 1821 года и 29 августа 1831 года: Фарадея и электромагнетизм» . Американское физическое общество. Архивировано из оригинала 15 июня 2010 года . Получено 2010-05-08 .
- ^ О'Коннор JJ; Робертсон Эф "Майкл Фарадей" . Школа математики и статистики, Университет Сент -Эндрюс, Шотландия . Архивировано из оригинала 2010-02-20 . Получено 2010-05-08 .
- ^ Jump up to: а беременный «Отбеливание» . Encyclopædia Britannica (9 -е издание (1875) и 10 -е издание (1902) изд.). Архивировано из оригинала 2012-05-24 . Получено 2012-05-02 .
- ^ Аспин, Крис (1981). Хлопковая промышленность . Shire Publications Ltd. P. 24 ISBN 978-0-85263-545-2 .
- ^ Пол Мэй. «Отбеливатель (гипохлорит натрия)» . Университет Бристоля. Архивировано с оригинала 13 декабря 2016 года . Получено 13 декабря 2016 года .
- ^ Jump up to: а беременный в Greenwood & Earnshaw 1997 , p. 798
- ^ Almqvist, Ebbe (2003). История промышленных газов . Springer Science & Business Media. п. 220. ISBN 978-0-306-47277-0 Полем Архивировано из оригинала в 2023-12-30 . Получено 2020-10-09 .
- ^ Jump up to: а беременный Буве, Морис (1950). «Великие фармацевты: Лабаррак (1777-1850)» Журнал истории аптеки (на французском языке). 38 (128): 97–107. Два : 10 3406/ферма .
- ^ «Хлор - история» (PDF) . Архивировано из оригинала (PDF) 21 февраля 2007 года . Получено 2008-07-10 .
- ^ «Оружие: использование газовых цилиндров хлора в Первой мировой войне» . ИСТОРИЯНАЯ. 2006-06-12. Архивировано из оригинала 2008-07-02 . Получено 2008-07-10 .
- ^ Персонал (29 июля 2004 г.). «На Западном фронте, Ипрес 1915» . Ветеран по делам Канады. Архивировано из оригинала 6 декабря 2008 года . Получено 2008-04-08 .
- ^ Лефебур, Виктор; Уилсон, Генри (2004). Загадка Рейна: Химическая стратегия в мире и войне . Kessinger Publishing. ISBN 978-1-4179-3546-8 .
- ^ Jump up to: а беременный в дюймовый и фон глин час Greenwood & Earnshaw 1997 , pp. 800–804
- ^ Jump up to: а беременный в Greenwood & Earnshaw 1997 , pp. 804–809
- ^ Cameron, AGW (1973). «Обилие элементов в солнечной системе» (PDF) . Обзоры космических наук . 15 (1): 121–46. Bibcode : 1973ssrv ... 15..121c . doi : 10.1007/bf00172440 . S2CID 120201972 . Архивировано из оригинала (PDF) 2011-10-21.
- ^ Audi, Жорж; Берсильон, Оливье; Блахто, Джин; Wapstra, Aaldert Hendrik (2003), «Оценка n Ubase ядерных и распадных свойств» , Ядерная физика A , 729 : 3–128, Bibcode : 2003nupha.729 .... 3a , doi : 10.1016/j.nuclphysa.2003.11 .001
- ^ М. Зреда; и др. (1991). «Космогенные показатели производства хлора-36 в наземных породах». Земля и планетарные научные письма . 105 (1–3): 94–109. Bibcode : 1991e & psl.105 ... 94Z . doi : 10.1016/0012-821x (91) 90123-y .
- ^ М. Шеппард и М. Ирод (2012). «Изменение фоновых концентраций и конкретных активностей 36cl, 129i и u/Th-радионуклидов в поверхностных водах». Журнал экологической радиоактивности . 106 : 27–34. doi : 10.1016/j.jenvrad.2011.10.015 . PMID 22304997 .
- ^ Jump up to: а беременный в дюймовый Greenwood & Earnshaw 1997 , с. 853–856
- ^ Jump up to: а беременный в Greenwood & Earnshaw 1997 , pp. 809–812
- ^ Greenwood & Earnshaw 1997 , с. 812–816
- ^ Greenwood & Earnshaw 1997 , pp. 818–819
- ^ Jump up to: а беременный в Greenwood & Earnshaw 1997 , pp. 821–844
- ^ Greenwood & Earnshaw 1997 , pp. 842–844
- ^ Jump up to: а беременный в дюймовый Greenwood & Earnshaw 1997 , pp. 824–828
- ^ Greenwood & Earnshaw 1997 , pp. 835–842
- ^ «Очистка на месте камер сердечно -сосудистых заболеваний» . Полупроводник International . 1 июня 1999 года. [ Постоянная мертвая ссылка ]
- ^ Greenwood & Earnshaw 1997 , с. 828–831
- ^ Greenwood & Earnshaw 1997 , pp. 832–835
- ^ Greenwood & Earnshaw 1997 , с. 875–880
- ^ Jump up to: а беременный в дюймовый и фон глин час Greenwood & Earnshaw 1997 , pp. 844–850
- ^ Greenwood & Earnshaw 1997 , pp. 883–885
- ^ Jump up to: а беременный Greenwood & Earnshaw 1997 , pp. 856–870
- ^ Уилер, Ральф А.; Хоффманн, Роальд. (Октябрь 1986). «Новое магическое кластерное количество электронов и множественное соединение металла» . Журнал Американского химического общества . 108 (21): 6605–6610. doi : 10.1021/ja00281a025 . ISSN 0002-7863 . Архивировано из оригинала 2023-03-10 . Получено 2023-11-08 .
- ^ Чжан, Вейвей; Оганов, Артем Р.; Гончаров, Александр Ф.; Чжу, Цянь; Boulfelfel, Salah Eddine; Lyahhov, Andriy O.; Ставру, Элиссайос; Сомайазулу, Мэддури; Пракапенка, Витали Б.; Конопкова, Зузана (2013-12-20). «Неожиданная стабильная стехиометрия хлоридов натрия» . Наука . 342 (6165): 1502–1505. Arxiv : 1211.3644 . Bibcode : 2013sci ... 342.1502Z . doi : 10.1126/science.1244989 . ISSN 0036-8075 . PMID 24357316 . Архивировано из оригинала 2023-09-07 . Получено 2023-11-08 .
- ^ Jump up to: а беременный в M. Rossberg et al. «Хлорированные углеводороды» в энциклопедии Ульмана промышленной химии 2006 года, Wiley-VCH, Вайнхайм. два : 10.1002/14356007.a06_233.pub2
- ^ Jump up to: а беременный Гордон В. Гриббл (1998). «Природные органогалогенные соединения». Акк. Химический Резерв 31 (3): 141–52. doi : 10.1021/ar9701777 .
- ^ Гордон В. Гриббл (1999). «Разнообразие природных органических соединений органобромина». Обзоры химического общества . 28 (5): 335–46. doi : 10.1039/a900201d .
- ^ Кьелд С. Энгвильд (1986). «Хлорсодержащие натуральные соединения у более высоких растений». Фитохимия . 25 (4): 7891–91. Bibcode : 1986pchem..25..781e . doi : 10.1016/0031-9422 (86) 80002-4 .
- ^ Gribble, GW (1994). «Естественное производство хлорированных соединений». Экологическая наука и техника . 28 (7): 310a - 319a. Bibcode : 1994enst ... 28..310G . doi : 10.1021/es00056a712 . PMID 22662801 .
- ^ Gribble, GW (1996). «Природные органогалогенные соединения - всеобъемлющее обследование». Прогресс в химии органических натуральных продуктов . 68 (10): 1–423. doi : 10.1021/np50088a001 . PMID 8795309 .
- ^ Заявление общественного здравоохранения-Хлорметан Архивировал 2007-09-27 на машине Wayback , Центры по борьбе с заболеваниями , Агентство по токсичным веществам и регистрации заболеваний
- ^ Коннелл, Д.; и др. (1999). Введение в экотоксикологию . Blackwell Science. п. 68. ISBN 978-0-632-03852-7 .
- ^ Эксперты, Арихант (2020-11-01). Общее сестринское и акушерское вступительное экзамен 2021 . Arihant Publications India Limited. ISBN 978-93-252-9132-4 .
- ^ Greenwood & Earnshaw 1997 , p. 795
- ^ Холмен, Арнольд Фредерик; Wiberg, Egon (2001), Wiberg, Nils (ed.), Неорганическая химия , переведенная Иглсоном, Мэри; Брюер, Уильям, Сан -Диего/Берлин: Академическая Пресса/Де Грюйтер, с. 408, ISBN 0-12-352651-5
- ^ «Производство хлора» . Институт хлора . Получено 2024-05-11 .
- ^ «О виниле: хлор» . Виниловый совет Австралия . Получено 2024-05-11 .
- ^ Jump up to: а беременный в Greenwood & Earnshaw 1997 , pp. 796–800
- ^ "Хлор" . Westlake Chemical.
- ^ "Хлор-Алкали" . Формоза пластмассы . Получено 2024-05-11 .
- ^ Pauling, Linus, General Chemistry , 1970 Ed., Dover Publications
- ^ «Электролитические процессы для хлора и каустической соды» . Очистка воды Lenntech и очистка воздуха BV, Rotterdamseweg 402 M, 2629 HH Delft, Нидерланды . Получено 2007-03-17 .
- ^ «Процесс ячейки диафрагма» . Евро Хлор. Архивировано из оригинала 2011-11-11 . Получено 2007-08-15 .
- ^ «Процесс мембранной ячейки» . Евро Хлор. Архивировано из оригинала 2011-11-11 . Получено 2007-08-15 .
- ^ Schmittinger, Peter et al. (2006) «Хлор» в энциклопедии промышленной химии Уллмана , Wiley-VCH Verlag Gmbh & Co., Два : 10.1002/14356007.a06_399.pub2
- ^ Бошам, Кэтрин С. (август 2023 г.). «Оценка потенциальных воздействий инспекторов по опасным материалам железной дороги» (PDF) . Национальный институт безопасности и здоровья США ( отчет об оценке опасности для здоровья ) . Получено 2024-05-04 .
- ^ Greenwood & Earnshaw 1997 , p. 798.
- ^ Greenwood & Earnshaw 1997 , p. 793.
- ^ Jump up to: а беременный Hoefer, Жан Кретиен Фердинанд (ред.). «Лабаррак, Антуан-Жермен». Nouvelle Biographie Universelle . Том. 323–24. OL 24229911M .
- ^ Jump up to: а беременный Рыцарь, Чарльз (1867). Искусство и науки . Тол. 1. Брэдбери, Эванс и Ко р. 427.
- ^ Ежегодный, Андрас (2006). Наука и техника в медицине . Пружины. стр. 181-82. ISBN 978-0-387-27874-2 Полем Архивировано из оригинала 2015-12-31.
- ^ Лабаррак, Антуан Жермен (1828). О дезинфекции свойств препаратов Лабаррака хлора . Перевод Джеймса Скотта. п. 8. Архивировано из оригинала 2015-12-31.
- ^ Скотт, Джеймс (транс.). О дезинфекции свойств препаратов Лабаррака архивировали хлор 2015-12-31 в The Wayback Machine (S. Highley, 1828), доступ к 1 ноября 2011 года.
- ^ Корбин, Ален (1988). Фол и ароматный: запах и французское социальное воображение архивировали 2015-12-31 на машине Wayback . Гарвардский университет издательство. С. 121–22.
- ^ Льюис, Кеннет А. (2010). «Гл. 9 Гипохлорирование - гипохлорит натрия» (PDF) . Справочник Уайта о хлорировании и альтернативных дезинфицирующих средствах . Хобокен, Нью -Джерси: Уайли. п. 452. DOI : 10.1002/9780470561331.CH9 . ISBN 978-0-470-56133-1 Полем Архивировано (PDF) из оригинала на 2022-10-09. [ Постоянная мертвая ссылка ]
- ^ Jump up to: а беременный Винтен-Джохансен, Питер, Говард Броди, Найджел Панет, Стивен Рахман и Майкл Рип. (2003). Холера, хлороформ и наука о медицине . Нью -Йорк: Оксфордский университет.
- ^ Хемфилл, Сандра. (2007). Странный случай насоса Брод -стрит: Джон Сноу и тайна холеры . Лос -Анджелес: Калифорнийский университет
- ^ Джонсон, Стивен . (2006). Карта призраков: история самой ужасной эпидемии Лондона и того, как она изменила науку, города и современный мир . Нью -Йорк: Riverhead Books
- ^ «История хлора» . Americanchemistry. Архивировано из оригинала 2011-04-29 . Получено 2008-07-10 .
{{cite web}}: CS1 Maint: Bot: исходный статус URL неизвестен ( ссылка ) - ^ Rezayat, C.; Widmann, WD; Харди, М.А. (2006). «Генри Дрисдейл Дакин: больше, чем его решение». Текущая операция . 63 (3): 194–96. doi : 10.1016/j.cursur.2006.04.009 . PMID 16757372 .
- ^ Джозеф Котон, Виктор Кимм, Арден Калверт. «Питьевая вода: полвека прогресса». Архивировано 2020-07-31 в Ассоциации выпускников EPA Wayback Machine . 1 марта 2016 года.
- ^ Хаммонд, Кр (2000). Элементы, в Справочнике по химии и физике (81 -е изд.). CRC Press. ISBN 978-0-8493-0481-1 .
- ^ «Хлорамины и работа в бассейне» . Центры для контроля и профилактики заболеваний. Архивировано из оригинала 13 марта 2022 года . Получено 13 марта 2022 года .
- ^ Коски Та; Стюарт Л.С.; Ортенцио Л.Ф. (1966). «Сравнение хлора, брома, йода в качестве дезинфицирующих средств для воды для бассейна» . Прикладная микробиология . 14 (2): 276–79. doi : 10.1128/aem.14.2.276-279.1966 . PMC 546668 . PMID 4959984 .
- ^ «Дезинфекция с хлорамином» . Центры для контроля и профилактики заболеваний (CDC) . Атланта, Джорджия. Архивировано с оригинала 2015-02-15 . Получено 2019-01-20 .
- ^ Greenwood & Earnshaw 1997 , p. 860.
- ^ Холмен, Арнольд Фредерик; Wiberg, Egon (2001), Wiberg, Nils (ed.), Неорганическая химия , переведенная Иглсоном, Мэри; Брюер, Уильям, Сан -Диего/Берлин: Академическая Пресса/Де Грюйтер, с. 411, ISBN 0-12-352651-5
- ^ "Битва при Ипрес" Канадская энциклопедия
- ^ Эвертс, Сара (23 февраля 2015 г.). «Когда химические вещества стали оружием войны» . Химические и инженерные новости . 93 (8). Архивировано с оригинала 30 марта 2016 года.
- ^ Паттон, Джеймс. «Газ в Великой войне» . Медицинский центр KU . Архивировано из оригинала 15 июня 2024 года . Получено 2024-06-21 .
- ^ Smil, Vaclav (2000). Обогащение земли: Фриц Хабер, Карл Бош и трансформация мировой продукции питания . MIT Press. п. 226. ISBN 978-0-262-69313-4 Полем Архивировано из оригинала 2015-12-31.
- ^ «Оружие войны: ядовитый газ» . Первая мировая война.com. Архивировано из оригинала на 2007-08-21 . Получено 2007-08-12 .
- ^ Махди, Базим (2007-03-17). «Иракский газовый атак увлекает сотни» . CNN. Архивировано из оригинала 2007-03-17 . Получено 2007-03-17 .
- ^ « Хлорная бомба» попадает в деревню в Ираке » . BBC News . 2007-05-17. Архивировано из оригинала 2007-05-26 . Получено 2007-05-17 .
- ^ Моррис, Lovalay (2014-10-23). «Боевики Исламского государства якобы использовали газ хлора против иракских сил безопасности» . The Washington Post . Архивировано из оригинала 2021-12-19 . Получено 2021-06-08 .
- ^ «Лабораторный отчет об использовании газа хлора» (PDF) . Курдистан Регион Совет безопасности. 14 марта 2015 года. Архивировал (PDF) с оригинала 30 декабря 2023 года . Получено 24 марта 2015 года .
- ^ Гладстон, Рик (2017-02-13). «Сирия систематически использовала хлорные бомбы в Алеппо, говорится в сообщении» . New York Times . Архивировано с оригинала 2017-05-15 . Получено 2017-05-10 .
- ^ «Сирийские силы« падают хлор »на Алеппо» . BBC News . 2016-09-07. Архивировано из оригинала 2017-05-13 . Получено 2017-05-10 .
- ^ «Игнорирование ООН, России и Асада продолжают сирийское химическое оружие и бомбардировки, названные военные преступления» . Fox News . 2017-03-06. Архивировано с оригинала 2017-04-25 . Получено 2017-05-11 .
- ^ «График исследований в области химического оружия Сирии», архивировав 2021-12-18 на машине Wayback . Рейтер. 9 апреля 2018 года.
- ^ «Сирийские ВВС за атакой хлора 2018 года на Саракеб, OPCW находит», архивировав 2021-12-18 в The Wayback Machine BBC News. 12 апреля 2021 года.
- ^ «Тест на уровень хлорида крови (сыворотка)» . Архивировано из оригинала 31 марта 2009 года . Получено 30 апреля 2010 года .
- ^ Лави, CJ; Крокер, EF; Ключ, KJ; Фергюсон, Т.Г. (октябрь 1986 г.). «Отмеченный гипохлоремический метаболический алкалоз с тяжелой компенсаторной гиповентиляцией». Юг. Медик Дж . 79 (10): 1296–99. doi : 10.1097/00007611-198610000-00025 . PMID 3764530 .
- ^ Левитин, ч; Branscome, w; Эпштейн, FH (декабрь 1958 г.). «Патогенез гипохлоремии при респираторном ацидозе» . J. Clin. Инвестировать 37 (12): 1667–75. doi : 10.1172/jci103758 . PMC 1062852 . PMID 13611033 .
- ^ Cambier, c; Detry, B; Beerens, D; и др. (Октябрь 1998). «Влияние гиперхлоремии на связывание кислорода в крови у здоровых телят». J. Appl. Физиол . 85 (4): 1267–72. doi : 10.1152/jappl.1998.85.4.1267 . PMID 9760315 .
- ^ «Хлор 295132» . Сигма-Альдрич. 2021-07-29. Архивировано из оригинала 2020-05-10 . Получено 2021-12-22 .
- ^ "MSDS - 295132" . Архивировано из оригинала 2021-04-27 . Получено 2018-10-03 .
- ^ «Факты о хлоре» . www.bt.cdc.gov . Архивировано с оригинала 2016-04-23 . Получено 2016-04-12 .
{{cite web}}: CS1 Maint: Bot: исходный статус URL неизвестен ( ссылка ) - ^ «Хлор MSDS» (PDF) . 1997-10-23. Архивировано из оригинала (PDF) на 2007-09-26.
- ^ Офис ответа и восстановления NOAA, Gov. "Хлор" . NOAA.gov . Архивировано с оригинала 15 октября 2015 года . Получено 25 августа 2015 года .
- ^ Jump up to: а беременный Niosh Pocket Guide к химическим опасностям. "#0115" . Национальный институт безопасности и гигиены труда (NIOSH).
- ^ Уиндер, Крис (2001). «Токсикология хлора». Экологические исследования . 85 (2): 105–14. Bibcode : 2001er ..... 85..105W . doi : 10.1006/regs2000.4110 . PMID 11161660 .
- ^ «Что у вас в воде?: Дезинфицирующие средства создают токсичные побочные продукты» . Тузы новости . Колледж сельского хозяйства, потребительских и экологических наук-Университет Иллинойса в Урбана-Шампейн. 2009-03-31. Архивировано из оригинала 2014-09-03 . Получено 2009-03-31 .
- ^ Ричардсон, Сьюзен Д.; Плева, Майкл Дж.; Вагнер, Элизабет Д.; Schoeny, Rita; Демарини, Дэвид М. (2007). «Возникновение, генотоксичность и канцерогенность регулируемых и возникающих дезинфекционных побочных продуктов в питьевой воде: обзор и дорожная карта для исследований». Исследование мутаций/обзоры в исследованиях мутаций . 636 (1–3): 178–242. Bibcode : 2007mrrmr.636..178r . doi : 10.1016/j.mrrev.2007.09.001 . PMID 17980649 .
- ^ Березов, Алекс. «Почему вы никогда не должны смешивать разные уборщики дренажа» . Форбс . Архивировано с оригинала 2016-04-25 . Получено 2016-04-12 .
- ^ «Опасности отбеливания: Департамент здоровья штата Вашингтон» . www.doh.wa.gov . Архивировано с оригинала 2016-04-14 . Получено 2016-04-12 .
- ^ Бертолини, Лука; Элсенер, Бернхард; Pedeferri, Pietro; Полдер, Роб Б. (2004). Коррозия стали в бетоне: профилактика, диагностика, восстановление . Wiley-Vch. п. 148. ISBN 978-3-527-30800-2 Полем Архивировано из оригинала в 2023-12-30 . Получено 2020-05-06 .
- ^ Льюис, PR (1 января 2000 г.). Полимерный сбой продукта Ismithers Rapra Publishing. Стр. 19–. ISBN 978-1-85957-192-7 Полем Архивировано из оригинала 10 мая 2013 года . Получено 2011-04-30 .
- ^ Jump up to: а беременный «Хлор: таблица данных продукта» (PDF) . Bayer MaterialScience Ag. 2008-04-21. Архивировано из оригинала (PDF) 15 сентября 2012 года . Получено 2013-12-17 .
- ^ Jump up to: а беременный Сандерс, Рой Э. (2004). Химическая безопасность процессов: обучение на истории случаев, 3 -е пересмотренное издание . Оксфорд: Elsevier Science & Technology. п. 92. ISBN 978-0-7506-7749-3 .
Библиография
- Гринвуд, Норман Н .; Эрншоу, Алан (1997). Химия элементов (2 -е изд.). Баттерворт-Хейнеманн . ISBN 978-0-08-037941-8 .
Внешние ссылки
- Хлор за периодической таблицей видео (Университет Ноттингема)
- Агентство по реестру токсичных веществ и заболеваний : хлор
- Электролитическое производство
- Производство и разжижение хлора
- Производство хлора с использованием ртути, экологических соображений и альтернатив
- Национальный инвентарь загрязняющих веществ - хлор
- Национальный институт безопасности и гигиены труда - страница хлора
- Институт Хлора Архивировал 2012-08-27 в The Wayback Machine -Торговая ассоциация, представляющая хлорную промышленность
- Chlorine Online -веб-портал Еврохлора-бизнес-ассоциация европейской индустрии хлор-алкали


