Уильямсон Эфир Синтез
| Уильямсон Эфир Синтез | |
|---|---|
| Назван в честь | Александр Уильям Уильямсон |
| Тип реакции | Реакция связи |
| Идентификаторы | |
| Органическая химическая портал | Уильямсон-синтез |
| RSC Ontology Id | RXNO: 0000090 |

Синтез эфира Уильямсона является органической реакцией , образующей эфир из органохалида и депротонированного спирта ( алкоксид ). Эта реакция была разработана Александром Уильямсоном в 1850 году. [ 2 ] Как правило, он включает реакцию алкоксидного иона с первичным алкилгалогенидом через реакцию S N 2 . Эта реакция важна в истории органической химии, потому что она помогла доказать структуру эфиров .
Общий механизм реакции заключается в следующем: [ 3 ]
Примером является реакция оксида натрия с хлорэтаном с образованием диэтилового эфира и хлорида натрия:
Механизм
[ редактировать ]Эфирная реакция Уильямсона следует механизму S N 2 (бимолекулярная нуклеофильная замена). В механизме реакции S N 2 есть задняя атака электрофила нуклеофилом, и он происходит в согласованном механизме (случается все сразу). Для того, чтобы реакция S N 2 имела место, должна быть хорошая уходная группа , которая сильно электроотрицательная, обычно галогенид. [ 4 ]
В эфирной реакции Уильямсона есть ион алкоксида (RO − ), который действует как нуклеофил, атаковая электрофильный углерод с помощью уходной группы, которая в большинстве случаев представляет собой алкилтозилат или алкилгалогенид. Уходящий участок должен быть первичным углеродом, потому что вторичные и третичные оставляющие участки обычно предпочитают действовать в качестве реакции элиминации . Кроме того, эта реакция не способствует образованию громоздких эфиров, таких как ди-тертбутиловый эфир, из-за стерического препятствия и преобладающего образования алкенов. [ 5 ]

Объем
[ редактировать ]Реакция Уильямсона имеет широкий охват, широко используется как в лабораторном, так и в промышленном синтезе и остается самым простым и самым популярным методом подготовки эфиров. Как симметричные, так и асимметричные эфиры легко подготовлены. внутримолекулярная реакция галогидринов В частности, дает эпоксиды .
В случае асимметричных эфиров есть две возможности для выбора реагентов, и одна из них является предпочтительностью либо на основе доступности, либо на реактивность. Реакция Уильямсона также часто используется для косвенного подготовки эфира от двух спиртов. Один из спиртов сначала преобразуется в уходную группу (обычно тозилат ), затем оба реагируют вместе.
Алкоксид (или арилоксид ) может быть первичным и вторичным. Третичные алкоксиды имеют тенденцию давать реакцию элиминации из -за стерического помеха. Алкилирующий агент, с другой стороны, наиболее предпочтительно первичный. Вторичные алкилирующие агенты также реагируют, но третичные, как правило, слишком склонны к боковым реакциям, чтобы они практические использования. Уходящая группа чаще всего представляет собой галогенид или сульфонатный сложный эфир, синтезированный с целью реакции. Поскольку условия реакции довольно навязывают, защитные группы часто используются для умиротворения других частей реагирующих молекул (например, другие спирты , амины и т. Д.)
Синтез эфира Уильямсона является распространенной органической реакцией в промышленном синтезе и в учебных лабораториях бакалавриата. Выходы для этих эфирных синтезов традиционно низки, когда время реакции сокращается, что может иметь место с периодами лабораторных классов бакалавриата. Не допустив, чтобы реакции в рефлюкс в течение правильного количества времени (где -то от 1 до 8 часов от 50 до 100 ° C) реакция может не перейти к завершению, генерируя плохую общую урожайность продукта. Чтобы помочь смягчить эту проблему, микроволновую технологию в настоящее время используется для ускорения времени реакции на такие реакции, как синтез эфира Уильямсона. Эта технология преобразовала время реакции, которое требовало рефлюкса не менее 1,5 часа до быстрого 10-минутного микроволнового прогона при 130 ° C, и это увеличило выход эфира, синтезированного из диапазона от 6 до 29% до 20-55% (данные был составлен из нескольких различных лабораторных секций, включающих технологию в их синтезах). [ 6 ]
Также были значительные шаги в синтезе эфиров при использовании температур 300 ° C и вверх и использовали более слабые алкилирующие агенты для облегчения более эффективного синтеза. Эта методология помогает упростить процесс синтеза и делает синтез в промышленном масштабе более осуществимым. Гораздо более высокая температура делает слабый алкилирующий агент более реактивным и менее склонна производить соли в качестве побочного продукта. Этот метод оказался очень селективным и особенно полезным в производстве ароматических эфиров, таких как анизол, который увеличивает промышленное применение. [ 7 ]
Условия
[ редактировать ]Поскольку ионы алкоксида очень реактивны, они обычно готовится непосредственно перед реакциями или генерируются in situ . В лабораторной химии, генерация in situ чаще всего осуществляется путем использования карбонатного основания или гидроксида калия , в то время как в промышленных синтезах фазового катализа очень распространен. Можно использовать широкий диапазон растворителей, но протоки растворителей и аполярных растворителей имеют тенденцию сильно замедлять скорость реакции в результате снижения доступности свободного нуклеофила. По этой причине ацетонитрил и N , N -диметилформамид особенно часто используются .
Типичная реакция Уильямсона проводится при 50-100 ° C и завершена через 1-8 часов. Часто трудно достичь полного исчезновения начального материала, и боковые реакции распространены. Выходы 50–95% обычно достигаются в лабораторных синтезах, в то время как почти квалифицированное преобразование может быть достигнуто в промышленных процедурах.
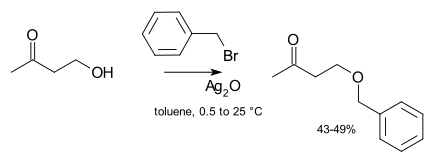
Катализ обычно не необходим в лабораторных синтезах. Однако, если используется нереактивный алкилирующий агент (например, алкилхлорид), то скорость реакции может быть значительно улучшена за счет добавления каталитического количества растворимой йодидной соли (которая подвергается обмену галогенидом с хлоридом, чтобы получить гораздо больший реактивный йодид, вариант реакции Финкельштейна ). В крайних случаях соединения серебра, такие как оксид серебра : могут быть добавлены [ 8 ]
Серебряный ион координирует с группой по уходу за галогенидом, чтобы сделать его отъезд более легким. Наконец, иногда используются катализаторы переноса фазы (например, бромид тетрабутиламмония или 18-краун-6 ), чтобы увеличить растворимость алкоксида, предлагая более мягкий противодействие . Еще одним примером реакции этерификации в трехфазической системе в каталитических условиях переноса фазы является реакция бензилхлорида и спирта-фурфурила . [ 9 ]
Боковые реакции
[ редактировать ]Реакция Уильямсона часто конкурирует с катализируемой базой устранением алкилирующего агента, [ 3 ] и природа уходной группы, а также условия реакции (особенно температура и растворитель) могут оказывать сильное влияние на то, что предпочитают. В частности, некоторые структуры алкилирующего агента могут быть особенно склонны к устранению.
Когда нуклеофил является ионом арилоксида, реакция Уильямсона также может конкурировать с алкилированием на кольце, поскольку арилоксид является нуклеофилом амбидентов .
Смотрите также
[ редактировать ]- Ullmann Condensation для формирования бис-арийских эфиров
- Диметилсульфат и диэтилсульфат , относительно недорогие органосульфаты, используемые в методах альтернативного синтеза эфира
Ссылки
[ редактировать ]- ^ Burgstahler, Albert W.; Уорден, Леонард Р. (1966). "Кумарон" . Органические синтезы . 46 : 28. doi : 10.15227/orgsyn.046.0028 ; Собранные объемы , вып. 5, с. 251 .
- ^ Уильямсон, Александр (1850). «Теория этерификации» . Философский журнал . 37 (251): 350–356. doi : 10.1080/14786445008646627 . ( Ссылка на выдержку. )
- ^ Jump up to: а беременный Бойд, Роберт Нейлсон; Моррисон, Роберт Торнтон (1992). Органическая химия (6 -е изд.). Englewood Cliffs, NJ: Prentice Hall . С. 241–242. ISBN 9780136436690 .
- ^ Уэйд, Леруа (2017). Органическая химия . Пирсон. С. 261–274. ISBN 9780321971371 .
- ^ Уэйд, Леруа (2017). Органическая химия . Пирсон. С. 682–683. ISBN 9780321971371 .
- ^ Баар, Марша Р.; Falcone, Даниэль; Гордон, Кристофер (2010). «Микроволновые органические синтезы для бакалавриата Лаборатории: циклическая циклу Diels-Alder, реакция Wittig и синтез Williamson Ether». Журнал химического образования . 87 (1): 84–86. Bibcode : 2010jched..87 ... 84b . doi : 10.1021/ed800001x .
- ^ Фурманн, Эдгар; Talbiersky, Jörg (2005). «Синтез алкил -ариловых эфиров каталитическим синтезом эфира Уильямсона со слабыми алкилирующими агентами». Органические процессы исследования и разработки . 9 (2): 206–211. doi : 10.1021/op050001h .
- ^ Танабе, Масато ; Петерс, Ричард Х. (1981). "( R , s ) -Mevalonolactone-2- 13 С (2 ч -пиран-2-о- 13 C, тетрагидро-4-гидрокси-4-метил-) " . Органические синтезы . 60 : 92. doi : 10.15227/orgsyn.060.0092 ; Собранные объемы , вып. 7, с. 386 .
- ^ Katole do, Yadav Gd. Процесс интенсификация и минимизация отходов с использованием жидкожидного жидкости трипхаза Катализ переноса для синтеза 2-(бензилокси) метила) фурана. Молекулярный катализ 2019; 466: 112–21. https://doi.org/10.1016/j.mcat.2019.01.004