Расстройство, связанное с употреблением опиоидов
| Расстройство, связанное с употреблением опиоидов | |
|---|---|
| Другие имена | Опиоидная зависимость, [ 1 ] проблемное употребление опиоидов, [ 1 ] злоупотребление опиоидами, [ 2 ] опиоидная зависимость [ 3 ] |
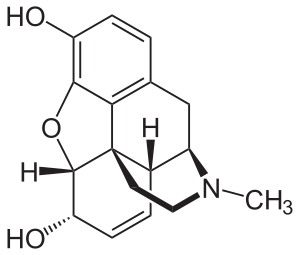 | |
| Молекулярная структура морфина | |
| Специальность | Наркология , психиатрия |
| Симптомы | Сильное желание употреблять опиоиды, повышенная толерантность к опиоидам, невыполнение обязательств, проблемы с сокращением употребления, синдром отмены с прекращением приема. [ 4 ] [ 5 ] |
| Осложнения | Передозировка опиоидов , гепатит С , проблемы брака, безработица, бедность [ 4 ] [ 5 ] |
| Продолжительность | Долгосрочная перспектива [ 6 ] |
| Причины | Опиоиды [ 3 ] |
| Метод диагностики | На основе критериев DSM-5 [ 4 ] |
| Дифференциальный диагноз | Алкоголизм |
| Уход | Заместительная опиоидная терапия , поведенческая терапия , программы двенадцати шагов , налоксон на дому. [ 7 ] [ 8 ] [ 9 ] |
| Медикамент | Бупренорфин , метадон , налтрексон [ 7 ] [ 10 ] |
| Частота | 16 миллионов [ 11 ] |
| Летальные исходы | 120,000 [ 11 ] |
Расстройство, связанное с употреблением опиоидов ( OUD ), — это расстройство, связанное с употреблением психоактивных веществ , характеризующееся тягой к опиоидам , продолжающимся употреблением, несмотря на физическое и/или психологическое ухудшение, повышением толерантности при употреблении и симптомами отмены после прекращения приема опиоидов. [ 12 ] Симптомы отмены опиоидов включают тошноту, мышечные боли, диарею, проблемы со сном, возбуждение и плохое настроение. [ 5 ] Пристрастие и зависимость являются важными компонентами расстройств, связанных с употреблением опиоидов. [ 13 ]
Факторы риска включают в себя историю злоупотребления опиоидами, текущее злоупотребление опиоидами, молодой возраст, социально-экономический статус, расу, нелеченные психические расстройства и среду, способствующую злоупотреблению (социальную, семейную, профессиональную и т. д.). [ 14 ] [ 15 ] Осложнения могут включать передозировку опиоидов , самоубийство , ВИЧ/СПИД , гепатит С и проблемы с выполнением социальных или профессиональных обязанностей. [ 5 ] [ 4 ] Диагноз может быть основан на критериях Американской психиатрической ассоциации в DSM-5 . [ 4 ]
К опиоидам относятся такие вещества, как героин , морфин , фентанил , кодеин , дигидрокодеин , оксикодон и гидрокодон . [ 5 ] [ 6 ] Полезным стандартом относительной силы различных опиоидов является миллиграммовый эквивалент морфина (ММЕ). [ 16 ] Врачам рекомендуется обращаться к ежедневным MME при назначении опиоидов, чтобы снизить риск неправильного использования и побочных эффектов. [ 17 ]
Длительное употребление опиоидов встречается примерно у 4% людей после их употребления из-за боли, связанной с травмой или хирургическим вмешательством. [ 18 ] В Соединенных Штатах большинство потребителей героина начинают с употребления опиоидов, отпускаемых по рецепту, которые также можно купить нелегально. [ 19 ] [ 20 ]
Людей с расстройством, связанным с употреблением опиоидов, часто лечат заместительной опиоидной терапией с использованием метадона или бупренорфина . [ 21 ] Такое лечение снижает риск смерти. [ 21 ] Кроме того, им может быть полезна когнитивно-поведенческая терапия , другие формы поддержки со стороны специалистов в области психического здоровья, такие как индивидуальная или групповая терапия, программы двенадцати шагов и другие программы поддержки со стороны сверстников. [ 22 ] Лекарство налтрексон также может быть полезно для предотвращения рецидива. [ 10 ] [ 8 ] Налоксон полезен при лечении передозировки опиоидами , а людям из группы риска полезно давать налоксон на дом. [ 23 ] По оценкам CDC, в 2020 году около 3 миллионов человек в США жили с ОУД и более 65 000 человек умерли от передозировки опиоидов, из которых более 15 000 были передозировкой героина. [ 24 ] [ 25 ]
Диагностика
[ редактировать ]Рекомендации DSM -5 по диагностике расстройств, связанных с употреблением опиоидов, требуют, чтобы у человека наблюдались значительные нарушения или дистресс, связанные с употреблением опиоидов. [ 4 ] Для постановки диагноза в течение года должны присутствовать два или более из 11 критериев: [ 4 ]
- Принимается больше опиоидов, чем предполагалось
- Человек не может уменьшить количество используемых опиоидов.
- Большое количество времени тратится на попытки получить опиоиды, использовать опиоиды или восстановиться после их приема.
- У человека возникает тяга к опиоидам
- Трудности с выполнением профессиональных обязанностей на работе или учебе.
- Продолжающееся употребление опиоидов приводит к социальным и межличностным последствиям
- Снижение социальной или развлекательной активности.
- Употребление опиоидов, несмотря на нахождение в физически опасных условиях
- Продолжение употребления, несмотря на то, что опиоиды ухудшают физическое или психологическое здоровье (например, депрессия, запор)
- Толерантность
- Снятие
Тяжесть можно классифицировать как легкую, среднюю или тяжелую в зависимости от количества присутствующих критериев. [ 6 ] Критерии толерантности и отмены не считаются соблюденными для лиц, принимающих опиоиды исключительно под соответствующим медицинским наблюдением. [ 4 ] Пристрастие и зависимость являются компонентами расстройства, вызванного употреблением психоактивных веществ ; зависимость – более тяжелая форма. [ 13 ]
Признаки и симптомы
[ редактировать ]Opioid intoxication
[ редактировать ]Signs and symptoms of opioid intoxication include:[5][26]
- Decreased perception of pain
- Euphoria
- Confusion
- Desire to sleep
- Nausea
- Constipation
- Miosis (pupil constriction)
- Bradycardia (slow heart rate)
- Hypotension (low blood pressure)
- Hypokinesis (slowed movement)
- Head nodding
- Slurred speech
- Hypothermia (low body temperature)
Opioid overdose
[edit]
Signs and symptoms of opioid overdose include, but are not limited to:[28]
- Pin-point pupils may occur. Patient presenting with dilated pupils may still be experiencing an opioid overdose.
- Decreased heart rate
- Decreased body temperature
- Decreased breathing
- Altered level of consciousness. People may be unresponsive or unconscious.
- Pulmonary edema (fluid accumulation in the lungs)
- Shock
- Death

Withdrawal
[edit]Opioid withdrawal can occur with a sudden decrease in, or cessation of, opioids after prolonged use.[29][30][31] Onset of withdrawal depends on the half-life of the opioid that was used last.[32] With heroin this typically occurs five hours after use; with methadone, it may take two days.[32] The length of time that major symptoms occur also depends on the opioid used.[32] For heroin withdrawal, symptoms are typically greatest at two to four days and can last up to two weeks.[33][32] Less significant symptoms may remain for an even longer period, in which case the withdrawal is known as post-acute-withdrawal syndrome.[32]
- Agitation[4]
- Anxiety[4]
- Muscle pains[4]
- Increased tearing[4]
- Trouble sleeping[4]
- Runny nose[4]
- Sweating[4]
- Yawning[4]
- Goose bumps[4]
- Dilated pupils[4]
- Diarrhea[4]
- Fast heart rate[32]
- High blood pressure[32]
- Abdominal cramps[32]
- Shakiness[32]
- Cravings[32]
- Sneezing[32]
- Bone pain
- Increased body temperature
- Hyperalgesia
- Ptosis (drooping eyelids)
- Teeth chattering
- Emotional pain
- Stress
- Weakness
- Malaise
- Alexithymia
- Dysphoria
Treatment of withdrawal may include methadone and buprenorphine. Medications for nausea or diarrhea may also be used.[30]
Cause
[edit]Opioid use disorder can develop as a result of self-medication.[34] Scoring systems have been derived to assess the likelihood of opiate addiction in chronic pain patients.[35] Healthcare practitioners have long been aware that despite the effective use of opioids for managing pain, empirical evidence supporting long-term opioid use is minimal.[36][37][38][39][40] Many studies of patients with chronic pain have failed to show any sustained improvement in their pain or ability to function with long-term opioid use.[37][41][42][43][40]
According to position papers on the treatment of opioid dependence published by the United Nations Office on Drugs and Crime and the World Health Organization, care providers should not treat opioid use disorder as the result of a weak moral character or will but as a medical condition.[15][44][45] Some evidence suggests the possibility that opioid use disorders occur due to genetic or other chemical mechanisms that may be difficult to identify or change, such as dysregulation of brain circuitry involving reward and volition. But the exact mechanisms involved are unclear, leading to debate over the influence of biology and free will.[46][47]
Mechanism
[edit]Addiction
[edit]Addiction is a brain disorder characterized by compulsive drug use despite adverse consequences.[13][48][49][50] Addiction involves the overstimulation of the brain's mesocorticolimbic reward circuit (reward system), essential for motivating behaviors linked to survival and reproductive fitness, like seeking food and sex.[51] This reward system encourages associative learning and goal-directed behavior. In addiction, substances overactivate this circuit, causing compulsive behavior due to changes in brain synapses.[52]
The incentive-sensitization theory differentiates between "wanting" (driven by dopamine in the reward circuit) and "liking" (related to brain pleasure centers).[53] This explains the addictive potential of non-pleasurable substances and the persistence of opioid addiction despite tolerance to their euphoric effects. Addiction surpasses mere avoidance of withdrawal, involving cues and stress that reactivate reward-driven behaviors.[51] This is an important reason detoxification alone is unsuccessful 90% of the time.[54][55][56]

Overexpression of the gene transcription factor ΔFosB in the nucleus accumbens plays a crucial role in the development of an addiction to opioids and other addictive drugs by sensitizing drug reward and amplifying compulsive drug-seeking behavior.[48][57][58][59] Like other addictive drugs, overuse of opioids leads to increased ΔFosB expression in the nucleus accumbens.[57][58][59][60] Opioids affect dopamine neurotransmission in the nucleus accumbens via the disinhibition of dopaminergic pathways as a result of inhibiting the GABA-based projections to the ventral tegmental area (VTA) from the rostromedial tegmental nucleus (RMTg), which negatively modulate dopamine neurotransmission.[61][62] In other words, opioids inhibit the projections from the RMTg to the VTA, which in turn disinhibits the dopaminergic pathways that project from the VTA to the nucleus accumbens and elsewhere in the brain.[61][62]
The differences in the genetic regions encoding the dopamine receptors for each individual may help to elucidate part of the risk for opioid addiction and general substance abuse.[10] Studies of the D2 Dopamine Receptor, in particular, have shown some promising results. One specific SNP is at the TaqI RFLP (rs1800497). In a study of 530 Han Chinese heroin-addicted individuals from a Methadone Maintenance Treatment Program, those with the specific genetic variation showed higher mean heroin consumption by around double those without the SNP.[63] This study helps to show the contribution of dopamine receptors to substance addiction and more specifically to opioid abuse.[63]
Neuroimaging has shown functional and structural alterations in the brain.[64] Chronic intake of opioids such as heroin may cause long-term effects in the orbitofrontal area (OFC), which is essential for regulating reward-related behaviors, emotional responses, and anxiety.[65] Moreover, neuroimaging and neuropsychological studies demonstrate dysregulation of circuits associated with emotion, stress and high impulsivity.[66]
Dependence
[edit]Opioid dependence can occur as physical dependence, psychological dependence, or both.[67] Drug dependence is an adaptive state associated with a withdrawal syndrome upon cessation of repeated exposure to a stimulus (e.g., drug intake).[48][49][50] Dependence is a component of a substance use disorder.[13][68] Opioid dependence can manifest as physical dependence, psychological dependence, or both.[67][49][68]
Increased brain-derived neurotrophic factor (BDNF) signaling in the ventral tegmental area (VTA) has been shown to mediate opioid-induced withdrawal symptoms via downregulation of insulin receptor substrate 2 (IRS2), protein kinase B (AKT), and mechanistic target of rapamycin complex 2 (mTORC2).[48][69] As a result of downregulated signaling through these proteins, opiates cause VTA neuronal hyperexcitability and shrinkage (specifically, the size of the neuronal soma is reduced).[48] It has been shown that when an opiate-naive person begins using opiates in concentrations that induce euphoria, BDNF signaling increases in the VTA.[70]
Upregulation of the cyclic adenosine monophosphate (cAMP) signal transduction pathway by cAMP response element binding protein (CREB), a gene transcription factor, in the nucleus accumbens is a common mechanism of psychological dependence among several classes of drugs of abuse.[67][48] Upregulation of the same pathway in the locus coeruleus is also a mechanism responsible for certain aspects of opioid-induced physical dependence.[67][48]
A scale was developed to compare the harm and dependence liability of 20 drugs.[71] The scale uses a rating of zero to three to rate physical dependence, psychological dependence, and pleasure to create a mean score for dependence.[71] Selected results can be seen in the chart below. Heroin and morphine both scored highest, at 3.0.[71]
| Drug | Mean | Pleasure | Psychological dependence | Physical dependence |
|---|---|---|---|---|
| Heroin/Morphine | 3.00 | 3.0 | 3.0 | 3.0 |
| Cocaine | 2.39 | 3.0 | 2.8 | 1.3 |
| Alcohol | 1.93 | 2.3 | 1.9 | 1.6 |
| Benzodiazepines | 1.83 | 1.7 | 2.1 | 1.8 |
| Tobacco | 2.21 | 2.3 | 2.6 | 1.8 |
Opioid receptors
[edit]A genetic basis for the efficacy of opioids in the treatment of pain has been demonstrated for several specific variations, but the evidence for clinical differences in opioid effects is ambiguous.[11] There is an estimated 50% genetic contribution to opioid use disorder.[11][72] The pharmacogenomics of the opioid receptors and their endogenous ligands have been the subject of intensive activity in association studies. These studies test broadly for a number of phenotypes, including opioid dependence, cocaine dependence, alcohol dependence, methamphetamine dependence/psychosis, response to naltrexone treatment, personality traits, and others. Major and minor variants have been reported for every receptor and ligand coding gene in both coding sequences, as well as regulatory regions.[72] Research on endogenous opioid receptors has focused around OPRM1 gene, which encodes the μ-opioid receptor, and the OPRK1 and OPRD1 genes, which encode the κ and δ receptors, respectively.[72] Newer approaches shift away from analysis of specific genes and regions, and are based on an unbiased screen of genes across the entire genome, which have no apparent relationship to the phenotype in question. These GWAS studies yield a number of implicated genes, although many of them code for seemingly unrelated proteins in processes such as cell adhesion, transcriptional regulation, cell structure determination, and RNA, DNA, and protein handling/modifying.[73]
118A>G variant
[edit]While over 100 variants have been identified for the opioid mu-receptor, the most studied mu-receptor variant is the non-synonymous 118A>G variant, which results in functional changes to the receptor, including lower binding site availability, reduced mRNA levels, altered signal transduction, and increased affinity for beta-endorphin. In theory, all these functional changes would reduce the impact of exogenous opioids, requiring a higher dose to achieve the same therapeutic effect. This points to a potential for greater addictive capacity in individuals who require higher dosages to achieve pain control. But evidence linking the 118A>G variant to opioid dependence is mixed, with associations shown in a number of study groups, but negative results in other groups. One explanation for the mixed results is the possibility of other variants that are in linkage disequilibrium with the 118A>G variant and thus contribute to different haplotype patterns more specifically associated with opioid dependence.[74]
Non-opioid receptor genes
[edit]While opioid receptors have been the most widely studied, a number of other genes have been implicated in OUD. Higher numbers of (CA) repeats flanking the preproenkephalin gene, PENK, have been associated with opiate dependence.[75] There have been mixed results for the MCR2 gene, encoding melanocortin receptor type 2, implicating both protection and risk to heroin addiction.[75] A number of enzymes in the cytochrome P450 family may also play a role in dependence and overdose due to variance in breakdown of opioids and their receptors. There are also multiple potential complications with combining opioids with antidepressants and antiepileptic drugs (both common drugs for chronic pain patients) because of their effects on inducing CYP enzymes.[76] Genotyping of CYP2D6 in particular may play a role in helping patients with individualized treatment for OUD and other drug addictions.[76]
Prevention
[edit]The CDC gives prescribers specific recommendations for starting opioids, clinically appropriate use, and assessing risks associated with opioid therapy.[77] Improving opioid prescribing guidelines and practices can help reduce unnecessary exposure to opioids, which in turn lowers the risk of developing OUD (opioid use disorder). Healthcare providers should strictly follow evidence-based guidelines, such as the CDC Clinical Practice Guideline for Prescribing Opioids for Pain, to ensure safe and appropriate use.[78] Another way to prevent OUD is educating the public about the risks of prescription opioids and illegal substances like fentanyl. Awareness campaigns, community outreach programs, and school-based education initiatives can help people make informed decisions about opioid use and recognize the signs of addiction early on.[79]
Large U.S. retail pharmacy chains are implementing protocols, guidelines, and initiatives to take back unused opioids, providing naloxone kits, and being vigilant about suspicious prescriptions.[80][81][82] Insurance programs can help limit opioid use by setting quantity limits on prescriptions or requiring prior authorizations for certain medications.[83] Many U.S. officials and government leaders have become involved in implementing preventative measures to decrease opioid usage in the United States.[84] Targeted education of medical providers and government officials can lead to provisions affecting opioid distribution by healthcare providers.[10]
Opioid-related deaths
[edit]Naloxone is used for the emergency treatment of an overdose.[85] It can be given by many routes (e.g., intramuscular (IM), intravenous (IV), subcutaneous, intranasal, and inhalation) and acts quickly by displacing opioids from opioid receptors and preventing the activation of these receptors.[82] Naloxone kits are recommended for laypersons who may witness an opioid overdose, for people with large prescriptions for opioids, those in substance use treatment programs, and those recently released from incarceration.[86] Since this is a life-saving medication, many areas of the U.S. have implemented standing orders for law enforcement to carry and give naloxone as needed.[87][88] In addition, naloxone can be used to challenge a person's opioid abstinence status before starting a medication such as naltrexone, which is used in the management of opioid addiction.[89]
Good Samaritan laws typically protect bystanders who administer naloxone. In the U.S., at least 40 states have Good Samaritan laws to encourage bystanders to take action without fear of prosecution.[90] As of 2019, 48 states give pharmacists the authority to distribute naloxone without an individual prescription.[91]
Homicide, suicide, accidents and liver disease are also opioid-related causes of death for those with OUD.[92][93] Many of these causes of death are unnoticed due to the often limited information on death certificates.[92][94]
Mitigation
[edit]The "CDC Clinical Practice Guideline for Prescribing Opioids for Pain-United States, 2022" provides recommendations related to opioid misuse, OUD, and opioid overdoses.[16] It reports a lack of clinical evidence that "abuse-deterrent" opioids (e.g., OxyContin), as labeled by the U.S. Food and Drug Administration, are effective for OUD risk mitigation.[16][95] CDC guidance suggests the prescription of immediate-release opioids instead of opioids that have a long duration (long-acting) or opioids that are released over time (extended release).[16] Other recommendations include prescribing the lowest opioid dose that successfully addresses the pain in opioid-naïve patients and collaborating with patients who already take opioid therapy to maximize the effect of non-opioid analgesics.[16]
While receiving opioid therapy, patients should be periodically evaluated for opioid-related complications and clinicians should review state prescription drug monitoring program systems.[16] The latter should be assessed to reduce the risk of overdoses in patients due to their opioid dose or medication combinations.[16] For patients receiving opioid therapy in whom the risks outweigh the benefits, clinicians and patients should develop a treatment plan to decrease their opioid dose incrementally.[16]
For more specific mitigation strategies regarding opioid overdoses, see opioid overdose § Prevention.
Management
[edit]Opioid use disorders typically require long-term treatment and care with the goal of reducing the person's risks and improving their long-term physical and psychological condition.[45]
First-line management involves the use of opioid replacement therapies, particularly methadone and buprenorphine/naloxone. Withdrawal management alone is strongly discouraged, because of its association with elevated risks of HIV and hepatitis C transmission, high rates of overdose deaths, and nearly universal relapse.[96][97] This approach is seen as ineffective without plans for transition to long-term evidence-based addiction treatment, such as opioid agonist treatment.[54] Though treatment reduces mortality rates, the first four weeks after treatment begins and the four weeks after treatment ceases are the riskiest times for drug-related deaths.[7] These periods of increased vulnerability are significant because many of those in treatment leave programs during these periods.[7] There is evidence that people with opioid use disorder who are dependent on pharmaceutical opioids may require a different management approach from those who take heroin.[98]
Medication
[edit]Opioid replacement therapy (ORT), also known as opioid substitution therapy (OST) or Medications for Opioid Use Disorder (MOUD), involves replacing an opioid, such as heroin.[99][100] Commonly used drugs for ORT are methadone and buprenorphine/naloxone (Suboxone), which are taken under medical supervision.[100] Buprenorphine/naloxone is usually preferred over methadone because of its safety profile, which is considered significantly better, primarily with regard to its risk of overdose[101] and effects on the heart (QTc prolongation).[102][103]
Buprenorphine/naloxone, methadone, and naltrexone are approved by the U.S. Food and Drug Administration (FDA) for medication-assisted treatment (MAT).[104] In the U.S., the Substance Abuse and Mental Health Services Administration (SAMHSA) certifies opioid treatment programs (OTPs), where methadone can be dispensed at methadone clinics.[105] As of 2023, the Waiver Elimination (MAT Act), also known as the "Omnibus Bill", removed the federal requirement for medical providers to obtain a waiver to prescribe buprenorphine, in an attempt to increase access to OUD treatment.[106]
The driving principle behind ORT is the patient's reclamation of a self-directed life.[107] ORT facilitates this process by reducing symptoms of drug withdrawal and drug cravings.[100][107] In some countries (not the U.S. or Australia),[100] regulations enforce a limited time for people on ORT programs that conclude when a stable economic and psychosocial situation is achieved. (People with HIV/AIDS or hepatitis C are usually excluded from this requirement.) In practice, 40–65% of patients maintain abstinence from additional opioids while receiving opioid replacement therapy and 70–95% can reduce their use significantly.[100] Medical (improper diluents, non-sterile injecting equipment), psychosocial (mental health, relationships), and legal (arrest and imprisonment) issues that can arise from the use of illegal opioids are concurrently eliminated or reduced.[100] Clonidine or lofexidine can help treat the symptoms of withdrawal.[108]
The period when initiating methadone and the time immediately after discontinuing treatment with both drugs are periods of particularly increased mortality risk, which should be dealt with by both public health and clinical strategies.[7] ORT has proved to be the most effective treatment for improving the health and living condition of people experiencing illegal opiate use or dependence, including mortality reduction[100][109][7] and overall societal costs, such as the economic loss from drug-related crime and healthcare expenditure.[100] A review of UK hospital policies found that local guidelines delayed access to substitute opioids, for instance by requiring lab tests to demonstrate recent use or input from specialist drug teams before prescribing. Delays to access can increase people's risk of discharging themselves early against medical advice.[110][111] ORT is endorsed by the World Health Organization, United Nations Office on Drugs and Crime and UNAIDS as effective at reducing injection, lowering risk for HIV/AIDS, and promoting adherence to antiretroviral therapy.[7]
Buprenorphine and methadone work by reducing opioid cravings, easing withdrawal symptoms, and blocking the euphoric effects of opioids via cross-tolerance,[112] and in the case of buprenorphine, a high-affinity partial opioid agonist, also due to opioid receptor saturation.[113]
Buprenorphine and buprenorphine/naloxone
[edit]Buprenorphine can be administered either as a standalone product or in combination with the opioid antagonist naloxone. This inclusion is strategic: it deters misuse by preventing the crushing and injecting of the medication, encouraging instead the prescribed sublingual (under the tongue) route.[100] Buprenorphine/naloxone formulations are available as tablets and films;[114] these formulations operate efficiently when taken sublingually. In this form, buprenorphine's bioavailability remains robust (35–55%), while naloxone's is significantly reduced (~10%).[115]
Buprenorphine's role as a partial opioid receptor agonist sets it apart from full agonists like methadone. Its unique pharmacological profile makes it less likely to cause respiratory depression, thanks to its "ceiling effect".[116][117] While the risk of misuse or overdose is higher with buprenorphine alone compared to the buprenorphine/naloxone combination or methadone, its usage is linked to a decrease in mortality.[118][7] Approved in the U.S. for opioid dependence treatment in 2002,[119] buprenorphine has since expanded in form, with the FDA approving a month-long injectable version in 2017.[120]
When initiating buprenorphine/naloxone therapy, several critical factors must be considered. These include the severity of withdrawal symptoms, the time elapsed since the last opioid use, and the type of opioid involved (long-acting vs. short-acting).[121] A standard induction method involves waiting until the patient exhibits moderate withdrawal symptoms, as measured by a Clinical Opiate Withdrawal Scale, achieving a score of around 12. Alternatively, "microdosing" commences with a small dose immediately, regardless of withdrawal symptoms, offering a more flexible approach to treatment initiation.[122] "Macrodosing" starts with a larger dose of Suboxone, a different induction strategy with its own set of considerations.[123]
Methadone
[edit]Methadone is a commonly used full-opioid agonist in the treatment of opioid use disorder. It is effective in relieving withdrawal symptoms and cravings in people with opioid addiction, and can also be used in pain control in certain situations.[118] While methadone is a widely prescribed form of OAT, it often requires more frequent clinical visits compared to buprenorphine/naloxone, which also has a better safety profile and lower risk of respiratory depression and overdose.[124]
Important considerations when initiating methadone include the patient's opioid tolerance, the time since last opioid use, the type of opioid used (long-acting vs. short-acting), and the risk of methadone toxicity.[125] Methadone comes in different forms: tablet, oral solution, or an injection.[118]
One of methadone's benefits is that it can last up to 56 hours in the body, so if a patient misses a daily dose, they will not typically struggle with withdrawal symptoms.[118] Other advantages of methadone include reduction in infectious disease related to injection drug use, and reduced mortality. Methadone has a number of potential side effects, including slowed breathing, nausea, vomiting, restlessness, and headache.[126]
Naltrexone
[edit]Naltrexone is an opioid receptor antagonist used for the treatment of opioid addiction.[127][128] It is not as widely used as buprenorphine or methadone for OUD due to low rates of patient acceptance, non-adherence due to daily dosing, and difficulty achieving abstinence from opioids before beginning treatment. Additionally, dosing naltrexone after recent opioid use can lead to precipitated withdrawal. Conversely, naltrexone antagonism at the opioid receptor can be overcome with higher doses of opioids.[129] Naltrexone monthly IM injections received FDA approval in 2010 for the treatment of opioid dependence in abstinent opioid users.[127][130]
Other opioids
[edit]Evidence of effects of heroin maintenance compared to methadone are unclear as of 2010.[131] A Cochrane review found some evidence in opioid users who had not improved with other treatments.[132] In Switzerland, Germany, the Netherlands, and the United Kingdom, long-term injecting drug users who do not benefit from methadone and other medication options may be treated with injectable heroin that is administered under the supervision of medical staff.[133] Other countries where it is available include Spain, Denmark, Belgium, Canada, and Luxembourg.[134]Dihydrocodeine in both extended-release and immediate-release form is also sometimes used for maintenance treatment as an alternative to methadone or buprenorphine in some European countries.[135] Dihydrocodeine is an opioid agonist.[136] It may be used as a second-line treatment.[137] A 2020 systematic review found low-quality evidence that dihydrocodeine may be no more effective than other routinely used medication interventions in reducing illicit opiate use.[138]An extended-release morphine confers a possible reduction of opioid use and with fewer depressive symptoms but overall more adverse effects compared to other forms of long-acting opioids. Retention in treatment was not found to be significantly different.[139] It is used in Switzerland and more recently in Canada.[140]
In pregnancy
[edit]Pregnant women with opioid use disorder can also receive treatment with methadone, naltrexone, or buprenorphine.[141] Buprenorphine appears to be associated with more favorable outcomes compared to methadone for treating opioid use disorder (OUD) in pregnancy. Studies show that buprenorphine is linked to lower risks of preterm birth, greater birth weight, and larger head circumference without increased harm.[142] Compared to methadone, it consistently results in improved birth weight and gestational age, though these findings should be interpreted with caution due to potential biases.[143] Buprenorphine use also correlates with a lower risk of adverse neonatal outcomes, with similar risks of adverse maternal outcomes as methadone.[144] Infants born to buprenorphine-treated mothers generally have higher birth weights, fewer withdrawal symptoms, and a lower likelihood of premature birth.[144] Additionally, these infants often require less treatment for neonatal abstinence syndrome and have mothers who are more likely to start treatment earlier in pregnancy, leading to longer gestations and larger infants.[145]
Behavioral therapy
[edit]Paralleling the variety of medical treatments, there are many forms of psychotherapy and community support for treating OUD. The primary evidence-based psychotherapies include cognitive behavioral therapy (CBT), motivational enhancement therapy (MET), contingency management (CM), and twelve-step programs. Community-based support such as support groups (e.g., Narcotics Anonymous) and therapeutic housing for those with OUD is also an important aspect of healing.[146][147]
Cognitive behavioral therapy
[edit]Cognitive behavioral therapy (CBT) is a form of psychosocial intervention that systematically evaluates thoughts, feelings, and behaviors about a problem and works to develop coping strategies to work through those problems.[148] This intervention has demonstrated success in many psychiatric conditions (e.g., depression) and substance use disorders (e.g., tobacco).[149] But the use of CBT alone for OUD has declined due to lack of efficacy, and many rely on medication therapy or medication therapy with CBT, since both were found to be more efficacious than CBT alone.[89] CBT has been shown to be more successful in relapse prevention than treatment of ongoing drug use.[146] It is particularly known for its durability.[150]
Motivational Enhancement Therapy
[edit]Motivational enhancement therapy (MET) is the manualized form of motivational interviewing (MI). MI leverages one's intrinsic motivation to recover through education, formulation of relapse prevention strategies, reward for adherence to treatment guidelines, and positive thinking to keep motivation high—which are based on a person's socioeconomic status, gender, race, ethnicity, sexual orientation, and readiness to recover.[89][151][152] Like CBT, MET alone has not shown convincing efficacy for OUD. There is stronger support for combining it with other therapies.[150]
Contingency Management Therapy
[edit]Contingency Management Therapy (CMT) employs similar principles as operant behavioral conditioning, such as using incentives to reach certain goals (e.g., verified abstinence, usually in the form of urine drug testing).[146] This form of psychotherapy has the strongest, most robust empirical support for treating drug addiction.[146][150][153] Outpatient clients are shown to have improved medication compliance, retention, and abstinence when using voucher-based incentives.[146][150] One way this is implemented is to offer take-home privileges for methadone programs. Despite its effectiveness during treatment, effects tend to wane once terminated. Additionally, the cost barrier limits its application in the clinical community.[146]
Twelve-step programs
[edit]While medical treatment may help with the initial symptoms of opioid withdrawal, once the first stages of withdrawal are through, a method for long-term preventative care is attendance at 12-step groups such as Narcotics Anonymous (NA).[154] NA's 12-step process is based on the 12-step facilitation of Alcoholic Anonymous (AA) and centers on peer support, self-help, and spiritual connectedness. Some evidence also supports the use of these programs for adolescents.[155] Multiple studies have shown increased abstinence for those in NA compared to those who are not.[11][156][157][158] Members report a median abstinence length of 5 years.[158]
Novel experimental treatments
[edit]Though medications and behavioral treatments are effective forms for treating OUD, relapse remains a common problem. The medical community has looked to novel technologies and traditional alternative medicines for new ways to approach the issues of continued cravings and impaired executive functioning. While consensus on their efficacy has not been reached, a number of reviews have shown promising results for the use of non-invasive brain stimulation (NIBS) for reducing cravings in OUD.[159][160] These results are consistent with the use of NIBS for reducing cravings of other substances. Additionally, investigations into the anecdotal evidence of psychedelics like ibogaine have also shown the possibility of decreased cravings and withdrawal symptoms.[161] Ibogaine is illegal in the U.S. but is unregulated in Mexico, Costa Rica, and New Zealand, where many clinics use it for addiction treatment.[162] Research has shown a minor mortality risk due to its cardiotoxic and neurotoxic effects.[161]
In 2024 the FDA approved the NET (NeuroElectric Therapy) device, which reduces withdrawal symptoms by neurostimulation. Used for three to five days of continuous treatment, NET delivers alternating current via surface electrodes placed trans-cranially at the base of the skull on each side of the head.[163][164]
Treatment challenges
[edit]The stigma surrounding addiction can heavily influence opioid addicts not to seek help. Many people view addiction as a moral failing rather than a medical condition, which can lead to feelings of shame and isolation. This stigma can also affect family members, making it difficult for them to support their loved ones effectively.[165]
Accessing appropriate treatment is often a significant barrier. Factors include:[166]
- Availability of services: In many areas, especially rural regions, there is a lack of treatment facilities or qualified healthcare providers who specialize in opioid use disorder.
- Insurance coverage: People without insurance or those whose plans do not cover substance use disorder treatment may struggle to find affordable care.
- Transportation: For many, getting to treatment facilities can be challenging due to a lack of transportation options.
The variety of treatment modalities available for OUD—such as medication-assisted treatment (MAT), counseling, and residential programs—can be overwhelming. Patients may have difficulty understanding which option best suits them, leading to confusion and potential disengagement from the treatment process. Withdrawal symptoms can be severe and uncomfortable, leading many people to relapse before they complete detoxification or engage fully in recovery programs. The fear of withdrawal often prevents people from seeking help altogether.[167]
Epidemiology
[edit]
Во всем мире число людей с опиоидной зависимостью увеличилось с 10,4 миллиона в 1990 году до 15,5 миллиона в 2010 году. [7] In 2016, the numbers rose to 27 million people who experienced this disorder.[169] Opioid use disorders resulted in 122,000 deaths worldwide in 2015,[170] up from 18,000 deaths in 1990.[171] Deaths from all causes rose from 47.5 million in 1990 to 55.8 million in 2013.[ 171 ] [ 170 ]
Соединенные Штаты
[ редактировать ]
Нынешняя эпидемия злоупотребления опиоидами является самой смертоносной эпидемией наркотиков в американской истории. [ 20 ] Кризис можно отличить по волнам смертей от передозировки опиоидов, как описывают Центры по контролю и профилактике заболеваний. [ 172 ] Первая волна началась в 1990-х годах и была связана с ростом числа назначений натуральных опиоидов (таких как кодеин и морфин), полусинтетических опиоидов (оксикодон, гидрокодон, гидроморфон и оксиморфон) и синтетических опиоидов, таких как метадон. [ 173 ] [ 172 ] В США «скорректированный по возрасту уровень смертности от отравлений наркотиками, включающими опиоидные анальгетики, увеличился с 1,4 до 5,4 смертей на 100 000 населения в период с 1999 по 2010 год. [ 174 ] Вторая волна датируется примерно 2010 годом, когда резко возросло число передозировок опиоидами из-за героина. [ 173 ] К этому времени смертей от передозировки уже было в четыре раза больше, чем в 1999 году. [ 174 ] Скорректированный по возрасту уровень смертности от отравлений наркотиками, связанными с героином, удвоился с 0,7 до 1,4 смертей на 100 000 человек в период с 1999 по 2011 год, а затем продолжил расти до 4,1 в 2015 году. [ 175 ] Третья волна смертей от передозировок началась в 2013 году и была связана с синтетическими опиоидами, особенно с незаконно производимым фентанилом. [ 173 ] Хотя незаконный рынок фентанила постоянно меняется, этот наркотик обычно продается как добавка к героину. Исследования показывают, что быстрое увеличение количества фентанила на незаконном рынке опиоидов было в значительной степени обусловлено предложением и датируется 2006 годом. Снижение чистоты героина, конкуренция из-за расширения доступа к рецептурным лекарствам и распространение «метода Зигфрида» (относительно простой метод). и экономически эффективный метод производства фентанила) были основными факторами, побудившими уличных торговцев включать фентанил в свою продукцию. [ 176 ] [ 177 ] Нынешняя, четвертая волна, начавшаяся в 2016 году, характеризуется передозировкой поливеществ из-за синтетических опиоидов, таких как фентанил, в смеси со стимуляторами, такими как метамфетамин или кокаин. [ 178 ] [ 179 ] В 2010 году около 0,5% смертей, связанных с опиоидами, были связаны с употреблением стимуляторов. Эта цифра увеличилась более чем в 50 раз к 2021 году, когда около трети смертей, связанных с опиоидами, или 34 000, были связаны с употреблением стимуляторов. [ 179 ]
В 2017 году Министерство здравоохранения и социальных служб США (HHS) объявило чрезвычайную ситуацию в области общественного здравоохранения из-за роста злоупотребления опиоидами. [ 180 ] Администрация представила стратегическую основу под названием «Опиоидная стратегия из пяти пунктов», которая включает предоставление услуг по восстановлению доступа, увеличение доступности противодействующих средств при передозировке, финансирование злоупотребления опиоидами и исследований боли, изменение методов лечения людей, справляющихся с болью, а также обновление отчетов общественного здравоохранения, связанных с борьбе со злоупотреблением опиоидными наркотиками. [ 180 ] [ 181 ]
Эпидемия в США в 2000-х годах связана с рядом факторов. [ 15 ] Уровень употребления опиоидов и зависимости варьируется в зависимости от возраста, пола, расы и социально-экономического статуса. [ 15 ] Что касается расы, то считается, что разница в смертности обусловлена взаимодействием между назначениями врачей и отсутствием доступа к здравоохранению и некоторым рецептурным лекарствам. [ 15 ] Мужчины подвергаются более высокому риску употребления опиоидов и возникновения зависимости, чем женщины. [ 182 ] [ 183 ] на мужчин также приходится больше случаев передозировки опиоидов, чем на женщин, хотя этот разрыв сокращается. [ 182 ] Женщинам с большей вероятностью будут прописывать обезболивающие, получать более высокие дозы, использовать их в течение более длительного времени и быстрее становиться зависимыми от них. [ 184 ]
Смертность от употребления опиоидов также имеет тенденцию искажаться в более старшем возрасте, чем смертность от употребления других запрещенных наркотиков. [ 183 ] [ 185 ] [ 186 ] Это не отражает употребление опиоидов в целом, включая молодых людей. Передозировки опиоидами наиболее распространены среди людей в возрасте от 40 до 50 лет. [ 186 ] в отличие от передозировки героина, которая чаще всего встречается среди людей в возрасте от 20 до 30 лет. [ 185 ] Люди в возрасте от 21 до 35 лет составляют 77% людей, которые обращаются за лечением расстройств, вызванных употреблением опиоидов. [ 187 ] однако средний возраст людей, впервые принявших рецептурные обезболивающие, в 2013 году составил 21,2 года. [ 188 ] Среди представителей среднего класса способы получения средств включают финансовые злоупотребления со стороны пожилых людей и международные дилеры, замечающие отсутствие правоприменения в своих мошеннических транзакциях по всему Карибскому региону. [ 189 ]
С 2018 года, с принятием федеральным правительством Закона о ПОДДЕРЖКЕ (Закон о профилактике употребления психоактивных веществ и расстройств, способствующих восстановлению и лечению опиоидов для пациентов и сообществ), федеральные ограничения на использование метадона для пациентов, получающих медицинскую помощь, были сняты. [ 190 ] С марта 2020 года в результате пандемии COVID-19 бупренорфин можно будет отпускать посредством телемедицины в США. [ 191 ] [ 192 ]
В октябре 2021 года губернатор Нью-Йорка Кэти Хоукул подписала закон о борьбе с опиоидным кризисом. Это включало создание программы лечения расстройств, вызванных употреблением психоактивных веществ, для заключенных в государственных и местных исправительных учреждениях, декриминализацию хранения и продажи игл и шприцев для подкожных инъекций, создание онлайн-каталога для распространителей опиоидных антагонистов и расширение количество подходящих преступлений, совершенных лицами, страдающими расстройствами, вызванными употреблением психоактивных веществ, которые могут быть рассмотрены для направления в программу лечения наркозависимости. [ 193 ] До тех пор, пока эти законы не были подписаны, заключенные жители Нью-Йорка не имели надежного доступа к медикаментозному лечению, а хранение шприцев все еще считалось правонарушением класса А, несмотря на то, что Нью-Йорк санкционировал и финансировал программы обмена шприцев и доступа к ним. [ 194 ] Этот закон признает, что законы штата Нью-Йорк способствовали смертности от опиоидов: в 2020 году от передозировки в штате Нью-Йорк умерло более 5112 человек, из них 2192 - в городе Нью-Йорке. [ 195 ]
По состоянию на 2023 год Закон об отмене отказа от права (MAT) в рамках раздела 1262 Закона о консолидированных ассигнованиях 2023 года (или «Сводного закона») отменил федеральное требование к поставщикам медицинских услуг получать отказ от назначения бупренорфина в попытке расширить доступ к лечению ОУД. [ 106 ] До принятия этого законопроекта практикующие врачи должны были получить отказ от Закона о лечении наркозависимости 2000 года (DATA), также известный как «x-waiver», прежде чем прописывать бупренорфин. Кроме того, теперь больше нет ограничений на количество пациентов, которым поставщик медицинских услуг может прописать бупренорфин для лечения ОУД. [ 106 ]
- Графики смертности от конкретных опиоидов и классов опиоидов - Национальный институт злоупотребления наркотиками США
-
Ежегодная смертность в США от всех опиоидных наркотиков. В это число входят опиоидные анальгетики, а также героин и запрещенные синтетические опиоиды. [ 196 ]
-
Ежегодная смертность в США по категориям наркотиков [ 196 ]
-
Ежегодная смертность от передозировки опиоидов в США, связанная с рецептурными опиоидами. Неметадоновые синтетические вещества представляют собой категорию, в которой доминирует незаконно приобретенный фентанил, и поэтому они исключены. [ 197 ]
-
Ежегодная смертность от передозировки опиоидами в США, связанной с героином [ 197 ]
-
Ежегодная смертность от передозировки опиоидов в США, включающая психостимуляторы (в первую очередь метамфетамин) [ 197 ]
Влияние COVID-19 на передозировку опиоидами и телемедицинское лечение
[ редактировать ]Эпидемиологические исследования показали, что пандемия COVID-19 ускорила опиоидный кризис. [ 177 ] [ 198 ] [ 199 ] Общая тенденция данных о передозировке опиоидов показала плато смертности примерно в 2017–2018 годах, при этом внезапный и резкий рост в 2019 году в основном связан с синтетическими опиоидами, такими как фентанил. [ 197 ] В 2020 году в США произошло 93 400 случаев передозировки наркотиков, из которых >73% (приблизительно 69 000) были связаны с передозировкой опиоидов. [ 200 ] Один обзор JAMA, проведенный Gomes et al. показали, что расчетные потери лет жизни (YLL) из-за токсичности опиоидов в США увеличились на 276%. Это увеличение особенно ощущалось среди людей в возрасте от 15 до 19 лет, чей YLL увеличился почти в три раза. Наибольший эффект наблюдался у молодых мужчин. [ 199 ] Другие обзоры данных по опиоидам в США и Канаде, совпадающие с началом COVID-19, свидетельствуют о значительном увеличении использования неотложной медицинской помощи, связанной с опиоидами, увеличении положительного результата в отношении опиоидов и, что удивительно, об отсутствии или уменьшении изменений в выдаче налоксона. [ 201 ]
Телездравоохранение сыграло большую роль в обеспечении доступа к лечению OUD, а законодательство в области телездравоохранения продолжает развиваться. Исследование участников программы Medicare с впервые возникшим ОУД показало, что у тех, кто получал телемедицинские услуги, риск смерти от передозировки был на 33% ниже. [ 202 ] Также было показано, что группы меньшинств, такие как чернокожие и латиноамериканцы, извлекают выгоду из расширенного доступа благодаря программам телемедицины, введенным во время пандемии, несмотря на увеличение разрыва в неравенстве в других результатах, связанных с OUD. [ 203 ] DEA и HHS расширили гибкость телемедицины в отношении назначения контролируемых веществ, таких как бупренорфин, для OUD до 31 декабря 2024 года. [ 204 ]
История
[ редактировать ]
Злоупотребление опиатами регистрируется как минимум с 300 г. до н.э. Греческая мифология описывает Непенту (по-гречески «свободная от печали») и то, как ее использовал герой Одиссеи . Опиоиды использовались на Ближнем Востоке на протяжении веков. Очистка и выделение опиатов произошли в начале 19 века. [ 28 ] Бупренорфин был одним из первых одобренных препаратов от опиоидной зависимости, представленных в США в начале 2000-х годов для борьбы со злоупотреблением опиоидами. Это открытие произошло после десятилетий исследований и привело к разработке других лекарств для борьбы с расстройствами, связанными с употреблением опиоидов. [ 205 ]
Левацетилметадол ранее использовался для лечения опиоидной зависимости. В 2003 году производитель препарата прекратил производство. Доступных универсальных версий нет. LAAM дал долгосрочный эффект, что позволило человеку, проходящему лечение, посещать клинику только три раза в неделю, а не ежедневно, как при использовании метадона. [ 206 ] В 2001 году левацетилметадол был удален с европейского рынка из-за сообщений об опасных для жизни нарушениях желудочкового ритма . [ 207 ] В 2003 году Roxane Laboratories, Inc. прекратила выпуск препарата Орлаам в США. [ 208 ]
Ссылки
[ редактировать ]- ^ Jump up to: а б «FDA одобрило первый имплантат бупренорфина для лечения опиоидной зависимости» . США Управление по контролю за продуктами и лекарствами (FDA) (пресс-релиз). 26 мая 2016 года . Проверено 16 марта 2017 г.
- ^ «3 Оценка пациента» . Клинические рекомендации по использованию бупренорфина при лечении опиоидной зависимости . Роквилл (Мэриленд): Управление служб по борьбе со злоупотреблением психоактивными веществами и психическим здоровьем (США). 2004.
- ^ Jump up to: а б «Обычно используемые термины» . www.cdc.gov . 29 августа 2017 года . Проверено 16 июля 2018 г.
- ^ Jump up to: а б с д и ж г час я дж к л м н тот п д р с Американская психиатрическая ассоциация (2013), Диагностическое и статистическое руководство по психическим расстройствам (5-е изд.) , Арлингтон: Американское психиатрическое издание, стр. 540–546 , ISBN 978-0-89042-555-8
- ^ Jump up to: а б с д и ж Управление служб по борьбе с употреблением психоактивных веществ и психическим здоровьем (30 сентября 2014 г.). «Расстройства, вызванные употреблением психоактивных веществ» .
- ^ Jump up to: а б с «Употребление опиоидов и расстройства, связанные с употреблением опиоидов во время беременности» . АКОГ . Август 2017 года . Проверено 16 июля 2018 г.
- ^ Jump up to: а б с д и ж г час я Сордо Л., Баррио Г., Браво М.Дж., Индаве Б.И., Дегенхардт Л., Виссинг Л. и др. (апрель 2017 г.). «Риск смертности во время и после опиоидной заместительной терапии: систематический обзор и метаанализ когортных исследований» . БМЖ . 357 : j1550. дои : 10.1136/bmj.j1550 . ПМЦ 5421454 . ПМИД 28446428 .
- ^ Jump up to: а б «Лечение расстройств, вызванных употреблением психоактивных веществ» . Управление служб по борьбе со злоупотреблением психоактивными веществами и психическим здоровьем. Октябрь 2014.
- ^ Макдональд Р., Стрэнг Дж. (июль 2016 г.). «Эффективны ли программы приема налоксона на дому? Систематический обзор с использованием критериев Брэдфорда Хилла» . Зависимость . 111 (7): 1177–1187. дои : 10.1111/add.13326 . ПМК 5071734 . ПМИД 27028542 .
- ^ Jump up to: а б с д Шарма Б., Брунер А., Барнетт Г., Фишман М. (июль 2016 г.). «Расстройства, связанные с употреблением опиоидов» . Детские и подростковые психиатрические клиники Северной Америки . 25 (3): 473–487. дои : 10.1016/j.chc.2016.03.002 . ПМЦ 4920977 . ПМИД 27338968 .
- ^ Jump up to: а б с д и Дыдык А.М., Джайн Н.К., Гупта М. (2022). «Расстройство, связанное с употреблением опиоидов» . СтатПерлс . Остров сокровищ (Флорида): StatPearls Publishing. ПМИД 31985959 . NCBI NBK553166 . Проверено 16 ноября 2022 г.
- ^ Диагностический и статистический справочник психических расстройств: DSM-5 . Арлингтон, Вирджиния: Американская психиатрическая ассоциация. 2013. ISBN 978-0-89042-554-1 .
- ^ Jump up to: а б с д Волков Н.Д., Кооб Г.Ф., Маклеллан А.Т. (январь 2016 г.). «Нейробиологические достижения модели зависимости от заболеваний головного мозга» . Медицинский журнал Новой Англии . 374 (4): 363–371. дои : 10.1056/NEJMra1511480 . ПМК 6135257 . ПМИД 26816013 .
Наркомания: термин, используемый для обозначения наиболее тяжелой, хронической стадии расстройства, связанного с употреблением психоактивных веществ, при которой происходит значительная потеря самоконтроля, о чем свидетельствует компульсивный прием наркотиков, несмотря на желание прекратить их прием. В DSM-5 термин «зависимость» является синонимом классификации тяжелого расстройства, связанного с употреблением психоактивных веществ.
- ^ Вебстер Л.Р. (ноябрь 2017 г.). «Факторы риска расстройств, связанных с употреблением опиоидов, и передозировки» . Анестезия и анальгезия . 125 (5): 1741–1748. дои : 10.1213/ANE.0000000000002496 . ПМИД 29049118 . S2CID 19635834 .
- ^ Jump up to: а б с д и Санторо, Теннесси, Санторо, Джей Ди (декабрь 2018 г.). «Расовая предвзятость в эпидемии опиоидов в США: обзор истории системной предвзятости и последствий для ухода» . Куреус . 10 (12): е3733. дои : 10.7759/cureus.3733 . ПМК 6384031 . ПМИД 30800543 .
- ^ Jump up to: а б с д и ж г час Доуэлл Д., Рэган К.Р., Джонс С.М., Болдуин Г.Т., Чоу Р. (ноябрь 2022 г.). «Руководство CDC по клинической практике назначения опиоидов при боли – США, 2022 г.» . ММВР. Рекомендации и отчеты . 71 (3): 1–95. дои : 10.15585/mmwr.rr7103a1 . ПМЦ 9639433 . ПМИД 36327391 .
- ^ «Руководство для врачей по политике в отношении опиоидных препаратов, отпускаемых по рецепту Medicare (Часть D)» (PDF) .
- ^ Мохамади А., Чан Дж. Дж., Лиан Дж., Райт К. Л., Марин А. М., Родригес Е. К. и др. (август 2018 г.). «Факторы риска и совокупная частота длительного употребления опиоидов после травмы или операции: систематический обзор и мета-(регрессионный) анализ». Журнал костной и суставной хирургии. Американский том . 100 (15): 1332–1340. дои : 10.2106/JBJS.17.01239 . ПМИД 30063596 . S2CID 51891341 .
- ^ «Употребление опиоидов, отпускаемых по рецепту, является фактором риска употребления героина» . Национальный институт по борьбе со злоупотреблением наркотиками . Октябрь 2015 года . Проверено 16 июля 2018 г.
- ^ Jump up to: а б Хьюз Э. (2 мая 2018 г.). «Пожиратели боли» . Нью-Йорк Таймс . Проверено 3 мая 2018 г.
- ^ Jump up to: а б «Тенденции в использовании метадона, бупренорфина и налтрексона пролонгированного действия в наркологических учреждениях: 2003–2015 гг. (обновленная информация)» . www.samhsa.gov . Проверено 16 ноября 2022 г.
- ^ Донован Д.М., Ингалсбе М.Х., Бенбоу Дж., Дейли, округ Колумбия (2013). «12-шаговые вмешательства и программы взаимной поддержки при расстройствах, связанных с употреблением психоактивных веществ: обзор» . Социальная работа в здравоохранении . 28 (3–4): 313–332. дои : 10.1080/19371918.2013.774663 . ПМЦ 3753023 . ПМИД 23731422 .
- ^ «Программы профилактики передозировки опиоидами, обеспечивающие налоксоном непрофессионалов — США, 2014 г.» . www.cdc.gov . Проверено 16 ноября 2022 г.
- ^ CDC (30 августа 2022 г.). «Болезнь недели – расстройство, связанное с употреблением опиоидов» . Центры по контролю и профилактике заболеваний . Проверено 16 ноября 2022 г.
- ^ «Краткий обзор данных 294. Смертность от передозировки наркотиков в США, 1999–2016 гг.» (PDF) . CDC . Проверено 18 мая 2018 г.
- ^ Центр лечения наркозависимости (2006 г.). «[Таблица], Рисунок 4-4: Признаки и симптомы опиоидной интоксикации и синдрома отмены» . www.ncbi.nlm.nih.gov . Проверено 6 апреля 2019 г.
- ^ Фентанил . Изображение 4 из 17. DEA США ( Управление по борьбе с наркотиками ). См. архив с подписью: «Фотоиллюстрация 2 миллиграммов фентанила, смертельной дозы для большинства людей».
- ^ Jump up to: а б Костен Т.Р., Хайле CN. Расстройства, связанные с опиоидами. В: Каспер Д., Фаучи А., Хаузер С., Лонго Д., Джеймсон Дж., Лоскальцо Дж., ред. Принципы внутренней медицины Харрисона, 19e Нью-Йорк, штат Нью-Йорк: McGraw-Hill; 2014. http://accessmedicine.mhmedical.com/content.aspx?bookid=1130§ionid=79757372 По состоянию на 9 марта 2017 г.
- ^ Диагностическое и статистическое руководство по психическим расстройствам: DSM-5 (5-е изд.). Американская психиатрическая ассоциация. 2013. С. 547–549. ISBN 978-0-89042-554-1 .
- ^ Jump up to: а б Шах М., Хюкер М.Р. (2019). Отмена опиоидов . Издательство StatPearls. ПМИД 30252268 . NCBI NBK526012 . Проверено 21 октября 2019 г.
- ^ Перголицци СП, Раффа РБ, Розенблатт МХ (октябрь 2020 г.). «Симптомы отмены опиоидов, последствия хронического употребления опиоидов и расстройства, связанные с употреблением опиоидов: современное понимание и подходы к лечению» . Журнал клинической фармации и терапии . 45 (5): 892–903. дои : 10.1111/jcpt.13114 . ПМИД 31986228 .
- ^ Jump up to: а б с д и ж г час я дж к Райс Р.К., Миллер С.К., Филлин Д.А. (2009). Принципы наркологии . Липпинкотт Уильямс и Уилкинс. стр. 593–594. ISBN 978-0-7817-7477-2 .
- ^ Рахими-Мовагар А., Голами Дж., Амато Л., Хосейни Л., Юсефи-Нураи Р., Амин-Эсмаили М. (июнь 2018 г.). «Фармакологическая терапия при синдроме отмены опиума» . Кокрановская база данных систематических обзоров . 2018 (6): CD007522. дои : 10.1002/14651858.CD007522.pub2 . ПМК 6513031 . ПМИД 29929212 .
- ^ Чен К.В., Бандуччи А.Н., Гуллер Л., Макати Р.Дж., Лавель А., Дочерс С.Б. и др. (ноябрь 2011 г.). «Обследование сопутствующих психиатрических заболеваний в зависимости от пола и типа психоактивного вещества в рамках стационарной программы лечения наркозависимости» . Наркотическая и алкогольная зависимость . 118 (2–3): 92–99. doi : 10.1016/j.drugalcdep.2011.03.003 . ПМЦ 3188332 . ПМИД 21514751 .
- ^ Вебстер Л.Р., Вебстер Р.М. (2005). «Прогнозирование аберрантного поведения у пациентов, получающих опиоиды: предварительная проверка инструмента опиоидного риска» . Лекарство от боли . 6 (6): 432–442. дои : 10.1111/j.1526-4637.2005.00072.x . ПМИД 16336480 .
- ^ Папалеонтиу М., Хендерсон Ч.Р., Тернер Б.Дж., Мур А.А., Ольховская Ю., Аманфо Л. и др. (июль 2010 г.). «Результаты, связанные с употреблением опиоидов при лечении хронической нераковой боли у пожилых людей: систематический обзор и метаанализ» . Журнал Американского гериатрического общества . 58 (7): 1353–1369. дои : 10.1111/j.1532-5415.2010.02920.x . ПМК 3114446 . ПМИД 20533971 .
- ^ Jump up to: а б Ноубл М., Трегир С.Дж., Тредуэлл-младший, Шоэльс К. (февраль 2008 г.). «Долгосрочная опиоидная терапия хронической нераковой боли: систематический обзор и метаанализ эффективности и безопасности» . Журнал управления болью и симптомами . 35 (2): 214–228. дои : 10.1016/j.jpainsymman.2007.03.015 . ПМИД 18178367 .
- ^ Мартелл Б.А., О'Коннор П.Г., Кернс Р.Д., Беккер В.К., Моралес К.Х., Костен Т.Р. и др. (январь 2007 г.). «Систематический обзор: опиоидное лечение хронической боли в спине: распространенность, эффективность и связь с зависимостью». Анналы внутренней медицины . 146 (2): 116–127. дои : 10.7326/0003-4819-146-2-200701160-00006 . ПМИД 17227935 . S2CID 28969290 .
- ^ Калсо Э., Эдвардс Дж.Э., Мур А.Р., Маккуэй Х.Дж. (декабрь 2004 г.). «Опиоиды при хронической нераковой боли: систематический обзор эффективности и безопасности». Боль . 112 (3): 372–380. дои : 10.1016/j.pain.2004.09.019 . ПМИД 15561393 . S2CID 25807828 .
- ^ Jump up to: а б Гослинг Дж., ДеДжонкхир М., Пирс Дж., Уильямс Д.А., Брамметт К.М., Хассетт А.Л. и др. (май 2019 г.). «Отказ от опиоидов и хроническая боль: перспективы бывших потребителей опиоидов» . Боль . 160 (5): 1131–1145. doi : 10.1097/j.pain.0000000000001493 . ПМЦ 8442035 . ПМИД 30889052 .
- ^ Кребс Э.Э., Грейвли А., Ньюджент С., Дженсен А.С., ДеРонн Б., Голдсмит Э.С. и др. (март 2018 г.). «Влияние опиоидных и неопиоидных препаратов на функцию, связанную с болью, у пациентов с хронической болью в спине или болью при остеоартрите бедра или колена: рандомизированное клиническое исследование SPACE» . ДЖАМА . 319 (9): 872–882. дои : 10.1001/jama.2018.0899 . ПМЦ 5885909 . ПМИД 29509867 .
- ^ Эриксен Дж., Сьёгрен П., Брюэра Э., Экхольм О., Расмуссен Н.К. (ноябрь 2006 г.). «Критические проблемы опиоидов при хронической нераковой боли: эпидемиологическое исследование». Боль . 125 (1–2): 172–179. дои : 10.1016/j.pain.2006.06.009 . ПМИД 16842922 . S2CID 24858908 .
- ^ Чапарро Л.Е., Фурлан А.Д., Дешпанде А., Майлис-Ганьон А., Атлас С., Тёрк, округ Колумбия (апрель 2014 г.). «Опиоиды по сравнению с плацебо или другими методами лечения хронической боли в пояснице: обновленная информация Кокрейновского обзора». Позвоночник . 39 (7): 556–563. дои : 10.1097/BRS.0000000000000249 . ПМИД 24480962 . S2CID 25356400 .
- ^ Заместительная поддерживающая терапия в лечении опиоидной зависимости и профилактике ВИЧ/СПИДа (PDF) . Всемирная организация здравоохранения. 2004. ISBN 978-92-4-159115-7 .
- ^ Jump up to: а б «Лечение опиоидной зависимости» . ВОЗ. 2004. Архивировано из оригинала 14 июня 2010 года . Проверено 28 августа 2016 г. [ нужно обновить ]
- ^ Волков Н.Д., Кооб Г.Ф., Маклеллан А.Т. (январь 2016 г.). «Нейробиологические достижения модели зависимости от заболеваний головного мозга» . Медицинский журнал Новой Англии . 374 (4): 363–371. дои : 10.1056/NEJMra1511480 . ПМК 6135257 . ПМИД 26816013 .
- ^ Хайман С.Е. (январь 2007 г.). «Нейробиология зависимости: последствия для произвольного контроля поведения» . Американский журнал биоэтики . 7 (1): 8–11. дои : 10.1080/15265160601063969 . ПМИД 17366151 . S2CID 347138 .
- ^ Jump up to: а б с д и ж г Нестлер Э.Дж. (декабрь 2013 г.). «Клеточная основа памяти при наркомании» . Диалоги в клинической неврологии . 15 (4): 431–443. doi : 10.31887/DCNS.2013.15.4/enestler . ПМЦ 3898681 . ПМИД 24459410 .
Несмотря на важность многочисленных психосоциальных факторов, по своей сути наркомания представляет собой биологический процесс.
- ^ Jump up to: а б с Маленка Р.К., Нестлер Э.Дж., Хайман С.Е. (2009). «Глава 15: Подкрепление и аддиктивные расстройства». В Сидоре А., Брауне Р.Ю. (ред.). Молекулярная нейрофармакология: фонд клинической неврологии (2-е изд.). Нью-Йорк: McGraw-Hill Medical. стр. 364–375. ISBN 978-0-07-148127-4 .
- ^ Jump up to: а б «Словарь терминов» . Медицинская школа Маунт-Синай . Кафедра неврологии. Архивировано из оригинала 10 мая 2019 года . Проверено 9 февраля 2015 г.
- ^ Jump up to: а б Шульц В. (июль 2015 г.). «Нейронное вознаграждение и сигналы решения: от теорий к данным» . Физиологические обзоры . 95 (3): 853–951. doi : 10.1152/physrev.00023.2014 . ПМЦ 4491543 . ПМИД 26109341 .
- ^ Фонд исследований мозга и поведения (13 марта 2019 г.). «Биология зависимости». Ютуб.
- ^ Робинсон Т.Е., Берридж К.К. (октябрь 2008 г.). «Обзор. Теория стимулирующей сенсибилизации зависимости: некоторые актуальные проблемы» . Философские труды Лондонского королевского общества. Серия Б, Биологические науки . 363 (1507): 3137–3146. дои : 10.1098/rstb.2008.0093 . ПМК 2607325 . ПМИД 18640920 .
- ^ Jump up to: а б «Расстройство, связанное с употреблением опиоидов» .
- ^ «Отмена (детоксикация) от опиоидов под медицинским наблюдением» . pcssnow.org . 11 июня 2021 г.
- ^ Вайс Р.Д., Поттер Дж.С., Филлин Д.А., Бирн М., Коннери Х.С., Дикинсон В. и др. (декабрь 2011 г.). «Дополнительное консультирование во время кратковременного и длительного лечения бупренорфином-налоксоном при рецептурной опиоидной зависимости: двухфазное рандомизированное контролируемое исследование» . Архив общей психиатрии . 68 (12): 1238–1246. doi : 10.1001/archgenpsychiatry.2011.121 . ПМК 3470422 . ПМИД 22065255 .
- ^ Jump up to: а б Робисон А.Дж., Нестлер Э.Дж. (октябрь 2011 г.). «Транскрипционные и эпигенетические механизмы зависимости» . Обзоры природы. Нейронаука . 12 (11): 623–637. дои : 10.1038/nrn3111 . ПМЦ 3272277 . ПМИД 21989194 .
- ^ Jump up to: а б Олсен CM (декабрь 2011 г.). «Естественные награды, нейропластичность и ненаркотическая зависимость» . Нейрофармакология . 61 (7): 1109–1122. doi : 10.1016/j.neuropharm.2011.03.010 . ПМК 3139704 . ПМИД 21459101 .
- ^ Jump up to: а б Раффл Дж.К. (ноябрь 2014 г.). «Молекулярная нейробиология зависимости: о чем вообще (Δ)FosB?». Американский журнал о злоупотреблении наркотиками и алкоголем . 40 (6): 428–437. дои : 10.3109/00952990.2014.933840 . ПМИД 25083822 . S2CID 19157711 .
- ^ Блюм К., Вернер Т., Карнес С., Карнес П., Боуиррат А., Джордано Дж. и др. (2012). «Секс, наркотики и рок-н-ролл: гипотеза об общей мезолимбической активации как функции полиморфизма гена вознаграждения» . Журнал психоактивных препаратов . 44 (1): 38–55. дои : 10.1080/02791072.2012.662112 . ПМК 4040958 . ПМИД 22641964 .
- ^ Jump up to: а б Бурди Р., Барро М. (ноябрь 2012 г.). «Новый центр управления дофаминергическими системами: тянем ВТА за хвост». Тенденции в нейронауках . 35 (11): 681–690. дои : 10.1016/j.tins.2012.06.007 . ПМИД 22824232 . S2CID 43434322 .
- ^ Jump up to: а б «Морфиновая зависимость – Homo sapiens (человек)» . КЕГГ . Лаборатории Канеиса. 18 июня 2013 года . Проверено 11 сентября 2014 г.
- ^ Jump up to: а б Мистри СиДжей, Бавор М., Десаи Д., Марш Д.С., Самаан З. (май 2014 г.). «Генетика опиоидной зависимости: обзор генетического вклада в опиоидную зависимость» . Текущие обзоры психиатрии . 10 (2): 156–167. дои : 10.2174/1573400510666140320000928 . ПМЦ 4155832 . ПМИД 25242908 .
- ^ Гольдштейн Р.З., Волков Н.Д. (октябрь 2011 г.). «Дисфункция префронтальной коры при зависимости: данные нейровизуализации и клинические последствия» . Обзоры природы. Нейронаука . 12 (11): 652–669. дои : 10.1038/nrn3119 . ПМЦ 3462342 . ПМИД 22011681 .
- ^ Шенбаум Г., Шахам Ю. (февраль 2008 г.). «Роль орбитофронтальной коры при наркозависимости: обзор доклинических исследований» . Биологическая психиатрия . 63 (3): 256–262. doi : 10.1016/j.biopsych.2007.06.003 . ПМК 2246020 . ПМИД 17719014 .
- ^ Ионг Х.Ф., Юань Цзи (1 января 2017 г.). «Нейровизуализация в состоянии покоя и нейропсихологические данные при расстройстве, связанном с употреблением опиоидов во время абстиненции: обзор» . Границы человеческой неврологии . 11 : 169. дои : 10.3389/fnhum.2017.00169 . ПМЦ 5382168 . ПМИД 28428748 .
- ^ Jump up to: а б с д Нестлер Э.Дж. (август 2016 г.). «Размышления о: «Общая роль адаптации G-белков и системы циклического АМФ в опосредовании хронического действия морфина и кокаина на функции нейронов» » . Исследования мозга . 1645 : 71–74. дои : 10.1016/j.brainres.2015.12.039 . ПМЦ 4927417 . ПМИД 26740398 .
В частности, опиаты в нескольких регионах ЦНС, включая NAc, и кокаин, более избирательно в NAc, индуцируют экспрессию определенных изоформ аденилатциклазы и субъединиц PKA через фактор транскрипции, CREB, и эти транскрипционные адаптации выполняют гомеостатическую функцию, противодействуя действию лекарств. В определенных областях мозга, таких как голубое пятно, эти адаптации опосредуют аспекты физической опиатной зависимости и абстиненции, тогда как в NAc они опосредуют толерантность к вознаграждению и зависимость, которая приводит к увеличению самостоятельного приема наркотиков.
- ^ Jump up to: а б «Расстройство, связанное с употреблением опиоидов: диагностические критерии». Диагностическое и статистическое руководство по психическим расстройствам, пятое издание (PDF) . Американская психиатрическая ассоциация. стр. 1–9. Архивировано из оригинала (PDF) 26 ноября 2017 года . Проверено 27 марта 2017 г.
- ^ Варгас-Перес Х., Тинг-А Ки Р., Уолтон Ч.Х., Хансен Д.М., Разави Р., Кларк Л. и др. (июнь 2009 г.). «Вентральная покрышка области BDNF вызывает у наивных крыс состояние вознаграждения, подобное опиатно-зависимому» . Наука . 324 (5935): 1732–1734. Бибкод : 2009Sci...324.1732V . дои : 10.1126/science.1168501 . ПМК 2913611 . ПМИД 19478142 .
- ^ Лавиолетт С.Р., ван дер Кой Д. (март 2001 г.). «рецепторы ГАМК (А) в вентральной покрышке контролируют двунаправленную передачу сигналов вознаграждения между дофаминергическими и недофаминергическими нервными мотивационными системами». Европейский журнал неврологии . 13 (5): 1009–1015. дои : 10.1046/j.1460-9568.2001.01458.x . ПМИД 11264674 . S2CID 46694281 .
- ^ Jump up to: а б с Натт Д., Кинг Л.А., Солсбери В., Блейкмор К. (март 2007 г.). «Разработка рациональной шкалы оценки вреда наркотиков, потенциально злоупотребляемых». Ланцет . 369 (9566): 1047–1053. дои : 10.1016/S0140-6736(07)60464-4 . ПМИД 17382831 . S2CID 5903121 .
- ^ Jump up to: а б с Дик Д.М., Агравал А. (2008). «Генетика алкогольной и другой наркотической зависимости» . Исследования алкоголя и здоровье . 31 (2): 111–118. ПМЦ 3860452 . ПМИД 23584813 .
- ^ Холл Ф.С., Дргонова Дж., Джайн С., Уль Г.Р. (декабрь 2013 г.). «Последствия полногеномных исследований ассоциаций зависимости: все ли наши априорные предположения ошибочны?» . Фармакология и терапия . 140 (3): 267–279. doi : 10.1016/j.pharmthera.2013.07.006 . ПМЦ 3797854 . ПМИД 23872493 .
- ^ Брюль С., Апкариан А.В., Баллантайн Дж.К., Бергер А., Борсук Д., Чен В.Г. и др. (февраль 2013 г.). «Персонализированная медицина и назначение опиоидных анальгетиков при хронической боли: возможности и проблемы» . Журнал боли . 14 (2): 103–113. дои : 10.1016/j.jpain.2012.10.016 . ПМК 3564046 . ПМИД 23374939 .
- ^ Jump up to: а б Хохар Дж.Ю., Фергюсон К.С., Чжу А.З., Тиндейл РФ (2010). «Фармакогенетика лекарственной зависимости: роль вариаций генов в восприимчивости и лечении». Ежегодный обзор фармакологии и токсикологии . 50 : 39–61. doi : 10.1146/annurev.pharmtox.010909.105826 . ПМИД 20055697 . S2CID 2158248 .
- ^ Jump up to: а б Солхауг В., Молден Э. (октябрь 2017 г.). «Индивидуальная вариабельность клинического эффекта и переносимости опиоидных анальгетиков - важность лекарственного взаимодействия и фармакогенетики». Скандинавский журнал боли . 17 : 193–200. дои : 10.1016/j.sjpain.2017.09.009 . ПМИД 29054049 .
- ^ «Руководство CDC по назначению опиоидов при хронической боли | Передозировка наркотиками | Центр травм CDC» . www.cdc.gov . 31 августа 2018 года . Проверено 3 ноября 2018 г.
- ^ Уэйкман С., Ларошель М., Амели О. (2020). «Сравнительная эффективность различных способов лечения расстройств, связанных с употреблением опиоидов» . Открытая сеть JAMA . 3 (2): e1920622. doi : 10.1001/jamanetworkopen.2019.20622 . ПМЦ 11143463 . ПМИД 32022884 . Проверено 15 июля 2024 г.
- ^ Маккарти Д., Прист К.К., Кортуис П.Т. (1 апреля 2018 г.). «Лечение и профилактика расстройств, вызванных употреблением опиоидов: проблемы и возможности» . Ежегодный обзор общественного здравоохранения . 39 (1): 525–541. doi : 10.1146/annurev-publhealth-040617-013526 . ISSN 0163-7525 . ПМК 5880741 . ПМИД 29272165 .
- ^ «Наша приверженность борьбе со злоупотреблением опиоидами | CVS Health» . CVS Здоровье . Проверено 3 ноября 2018 г.
- ^ «Борьба со злоупотреблением опиоидами | Walgreens» . Уолгринс . Проверено 3 ноября 2018 г.
- ^ Jump up to: а б «Налоксон для лечения передозировки опиоидами» (PDF) . США Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) . Проверено 7 ноября 2017 г.
- ^ «Предотвратить расстройство, связанное с употреблением опиоидов | Передозировка наркотиков | Центр травм CDC» . www.cdc.gov . 31 августа 2018 года . Проверено 20 ноября 2018 г.
- ^ Маккарти Д., Прист К.К., Кортуис П.Т. (апрель 2018 г.). «Лечение и профилактика расстройств, вызванных употреблением опиоидов: проблемы и возможности» . Ежегодный обзор общественного здравоохранения . 39 (1): 525–541. doi : 10.1146/annurev-publhealth-040617-013526 . ПМК 5880741 . ПМИД 29272165 .
- ^ «Налоксон» . База данных метаболомов человека – версия 4.0 . 23 октября 2017 г. Проверено 2 ноября 2017 г.
- ^ «Программы профилактики передозировки опиоидами, обеспечивающие налоксоном непрофессионалов — США, 2014 г.» . www.cdc.gov . Проверено 9 марта 2017 г.
- ^ Чайлдс Р. (июль 2015 г.). «Правоохранительная деятельность и использование налоксона в США» (PDF) . США Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) . Коалиция снижения вреда Северной Каролины. стр. 1–24 . Проверено 2 ноября 2017 г.
- ^ «Кейс-стади: Постоянные распоряжения» . НалоксонИнфо.org . Фонды открытого общества. Архивировано из оригинала 7 ноября 2017 года . Проверено 2 ноября 2017 г.
- ^ Jump up to: а б с Шукит М.А. (июль 2016 г.). «Лечение расстройств, связанных с употреблением опиоидов» . Медицинский журнал Новой Англии . 375 (4): 357–368. дои : 10.1056/NEJMra1604339 . ПМИД 27464203 .
- ^ Кристи С., Бейкер С., Купер Р., Кеннеди С.П., Мадрас Б, Бонди Ф.А. Комиссия президента по борьбе с наркоманией и опиоидным кризисом. Вашингтон, округ Колумбия, Типография правительства США, ноябрь 2017 г.;1.
- ^ «Лекарственное средство для устранения передозировки опиоидами налоксона» . CVS Здоровье . Проверено 4 февраля 2019 г.
- ^ Jump up to: а б Морин К.А., Войтесек Ф., Ачарья С., Дабус-младший, Марш, округ Колумбия (октябрь 2021 г.). «Доказательства увеличения стандартизованного по возрасту и полу уровня смертности среди людей, которые обращались к лечению опиоидными агонистами до эры синтетических опиоидов в Онтарио, Канада» . Куреус . 13 (10): e19051. дои : 10.7759/cureus.19051 . ПМЦ 8608679 . ПМИД 34853762 .
- ^ Хсер Й.И., Хоффман В., Грелла К.Э., Энглин, доктор медицинских наук (май 2001 г.). «33-летнее наблюдение за наркоманами». Архив общей психиатрии . 58 (5): 503–508. дои : 10.1001/archpsyc.58.5.503 . ПМИД 11343531 .
- ^ Хорон И.Л., Сингал П., Фаулер Д.Р., Шарфштейн Дж.М. (июнь 2018 г.). «Стандартные свидетельства о смерти в сравнении с усиленным надзором для выявления случаев смерти, связанных с передозировкой героина» . Американский журнал общественного здравоохранения . 108 (6): 777–781. дои : 10.2105/ajph.2018.304385 . ПМЦ 5944879 . ПМИД 29672148 .
- ^ «Опиоидные анальгетики, сдерживающие злоупотребление» . Центр оценки и исследования лекарственных средств . Управление по контролю за продуктами и лекарствами США. 2 марта 2021 г.
- ^ Амато Л., Даволи М., Миноцци С., Феррони Э., Али Р., Ферри М. (февраль 2013 г.). «Метадон в сниженных дозах для лечения синдрома отмены опиоидов» . Кокрановская база данных систематических обзоров . 2013 (2): CD003409. дои : 10.1002/14651858.CD003409.pub4 . ПМК 7017622 . ПМИД 23450540 .
- ^ Макартур Г.Дж., ван Вельцен Э., Палматир Н., Кимбер Дж., Фаррис А., Хоуп В. и др. (январь 2014 г.). «Вмешательства по профилактике ВИЧ и гепатита С у людей, употребляющих инъекционные наркотики: обзор обзоров для оценки доказательств эффективности». Международный журнал по наркополитике . 25 (1): 34–52. дои : 10.1016/j.drugpo.2013.07.001 . ПМИД 23973009 .
- ^ Нильсен С., Це В.К., Ларанс Б. и др. (Кокрейновская группа по наркотикам и алкоголю) (сентябрь 2022 г.). «Лечение опиоидными агонистами людей, страдающих зависимостью от фармацевтических опиоидов» . Кокрановская база данных систематических обзоров . 2022 (9): CD011117. дои : 10.1002/14651858.CD011117.pub3 . ПМЦ 9443668 . ПМИД 36063082 .
- ^ «Опиоидная заместительная терапия или лечение (ОЗТ)» . Миграция и внутренние дела . Европейская комиссия. 14 марта 2017 г.
- ^ Jump up to: а б с д и ж г час я Ричард П. Мэттик и др.: Национальная оценка фармакотерапии опиоидной зависимости (NEPOD): отчет о результатах и рекомендации
- ^ Уилан П.Дж., Ремски К. (январь 2012 г.). «Лечение бупренорфином и метадоном: обзор фактических данных как в развитых, так и в развивающихся странах» . Журнал нейронаук в сельской практике . 3 (1): 45–50. дои : 10.4103/0976-3147.91934 . ПМК 3271614 . ПМИД 22346191 .
- ^ Мартин Дж.А., Кэмпбелл А., Киллип Т., Коц М., Кранц М.Дж., Крик М.Дж. и др. (октябрь 2011 г.). «Скрининг интервала QT при поддерживающем лечении метадоном: отчет экспертной группы SAMHSA» . Журнал аддиктивных заболеваний . 30 (4): 283–306. дои : 10.1080/10550887.2011.610710 . ПМК 4078896 . ПМИД 22026519 .
- ^ https://www.bccsu.ca/wp-content/uploads/2023/11/BC-OUD-Treatment-Guideline_2023-Update.pdf [ только URL-адрес PDF ]
- ^ «Лекарства MAT, консультирование и связанные с ними состояния» . www.samhsa.gov . Проверено 10 ноября 2022 г.
- ^ «Метадон» . www.samhsa.gov . Проверено 10 ноября 2022 г.
- ^ Jump up to: а б с «Отмена отказа (Закон MAT)» . 10 января 2023 г.
- ^ Jump up to: а б «Медикаментозное лечение (МАТ)» . www.samhsa.gov . Проверено 9 ноября 2022 г.
- ^ Гоуинг Л., Фаррелл М., Али Р., Уайт Дж. М. (май 2016 г.). «Альфа₂-адренергические агонисты для лечения синдрома отмены опиоидов» . Кокрановская база данных систематических обзоров . 2016 (5): CD002024. дои : 10.1002/14651858.CD002024.pub5 . ПМК 7081129 . ПМИД 27140827 .
- ^ Михельс II, Стёвер Х, Герлах Р. (февраль 2007 г.). «Заместительная терапия для опиоидных наркоманов в Германии» . Журнал снижения вреда . 4 (1): 5. дои : 10.1186/1477-7517-4-5 . ПМК 1797169 . ПМИД 17270059 .
- ^ «Многие больничные правила создают препятствия для эффективного лечения синдрома отмены опиоидов» . Доказательства НИХР . 16 ноября 2022 г. doi : 10.3310/nihrevidence_54639 . S2CID 253608569 .
- ^ Харрис М., Холланд А., Льюер Д., Браун М., Иствуд Н., Саттон Г. и др. (апрель 2022 г.). «Барьеры на пути отмены опиоидов в больницах Англии: анализ документов больничной политики по лечению зависимости от психоактивных веществ» . БМК Медицина . 20 (1): 151. дои : 10.1186/s12916-022-02351-y . ПМЦ 9007696 . ПМИД 35418095 .
- ^ Боном Дж., Шим Р.С., Гуден Р., Тайус Д., Раст Дж. (июль 2012 г.). «Опиоидная зависимость и злоупотребление ими в практике первичной медико-санитарной помощи: сравнение метадона и бупренорфина как вариантов лечения» . Журнал Национальной медицинской ассоциации . 104 (7–8): 342–350. дои : 10.1016/S0027-9684(15)30175-9 . ПМК 4039205 . ПМИД 23092049 .
- ^ Орман Дж.С., Китинг Г.М. (2009). «Бупренорфин/налоксон: обзор его использования при лечении опиоидной зависимости». Наркотики . 69 (5): 577–607. дои : 10.2165/00003495-200969050-00006 . ПМИД 19368419 . S2CID 209147406 .
- ^ «Бупренорфин» . www.samhsa.gov . Проверено 10 ноября 2022 г.
- ^ Йокелл М.А., Заллер Н.Д., Грин Т.К., Рич Дж.Д. (март 2011 г.). «Утечка, неправильное и незаконное использование бупренорфина и бупренорфина/налоксона: международный обзор» . Текущие обзоры злоупотребления наркотиками . 4 (1): 28–41. дои : 10.2174/1874473711104010028 . ПМК 3154701 . ПМИД 21466501 .
- ^ «Лекарства от расстройств, вызванных употреблением опиоидов – Протокол улучшения лечения 63» . Администрация служб по борьбе со злоупотреблением психоактивными веществами и психическим здоровьем . Проверено 20 ноября 2018 г. [ постоянная мертвая ссылка ]
- ^ «Что такое бупренорфин? | Институт психиатрических исследований UAMS» . psychiatry.uams.edu/ . Проверено 17 ноября 2022 г.
- ^ Jump up to: а б с д Кёль Дж.Л., Циммерман Д.Э., Бриджман П.Дж. (июль 2019 г.). «Лекарства для лечения расстройств, связанных с употреблением опиоидов». Американский журнал аптеки системы здравоохранения . 76 (15): 1097–1103. дои : 10.1093/ajhp/zxz105 . ПМИД 31361869 .
- ^ «Субутекс и субоксон одобрены для лечения опиатной зависимости» . США Управление по контролю за продуктами и лекарствами (FDA). 8 октября 2002 года . Проверено 1 ноября 2014 г.
- ^ «История одобрения субблокада (бупренорфин) FDA» . Наркотики.com . Проверено 10 ноября 2022 г.
- ^ «Краткое руководство по применению бупренорфина SAMHSA» (PDF) .
- ^ Вонг Дж.С., Нику М., Вестенберг Дж.Н., Суен Дж.Г., Вонг Дж.Ю., Крауш Р.М. и др. (февраль 2021 г.). «Сравнение быстрой микроиндукции и стандартной индукции бупренорфина/налоксона для лечения расстройств, связанных с употреблением опиоидов: протокол открытого рандомизированного контролируемого исследования в параллельных группах превосходства» . Наука о зависимостях и клиническая практика . 16 (1): 11. дои : 10.1186/s13722-021-00220-2 . ПМЦ 7881636 . ПМИД 33579359 .
- ^ "До настоящего времени" .
- ^ «О лечении опиоидной зависимости» .
- ^ «Департамент здравоохранения и ресурсов Западной Вирджинии_Бюро медицинских услуг_Метадон» (PDF) .
- ^ «Побочные эффекты метадона: распространенные, тяжелые, долгосрочные» . Наркотики.com . Проверено 10 ноября 2022 г.
- ^ Jump up to: а б «Информация о назначении вивитрола» (PDF) . Alkermes Inc., июль 2013 г. Архивировано из оригинала (PDF) 10 февраля 2017 г. . Проверено 2 ноября 2017 г.
- ^ Сколник П. (январь 2018 г.). «Опиоидная эпидемия: кризис и пути решения» . Ежегодный обзор фармакологии и токсикологии . 58 (1): 143–159. doi : 10.1146/annurev-pharmtox-010617-052534 . ПМИД 28968188 .
- ^ Салливан М.А., Гарави Ф., Бисага А., Комер С.Д., Карпентер К., Раби В.Н. и др. (декабрь 2007 г.). «Лечение рецидивов терапии налтрексоном при героиновой зависимости» . Наркотическая и алкогольная зависимость . 91 (2–3): 289–292. doi : 10.1016/j.drugalcdep.2007.06.013 . ПМЦ 4153601 . ПМИД 17681716 .
- ^ Центр лечения наркозависимости (2009). Глава 4. Налтрексон для перорального применения . Администрация служб по борьбе со злоупотреблением психоактивными веществами и психическим здоровьем (США).
- ^ Далсбё Т.К., Стейро А.К., Хаммерстрем К.Т., Смедслунд Г. (2010). Поддержка героина для лиц с хронической героиновой зависимостью (Отчет). Осло, Норвегия: Центр знаний по службам здравоохранения при Норвежском институте общественного здравоохранения. ПМИД 29320074 .
- ^ Ферри М., Даволи М., Перуччи Калифорния (декабрь 2011 г.). «Поддержка героина для лиц с хронической героиновой зависимостью» . Кокрановская база данных систематических обзоров . 2011 (12): CD003410. дои : 10.1002/14651858.CD003410.pub4 . ПМК 7017638 . ПМИД 22161378 . S2CID 6772720 .
- ^ Рем Дж., Гшвенд П., Штеффен Т., Гуцвиллер Ф., Доблер-Микола А., Ухтенхаген А. (октябрь 2001 г.). «Осуществимость, безопасность и эффективность назначения инъекционного героина рефрактерным опиоидным наркоманам: последующее исследование». Ланцет . 358 (9291): 1417–1423. дои : 10.1016/S0140-6736(01)06529-1 . ПМИД 11705488 . S2CID 24542893 .
- ^ «Лечение героином | Альянс по наркополитике» . Архивировано из оригинала 16 марта 2016 года . Проверено 4 марта 2016 г.
- ^ Робертсон-младший, Рааб GM, Брюс М., Маккензи Дж.С., Сторки HR, Солтер А. (декабрь 2006 г.). «Рассмотрение эффективности дигидрокодеина по сравнению с метадоном как альтернативного поддерживающего лечения опиатной зависимости: рандомизированное контролируемое исследование». Зависимость . 101 (12): 1752–1759. дои : 10.1111/j.1360-0443.2006.01603.x . ПМИД 17156174 .
- ^ «Дигидрокодеин» . Пубчем .
- ^ "Авторизоваться" . online.lexi.com . Проверено 2 ноября 2018 г.
- ^ Карни Т., Ван Хаут MC, Норман I, Дада С., Зигфрид Н., Парри CD (февраль 2020 г.). «Дигидрокодеин для детоксикации и поддерживающего лечения у лиц с расстройствами, вызванными употреблением опиатов» . Кокрановская база данных систематических обзоров . 2 (2): CD012254. дои : 10.1002/14651858.CD012254.pub2 . ПМК 7027221 . ПМИД 32068247 .
- ^ Ферри М., Миноцци С., Бо А., Амато Л. (июнь 2013 г.). «Пероральный морфин медленного высвобождения в качестве поддерживающей терапии при опиоидной зависимости». Кокрейновская база данных систематических обзоров (6): CD009879. дои : 10.1002/14651858.CD009879.pub2 . ПМИД 23740540 .
- ^ «Федеральное управление общественного здравоохранения – Заместительная терапия диацетилморфином (героином)» . Архивировано из оригинала 13 марта 2016 года.
- ^ Тран Т.Х., Гриффин Б.Л., Стоун Р.Х., Вест К.М., Тодд Т.Дж. (июль 2017 г.). «Метадон, бупренорфин и налтрексон для лечения расстройств, связанных с употреблением опиоидов, у беременных». Фармакотерапия . 37 (7). Уайли: 824–839. дои : 10.1002/фар.1958 . ПМИД 28543191 . S2CID 13772333 .
- ^ Зедлер Б.К., Манн А.Л., Ким М.М., Амик Х.Р., Джойс А.Р., Муррелл Э.Л. и др. (декабрь 2016 г.). «Бупренорфин по сравнению с метадоном для лечения беременных женщин с расстройством, вызванным употреблением опиоидов: систематический обзор и метаанализ безопасности для матери, плода и ребенка» . Зависимость . 111 (12): 2115–2128. дои : 10.1111/add.13462 . ПМК 5129590 . ПМИД 27223595 .
- ^ Кинселла М., Холлидей Л.О., Шоу М., Кейпел Ю., Нельсон С.М., Кернс Р.Дж. (29 июля 2022 г.). «Бупренорфин по сравнению с метадоном при беременности: систематический обзор и метаанализ» . Употребление и злоупотребление психоактивными веществами . 57 (9): 1400–1416. дои : 10.1080/10826084.2022.2083174 . PMID 35758300 .
- ^ Jump up to: а б Суарес Э.А., Хайбрехтс К.Ф., Штрауб Л., Эрнандес-Диас С. , Джонс Х.Э., Коннери Х.С. и др. (декабрь 2022 г.). «Бупренорфин в сравнении с метадоном при расстройствах, связанных с употреблением опиоидов во время беременности» . Медицинский журнал Новой Англии . 387 (22): 2033–2044. дои : 10.1056/NEJMoa2203318 . ПМЦ 9873239 . ПМИД 36449419 .
- ^ Мейер MC, Джонстон AM, Крокер AM, Хайль Ш.Х. (2015). «Метадон и бупренорфин при опиоидной зависимости во время беременности: ретроспективное когортное исследование» . Журнал наркологии . 9 (2): 81–86. doi : 10.1097/ADM.0000000000000092 . ПМЦ 4375023 . ПМИД 25622120 .
- ^ Jump up to: а б с д и ж Карли Дж.А., Остерле Т. (3 июня 2021 г.). «Терапевтические подходы к расстройствам, связанным с употреблением опиоидов: каковы современные стандарты лечения?» . Международный журнал общей медицины . 14 : 2305–2311. дои : 10.2147/IJGM.S295461 . ПМЦ 8184146 . ПМИД 34113160 .
- ^ Дугош К., Абрахам А., Сеймур Б., Маклойд К., Чок М., Фестингер Д. (март – апрель 2016 г.). «Систематический обзор использования психосоциальных вмешательств в сочетании с лекарствами для лечения опиоидной зависимости» . Журнал наркологии . 10 (2): 93–103. doi : 10.1097/ADM.0000000000000193 . ПМК 4795974 . ПМИД 26808307 .
- ^ Бек Дж.С. (18 августа 2011 г.). Когнитивно-поведенческая терапия: основы и не только (второе изд.). Нью-Йорк: Гилфорд Пресс. стр. 19–20. ISBN 978-1-60918-504-6 . OCLC 698332858 .
- ^ Хейберс М.Дж., Берскенс А.Дж., Блейенберг Г., ван Шайк К.П. (июль 2007 г.). «Психосоциальные вмешательства врачей общей практики» . Кокрановская база данных систематических обзоров . 2007 (3): CD003494. дои : 10.1002/14651858.CD003494.pub2 . hdl : 2066/52984 . ПМЦ 7003673 . ПМИД 17636726 .
- ^ Jump up to: а б с д Кэрролл К.М., Онкен Л.С. (август 2005 г.). «Поведенческая терапия наркозависимости» . Американский журнал психиатрии . 162 (8): 1452–1460. дои : 10.1176/appi.ajp.162.8.1452 . ПМЦ 3633201 . ПМИД 16055766 .
- ^ Василаки Э.И., Хозиер С.Г., Кокс В.М. (май 2006 г.). «Эффективность мотивационного интервью как краткосрочного вмешательства при чрезмерном употреблении алкоголя: метааналитический обзор» . Алкоголь и алкоголизм . 41 (3): 328–335. дои : 10.1093/alcalc/agl016 . ПМИД 16547122 .
- ^ «Психосоциальные вмешательства при расстройствах, связанных с употреблением опиоидов» . До настоящего времени . Проверено 2 ноября 2017 г.
- ^ Дутра Л., Статопулу Дж., Басден С.Л., Лейро Т.М., Пауэрс М.Б., Отто М.В. (февраль 2008 г.). «Метааналитический обзор психосоциальных вмешательств при расстройствах, связанных с употреблением психоактивных веществ». Американский журнал психиатрии . 165 (2): 179–187. дои : 10.1176/appi.ajp.2007.06111851 . ПМИД 18198270 . S2CID 29327821 .
- ^ Мелемис С.М. (сентябрь 2015 г.). «Профилактика рецидивов и пять правил выздоровления» . Йельский журнал биологии и медицины . 88 (3): 325–332. ПМЦ 4553654 . ПМИД 26339217 .
- ^ Сассман С. (март 2010 г.). «Обзор программ Анонимных Алкоголиков/Анонимных Наркоманов для подростков» . Оценка и профессии здравоохранения . 33 (1): 26–55. дои : 10.1177/0163278709356186 . ПМК 4181564 . ПМИД 20164105 .
- ^ Галантер М (28 октября 2016 г.). «Сочетание медикаментозного лечения и программы Двенадцати шагов: взгляд и обзор» . Американский журнал о злоупотреблении наркотиками и алкоголем . 44 (2): 151–159. дои : 10.1080/00952990.2017.1306747 . ПМИД 28387530 .
- ^ Гэмбл Дж., О'Лоуренс Х. (лето 2016 г.). «Обзор эффективности 12-ступенчатой групповой терапии для лечения наркозависимости». Журнал управления здравоохранением и социальными службами . 39 (1): 142–160. дои : 10.1177/107937391603900108 . ПМИД 27483978 .
- ^ Jump up to: а б Донован Д.М., Ингалсбе М.Х., Бенбоу Дж., Дейли, округ Колумбия (26 августа 2013 г.). «12-шаговые вмешательства и программы взаимной поддержки при расстройствах, связанных с употреблением психоактивных веществ: обзор» . Социальная работа в здравоохранении . 28 (3–4): 313–332. дои : 10.1080/19371918.2013.774663 . ПМЦ 3753023 . ПМИД 23731422 .
- ^ Уорд Х.Б., Москера М.Дж., Сузуки Дж., Мариано Т.И. (апрель 2020 г.). «Систематический обзор неинвазивной стимуляции мозга при расстройствах, связанных с употреблением опиоидов». Нейромодуляция . 23 (3): 301–311. дои : 10.1111/ner.13108 . ПМИД 32059080 . S2CID 211122521 .
- ^ Янг Дж.Р., Смани С.А., Мишель Н.А., Критцер М.Д., Аппельбаум Л.Г., Паткар А.А. (апрель – июнь 2020 г.). «Неинвазивные методы стимуляции мозга для лечения и профилактики расстройств, связанных с употреблением опиоидов: систематический обзор литературы». Журнал аддиктивных заболеваний . 38 (2): 186–199. дои : 10.1080/10550887.2020.1736756 . ПМИД 32469286 . S2CID 216247971 .
- ^ Jump up to: а б Кёк П., Фрёлих К., Вальтер М., Ланг У., Дюрстелер К.М. (июль 2022 г.). «Систематический обзор литературы клинических испытаний и терапевтического применения ибогаина». Журнал лечения наркозависимости . 138 : 108717. doi : 10.1016/j.jsat.2021.108717 . ПМИД 35012793 .
- ^ Салливан К. (24 января 2023 г.). «Психоделический ибогаин может лечить зависимость. Гонка за прибылью продолжается» . Хранитель .
- ^ Пассмор Дж. (26 июня 2024 г.). «Революционное устройство для лечения расстройств, вызванных употреблением опиоидов, из Кентукки, получило одобрение FDA» . www.wkyt.com . Проверено 29 июня 2024 г.
- ^ «Клинические испытания медицинского устройства могут оказаться достойной альтернативой лекарствам для воздержания от опиоидов» . Новости медицинского факультета . 8 марта 2019 года . Проверено 29 июня 2024 г.
- ^ Хоффман К.А., Терашима Дж.П., Маккарти Д. (25 ноября 2019 г.). «Расстройство, связанное с употреблением опиоидов, и его лечение: проблемы и возможности» (PDF) . Исследование услуг здравоохранения BMC . 19 (1): 884. doi : 10.1186/s12913-019-4751-4 . ПМК 6876068 . ПМИД 31767011 .
- ^ Сигмон СК (1 апреля 2014 г.). «Доступ к лечению опиоидной зависимости в сельской Америке: проблемы и будущие направления» . JAMA Психиатрия . 71 (4): 359–360. doi : 10.1001/jamapsychiatry.2013.4450 . ISSN 2168-622X . ПМИД 24500040 .
- ^ Килюк Б.Д., Клейкамп Б.А., Комер С.Д., Гриффитс Р.Р., Хун А.С., Джонсон М.В. и др. (1 января 2023 г.). «Проблемы дизайна клинических исследований и возможности новых методов лечения расстройств, вызванных употреблением опиоидов. Обзор» . JAMA Психиатрия . 80 (1): 84–92. doi : 10.1001/jamapsychiatry.2022.4020 . ISSN 2168-622X . ПМЦ 10297827 . ПМИД 36449315 .
- ^ «Одна таблетка может убить» . Управление по борьбе с наркотиками США . Архивировано из оригинала 15 ноября 2023 года . Проверено 15 ноября 2023 г.
- ^ «ВОЗ | Информационный бюллетень о передозировке опиоидами» . ВОЗ . Проверено 6 апреля 2019 г.
- ^ Jump up to: а б Ван Х., Нагави М., Аллен С., Барбер Р.М., Бхутта З.А., Картер А. и др. (октябрь 2016 г.). «Глобальная, региональная и национальная продолжительность жизни, смертность от всех причин и смертность от конкретных причин по 249 причинам смерти, 1980-2015 гг.: систематический анализ для исследования глобального бремени болезней 2015 г.» . Ланцет . 388 (10053): 1459–1544. дои : 10.1016/S0140-6736(16)31012-1 . ПМЦ 5388903 . ПМИД 27733281 .
{{cite journal}}: CS1 maint: переопределенная настройка ( ссылка ) - ^ Jump up to: а б «Глобальная, региональная и национальная смертность от всех причин и по конкретным причинам в разбивке по возрасту и по конкретным причинам по 240 причинам смерти, 1990–2013 гг.: систематический анализ для исследования глобального бремени болезней, 2013 г.» . Ланцет . 385 (9963): 117–171. Январь 2015 г. doi : 10.1016/S0140-6736(14)61682-2 . ПМК 4340604 . ПМИД 25530442 .
- ^ Jump up to: а б «Понимание эпидемии передозировки опиоидами» . cdc.gov . 8 августа 2023 г.
- ^ Jump up to: а б с Анализ данных и ресурсы по опиоидам. Передозировка наркотиками. Центр травм CDC . Центры по контролю и профилактике заболеваний . Нажмите на вкладку «Рост ставок», чтобы увидеть график. См. таблицу данных под графиком.
- ^ Jump up to: а б Американское общество наркологии. «Опиоидная зависимость, 2016 г.: факты и цифры» (PDF) .
- ^ Здоровье, США, 2016 г.: Со схемой долгосрочных тенденций в области здравоохранения (PDF) . Хаяттсвилл, Мэриленд: CDC, Национальный центр статистики здравоохранения. 2017. с. 4.
- ^ Хемпстед К., Йилдирим Э.О. (июнь 2014 г.). «Реакция со стороны предложения на снижение чистоты героина: эпизод передозировки фентанила в Нью-Джерси». Экономика здравоохранения . 23 (6): 688–705. дои : 10.1002/гек.2937 . ПМИД 23740651 .
- ^ Jump up to: а б Чиккароне Д. (июль 2021 г.). «Рост запрещенных фентанилов, стимуляторов и четвертая волна кризиса передозировки опиоидами» . Современное мнение в психиатрии . 34 (4): 344–350. дои : 10.1097/YCO.0000000000000717 . ПМЦ 8154745 . ПМИД 33965972 .
- ^ Манчиканти Л., Сингх В.М., Стаатс П.С., Трескот А.М., Прунскис Дж., Кнежевич Н.Н. и др. (март 2022 г.). «Четвертая волна смертей от передозировки опиоидов (незаконных наркотиков) и сокращение доступа к рецептурным опиоидам и интервенционным методам: причина и следствие». Врач боли . 25 (2): 97–124. ПМИД 35322965 .
- ^ Jump up to: а б Фридман Дж., Шовер К.Л. (декабрь 2023 г.). «Составление диаграммы четвертой волны: географические, временные, расовые/этнические и демографические тенденции в смертности от передозировки поливеществами фентанилом в Соединенных Штатах, 2010–2021 годы» . Зависимость . 118 (12): 2477–2485. дои : 10.1111/доп.16318 . ПМИД 37705148 .
- ^ Jump up to: а б Отдел цифровых коммуникаций (8 мая 2018 г.). «Стратегия из 5 пунктов по борьбе с опиоидным кризисом» . Министерство здравоохранения и социальных служб США . Проверено 2 ноября 2018 г.
- ^ «Стратегия борьбы с опиоидами, злоупотреблением, неправильным употреблением и передозировкой» (PDF) . Министерство здравоохранения и социальных служб США . Проверено 18 ноября 2018 г.
- ^ Jump up to: а б «Данные о передозировке рецептурных опиоидов» . Центр по контролю и профилактике заболеваний . Проверено 12 сентября 2016 г.
- ^ Jump up to: а б Паулоцци Л. (12 апреля 2012 г.). «Популяции, подверженные риску передозировки опиоидов» (PDF) . США Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) . Отдел предотвращения непреднамеренных травм, Национальный центр профилактики и контроля травматизма, Центры по контролю и профилактике заболеваний . Проверено 12 сентября 2016 г.
- ^ «Опиоидная зависимость: факты и цифры 2016 г.» (PDF) . Американское общество наркологии . Проверено 12 сентября 2016 г.
- ^ Jump up to: а б «Насколько серьезна опиоидная эпидемия?» . ПБС . Проверено 12 сентября 2016 г.
- ^ Jump up to: а б Хан Б., Полидору С., Феррис Р., Блаум К.С., Росс С., Макнили Дж. (10 ноября 2015 г.). «Демографические тенденции среди взрослых в программах лечения опиоидами города Нью-Йорка - старение населения». Употребление и злоупотребление психоактивными веществами . 50 (13): 1660–1667. дои : 10.3109/10826084.2015.1027929 . ПМИД 26584180 . S2CID 5520930 .
- ^ «Факты и лица опиоидной зависимости: новые идеи» . Управление здоровьем MAP . 2015. Архивировано из оригинала 29 февраля 2020 года . Проверено 12 сентября 2016 г.
- ^ «Опиоиды» . Администрация служб по борьбе со злоупотреблением психоактивными веществами и психическим здоровьем . 23 февраля 2016 года. Архивировано из оригинала 12 сентября 2016 года . Проверено 12 сентября 2016 г.
- ^ ДеВенсентис П. (24 июля 2017 г.). «Внук продал холодильник за наркотики, — говорит бабушка» . США сегодня .
- ^ Петерман Н.Дж., Палсгаард П., Ваши А., Ваши Т., Каптур Б.Д., Йео Э. и др. (май 2022 г.). «Демографический и геопространственный анализ частоты выписывания рецептов на бупренорфин и метадон» . Куреус . 14 (5): e25477. дои : 10.7759/cureus.25477 . ПМЦ 9246456 . ПМИД 35800815 .
- ^ «Использование телемедицины при проведении медикаментозного лечения (MAT)» (PDF) . САМХСА . 15 мая 2018 года . Проверено 15 мая 2018 г.
- ^ Нуньес Е.В., Левин Ф.Р., Рейли член парламента, Эль-Бассель Н. (март 2021 г.). «Медикаментозное лечение расстройств, вызванных употреблением опиоидов, в эпоху COVID-19: могут ли новые правила изменить опиоидный каскад?» . Журнал лечения наркозависимости . 122 : 108196. doi : 10.1016/j.jsat.2020.108196 . ПМК 7666540 . ПМИД 33221125 .
- ^ «Хочул подписывает пакет законов по борьбе с опиоидным кризисом» .
- ^ «Нью-Йорк декриминализует хранение шприцев в рамках усилий по предотвращению передозировки» . 7 октября 2021 г.
- ^ «Продукты – быстрый выпуск статистики естественного движения населения – предварительные данные о передозировке наркотиками» . 4 ноября 2021 г.
- ^ Jump up to: а б «Уровень смертности от передозировки» . Национальный институт по борьбе со злоупотреблением наркотиками . 20 января 2022 г. Проверено 10 ноября 2022 г.
- ^ Jump up to: а б с д Смертность от передозировки . Национальный институт по борьбе со злоупотреблением наркотиками (NIDA).
- ^ Сколник П. (май 2022 г.). «Лечение передозировки в эпоху синтетических опиоидов» . Фармакология и терапия . 233 : 108019. doi : 10.1016/j.pharmthera.2021.108019 . ПМИД 34637841 .
- ^ Jump up to: а б Гомес Т., Ледли С., Тадроус М., Мамдани М., Патерсон Дж.М., Юурлинк Д.Н. (июль 2023 г.). «Тенденции смертности, связанной с опиоидной токсичностью, в США до и после начала пандемии COVID-19, 2011–2021 гг.» . Открытая сеть JAMA . 6 (7): e2322303. doi : 10.1001/jamanetworkopen.2023.22303 . ПМЦ 10329206 . ПМИД 37418260 .
- ^ «Качественная оценка обстоятельств смерти от передозировки наркотиков на ранних стадиях пандемии COVID-19» . cdc.gov . Август 2022.
- ^ Симха С., Ахмед Ю., Брамметт К.М., Уолджи Дж.Ф., Энглсби М.Дж., Бикет М.К. (январь 2023 г.). «Влияние пандемии COVID-19 на передозировку опиоидов и другие побочные эффекты в США и Канаде: систематический обзор». Регионарная анестезия и медицина боли . 48 (1): 37–43. дои : 10.1136/rapm-2022-103591 . ПМИД 36202619 . S2CID 252753865 .
- ^ Джонс СМ, Шофф С, Бланко С, Лосби Дж. Л., Линг С. М., Комптон В. М. (май 2023 г.). «Ассоциация получения телемедицинских услуг, связанных с расстройствами, связанными с употреблением опиоидов, и лекарств от расстройств, связанных с употреблением опиоидов, со смертельными передозировками наркотиков среди получателей медицинской помощи до и во время пандемии COVID-19» . JAMA Психиатрия . 80 (5): 508–514. doi : 10.1001/jamapsychiatry.2023.0310 . ПМЦ 10061313 . ПМИД 36988913 .
- ^ Моран К.М., Маллачери П.Х., Ланкенау С., Билал У. (июль 2022 г.). «Изменения расовых/этнических различий в результатах употребления опиоидов в городских районах во время пандемии COVID-19: быстрый обзор литературы» . Международный журнал экологических исследований и общественного здравоохранения . 19 (15): 9283. doi : 10.3390/ijerph19159283 . ПМЦ 9368442 . ПМИД 35954640 .
- ^ «Назначение контролируемых веществ посредством телемедицины» . 16 октября 2023 г.
- ^ Хайдбредер С., Фудала П.Дж., Гринвальд М.К. (2023). «История открытия, разработки и одобрения FDA препаратов бупренорфина для лечения расстройств, связанных с употреблением опиоидов» . Отчеты о наркотической и алкогольной зависимости . 6 . дои : 10.1016/j.dadr.2023.100133 . ПМЦ 10040330 . ПМИД 36994370 .
- ^ Джеймс В. Калат, Биологическая психология . Cengage Обучение. Страница 81.
- ^ EMEA, 19 апреля 2001 г. Публичное заявление EMEA о рекомендации приостановить действие регистрационного удостоверения для Орлаама (левацетилметадол) в Европейском Союзе. Архивировано 4 февраля 2017 г. на Wayback Machine.
- ^ «Орлаам (левометадилацетат гидрохлорид)» . Предупреждения FDA о безопасности . Управление по контролю за продуктами и лекарствами США. 20 августа 2013 г. Архивировано из оригинала 18 января 2017 г.
Дальнейшее чтение
[ редактировать ]- Браун Т.К., Альпер К. (2018). «Лечение расстройства, связанного с употреблением опиоидов, ибогаином: результаты детоксикации и употребления наркотиков» . Американский журнал о злоупотреблении наркотиками и алкоголем . 44 (1): 24–36. дои : 10.1080/00952990.2017.1320802 . ПМИД 28541119 . S2CID 4401865 .
- Соседи CJ, Чой С., Хили С., Ернени Р., Сан Т., Шаповал Л. (июнь 2019 г.). «Применение возрастных препаратов для лечения зависимости (MAT) при расстройствах, связанных с употреблением опиоидов, среди пациентов, застрахованных Medicaid, в Нью-Йорке» . Лечение, профилактика и политика злоупотребления психоактивными веществами . 14 (1): 28. дои : 10.1186/s13011-019-0215-4 . ПМК 6593566 . ПМИД 31238952 .
- Сибра П., Секейра А., Филипе Ф., Амарал П., Симойнс А., Секейра Р. (июнь 2022 г.). «Последствия наркозависимости: показатели тяжести амбулаторных пациентов в рамках медикаментозной программы». Международный журнал психического здоровья и наркомании . 20 (3): 1837–1853. дои : 10.1007/s11469-021-00485-3 .
![Ежегодная смертность в США от всех опиоидных наркотиков. В это число входят опиоидные анальгетики, а также героин и запрещенные синтетические опиоиды.[196]](http://upload.wikimedia.org/wikipedia/commons/thumb/c/cb/NIDA_overdose_deaths.png/467px-NIDA_overdose_deaths.png)
![Ежегодная смертность в США по категориям наркотиков[196]](http://upload.wikimedia.org/wikipedia/commons/thumb/8/84/NIDA_overdose_all.png/501px-NIDA_overdose_all.png)
![Ежегодная смертность от передозировки опиоидов в США, связанная с рецептурными опиоидами. Неметадоновые синтетические вещества представляют собой категорию, в которой доминирует незаконно приобретенный фентанил, и поэтому они были исключены.[197]](http://upload.wikimedia.org/wikipedia/commons/thumb/b/b3/NIDA_overdose_prescription.png/454px-NIDA_overdose_prescription.png)
![Ежегодная смертность от передозировки опиоидами, включающими героин, в США[197]](http://upload.wikimedia.org/wikipedia/commons/thumb/9/92/NIDA_overdose_heroin.png/439px-NIDA_overdose_heroin.png)
![Ежегодная смертность от передозировки опиоидов в США, включающая психостимуляторы (в первую очередь метамфетамин)[197]](http://upload.wikimedia.org/wikipedia/commons/thumb/7/78/NIDA_overdose_stimulants.png/451px-NIDA_overdose_stimulants.png)