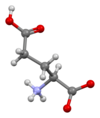
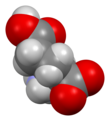
Глутаминовая кислота
 Скелетная формула кислоты L -глютаминовой
| |||
| |||

| |||
| Имена | |||
|---|---|---|---|
| Имя IUPAC
Глутаминовая кислота
| |||
| Систематическое имя IUPAC
2-аминопентановая кислота | |||
Другие имена
| |||
| Идентификаторы | |||
3D model ( JSmol )
|
| ||
| 3dmet |
| ||
| 1723801 (L) 1723799 (RAC) 1723800 (D) | |||
| Чеби |
| ||
| Химический |
| ||
| Chemspider |
| ||
| Наркоман | |||
| Echa Infocard | 100.009.567 | ||
| ЕС номер |
| ||
| E номер | E620 (энхансер вкуса) | ||
| 3502 (L) 101971 (RAC) 201189 (D) | |||
| Кегг | |||
PubChem CID
|
|||
| НЕКОТОРЫЙ |
| ||
Comptox Dashboard ( EPA )
|
| ||
| Характеристики | |||
| C 5 H 9 N O 4 | |||
| Молярная масса | 147.130 g·mol −1 | ||
| Появление | Белый кристаллический порошок | ||
| Плотность | 1,4601 (20 ° C) | ||
| Точка плавления | 199 ° C (390 ° F; 472 K) разлагается | ||
| 8,57 г/л [ 1 ] | |||
| Растворимость | Этанол: 350 мкг/100 г (25 ° C) [ 2 ] | ||
| Кислотность (p k a ) | 2.10, 4.07, 9.47 [ 3 ] | ||
| −78.5·10 −6 см 3 /мол | |||
| Опасности | |||
| GHS Маркировка : | |||

| |||
| Предупреждение | |||
| H315 , H319 , H335 | |||
| P261 , P264 , P271 , P280 , P302+P352 , P304+P340 , P305+P351+P338 , P312, P321 , P332+P313, P337+P313 , P362 , P403+P233 , P405, P501, P501, P501, P501, P362 , P403 +P233 , P405 , P501, P362, P403+P233 , P3 | |||
| NFPA 704 (Огненная бриллиант) | |||
| Дополнительная страница данных | |||
| Глутаминовая кислота (страница данных) | |||
За исключением случаев, когда отмечены, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа).
| |||
Глутаминовая кислота (символ Glu или E ; [ 4 ] Анионная форма известна как глутамат ) представляет собой α- , которая используется почти всеми живыми существами в биосинтезе белков аминокислоту . Это несущественное питательное вещество для людей, что означает, что человеческое тело может синтезировать достаточно для его использования. Это также самый распространенный возбуждающий нейротрансмиттер в нервной системе позвоночных . Он служит предшественником синтеза ингибирующей гамма-аминобутирической кислоты (ГАМК) в ГАМКергических нейронах.
Его молекулярная формула c
5 часов
9 Нет
4 Глутаминовая кислота существует в двух оптически изомерных формах; Декстроротационная -форма L обычно получается путем гидролиза глютена или из сточных вод из производства свеклевой свеклы или с помощью ферментации. [ 5 ] [ Полная цитата необходима ] Его молекулярная структура может быть идеализирована как hooc -ch ( NH
2 ) - ( гл
2 ) 2 -coOH, с двумя карбоксильными группами -coOH и одной аминогруппой - NH
2 Однако в твердом состоянии и мягко кислотных водных растворах молекула предполагает электрически нейтральную цвиттерирования структуру − OOC - Ch ( NH +
3 ) - ( гл
2 ) 2 -coOH. Это кодируется кодонами . GAA или GAG
Кислота может потерять один протон из своей второй карбоксильной группы, чтобы сформировать конъюгатную основу , отдельный анионный глутамат. − OOC - Ch ( NH +
3 ) - ( гл
2 ) 2 -ку − Полем Эта форма соединения распространена в нейтральных решениях. Глутаматный нейротрансмиттер играет главную роль в нейронной активации . [ 6 ] Этот анион создает пикантный аромат пищевых продуктов и обнаружен в ароматизациях глутамата, таких как MSG . В Европе он классифицируется как пищевая добавка E620 . В очень щелочных растворах вдвойной негативный анион − OOC - Ch ( NH
2 ) - ( гл
2 ) 2 -ку − преобладает. Радикал , соответствующий глутамату, называется глутамил .
Символ однобуквенного платежа для глутамата был назначен в качестве буквы, следующей D для аспартата , так как глутамат больше на одну метилена --ч 2- . группу [ 7 ]
Химия
[ редактировать ]Ионизация
[ редактировать ]
Когда глутаминовая кислота растворяется в воде, аминогруппа ( - NH
2 ) может получить протон ( h +
) и/или карбоксильные группы могут потерять протоны, в зависимости от кислотности среды.
В достаточно кислотных средах обе карбоксильные группы протонируются, и молекула становится катионом с одним положительным зарядом, hooc -ch ( NH +
3 ) - ( гл
2 ) 2 -coOH. [ 8 ]
При значениях pH от 2,5 до 4,1, [ 8 ] Карбоновая кислота ближе к амине обычно теряет протон, и кислота становится нейтральным − OOC - Ch ( NH +
3 ) - ( гл
2 ) 2 -coOH. Это также форма соединения в кристаллическом твердом состоянии. [ 9 ] [ 10 ] Изменение в состоянии протонации постепенно; Две формы находятся в равных концентрациях при рН 2,10. [ 11 ]
При еще более высоком pH другая группа карбоновой кислоты теряет свой протон, а кислота существует почти полностью как глутаматный анион − OOC - Ch ( NH +
3 ) - ( гл
2 ) 2 -ку − , с одним отрицательным зарядом в целом. Изменение состояния протонации происходит при рН 4,07. [ 11 ] Эта форма с обоими карбоксилатами, лишенными протонов, доминирует в физиологическом диапазоне рН (7,35–7,45).
При еще более высоком pH аминогруппа теряет дополнительный протон, а распространенный вид-дважды отрицательный анион − OOC - Ch ( NH
2 ) - ( гл
2 ) 2 -ку − Полем Изменение в состоянии протонации происходит при рН 9.47. [ 11 ]
Оптическая изомерия
[ редактировать ]Глутаминовая кислота является хиральной ; зеркального изображения Существуют два энантиомера : D ( -) и L (+). А L форма более широко встречается по своей природе, но d форма возникает в некоторых специальных контекстах, таких как бактериальная капсула и клеточные стенки бактерий ( которые производят ее из L образует с ферментом глутамат -ракемазы и печень млекопитающих . ) [ 12 ] [ 13 ]
История
[ редактировать ]Хотя они встречаются естественным образом во многих пищевых продуктах, вклад вкуса, внесенный глутаминовой кислотой и другими аминокислотами, был только научно идентифицирован в начале 20 -го века. Вещество было обнаружено и идентифицировано в 1866 году немецким химиком Карлом Генрихом Риттхаузеном , который обрабатывал глютен пшеницы (для которого оно было названо) серной кислотой . [ 14 ] В 1908 году японский исследователь Kikunae Ikeda из Токийского имперского университета идентифицировал коричневые кристаллы, оставленные после испарения большого количества бульона комбу в качестве глутаминовой кислоты. Эти кристаллы, когда они были на вкус, воспроизводили невыразимый, но неоспоримый аромат, который он обнаружил во многих продуктах, особенно в морских водорослях. Профессор Икеда назвал этот аромат Умами . Затем он запатентовал метод массового производства кристаллической соли глутаминовой кислоты, моносодий глутамат . [ 15 ] [ 16 ]
Синтез
[ редактировать ]Биосинтез
[ редактировать ]| Реагенты | Продукция | Ферменты | |
|---|---|---|---|
| Глютамин + h 2 o | → | Glu + NH 3 | GLS , GLS2 |
| Nacglu + h 2 o | → | Glu + ацетат | N -ацетил -глутамат -синтаза |
| α-кетоглутарат + NADP H + NH 4 + | → | Glu + nadp + + H 2 o | Glud1 , Glud2 [ 17 ] |
| α-кетоглутарат + α-аминокислота | → | Glu + α-кето кислота | Трансаминаза |
| 1-пирролин-5-карбоксилат + NAD + + H 2 o | → | Glu + nay | ALDH4A1 |
| N-formimo-l-glutamate + fh 4 | → | Glu + 5-formimo-fh 4 | FTCD |
| Женщина | → | Glu + na | GCPII |
Промышленный синтез
[ редактировать ]Глутаминовая кислота производится в наибольшем масштабе любой аминокислоты, причем в 2006 году оценивается около 1,5 млн. Тонн в 2006 году. [ 18 ] Химический синтез был вытеснен аэробной ферментацией сахаров и аммиака в 1950 -х годах, при этом организм Corynebacterium glutamicum (также известный как Brevibacterium flavum ), наиболее широко используемый для производства. [ 19 ] Выделение и очищение могут быть достигнуты путем концентрации и кристаллизации ; Он также широко доступен в качестве соли гидрохлорида . [ 20 ]
Функция и использование
[ редактировать ]Метаболизм
[ редактировать ]Глутамат является ключевым соединением в клеточном метаболизме . У людей пищевые белки разбиваются путем расщепления на аминокислоты , которые служат метаболическим топливом для других функциональных ролей в организме. Ключевым процессом в деградации аминокислот является трансамирование , при котором аминогрузка аминокислоты переносится в α- кетоцид , обычно катализируется трансаминазой . Реакция может быть обобщена как таковая:
- R 1 -аминокислота + r 2 -α -кетоцид ⇌ r 1 -α -кетоцид + r 2 -аминокислота
Очень распространенным α-кето кислотой является α-кетоглутарат , промежуточный в цикле лимонной кислоты . Трансаминация α-кетоглутарата дает глутамат. Полученный α-кетоцидный продукт часто также является полезным, который может вносить вклад в качестве топлива или в качестве субстрата для дальнейших процессов метаболизма. Примеры следующие:
- Аспартат + α-кетоглутарат ⇌ оксалоацетат + глутамат
Как пируват , так и оксалоацетат являются ключевыми компонентами клеточного метаболизма, способствующих в качестве субстратов или промежуточных соединений в фундаментальных процессах, таких как гликолиз , глюконеогенез и цикл лимонной кислоты .
Глутамат также играет важную роль в утилизации избытка или отходов азота . Глутамат подвергается дезаминированию , окислительной реакции, катализируемой глутаматдегидрогеназой , [ 17 ] следующее:
Аммиак (как аммоний ) затем выделяется преимущественно в виде мочевины , синтезируемой в печени . Таким образом, трансаминация может быть связана с дезаминированием, эффективно позволяя удалять азот из аминовых групп аминокислот через глутамат в качестве промежуточного и, наконец, выводится из организма в форме мочевины.
Глутамат также является нейротрансмиттером (см. Ниже), что делает его одной из самых распространенных молекул в мозге. Злокачественные опухоли головного мозга, известные как глиома или глиобластома, используют это явление, используя глутамат в качестве источника энергии, особенно когда эти опухоли становятся все более зависящими от глутамата из -за мутаций в геном IDH1 . [ 21 ] [ 22 ]
Нейротрансмиттер
[ редактировать ]Глутамат является наиболее распространенным возбуждающим нейротрансмиттером позвоночных в нервной системе . [ 23 ] При химических синапсах глутамат хранится в везикулах . Нервные импульсы запускают высвобождение глутамата из пресинаптической клетки. Глутамат действует на ионотропные и метаботропные ( G-белоновые ) рецепторы. [ 23 ] В противоположных постсинаптических клетках глутаматные рецепторы , такие как рецептор NMDA или рецептор AMPA , связывают глутамат и активируются. Из -за своей роли в синаптической пластичности глутамат участвует в когнитивных функциях, таких как обучение и память в мозге. [ 24 ] Форма пластичности, известная как долгосрочное потенцирование в глутаматергических синапсах в гиппокампе , неокортекс и других частях мозга. Глутамат работает не только как передатчик с точки зрения , но и с помощью синаптического перекрестного столкновения разлива между синапсами, в которых суммирование глутамата, выделяемого из соседнего синапса, создает экстрасинаптическую передачу сигналов/ объем . [ 25 ] Кроме того, глутамат играет важную роль в регуляции конусов роста и синаптогенеза во время развития мозга, как первоначально описано Марком Маттсоном .
Беснаптические глутаматергические сигнальные циклы
[ редактировать ]внеклеточный глутамат в мозге дрозофилы регулирует кластеризацию постсинаптического глутаматного рецептора посредством процесса, включающей десенсибилизацию рецепторов. Было обнаружено, что [ 26 ] Ген, экспрессируемый в глиальных клетках, активно транспортирует глутамат во внеклеточный пространство , [ 26 ] В то время как в ядре accumbens -стимулирующей группы II метаботропные рецепторы глутамата , как было обнаружено, что этот ген снижает уровень внеклеточного глутамата. [ 27 ] Это повышает вероятность того, что этот внеклеточный глутамат играет «эндокринно-подобную» роль как часть большей гомеостатической системы.
Предшественник Габ
[ редактировать ]Глутамат также служит предшественником синтеза ингибирующей гамма-аминобутирической кислоты (ГАМК) в ГАМК-эгических нейронах. Эта реакция катализируется глутаматом декарбоксилазой (GAD). [ 28 ] ГАМК-эгические нейроны идентифицируются (для исследовательских целей), выявляя ее активность (с методами авторадиографии и иммуногистохимии ) [ 29 ] который наиболее распространен в мозжечке и поджелудочной железе . [ 30 ]
Синдром жесткого человека -это неврологическое расстройство, вызванное антителами против GAD, что приводит к снижению синтеза ГАМК и, следовательно, нарушена моторная функция, такая как мышечная жесткость и спазм. Поскольку поджелудочная железа имеет обильную GAD, в поджелудочной железе происходит прямое иммунологическое разрушение, а пациенты будут иметь сахарный диабет . [ 31 ]
Улучшитель вкуса
[ редактировать ]Глутаминовая кислота, являющаяся компонентом белка, присутствует в продуктах, содержащих белок, но ее можно попробовать только тогда, когда она присутствует в несвязанной форме. Значительное количество свободной глутаминовой кислоты присутствует в самых разных продуктах, в том числе сырах и соевом соусе , и глутаминовая кислота отвечает за Умами , один из пяти основных вкусов человеческого чувства вкуса . Глутаминовая кислота часто используется в качестве пищевой добавки и энхансера вкуса в форме его соли натрия , известной как глутамат монозодий (MSG).
Питательное вещество
[ редактировать ]Все мясо, птица, рыба, яйца, молочные продукты и комбу являются отличными источниками глутаминовой кислоты. Некоторые богатые белком пищевые продукты также служат источниками. От 30% до 35% глютена (большая часть белка в пшенице) представляет собой глутаминовую кислоту. Девяносто пять процентов диетического глутамата метаболизируется кишечными клетками в первом проходе. [ 32 ]
Рост растений
[ редактировать ]Auxigro - это препарат роста растений, который содержит 30% глутаминовой кислоты.
ЯМР -спектроскопия
[ редактировать ]В последние годы, [ когда? ] Было проведено много исследований по использованию остаточной диполярной связи (RDC) в спектроскопии ядерной магнитно -резонанса (ЯМР). (PBLG) , производное глутаминовой кислоты Поли-бензил-L-глютамат (PBLG), часто используется в качестве среды выравнивания для контроля шкалы наблюдаемых диполярных взаимодействий. [ 33 ]
Роль глутамата в старении
[ редактировать ]Фармакология
[ редактировать ]Препарат фенциклидин (более широко известный как PCP или «пыль-ангел») глутаминовой кислоте противоречит в рецепторе NMDA . По тем же причинам декстрометорфан и кетамин также оказывают сильные диссоциативные и галлюциногенные эффекты. Острая инфузия препарата eglumetad (также известный как Eglumegad или Ly354740), агонист метаботропных рецепторов глутамата 2 и 3 ) приводил к заметному снижению yohimbine -индуцированной реакции на стресс в макаках капота ( Macaca radiata ); Хроническое пероральное введение eglumetad у этих животных привело к заметно сниженным уровням базового уровня кортизола (приблизительно 50 процентов) по сравнению с необработанными контрольными субъектами. [ 34 ] Также было продемонстрировано, что Eglumetad действует на метаботропном рецепторе глутамата 3 (GRM3) человеческих адренокортикальных клеток , подавляющих альдостерон -синтазу , CYP11B1 и выработку пособия стероидов (например, альдостерон и кортизол ). [ 35 ] Глутамат не легко проходит барьер кровавого мозга , но вместо этого транспортируется система транспорта с высоким сродством. [ 36 ] [ 37 ] Его также можно преобразовать в глутамин .
Токсичность глутамата может быть уменьшена антиоксидантами , а психоактивный принцип каннабиса , тетрагидроканнабинола (ТГК) и не психоактивный принцип каннабидиола (CBD) и других каннабиноидов блокирует нейротоксичность глутамата с одинаковой потенциалом и, таким образом, активные антителины. [ 38 ] [ 39 ]
Смотрите также
[ редактировать ]Ссылки
[ редактировать ]- ^ «L-глютаминовая кислота» . Национальная библиотека медицины . Получено 24 июня 2023 года .
- ^ Belitz, H.D.; Грош, Вернер; Шиберл, Питер (27 февраля 2009 г.). Пищевая химия . Спрингер. ISBN 978-3540699330 .
- ^ «Аминокислотные структуры» . cem.msu.edu. Архивировано из оригинала 11 февраля 1998 года.
- ^ «Номенклатура и символика для аминокислот и пептидов» . Объединенная комиссия IUPAC-IUB по биохимической номенклатуре. 1983. Архивировано из оригинала 29 августа 2017 года . Получено 5 марта 2018 года .
- ^ Третий новый международный словарь Вебстера «Непреодолимый», третье издание, 1971.
- ^ Роберт Сапольский (2005), Биология и поведение человека: неврологическое происхождение индивидуальности (2 -е издание); Учебная компания . С. 19–20 путеводителя.
- ^ Saffran, M. (апрель 1998 г.). «Аминокислотные названия и игры в гостиной: от тривиальных названий до однобуртового кода, аминокислотные названия имеют напряженные воспоминания студентов. Возможно ли более рациональная номенклатура?» Полем Биохимическое образование . 26 (2): 116–118. doi : 10.1016/s0307-4412 (97) 00167-2 .
- ^ Jump up to: а беременный Альберт Нойбергер (1936), «Константы диссоциации и структуры глутаминовой кислоты и ее эфиров». Биохимический журнал , том 30, выпуск 11, статья CCXCIII, с. 2085–2094. PMC 1263308 .
- ^ Роданте, Ф.; Marrosu, G. (1989). «Термодинамика второго процесса диссоциации протонов девяти α-аминокидов и третьих ионизационных процессов глутаминовой кислоты, аспартациновой кислоты и тирозина». Thermochimica Acta . 141 : 297–303. Bibcode : 1989tcac..141..297r . doi : 10.1016/0040-6031 (89) 87065-0 .
- ^ Lehmann, Mogens S.; Котцле, Томас Ф.; Гамильтон, Уолтер С. (1972). «Точная нейтронная дифракционная структура Определение компонентов белковой и нуклеиновой кислоты. VIII: кристаллическая и молекулярная структура β-формы аминокислотной глутаминовой кислоты». Журнал кристаллической и молекулярной структуры . 2 (5): 225–233. Bibcode : 1972jccry ... 2..225L . doi : 10.1007/bf01246639 . S2CID 93590487 .
- ^ Jump up to: а беременный в Уильям Х. Браун и Лоуренс С. Браун (2008), Органическая химия (5 -е издание). Cengage Learning. п. 1041. ISBN 0495388572 , 978-0495388579 .
- ^ Национальный центр биотехнологической информации, " D-Glutamate ". База данных COMPSHEM PUBCHEM , CID = 23327. Доступ 2017-02-17.
- ^ Лю, Л.; Йошимура, Т.; Эндо, К.; Кишимото, К.; Fuchikami, Y.; Мэннинг, JM; Esaki, N.; Сода, К. (1998). «Компенсация D -глютаматной ауксотрофии Escherichia coli WM335 с помощью гена аминотрансферазы D -аминокислоты и регуляции экспрессии MURI » . Биоссака, биотехнология и биохимия . 62 (1): 193–195. doi : 10.1271/bbb.62.193 . PMID 9501533 .
- ^ RHA Plimmer (1912) [1908]. RHA Plimmer; FG Hopkins (ред.). Химическая конституция белка . Монографии по биохимии. Тол. Часть I. Анализ (2 -е изд.). Лондон: Longmans, Green and Co. p. 114 Получено 3 июня 2012 года .
- ^ Рентон, Алекс (10 июля 2005 г.). «Если MSG так плохо для вас, почему у всех в Азии не болит голова?» Полем Хранитель . Получено 21 ноября 2008 года .
- ^ "Kikunae Ikeda Glutamate" . Японское патентное управление . 7 октября 2002 года. Архивировано с оригинала 28 октября 2007 года . Получено 21 ноября 2008 года .
- ^ Jump up to: а беременный Grabowska, A.; Nowicki, M.; Kwinta, J. (2011). «Глутаматдегидрогеназа прорастающих семян тритикала: экспрессия генов, распределение активности и кинетические характеристики» . Acta Physiolologiae Plantarum . 33 (5): 1981–1990. doi : 10.1007/s11738-011-0801-1 .
- ^ Алвиз Пероса; Фулвио Зеккини (2007). Методы и реагенты для зеленой химии: введение . Джон Уайли и сыновья. п. 25. ISBN 978-0-470-12407-9 .
- ^ Майкл С. Фликингер (2010). Энциклопедия промышленной биотехнологии: биопроцесс, биосепарация и клеточная технология, 7 объемных наборов . Уайли. С. 215–225. ISBN 978-0-471-79930-6 .
- ^ Фоли, Патрик; Керманшахи Поли, азаде; Пляж, Эван с.; Циммерман, Джули Б. (2012). «Вывод и синтез возобновляемых поверхностно -активных веществ». Химический Соц Преподобный 41 (4): 1499–1518. doi : 10.1039/c1cs15217c . ISSN 0306-0012 . PMID 22006024 .
- ^ из лит, SA; Навис, AC; Воскресение, k; Никло, SP; Создано, r; Западный, P; Вершины, б; Молен, R; Северного, CJ; Кредиторы, WP (август 2014 г.). «Глевата как хемотаксическая улыбка для диффузных клеток глиомы: они отлечивают присоски?» Полем Biucmics et Bioulisica Acta (BBA) - обзоры рака . 1846 (1): 66–74. doi : 10,1016/j.bby.2014 004 . PMID 2474768 .
- ^ van lith, sa; Моленаар, R; Ван Ноорден, CJ; Leenders, WP (декабрь 2014 г.). «Опухолевые клетки в поисках глутамата: альтернативное объяснение повышенной инвазивности мутантных глиомов IDH1» . Нейро-инкология . 16 (12): 1669–1670. doi : 10.1093/neuonc/nou152 . PMC 4232089 . PMID 25074540 .
- ^ Jump up to: а беременный Meldrum, BS (2000). «Глутамат как нейротрансмиттер в мозге: обзор физиологии и патологии» . Журнал питания . 130 (4S Suppl): 1007S - 1015S. doi : 10.1093/jn/130.4.1007s . PMID 10736372 .
- ^ Mcenee, WJ; Крук, Т. Т. (1993). «Глутамат: его роль в обучении, памяти и стареющем мозге». Психофармакология . 111 (4): 391–401. doi : 10.1007/bf02253527 . PMID 7870979 . S2CID 37400348 .
- ^ Okubo, Y.; Sekiya, H.; Namiki, S.; Sakamoto, H.; Iinuma, S.; Yamasaki, M.; Watanabe, M.; Хироз, К.; Iino, M. (2010). «Визуализация экстрасинаптическая динамика глутамата в мозге» . Труды Национальной академии наук . 107 (14): 6526–6531. Bibcode : 2010pnas..107.6526o . doi : 10.1073/pnas.0913154107 . PMC 2851965 . PMID 20308566 .
- ^ Jump up to: а беременный Августин Х., Гrosjean Y, Chen K, Sheng Q, Featherstone DE (2007). «Неваловое высвобождение глутамата с помощью глиальных транспортеров XCT подавляет кластеризацию рецептора глутамата in vivo» . Журнал нейробиологии . 27 (1): 111–123. doi : 10.1523/jneurosci.4770-06.2007 . PMC 2193629 . PMID 17202478 .
- ^ Чжэн XI; Бейкер да; Shen H; Карсон DS; Kalivas PW (2002). «Метаботропные рецепторы глутамата Журнал фармакологии и экспериментальной терапии . 300 (1): 162–171. doi : 10.1124/jpet.300.1.162 . PMID 11752112 .
- ^ Бак, Лассе К.; Schousboe, Arne; Waagepetersen, Helle S. (август 2006 г.). «Цикл глутамата/ГАМК-глутамина: аспекты транспорта, гомеостаз нейротрансмиттера и переноса аммиака» . Журнал нейрохимии . 98 (3): 641–653. doi : 10.1111/j.1471-4159.2006.03913.x . ISSN 0022-3042 . PMID 16787421 .
- ^ Керр, Диб; Ong, J. (январь 1995 г.). " ГАМК B Рецепторы " . Фармакология и терапия . 67 (2): 187–246. doi : 10.1016/0163-7258 (95) 00016-A . PMID 7494864 .
- ^ Крюгер, Кристиан; Стёкер, Винфрид; Шлоссер, Майкл (2007). «Аутоантитела к глутаминовой кислоте» . Аутоантитела (2 -е изд.). С. 369–378. doi : 10.1016/b978-044452763-9/50052-4 . ISBN 978-0-444-52763-9 .
- ^ Newsome, Scott D.; Джонсон, Тори (15 августа 2022 г.). «Спектр синдрома жесткого человека; больше, чем встречает глаз» . Журнал нейроиммунологии . 369 : 577915. DOI : 10.1016/j.jneuroim.2022.577915 . ISSN 0165-5728 . PMC 9274902 . PMID 35717735 .
- ^ Тростники, PJ; и др. (1 апреля 2000 г.). «Кишечный метаболизм глутамата» . Журнал питания . 130 (4S): 978S - 982S. doi : 10.1093/jn/130.4.978s . PMID 10736365 .
- ^ СМ Тиле, концепции Маг. Резон. A, 2007, 30A, 65–80
- ^ Копран Д.Д., Мэтью С.Дж., Смит Э.Л., Трост Р.К., Шарф Б.А., Мартинес Дж., Горман Дж. М., Монн Дж.А., Шопп Д.Д., Розенблум Л.А. (июль 2001 г.). «Влияние LY354740, нового глутаматергического метаботропного агониста, на нечеловеческий примат гипоталамо-гипофизационная ось и норадренергическая функция». CNS Spectr . 6 (7): 607–612, 617. DOI : 10.1017/S1092852900002157 . PMID 15573025 . S2CID 6029856 .
- ^ Felizola SJ, Namura Y, Satoh F, Morimoto R, Kikuchi K, Namura T, Hozawa A, Wang L, Onodera Y, Ise K, McNamara KM, Midonki S, Sasano H (январь 2014 г.). «Глутаматные рецепторы и регуляция стероодезиса в человеческой надпочечнике: метаботропный путь» Молекулярная и клеточная энокронология 382 (1): 170–1 Doi : 10.1016/ j.mce.2013.09.0 PMID 24080311 3357749S2CID
- ^ Смит, Квентин Р. (апрель 2000 г.). «Транспорт глутамата и других аминокислот на гематоэнцефалическом барьере» . Журнал питания . 130 (4S Suppl): 1016S - 1022S. doi : 10.1093/jn/130.4.1016s . PMID 10736373 .
- ^ Хокинс, Ричард А. (сентябрь 2009 г.). «Кровавый барьер и глутамат» . Американский журнал клинического питания . 90 (3): 867S - 874S. doi : 10.3945/ajcn.2009.27462bb . PMC 3136011 . PMID 19571220 .
Эта организация не позволяет чистоту глутамата в мозг; Скорее, это способствует удалению глутамата и поддержанию низких концентраций глутамата в ECF.
- ^ Хэмпсон, Эйдан Дж. (1998). «Каннабидиол и (-) Δ9-тетрагидроканнабинол являются нейропротекторными антиоксидантами» . Proc Natl Acad Sci USA . 95 (14): 8268–8273. doi : 10.1073/pnas.95.14.8268 . PMC 20965 . PMID 9653176 .
- ^ Хэмпсон, Эйдан Дж. (2006). «Нейропротекторные антиоксиданты от марихуаны» . Анналы нью -йоркской академии наук . 899 (1): 274–282. doi : 10.1111/j.1749-6632.2000.tb06193.x . S2CID 39496546 .
Дальнейшее чтение
[ редактировать ]- Нельсон, Дэвид Л.; Кокс, Майкл М. (2005). Принципы биохимии (4 -е изд.). Нью -Йорк: У. Х. Фриман. ISBN 0-7167-4339-6 .
Внешние ссылки
[ редактировать ]- Аминокислоты
- Протеиногенные аминокислоты
- Глюкогенные аминокислоты
- Возбуждающие аминокислоты
- Улучшители вкуса
- Умами -энхансеры
- Глутаматы
- Глутаминовые кислоты
- Возбуждающие аминокислотные рецепторные агонисты
- Глициновые рецепторные агонисты
- Периферически селективные лекарства
- Хелатирующие агенты
- Глутамат (нейротрансмиттер)
- Электронные добавки