1-Пропанол

| |

| |
| Имена | |
|---|---|
| Произношение | ˈprəʊpən.wən.ɒl |
| Предпочтительное название ИЮПАК
Пропан-1-ол [ 1 ] | |
Другие имена
| |
| Идентификаторы | |
3D model ( JSmol )
|
|
| 3DMeet | |
| 1098242 | |
| КЭБ | |
| ХЭМБЛ | |
| ХимическийПаук | |
| Лекарственный Банк | |
| Информационная карта ECHA | 100.000.679 |
| Номер ЕС |
|
| 25616 | |
| КЕГГ | |
| МеШ | 1-Пропанол |
ПабХим CID
|
|
| номер РТЭКС |
|
| НЕКОТОРЫЙ | |
| Число | 1274 |
Панель управления CompTox ( EPA )
|
|
| Характеристики | |
| C3H8C3H8O | |
| Молярная масса | 60.096 g·mol −1 |
| Появление | Бесцветная жидкость |
| Запах | мягкий, алкогольный [ 2 ] |
| Плотность | 0,803 г/мл |
| Температура плавления | −126 °С; −195 °Ф; 147 К |
| Точка кипения | от 97 до 98 °С; от 206 до 208 °F; от 370 до 371 К |
| смешиваемый | |
| войти P | 0.329 |
| Давление пара | 1,99 кПа (при 20 °C) |
| Кислотность ( pKa ) | 16 |
| Основность (p K b ) | −2 |
| −45.176·10 −6 см 3 /моль | |
Показатель преломления ( n D )
|
1.387 |
| Вязкость | 1,959 мПа·с (при 25 °C) [ 3 ] |
| 1,68 Д | |
| Термохимия | |
Теплоемкость ( С )
|
143,96 Дж/(К моль) |
Стандартный моляр
энтропия ( S ⦵ 298 ) |
192,8 Дж/(К моль) |
Стандартная энтальпия
образование (Δ f H ⦵ 298 ) |
−302,79…−302,29 кДж/моль |
Стандартная энтальпия
горение (Δ c H ⦵ 298 ) |
−2,02156…−2,02106 МДж/моль |
| Фармакология | |
| D08AX03 ( ВОЗ ) | |
| Опасности | |
| Безопасность и гигиена труда (OHS/OSH): | |
Основные опасности
|
Легковоспламеняющаяся жидкость |
| СГС Маркировка : | |
 
| |
| Опасность | |
| Х225 , Х302 , Х318 , Х336 | |
| П210 , П261 , П280 , П305+П351+П338 | |
| NFPA 704 (огненный алмаз) | |
| точка возгорания | 22 ° С (72 ° F; 295 К) |
| 371 ° С (700 ° F; 644 К) | |
| Взрывоопасные пределы | 2.2–13.7% [ 2 ] |
| Летальная доза или концентрация (LD, LC): | |
ЛД 50 ( средняя доза )
|
2800 мг/кг (кролик, перорально) 1699 мг/кг (мыши, перорально) 1870 мг/кг (крыса, перорально) [ 4 ] |
| NIOSH (пределы воздействия на здоровье в США): | |
ПЭЛ (допустимо)
|
TWA 200 частей на миллион (500 мг/м 3 ) [ 2 ] |
РЕЛ (рекомендуется)
|
TWA 200 частей на миллион (500 мг/м 3 ) ST 250 ppm (625 мг/м 3 ) [кожа] [ 2 ] |
IDLH (Непосредственная опасность)
|
800 частей на миллион [ 2 ] |
| Родственные соединения | |
Родственные соединения
|
Пропан Изопропиловый спирт Пропанамин Этанол Бутанол |
| Страница дополнительных данных | |
| 1-Пропанол (страница данных) | |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа).
| |
1-Пропанол (также пропан-1-ол , пропанол , н-пропиловый спирт ) — первичный спирт формулы CH 3 CH 2 CH 2 OH и иногда представлен как PrOH или n -PrOH . Это бесцветная жидкость и изомер пропанола 2- . 1-Пропанол используется в качестве растворителя в фармацевтической промышленности , главным образом для смол и эфиров целлюлозы , а иногда и как дезинфицирующее средство.
возникновение
[ редактировать ]Сивушные спирты, такие как 1-пропанол, являются побочными продуктами ферментации зерна, поэтому следовые количества 1-пропанола присутствуют во многих алкогольных напитках .
Химические свойства
[ редактировать ]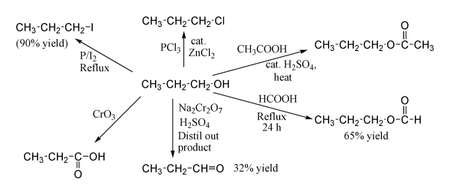
1-Пропанол демонстрирует нормальные реакции первичного спирта . Таким образом, его можно превратить в алкилгалогениды ; например, красный фосфор и йод производят н-пропилйодид с выходом 80%, а PCl 3 с каталитическим ZnCl 2 дает н-пропилхлорид . Реакция с уксусной кислотой в присутствии Катализатор H 2 SO 4 в этерификации Фишера условиях дает пропилацетат , тогда как кипячение пропанола с обратным холодильником в течение ночи с одной только муравьиной кислотой может дать пропилформиат с выходом 65%. Окисление 1-пропанола Na 2 Cr 2 O 7 и H 2 SO 4 дает 36% выход пропиональдегида , поэтому для этого типа реакции более высокопроизводительные методы с использованием PCC или окисления Сверна рекомендуются . Окисление хромовой кислотой дает пропионовую кислоту .
Подготовка
[ редактировать ]Пропанол получают каталитическим гидрированием пропиональдегида 1 - . Пропиональдегид получают оксо-процессом гидроформилированием этилена углерода монооксида с использованием октакарбонил и водорода в присутствии катализатора, такого как кобальта или комплекс родия . [ 5 ]
- Н 2 С=СН 2 + СО + Н 2 → СН 3 СН 2 СН=О
- СН 3 СН 2 СН=О + Н 2 → СН 3 СН 2 СН 2 ОН
Традиционный лабораторный способ получения 1-пропанола включает обработку н -пропилйодида влажным раствором. Аг 2 О.
Безопасность
[ редактировать ]Считается, что 1-пропанол аналогичен этанолу по своему воздействию на организм человека, но, согласно исследованию, проведенному на кроликах, в 2–4 раза более эффективен. Многие токсикологические исследования показывают, что острая ЛД 50 при пероральном приеме варьируется от 1,9 г/кг до 6,5 г/кг (по сравнению с 7,06 г/кг для этанола). Метаболизируется в пропионовую кислоту . Последствия включают алкогольную интоксикацию и метаболический ацидоз с высоким содержанием анионов . По состоянию на 2011 год был зарегистрирован один случай смертельного отравления после перорального приема 500 мл 1-пропанола. [ 6 ] Из-за отсутствия долгосрочных данных канцерогенность 1-пропанола для человека неизвестна.
1-Пропанол в качестве топлива
[ редактировать ]1-Пропанол имеет высокое октановое число и пригоден для использования в качестве моторного топлива. Однако пропанол слишком дорог для использования в качестве моторного топлива. Октановое число (RON) пропанола по исследовательскому методу составляет 118, а антидетонационный индекс (AKI) — 108. [ 7 ]
Ссылки
[ редактировать ]- ^ Фавр Х.А., Пауэлл WH (2014). Номенклатура органической химии: рекомендации ИЮПАК и предпочтительные названия 2013 г. (Синяя книга) . Кембридж: Королевское химическое общество . п. 61. дои : 10.1039/9781849733069 . ISBN 9780854041824 .
- ^ Перейти обратно: а б с д и Карманный справочник NIOSH по химическим опасностям. «#0533» . Национальный институт охраны труда и здоровья (NIOSH).
- ^ Пал А, Габа Р (2008). «Объемные, акустические и вискозиметрические исследования молекулярных взаимодействий в бинарных смесях диметилового эфира дипропиленгликоля с 1-алканолами при 298,15 К». Дж. Хим. Термодин. 40 (5): 818–828. дои : 10.1016/j.jct.2008.01.008 .
- ^ «Н-Пропиловый спирт» . Непосредственно опасные для жизни и здоровья концентрации (IDLH) . Национальный институт охраны труда и здоровья (NIOSH).
- ^ Папа Эй Джей (2011). «Пропанолы». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. дои : 10.1002/14356007.a22_173.pub2 . ISBN 9783527303854 .
- ^ Унмак Дж.Л. (2011). «Оценка и рекомендации по здоровью N-ПРОПАНОЛА для HEAC» (PDF) .
- ^ «Биоспирты» . Biofuel.org.uk . 2010 . Проверено 16 апреля 2014 г.
Дальнейшее чтение
[ редактировать ]- Фернисс, бакалавр наук; Ханнафорд, Эй Джей; Смит, PWG; Тэтчелл, А.Р. (1989), Учебник практической органической химии Фогеля (5-е изд.), Харлоу: Лонгман, ISBN 0-582-46236-3
- Лиде ДР, изд. (2006). Справочник CRC по химии и физике (87-е изд.). TF-CRC. ISBN 0849304873 .
- О'Нил М.Дж., изд. (2006). Индекс Merck: Энциклопедия химических веществ, лекарств и биологических препаратов (14-е изд.). Мерк. ISBN 091191000X .
- Перкин WH, Киппинг FS (1922). Органическая химия . Лондон: W. & R. Чемберс. ISBN 0080223540 .
