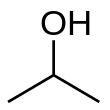
Изопропиловый спирт
| |||

| |||
| Имена | |||
|---|---|---|---|
| Предпочтительное название ИЮПАК
Пропан-2-ол [ 2 ] | |||
| Другие имена
2-Пропанол
изопропанол [ 1 ] Медицинский спирт сек -Пропиловый спирт 2-гидроксипропан и -PrOH Диметилкарбинол НАСИЛИЕ | |||
| Идентификаторы | |||
3D model ( JSmol )
|
|||
| 635639 | |||
| КЭБ | |||
| ХЭМБЛ | |||
| ХимическийПаук | |||
| Информационная карта ECHA | 100.000.601 | ||
| 1464 | |||
| КЕГГ | |||
ПабХим CID
|
|||
| номер РТЭКС |
| ||
| НЕКОТОРЫЙ | |||
| Число | 1219 | ||
Панель управления CompTox ( EPA )
|
|||
| Характеристики | |||
| C3H8C3H8O | |||
| Молярная масса | 60.096 g/mol | ||
| Появление | Бесцветная жидкость | ||
| Запах | Резкий спиртовой запах | ||
| Плотность | 0,786 г/см 3 (20 °С) | ||
| Температура плавления | -89 ° C (-128 ° F; 184 К) | ||
| Точка кипения | 82,6 ° С (180,7 ° F; 355,8 К) | ||
| Смешивается с водой | |||
| Растворимость | Смешивается с бензолом , хлороформом , этанолом , диэтиловым эфиром , глицерином ; растворим в ацетоне | ||
| войти P | −0.16 [ 3 ] | ||
| Кислотность ( pKa ) | 16.5 [ 4 ] | ||
| −45.794·10 −6 см 3 /моль | |||
Показатель преломления ( n D )
|
1.3776 | ||
| Вязкость | 2,86 сП при 15 °C 1,96 сП при 25 °C [ 5 ] 1,77 с П и 30 °С [ 5 ] | ||
| 1,66 Д (газ) | |||
| Фармакология | |||
| D08AX05 ( ВОЗ ) | |||
| Опасности | |||
| Безопасность и гигиена труда (OHS/OSH): | |||
Основные опасности
|
Легковоспламеняющийся, слаботоксичный [ 6 ] | ||
| СГС Маркировка : | |||
 
| |||
| Опасность | |||
| Х225 , Х302 , Х319 , Х336 | |||
| П210 , П261 , П305+П351+П338 | |||
| NFPA 704 (огненный алмаз) | |||
| точка возгорания | Открытая чашка: 11,7 ° C (53,1 ° F; 284,8 К) Закрытая чашка: 13 ° C (55 ° F) | ||
| 399 ° С (750 ° F, 672 К) | |||
| Взрывоопасные пределы | 2–12.7% | ||
| 980 мг/м 3 (СВВ), 1225 мг/м 3 (НАБОР) | |||
| Летальная доза или концентрация (LD, LC): | |||
ЛД 50 ( средняя доза )
|
|||
ЛК 50 ( средняя концентрация )
|
| ||
LC Lo ( самый низкий из опубликованных )
|
| ||
| NIOSH (пределы воздействия на здоровье в США): | |||
ПЭЛ (допустимо)
|
СВВ 400 частей на миллион (980 мг/м 3 ) [ 7 ] | ||
РЕЛ (рекомендуется)
|
СВВ 400 частей на миллион (980 мг/м 3 ), ST 500 ppm (1225 мг/м 3 ) [ 7 ] | ||
IDLH (Непосредственная опасность)
|
2000 частей на миллион [ 7 ] | ||
| Паспорт безопасности (SDS) | [1] | ||
| Родственные соединения | |||
Родственные спирты
|
1-Пропанол , этанол , 2-бутанол | ||
| Страница дополнительных данных | |||
| Изопропиловый спирт (страница данных) | |||
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа).
| |||
Изопропиловый спирт ( IUPAC название пропан-2-ол , также называемый изопропанолом или 2-пропанолом ) представляет собой бесцветное , легковоспламеняющееся органическое соединение с резким спиртовым запахом . [ 9 ]
Изопропиловый спирт, органическая полярная молекула , смешивается с водой, этанолом и хлороформом , демонстрируя свою способность растворять широкий спектр веществ, включая этилцеллюлозу , поливинилбутираль , масла, алкалоиды и природные смолы . Примечательно, что он не смешивается с растворами солей и может быть отделен добавлением хлорида натрия в процессе, известном как высаливание . Он образует азеотроп с водой, что приводит к температуре кипения 80,37 ° C, и характеризуется слегка горьким вкусом. Изопропиловый спирт становится вязким при более низких температурах, замерзает при -89,5 ° C и имеет значительное поглощение в ультрафиолетовой и видимой области спектра при 205 нм. Химически он может окисляться до ацетона или подвергаться различным реакциям с образованием таких соединений, как изопропоксиды или изопропоксид алюминия. Поскольку изопропильная группа связана с гидроксильной группой ( химическая формула (CH 3 ) 2 CHOH ) — простейший пример вторичного спирта , где атом углерода спирта присоединен к двум другим атомам углерода. Это структурный изомер пропан -1-ола и этилметилового эфира . У всех есть формула C3H8O 3H8.
Впервые он был синтезирован в 1853 году Александром Уильямсоном , а затем использован для приготовления кордита . Его производят путем гидратации пропена или гидрирования ацетона, при этом современные процессы позволяют получить безводный спирт путем азеотропной перегонки . Помимо производства, изопропиловый спирт используется в медицинских учреждениях в качестве медицинского спирта и дезинфицирующего средства для рук , а также в промышленности и быту в качестве растворителя. Это обычный ингредиент таких продуктов, как антисептики , дезинфицирующие и моющие средства . Ежегодно во всем мире производится более миллиона тонн. Несмотря на свою полезность, изопропиловый спирт представляет угрозу безопасности из-за его воспламеняемости и возможности образования перекиси . Его проглатывание или абсорбция приводит к токсическим эффектам, включая депрессию центральной нервной системы и кому , которые в первую очередь лечатся поддерживающими мерами.
Характеристики
[ редактировать ]Изопропиловый спирт смешивается с водой, этанолом и хлороформом , так как это органическая полярная молекула . Растворяет этилцеллюлозу , поливинилбутираль , многие масла, алкалоиды и природные смолы. [ 10 ] В отличие от этанола или метанола , изопропиловый спирт не смешивается с растворами солей и может быть отделен от водных растворов добавлением соли, такой как хлорид натрия . Этот процесс в просторечии называется высаливанием и приводит к разделению концентрированного изопропилового спирта на отдельный слой. [ 11 ]
Изопропиловый спирт образует азеотроп с водой, что дает температуру кипения 80,37 ° C (176,67 ° F) и состав изопропилового спирта, составляющий 87,7% по массе (91% по объему). Он имеет горьковатый привкус, пить его небезопасно. [ 11 ] [ 12 ]
Изопропиловый спирт становится все более вязким с понижением температуры и замерзает при -89,5 ° C (-129,1 ° F). [ 9 ] Смеси с водой имеют более высокие температуры замерзания: 99% при -89,5 ° C (-129,1 ° F), 91% (азеотроп) при -75,5 ° C (-103,9 ° F) и 70% при -61,7 ° C (- 79,1 °Ф). [ 13 ]
Изопропиловый спирт имеет максимальное поглощение при 205 нм в ультрафиолетовом и видимом спектрах. [ 14 ] [ 15 ]
Реакции
[ редактировать ]Изопропиловый спирт можно окислить до ацетона , который является соответствующим кетоном . Этого можно достичь, используя окислители, такие как хромовая кислота , или дегидрирование изопропилового спирта над нагретым медным катализатором :
- (CH 3 ) 2 CHOH → (CH 3 ) 2 CO + H 2
Изопропиловый спирт часто используется как растворитель и источник гидрида в реакции восстановления Меервейна-Понндорфа-Верли и других реакциях трансферного гидрирования . Изопропиловый спирт можно превратить в 2-бромпропан с помощью трибромида фосфора или дегидратировать до пропена путем нагревания с серной кислотой .
Как и большинство спиртов, изопропиловый спирт реагирует с активными металлами, такими как калий, с образованием алкоксидов , которые называются изопропоксидами . Изопропиловый спирт с тетрахлоридом титана реагирует с образованием изопропоксида титана :
- TiCl 4 + 4 (CH 3 ) 2 CHOH → Ti(OCH(CH 3 ) 2 ) 4 + 4 HCl
Эту и подобные реакции часто проводят в присутствии основания.
Реакция с алюминием инициируется следами ртути с образованием изопропоксида алюминия . [ 16 ]
История
[ редактировать ]Изопропиловый спирт впервые синтезировал химик Александр Уильям Уильямсон в 1853 году. Он добился этого путем нагревания смеси пропена и серной кислоты. Компания Standard Oil производила изопропиловый спирт путем гидратации пропена . Изопропиловый спирт окисляли до ацетона для получения кордита — бездымного маловзрывоопасного топлива. [ 17 ]
Производство
[ редактировать ]В 1994 году в США, Европе и Японии было произведено 1,5 миллиона тонн изопропилового спирта. [ 18 ] В основном его получают путем объединения воды и пропена в реакции гидратации или гидрирования ацетона . [ 18 ] [ 19 ] Существует два пути процесса гидратации, и оба процесса требуют отделения изопропилового спирта от воды и других побочных продуктов путем перегонки . Изопропиловый спирт и вода образуют азеотроп , а простая перегонка дает материал, который на 87,9% по массе состоит из изопропилового спирта и на 12,1% по массе воды. [ 20 ] Чистый ( безводный ) изопропиловый спирт получают азеотропной перегонкой влажного изопропилового спирта с использованием диизопропилового эфира или циклогексана в качестве азеотропных агентов. [ 18 ]
Биологический
[ редактировать ]Небольшие количества изопропилового спирта вырабатываются в организме при диабетическом кетоацидозе . [ 21 ]
Непрямое увлажнение
[ редактировать ]При непрямой гидратации пропен реагирует с серной кислотой с образованием смеси сульфатных эфиров. В этом процессе может использоваться низкокачественный пропен, и он преобладает в США. Эти процессы дают в основном изопропиловый спирт, а не 1-пропанол, поскольку добавление воды или серной кислоты к пропену соответствует правилу Марковникова . Последующий гидролиз этих эфиров паром дает изопропиловый спирт путем перегонки. Диизопропиловый эфир является важным побочным продуктом этого процесса; его возвращают в процесс и гидролизуют с получением желаемого продукта. [ 18 ]
- СН 3 СН=СН 2 + Н 2 О (СН 3 ) 2 СНОН
Прямое увлажнение
[ редактировать ]Прямая гидратация реагирует с пропеном и водой, либо в газовой, либо в жидкой фазе , при высоких давлениях в присутствии твердых или нанесенных кислотных катализаторов . Для этого типа процесса обычно требуется пропилен более высокой чистоты (> 90%). [ 18 ] Прямая гидратация чаще используется в Европе.
Гидрирование ацетона
[ редактировать ]спирт можно получить гидрированием ацетона Изопропиловый ; однако этот подход включает в себя дополнительный этап по сравнению с вышеуказанными методами, поскольку ацетон сам по себе обычно получают из пропилена посредством кумолового процесса . [ 18 ] Стоимость IPA в первую очередь зависит от стоимости сырья (ацетона или пропилена). Известная проблема – образование МИБК и других продуктов самоконденсации. Никель Ренея был одним из первых промышленных катализаторов, современные катализаторы часто поддерживаются биметаллическими материалами.
Использование
[ редактировать ]
В 1990 году в США было использовано 45 000 тонн изопропилового спирта, в основном в качестве растворителя для покрытий или в промышленных процессах. В том году 5400 метрических тонн было использовано для бытовых нужд и средств личной гигиены. Изопропиловый спирт особенно популярен в фармацевтических целях. [ 18 ] из-за его низкой токсичности. Некоторое количество изопропилового спирта используется в качестве химического промежуточного продукта. Изопропиловый спирт можно превратить в ацетон, но кумоловый процесс более важен. [ 18 ]
Растворитель
[ редактировать ]Изопропиловый спирт растворяет широкий спектр неполярных соединений. Он быстро испаряется, и обычно доступные сорта, как правило, не оставляют после себя масляных следов при использовании в качестве чистящей жидкости, в отличие от некоторых других распространенных растворителей. Он также относительно нетоксичен. Таким образом, он широко используется в качестве растворителя и чистящей жидкости, особенно там, где присутствуют масла или остатки масел на основе, которые трудно очистить водой, которые легко испаряются и (в зависимости от содержания воды и других переменных) представляют меньший риск загрязнения. коррозии или ржавления, чем обычная вода. Вместе с этанолом , н -бутанолом и метанолом он относится к группе спиртовых растворителей.
Изопропиловый спирт обычно используется для чистки очков , электрических контактов аудио- и видеокассет , головок DVD и других оптических дисков , линз , бонгов , [ 22 ] удаление термопасты с радиаторов процессора [ 23 ] и другие пакеты IC .
Средний
[ редактировать ]Изопропиловый спирт этерифицируется с образованием изопропилацетата , другого растворителя. Он реагирует с сероуглеродом и гидроксидом натрия с образованием изопропилксантогената натрия , гербицида и флотореагента для руды . [ 24 ] Изопропиловый спирт реагирует с тетрахлоридом титана и металлическим алюминием с образованием изопропоксидов титана и алюминия соответственно, первый из которых является катализатором, а второй - химическим реагентом. [ 18 ] Это соединение само по себе может служить химическим реагентом, действуя как донор диводорода при трансферном гидрировании .
Медицинский
[ редактировать ]Медицинский спирт , дезинфицирующее средство для рук и дезинфицирующие подушечки обычно содержат 60–70% раствор изопропилового спирта или этанола в воде . Вода необходима для открытия пор мембраны бактерий, которые действуют как ворота для изопропилового спирта. 75% -ный водный раствор можно использовать в качестве дезинфицирующего средства для рук. [ 25 ] Изопропиловый спирт используется в качестве средства для осушения воды для профилактики наружного отита , более известного как «ухо пловца». [ 26 ]
В некоторых случаях для лечения тошноты можно использовать вдыхание изопропилового спирта, поместив под нос дезинфицирующую подушечку. [ 27 ]
Раннее использование в качестве анестетика
[ редактировать ]Хотя изопропиловый спирт можно использовать для анестезии, его многочисленные отрицательные свойства или недостатки запрещают такое использование. Изопропиловый спирт также можно использовать в качестве растворителя, как и эфир. [ 28 ] или в качестве анестетика, вдыхая пары или перорально. Раннее использование растворителя включало использование его в качестве общего анестетика для мелких млекопитающих. [ 29 ] и грызунов учеными и некоторыми ветеринарами. Однако вскоре его прекратили, так как возникло множество осложнений, включая раздражение дыхательных путей, внутреннее кровотечение, проблемы со зрением и слухом. В редких случаях наблюдалась дыхательная недостаточность, приводящая к гибели животных.
Автомобильная промышленность
[ редактировать ]«газосушилки» Изопропиловый спирт является основным ингредиентом топливных присадок . В значительных количествах вода представляет собой проблему в топливных баках, поскольку она отделяется от бензина и может замерзнуть в линиях подачи при низких температурах. Спирт не удаляет воду из бензина, но растворяет воду в бензине. Будучи растворимой , вода не представляет такого же риска, как нерастворимая вода, поскольку она больше не накапливается в линиях подачи и не замерзает, а растворяется в самом топливе. Изопропиловый спирт часто продается в аэрозольных баллончиках в качестве антиобледенителя лобового стекла или дверного замка. Изопропиловый спирт также используется для удаления следов тормозной жидкости из гидравлических тормозных систем, чтобы тормозная жидкость (обычно DOT 3 , DOT 4 или минеральное масло ) не загрязняла тормозные колодки и не вызывала плохое торможение. Смеси изопропилового спирта и воды также часто используются в самодельной жидкости для омывателя ветрового стекла.
Лаборатория
[ редактировать ]В качестве консерванта биологических образцов изопропиловый спирт представляет собой сравнительно нетоксичную альтернативу формальдегиду и другим синтетическим консервантам. Для консервации препаратов применяют растворы изопропилового спирта 70–99 %.
Изопропиловый спирт часто используется при экстракции ДНК . Лаборант добавляет его в раствор ДНК для осаждения ДНК, которая затем после центрифугирования образует осадок. Это возможно, поскольку ДНК нерастворима в изопропиловом спирте.
Полупроводники
[ редактировать ]Изопропиловый спирт используется в качестве добавки при щелочном анизотропном травлении монокристаллического кремния , например, гидроксидом калия или гидроксидом тетраметиламмония . Этот процесс используется при текстурировании кремниевых солнечных элементов и микропроизводстве (например, в устройствах MEMS ). Изопропиловый спирт увеличивает анизотропию травления за счет увеличения скорости травления плоскости [100] по сравнению с плоскостями с более высоким индексом . [ 30 ]
Безопасность
[ редактировать ]Пары изопропилового спирта плотнее воздуха и огнеопасны , диапазон воспламеняемости в воздухе составляет от 2 до 12,7%. Его следует хранить вдали от источников тепла, искр и открытого огня. [ 31 ] Сообщалось, что перегонка изопропилового спирта над магнием приводит к образованию пероксидов , которые могут взрываться при концентрации. [ 32 ] [ 33 ] Изопропиловый спирт может со временем вступать в реакцию с воздухом и кислородом, образуя нестабильные пероксиды, которые могут взорваться. [ 34 ]
Токсикология
[ редактировать ]Изопропиловый спирт через свои метаболиты несколько более токсичен, чем этанол, но значительно менее токсичен, чем этиленгликоль или метанол . Смерть от проглатывания или абсорбции даже относительно больших количеств встречается редко. И изопропиловый спирт, и его ацетон метаболит действуют как центральной нервной системы (ЦНС) депрессанты . [ 35 ] Отравление может произойти при проглатывании, вдыхании или попадании через кожу. [ 36 ] Симптомы отравления изопропиловым спиртом включают приливы , головную боль , головокружение , угнетение ЦНС , тошноту , рвоту , анестезию , гипотермию , низкое кровяное давление , шок , угнетение дыхания и кому . [ 35 ] Передозировка может вызвать фруктовый запах изо рта в результате его метаболизма в ацетон . [ 37 ] Изопропиловый спирт не вызывает ацидоза анионной разницы , но он создает осмоляльную разницу между расчетной и измеренной осмоляльностью сыворотки, как и другие спирты. [ 35 ] Результаты исследования ацетона без ацидоза приводят к непременным условиям «кетоза без ацидоза».
Изопропиловый спирт окисляется с образованием ацетона под действием алкогольдегидрогеназы в печени. [ 35 ] и имеет биологический период полураспада у человека от 2,5 до 8,0 часов. [ 35 ] В отличие от отравления метанолом или этиленгликолем , метаболиты изопропилового спирта значительно менее токсичны, и лечение в основном носит поддерживающий характер. Кроме того, нет показаний к использованию фомепизола , ингибитора алкогольдегидрогеназы, за исключением случаев, когда есть подозрение на его одновременный прием с метанолом или этиленгликолем. [ 38 ]
В судебно-медицинской экспертизе у людей, умерших в результате диабетического кетоацидоза, концентрация изопропилового спирта в крови обычно составляет десятки мг/дл, тогда как у людей, умерших в результате смертельного проглатывания изопропилового спирта, концентрация в крови обычно составляет сотни мг/дл. [ 21 ]
Ссылки
[ редактировать ]- ^ «Правило об алкоголе C-201.1». Номенклатура органической химии («Синяя книга» ИЮПАК), разделы A, B, C, D, E, F и H. Оксфорд: Пергамон Пресс. 1979.
Такие обозначения, как изопропанол, втор-бутанол и трет-бутанол, неверны, поскольку не существует углеводородов изопропан, втор-бутан и трет-бутан, к которым можно добавить суффикс «-ол»; от таких названий следует отказаться. Однако изопропиловый спирт, втор-бутиловый спирт и трет-бутиловый спирт допустимы (см. Правило C-201.3), поскольку радикалы изопропил, втор-бутил и трет-бутил действительно существуют.
- ^ Фавр, Анри А.; Пауэлл, Уоррен Х. (2014). Номенклатура органической химии: Рекомендации ИЮПАК и предпочтительные названия 2013 (Синяя книга) . Кембридж: Королевское химическое общество . п. 631. дои : 10.1039/9781849733069 . ISBN 978-0-85404-182-4 .
- ^ «Изопропанол_msds» . chemsrc.com. Архивировано из оригинала 10 марта 2020 года . Проверено 4 мая 2018 г.
- ^ Рив, В.; Эриксон, CM; Алуотто, ПФ (1979). «Новый метод определения относительной кислотности спиртов в спиртовых растворах. Нуклеофильность и конкурентная реакционная способность алкоксидов и феноксидов» . Может. Дж. Чем . 57 (20): 2747–2754. дои : 10.1139/v79-444 .
- ^ Перейти обратно: а б Явс, CL (1999). Справочник по химическим свойствам . МакГроу-Хилл . ISBN 978-0-07-073401-2 .
- ^ Токсичность изопропилового спирта
- ^ Перейти обратно: а б с Карманный справочник NIOSH по химическим опасностям. «#0359» . Национальный институт охраны труда и здоровья (NIOSH).
- ^ Перейти обратно: а б с д «Изопропиловый спирт» . Непосредственно опасные для жизни и здоровья концентрации (IDLH) . Национальный институт охраны труда и здоровья (NIOSH).
- ^ Перейти обратно: а б «Изопропанол» . ПабХим . Архивировано из оригинала 12 февраля 2019 года . Проверено 10 февраля 2019 г.
- ^ Дулитл, Артур К. (1954). Технология растворителей и пластификаторов . Нью-Йорк: John Wiley & Sons, Inc., с. 628.
- ^ Перейти обратно: а б Индекс Merck (10-е изд.). Рэуэй, Нью-Джерси: Merck & Co., 1983. с. 749 . ISBN 9780911910278 .
- ^ Логсден, Джон Э.; Локи, Ричард А. (1999). «Пропиловые спирты». В Крошвице, Жаклин И. (ред.). Краткая энциклопедия химической технологии Кирка-Отмера (4-е изд.). Нью-Йорк: John Wiley & Sons, Inc., стр. 1654–1656. ISBN 978-0-471-41961-7 .
- ^ «Какова температура замерзания изопропилового спирта?» . 21 сентября 2023 г. Проверено 18 декабря 2023 г.
- ^ «Изопропиловый спирт, подходящий для жидкостной хроматографии, экстракции, УФ-спектрофотометрии» . ВВР Интернешнл . Архивировано из оригинала 31 марта 2016 года . Проверено 25 августа 2014 г.
- ^ «УФ-отсечка» (PDF) . Университет Торонто . Архивировано (PDF) из оригинала 8 октября 2013 года . Проверено 25 августа 2014 г.
- ^ Исихара, К.; Ямамото, Х. (2001). «Изопропоксид алюминия». Энциклопедия реагентов для органического синтеза . Джон Уайли и сыновья . дои : 10.1002/047084289X.ra084 . ISBN 0471936235 .
- ^ Виткофф, ММ; Грин, ХА (2003). Принципы органической химии и производственная практика (1-е изд., 1-е переиздание. Изд.). Вайнхайм: Wiley-VCH. п. 4. ISBN 978-3-527-30289-5 .
- ^ Перейти обратно: а б с д и ж г час я Папа, А.Дж. «Пропанолы». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. дои : 10.1002/14356007.a22_173 . ISBN 978-3527306732 .
- ^ Логсдон, Джон Э.; Локи, Ричард А. (4 декабря 2000 г.). «Изопропиловый спирт». Энциклопедия химической технологии Кирка-Отмера . Энциклопедия химической технологии Кирка-Отмера . John Wiley & Sons, Inc. doi : 10.1002/0471238961.0919151612150719.a01 . ISBN 978-0471238966 .
- ^ Справочник CRC по химии и физике, 44-е изд. стр. 2143–2184.
- ^ Перейти обратно: а б Петерсен, Томас Х.; Уильямс, Тимоти; Нувайхид, Назиха; Харрафф, Ричард (2012). «Посмертное обнаружение изопропанола при кетоацидозе». Журнал судебной медицины . 57 (3): 674–678. дои : 10.1111/j.1556-4029.2011.02045.x . ISSN 0022-1198 . ПМИД 22268588 . S2CID 21101240 .
- ^ Директоро-Местон, Даниэль (9 февраля 2021 г.). «Как правильно чистить бонг, по мнению экспертов по каннабису» . Роллинг Стоун . Проверено 31 марта 2024 г.
- ^ Метод применения Intel arcticsilver.com
- ^ «Натрия изопропилксантогенат, SIPX, ксантогенат» . 3DChem.com. Архивировано из оригинала 4 мая 2012 года . Проверено 17 июня 2012 г.
- ^ «Руководство по местному производству: рекомендованные ВОЗ составы средств для ухода за руками» (PDF) . Всемирная организация здравоохранения. Август 2009 г. Архивировано (PDF) из оригинала 19 мая 2009 г. . Проверено 5 октября 2020 г.
- ^ Наружный отит (ухо пловца) . Медицинский колледж Висконсина.
- ^ Линдблад, Адриенн Дж.; Тинг, Ронда; Харрис, Кевин (август 2018 г.). «Ингаляционный изопропиловый спирт при тошноте и рвоте в отделении неотложной помощи» . Канадский семейный врач . 64 (8): 580. ISSN 1715-5258 . ПМК 6189884 . ПМИД 30108075 .
- ^ Берладж, Генри М.; Уэлч, Х.; Прайс, CW (2006). «Фармацевтическое применение изопропилового спирта II. Растворимость местных анестетиков». Журнал Американской фармацевтической ассоциации . 36 (1): 17–19. дои : 10.1002/jps.3030360105 . ПМИД 20285822 .
- ^ Общество экспериментальной биологии и медицины (1922). Труды Общества экспериментальной биологии и медицины, Том 19 . п. 85. Архивировано из оригинала 20 декабря 2021 года . Проверено 24 сентября 2016 г.
- ^ Зубель, Ирена; Крамковская, Малгожата (30 октября 2002 г.). «Влияние спиртовых добавок на характеристики травления в растворах КОН» . Датчики и исполнительные механизмы A: Физические . 101 (3): 255–261. дои : 10.1016/S0924-4247(02)00265-0 . ISSN 0924-4247 .
- ^ «Изопропанол» . Сигма-Олдрич. 19 января 2012 года. Архивировано из оригинала 17 января 2021 года . Проверено 6 июля 2012 г.
- ^ Мирафзал, Голам А.; Баумгартен, Генри Э. (1988). «Контроль перекисных соединений: Приложение». Журнал химического образования . 65 (9): А226. Бибкод : 1988ЖЧЭд..65А.226М . дои : 10.1021/ed065pA226 .
- ^ «Химическая безопасность: образование перекиси в 2-пропаноле» . Новости химии и техники . 94 (31): 2. 1 августа 2016. Архивировано из оригинала 7 ноября 2017 года . Проверено 2 ноября 2017 г.
- ^ «Информационный бюллетень об опасных веществах» (PDF) . Официальный сайт штата Нью-Джерси . Проверено 4 ноября 2023 г.
- ^ Перейти обратно: а б с д и Слотер Р.Дж., Мейсон Р.В., Бизли Д.М., Вейл Дж.А., Шеп Л.Дж. (2014). «Отравление изопропанолом». Клиническая токсикология . 52 (5): 470–8. дои : 10.3109/15563650.2014.914527 . ПМИД 24815348 . S2CID 30223646 .
- ^ Чавес, Эндрю Р.; Суини, Майкл; Акпунону, Питер (14 декабря 2021 г.). «Случай непреднамеренного отравления изопропанолом в результате трансдермальной абсорбции, задержанной еженедельным гемодиализом» . Американский журнал клинических случаев . 22 : е934529. дои : 10.12659/AJCR.934529 . ISSN 1941-5923 . ПМЦ 8689373 . ПМИД 34905533 .
- ^ Калапос, член парламента (2003). «О метаболизме ацетона у млекопитающих: от химии к клиническим последствиям». Biochimica et Biophysical Acta (BBA) – Общие предметы . 1621 (2): 122–39. дои : 10.1016/S0304-4165(03)00051-5 . ПМИД 12726989 .
- ^ «Отравление изопропиловым спиртом» . uptodate.com . Архивировано из оригинала 10 октября 2017 года . Проверено 10 октября 2017 г.