Ядерный рецептор 4A2
| NR4A2 | |||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| Идентификаторы | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Псевдонимы | NR4A2 , HZF-3, NO, NURR1, RNR1, TINUR, Подсемейство ядерного рецептора 4 Группа A Член 2 | ||||||||||||||||||||||||||||||||||||||||||||||||||
| Внешние идентификаторы | Омим : 601828 ; MGI : 1352456 ; Гомологен : 4509 ; GeneCards : NR4A2 ; OMA : NR4A2 - ортологи | ||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| Викидид | |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
Ядерный рецептор 4A2 ( NR4A2 ) (подсемейство ядерного рецептора 4 Группа A -член 2), также известный как 1 белок, связанный с ядерным рецептором 1 ( NURR1 ), является белком , который у людей кодируется NR4A2 геном . [ 5 ] NR4A2 является членом семейства рецепторов ядерных внутриклеточных транскрипционных факторов .
NR4A2 играет ключевую роль в поддержании дофаминергической системы мозга. [ 6 ] Мутации в этом геном были связаны с расстройствами, связанными с дофаминергической дисфункцией, включая болезнь Паркинсона и шизофрения . Неправильная регистрация этого гена может быть связана с ревматоидным артритом . Для этого гена были идентифицированы четыре варианта транскрипта, кодирующие четыре различных изоформы. Могут существовать дополнительные альтернативные варианты сплайсинга, но их полноразмерная природа не была определена. [ 7 ]
Считается, что этот белок имеет решающее значение для развития фенотипа дофамина в среднем мозге, поскольку у мышей без NR4A2 не хватает экспрессии этого фенотипа. Это дополнительно подтверждается исследованиями, показывающими, что при применении экспрессии NR4A2 в наивных клетках -предшественниках существует полная экспрессия гена фенотипа дофамина. [ 8 ]
В то время как NR4A2 является ключевым белком, существуют другие факторы, необходимые, поскольку исследования показывают, что исключительно экспрессия NR4A2 не стимулирует эту фенотипическую экспрессию генов. Одним из этих предполагаемых факторов является транскрипционный фактор 2 крылатой спирали (FOXA2). Исследования показали, что эти два фактора находятся в пределах одной и той же области развивающихся дофаминергических нейронов, оба этих фактора присутствовали, чтобы иметь экспрессию для фенотипа дофамина. [ 8 ]
NR4A2 и расстройства развития
[ редактировать ]Мутации в NR4A2 были связаны с различными нарушениями развития, включая болезнь Паркинсона, шизофрении, маниакальную депрессию и аутизм. Делеции de novo, которые влияют на NR4A2, были выявлены у некоторых людей с интеллектуальными нарушениями и языковыми нарушениями, некоторые из которых соответствуют критериям DSM-5 для диагностики аутизма. [ 9 ]
NR4A2 и воспаление
[ редактировать ]Было проведено исследование о роли NR4A2 в воспалении и может предоставить важную информацию при лечении расстройств, вызванных дофаминергическим заболеванием нейронов. Воспаление в ЦНС может быть результатом активированной микроглии (аналогов макрофагов для центральной нервной системы) и других провоспалительных факторов, таких как бактериальный липополисахарид (LPS). LPS связывается с Toll-подобными рецепторами (TLR), что вызывает воспалительную экспрессию генов путем стимулирования сигнальных факторов транскрипции. Чтобы определить, какие клетки являются дофаминергическими, эксперименты измеряли фермент тирозин -гидроксилазу (TH), которая необходима для синтеза дофамина. Было показано, что NR4A2 защищает дофаминергические нейроны от LPS-индуцированного воспаления, путем снижения экспрессии воспалительных генов в микроглии и астроцитах. Когда короткая шпилька для NR4A2 была экспрессирована в микроглии и астроцитах, эти клетки продуцировали воспалительные медиаторы, такие как TNFA, без синтазы и IL-1β, подтверждая вывод, что снижение NR4A2 способствует воспалению и приводит к гибели клеток допаминергических нейрон. NR4A2 взаимодействует с комплексом фактора транскрипции NF-κB-P65 на воспалительных промоторах генов. Тем не менее, NR4A2 зависит от других факторов, которые могут участвовать в этих взаимодействиях. NR4A2 должен быть сумоилирован, и его корегулирующий фактор, гликогенсинтаза-киназа 3, должна быть фосфорилирована для этих взаимодействий. Sumolyated NR4A2 рекрутирует COREST, комплекс, изготовленный из нескольких белков, который собирает ферменты, модифицирующие хроматин. Комплекс NR4A2/COREST ингибирует транскрипцию воспалительных генов. [ 10 ]
Структура
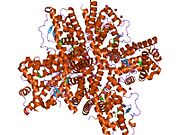
[ редактировать ]Одно исследование провело исследование структуры и показало, что NR4A2 не содержит лиганд-связывающую полость, а пятно, заполненное гидрофобными боковыми цепями. Неполярные аминокислотные остатки коререгуляторов NR4A2, SMRT и NCOR, связываются с этим гидрофобным пластырем. Анализ третичной структуры показал, что связывающая поверхность лиганд-связывающего домена расположена на канавках 11-й и 12-й альфа-спиралей. Это исследование также обнаружило, что необходимые структурные компоненты этого гидрофобного участка являются тремя аминокислотными остатками, F574, F592, L593; Мутация любых этих трех ингибирует активность LBD. [ 11 ]
Приложения
[ редактировать ]NR4A2 индуцирует экспрессию тирозин -гидроксилазы (TH), которая в конечном итоге приводит к дифференцировке в дофаминергические нейроны. Было продемонстрировано, что NR4A2 индуцирует дифференцировку в клетках -предшественниках ЦНС in vitro, но они требуют дополнительных факторов, чтобы достичь полной зрелости и дофаминергической дифференцировки. [ 12 ] Следовательно, модуляция NR4A2 может быть перспективной для генерации дофаминергических нейронов для исследований болезни Паркинсона, однако имплантация этих индуцированных клеток в качестве лечения терапии имела ограниченные результаты.
Нокаутные исследования
[ редактировать ]Исследования показали, что гетерозиготные нокаутированные мыши для гена NR4A2 демонстрируют снижение высвобождения дофамина. Первоначально это было компенсировано снижением скорости обратного захвата дофамина; Однако со временем это обратное захват не мог компенсировать уменьшенное количество выпущенного дофамина. В сочетании с потерей нейронов дофаминовых рецепторов, это может привести к появлению симптомов болезни Паркинсона. [ 13 ]
Взаимодействия
[ редактировать ]Было показано, что NR4A2 взаимодействует :
- Бета-катенин , [ 14 ]
- Гипофиз гомеобокс 3 , [ 15 ]
- Рецептор ретиноевой кислоты Альфа , [ 16 ] и
- Рецептор ретиноевой кислоты бета . [ 16 ]
Ссылки
[ редактировать ]- ^ Jump up to: а беременный в GRCH38: Ensembl Release 89: ENSG00000153234 - ENSEMBL , май 2017 г.
- ^ Jump up to: а беременный в GRCM38: Ensembl Release 89: Ensmusg00000026826 - Ensembl , май 2017 г.
- ^ «Человеческая PubMed ссылка:» . Национальный центр информации о биотехнологии, Национальная медицина США .
- ^ «Мышь Pubmed ссылка:» . Национальный центр информации о биотехнологии, Национальная медицина США .
- ^ Окабе Т, Такаяган «Клонирование кДНК коэффициента транспорта, связанного с NGFI-B/NUR7 . Журнал иммунологии 154 (8) (8): 3871–3 doi : 10.4049/jimmunol . PMID 7706727 . S2CID 36075352 .
- ^ Sacchetti P, Carpentier R, Ségard P, Olivé-Cren C, Lefebvre P (2006). «Множественные сигнальные пути регулируют транскрипционную активность ядерного рецептора сироты Nurr1» . Исследование нуклеиновых кислот . 34 (19): 5515–5527. doi : 10.1093/nar/gkl712 . PMC 1636490 . PMID 17020917 .
- ^ «Ген Entrez: подсемейство ядерного рецептора NR4A2 4, группа A, член 2» .
- ^ Jump up to: а беременный Yi Sh, He XB, Rhee YH, Park CH, Takizawa T, Nakashima K, Lee Sh (февраль 2014 г.). «FOXA2 действует как ко-активатор, потенциальный экспрессию фенотипа DA-индуцированного NURR1 посредством эпигенетической регуляции» . Разработка . 141 (4): 761–772. doi : 10.1242/dev.095802 . PMID 24496614 . S2CID 16677797 .
- ^ Баржа-Шапд, Леппа, Рейтер. "Джин: NR4A2 - " ген Sfari Получено 16 января
- ^ Saijo K, Winner B, Carson CT, Collier JG, Boyer L, Rosenfeld MG, et al. (Апрель 2009 г.). «Путь Nurr1/Corest в микроглии и астроцитах защищает дофаминергические нейроны от смерти, вызванной воспалением» . Клетка . 137 (1): 47–59. doi : 10.1016/j.cell.2009.01.038 . PMC 2754279 . PMID 19345186 .
- ^ Codina A, Benoit G, Gooch JT, Neuhaus D, Perlmann T, Schwabe JW (декабрь 2004 г.). «Идентификация новой поверхности взаимодействия коререгулятора на домене связывания лиганда NURR1 с использованием NMR-следа» . Журнал биологической химии . 279 (51): 53338–53345. doi : 10.1074/jbc.m409096200 . PMID 15456745 .
- ^ Ким Дж.Ю., Ко Х.К., Ли Дж.Ю., Чанг М.И., Ким Ю.К., Чунг Х. Х. и др. (Июнь 2003 г.). «Дифференцировка дофаминергической нейронов от эмбриональных нейронных предшественников у крыс с помощью сверхэкспрессии Nurr1» . Журнал нейрохимии . 85 (6): 1443–1454. doi : 10.1046/j.1471-4159.2003.01780.x . PMID 12787064 . S2CID 21991471 .
- ^ Zhang L, Le W, Xie W, Dani JA (май 2012 г.). «Возрастные изменения в передаче сигналов дофамина у мышей с дефицитом Nurr1 в качестве модели болезни Паркинсона» . Нейробиология старения . 33 (5): 1001.e7–1001.16. doi : 10.1016/j.neurobiolaging.2011.03.022 . PMC 3155628 . PMID 21531044 .
- ^ Zhang L, Cen L, Qu S, Wei L, Mo M, Feng J, et al. (Apr 2016). «Увеличение активности бета-катенина посредством ингибирования GSK3beta защищает клетки PC12 от токсичности ротенона посредством индукции NURR1» . Plos один . 11 (4): E0152931. Bibcode : 2016ploso..1152931Z . doi : 10.1371/journal.pone.0152931 . PMC 4821554 . PMID 27045591 .
- ^ Джейкобс Ф.М., Ван Эрп С., Ван дер Линден А.Дж., фон Ортел Л., Бурбах Дж.П., Смидт МП (февраль 2009 г.). «Pitx3 усиливает Nurr1 в терминальной дифференцировке дофаминовых нейронов за счет высвобождения SMRT-опосредованной репрессии». Разработка . 136 (4): 531–540. doi : 10.1242/dev.029769 . PMID 19144721 . S2CID 5989601 .
- ^ Jump up to: а беременный Perlmann T, Jansson L (апрель 1995 г.). «Новый путь для передачи сигналов витамина А, опосредованной гетеродимеризацией RXR с NGFI-B и Nurr1» . Гены и развитие . 9 (7): 769–782. doi : 10.1101/gad.9.7.769 . PMID 7705655 .
Дальнейшее чтение
[ редактировать ]- Le W, Appel SH (февраль 2004 г.). «Мутантные гены, ответственные за болезнь Паркинсона». Современное мнение о фармакологии . 4 (1): 79–84. doi : 10.1016/j.coph.2003.09.005 . PMID 15018843 .
- Wedler B, Wüstenberg PW, Naumann G (июль 1975 г.). «[Лечение гипертона в сахарном диабете]». Журнал для всей внутренней медицины и ее пограничных районов . 30 (13): 437–442. PMID 4929 .
- Perlmann T, Jansson L (апрель 1995 г.). «Новый путь для передачи сигналов витамина А, опосредованной гетеродимеризацией RXR с NGFI-B и Nurr1» . Гены и развитие . 9 (7): 769–782. doi : 10.1101/gad.9.7.769 . PMID 7705655 .
- Forman BM, Umesono K, Chen J, Evans RM (май 1995). «Уникальные пути ответа устанавливаются аллостерическими взаимодействиями между рецепторами ядерных гормонов» . Клетка . 81 (4): 541–550. doi : 10.1016/0092-8674 (95) 90075-6 . PMID 7758108 . S2CID 3203590 .
- Mages HW, Rilke O, Bravo R, Senger G, Kroczek RA (ноябрь 1994 г.). «Нет, ген немедленного ответа человека, тесно связанный с рецептором стероидного/гормона щитовидной железы NAK1/TR3» . Молекулярная эндокринология . 8 (11): 1583–1591. doi : 10.1210/mend.8.11.7877627 . PMID 7877627 .
- Maruyama K, Sugano S (январь 1994 г.). «Олиго-капитализация: простой метод замены структуры крышки эукариотических мРНК олигорибонуклеотидами». Ген . 138 (1–2): 171–174. doi : 10.1016/0378-1119 (94) 90802-8 . PMID 8125298 .
- Suzuki Y, Yoshitomo-Nakagawa K, Maruyama K, Suyama A, Sugano S (октябрь 1997 г.). «Строительство и характеристика обогащенной полной длиной и библиотекой кДНК с 5'-эндом». Ген . 200 (1–2): 149–156. doi : 10.1016/s0378-1119 (97) 00411-3 . PMID 9373149 .
- Torii T, Kawarai T, Nakamura S, Kawakami H (апрель 1999 г.). «Организация гена ядерного рецептора Orphan nurpar1 человека». Ген . 230 (2): 225–232. doi : 10.1016/s0378-1119 (99) 00064-5 . PMID 10216261 .
- Ichinose H, Ohye T, Suzuki T, Sumi-Ichinose C, Nomura T, Hagino Y, Nagatsu T (апрель 1999 г.). «Молекулярное клонирование гена Nurr1 человека: характеристика гена человека и кДНК». Ген . 230 (2): 233–239. doi : 10.1016/s0378-1119 (99) 00065-7 . PMID 10216262 .
- Чен Й.Х., Цай М.Т., Шоу К.К., Чен Ч. (декабрь 2001 г.). «Мутационный анализ гена NR4A2 человека, необходимый ген для дофаминергического нейрогенеза среднего мозга у пациентов с шизофренией». Американский журнал медицинской генетики . 105 (8): 753–757. doi : 10.1002/ajmg.10036 . PMID 11803525 .
- Ишигуро Х., Окубо Y, Оцуки Т., Ямакава-Кобаяши К., Аринами Т (январь 2002 г.). «Мутационный анализ бета-рецептора ретиноида X, рецептора 1 ядерного рецептора и пролифератора, активируемых пролифератором пероксисом, альфа-генов, связанных с шизофренией и алкогольной зависимостью: возможная связь с гаплотипами гена рецептора 1 ядерного рецептора с алкогольной зависимостью». Американский журнал медицинской генетики . 114 (1): 15–23. doi : 10.1002/ajmg.1620 . PMID 11840500 .
- Mcevoy AN, Murphy EA, Ponnio T, Connely OM, Bresnihan B, Fitzgerald O, EP Murphy (март 2002 г.). «Активация транскрипции ядерного сироты NURR1 с помощью NF-Kappa B и циклического аденозина 5'-монофосфатного ответа, связывающего белок, в синовиальном ткани ревматоидного артрита» . Журнал иммунологии . 168 (6): 2979–2987. doi : 10.4049/jimmunol.168.6.2979 . PMID 11884470 .
- Сюй П.Ю., Лян Р., Янкович Дж., Хантер С., Цзэн Юкс, Ашизава Т. и др. (Март 2002 г.). «Ассоциация гомозиготных 7048G7049 вариант в интроне шесть гена Nurr1 с болезнью Паркинсона». Неврология . 58 (6): 881–884. doi : 10.1212/wnl.58.6.881 . PMID 11914402 . S2CID 19632736 .
- Bannon MJ, Pruetz B, Manning-Bog AB, Whitty CJ, Michelhaugh SK, Sacchetti P, et al. (Апрель 2002 г.). «Снижение экспрессии транскрипционного фактора Nurr1 в дофаминовых нейронах злоупотреблений кокаина» . Труды Национальной академии наук Соединенных Штатов Америки . 99 (9): 6382–6385. Bibcode : 2002pnas ... 99.6382b . doi : 10.1073/pnas.092654299 . PMC 122957 . PMID 11959923 .
- Le WD, Xu P, Jankovic J, Jiang H, Appel SH, Smith RG, Vassilatis DK (январь 2003 г.). «Мутации в NR4A2, связанные с семейной болезнью Паркинсона». Природа генетика . 33 (1): 85–89. doi : 10.1038/ng1066 . PMID 12496759 . S2CID 10699494 .
- Satoh J, Kuroda Y (декабрь 2002 г.). «Конститутивная и индуцируемая экспрессия NURR1, ключевого регулятора дофаминергической дифференцировки нейронов, в нейронных и ненейронных клеточных линиях человека». Невропатология . 22 (4): 219–232. doi : 10.1046/j.1440-1789.2002.00460.x . PMID 12564761 . S2CID 30708166 .
- Iwayama-Shigeno Y, Yamada K, Toyota T, Shimizu H, Hattori E, Yoshitsugu K, et al. (Апрель 2003 г.). «Распределение гаплотипов, полученных из трех общих вариантов гена NR4A2 у японских пациентов с шизофренией» . Американский журнал медицинской генетики. Часть B, нейропсихиатрическая генетика . 118b (1): 20–24. doi : 10.1002/ajmg.b.10053 . PMID 12627459 . S2CID 35675105 .
- Kim KS, Kim CH, Hwang Dy, Seo H, Chung S, Hong SJ, et al. (Май 2003 г.). «Ядерный рецептор сироты Nurr1 напрямую трансактивирует промоторную активность гена тирозин-гидроксилазы в клеточной специфической форме» . Журнал нейрохимии . 85 (3): 622–634. doi : 10.1046/j.1471-4159.2003.01671.x . PMID 12694388 . S2CID 6219768 .
- Рамос Л.Л., Монтейро Ф.П., Сампайо Л.П., Коста Л.А., Рибейро М.Д., Фрейтас Э.Л. и др. (Август 2019). «Гетерозиготная потеря функции NR4A2 связана с интеллектуальным дефицитом, роландической эпилепсией и языковыми нарушениями» . Отчеты о клинических случаях . 7 (8): 1582–1584. doi : 10.1002/ccr3.2260 . PMC 6693049 . PMID 31428396 .
Внешние ссылки
[ редактировать ]- NURR1+ядерный+рецептор в Национальной медицинской библиотеке Медицинской библиотеки США (Mesh)