Эстрадиол

| |

| |
| Имена | |
|---|---|
| Произношение | / ˌ ɛ s t r ə ˈ d aɪ oʊ l / ES -trə- DY -ohl [ 1 ] [ 2 ] |
| Название ИЮПАК
Эстра-1,3,5(10)-триен-3,17β-диол
| |
| Систематическое название ИЮПАК
(1 S ,3a S ,3b R ,9b S ,11a S )-11a-Метил-2,3,3a,3b,4,5,9b,10,11,11a-декагидро-1 H -циклопента[ a ] фенантрен-1,7-диол | |
| Другие имена
эстрадиол; Е2; 17β-эстрадиол; 17β-эстрадиол
| |
| Идентификаторы | |
3D model ( JSmol )
|
|
| КЭБ | |
| ХЭМБЛ | |
| ХимическийПаук | |
| Лекарственный Банк | |
| Информационная карта ECHA | 100.000.022 |
| Номер ЕС |
|
| КЕГГ | |
ПабХим CID
|
|
| НЕКОТОРЫЙ | |
Панель управления CompTox ( EPA )
|
|
| Характеристики | |
| С 18 Н 24 О 2 | |
| Молярная масса | 272.38 g/mol |
| -186.6·10 −6 см 3 /моль | |
| Фармакология | |
| G03CA03 ( ВОЗ ) | |
| Данные лицензии | |
| Пероральный , сублингвальный , интраназальный , местный / трансдермальный , вагинальный , внутримышечный или подкожный (в виде сложного эфира ), подкожный имплантат. | |
| Фармакокинетика : | |
| Оральный: <5% [ 3 ] | |
| ~98%: [ 3 ] [ 4 ] • Альбумин : 60% • ГСПГ : 38% • Бесплатно: 2 % | |
| Печень (путем гидроксилирования , сульфатирования , глюкуронидации ) | |
| Оральный: 13–20 часов. [ 3 ] Сублингвально: 8–18 часов. [ 5 ] Местно (гель): 36,5 часов. [ 6 ] | |
| Моча : 54% [ 3 ] Фекалии : 6% [ 3 ] | |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа).
| |
Эстрадиол ( Е2 ), также называемый эстрогеном , эстрадиол , представляет собой эстроген стероидный гормон и основной женский половой гормон . Он участвует в регуляции женских репродуктивных циклов, таких как эстральный и менструальный циклы . Эстрадиол отвечает за развитие женских вторичных половых признаков, таких как грудь , расширение бедер и женский тип распределения жира . Он также важен для развития и поддержания женских репродуктивных тканей, таких как молочные железы , матка и влагалище, в период полового созревания , зрелого возраста и беременности . [ 7 ] Он также оказывает важное воздействие на многие другие ткани, включая кости , жир , кожу , печень и мозг .
Хотя уровень эстрадиола у мужчин намного ниже, чем у женщин, эстрадиол играет важную роль и у мужчин. Помимо человека и других млекопитающих , эстрадиол также обнаружен у большинства позвоночных и ракообразных , насекомых , рыб и других животных видов . [ 8 ] [ 9 ]
Эстрадиол вырабатывается главным образом в фолликулах яичников яички , а также в других тканях, включая , надпочечники , жир, печень , молочные железы и мозг. Эстрадиол вырабатывается в организме из холестерина посредством ряда реакций и промежуточных продуктов . [ 10 ] Основной путь включает образование андростендиона , который затем преобразуется ароматазой в эстрон и впоследствии превращается в эстрадиол. Альтернативно, андростендион может быть преобразован в тестостерон , который затем может быть преобразован в эстрадиол. При наступлении менопаузы у женщин выработка эстрогенов яичниками прекращается, а уровень эстрадиола снижается до очень низкого уровня.
Помимо своей роли естественного гормона, эстрадиол используется в качестве лекарства , например, при менопаузальной гормональной терапии и феминизирующей гормональной терапии для трансгендерных женщин ; Информацию об эстрадиоле как о лекарстве см. в статье об эстрадиоле (лекарстве) .
Биологическая функция
[ редактировать ]Сексуальное развитие
[ редактировать ]Развитие вторичных половых признаков у женщин обусловлено эстрогенами, а именно эстрадиолом. [ 11 ] [ 12 ] Эти изменения начинаются в период полового созревания , большинство из них усиливаются в репродуктивном возрасте и становятся менее выраженными при снижении поддержки эстрадиола после менопаузы . Таким образом, эстрадиол способствует развитию груди и отвечает за изменения формы тела , влияя на кости, суставы и отложение жира . [ 11 ] [ 12 ] У женщин эстрадиол вызывает развитие груди, расширение бедер , женское распределение жира (при этом жир откладывается, в частности, на груди, бедрах, бедрах и ягодицах), а также созревание влагалища и вульвы , тогда как он опосредует скачок полового созревания ( косвенно через повышенную секрецию гормона роста ) [ 13 ] и закрытие эпифизов (тем самым ограничивая окончательную высоту ) у обоих полов. [ 11 ] [ 12 ]
Воспроизведение
[ редактировать ]Женская репродуктивная система
[ редактировать ]У женщин эстрадиол действует как гормон роста тканей репродуктивных органов, поддерживая слизистую оболочку влагалища , шейные железы, эндометрий и слизистую оболочку маточных труб. Усиливает рост миометрия . Эстрадиол, по-видимому, необходим для поддержания яйцеклеток в яичнике . Во время менструального цикла эстрадиол, вырабатываемый растущими фолликулами, через систему положительной обратной связи запускает гипоталамо-гипофизарные события, которые приводят к выбросу лютеинизирующего гормона , вызывая овуляцию. В лютеиновой фазе эстрадиол в сочетании с прогестероном подготавливает эндометрий к имплантации . Во время беременности уровень эстрадиола увеличивается за счет выработки плаценты . Эффект эстрадиола вместе с эстроном и эстриолом при беременности менее ясен. Они могут способствовать маточному кровотоку, росту миометрия, стимулировать рост груди, а в доношенном возрасте способствовать размягчению шейки матки и экспрессии рецепторов окситоцина в миометрии . [ нужна ссылка ] У павианов блокирование выработки эстрогена приводит к потере беременности, что позволяет предположить, что эстрадиол играет роль в поддержании беременности. Исследования изучают роль эстрогенов в процессе начала родов . Действие эстрадиола необходимо до воздействия прогестерона в лютеиновую фазу. [ нужна ссылка ]
Мужская репродуктивная система
[ редактировать ]Влияние эстрадиола (и эстрогенов в целом) на мужскую репродукцию является сложным. Эстрадиол вырабатывается под действием ароматазы образом в клетках Лейдига семенников млекопитающих главным , а также в некоторых половых клетках и клетках Сертоли неполовозрелых млекопитающих. [ 14 ] Он действует ( in vitro ) для предотвращения апоптоза мужских сперматозоидов . [ 15 ] Хотя некоторые исследования начала 1990-х годов утверждали, что существует связь между глобальным снижением количества сперматозоидов и воздействием эстрогена в окружающей среде, [ 16 ] более поздние исследования не обнаружили ни такой связи, ни доказательств общего снижения количества сперматозоидов. [ 17 ] [ 18 ] Подавление выработки эстрадиола в субпопуляции мужчин с субфертильностью может улучшить анализ спермы . [ 19 ]
Мужчины с определенными половых хромосом генетическими заболеваниями , такими как синдром Клайнфельтера , будут иметь более высокий уровень эстрадиола. [ 20 ]
Скелетная система
[ редактировать ]Эстрадиол оказывает глубокое воздействие на кости. Лица без него (или других эстрогенов) станут высокими и евнухоидными , поскольку закрытие эпифизов задерживается или может не произойти. [ 21 ] На плотность костей также влияет, что приводит к ранней остеопении и остеопорозу . [ 22 ] Низкий уровень эстрадиола также может предсказать переломы, причем у женщин в постменопаузе самая высокая частота переломов костей . [ 23 ] Женщины после менопаузы испытывают ускоренную потерю костной массы из-за относительного дефицита эстрогена. [ 24 ]
Здоровье кожи
[ редактировать ]Рецептор эстрогена , как и рецептор прогестерона , обнаружен в коже , в том числе в кератиноцитах и фибробластах . [ 25 ] [ 26 ] В период менопаузы и в последующий период снижение уровня женских половых гормонов приводит к атрофии , истончению и усилению морщинистости кожи, а также к снижению эластичности , упругости и прочности кожи. [ 25 ] [ 26 ] ускорение старения кожи и являются результатом снижения содержания коллагена , нарушений морфологии клеток , Эти изменения кожи представляют собой эпидермиса уменьшения основного вещества между волокнами кожи , а также уменьшения капилляров и кровотока . [ 25 ] [ 26 ] Кожа также становится более сухой во время менопаузы, что связано с уменьшением гидратации кожи и поверхностных липидов (выработка кожного сала). [ 25 ] Наряду с хронологическим старением и фотостарением дефицит эстрогенов в климактерическом периоде является одним из трех основных факторов, преимущественно влияющих на старение кожи. [ 25 ]
Заместительная гормональная терапия, состоящая из системного лечения эстрогеном отдельно или в сочетании с прогестагеном, имеет хорошо документированные и значительные положительные эффекты на кожу женщин в постменопаузе. [ 25 ] [ 26 ] Эти преимущества включают увеличение содержания коллагена в коже, увеличение толщины и эластичности кожи, а также увлажнение кожи и поверхностных липидов. [ 25 ] [ 26 ] Было обнаружено, что местный эстроген оказывает аналогичное благотворное воздействие на кожу. [ 25 ] Кроме того, исследование показало, что местный крем с 2% прогестерона значительно повышает эластичность и упругость кожи, а также заметно уменьшает морщины у женщин в пери- и постменопаузе. [ 26 ] С другой стороны, гидратация кожи и поверхностные липиды существенно не изменились при местном применении прогестерона. [ 26 ] Эти данные свидетельствуют о том, что прогестерон, как и эстроген, также оказывает благотворное воздействие на кожу и может независимо защищать ее от старения. [ 26 ]
Нервная система
[ редактировать ]Эстрогены могут вырабатываться в мозге из предшественников стероидов. как антиоксиданты Было обнаружено, что они обладают нейропротекторной функцией. [ 27 ]
Петли положительной и отрицательной обратной связи менструального цикла включают эстрадиол яичников как связующее звено с гипоталамо-гипофизарной системой, регулирующее гонадотропины . [ 28 ]
Считается, что эстроген играет важную роль в психическом здоровье женщин, при этом предполагается связь между уровнем гормонов, настроением и самочувствием. Внезапные падения или колебания или длительные периоды устойчивого низкого уровня эстрогена могут быть связаны со значительным снижением настроения. Было показано, что клиническое выздоровление от депрессии после родов, перименопаузы и постменопаузы эффективно после стабилизации и/или восстановления уровня эстрогена. [ 29 ] [ 30 ]
Было обнаружено, что объемы половодиморфных структур мозга у трансгендерных женщин изменяются и приближаются к типичным женским структурам мозга при воздействии эстрогена одновременно с андрогенной депривацией в течение нескольких месяцев. [ 31 ] предполагая, что эстрогены и/или андрогены играют значительную роль в половой дифференциации мозга как внутриутробно , так и в более позднем возрасте.
Есть также свидетельства того, что программирование сексуального поведения взрослых самцов у многих позвоночных во многом зависит от эстрадиола, вырабатываемого во время внутриутробного развития и в раннем детстве. [ 32 ] Пока неизвестно, играет ли этот процесс значительную роль в сексуальном поведении человека, хотя данные, полученные от других млекопитающих, указывают на связь. [ 33 ]
Было обнаружено, что эстроген увеличивает секрецию окситоцина и усиливает экспрессию его рецептора , рецептора окситоцина , в мозге . [ 34 ] Было обнаружено, что у женщин однократной дозы эстрадиола достаточно для повышения концентрации циркулирующего окситоцина. [ 35 ]
Гинекологический рак
[ редактировать ]Эстрадиол связан с развитием и прогрессированием таких видов рака, как рак молочной железы, рак яичников и рак эндометрия. Эстрадиол влияет на ткани-мишени главным образом путем взаимодействия с двумя ядерными рецепторами, называемыми рецептором эстрогена α (ERα) и рецептором эстрогена β (ERβ). [ 36 ] [ 37 ] Одной из функций этих рецепторов эстрогена является модуляция экспрессии генов . Как только эстрадиол связывается с ЭР, рецепторные комплексы затем связываются со специфическими последовательностями ДНК , что может вызвать повреждение ДНК и увеличение деления клеток и репликации ДНК . Эукариотические клетки реагируют на поврежденную ДНК, стимулируя или ослабляя фазы G1, S или G2 клеточного цикла, чтобы инициировать восстановление ДНК . В результате происходит клеточная трансформация и пролиферация раковых клеток. [ 38 ]
Сердечно-сосудистая система
[ редактировать ]Эстроген влияет на определенные кровеносные сосуды . Улучшение артериального кровотока было продемонстрировано в коронарных артериях . [ 39 ] 17-бета-эстрадиол (Е2) считается самым мощным эстрогеном, обнаруженным у человека. Е2 влияет на функцию сосудов, апоптоз и повреждение во время ишемии и реперфузии сердца. E2 может защитить сердце и отдельные кардиомиоциты от повреждений, связанных с ишемией. После сердечного приступа или длительных периодов гипертонии Е2 подавляет побочные эффекты патологического ремоделирования сердца. [ 40 ]
Во время беременности высокий уровень эстрогенов, а именно эстрадиола, увеличивает свертываемость крови и риск венозной тромбоэмболии .
| Абсолютная частота возникновения первой ВТЭ на 10 000 человеко-лет во время беременности и в послеродовом периоде | ||||||||
|---|---|---|---|---|---|---|---|---|
| Шведские данные А | Шведские данные B | Английские данные | Датские данные | |||||
| Период времени | Н | Ставка (95% ДИ) | Н | Ставка (95% ДИ) | Н | Ставка (95% ДИ) | Н | Ставка (95% ДИ) |
| Вне беременности | 1105 | 4.2 (4.0–4.4) | 1015 | 3.8 (?) | 1480 | 3.2 (3.0–3.3) | 2895 | 3.6 (3.4–3.7) |
| Дородовый период | 995 | 20.5 (19.2–21.8) | 690 | 14.2 (13.2–15.3) | 156 | 9.9 (8.5–11.6) | 491 | 10.7 (9.7–11.6) |
| Триместр 1 | 207 | 13.6 (11.8–15.5) | 172 | 11.3 (9.7–13.1) | 23 | 4.6 (3.1–7.0) | 61 | 4.1 (3.2–5.2) |
| Триместр 2 | 275 | 17.4 (15.4–19.6) | 178 | 11.2 (9.7–13.0) | 30 | 5.8 (4.1–8.3) | 75 | 5.7 (4.6–7.2) |
| Триместр 3 | 513 | 29.2 (26.8–31.9) | 340 | 19.4 (17.4–21.6) | 103 | 18.2 (15.0–22.1) | 355 | 19.7 (17.7–21.9) |
| Вокруг доставки | 115 | 154.6 (128.8–185.6) | 79 | 106.1 (85.1–132.3) | 34 | 142.8 (102.0–199.8) | –
| |
| Послеродовой | 649 | 42.3 (39.2–45.7) | 509 | 33.1 (30.4–36.1) | 135 | 27.4 (23.1–32.4) | 218 | 17.5 (15.3–20.0) |
| Ранний послеродовой период | 584 | 75.4 (69.6–81.8) | 460 | 59.3 (54.1–65.0) | 177 | 46.8 (39.1–56.1) | 199 | 30.4 (26.4–35.0) |
| Поздний послеродовой период | 65 | 8.5 (7.0–10.9) | 49 | 6.4 (4.9–8.5) | 18 | 7.3 (4.6–11.6) | 319 | 3.2 (1.9–5.0) |
| Коэффициенты заболеваемости (IRR) первой ВТЭ во время беременности и в послеродовом периоде | ||||||||
| Шведские данные А | Шведские данные B | Английские данные | Датские данные | |||||
| Период времени | ВНД* (95% ДИ) | ВНД* (95% ДИ) | ВНД (95% ДИ)† | ВНД (95% ДИ)† | ||||
| Вне беременности | Ссылка (т. е. 1,00)
| |||||||
| Дородовый период | 5.08 (4.66–5.54) | 3.80 (3.44–4.19) | 3.10 (2.63–3.66) | 2.95 (2.68–3.25) | ||||
| Триместр 1 | 3.42 (2.95–3.98) | 3.04 (2.58–3.56) | 1.46 (0.96–2.20) | 1.12 (0.86–1.45) | ||||
| Триместр 2 | 4.31 (3.78–4.93) | 3.01 (2.56–3.53) | 1.82 (1.27–2.62) | 1.58 (1.24–1.99) | ||||
| Триместр 3 | 7.14 (6.43–7.94) | 5.12 (4.53–5.80) | 5.69 (4.66–6.95) | 5.48 (4.89–6.12) | ||||
| Вокруг доставки | 37.5 (30.9–44.45) | 27.97 (22.24–35.17) | 44.5 (31.68–62.54) | –
| ||||
| Послеродовой | 10.21 (9.27–11.25) | 8.72 (7.83–9.70) | 8.54 (7.16–10.19) | 4.85 (4.21–5.57) | ||||
| Ранний послеродовой период | 19.27 (16.53–20.21) | 15.62 (14.00–17.45) | 14.61 (12.10–17.67) | 8.44 (7.27–9.75) | ||||
| Поздний послеродовой период | 2.06 (1.60–2.64) | 1.69 (1.26–2.25) | 2.29 (1.44–3.65) | 0.89 (0.53–1.39) | ||||
| Примечания: шведские данные A = использование любого кода для VTE независимо от подтверждения. Шведские данные B = использование только ВТЭ, подтвержденного алгоритмом. Ранний послеродовой период = первые 6 недель после родов. Поздний послеродовой период = более 6 недель после родов. * = Скорректировано с учетом возраста и календарного года. † = Нескорректированный коэффициент, рассчитанный на основе предоставленных данных. Источник: [ 41 ] | ||||||||
Другие функции
[ редактировать ]Эстрадиол оказывает комплексное воздействие на печень . Он влияет на выработку множества белков , включая липопротеины , связывающие белки и белки, ответственные за свертывание крови . [ нужна ссылка ] В больших количествах эстрадиол может привести к холестазу , например, холестазу беременных .
Определенные гинекологические состояния зависят от эстрогена, такие как эндометриоз , лейомиома матки и маточные кровотечения . [ нужна ссылка ]
Биологическая активность
[ редактировать ]Эстрадиол действует главным образом как агонист ( рецептора эстрогена ER), ядерного рецептора стероидных гормонов . Существует два подтипа ER: ERα и ERβ , и эстрадиол мощно связывается и активирует оба этих рецептора. Результатом активации ER является модуляция генов транскрипции и экспрессии , экспрессирующих ER в клетках , что является преобладающим механизмом, с помощью которого эстрадиол опосредует свои биологические эффекты в организме. Эстрадиол также действует как агонист мембранных рецепторов эстрогена (mER), таких как GPER (GPR30), недавно обнаруженный неядерный рецептор эстрадиола, посредством которого он может опосредовать множество быстрых негеномных эффектов . [ 42 ] В отличие от случая ER, GPER, по-видимому, селективен в отношении эстрадиола и демонстрирует очень низкое сродство к другим эндогенным эстрогенам, таким как эстрон и эстриол . [ 43 ] Дополнительные mER, помимо GPER, включают ER-X , ERx и Gq - mER . [ 44 ] [ 45 ]
ERα/ERβ находятся в неактивном состоянии и захвачены мультимолекулярными шаперонными комплексами, организованными вокруг белка теплового шока 90 (HSP90), содержащего белок p23, и иммунофилина, и локализованы в основном в цитоплазме и частично в ядре. По классическому пути E2 или классическому пути эстрогена эстрадиол попадает в цитоплазму , где взаимодействует с ЭР. После связывания E2 ER диссоциируют от комплексов молекулярных шаперонов и становятся способными димеризоваться, мигрировать в ядро и связываться со специфическими последовательностями ДНК ( элемент ответа на эстроген , ERE), что обеспечивает транскрипцию генов, которая может происходить в течение часов и дней.
При подкожной инъекции мышам эстрадиол примерно в 10 раз более эффективен, чем эстрон, и примерно в 100 раз более эффективен, чем эстриол. [ 46 ] [ 47 ] [ 48 ] Таким образом, эстрадиол является основным эстрогеном в организме, хотя считается, что роль эстрона и эстриола как эстрогенов не является незначительной. [ 48 ]
| Эстроген | Подсказка ER Подсказка RBA (%) | Вес матки (%) | Утеротрофия | Подсказка по ЛГ (%) | SHBG RBA (%) |
|---|---|---|---|---|---|
| Контроль | – | 100 | – | 100 | – |
| Эстрадиол (E2) | 100 | 506 ± 20 | +++ | 12–19 | 100 |
| Эстрон (E1) | 11 ± 8 | 490 ± 22 | +++ | ? | 20 |
| Эстриол (Е3) | 10 ± 4 | 468 ± 30 | +++ | 8–18 | 3 |
| Эстетрол (Е4) | 0.5 ± 0.2 | ? | Неактивный | ? | 1 |
| 17α-эстрадиол | 4.2 ± 0.8 | ? | ? | ? | ? |
| 2-гидроксиэстрадиол | 24 ± 7 | 285 ± 8 | + б | 31–61 | 28 |
| 2-метоксиэстрадиол | 0.05 ± 0.04 | 101 | Неактивный | ? | 130 |
| 4-гидроксиэстрадиол | 45 ± 12 | ? | ? | ? | ? |
| 4-метоксиэстрадиол | 1.3 ± 0.2 | 260 | ++ | ? | 9 |
| 4-фторэстрадиол а | 180 ± 43 | ? | +++ | ? | ? |
| 2-гидроксиэстрон | 1.9 ± 0.8 | 130 ± 9 | Неактивный | 110–142 | 8 |
| 2-метоксиэстрон | 0.01 ± 0.00 | 103 ± 7 | Неактивный | 95–100 | 120 |
| 4-гидроксиэстрон | 11 ± 4 | 351 | ++ | 21–50 | 35 |
| 4-метоксиэстрон | 0.13 ± 0.04 | 338 | ++ | 65–92 | 12 |
| 16α-гидроксиэстрон | 2.8 ± 1.0 | 552 ± 42 | +++ | 7–24 | <0,5 |
| 2-гидроксистриол | 0.9 ± 0.3 | 302 | + б | ? | ? |
| 2-метоксиэстриол | 0.01 ± 0.00 | ? | Неактивный | ? | 4 |
| Примечания: Значения являются средними ± SD или диапазоном. ER RBA = Относительное сродство связывания с эстрогеновыми рецепторами крысы матки цитозоля . Масса матки = процентное изменение сырой массы матки у крыс с удаленными яичниками через 72 часа при непрерывном введении 1 мкг/час с помощью подкожно имплантированных осмотических насосов . Уровни ЛГ = уровни лютеинизирующего гормона относительно исходного уровня у крыс с удаленными яичниками после 24–72 часов непрерывного введения через подкожный имплантат. Сноски: а = Синтетический (т.е. не эндогенный ). б = Атипичный утеротрофический эффект, который достигает плато в течение 48 часов (утеротрофия эстрадиола продолжается линейно до 72 часов). Источники: см. шаблон. | |||||
Биохимия
[ редактировать ]
Биосинтез
[ редактировать ]Эстрадиол, как и другие стероидные гормоны , образуется из холестерина . После расщепления боковой цепи и использования Δ 5 или Δ 4 - путь, андростендион ключевым посредником является . Часть андростендиона превращается в тестостерон, который, в свою очередь, под действием ароматазы превращается в эстрадиол. Альтернативным путем андростендион ароматизируется в эстрон , который впоследствии превращается в эстрадиол с помощью 17β-гидроксистероиддегидрогеназы (17β-HSD). [ 50 ]
В репродуктивном возрасте большая часть эстрадиола у женщин вырабатывается гранулезными клетками яичников путем ароматизации андростендиона (продуцируемого в клетках теки фолликулов) в эстрон с последующим превращением эстрона в эстрадиол с помощью 17β-HSD. Меньшие количества эстрадиола также вырабатываются корой надпочечников , а у мужчин - яичками. [ нужна медицинская ссылка ]
Эстрадиол вырабатывается не только в гонадах ; в частности, жировые клетки производят активные предшественники эстрадиола и будут продолжать делать это даже после менопаузы. [ 51 ] Эстрадиол также вырабатывается в головном мозге и стенках артерий .
У мужчин примерно от 15 до 25% циркулирующего эстрадиола вырабатывается в яичках . [ 52 ] [ 53 ] Остальное синтезируется посредством периферической ароматизации тестостерона в эстрадиол и андростендиона в эстрон (который затем трансформируется в эстрадиол через периферический 17β-HSD). [ 52 ] [ 53 ] Эта периферическая ароматизация происходит преимущественно в жировой ткани , но также происходит и в других тканях, таких как кости , печень и мозг . [ 52 ] У мужчин в день вырабатывается примерно от 40 до 50 мкг эстрадиола. [ 52 ]
Распределение
[ редактировать ]В плазме эстрадиол в значительной степени связан с ГСПГ и альбумином . Лишь около 2,21% (±0,04%) эстрадиола является свободным и биологически активным. Процент остается постоянным на протяжении всего менструального цикла . [ 54 ]
Метаболизм
[ редактировать ] Метаболические пути эстрадиола у человека
|
Инактивация эстрадиола включает преобразование в менее активные эстрогены, такие как эстрон и эстриол. Эстриол является основным метаболитом мочи . [ нужна ссылка ] Эстрадиол конъюгируется в печени с образованием конъюгатов эстрогена, таких как сульфат эстрадиола , глюкуронид эстрадиола , и, как таковые, выводится через почки . Некоторые из водорастворимых конъюгатов выводятся через желчные протоки и частично реабсорбируются после гидролиза из кишечного тракта . Эта энтерогепатическая циркуляция способствует поддержанию уровня эстрадиола.
Эстрадиол также метаболизируется посредством гидроксилирования в катехол-эстрогены . В печени он неспецифически метаболизируется CYP1A2 , CYP3A4 и CYP2C9 посредством 2-гидроксилирования в 2-гидроксиэстрадиол , а также CYP2C9 , CYP2C19 и CYP2C8 посредством 17β-гидроксидегидрирования в эстрон . [ 55 ] различные другие цитохрома P450 (CYP) ферменты и метаболические преобразования . при этом также участвуют [ 56 ]
Эстрадиол дополнительно конъюгируется со сложным эфиром в липоидные формы эстрадиола, такие как пальмитат эстрадиола и стеарат эстрадиола, в определенной степени; эти эфиры хранятся в жировой ткани и могут действовать как очень длительный резервуар эстрадиола. [ 57 ] [ 58 ]
Экскреция
[ редактировать ]Эстрадиол выводится в виде глюкуронидных и сульфатных эстрогеновых конъюгатов с мочой . После внутривенного введения меченого . эстрадиола женщинам почти 90% выводится с мочой и калом в течение 4–5 дней [ 59 ] [ 60 ] Энтерогепатическая рециркуляция вызывает задержку выведения эстрадиола. [ 59 ]
Уровни
[ редактировать ]
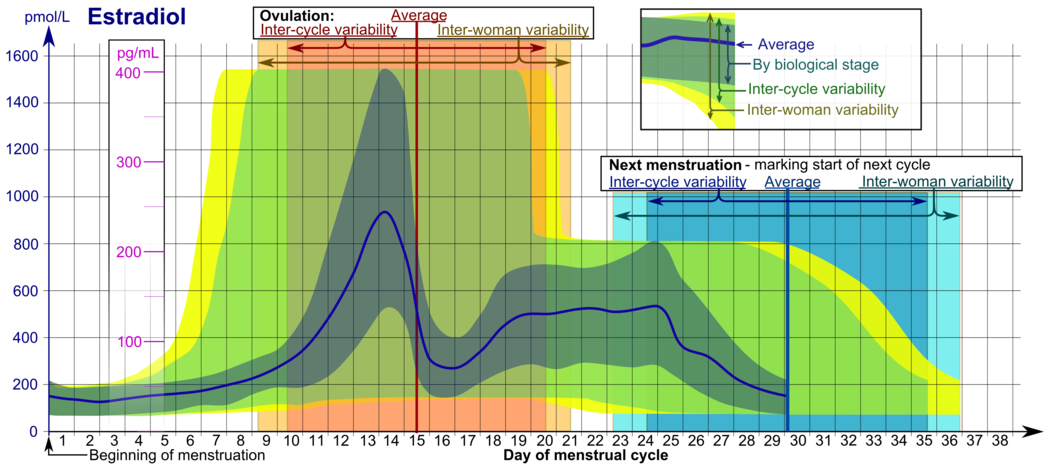
Уровни эстрадиола у женщин в пременопаузе сильно варьируются на протяжении менструального цикла, а референтные диапазоны широко варьируются от источника к источнику. [ 62 ] Уровни эстрадиола минимальны и, по данным большинства лабораторий, колеблются от 20 до 80 пг/мл во время ранней и средней фолликулярной фазы (или первой недели менструального цикла, также известной как менструация). [ 63 ] [ 64 ] Уровни эстрадиола постепенно повышаются в это время и в середине и конце фолликулярной фазы (или второй недели менструального цикла) до предовуляторной фазы. [ 62 ] [ 63 ] Во время предовуляции (период примерно от 24 до 48 часов) уровни эстрадиола ненадолго повышаются и достигают самых высоких концентраций в любое другое время менструального цикла. [ 62 ] Уровни циркулирующей крови в это время обычно составляют от 130 до 200 пг/мл, но у некоторых женщин могут достигать 300–400 пг/мл, а верхний предел референсного диапазона некоторых лабораторий даже выше (например, 750 пг/мл). пг/мл). [ 62 ] [ 63 ] [ 65 ] [ 66 ] [ 67 ] После овуляции (или в середине цикла) и во второй половине менструального цикла или лютеиновой фазы уровни эстрадиола выходят на плато и колеблются между 100 и 150 пг/мл в раннюю и среднюю лютеиновую фазы, а также во время поздней овуляции. лютеиновая фаза или за несколько дней до менструации достигают минимума около 40 пг/мл. [ 62 ] [ 64 ] В разных источниках сообщается, что средние интегрированные уровни эстрадиола в течение полного менструального цикла составляют 80, 120 и 150 пг/мл. [ 64 ] [ 68 ] [ 69 ] Хотя существуют противоречивые сообщения, одно исследование показало, что средний интегрированный уровень эстрадиола составляет 150 пг/мл у молодых женщин, тогда как средний интегрированный уровень варьируется от 50 до 120 пг/мл у пожилых женщин. [ 69 ]
В репродуктивном возрасте у женщин уровень эстрадиола несколько выше, чем уровень эстрона, за исключением ранней фолликулярной фазы менструального цикла; таким образом, эстрадиол можно считать преобладающим эстрогеном в репродуктивный период у женщин с точки зрения абсолютных уровней в сыворотке и эстрогенной активности. [ нужна ссылка ] Во время беременности эстриол становится преобладающим циркулирующим эстрогеном, и это единственный раз, когда эстрол появляется в организме, тогда как во время менопаузы преобладает эстрон (оба основаны на уровнях сыворотки). [ нужна ссылка ] Эстрадиол, вырабатываемый мужчинами из тестостерона, присутствует на уровнях сыворотки, примерно сопоставимых с уровнями у женщин в постменопаузе (14–55 против <35 пг/мл соответственно). [ нужна ссылка ] Также сообщалось, что если сравнить концентрацию эстрадиола у 70-летнего мужчины с концентрацией эстрадиола у 70-летней женщины, то уровни у мужчины будут примерно в 2–4 раза выше. [ 70 ]
| Группа | E2 ( прод .) | E2 (уровни) | E1 (уровни) | Соотношение |
|---|---|---|---|---|
| пубертатного возраста Девочки а Таннер I стадия (детство) Таннер, стадия II (8–12 лет) Стадия Таннера III (10–13 лет) Таннер, стадия IV (11–14 лет) Таннер, стадия V (12–15 лет) Фолликулярный (дни 1–14) Лютеиновая (15–28 дни) |
? ? ? ? ? ? |
9 (<9–20) пг/мл 15 (<9–30) пг/мл 27 (<9–60) пг/мл 55 (16-85) пг/мл 50 (30–100) пг/мл 130 (70–300) пг/мл |
13 (<9–23) пг/мл 18 (10-37) пг/мл 26 (17–58) пг/мл 36 (23-69) пг/мл 44 (30-89) пг/мл 75 (39–160) пг/мл |
? ? ? ? ? ? |
| препубертатного возраста Мальчики | ? | 2–8 пг/мл | ? | ? |
| в пременопаузе Женщины Ранняя фолликулярная фаза (1–4 дни) Средняя фолликулярная фаза (5–9 дни) Поздняя фолликулярная фаза (10–14 дни) Лютеиновая фаза (15–28 дни) Оральные контрацептивы ( ановуляторные ) |
30–100 мкг/день 100–160 мкг/день 320–640 мкг/день 300 мкг/день ? |
40-60 пг/мл 60–100 пг/мл 200–400 пг/мл 190 пг/мл 12–50 пг/мл |
40-60 пг/мл ? 170-200 пг/мл 100-150 пг/мл ? |
0.5–1 ? 1–2 1.5 ? |
| в постменопаузе Женщины | 18 мкг/день | 5–20 пг/мл | 30–70 пг/мл | 0.3–0.8 |
| Беременные женщины Первый триместр (1–12 недели) Второй триместр (13–26 недели) Третий триместр (27–40 недели) |
? ? ? |
1000–5000 пг/мл 5 000–15 000 пг/мл 10 000–40 000 пг/мл |
? ? ? |
? ? ? |
| Мужчины а | 20–60 мкг/день | 27 (20–55) пг/мл | 20–90 пг/мл | 0.4–0.6 |
| Сноски: а = Формат: «среднее значение (диапазон)» или просто «диапазон». Источники: [ 71 ] [ 72 ] [ 73 ] [ 74 ] [ 75 ] [ 61 ] [ 76 ] | ||||
Измерение
[ редактировать ]У женщин уровень эстрадиола в сыворотке крови измеряется в клинической лаборатории и отражает прежде всего активность яичников. Анализ крови на эстрадиол измеряет количество эстрадиола в крови. [ 77 ] Его применяют для проверки функции яичников, плаценты, надпочечников. [ 77 ] Это позволяет выявить исходный уровень эстрогена у женщин с аменореей или менструальной дисфункцией, а также выявить состояние гипоэстрогенности и менопаузы. Кроме того, мониторинг эстрогена во время терапии бесплодия позволяет оценить рост фолликулов и полезен при мониторинге лечения. Эстрогенпродуцирующие опухоли будут демонстрировать стойкие высокие уровни эстрадиола и других эстрогенов. При преждевременном половом созревании уровень эстрадиола неадекватно повышается.
Диапазоны
[ редактировать ]Результаты отдельных лабораторных исследований всегда следует интерпретировать с использованием диапазонов, предоставленных лабораторией, проводившей тест.
| Тип пациента | Нижний предел | Верхний предел | Единица |
|---|---|---|---|
| Взрослый мужчина | 50 [ 78 ] | 200 [ 78 ] | пмоль/л |
| 14 | 55 | пг/мл | |
| Взрослая самка ( фолликулярная фаза , день 5) |
70 [ 78 ] 95% ПИ (стандарт) |
500 [ 78 ] 95% ПИ |
пмоль/л |
| 110 [ 79 ] 90% ПИ (используется на схеме ) |
220 [ 79 ] 90% ПИ | ||
| 19 (95% ПИ) | 140 (95% ПИ) | пг/мл | |
| 30 (90% ПИ) | 60 (90% ПИ) | ||
| Взрослая самка ( преовуляторный пик) |
400 [ 78 ] | 1500 [ 78 ] | пмоль/л |
| 110 | 410 | пг/мл | |
| Взрослая женщина ( лютеиновая фаза ) |
70 [ 78 ] | 600 [ 78 ] | пмоль/л |
| 19 | 160 | пг/мл | |
| Взрослая женщина – бесплатно. (не связан с белком) |
0.5 [ 80 ] [ оригинальное исследование? ] | 9 [ 80 ] [ оригинальное исследование? ] | пг/мл |
| 1.7 [ 80 ] [ оригинальное исследование? ] | 33 [ 80 ] [ оригинальное исследование? ] | пмоль/л | |
| Женщина в постменопаузе | Н/Д [ 78 ] | < 130 [ 78 ] | пмоль/л |
| Н/Д | < 35 | пг/мл |
В нормальном менструальном цикле уровни эстрадиола обычно составляют <50 пг/мл во время менструации, повышаются по мере развития фолликула (пик: 200 пг/мл), кратковременно падают при овуляции и снова повышаются во время лютеиновой фазы, достигая второго пика. В конце лютеиновой фазы уровень эстрадиола падает до менструального уровня, если только не наступила беременность.
Во время беременности уровень эстрогена, включая эстрадиол, неуклонно повышается по мере приближения срока беременности. Источником этих эстрогенов является плацента , которая ароматизирует прогормоны, вырабатываемые в надпочечниках плода.
Медицинское использование
[ редактировать ]Эстрадиол используется в качестве менопаузы , а также в лекарства, в первую очередь в гормональной терапии симптомов феминизирующей гормональной терапии для трансгендеров. [ 82 ]
Химия
[ редактировать ] Структуры основных эндогенных эстрогенов
|
Эстрадиол – это эстрана стероид . [ 82 ] Он также известен как 17β-эстрадиол (в отличие от 17α-эстрадиола ) или как эстра-1,3,5(10)-триен-3,17β-диол. Он имеет две гидроксильные группы , одну в положении C3, другую в положении 17β, а также три двойные связи в кольце А. Из-за наличия двух гидроксильных групп эстрадиол часто обозначают сокращенно E2. Структурно родственные эстрогены: эстрон (Е1), эстриол (Е3) и эстетрол (Е4) имеют одну, три и четыре гидроксильные группы соответственно.
Нейропсихофармакология
[ редактировать ]В рандомизированном двойном слепом плацебо-контролируемом исследовании было показано, что эстрадиол не оказывает гендерно-специфического влияния на чувствительность к справедливости. В целом, когда разделение определенной суммы денег было представлено как справедливое или несправедливое в модифицированной версии игры-ультиматума , эстрадиол повышал уровень принятия справедливых предложений среди мужчин и снижал его среди женщин. Однако в группе плацебо «простая вера в получение лечения эстрадиолом значительно увеличила принятие несправедливо оформленных предложений у обоих полов», что указывает на то, что так называемые «окружающие» факторы сыграли роль в организации ответов на эти представления игра ультиматум . [ 83 ]
История
[ редактировать ]Открытие эстрогена обычно приписывают американским ученым Эдгару Аллену и Эдварду А. Дойзи . [ 84 ] [ 85 ] что инъекция жидкости из свиней фолликулов яичников вызывает изменения типа полового созревания и эструса (включая влагалища , матки и молочных желез изменения , а также сексуальную восприимчивость ) у половозрелых В 1923 году они заметили , мышей и крыс с удаленными яичниками . [ 84 ] [ 85 ] [ 86 ] Эти результаты продемонстрировали существование гормона , который вырабатывается яичниками и участвует в половом созревании и размножении . [ 84 ] [ 85 ] [ 86 ] На момент открытия Аллен и Дойзи не дали этому гормону названия, а просто называли его «гормоном яичников» или «фолликулярным гормоном»; [ 85 ] другие называли его по-разному: феминин , фолликулин , менформон , теликинин и эмменин . [ 87 ] [ 88 ] В 1926 году Паркс и Беллерби ввели термин «эстрин» для описания гормона, поскольку он вызывает течку у животных. [ 89 ] [ 87 ] Эстрон был выделен и очищен независимо Алленом, Дойзи и немецким ученым Адольфом Бутенандтом в 1929 году, а эстриол был выделен и очищен Маррианом в 1930 году; они были первыми идентифицированными эстрогенами. [ 85 ] [ 90 ] [ 91 ]
Эстрадиол, самый мощный из трех основных эстрогенов, был идентифицирован последним. [ 85 ] [ 89 ] Он был открыт Швенком и Хильдебрантом в 1933 году, которые синтезировали его путем восстановления эстрона. [ 85 ] Эстрадиол был впоследствии выделен и очищен из яичников свиноматок Дойзи в 1935 году, при этом его химическая структура : одновременно была определена [ 92 ] и назывался по-разному: дигидротелин , дигидрофолликулин , дигидрофолликулярный гормон и дигидроксиэстрин . [ 85 ] [ 93 ] [ 94 ] В 1935 году название «эстрадиол» и термин «эстроген» были официально установлены Комитетом по половым гормонам Организации здравоохранения Лиги Наций ; это последовало за названиями эстрон (который первоначально назывался теелин, прогинон, фолликулин и кетогидроксиэстрин) и эстриол (первоначально назывался теелол и тригидроксиэстрин), которые были установлены в 1932 году на первом заседании Международной конференции по стандартизации половых гормонов в Лондоне . [ 89 ] [ 95 ] После его открытия частичный синтез эстрадиола из холестерина был разработан Инхоффеном и Хольвегом в 1940 году, а полный синтез был разработан Аннером и Мишером в 1948 году. [ 85 ]
Общество и культура
[ редактировать ]Этимология
[ редактировать ]Название эстрадиол происходит от слова эстра- , греч. οἶστρος ( oistros , буквально означает «воодушевление или вдохновение»), [ 96 ] который относится к системе эстранового стероида кольцевой , и -диолу , химическому термину и суффиксу, указывающему на то, что соединение представляет собой тип спирта, несущего две гидроксильные группы .
Ссылки
[ редактировать ]- ^ Ford SR, Roach SS (7 октября 2013 г.). Вводная клиническая фармакология Роуча . Липпинкотт Уильямс и Уилкинс. стр. 525–. ISBN 978-1-4698-3214-2 .
- ^ Хочадел М. (1 апреля 2015 г.). Справочник Мосби по лекарствам для работников здравоохранения . Elsevier Науки о здоровье. стр. 602–. ISBN 978-0-323-31103-8 .
- ^ Перейти обратно: а б с д и Станчик Ф.З., Арчер Д.Ф., Бхавнани Б.Р. (июнь 2013 г.). «Этинилэстрадиол и 17β-эстрадиол в комбинированных пероральных контрацептивах: фармакокинетика, фармакодинамика и оценка риска». Контрацепция . 87 (6): 706–27. дои : 10.1016/j.contraception.2012.12.011 . ПМИД 23375353 .
- ^ Фальконе Т., Херд WW (2007). Клиническая репродуктивная медицина и хирургия . Elsevier Науки о здоровье. стр. 22–. ISBN 978-0-323-03309-1 . Архивировано из оригинала 10 января 2023 года . Проверено 22 октября 2016 г. .
- ^ Прайс ТМ, Блауэр К.Л., Хансен М., Станчик Ф., Лобо Р., Бейтс Г.В. (март 1997 г.). «Фармакокинетика однократного сублингвального и перорального введения микронизированного 17 бета-эстрадиола». Акушерство и гинекология . 89 (3): 340–5. дои : 10.1016/S0029-7844(96)00513-3 . ПМИД 9052581 . S2CID 71641652 .
- ^ Наунтон М., Аль Хадити А.Ф., Брауэрс-младший, Арчер Д.Ф. (2006). «Гель эстрадиола: обзор фармакологии, фармакокинетики, эффективности и безопасности у женщин в менопаузе». Менопауза . 13 (3): 517–27. дои : 10.1097/01.gme.0000191881.52175.8c . ПМИД 16735950 . S2CID 42748448 .
- ^ Райан К.Дж. (август 1982 г.). «Биохимия ароматазы: значение для женской репродуктивной физиологии». Исследования рака . 42 (8 дополнений): 3342–3344 с. ПМИД 7083198 .
- ^ Мешулам Р., Брюггемайер Р.В., Денлингер Д.Л. (сентябрь 1984 г.). «Эстрогены у насекомых». Клеточные и молекулярные науки о жизни . 40 (9): 942–944. дои : 10.1007/BF01946450 . S2CID 31950471 .
- ^ Озон Р. (1972). «Эстрогены у рыб, амфибий, рептилий и птиц» . В Idler DR (ред.). Стероиды у немлекопитающих позвоночных . Оксфорд: Elsevier Science. стр. 390–414. ISBN 978-0323140980 . Архивировано из оригинала 10 января 2023 года . Проверено 17 октября 2020 г.
- ^ Салданья, Колин Дж., Люк Ремидж-Хили и Барни А. Шлингер. «Синаптокринная передача сигналов: синтез стероидов и действие в синапсе». Эндокринные обзоры 32.4 (2011): 532–549.
- ^ Перейти обратно: а б с Макмиллан Дж. А., Фейгин Р. Д., ДеАнджелис С., Джонс, доктор медицинских наук (2006). Педиатрия Оски: принципы и практика . Липпинкотт Уильямс и Уилкинс. стр. 550–. ISBN 978-0-7817-3894-1 .
- ^ Перейти обратно: а б с Крейг CR, Ститцель Р.Э. (2004). Современная фармакология с клиническим применением . Липпинкотт Уильямс и Уилкинс. стр. 706–. ISBN 978-0-7817-3762-3 .
- ^ Preedy VR (2 декабря 2011 г.). Справочник по росту и мониторингу роста в сфере здравоохранения и болезней . Springer Science & Business Media. стр. 2661–. ISBN 978-1-4419-1794-2 . Архивировано из оригинала 10 января 2023 года . Проверено 9 июня 2017 г.
- ^ Карро С., Ламбард С., Делаланд С., Дени-Галеро И., Билинска Б., Бургиба С. (апрель 2003 г.). «Экспрессия ароматазы и роль эстрогенов в мужских гонадах: обзор» . Репродуктивная биология и эндокринология . 1:35 . дои : 10.1186/1477-7827-1-35 . ПМК 155680 . ПМИД 12747806 .
- ^ Пентикайнен В., Эрккиля К., Суомалайнен Л., Парвинен М., Дункель Л. (май 2000 г.). «Эстрадиол действует как фактор выживания зародышевых клеток в семенниках человека in vitro» . Журнал клинической эндокринологии и метаболизма . 85 (5): 2057–67. дои : 10.1210/jcem.85.5.6600 . ПМИД 10843196 .
- ^ Шарп Р.М., Скаккебек Н.Е. (май 1993 г.). «Участвуют ли эстрогены в падении количества сперматозоидов и нарушениях мужской репродуктивной системы?». Ланцет . 341 (8857): 1392–5. дои : 10.1016/0140-6736(93)90953-E . ПМИД 8098802 . S2CID 33135527 .
- ^ Хандельсман DJ (2001). «Эстрогены и падение количества сперматозоидов». Воспроизводство, рождаемость и развитие . 13 (4): 317–24. дои : 10.1071/rd00103 . ПМИД 11800170 .
- ^ Фиш Х., Гольдштедин Р. (2003). «Эстрогены окружающей среды и количество сперматозоидов» (PDF) . Чистая и прикладная химия . 75 (11–12): 2181–2193. дои : 10.1351/pac200375112181 . S2CID 11068097 . Архивировано из оригинала (PDF) 4 марта 2016 года . Проверено 29 декабря 2015 г.
- ^ Раман Дж.Д., Шлегель П.Н. (февраль 2002 г.). «Ингибиторы ароматазы при мужском бесплодии». Журнал урологии . 167 (2 Части 1): 624–9. дои : 10.1016/S0022-5347(01)69099-2 . ПМИД 11792932 .
- ^ Висоотсак Дж., Грэм Дж. М. (октябрь 2006 г.). «Синдром Клайнфельтера и другие половые хромосомные анеуплоидии» . Сиротский журнал редких заболеваний . 1 (42): 42. дои : 10.1186/1750-1172-1-42 . ПМЦ 1634840 . ПМИД 17062147 .
- ^ Вандершуерен Д., Лоран М.Р., Классенс Ф., Гилен Э., Лагерквист М.К., Ванденпут Л. и др. (декабрь 2014 г.). «Действие половых стероидов на мужские кости» . Эндокринные обзоры . 35 (6): 906–60. дои : 10.1210/er.2014-1024 . ПМЦ 4234776 . ПМИД 25202834 .
- ^ Карани С., Цинь К., Симони М., Фаустини-Фустини М., Серпенте С., Бойд Дж. и др. (июль 1997 г.). «Влияние тестостерона и эстрадиола на мужчину с дефицитом ароматазы» . Медицинский журнал Новой Англии . 337 (2): 91–5. дои : 10.1056/NEJM199707103370204 . ПМИД 9211678 .
- ^ Берг К., Веннергрен Д., Мёллер М., Брисби Х. (21 декабря 2020 г.). «Распространенность переломов у взрослых в зависимости от возраста и пола: исследование 27 169 переломов в Шведском регистре переломов в четко определенной зоне охвата» . ПЛОС ОДИН . 15 (12): e0244291. Бибкод : 2020PLoSO..1544291B . дои : 10.1371/journal.pone.0244291 . ПМК 7751975 . ПМИД 33347485 .
- ^ Олбрайт Ф. , Смит П.Х., Ричардсон А.М. (31 мая 1941 г.). «Постменопаузальный остеопороз: его клинические особенности». ДЖАМА . 116 (22): 2465–2474. дои : 10.1001/jama.1941.02820220007002 .
- ^ Перейти обратно: а б с д и ж г час Рейн-Феннинг, штат Нью-Джерси, член парламента от Бринката, Маскат-Барон Y (2003). «Старение кожи и менопауза: последствия для лечения». Американский журнал клинической дерматологии . 4 (6): 371–8. дои : 10.2165/00128071-200304060-00001 . ПМИД 12762829 . S2CID 20392538 .
- ^ Перейти обратно: а б с д и ж г час Хольцер Г., Риглер Э., Хёнигсманн Х., Фарохния С., Шмидт Ю.Б., Шмидт Б. (сентябрь 2005 г.). «Влияние и побочные эффекты 2% крема с прогестероном на кожу женщин в пери- и постменопаузе: результаты двойного слепого, контролируемого, рандомизированного исследования». Британский журнал дерматологии . 153 (3): 626–34. дои : 10.1111/j.1365-2133.2005.06685.x . ПМИД 16120154 . S2CID 6077829 .
- ^ Бел С., Видманн М., Трапп Т., Холсбур Ф. (ноябрь 1995 г.). «17-бета-эстрадиол защищает нейроны от гибели клеток, вызванной окислительным стрессом in vitro». Связь с биохимическими и биофизическими исследованиями . 216 (2): 473–82. дои : 10.1006/bbrc.1995.2647 . ПМИД 7488136 .
- ^ Митал С.В., Лю Т., Чан Х.В., Гинзбург Э., Уилсон А.С., Грей Д.Н., Боуэн Р.Л., Вондерхаар Б.К., Этвуд К.С. (август 2009 г.). «Идентификация регуляторной петли синтеза нейростероидов: стероидогенный острый регуляторный белково-зависимый механизм с участием рецепторов гипоталамо-гипофизарно-гонадной оси» . Журнал нейрохимии . 110 (3): 1014–27. дои : 10.1111/j.1471-4159.2009.06192.x . ПМЦ 2789665 . ПМИД 19493163 .
- ^ Дума С.Л., Муж С., О'Доннелл М.Э., Барвин Б.Н., Вуденд А.К. (2005). «Расстройства настроения, связанные с эстрогеном: факторы репродуктивного жизненного цикла». Достижения в области сестринского дела . 28 (4): 364–75. дои : 10.1097/00012272-200510000-00008 . ПМИД 16292022 . S2CID 9172877 .
- ^ Ласюк Г.Ц., Хегадорен К.М. (октябрь 2007 г.). «Влияние эстрадиола на центральные серотонинергические системы и его связь с настроением у женщин». Биологические исследования для медсестер . 9 (2): 147–60. дои : 10.1177/1099800407305600 . ПМИД 17909167 . S2CID 37965502 .
- ^ Хулсхофф Х.Э., Коэн-Кеттенис П.Т., Ван Харен Н.Е., Пепер Дж.С., Бранс Р.Г., Кан В., Шнак Х.Г., Гурен Л.Дж., Кан Р.С. (июль 2006 г.). «Смена пола меняет ваш мозг: влияние тестостерона и эстрогена на структуру мозга взрослого человека» . Европейский журнал эндокринологии . 155 (приложение_1): 107–114. дои : 10.1530/eje.1.02248 .
- ^ Хардинг CF (июнь 2004 г.). «Гормональная модуляция пения: гормональная модуляция мозга певчих птиц и певческое поведение» . Анналы Нью-Йоркской академии наук . 1016 (1): 524–39. Бибкод : 2004NYASA1016..524H . дои : 10.1196/анналы.1298.030 . ПМИД 15313793 . S2CID 12457330 . Архивировано из оригинала 27 сентября 2007 года.
- ^ Симерли РБ (27 марта 2002 г.). «Настроен на размножение: организация и развитие цепей полового диморфизма в переднем мозге млекопитающих» (PDF) . Ежегодный обзор неврологии . 25 : 507–36. дои : 10.1146/annurev.neuro.25.112701.142745 . ПМИД 12052919 . Архивировано из оригинала (PDF) 1 октября 2008 года . Проверено 7 марта 2007 г.
- ^ Гольдштейн И., Местон С.М., Дэвис С., Трейш А. (17 ноября 2005 г.). Женская сексуальная функция и дисфункция: исследование, диагностика и лечение . ЦРК Пресс. стр. 205–. ISBN 978-1-84214-263-9 .
- ^ Асеведо-Родригес А., Мани С.К., Ханда Р.Дж. (2015). «Окситоцин и рецептор эстрогена β в мозге: обзор» . Границы эндокринологии . 6 : 160. дои : 10.3389/fendo.2015.00160 . ПМК 4606117 . ПМИД 26528239 .
- ^ Бульзоми П., Болли А., Галлуццо П., Леоне С., Акконча Ф., Марино М. (январь 2010 г.). «Совместное применение нарингенина и 17-бета-эстрадиола предотвращает гормон-индуцированный рост раковых клеток человека» . ИУБМБ Жизнь . 62 (1): 51–60. дои : 10.1002/iub.279 . ПМИД 19960539 . S2CID 7903757 .
- ^ Шриджа С., Сантош Кумар Т.Р., Лакшми Б.С., Шриджа С. (июль 2012 г.). «Экстракт граната демонстрирует профиль селективного модулятора рецепторов эстрогена в линиях опухолевых клеток человека и моделях депривации эстрогена in vivo». Журнал пищевой биохимии . 23 (7): 725–32. дои : 10.1016/j.jnutbio.2011.03.015 . ПМИД 21839626 .
- ^ Томас К.Г., Стром А., Линдберг К., Густафссон Дж.А. (июнь 2011 г.). «Бета-рецептор эстрогена снижает выживаемость раковых клеток с дефектом p53 после повреждения ДНК за счет нарушения передачи сигналов контрольной точки G₂/M». Исследование и лечение рака молочной железы . 127 (2): 417–27. дои : 10.1007/s10549-010-1011-z . ПМИД 20623183 . S2CID 6752694 .
- ^ Коллинз П., Розано Г.М., Саррел П.М., Ульрих Л., Адамопулос С., Бил К.М., Макнил Дж.Г., Пул-Уилсон П.А. (июль 1995 г.). «17-бета-эстрадиол ослабляет вызванное ацетилхолином сужение коронарных артерий у женщин, но не у мужчин с ишемической болезнью сердца». Тираж . 92 (1): 24–30. дои : 10.1161/01.CIR.92.1.24 . ПМИД 7788912 .
- ^ Ноултон, А.А.; Ли, Арканзас (июль 2012 г.). «Эстроген и сердечно-сосудистая система» . Фармакология и терапия . 135 (1): 54–70. doi : 10.1016/j.pharmthera.2012.03.007 . ПМК 5688223 . ПМИД 22484805 .
- ^ Абдул Султан А, Вест Дж, Стефанссон О, Грейндж М.Дж., Тата Л.Дж., Флеминг К.М., Хьюмс Д., Людвигссон Дж.Ф. (ноябрь 2015 г.). «Определение венозной тромбоэмболии и измерение ее заболеваемости с использованием шведских реестров здравоохранения: общенациональное когортное исследование беременных» . БМЖ Опен . 5 (11): e008864. doi : 10.1136/bmjopen-2015-008864 . ПМЦ 4654387 . ПМИД 26560059 .
- ^ Просниц Э.Р., Бартон М. (май 2014 г.). «Биология эстрогена: новое понимание функции GPER и клинических возможностей» . Молекулярная и клеточная эндокринология . 389 (1–2): 71–83. дои : 10.1016/j.mce.2014.02.002 . ПМК 4040308 . ПМИД 24530924 .
- ^ Просниц Э.Р., Артерберн Дж.Б., Склар Л.А. (2007). «GPR30: рецептор эстрогена, связанный с белком AG» . Мол. Клетка. Эндокринол . 265–266: 138–42. дои : 10.1016/j.mce.2006.12.010 . ПМЦ 1847610 . ПМИД 17222505 .
- ^ Солтысик К., Чекай П. (апрель 2013 г.). «Мембранные рецепторы эстрогена – альтернативный ли путь действия эстрогенов?». Журнал физиологии и фармакологии . 64 (2): 129–42. ПМИД 23756388 .
- ^ Мицевич П.Е., Келли М.Дж. (2012). «Мембранная регуляция функции гипоталамуса эстрогеновыми рецепторами» . Нейроэндокринология . 96 (2): 103–10. дои : 10.1159/000338400 . ПМЦ 3496782 . ПМИД 22538318 .
- ^ Лабхарт А. (6 декабря 2012 г.). Клиническая эндокринология: теория и практика . Springer Science & Business Media. стр. 548–. ISBN 978-3-642-96158-8 . Архивировано из оригинала 10 января 2023 года . Проверено 11 ноября 2018 г.
- ^ Такер С.Б. (2007). Физиология матери, плода и новорожденного: клиническая перспектива . Elsevier Науки о здоровье. стр. 43–. ISBN 978-1-4160-2944-1 . Архивировано из оригинала 10 января 2023 года . Проверено 7 июня 2017 г.
- ^ Перейти обратно: а б Зал JE (31 мая 2015 г.). Электронная книга «Учебник медицинской физиологии Гайтона и Холла» . Elsevier Науки о здоровье. стр. 1043–. ISBN 978-0-323-38930-3 .
- ^ Хэггстрем М., Ричфилд Д. (2014). «Схема путей стероидогенеза человека» . Викижурнал медицины . 1 (1). дои : 10.15347/wjm/2014.005 . ISSN 2002-4436 .
- ^ Бор В.Ф., Булпаеп Э.Л. (2003). Медицинская физиология: клеточный и молекулярный подход . Эльзевир/Сондерс. п. 1300. ISBN 978-1-4160-2328-9 .
- ^ Мучлер Э., Шефер-Кортинг М (2001). Эффекты лекарств (на немецком языке) (8-е изд.). Штутгарт: Научное издательство. стр. 434, 444. ISBN. 978-3-8047-1763-3 .
- ^ Перейти обратно: а б с д Мелмед С. (1 января 2016 г.). Учебник эндокринологии Уильямса . Elsevier Науки о здоровье. стр. 710–. ISBN 978-0-323-29738-7 . Архивировано из оригинала 10 января 2023 года . Проверено 21 марта 2018 г.
- ^ Перейти обратно: а б Маркус Р., Фельдман Д., Демпстер Д.В., Лаки М., Коли Дж.А. (13 июня 2013 г.). Остеопороз . Академическая пресса. стр. 331–. ISBN 978-0-12-398252-0 .
- ^ Ву Ч., Мотохаши Т., Абдель-Рахман Х.А., Фликингер Г.Л., Михаил Г. (август 1976 г.). «Свободный и связанный с белками эстрадиол-17 бета в плазме во время менструального цикла». Журнал клинической эндокринологии и метаболизма . 43 (2): 436–45. doi : 10.1210/jcem-43-2-436 . ПМИД 950372 .
- ^ Ченг З.Н., Шу Ю, Лю Цзюй, Ван Л.С., Оу-Ян Д.С., Чжоу Х.Х. (февраль 2001 г.). «Роль цитохрома P450 в метаболизме эстрадиола in vitro». Акта Фармакологика Синика . 22 (2): 148–54. ПМИД 11741520 .
- ^ Ли А.Дж., Цай М.Х., Томас П.Е., Конни А.Х., Чжу Б.Т. (август 2003 г.). «Характеристика окислительных метаболитов 17бета-эстрадиола и эстрона, образованных 15 селективно экспрессируемыми изоформами цитохрома p450 человека» . Эндокринология . 144 (8): 3382–98. дои : 10.1210/en.2003-0192 . ПМИД 12865317 .
- ^ Эттель М., Шиллингер Э (6 декабря 2012 г.). Эстрогены и антиэстрогены I: физиология и механизмы действия эстрогенов и антиэстрогенов . Springer Science & Business Media. стр. 235–237. ISBN 978-3-642-58616-3 .
- ^ Эттель М., Шиллингер Э (6 декабря 2012 г.). Эстрогены и антиэстрогены II: фармакология и клиническое применение эстрогенов и антиэстрогенов . Springer Science & Business Media. стр. 268, 271. ISBN. 978-3-642-60107-1 .
- ^ Перейти обратно: а б Дорфман, Ральф И. (1961). «Метаболизм стероидных гормонов». Радиоактивные изотопы в физиологической диагностике и терапии / Искусственные радиоактивные изотопы в физиологической диагностике и терапии . стр. 1223–1241. дои : 10.1007/978-3-642-49761-2_39 . ISBN 978-3-642-49477-2 .
- ^ Сандберг А.А., Слонуайт В.Р. (август 1957 г.). «Исследования фенольных стероидов на людях. II. Метаболическая судьба и гепато-билиарно-энтеральная циркуляция С14-эстрона и С14-эстрадиола у женщин» . Дж. Клин. Инвестируйте . 36 (8): 1266–78. дои : 10.1172/JCI103524 . ПМЦ 1072719 . ПМИД 13463090 .
- ^ Перейти обратно: а б «Эстрадиол» (PDF) . ilexmedical.com . Архивировано (PDF) из оригинала 4 февраля 2024 года . Проверено 4 июля 2024 г.
- ^ Перейти обратно: а б с д и Беккер Дж.Б., Беркли К.Дж., Гири Н., Хэмпсон Э., Херман Дж.П. , Янг Э. (4 декабря 2007 г.). Половые различия в мозге: от генов к поведению . Издательство Оксфордского университета. стр. 64–. ISBN 978-0-19-804255-6 .
Уровни эстрадиола минимальны в первые дни фолликулярной фазы, но по мере созревания фолликула его концентрация увеличивается в общем кровообращении. Самые высокие уровни достигаются примерно за 24–48 часов до пика ЛГ. Фактически, предовуляторный пик эстрадиола представляет собой его самую высокую концентрацию в течение всего менструального цикла. Концентрации в сыворотке крови в это время обычно составляют около 130–200 пг/мл, но у некоторых женщин могут достигаться концентрации до 300–400 пг/мл. После временного снижения, связанного с овуляцией, секреция эстрадиола восстанавливается за счет продукции желтого тела во время лютеиновой фазы. Уровни плато около 100–150 пг/мл (Abraham, 1978; Thorneycroft et al., 1971) чаще всего наблюдаются в период от -10 до -5 дней до начала менструации. По мере регрессии желтого тела уровень эстрадиола падает постепенно у некоторых женщин и резко у других в течение последних нескольких дней лютеиновой фазы. Это приводит к наступлению менструации и отторжению эндометрия. Уровень эстрадиола в сыворотке крови во время менструации составляет примерно 30–50 пг/мл. (Источник.)
- ^ Перейти обратно: а б с Штраус-младший, Барбьери Р.Л. (2009). Репродуктивная эндокринология Йена и Яффе: физиология, патофизиология и клиническое ведение . Elsevier Науки о здоровье. стр. 807–. ISBN 978-1-4160-4907-4 . Архивировано из оригинала 10 января 2023 года . Проверено 21 декабря 2016 г.
В большинстве лабораторий уровни эстрадиола в сыворотке колеблются от 20 до 80 пг/мл в раннюю и среднюю фолликулярную фазу менструального цикла и достигают пика от 200 до 500 пг/мл во время предовуляторного всплеска. В среднелютеиновую фазу уровни эстрадиола в сыворотке колеблются от 60 до 200 пг/мл.
- ^ Перейти обратно: а б с Кристиан С., фон Шульц Б (15 марта 1994 г.). Заместительная гормональная терапия: стандартизированные или индивидуально адаптированные дозы? . ЦРК Пресс. стр. 60–. ISBN 978-1-85070-545-1 .
Уровни эстрадиола в плазме колеблются от 40 до 80 пг/мл в течение 1-й недели овариального цикла (ранняя фолликулярная фаза) и от 80 до 300 пг/мл в течение 2-й недели (средняя и поздняя фолликулярная фаза, включая периовуляторный пик). Затем в течение 3-й и 4-й недель уровень эстрадиола колеблется от 100–150 пг/мл (ранняя и средняя лютеиновая фаза) до 40 пг/мл за несколько дней до менструации (поздняя лютеиновая фаза). Средний уровень интегрированного эстрадиола в течение полного 28-дневного нормального цикла составляет около 80 пг/мл.
- ^ Джеймсон Дж.Л., Де Гроот LJ (18 мая 2010 г.). Эндокринология: взрослая и детская . Elsevier Науки о здоровье. стр. 2812–. ISBN 978-1-4557-1126-0 .
Середина цикла: 150–750 пг/мл.
- ^ Хэй И.Д., Васс Дж.А. (26 января 2009 г.). Клиническая эндокринная онкология . Джон Уайли и сыновья. стр. 623–. ISBN 978-1-4443-0023-9 .
Середина цикла: 110–330 пг/мл.
- ^ Донс РФ (12 июля 1994 г.). Руководство по эндокринным и метаболическим тестам . ЦРК Пресс. стр. 8–. ISBN 978-0-8493-7657-3 .
Овуляторный: 200-400 пг/мл
- ^ Нотеловиц М., ван Кип, Пенсильвания (6 декабря 2012 г.). Климактерический период в перспективе: материалы Четвертого Международного конгресса по менопаузе, проходившего в Лейк-Буэна-Виста, Флорида, 28 октября - 2 ноября 1984 г. Springer Science & Business Media. стр. 397–. ISBN 978-94-009-4145-8 . Архивировано из оригинала 10 января 2023 года . Проверено 22 октября 2016 г. .
[...] после менопаузы уровень циркулирующего эстрадиола снижается со среднего значения в пременопаузе, составляющего 120 пг/мл, до всего лишь 13 пг/мл.
- ^ Перейти обратно: а б Мюллер Э.Э., Маклауд Р.М. (6 декабря 2012 г.). Нейроэндокринные перспективы . Springer Science & Business Media. стр. 121–. ISBN 978-1-4612-3554-5 . Архивировано из оригинала 10 января 2023 года . Проверено 22 октября 2016 г. .
[...] [пременопаузальная] средняя концентрация [эстрадиола] 150 пг/мл [...]
- ^ Сайед Ю., Таксел П. (декабрь 2003 г.). «Применение эстрогеновой терапии у мужчин». Современное мнение в фармакологии . 3 (6): 650–4. дои : 10.1016/j.coph.2003.07.004 . ПМИД 14644018 .
- ^ Николс К.К., Шенкель Л., Бенсон Х. (1984). «17-бета-эстрадиол для заместительной терапии эстрогенами в постменопаузе». Акушерский гинекологический сурв . 39 (4): 230–45. дои : 10.1097/00006254-198404000-00022 . ПМИД 6717863 .
- ^ Синтия К. Чернеки; Барбара Дж. Бергер (31 октября 2012 г.). Лабораторные исследования и диагностические процедуры – Электронная книга . Elsevier Науки о здоровье. стр. 100-1 488–. ISBN 978-1-4557-4502-9 . Архивировано из оригинала 22 августа 2023 года . Проверено 22 августа 2023 г.
- ^ Пауэрс М.С., Шенкель Л., Дарли П.Е., Гуд В.Р., Балестра Дж.К., Плейс, Вирджиния (август 1985 г.). «Фармакокинетика и фармакодинамика трансдермальных лекарственных форм 17 бета-эстрадиола: сравнение с обычными пероральными эстрогенами, используемыми для заместительной гормональной терапии». Являюсь. Дж. Обстет. Гинекол . 152 (8): 1099–106. дои : 10.1016/0002-9378(85)90569-1 . ПМИД 2992279 .
- ^ Кеннет Л. Беккер (2001). Принципы и практика эндокринологии и обмена веществ . Липпинкотт Уильямс и Уилкинс. стр. 889, 1059–1060, 2153. ISBN. 978-0-7817-1750-2 .
- ^ Лалит Баджадж; Стивен Берман (1 января 2011 г.). Принятие педиатрических решений по Берману . Elsevier Науки о здоровье. стр. 160–. ISBN 978-0-323-05405-8 . Архивировано из оригинала 11 января 2023 года . Проверено 22 августа 2023 г.
- ^ Куль Х (2003). «Эстрогены для мужчин?» [Эстрогены для мужчины?]. Сосредоточьтесь на мужчине . 1 (3): 6–12. ISSN 1727-0669 . Архивировано из оригинала 22 августа 2023 года . Проверено 22 августа 2023 г.
- ^ Перейти обратно: а б «Анализ крови на эстрадиол: Медицинская энциклопедия MedlinePlus» . medlineplus.gov . Архивировано из оригинала 18 марта 2021 года . Проверено 6 мая 2019 г.
- ^ Перейти обратно: а б с д и ж г час я дж GPNotebook — референтный диапазон (эстрадиол). Архивировано 9 июня 2012 г. на Wayback Machine. Проверено 27 сентября 2009 г.
- ^ Перейти обратно: а б Значения, полученные с 1-го дня после резкого повышения ЛГ: Стрикер Р., Эберхарт Р., Шевайеллер М.К., Куинн Ф.А., Бишоф П., Стрикер Р. (2006). «Установление подробных эталонных значений лютеинизирующего гормона, фолликулостимулирующего гормона, эстрадиола и прогестерона в разные фазы менструального цикла на анализаторе Abbott ARCHITECT». Клиническая химия и лабораторная медицина . 44 (7): 883–7. дои : 10.1515/CCLM.2006.160 . ПМИД 16776638 . S2CID 524952 . как PDF
- ^ Перейти обратно: а б с д Общая сумма, умноженная на 0,022 согласно 2,2%, представлена в: Ву Ч., Мотохаши Т., Абдель-Рахман Х.А., Фликингер Г.Л., Михаил Г. (август 1976 г.). «Свободный и связанный с белками эстрадиол-17 бета в плазме во время менструального цикла». Журнал клинической эндокринологии и метаболизма . 43 (2): 436–45. doi : 10.1210/jcem-43-2-436 . ПМИД 950372 . [ оригинальное исследование? ]
- ^ Хэггстрем М (2014). «Референтные диапазоны эстрадиола, прогестерона, лютеинизирующего гормона и фолликулостимулирующего гормона во время менструального цикла» . Викижурнал медицины . 1 (1). дои : 10.15347/wjm/2014.001 . ISSN 2002-4436 .
- ^ Перейти обратно: а б Куль Х. (август 2005 г.). «Фармакология эстрогенов и прогестагенов: влияние различных путей введения». Климактерический . 8 (1 Приложение 1): 3–63. дои : 10.1080/13697130500148875 . ПМИД 16112947 . S2CID 24616324 .
- ^ Коэньертс М., Папе Ф., Сантосо В., Грау Ф., Стоффель-Вагнер Б., Филипсен А., Шульц Дж., Хёрлеманн Р., Шееле Д. (сентябрь 2021 г.). «Половые различия в принятии экономических решений: экзогенный эстрадиол оказывает противоположное влияние на формирование справедливости у женщин и мужчин». Евро. Нейропсихофармакол . 50 (2): 46–54. doi : 10.1016/j.euroneuro.2021.04.006 . hdl : 20.500.11811/11066 . ISSN 0924-977X . ПМИД 33957337 . S2CID 233982738 .
- ^ Перейти обратно: а б с Лорио ДЛ, Лорио Л (14 марта 2016 г.). Биографическая история эндокринологии . Джон Уайли и сыновья. стр. 345–. ISBN 978-1-119-20246-2 .
- ^ Перейти обратно: а б с д и ж г час я Лауритцен С., Стадд Дж.В. (22 июня 2005 г.). Текущее управление менопаузой . ЦРК Пресс. стр. 44–. ISBN 978-0-203-48612-2 .
- ^ Перейти обратно: а б Аллен Э., Дойзи Э.А. (1923). «Гормон яичников». Журнал Американской медицинской ассоциации . 81 (10): 819. дои : 10.1001/jama.1923.02650100027012 . ISSN 0002-9955 .
- ^ Перейти обратно: а б Грюн Дж.Г., Казер Р.Р. (11 ноября 2013 г.). Гормональная регуляция менструального цикла: эволюция представлений . Springer Science & Business Media. стр. 69–73. ISBN 978-1-4899-3496-3 .
- ^ Неверла Г.Дж. (1944). «История открытия и выделения женских половых гормонов». Медицинский журнал Новой Англии . 230 (20): 595–604. дои : 10.1056/NEJM194405182302001 . ISSN 0028-4793 .
- ^ Перейти обратно: а б с Фриц М.А., Сперофф Л. (28 марта 2012 г.). Клиническая гинекологическая эндокринология и бесплодие . Липпинкотт Уильямс и Уилкинс. стр. 750–. ISBN 978-1-4511-4847-3 .
- ^ Парл ФФ (2000). Эстрогены, рецепторы эстрогена и рак молочной железы . ИОС Пресс. стр. 4–. ISBN 978-0-9673355-4-4 . Архивировано из оригинала 10 января 2023 года . Проверено 27 ноября 2016 г.
- ^ Сарторелли AC, Johns DG (27 ноября 2013 г.). Противоопухолевые и иммунодепрессивные средства . Springer Science & Business Media. стр. 104–. ISBN 978-3-642-65806-8 .
- ^ Шупе Д., Хазелтин Ф.П. (6 декабря 2012 г.). Контрацепция . Springer Science & Business Media. стр. 2–. ISBN 978-1-4612-2730-4 .
- ^ МакКоркодейл Д.В., Тайер С.А., Дойзи Э.А. (1935). «Кристаллический фолликулярный гормон яичников». Экспериментальная биология и медицина . 32 (7): 1182. дои : 10.3181/00379727-32-8020P . ISSN 1535-3702 . S2CID 83557813 .
- ^ Химические вещества, обнаруженные в биологических средах человека: база данных . Отдел проектирования и разработок, Отдел исследований и анализа, Управление программной интеграции и информации, Управление пестицидов и токсичных веществ, Агентство по охране окружающей среды. 1981. С. 114–.
- ^ Фаусто-Стерлинг А (2000). Определение пола тела: гендерная политика и конструирование сексуальности . Основные книги. стр. 189 –. ISBN 978-0-465-07714-4 .
- ^ «Инструмент для изучения греческого слова: oistros» . Цифровая библиотека Персея . Архивировано из оригинала 17 марта 2012 года . Проверено 28 декабря 2011 г.
- Эстрадиол
- Вторичные спирты
- Репродуктивная система животных
- Антигонадотропины
- Антиоксиданты
- Стране
- Эстрогены
- агонисты ГПЕР
- Гепатотоксины
- Гормоны оси гипоталамус-гипофиз-гонады
- Гормоны гипоталамо-гипофизарно-пролактиновой оси
- Гормоны беременной женщины
- Женская эндокринная система человека
- Фенолы
- Релизеры пролактина
- Половые гормоны