Транскрипционный фактор AP-1
| Белки AP-1 (Fos, ATF, JDP) | |
|---|---|
| Идентификаторы | |
| Символ | АП-1 |
| ИнтерПро | ИПР000837 |
| Транскрипционный фактор Jun | |
|---|---|
| Идентификаторы | |
| Символ | Леузип_июнь |
| ИнтерПро | ИПР002112 |
Белок-активатор 1 ( AP-1 ) представляет собой фактор транскрипции , который регулирует экспрессию генов в ответ на различные стимулы, включая цитокины , факторы роста , стресс, а также бактериальные и вирусные инфекции. [ 1 ] AP-1 контролирует ряд клеточных процессов, включая дифференцировку , пролиферацию и апоптоз . [ 2 ] Структура AP-1 представляет собой гетеродимер, состоящий из белков, принадлежащих к семействам c-Fos , c-Jun , ATF и JDP .
История
[ редактировать ]AP-1 был впервые обнаружен как TPA-активируемый транскрипционный фактор, который связывался с цис-регуляторным элементом человека металлотионеина IIa ( hMTIIa ) промотора и SV40 . [ 3 ] AP-1 Сайт связывания был идентифицирован как ответный элемент 12-O-тетрадеканоилфорбол-13-ацетат ( TPA ) (TRE) с консенсусной последовательностью 5'-TGA G/C TCA-3'. [ 4 ] AP-1 Субъединица Jun была идентифицирована как новый онкопротеин вируса саркомы птиц , а Fos-ассоциированный белок p39 был идентифицирован как транскрипт клеточного гена Jun. Fos был впервые выделен как клеточный гомолог двух вирусных онкогенов v-fos, оба из которых вызывают остеосаркому у мышей и крыс. [ 5 ] С момента своего открытия было обнаружено, что AP-1 связан с многочисленными регуляторными и физиологическими процессами, и новые взаимосвязи все еще исследуются.
Структура
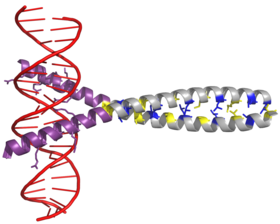
[ редактировать ]Фактор транскрипции AP-1 собирается посредством димеризации характерного домена bZIP ( лейциновая застежка-молния основной области ) в субъединицах Fos и Jun . Типичный домен bZIP состоит из области « лейциновой молнии » и «базовой области». Лейциновая молния отвечает за димеризацию белковых субъединиц Jun и Fos . Этот структурный мотив скручивает два альфа-спиральных белковых домена в « скрученную спираль », характеризующуюся периодичностью 3,5 остатков на оборот и повторяющимися лейцинами, появляющимися в каждом седьмом положении полипептидной цепи . Благодаря аминокислотной последовательности и периодичности спиралей боковые цепи лейцина располагаются вдоль одной стороны α-спирали и образуют гидрофобную поверхность, которая модулирует димеризацию. [ 6 ] Гидрофобные остатки, дополнительные к лейцину, также образуют характерные 3-4 повтора α-спиралей, участвующих во взаимодействиях «спираль-спираль», и способствуют гидрофобной упаковке, которая приводит к димеризации. Вместе эта гидрофобная поверхность удерживает две субъединицы вместе. [ 7 ] [ 8 ]
Основная область домена bZIP находится непосредственно перед лейциновой застежкой и содержит положительно заряженные остатки. Эта область взаимодействует с сайтами-мишенями ДНК . [ 9 ] Помимо «лейциновой молнии» и «основного участка», которые важны для димеризации и связывания ДНК, белок c-jun содержит три коротких участка, состоящих из кластеров отрицательно заряженных аминокислот в его N-концевой половине, которые важен для активации транскрипции in vivo. [ 10 ]
Димеризация происходит между продуктами протоонкогенов c-jun и c-fos и необходима для связывания ДНК. Белки Jun могут образовывать как гомо-, так и гетеродимеры и, следовательно, способны сами связываться с ДНК. Однако белки Fos не димеризуются друг с другом и поэтому могут связываться с ДНК только при связывании с Jun. [ 11 ] [ 12 ] Гетеродимер Jun-Fos более стабилен и обладает более высокой ДНК-связывающей активностью, чем гомодимеры Jun.
Функция
[ редактировать ]Было показано, что фактор транскрипции AP-1 участвует в широком спектре клеточных процессов, включая рост клеток , дифференцировку и апоптоз . Активность AP-1 часто регулируется посредством посттрансляционных модификаций , состава ДНК-связывающих димеров и взаимодействия с различными партнерами по связыванию. организмов Факторы транскрипции AP-1 также связаны с многочисленными физиологическими функциями, особенно с определением продолжительности жизни и регенерацией тканей . Ниже приведены некоторые другие важные функции и биологические роли, в которых, как было показано, участвуют факторы транскрипции AP-1.
Рост клеток, пролиферация и старение
[ редактировать ]Было показано, что фактор транскрипции AP-1 играет многочисленные роли в росте и пролиферации клеток. В частности, c-Fos и c-Jun, похоже, являются основными игроками в этих процессах. Было показано, что C-jun необходим для фибробластов . пролиферации [ 13 ] и было показано, что уровни обеих субъединиц AP-1 экспрессируются выше базальных уровней во время клеточного деления . [ 14 ] Также было показано, что C-fos увеличивает экспрессию в ответ на введение факторов роста в клетку, что дополнительно подтверждает его предполагаемое участие в клеточном цикле. факторы роста TGF-альфа , TGF-бета и IL2 стимулируют c-Fos и тем самым стимулируют клеточную пролиферацию посредством активации AP-1. Было показано, что [ 10 ]
Клеточное старение было идентифицировано как «динамический и обратимый процесс, регулируемый (ин)активацией заранее определенного ландшафта энхансеров , контролируемого пионером транскрипционного фактора AP-1», который «определяет организационные принципы сети транскрипционных факторов , которые управляют транскрипционной программой». стареющих клеток». [ 15 ] [ 16 ]
Клеточная дифференциация
[ редактировать ]Транскрипция AP-1 глубоко вовлечена в модуляцию экспрессии генов . Изменения в экспрессии клеточных генов при инициации синтеза ДНК и образовании дифференцированных производных могут привести к клеточной дифференцировке . [ 10 ] Было показано, что AP-1 участвует в дифференцировке клеток в нескольких системах. Например, образуя стабильные гетеродимеры с c-Jun, область bZIP c-Fos увеличивает связывание c-Jun с генами-мишенями, активация которых участвует в дифференцировке фибробластов куриных эмбрионов (CEF). [ 17 ] Также было показано, что он участвует в спецификации эндодермы . [ 18 ]
Апоптоз
[ редактировать ]Транскрипционный фактор AP-1 связан с широким спектром взаимодействий, связанных с апоптозом . Активность AP-1 индуцируется многочисленными внеклеточными матриксами и генотоксичными агентами , что позволяет предположить участие в запрограммированной гибели клеток . [ 2 ] Многие из этих стимулов активируют N-концевые киназы c-Jun (JNK), что приводит к фосфорилированию белков Jun и усилению транскрипционной активности AP-1-зависимых генов. [ 2 ] Сообщалось о повышении уровней белков Jun и Fos и активности JNK в сценариях, в которых клетки подвергаются апоптозу. Например, инактивированные клетки c-Jun-ER демонстрируют нормальную морфологию, тогда как активированные клетки c-Jun-ER являются апоптозными. [ 19 ]
Регламент АП-1
[ редактировать ]Повышенные уровни AP-1 приводят к усилению трансактивации экспрессии целевого гена. Таким образом, регуляция активности AP-1 имеет решающее значение для функции клеток и происходит посредством специфических взаимодействий, контролируемых составом димеров, транскрипционными и посттрансляционными событиями, а также взаимодействием с вспомогательными белками. [ 20 ]
Функции AP-1 во многом зависят от конкретных субъединиц Fos и Jun, вносящих вклад в димеры AP-1. [ 10 ] Результат активации AP-1 зависит от сложных комбинаторных паттернов димеров компонентов AP-1. [ 2 ] Комплекс AP-1 связывается с палиндромным мотивом ДНК (5'-TGA G/C TCA-3') для регулирования экспрессии генов, но специфичность зависит от димерного состава субъединицы bZIP. [ 2 ]
Физиологическая значимость
[ редактировать ]Было показано, что транскрипционный фактор AP-1 участвует в физиологии кожи, особенно в регенерации тканей . Процесс метаболизма кожи инициируется сигналами, которые заставляют недифференцированные пролиферативные клетки подвергаться клеточной дифференцировке. Следовательно, активность субъединиц AP-1 в ответ на внеклеточные сигналы может быть изменена в условиях, когда баланс пролиферации и дифференцировки кератиноцитов должен быть быстро и во времени изменен. [ 21 ] Также было показано, что фактор транскрипции AP-1 участвует в росте клеток рака молочной железы посредством множества механизмов, включая регуляцию циклина D1 , факторов E2F и их генов-мишеней. c-Jun, одна из субъединиц AP-1, регулирует рост клеток рака молочной железы. Активированный c-Jun преимущественно экспрессируется на инвазивном фронте рака молочной железы и связан с пролиферацией клеток молочной железы. [ 22 ] Благодаря регуляторным функциям AP-1 в раковых клетках модуляция AP-1 изучается как потенциальная стратегия профилактики и терапии рака. [ 23 ] [ 24 ] [ 25 ]
регулярно
[ редактировать ]См. также
[ редактировать ]- Белок-активатор
- Непосредственные ранние гены - гены, которые быстро экспрессируются в ответ на различные стимулы без необходимости синтеза новых белков, включая c-fos и c-jun. [ 76 ]
- Транскрипционный фактор
Ссылки
[ редактировать ]- ^ Хесс Дж., Анхель П., Шорпп-Кистнер М. (декабрь 2004 г.). «Подразделения AP-1: ссора и согласие между братьями и сестрами» . Журнал клеточной науки . 117 (Часть 25): 5965–73. дои : 10.1242/jcs.01589 . ПМИД 15564374 .
- ^ Jump up to: а б с д и Амейар М., Вишневска М., Вайцман Дж.Б. (август 2003 г.). «Роль AP-1 в апоптозе: доводы за и против». Биохимия . 85 (8): 747–52. дои : 10.1016/j.biochi.2003.09.006 . ПМИД 14585541 .
- ^ Ли В., Хаслингер А., Карин М., Цзян Р. (январь 1987 г.). «Активация транскрипции двумя факторами, которые связывают промоторные и энхансерные последовательности гена металлотионеина человека и SV40». Природа . 325 (6102): 368–72. Бибкод : 1987Natur.325..368L . дои : 10.1038/325368a0 . ПМИД 3027570 . S2CID 4314423 .
- ^ Анхель П., Имагава М., Чиу Р., Штейн Б., Имбра Р.Дж., Рамсдорф Х.Дж., Йонат С., Херрлих П., Карин М. (июнь 1987 г.). «Гены, индуцируемые эфиром форбола, содержат общий цис-элемент, распознаваемый транс-действующим фактором, модулированным ТРА». Клетка . 49 (6): 729–39. дои : 10.1016/0092-8674(87)90611-8 . ПМИД 3034432 . S2CID 23154076 .
- ^ Вагнер Э.Ф. (апрель 2001 г.). «АП-1 -- Вступительное слово» . Онкоген . 20 (19): 2334–5. дои : 10.1038/sj.onc.1204416 . ПМИД 11402330 .
- ^ Ландшульц В.Х., Джонсон П.Ф., Макнайт С.Л. (июнь 1988 г.). «Лейциновая молния: гипотетическая структура, общая для нового класса ДНК-связывающих белков». Наука . 240 (4860): 1759–64. Бибкод : 1988Sci...240.1759L . дои : 10.1126/science.3289117 . ПМИД 3289117 .
- ^ О'Ши Э.К., Рутковски Р., Ким П.С. (январь 1989 г.). «Доказательства того, что лейциновая молния представляет собой скрученную спираль». Наука . 243 (4890): 538–42. Бибкод : 1989Sci...243..538O . дои : 10.1126/science.2911757 . ПМИД 2911757 .
- ^ О'Ши Э.К., Рутковски Р., Стаффорд В.Ф., Ким П.С. (август 1989 г.). «Преимущественное образование гетеродимеров изолированными лейциновыми молниями из fos и jun». Наука . 245 (4918): 646–8. Бибкод : 1989Sci...245..646O . дои : 10.1126/science.2503872 . ПМИД 2503872 .
- ^ Фогт П.К., Бос Т.Дж. (1990). «jun: онкоген и фактор транскрипции». Достижения в области исследований рака . 55 : 1–35. дои : 10.1016/s0065-230x(08)60466-2 . ISBN 9780120066551 . ПМИД 2166997 .
- ^ Jump up to: а б с д Анхель П., Карин М. (декабрь 1991 г.). «Роль Jun, Fos и комплекса AP-1 в пролиферации и трансформации клеток». Biochimica et Biophysical Acta (BBA) - Обзоры о раке . 1072 (2–3): 129–57. дои : 10.1016/0304-419X(91)90011-9 . ПМИД 1751545 .
- ^ Кузаридес Т., Зифф Э. (декабрь 1988 г.). «Роль лейциновой молнии во взаимодействии фос-джун». Природа . 336 (6200): 646–51. Бибкод : 1988Natur.336..646K . дои : 10.1038/336646a0 . ПМИД 2974122 . S2CID 4355663 .
- ^ Накабеппу Ю., Райдер К., Натанс Д. (декабрь 1988 г.). «ДНК-связывающая активность трех мышиных белков Jun: стимуляция Fos». Клетка . 55 (5): 907–15. дои : 10.1016/0092-8674(88)90146-8 . ПМИД 3142691 . S2CID 11057487 .
- ^ Карин М., Лю З., Занди Э. (апрель 1997 г.). «Функция и регулирование АП-1». Современное мнение в области клеточной биологии . 9 (2): 240–6. дои : 10.1016/S0955-0674(97)80068-3 . ПМИД 9069263 .
- ^ Ямасита Дж., МакКоли Л.К. (2006). «Транскрипционный комплекс активирующего белка-1: важные и многогранные роли в костях». Клинические обзоры костного и минерального метаболизма . 4 (2): 107–122. дои : 10.1385/БММ:4:2:107 . S2CID 90318354 .
- ^ Зумерле С., Алимонти А. (2020). «Вход и выход из старения» . Nat Cell Biol . 22 (7): 753–754. дои : 10.1038/s41556-020-0540-x . ПМИД 32591745 . S2CID 220071911 .
- ^ Мартинес-Самудио Р., Ру П., де Фрейтас Дж. и др. (2020). «AP-1 импринтирует обратимую транскрипционную программу стареющих клеток» . Nat Cell Biol . 22 (7): 842–855. дои : 10.1038/s41556-020-0529-5 . ПМЦ 7899185 . ПМИД 32514071 . S2CID 219543898 .
- ^ Шаулян Э., Карин М. (май 2002 г.). «AP-1 как регулятор жизни и смерти клеток». Природная клеточная биология . 4 (5): Е131–6. дои : 10.1038/ncb0502-e131 . ПМИД 11988758 . S2CID 34337538 .
- ^ Мадригал П., Денг С., Фэн Ю., Милити С., Го К.Дж., Нибхани Р., Гранди Р., Оснато А., Ортманн Д., Браун С., Пауклин С. (25 января 2023 г.). «Эпигенетические и транскрипционные регуляции определяют судьбу клеток перед делением во время дифференцировки плюрипотентных стволовых клеток человека» (PDF) . Природные коммуникации . 14 (405): 405. Бибкод : 2023NatCo..14..405M . дои : 10.1038/s41467-023-36116-9 . ПМЦ 9876972 . ПМИД 36697417 .
- ^ Босси-Ветцель Э., Бакири Л., Янив М. (апрель 1997 г.). «Индукция апоптоза транскрипционным фактором c-Jun» . Журнал ЭМБО . 16 (7): 1695–709. дои : 10.1093/emboj/16.7.1695 . ПМК 1169773 . ПМИД 9130714 .
- ^ Веселый П.В., Стабер П.Б., Хефлер Г., Кеннер Л. (июль 2009 г.). «Механизмы трансляционной регуляции белков AP-1». Мутационные исследования . 682 (1): 7–12. Бибкод : 2009MRRMR.682....7В . дои : 10.1016/j.mrrev.2009.01.001 . ПМИД 19167516 .
- ^ Анхель П., Шабовский А., Шорпп-Кистнер М. (апрель 2001 г.). «Функция и регуляция субъединиц AP-1 в физиологии и патологии кожи» . Онкоген . 20 (19): 2413–23. дои : 10.1038/sj.onc.1204380 . ПМИД 11402337 .
- ^ Шен К., Урай И.П., Ли Ю, Криско Т.И., Стрекер Т.Е., Ким Х.Т., Браун П.Х. (январь 2008 г.). «Фактор транскрипции AP-1 регулирует рост клеток рака молочной железы посредством циклинов и факторов E2F» . Онкоген . 27 (3): 366–77. дои : 10.1038/sj.onc.1210643 . ПМИД 17637753 .
- ^ Эферл Р., Вагнер Э.Ф. (ноябрь 2003 г.). «AP-1: палка о двух концах в онкогенезе». Обзоры природы. Рак . 3 (11): 859–68. дои : 10.1038/nrc1209 . PMID 14668816 . S2CID 35328722 .
- ^ Тевари Д., Набави С.Ф., Набави С.М., Суреда А., Фаруки А.А., Атанасов А.Г., Вакка Р.А., Сетхи Г., Бишайи А. (февраль 2018 г.). «Нацеливание на сигнальный путь активатора белка 1 с помощью биоактивных природных агентов: возможная терапевтическая стратегия профилактики и лечения рака». Фармакологические исследования . 128 : 366–375. дои : 10.1016/j.phrs.2017.09.014 . ПМИД 28951297 . S2CID 20160666 .
- ^ Камид Д., Ямасита Т., Араки К., Томифудзи М., Танака Ю., Танака С., Сиодзава С., Сиотани А. (май 2016 г.). «Селективный ингибитор белка-активатора-1 Т-5224 предотвращает метастазирование в лимфатические узлы на модели рака полости рта» . Раковая наука . 107 (5): 666–73. дои : 10.1111/cas.12914 . ПМЦ 4970834 . ПМИД 26918517 .
- ^ Проффитт Дж., Крэбтри Дж., Гроув М., Доберси П., Байёль Б., Райт Э., Пламб М. (январь 1995 г.). «Сайт связывания ATF/CREB необходим для клеточно-специфической и индуцируемой транскрипции мышиного гена бета-цитокина MIP-1». Джин . 152 (2): 173–9. дои : 10.1016/0378-1119(94)00701-С . ПМИД 7835696 .
- ^ Райнио Э.М., Сандхольм Дж., Коскинен П.Дж. (февраль 2002 г.). «Авангард: транскрипционная активность NFATc1 усиливается киназой Pim-1» . Журнал иммунологии . 168 (4): 1524–7. дои : 10.4049/jimmunol.168.4.1524 . ПМИД 11823475 .
- ^ Саньял С., Сандстром Д.Д., Хёффер К.А., Рамасвами М. (апрель 2002 г.). «AP-1 действует выше CREB, контролируя синаптическую пластичность у дрозофилы». Природа . 416 (6883): 870–4. Бибкод : 2002Natur.416..870S . дои : 10.1038/416870a . ПМИД 11976688 . S2CID 4329320 .
- ^ Хираяма Дж., Кардоне Л., Дой М., Сассоне-Корси П. (июль 2005 г.). «Общие пути циркадных и клеточных циклов: светозависимая активация Fos/AP-1 у рыбок данио контролирует CRY-1a и WEE-1» . Труды Национальной академии наук Соединенных Штатов Америки . 102 (29): 10194–9. Бибкод : 2005PNAS..10210194H . дои : 10.1073/pnas.0502610102 . ПМЦ 1177375 . ПМИД 16000406 .
- ^ Вай ПЯ, Ми З, Гао С, Го Х, Маррокин С, Куо ПК (июль 2006 г.). «Ets-1 и runx2 регулируют транскрипцию метастатического гена остеопонтина в клетках колоректального рака мышей» . Журнал биологической химии . 281 (28): 18973–82. дои : 10.1074/jbc.M511962200 . ПМИД 16670084 .
- ^ Коллинз-Хикок Дж., Лин Л., Спиро С., Лейборн П.Дж., Чумпер Р., Рапач Б., МакМюррей К.Т. (май 1994 г.). «Индукция гена продинорфина крысы через Gs-связанные рецепторы может включать зависимую от фосфорилирования дерепрессию и активацию» . Молекулярная и клеточная биология . 14 (5): 2837–48. дои : 10.1128/MCB.14.5.2837 . ПМК 358652 . ПМИД 8164647 .
- ^ Jump up to: а б Берен А., Саймон С., Шваб Р.М., Лётч Э., Бродбек С., Хубер Э., Штубенраух Ф., Ценнер Х.П., Ифтнер Т. (декабрь 2005 г.). «Белок E2 папилломавируса индуцирует экспрессию матриксной металлопротеиназы-9 через регулируемый внеклеточный сигнал сигнальный путь киназа/активаторный белок-1» . Исследования рака . 65 (24): 11613–21. дои : 10.1158/0008-5472.CAN-05-2672 . ПМИД 16357172 .
- ^ Хенниган Р.Ф., Стэмбрук П.Дж. (август 2001 г.). «Доминантно-негативный c-jun ингибирует активацию киназных комплексов циклин D1 и циклин E» . Молекулярная биология клетки . 12 (8): 2352–63. дои : 10.1091/mbc.12.8.2352 . ПМК 58599 . ПМИД 11514621 .
- ^ Кнехель С., Шулер-Мец А., Кнехель В. (ноябрь 2000 г.). «c-Jun (AP-1) активирует транскрипцию BMP-4 у эмбрионов Xenopus» . Механизмы развития . 98 (1–2): 29–36. дои : 10.1016/S0925-4773(00)00448-2 . ПМИД 11044605 . S2CID 18150052 .
- ^ Jump up to: а б Кидд М., Хиноуэ Т., Эйк Г., Лай К.Д., Мане С.М., Вэнь Ю., Модлин И.М. (декабрь 2004 г.). «Анализ глобальной экспрессии клеток ECL в слизистой оболочке желудка Mastomys natalensis выявляет изменения в пути AP-1, индуцированные гастрин-опосредованной трансформацией». Физиологическая геномика . 20 (1): 131–42. doi : 10.1152/физиологгеномика.00216.2003 . ПМИД 15602048 .
- ^ Хайм Дж.М., Сингх С., Фюлле Х.Дж., Герцер Р. (январь 1992 г.). «Сравнение клонированной ANF-чувствительной гуанилатциклазы (GC-A) с гуанилатциклазой в виде частиц из коры надпочечников». Архив фармакологии Наунина-Шмидеберга . 345 (1): 64–70. дои : 10.1007/BF00175471 . ПМИД 1347156 . S2CID 22605840 .
- ^ Куо Ю.Р., Ву В.С., Ван Ф.С. (апрель 2007 г.). «Импульсный лазер на красителе с лампой-вспышкой подавляет экспрессию и пролиферацию TGF-бета1 в культивируемых келоидных фибробластах, опосредованную путем MAPK». Лазеры в хирургии и медицине . 39 (4): 358–64. дои : 10.1002/lsm.20489 . ПМИД 17457842 . S2CID 25556684 .
- ^ Ву Дж, Бресник Э.Х. (март 2007 г.). «Требования к синергизму глюкокортикоидов и факторов роста для активации домена хроматина Notch4» . Молекулярная и клеточная биология . 27 (6): 2411–22. дои : 10.1128/MCB.02152-06 . ПМК 1820485 . ПМИД 17220278 .
- ^ Мартинс Г., Каламе К. (2008). «Регуляция и функции Blimp-1 в Т- и В-лимфоцитах». Ежегодный обзор иммунологии . 26 : 133–69. doi : 10.1146/annurev.immunol.26.021607.090241 . ПМИД 18370921 .
- ^ Лунек Дж., Холлоуэй К., Кук М., Эванс М. (2003). «Окислительно-восстановительная регуляция репарации ДНК». Биофакторы . 17 (1–4): 315–24. дои : 10.1002/biof.5520170131 . ПМИД 12897453 . S2CID 30654477 .
- ^ Маникассами С., Гупта С., Хуан З., Сунь З. (июнь 2006 г.). «Сигналы, опосредованные протеинкиназой C-тета, повышают выживаемость CD4+ Т-клеток за счет повышения регуляции Bcl-xL» . Журнал иммунологии . 176 (11): 6709–16. дои : 10.4049/jimmunol.176.11.6709 . ПМИД 16709830 .
- ^ Ван Н., Верна Л., Харди С., Форсайет Дж., Чжу Ю., Стемерман М.Б. (сентябрь 1999 г.). «Опосредованная аденовирусом сверхэкспрессия c-Jun и c-Fos индуцирует молекулу межклеточной адгезии-1 и моноцитарный хемоаттрактантный белок-1 в эндотелиальных клетках человека» . Атеросклероз, тромбоз и сосудистая биология . 19 (9): 2078–84. дои : 10.1161/01.ATV.19.9.2078 . ПМИД 10479648 .
- ^ Фудзита С., Ито Т., Мизутани Т., Миногучи С., Ямамичи Н., Сакураи К., Иба Х. (май 2008 г.). «Экспрессия гена миР-21, запускаемая AP-1, поддерживается посредством механизма двойной отрицательной обратной связи». Журнал молекулярной биологии . 378 (3): 492–504. дои : 10.1016/j.jmb.2008.03.015 . ПМИД 18384814 .
- ^ фон Кнетен А., Кальсен Д., Брюне Б. (февраль 1999 г.). «Активация NF-kappaB и AP-1 оксидом азота ослабляет апоптотическую гибель клеток в макрофагах RAW 264.7» . Молекулярная биология клетки . 10 (2): 361–72. дои : 10.1091/mbc.10.2.361 . ПМК 25174 . ПМИД 9950682 .
- ^ Фелан Дж.П., Миллсон С.Х., Паркер П.Дж., Пайпер П.В., Кук Ф.Т. (октябрь 2006 г.). «Fab1p и AP-1 необходимы для доставки эндогенно убиквитилированных грузов в просвет вакуоли S. cerevisiae» . Журнал клеточной науки . 119 (Часть 20): 4225–34. дои : 10.1242/jcs.03188 . ПМИД 17003107 .
- ^ Ноласко Л.Х., Тернер Н.А., Бернардо А., Тао З., Клири Т.Г., Донг Дж.Ф., Моак Дж.Л. (декабрь 2005 г.). «Связанные с гемолитико-уремическим синдромом шига-токсины способствуют секреции эндотелиальных клеток и ухудшают расщепление ADAMTS13 необычно крупных мультимеров фактора фон Виллебранда» . Кровь . 106 (13): 4199–209. дои : 10.1182/кровь-2005-05-2111 . ПМЦ 1895236 . ПМИД 16131569 .
- ^ Хоммура Ф., Катабами М., Линер В.Д., Доннингер Х., Самтер Т.Ф., Ресар Л.М., Биррер М.Дж. (май 2004 г.). «HMG-I/Y представляет собой целевой ген c-Jun/белка-активатора-1 и необходим для индуцированного c-Jun независимого от закрепления роста в клетках Rat1a» . Молекулярные исследования рака . 2 (5): 305–14. дои : 10.1158/1541-7786.305.2.5 . ПМИД 15192124 . S2CID 25127065 .
- ^ Чанг CJ, Чао JC (апрель 2002 г.). «Влияние женского молока и эпидермального фактора роста на рост клеток Caco-2 кишечника человека» . Журнал детской гастроэнтерологии и питания . 34 (4): 394–401. дои : 10.1097/00005176-200204000-00015 . ПМИД 11930096 . S2CID 25446228 .
- ^ Вебер-младший, Скин Дж.Х. (июль 1998 г.). «Активность весьма беспорядочного элемента AP-1 может быть ограничена нейронами с помощью тканеселективного репрессивного элемента» . Журнал неврологии . 18 (14): 5264–74. doi : 10.1523/jneurosci.18-14-05264.1998 . ПМК 6793474 . ПМИД 9651209 .
- ^ Ли В., Митчелл П., Цзян Р. (июнь 1987 г.). «Очищенный фактор транскрипции AP-1 взаимодействует с ТРА-индуцируемыми энхансерными элементами». Клетка . 49 (6): 741–52. дои : 10.1016/0092-8674(87)90612-X . ПМИД 3034433 . S2CID 37036603 .
- ^ Коэн, член парламента, Зияде Ф.Н., Лаутенслагер Г.Т., Коэн Дж.А., Ширман К.В. (май 1999 г.). «Стимуляция активности PKC-бета гликированным альбумином связана с увеличением коллагена IV в мезангиальных клетках» . Американский журнал физиологии . 276 (5, часть 2): F684–90. дои : 10.1152/ajprenal.1999.276.5.F684 . ПМИД 10330050 .
- ^ Старк CJ, компакт-диск Atreya (апрель 2005 г.). «Молекулярные достижения в клеточной биологии SARS-CoV и современные стратегии профилактики заболеваний» . Вирусологический журнал . 2:35 . дои : 10.1186/1743-422X-2-35 . ПМЦ 1087510 . ПМИД 15833113 .
- ^ Jump up to: а б с Лейн С.Дж., Адкок И.М., Ричардс Д., Гаврилович С., Барнс П.Дж., Ли Т.Х. (декабрь 1998 г.). «Кортикостероидорезистентная бронхиальная астма связана с повышенной экспрессией c-fos в моноцитах и Т-лимфоцитах» . Журнал клинических исследований . 102 (12): 2156–64. дои : 10.1172/JCI2680 . ПМК 509170 . ПМИД 9854051 .
- ^ Штайнер С., Питерс В.Х., Галлахер Э.П., Маги П., Роуленд И., Пул-Зобель Б.Л. (март 2007 г.). «Генистеин защищает эпителиальные клетки молочной железы человека от генотоксичности бензо(а)пирен-7,8-дигидродиол-9,10-эпоксида и 4-гидрокси-2-ноненаля путем модуляции системы глутатион/глутатион-S-трансферазы» . Канцерогенез . 28 (3): 738–48. дои : 10.1093/carcin/bgl180 . ПМИД 17065199 .
- ^ Ан Дж.Д., Моришита Р., Канеда Ю., Ли КУ, Пак Дж.Й., Чон Ю.Дж., Сон Х.С., Ли И.К. (июнь 2001 г.). «Фактор транскрипции-приманка для белка-активатора-1 (AP-1) ингибирует высокую экспрессию генов ингибитора активатора плазминогена 1-го типа (PAI-1), индуцированную глюкозой и ангиотензином II, в культивируемых гладкомышечных клетках сосудов человека» . Диабетология . 44 (6): 713–20. дои : 10.1007/s001250051680 . ПМИД 11440364 .
- ^ Канг С., Фишер Дж.Дж., Вурхис Дж.Дж. (ноябрь 2001 г.). «Фотостарение: патогенез, профилактика и лечение». Клиники гериатрической медицины . 17 (4): 643–59, v–vi. дои : 10.1016/S0749-0690(05)70091-4 . ПМИД 11535421 .
- ^ Наваса М., Гордон Д.А., Харихаран Н., Джамиль Х., Сигенага Дж.К., Мозер А., Фирс В., Поллок А., Грюнфельд С., Фейнгольд К.Р. (июнь 1998 г.). «Регуляция экспрессии мРНК микросомального белка-переносчика триглицеридов с помощью эндотоксина и цитокинов» . Журнал исследований липидов . 39 (6): 1220–30. дои : 10.1016/S0022-2275(20)32546-3 . ПМИД 9643353 .
- ^ Суэцугу М., Такано А., Нагай А., Такешита А., Хиросе К., Мацумото К. и др. (2007). «Ретиноевая кислота ингибирует стимулируемый сывороткой белок-активатор-1 посредством подавления экспрессии генов c-fos и c-jun во время индуцированной витамином дифференцировки клеток линии остеобластов мыши MC3T3-E1» (PDF) . Дж. Мейкай Дент. Мед . 36 (1): 42–50.
- ^ Инаги Р., Мията Т., Нангаку М., Уэяма Х., Такеяма К., Като С., Курокава К. (ноябрь 2002 г.). «Регуляция транскрипции гена с преобладанием мезангиума, мегсина» . Журнал Американского общества нефрологов . 13 (11): 2715–22. дои : 10.1097/01.ASN.0000033507.32175.FA . ПМИД 12397041 .
- ^ Ким С., Ю СС, Ли И.С., Оно С., Йим Дж., Ким С., Кан Х.С. (апрель 1999 г.). «Белок IE1 цитомегаловируса человека активирует AP-1 посредством клеточной протеинкиназы» . Журнал общей вирусологии . 80 (Часть 4) (4): 961–9. дои : 10.1099/0022-1317-80-4-961 . ПМИД 10211966 .
- ^ Масуда А., Ёшикай Ю., Куме Х., Мацугути Т. (ноябрь 2004 г.). «Взаимодействие между белками GATA и белком-активатором-1 способствует транскрипции IL-13 в тучных клетках» . Журнал иммунологии . 173 (9): 5564–73. дои : 10.4049/jimmunol.173.9.5564 . ПМИД 15494506 .
- ^ Навас Т.А., Болдуин Д.Т., Стюарт Т.А. (ноябрь 1999 г.). «RIP2 представляет собой Raf1-активируемую митоген-активируемую протеинкиназную киназу» . Журнал биологической химии . 274 (47): 33684–90. дои : 10.1074/jbc.274.47.33684 . ПМИД 10559258 .
- ^ Симантов Р. (август 1995 г.). «Нейротранспортеры: регуляция, участие в нейротоксичности и полезность антисмысловых нуклеиновых кислот». Биохимическая фармакология . 50 (4): 435–42. дои : 10.1016/0006-2952(95)00068-Б . ПМИД 7646547 .
- ^ Ян Х.С., Янсен А.П., Наир Р., Шибахара К., Верма А.К., Цмарик Дж.Л., Колберн Н.Х. (февраль 2001 г.). «Новый супрессор трансформации, Pdcd4, ингибирует трансактивацию AP-1, но не трансактивацию NF-kappaB или ODC» . Онкоген . 20 (6): 669–76. дои : 10.1038/sj.onc.1204137 . ПМИД 11314000 .
- ^ Се Дж., Пан Х., Ю С., Гао С.Дж. (декабрь 2005 г.). «Связанная с саркомой Капоши герпесвирусная индукция AP-1 и интерлейкина 6 во время первичной инфекции, опосредованная множественными митоген-активируемыми протеинкиназными путями» . Журнал вирусологии . 79 (24): 15027–37. doi : 10.1128/JVI.79.24.15027-15037.2005 . ПМК 1316010 . ПМИД 16306573 .
- ^ Хан М.А., Бузари С., Ма С., Розенбергер К.М., Бергстром К.С., Гибсон Д.Л., Штайнер Т.С., Валланс Б.А. (апрель 2008 г.). «Флагеллин-зависимые и независимые воспалительные реакции после заражения энтеропатогенными Escherichia coli и Citrobacter Rodentium» . Инфекция и иммунитет . 76 (4): 1410–22. дои : 10.1128/IAI.01141-07 . ПМК 2292885 . ПМИД 18227166 .
- ^ Кида Ю, Иноуэ Х, Симидзу Т, Кувано К (январь 2007 г.). «Серрализин Serratia marcescens индуцирует воспалительные реакции через активируемый протеазой рецептор 2» . Инфекция и иммунитет . 75 (1): 164–74. дои : 10.1128/IAI.01239-06 . ПМЦ 1828393 . ПМИД 17043106 .
- ^ Гуцман Дж. Х., Руговски Д. Е., Шредер, доктор медицинских наук, Уоттерс Дж. Дж., Шулер Л. А. (декабрь 2004 г.). «Множественные киназные каскады передают сигналы пролактина для активации белка-1 в клетках рака молочной железы» . Молекулярная эндокринология . 18 (12): 3064–75. дои : 10.1210/me.2004-0187 . ПМЦ 1634796 . ПМИД 15319452 .
- ^ Бринкманн М.М., Гленн М., Рэйнбоу Л., Кизер А., Хенке-Гендо С., Шульц Т.Ф. (сентябрь 2003 г.). «Активация митоген-активируемой протеинкиназы и путей NF-kappaB мембранным белком K15 герпесвируса, ассоциированного с саркомой Капоши» . Журнал вирусологии . 77 (17): 9346–58. doi : 10.1128/JVI.77.17.9346-9358.2003 . ЧВК 187392 . ПМИД 12915550 .
- ^ Гринштейн С., Гиас К., Кретт Н.Л., Розен С.Т. (июнь 2002 г.). «Механизмы глюкокортикоид-опосредованного апоптоза при гематологических злокачественных новообразованиях» . Клинические исследования рака . 8 (6): 1681–94. ПМИД 12060604 .
- ^ Ёко Т., Китамура М. (май 1996 г.). «Антиоксидант PDTC индуцирует экспрессию стромелизина в мезангиальных клетках через путь тирозинкиназа-AP-1». Американский журнал физиологии . 270 (5, часть 2): F806–11. дои : 10.1152/ajprenal.1996.270.5.F806 . ПМИД 8928842 .
- ^ Чанг К.Ф., Чо С., Ван Дж. (апрель 2014 г.). «(-)-Эпикатехин защищает геморрагический мозг посредством синергических путей Nrf2» . Анналы клинической и трансляционной неврологии . 1 (4): 258–271. дои : 10.1002/acn3.54 . ПМЦ 3984761 . ПМИД 24741667 .
- ^ Гиббингс DJ, Ghetu AF, Дери Р., Бефус AD (февраль 2008 г.). «Фактор, ингибирующий миграцию макрофагов, имеет мотив и функцию, подобные MHC класса I» . Скандинавский журнал иммунологии . 67 (2): 121–32. дои : 10.1111/j.1365-3083.2007.02046.x . ПМИД 18201367 .
- ^ База данных Юнипрот
- ^ Сю Ю.К., Вудхья Гоурисанкар Ю., Чен XZ, Ян Ю.К., Ян Х.Л. (февраль 2020 г.). «Антивозрастная активность эрготионеина в дермальных фибробластах человека, облученных UVA, посредством ингибирования пути AP-1 и активации Nrf2-опосредованных антиоксидантных генов» . Оксид Мед Селл Лонгев . 2020 (2576823): 1–13. дои : 10.1155/2020/2576823 . ПМК 7038158 . ПМИД 32104530 .
- ^ Бахрами С., Драблёс Ф. (2016). «Геновая регуляция в процессе немедленного и раннего ответа» . Достижения в области биологического регулирования . 62 : 37–49. дои : 10.1016/j.jbior.2016.05.001 . ПМИД 27220739 .

