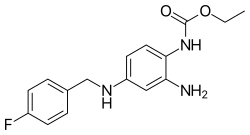
Ретигабин
 | |
| Клинические данные | |
|---|---|
| Торговые названия | Найден, Потига |
| Другие имена | D-23129, эзогабин ( США , США ) |
| AHFS / Drugs.com | Профессиональные факты о наркотиках |
| Медлайн Плюс | а612028 |
| Данные лицензии | |
| Маршруты администрация | Через рот |
| код АТС | |
| Юридический статус | |
| Юридический статус |
|
| Фармакокинетические данные | |
| Биодоступность | 60% |
| Связывание с белками | 60–80% |
| Метаболизм | печени Глюкуронидация и ацетилирование . CYP не участвует |
| Период полувыведения | 8 часов (в среднем), диапазон: 7–11 часов [ 1 ] |
| Экскреция | Почки (84%) |
| Идентификаторы | |
| Номер CAS | |
| ПабХим CID | |
| ИЮФАР/БПС | |
| Лекарственный Банк | |
| ХимическийПаук | |
| НЕКОТОРЫЙ | |
| КЕГГ | |
| ХЭМБЛ | |
| Панель управления CompTox ( EPA ) | |
| Информационная карта ECHA | 100.158.123 |
| Химические и физические данные | |
| Формула | С 16 Ч 18 Ф Н 3 О 2 |
| Молярная масса | 303.337 g·mol −1 |
| 3D model ( JSmol ) | |
Ретигабин ( МНН ) или эзогабин ( USAN ) — противосудорожное средство, используемое в качестве дополнительного лечения парциальной эпилепсии у взрослых пациентов, ранее проходивших лечение. [ 2 ] Препарат разработан компаниями Valeant Pharmaceuticals и GlaxoSmithKline . Он был одобрен Европейским агентством по лекарственным средствам под торговым названием Trobalt 28 марта 2011 г. и Управлением США по контролю за продуктами и лекарствами (FDA) под торговым названием Potiga 10 июня 2011 г. Производство было прекращено в июне 2017 г. . [ 3 ] [ 4 ]
Ретигабин действует главным образом как открыватель калиевых каналов , то есть активируя определенное семейство потенциалзависимых калиевых каналов в мозге. [ 5 ] [ 6 ] [ 7 ] Этот механизм действия уникален среди противоэпилептических препаратов и может быть перспективным для лечения других неврологических заболеваний, включая шум в ушах , мигрень и нейропатическую боль . Производитель отозвал ретигабин из клинического применения в 2017 году.
Побочные эффекты
[ редактировать ], Побочные эффекты обнаруженные в ходе исследования фазы II, в основном затрагивали центральную нервную систему и, по-видимому, были связаны с дозой. [ 8 ] Наиболее распространенными побочными эффектами были сонливость , головокружение , шум в ушах и головокружение , спутанность сознания и невнятная речь . [ 9 ] Менее распространенные побочные эффекты включали тремор , потерю памяти, нарушения походки и двоение в глазах . [ 10 ] В 2013 году FDA предупредило общественность, что Потига (эзогабин) может вызывать посинение кожи и аномалии глаз, характеризующиеся пигментными изменениями сетчатки. FDA в настоящее время не знает, обратимы ли эти изменения. FDA работает с производителем над сбором и оценкой всей доступной информации, чтобы лучше понять эти события. FDA сообщит общественности, когда появится дополнительная информация. [ 11 ] Сообщалось также о психических симптомах и затруднении мочеиспускания, причем большинство случаев возникало в первые 2 месяца лечения. [ 12 ] [ 13 ]
Взаимодействия
[ редактировать ]Ретигабин, по-видимому, не взаимодействует препаратами с наиболее часто используемыми противосудорожными . Он может усиливать метаболизм ламотриджина (ламиктала), тогда как фенитоин (дилантин) и карбамазепин (CBZ, тегретол) увеличивают клиренс ретигабина. [ 13 ] [ 14 ]
Одновременное применение ретигабина и дигоксина может повысить концентрацию последнего в сыворотке крови. Исследования in vitro показывают, что основной метаболит ретигабина действует как ингибитор P-гликопротеина и, таким образом, может увеличивать абсорбцию и снижать выведение дигоксина. [ 13 ]
Фармакология
[ редактировать ]Механизм действия
[ редактировать ]Ретигабин действует как KCNQ / Kv7 открыватель калиевых каналов в нейронах , механизм действия которого заметно отличается от механизма действия любых современных противосудорожных препаратов. [ 5 ] [ 6 ] [ 7 ] Этот механизм действия подобен механизму действия химически близкого флупиртина . [ 15 ] который используется главным образом из-за его обезболивающих свойств.
Термин «открытие канала» относится к сдвигу зависимости открытия канала от напряжения в сторону более отрицательных потенциалов. Это означает, что каналы KCNQ/Kv7 открываются при более отрицательных потенциалах в присутствии ретигабина. Недавно также было показано, что ретигабин стабилизирует открытый канал Kv7.2/7.3, замедляя дезактивацию с небольшими изменениями в зависимости от напряжения. Этот эффект ретигабина наблюдается при концентрациях ниже 10 микромолярных. [ 16 ] Аналогичный эффект наблюдается на гомомерном канале Kv7.2. [ 17 ]
Фармакокинетика
[ редактировать ]Ретигабин быстро всасывается и достигает максимальной концентрации в плазме через полчаса-два часа после однократного перорального приема. Он имеет умеренно высокую биодоступность при пероральном приеме (50–60%), высокий объем распределения (6,2 л/кг) и конечный период полувыведения от 8 до 11 часов. [ 14 ] Ретигабин требуется принимать трижды в день из-за его короткого периода полувыведения. [ 8 ] [ 9 ] [ 13 ]
Ретигабин метаболизируется в печени путем N - глюкуронирования и ацетилирования . Система цитохрома Р450 не участвует. Ретигабин и его метаболиты практически полностью (84%) выводятся почками. [ 13 ] [ 14 ]
История
[ редактировать ]Среди новых противосудорожных препаратов ретигабин был одним из наиболее широко изученных в доклинических условиях: до начала клинических испытаний на него было опубликовано более 100 исследований. В доклинических испытаниях было обнаружено, что он имеет очень широкий спектр активности и эффективен практически во всех животных моделях судорог и эпилепсии: ретигабин подавляет судороги, вызванные электрошоком, электрическим возбуждением миндалевидного тела , пентилентетразолом , каинатом , NMDA и пикротоксин . [ 18 ] Исследователи надеялись, что эта широкомасштабная деятельность приведет и к исследованиям на людях. [ 8 ]
Клинические испытания
[ редактировать ]В двойном слепом рандомизированном плацебо-контролируемом клиническом исследовании фазы II ретигабин был добавлен к схеме лечения 399 участников с парциальными припадками, резистентными к терапии другими противоэпилептическими препаратами. Частота возникновения припадков была значительно снижена (на 23–35%) у участников, получавших ретигабин, и примерно у одной четверти–одной трети участников частота припадков снизилась более чем на 50%. Более высокие дозы были связаны с лучшим ответом на лечение. [ 8 ] [ 10 ] [ 9 ]
Исследование фазы II , предназначенное для оценки безопасности и эффективности ретигабина при лечении постгерпетической невралгии , было завершено в 2009 году, но не достигло основной конечной точки . Предварительные результаты были названы Valeant «неубедительными». [ 19 ]
Нормативное одобрение
[ редактировать ]Valeant Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США приняло новую заявку на ретигабин 30 декабря 2009 года. [ 20 ] Консультативный комитет FDA по препаратам для лечения периферической и центральной нервной системы собрался 11 августа 2010 г., чтобы обсудить процесс, и единогласно рекомендовал одобрить Потигу по предполагаемому показанию (дополнительное лечение парциальных судорог у взрослых). [ 21 ] [ 22 ] Однако возможность задержки мочи как побочного эффекта была сочтена серьезной проблемой, и члены группы рекомендовали использовать какую-то стратегию мониторинга для выявления пациентов с риском дисфункции мочевого пузыря. [ 21 ] Потига был одобрен FDA 10 июня 2010 года, но не стал доступен на рынке США до тех пор, пока его не запланировало Управление по борьбе с наркотиками . [ 12 ]
США В декабре 2011 года Управление по борьбе с наркотиками (DEA) поместило это вещество в Список V Закона о контролируемых веществах (CSA), категорию веществ со сравнительно низким потенциалом злоупотребления. Это вступило в силу 15 декабря 2011 года. [ 23 ]
Имя
[ редактировать ]Международное непатентованное название «ретигабин» первоначально было опубликовано как находящееся на рассмотрении ВОЗ в 1996 году. [ 24 ] Позже оно было принято в качестве рекомендуемого международного непатентованного названия (rINN) для препарата, а в 2005 или 2006 году Совет USAN — программа, спонсируемая Американской медицинской ассоциацией, Фармакопейной конвенцией США и Американской ассоциацией фармацевтов, которая выбирает непатентованные названия лекарств, продаваемых в США, — принято то же название. [ 25 ] Однако в 2010 году Совет USAN отменил свое предыдущее решение и присвоил название «эзогабин», принятое в США . препарату [ 26 ] Таким образом, препарат будет известен как «эзогабин» в США и «ретигабин» в других странах.
Ссылки
[ редактировать ]- ^ Феррон Г.М., Пол Дж., Фрунчилло Р., Ричардс Л., Кнебель Н., Гетси Дж., Трой С. (февраль 2002 г.). «Многодозовая, линейная, пропорциональная дозе фармакокинетика ретигабина у здоровых добровольцев». Журнал клинической фармакологии . 42 (2): 175–182. дои : 10.1177/00912700222011210 . ПМИД 11831540 . S2CID 5568963 .
- ^ «Таблетки ПОТИГА (эзогабин), резюме. Полная информация о назначении» (PDF) . GlaxoSmithKline и Valeant Pharmaceuticals . Проверено 4 июня 2014 г.
- ^ https://assets.publishing.service.gov.uk/media/57fe4b6640f0b6713800000c/Trobalt_letter.pdf . [ только URL-адрес PDF ]
- ^ «Препарат от эпилепсии Тробалт (ретигабин) будет прекращен» . epilepsysociety.org.uk . 14 сентября 2016 г.
- ^ Перейти обратно: а б Рундфельдт С. (октябрь 1997 г.). «Новый противосудорожный препарат ретигабин (D-23129) действует как открыватель K+-каналов в нейрональных клетках». Европейский журнал фармакологии . 336 (2–3): 243–249. дои : 10.1016/S0014-2999(97)01249-1 . ПМИД 9384239 .
- ^ Перейти обратно: а б Мейн М.Дж., Крайан Дж.Э., Дюпер Дж.Р., Кокс Б., Клэр Дж.Дж., Бербидж С.А. (август 2000 г.). «Модуляция калиевых каналов KCNQ2/3 новым противосудорожным средством ретигабином». Молекулярная фармакология . 58 (2): 253–262. дои : 10.1124/моль.58.2.253 . ПМИД 10908292 . S2CID 11112809 .
- ^ Перейти обратно: а б Рогавский М.А., Базиль К.В. (июль 2008 г.). «Новые молекулярные мишени для противоэпилептических препаратов: альфа (2) дельта, SV2A и калиевые каналы K (v) 7 / KCNQ / M» . Текущие отчеты по неврологии и нейробиологии . 8 (4): 345–352. дои : 10.1007/s11910-008-0053-7 . ПМК 2587091 . ПМИД 18590620 .
- ^ Перейти обратно: а б с д Бен-Менахем Э (2007). «Ретигабин: нашла ли сирота дом?» . Течения эпилепсии . 7 (6): 153–154. дои : 10.1111/j.1535-7511.2007.00209.x . ПМК 2096728 . ПМИД 18049722 .
- ^ Перейти обратно: а б с Плоскер Г.Л., Скотт Л.Дж. (2006). «Ретигабин: при парциальных припадках». Препараты ЦНС . 20 (7): 601–8, обсуждение 609–10. дои : 10.2165/00023210-200620070-00005 . ПМИД 16800718 . S2CID 23557118 .
- ^ Перейти обратно: а б Портер Р.Дж., Партиот А, Сачдео Р., Нория В., Алвес В.М. (апрель 2007 г.). «Рандомизированное многоцентровое исследование ретигабина с диапазоном доз при парциальных припадках». Неврология . 68 (15): 1197–1204. дои : 10.1212/01.wnl.0000259034.45049.00 . ПМИД 17420403 . S2CID 24574886 .
- ^ «Потига (Эзогабин): Сообщение о безопасности лекарств» . Управление по контролю за продуктами и лекарствами .
- ^ Перейти обратно: а б Хитт Э (13 июня 2011 г.). «FDA одобрило эзогабин для лечения судорог у взрослых» . Медскейп . Проверено 13 июня 2011 г.
- ^ Перейти обратно: а б с д и «Тробальт – Сводные характеристики продукта (SPC)» . электронный справочник лекарственных средств. 05 мая 2011 г. Проверено 13 июня 2011 г.
- ^ Перейти обратно: а б с Лущки Ю.Дж. (2009). «Противоэпилептические препараты третьего поколения: механизмы действия, фармакокинетика и взаимодействие». Фармакологические отчеты . 61 (2): 197–216. дои : 10.1016/s1734-1140(09)70024-6 . ПМИД 19443931 . S2CID 72918370 .
- ^ Браун Д.А., генеральный директор Пассмор (апрель 2009 г.). «Нейронные каналы KCNQ (Kv7)» . Британский журнал фармакологии . 156 (8): 1185–1195. дои : 10.1111/j.1476-5381.2009.00111.x . ПМЦ 2697739 . ПМИД 19298256 .
- ^ Корбин-Лефтвич А., Моссадек С.М., Ха Дж., Ручала И., Ле А.Х., Вильяльба-Галеа, Калифорния (март 2016 г.). «Ретигабин удерживает каналы KV7 открытыми и стабилизирует потенциал покоя» . Журнал общей физиологии . 147 (3): 229–241. дои : 10.1085/jgp.201511517 . ПМЦ 4772374 . ПМИД 26880756 .
- ^ Вильяльба-Галеа, Калифорния (19 июня 2020 г.). «Модуляция дезактивации канала КВ 7 с помощью ПИ(4,5)П 2 » . Границы в фармакологии . 11 : 895. дои : 10.3389/fphar.2020.00895 . ПМЦ 7318307 . ПМИД 32636742 .
- ^ Рогавский М.А. (июнь 2006 г.). «Различные механизмы разработки противоэпилептических препаратов» . Исследования эпилепсии . 69 (3): 273–294. doi : 10.1016/j.eplepsyres.2006.02.004 . ПМЦ 1562526 . ПМИД 16621450 .
- ^ «Valeant Pharmaceuticals объявляет предварительные результаты исследования ретигабина фазы IIa для лечения постгерпетической невралгии (PHN)» (пресс-релиз). PRNewswire. 24 августа 2009 г. Проверено 13 июня 2011 г.
- ^ «Ретигабин NDA принят к подаче» (Пресс-релиз). PRNewswire. 30 декабря 2009 г. Проверено 19 июля 2010 г.
- ^ Перейти обратно: а б Лоури Ф (12 августа 2010 г.). «Лекарственное средство от эпилепсии экзогабин получило зеленый свет от Консультативной группы FDA» . Медскейп . Проверено 13 августа 2010 г.
- ^ [Авторы не указаны] (25 июня 2010 г.). «11 августа 2010 г.: Объявление о заседании Консультативного комитета по препаратам для лечения заболеваний периферической и центральной нервной системы» . США Управление по контролю за продуктами и лекарствами . Проверено 19 июля 2010 г.
- ^ Управление по борьбе с наркотиками США (15 декабря 2011 г.). «Списки контролируемых веществ: включение эзогабина в список V» (PDF) . Федеральный реестр . 76 (241).
- ^ Всемирная организация здравоохранения (1996). «Международные непатентованные наименования фармацевтических веществ (МНН). Предлагаемое МНН: Список 76» (PDF) . Информация ВОЗ о лекарствах . 10 (4): 215. Архивировано из оригинала (PDF) 27 июня 2004 г.
- ^ [Авторы не указаны] (2005–2006). «Заявление о непатентованном названии, принятом советом USAN: Ретигабин» (PDF) . Американская медицинская ассоциация . Проверено 19 июля 2010 г.
- ^ [Авторы не указаны] (2010). «Заявление о непатентованном названии, принятом советом USAN: Эзогабин» (PDF) . Американская медицинская ассоциация . Архивировано из оригинала (PDF) 2 апреля 2012 г. Проверено 19 июля 2010 г.
Дальнейшее чтение
[ редактировать ]- Блэкберн-Манро Дж., Долби-Браун В., Мирза Н.Р., Миккельсен Дж.Д., Блэкберн-Манро Р.Э. (2005). «Ретигабин: химический синтез и клиническое применение» . Обзоры препаратов для ЦНС . 11 (1): 1–20. дои : 10.1111/j.1527-3458.2005.tb00033.x . ПМК 6741764 . ПМИД 15867950 .
- Хемпель Р., Шупке Х., Макнилли П.Дж., Хайнеке К., Кронбах С., Грюнвальд С. и др. (май 1999 г.). «Метаболизм ретигабина (D-23129), нового противосудорожного средства» . Метаболизм и распределение лекарств . 27 (5): 613–622. ПМИД 10220491 .