Диэтиловый эфир
| |

| |

| |
| Имена | |
|---|---|
| Предпочтительное название ИЮПАК
Этоксиэтан | |
Другие имена
| |
| Идентификаторы | |
3D model ( JSmol )
|
|
| 1696894 | |
| КЭБ | |
| ХЭМБЛ | |
| ХимическийПаук | |
| Информационная карта ECHA | 100.000.425 |
| Номер ЕС |
|
| 25444 | |
| КЕГГ | |
ПабХим CID
|
|
| номер РТЭКС |
|
| НЕКОТОРЫЙ | |
| Число | 1155 |
Панель управления CompTox ( EPA )
|
|
| Характеристики | |
| С 4 Н 10 О | |
| Молярная масса | 74.123 g·mol −1 |
| Появление | Бесцветная жидкость |
| Запах | Сухой, ромовый, сладковатый запах [ 1 ] |
| Плотность | 0,7134 г/см 3 , жидкость |
| Температура плавления | -116,3 ° C (-177,3 ° F; 156,8 К) |
| Точка кипения | 34,6 ° C (94,3 ° F; 307,8 К) [ 4 ] |
| 6,05 г/(100 мл) [ 2 ] | |
| войти P | 0.98 [ 3 ] |
| Давление пара | 440 мм рт.ст. (58,66 кПа) при 20 °C [ 1 ] |
| −55.1·10 −6 см 3 /моль | |
Показатель преломления ( n D )
|
1,353 (20 °С) |
| Вязкость | 0,224 сП (25 °С) |
| Структура | |
| 1,15 Д (газ) | |
| Термохимия | |
Теплоемкость ( С )
|
172,5 Дж/(моль К) |
Стандартный моляр
энтропия ( S ⦵ 298 ) |
253,5 Дж/(моль К) |
Стандартная энтальпия
образование (Δ f H ⦵ 298 ) |
−271,2 ± 1,9 кДж/моль |
Стандартная энтальпия
горение (Δ c H ⦵ 298 ) |
−2732,1 ± 1,9 кДж/моль |
| Фармакология | |
| N01AA01 ( ВОЗ ) | |
| Опасности | |
| Безопасность и гигиена труда (OHS/OSH): | |
Основные опасности
|
Чрезвычайно воспламеняем, вреден для кожи, разлагается до взрывоопасных перекисей на воздухе и на свету. [ 1 ] |
| СГС Маркировка : | |
 
| |
| Опасность | |
| Х224 , Х302 , Х336 | |
| P210 , P233 , P240 , P241 , P242 , P243 , P261 , P264 , P270 , P271 , P280 , P301+P312 , P303+P361+P353 , P304+P340 , P312 , P330 , П370+П378 , П403+П233 , П403+П235 , П405 , П501 | |
| NFPA 704 (огненный алмаз) | |
| точка возгорания | -45 ° C (-49 ° F; 228 К) [ 7 ] |
| 160 ° С (320 ° F; 433 К) [ 7 ] | |
| Взрывоопасные пределы | 1.9–48.0% [ 5 ] |
| Летальная доза или концентрация (LD, LC): | |
ЛК 50 ( средняя концентрация )
|
73 000 частей на миллион (крыса, 2 часа) 6500 частей на миллион (мышь, 1,65 часа) [ 6 ] |
LC Lo ( самый низкий из опубликованных )
|
106 000 частей на миллион (кролик) 76 000 частей на миллион (собака) [ 6 ] |
| NIOSH (пределы воздействия на здоровье в США): | |
ПЭЛ (допустимо)
|
TWA 400 частей на миллион (1200 мг/м 3 ) [ 1 ] |
РЕЛ (рекомендуется)
|
Нет установленного REL [ 1 ] |
IDLH (Непосредственная опасность)
|
1900 частей на миллион [ 1 ] |
| Паспорт безопасности (SDS) | Внешний паспорт безопасности материалов |
| Родственные соединения | |
Связанные эфиры
|
|
Родственные соединения
|
|
| Страница дополнительных данных | |
| Диэтиловый эфир (страница данных) | |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа).
| |
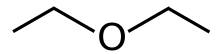
Диэтиловый эфир , или просто эфир , представляет собой органическое соединение с химической формулой (CH 3 CH 2 ) 2 O , иногда сокращенно Эт 2 О. [ а ] Это бесцветная, очень летучая , сладко пахнущая («эфирный запах»), чрезвычайно легковоспламеняющаяся жидкость . Относится к эфирному классу органических соединений. Это обычный растворитель . Раньше его использовали в качестве общего анестетика . [ 8 ]
Производство
[ редактировать ]Большая часть диэтилового эфира производится как побочный продукт паровой гидратации этилена этанола получением с . на твердом носителе на основе фосфорной кислоты В этом процессе используются катализаторы , и при необходимости его можно отрегулировать для производства большего количества эфира: [ 9 ] Парофазная дегидратация этанола на некоторых катализаторах на основе оксида алюминия может давать выходы диэтилового эфира до 95%. [ 10 ]
- 2 СН 3 СН 2 ОН → (СН 3 СН 2 ) 2 О + Н 2 О
Диэтиловый эфир можно получать как в лабораториях, так и в промышленных масштабах путем синтеза кислого эфира. [ 11 ]
Использование
[ редактировать ]Диэтиловый эфир преимущественно используется в качестве растворителя. Одним из конкретных применений является производство целлюлозных пластиков, таких как ацетат целлюлозы . [ 9 ]
Лабораторный растворитель
[ редактировать ]Это обычный растворитель реакции Гриньяра в дополнение к другим реакциям с участием металлоорганических реагентов. [ 12 ] Эти виды использования используют его простоту. Диэтиловый эфир — популярный неполярный растворитель в жидкостно-жидкостной экстракции . Как экстрагент он несмешивается с водой и имеет меньшую плотность , чем вода.
Хотя он несмешивается, он обладает значительной растворимостью в воде (6,05 г/(100 мл) при 25 °C. [ 2 ] ) и растворяет 1,5 г/(100 г) (1,0 г/(100 мл)) воды при 25 °C. [ 13 ]
Топливо
[ редактировать ]Диэтиловый эфир имеет высокое цетановое число 85–96 и в сочетании с нефтяными дистиллятами для бензиновых и дизельных двигателей [ 14 ] используется в качестве стартовой жидкости из-за ее высокой летучести и низкой температуры вспышки . Эфирная пусковая жидкость продается и используется в странах с холодным климатом, так как может помочь при холодном запуске двигателя при минусовой температуре. По той же причине он также используется в качестве компонента топливной смеси карбюраторных двигателей моделей с воспламенением от сжатия .
Химические реакции
[ редактировать ]Тетрафторборат триэтилоксония получают из трифторида бора , диэтилового эфира и эпихлоргидрина : [ 15 ]
- 4 Et 2 O BF 3 + 2 Et 2 O + 3 C 2 H 3 OCH 2 Cl → 3 [Et 3 O] + [БФ 4 ] − + B(OCH(CH 2 Cl)CH 2 OEt) 3
Диэтиловый эфир представляет собой твердое основание Льюиса, которое реагирует с различными кислотами Льюиса, такими как йод , фенол и триметилалюминий , а параметры его основания в модели ECW составляют EB = 1,80 и CB = 1,63. Диэтиловый эфир — распространенный лабораторный апротонный растворитель .
Диэтиловый эфир склонен к образованию гидропероксидов .
Метаболизм
[ редактировать ]эфир . Предполагается, что фермент цитохрома P450 метаболизирует диэтиловый [ 16 ]
Диэтиловый эфир ингибирует алкогольдегидрогеназу и тем самым замедляет метаболизм этанола . [ 17 ] Он также ингибирует метаболизм других лекарств, требующих окислительного метаболизма . Например, диазепам требует окисления в печени, тогда как его окисленный метаболит оксазепам этого не делает. [ 18 ]
Безопасность, стабильность, правила
[ редактировать ]Диэтиловый эфир чрезвычайно огнеопасен и может образовывать взрывоопасные смеси паров и воздуха. [ 19 ]
Поскольку эфир тяжелее воздуха, он может собираться низко над землей, а пары могут перемещаться на значительные расстояния к источникам возгорания. Эфир воспламеняется при воздействии открытого огня, однако из-за его высокой воспламеняемости для воспламенения не требуется открытое пламя. Другие возможные источники воспламенения включают, помимо прочего, горячие плиты, паровые трубы, нагреватели и электрические дуги, создаваемые выключателями или розетками. [ 19 ] Пар также может воспламениться из-за статического электричества, которое может накапливаться, когда эфир переливается из одного сосуда в другой. Температура самовоспламенения диэтилового эфира составляет 160 ° C (320 ° F). Диффузия диэтилового эфира в воздухе составляет 9,18×10. −6 м 2 /с (298 К, 101325 кПа). [ нужна ссылка ]
Эфир чувствителен к свету и воздуху и имеет тенденцию образовывать взрывоопасные перекиси . [ 19 ] Пероксиды эфира имеют более высокую температуру кипения, чем эфир, и в сухом состоянии являются контактными взрывчатыми веществами. [ 19 ] Коммерческий диэтиловый эфир обычно поставляется со следовыми количествами антиоксиданта бутилированного гидрокситолуола (ВНТ), который снижает образование пероксидов. При хранении над гидроксидом натрия осаждаются промежуточные гидроперекиси эфира. Воду и пероксиды можно удалить либо перегонкой натрия и бензофенона , либо пропусканием через колонну с активированным оксидом алюминия . [ 20 ]
Из-за его применения при производстве незаконных веществ он внесен в Таблицу прекурсоров II согласно Конвенции Организации Объединенных Наций против незаконного оборота наркотических средств и психотропных веществ, а также таких веществ, как ацетон , толуол и серная кислота . [ 21 ]
История
[ редактировать ]Соединение могло быть синтезировано Джабиром ибн Хайяном в 8 веке. [ 22 ] или Рамон Луллий в 1275 году. [ 22 ] [ 23 ] Оно было синтезировано в 1540 году Валериусом Кордусом , который назвал его «сладким купоросным маслом» ( oleum dulce vitrioli ) — название отражает тот факт, что его получают путем перегонки смеси этанола и серной кислоты (тогда известной как купоросное масло). – и отметил некоторые его лечебные свойства . [ 22 ] Примерно в то же время Парацельс обнаружил у собак обезболивающие свойства этой молекулы. [ 22 ] Название «эфир» веществу дал в 1729 году Август Зигмунд Фробениус . [ 24 ]
Считалось, что это соединение серы, пока эта идея не была опровергнута примерно в 1800 году. [ 25 ]
Синтез диэтилового эфира реакцией этанола с серной кислотой известен с 13 века. [ 25 ]
Анестезия
[ редактировать ]

Уильям Т.Г. Мортон участвовал в публичной демонстрации эфирной анестезии 16 октября 1846 года в Эфирном куполе в Бостоне, штат Массачусетс . Мортон назвал свой препарат эфира с ароматическими маслами, чтобы скрыть его запах, « Летеон » в честь реки Леты (Λήθη, что означает «забвение, забвение»). [ 26 ] Однако теперь известно, что Кроуфорд Уильямсон Лонг в частном порядке продемонстрировал его использование в качестве общего анестетика в хирургии официальным лицам в Джорджии еще 30 марта 1842 года, а Лонг публично продемонстрировал использование эфира в качестве хирургического анестетика шесть раз перед демонстрацией в Бостоне. . [ 27 ] [ 28 ] [ 29 ] Британские врачи знали об анестезирующих свойствах эфира еще в 1840 году, когда его широко прописывали в сочетании с опиумом. [ 30 ] Некоторые практикующие врачи предпочли диэтиловый эфир хлороформу в качестве общего анестетика из-за более благоприятного терапевтического индекса эфира , то есть большей разницы между эффективной дозой и потенциально токсичной дозой. [ 31 ]
Диэтиловый эфир не угнетает миокард , а скорее стимулирует симпатическую нервную систему, что приводит к гипертензии и тахикардии. Его безопасно использовать у пациентов с шоком, поскольку он сохраняет барорецепторный рефлекс . [ 32 ] Его минимальное влияние на угнетение миокарда и дыхательную активность, а также его низкая стоимость и высокий терапевтический индекс позволяют продолжать его использование в развивающихся странах. [ 33 ] Диэтиловый эфир также можно смешивать с другими анестетиками, такими как хлороформ для получения смеси CE , или хлороформ и спирт для получения смеси ACE . В 21 веке эфир используется редко. Использование горючего эфира было заменено негорючими фторсодержащими углеводородными анестетиками. Галотан был первым разработанным таким анестетиком, а другие используемые в настоящее время ингаляционные анестетики, такие как изофлюран , десфлюран и севофлуран , представляют собой галогенированные эфиры. [ 34 ] Было обнаружено, что диэтиловый эфир имеет нежелательные побочные эффекты, такие как послеанестезионная тошнота и рвота. Современные анестетики уменьшают эти побочные эффекты. [ 27 ]

До 2005 года он входил в Список основных лекарственных средств Всемирной организации здравоохранения для использования в качестве анестетика. [ 35 ] [ 36 ]
Лекарство
[ редактировать ]Эфир когда-то использовался в фармацевтических препаратах. Смесь спирта и эфира, одна часть диэтилового эфира и три части этанола, была известна как «Дух эфира» Гофмана , «Анодин » или «Капли Гофмана». В Соединенных Штатах эта смесь была исключена из Фармакопеи в какой-то момент до июня 1917 года. [ 37 ] как исследование, опубликованное Уильямом Проктером-младшим в Американском фармацевтическом журнале еще в 1852 году, показало, что существуют различия в рецептуре между коммерческими производителями, между международной фармакопеей и оригинальным рецептом Хоффмана. [ 38 ] Его также применяют для лечения икоты путем закапывания в полость носа. [ 39 ]
Рекреационное насилие
[ редактировать ]Рекреационное использование эфира также имело место на организованных вечеринках в 19 веке, называемых эфирными развлечениями , где гостям предлагалось вдыхать терапевтическое количество диэтилового эфира или закиси азота , вызывая состояние возбуждения. Лонг, а также его коллеги-дантисты Хорас Уэллс , Уильям Эдвард Кларк и Уильям Т.Г. Мортон заметили, что во время этих собраний люди часто получали легкие травмы, но, похоже, не проявляли никакой реакции на травму или воспоминаний о том, что это произошло, демонстрируя анестезирующее действие эфира. . [ 40 ]
В 19-м и начале 20-го века употребление эфира было популярно среди польских крестьян. [ 41 ] Это традиционный и до сих пор относительно популярный рекреационный наркотик среди лемков . [ 42 ] Его обычно употребляют в небольшом количестве ( кропка , или «точка»), заливая молоком , сахарной водой или апельсиновым соком в рюмке . Известно, что как наркотик он вызывает психологическую зависимость , иногда называемую эфироманией . [ 43 ] [ нужна медицинская ссылка ]
См. также
[ редактировать ]- Великий момент - фильм об Уильяме Т.Г. Мортоне и эфире
Пояснительные примечания
[ редактировать ]- ^ Et означает одновалентную этильную группу. CH 3 CH 2, который часто записывается как C 2 H 5 (см. обозначение псевдоэлемента )
Ссылки
[ редактировать ]- ^ Перейти обратно: а б с д и ж Карманный справочник NIOSH по химическим опасностям. «#0277» . Национальный институт охраны труда и здоровья (NIOSH).
- ^ Перейти обратно: а б Индекс Merck , 10-е изд., Марта Виндхольц, редактор, Merck & Co., Inc, Рэуэй, Нью-Джерси, 1983, стр. 551
- ^ «Диэтиловый эфир_msds» .
- ^ «Диэтиловый эфир» . Химический Паук . Проверено 19 января 2017 г.
- ^ Карл Л. Явс, Справочник по химическим свойствам , McGraw-Hill, Нью-Йорк, 1999, стр. 567
- ^ Перейти обратно: а б «Этиловый эфир» . Непосредственно опасные для жизни и здоровья концентрации (IDLH) . Национальный институт охраны труда и здоровья (NIOSH).
- ^ Перейти обратно: а б «Этиловый эфир, Паспорт безопасности» . Джей Ти Бейкер. Архивировано из оригинала 28 марта 2012 г. Проверено 24 июня 2010 г.
- ^ Сакут, Майкл; Менсинг, Томас; Шулер, Иоахим; Хайтманн, Вильгельм; Стрелке, Гюнтер; Майер, Дитер (2010). «Эфиры алифатические». Энциклопедия промышленной химии Ульмана . дои : 10.1002/14356007.a10_023.pub2 . ISBN 978-3-527-30385-4 .
- ^ Перейти обратно: а б «Эфиры Лоуренса Караса и У. Дж. Пиля». Энциклопедия химической технологии Кирка-Отмера . Джон Вили и сыновья, Inc., 2004 г.
- ^ Этиловый эфир, Chem. Справочник по экономике . Менло-Парк, Калифорния: SRI International. 1991.
- ^ Коэн, Юлиус Беренд (1920). Учебник органической химии, том 1 . Лондон: Macmillan and Co. p. 39 .
строение диэтилового эфира этилового спирта Коэна Юлиуса.
- ^ Мойер, WW; Marveltitle = Триэтилкарбинол, CS (1931). Органические синтезы . 11 : 98. дои : 10.15227/orgsyn.011.0098 .
{{cite journal}}: Отсутствует или пусто|title=( помощь ) - ^ Х.Х. Роули; Вм. Р. Рид (1951). «Растворимость воды в диэтиловом эфире при 25°». Дж. Ам. хим. Соц . 73 (6): 2960. doi : 10.1021/ja01150a531 .
- ^ «Стартовая жидкость повышенной прочности: как она работает» . Вальвовина. Архивировано из оригинала 27 сентября 2007 г. Проверено 5 сентября 2007 г.
- ^ Х. Меервейн (1966). «Триэтилоксониум фторборат». Органические синтезы . 46 : 113. дои : 10.15227/orgsyn.046.0113 .
- ^ 109. Мутантный штамм 241 Aspergillus flavus, заблокированный в биосинтезе афлатоксина, не накапливает транскрипт aflR. Архивировано 17 сентября 2017 г. в Wayback Machine. Мэтью П. Браун и Гэри А. Пейн, Университет штата Северная Каролина , Роли, Северная Каролина, fgsc.net.
- ^ П.Т. Норманн; А. Рипель; Дж. Морланд (1987). «Диэтиловый эфир ингибирует метаболизм этанола in vivo путем взаимодействия с алкогольдегидрогеназой». Алкоголизм: клинические и экспериментальные исследования . 11 (2): 163–166. дои : 10.1111/j.1530-0277.1987.tb01282.x . ПМИД 3296835 .
- ^ Ларри К. Кифер; Уильям А. Гарланд; Нил Ф. Олдфилд; Джеймс Э. Свагдис; Брюс А. Мико (1985). «Ингибирование метаболизма N-нитрозодиметиламина у крыс эфирной анестезией» (PDF) . Исследования рака . 45 (11, ч. 1): 5457–5460. ПМИД 4053020 .
- ^ Перейти обратно: а б с д «Архивная копия» (PDF) . Архивировано из оригинала (PDF) 13 ноября 2014 г. Проверено 15 февраля 2014 г.
{{cite web}}: CS1 maint: архивная копия в заголовке ( ссылка ) - ^ ВЛФ Армарего; CLL Чай (2003). Очистка лабораторных химикатов . Бостон: Баттерворт-Хайнеманн. ISBN 978-0-7506-7571-0 .
- ^ Microsoft Word - RedListE2007.doc. Архивировано 27 февраля 2008 г. на Wayback Machine.
- ^ Перейти обратно: а б с д Тоски, Джудит А; Бэкон, Дуглас Р.; Калверли, Род К. (2001). История анестезиологии В: Бараш, Пол Г; Каллен, Брюс Ф; Стултинг, Роберт К. Клиническая анестезия (4-е изд.). Липпинкотт Уильямс и Уилкинс. п. 3. ISBN 978-0-7817-2268-1 .
- ^ Хадеменос, Джордж Дж.; Мерфри, Шон; Залер, Кэти; Уорнер, Дженнифер М. (2008). PCAT компании McGraw-Hill . МакГроу-Хилл. п. 39. ИСБН 978-0-07-160045-3 . Проверено 25 мая 2011 г.
- ^ «VIII. Отчет о Spiritus Vini æthereus, а также о нескольких экспериментах, проведенных с ним». Философские труды Лондонского королевского общества . 36 (413): 283–289. 1730. дои : 10.1098/rstl.1729.0045 . S2CID 186207852 .
- ^ Перейти обратно: а б Чисхолм, Хью , изд. (1911). . Британская энциклопедия . Том. 9 (11-е изд.). Издательство Кембриджского университета. п. 806.
- ^ Кавендиш, Маршалл (2008). Изобретатели и изобретения, Том 4 . Маршалл Кавендиш. п. 1129. ИСБН 978-0-7614-7767-9 .
- ^ Перейти обратно: а б Хилл, Джон В. и Колб, Дорис К. Химия в эпоху перемен: 10-е издание . п. 257. Пирсон: Прентис Холл. Река Аппер-Сэддл, Нью-Джерси. 2004.
- ^ Мэдден, М. Лесли (14 мая 2004 г.). «Кроуфорд Лонг (1815–1878)» . Энциклопедия Новой Джорджии . Издательство Университета Джорджии . Проверено 13 февраля 2015 г.
- ^ «Кроуфорд В. Лонг» . День врачей . Южная медицинская ассоциация. Архивировано из оригинала 13 февраля 2015 года . Проверено 13 февраля 2015 г.
- ^ Граттан, Н. «Лечение маточного кровотечения». Провинциальный медико-хирургический журнал . Том. 1, № 6 (7 ноября 1840 г.), с. 107.
- ^ Кальдероне, ФА (1935). «Исследования дозировки эфира после преданестезирующего лечения наркотиками (барбитураты, сульфат магния и морфин)» (PDF) . Журнал фармакологии и экспериментальной терапии . 55 (1): 24–39.
- ^ «Эфирные эффекты» . 31 октября 2010 г.
- ^ «Эфир и его эффекты в анестезии» . Общая анестезия . 31 октября 2010 г.
- ^ Морган, Г. Эдвард-младший и др. (2002). Клиническая анестезиология 3-е изд. Нью-Йорк: МакГроу-Хилл. п. 3.
- ^ «Модельный список основных лекарственных средств ВОЗ (пересмотренный в апреле 2003 г.)» (PDF) . apps.who.int (13-е изд.). Женева, Швейцария: Всемирная организация здравоохранения. Апрель 2003 года . Проверено 6 сентября 2017 г.
- ^ «Модельный список основных лекарственных средств ВОЗ (пересмотренный в марте 2005 г.)» (PDF) . apps.who.int (14-е изд.). Женева, Швейцария: Всемирная организация здравоохранения. Март 2005 г. Архивировано из оригинала (PDF) 5 августа 2005 г. Проверено 6 сентября 2017 г.
- ^ Национальный фармацевт, том 47, июнь 1917 г., стр. 220.
- ^ Проктер, Уильям младший (1852). «Об болеутоляющем ликере Хоффмана» . Американский фармацевтический журнал . 28 .
- ^ ncbi, Лечение икоты закапыванием эфира в полость носа.
- ^ «Как эфир превратился из развлекательного наркотика в первый хирургический анестетик» . Смитсоновский журнал . Проверено 11 октября 2020 г.
- ^ Зандберг, Адриан (2010). «Краткая статья «Деревни… Вонь паров эфира»: употребление эфира в Силезии до 1939 года» . Медицинская история . 54 (3): 387–396. дои : 10.1017/s002572730000466x . ПМК 2890321 . ПМИД 20592886 .
- ^ Кашицкий, Нестор (30 августа 2006 г.). «Лемковская Ватра в Ждыне 2006 – охраняем огонь памяти» . Histmag.org – история изнутри (на польском языке). Краков, Польша: i-Press . Проверено 25 ноября 2009 г.
В прошлом эфир использовался в медицине для наркоза, поскольку он обладает галлюциногенными свойствами, и всего нескольких капель при вдыхании было достаточно, чтобы сильно обезболить пациента. Однако эфир, как и любая жидкость, теоретически может быть напитком. Лемки практикуют эту теорию. И все же называть сжиженный эфир - "точку" - их "национальным напитком" было бы преувеличением. Хотя это часть мифа о «лемковости».
- ^ Кренц, Соня; Циммерманн, Грегуар; Колли, Стефан; Зуллино, Даниэле Фабио (август 2003 г.). «Эфир: забытая зависимость» . Зависимость . 98 (8): 1167–1168. дои : 10.1046/j.1360-0443.2003.00439.x . ПМИД 12873252 .
Внешние ссылки
[ редактировать ]- Заявление Майкла Фарадея об эфире как обезболивающем средстве в 1818 году. Архивировано 22 мая 2011 г. в Wayback Machine.
- Расчет давления пара , плотности жидкости , динамической вязкости жидкости , поверхностного натяжения диэтилового эфира, ddbonline.ddbst.de
- CDC - Карманный справочник NIOSH по химическим опасностям
