Солриамфетол
 | |
| Клинические данные | |
|---|---|
| Торговые названия | Суноси |
| Другие имена | SKL-N05, ADX-N05, ARL-N05, YKP10A, R228060 и JZP-110; ( R )-2-амино-3-фенилпропилкарбамат гидрохлорид |
| AHFS / Drugs.com | Монография |
| МедлайнПлюс | а619040 |
| Данные лицензии |
|
| Маршруты администрация | Через рот [ 1 ] |
| Класс препарата | Ингибиторы обратного захвата норадреналина и дофамина ; Агенты, способствующие бодрствованию ; Психостимуляторы |
| код АТС | |
| Юридический статус | |
| Юридический статус | |
| Фармакокинетические данные | |
| Биодоступность | ~95% [ 1 ] |
| Связывание с белками | 13.3–19.4% [ 1 ] |
| Метаболизм | Минимальный (~1%) [ 1 ] |
| Метаболиты | • N -ацетилзолриамфетол (~1%) [ 1 ] |
| Период полувыведения | ~7,1 часа [ 1 ] |
| Экскреция | Моча (95% без изменений) |
| Идентификаторы | |
| Номер CAS | |
| ПабХим CID | |
| ИЮФАР/БПС | |
| Лекарственный Банк | |
| ХимическийПаук | |
| НЕКОТОРЫЙ | |
| КЕГГ | |
| ХЭМБЛ | |
| Панель управления CompTox ( EPA ) | |
| Химические и физические данные | |
| Формула | С 10 Н 14 Н 2 О 2 |
| Молярная масса | 194.234 g·mol −1 |
| 3D model ( JSmol ) | |
Солриамфетол , продаваемый под торговой маркой Sunosi , представляет собой лекарство, способствующее бодрствованию, используемое при лечении чрезмерной сонливости , связанной с нарколепсией и апноэ во сне . [ 1 ] [ 5 ] [ 6 ] Его принимают внутрь . [ 1 ]
Общие побочные эффекты солриамфетола включают головную боль , тошноту , беспокойство и проблемы со сном . [ 1 ] Это ингибитор обратного захвата норэпинефрина-дофамина (NDRI), который, как полагают, действует за счет повышения уровня нейротрансмиттеров норадреналина и дофамина в мозге . [ 1 ] [ 5 ] Также было обнаружено, что солриамфетол действует как TAAR1 агонист , и это действие также может быть связано с его эффектами. [ 7 ]
Препарат был обнаружен дочерней компанией SK Group , которая в 2011 году лицензировала права компании Aerial Pharma за пределами одиннадцати стран Азии. [ 8 ] Помимо одобренного показания к чрезмерной сонливости, солриамфетол находится в стадии разработки для некоторых других целей, включая лечение синдрома дефицита внимания и гиперактивности (СДВГ), компульсивного переедания и нарушений циркадных ритмов сна . [ 9 ]
Медицинское использование
[ редактировать ]Солриамфетол используется для улучшения бодрствования при лечении чрезмерной дневной сонливости , связанной с нарколепсией или обструктивным апноэ во сне у взрослых. [ 1 ] По-видимому, он более эффективен в снижении чрезмерной сонливости в дневное время, связанной с обструктивным апноэ во сне, чем некоторые другие средства, способствующие бодрствованию, включая модафинил , армодафинил и питолизант . [ 10 ]
Доступные формы
[ редактировать ]Солриамфетол выпускается в форме по 75 и 150 мг для перорального применения таблеток . [ 1 ]
Побочные эффекты
[ редактировать ]Побочные эффекты солриамфетола включают головную боль , тошноту , снижение аппетита , бессонницу , беспокойство , раздражительность , нервозность , головокружение , дискомфорт в груди учащенное , сердцебиение , сухость во рту , повышенное потоотделение , боли в животе , запор и диарею . [ 1 ]
Потенциал неправильного использования
[ редактировать ]Солриамфетол в дозах, превышающих одобренные, а именно в дозах 300, 600 и 1200 мг, что в 2–4 раза превышает максимальную рекомендуемую дозу, вызывает сходные с приемом препарата реакции, , включая повышенное настроение и чувство расслабления , которые схожи по степени тяжести. к фентермину ( Списка IV контролируемому веществу ). [ 1 ] Повышенное настроение наблюдалось у 2,4% при приеме плацебо , от 8 до 24% при приеме солриамфетола и от 10 до 18% при приеме фентермина, тогда как чувство расслабления возникало у 5% при приеме плацебо, от 5 до 19% при приеме солриамфетола и от 15 до 20% при приеме фентермина. [ 1 ] Таким образом, солриамфетол имеет значительный потенциал злоупотребления и является контролируемым веществом в Соединенных Штатах . [ 1 ] Однако солриамфетол показал меньший потенциал злоупотребления, чем Списка II, контролируемые стимуляторы такие как амфетамин и кокаин . [ 11 ] Следовательно, потенциал злоупотребления солриамфетола был оценен как низкий, и он был помещен в категорию контролируемых веществ Списка IV наряду с фентермином. [ 11 ]
Фармакология
[ редактировать ]Фармакодинамика
[ редактировать ]Солриамфетол является ингибитором обратного захвата норадреналина и дофамина (NDRI). [ 1 ] Он связывается с переносчиком дофамина (DAT) и переносчиком норадреналина (NET) со сродством (K i ) 14,2 мкМ и 3,7 мкМ соответственно. [ 1 ] Он ингибирует обратный захват дофамина и норадреналина со значениями IC 50 2,9 мкМ и 4,4 мкМ соответственно. [ 1 ] Он имеет слабое сродство к переносчику серотонина (K i = 81,5 мкМ) и существенно не ингибирует обратный захват серотонина (IC 50 > 100 мкМ). [ 1 ] Было обнаружено, что в дополнение к ингибированию обратного захвата дофамина и норэпинефрина солриамфетол действует как агонист человека и грызунов TAAR1 ( EC 50 = 10–16 мкМ) в клинически значимых концентрациях, аналогичных концентрациям, вызывающим ингибирование DAT и NET. [ 7 ] Солриамфетол не имеет заметного сродства к ряду других мишеней, включая дофаминовые , серотониновые , адренергические , ГАМК , аденозиновые , гистаминовые , орексиновые , бензодиазепиновые и ацетилхолиновые рецепторы . [ 1 ]
Фармакокинетика
[ редактировать ]биодоступность Пероральная . солриамфетола составляет примерно 95% [ 1 ] Среднее время достижения пикового уровня солриамфетола составляет 2 часа с диапазоном от 1,25 до 3,0 часов. [ 1 ] Прием пищи с высоким содержанием жиров оказывает минимальное влияние на пиковую и общую концентрацию солриамфетола, но задерживает время достижения пиковых уровней примерно на 1 час. [ 1 ] Видимый объем распределения солриамфетола составляет примерно 199 л. [ 1 ] Связывание солриамфетола с белками плазмы составляет от 13,3% до 19,4% в диапазоне концентраций от 0,059 до 10,1 мкг/мл. [ 1 ] Солриамфетол минимально метаболизируется у человека. [ 1 ] Он демонстрирует первого порядка выведение при пероральном приеме и имеет период полувыведения около 7,1 часа. [ 1 ] Период полувыведения солриамфетола увеличивается на фоне нарушения функции почек . [ 1 ] Примерно 95% дозы солриамфетола выводится с мочой в виде неизмененного солриамфетола, а 1% или менее выводится в виде второстепенного неактивного метаболита N -ацетилсолриамфетола. [ 1 ]
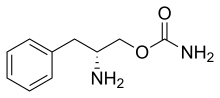
Химия
[ редактировать ]Солриамфетол представляет собой замещенный фенэтиламин, производный d- фенилаланина . [ 12 ] Его химическое название — ( R )-2-амино-3-фенилпропилкарбамат. [ 12 ]
История
[ редактировать ]Препарат был обнаружен дочерней компанией SK Group , которая в 2011 году лицензировала права компании Aerial Pharma за пределами одиннадцати стран Азии. [ 8 ] Компания Aerial провела два исследования фазы II препарата при нарколепсии. [ 13 ] перед продажей лицензии на солриамфетол компании Jazz в 2014 году; Jazz Pharmaceuticals выплатила Aerial 125 миллионов долларов авансом и выплатит Aerial и SK до 272 миллионов долларов в виде поэтапных платежей, а также выплатит SK двузначные роялти. [ 8 ] [ 14 ]
В 2019 году солриамфетол был одобрен в США для улучшения бодрствования у взрослых с нарколепсией или обструктивным апноэ во сне (СОАС). [ 15 ] [ 16 ] Ему был присвоен статус орфанного препарата . [ 17 ]
США Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) одобрило солриамфетол, главным образом, на основании данных пяти клинических исследований (Исследование 1/NCT02348593, Испытание 2/NCT02348606, Испытание 3/NCT02348619, Испытание 4/NCT02348632, Испытание 5 NCT01681121) с участием 622 пациентов с нарколепсия или обструктивное апноэ во сне (СОАС). [ 15 ] Испытания проводились в Канаде, Европе и США. [ 15 ]
Солриамфетол был одобрен для медицинского применения в Европейском Союзе в январе 2020 года. [ 4 ]
В марте 2022 года было объявлено, что Axsome Therapeutics приобретет Солриамфетол под торговой маркой Sunosi у Jazz Pharmaceuticals за первоначальную сумму в 53 миллиона долларов. Jazz получит высокий однозначный гонорар от чистых продаж Sunosi компанией Axsome в США в текущих показателях и средний однозначный гонорар в будущем. Axsome также возьмет на себя обязательства Jazz перед SK Biopharmaceuticals и Aerial Biopharma. [ 18 ]
Общество и культура
[ редактировать ]Имена
[ редактировать ]Во время разработки он назывался SKL-N05, ADX-N05, ARL-N05 и JZP-110. [ 9 ]
Юридический статус
[ редактировать ]В США солриамфетол внесен в список контролируемых веществ IV . [ 1 ] это означает, что он разрешен к использованию в медицинских целях и имеет низкую вероятность злоупотребления, но такое злоупотребление может привести к физической или психологической зависимости. [ 19 ] Требуется рецепт, и его можно пополнять не более пяти раз в течение шести месяцев. [ 20 ] В странах Евросоюза требуется рецепт. [ 4 ]
Исследовать
[ редактировать ]Солриамфетол находится в стадии разработки для лечения синдрома дефицита внимания и гиперактивности (СДВГ), компульсивного переедания и нарушений циркадных ритмов сна . [ 9 ] [ 21 ] По состоянию на сентябрь 2023 года он находится на стадии клинических испытаний 3 для лечения СДВГ и клинических исследований фазы 2 для лечения компульсивного переедания и нарушений циркадных ритмов сна. [ 9 ] [ 21 ] СДВГ . Опубликован отчет о применении солриамфетола для лечения [ 22 ] Солриамфетол также находился в стадии разработки для лечения депрессивных расстройств , но разработка по этому показанию была прекращена. [ 9 ] В мае 2024 года Национальные институты здравоохранения (NIH) объявили об испытании солриамфетола для лечения длительного COVID . [ 23 ]
Ссылки
[ редактировать ]- ^ Перейти обратно: а б с д и ж г час я дж к л м н тот п д р с т в v В х и С аа аб и объявление но из «Суноси – солриамфетол таблетки, покрытые пленочной оболочкой» . ДейлиМед . 16 октября 2019 г. Проверено 24 ноября 2019 г.
- ^ «Краткая основа решения (SBD) для Суноси» . Здоровье Канады . 23 октября 2014 года . Проверено 29 мая 2022 г.
- ^ «Основные продукты для здоровья 2021 года: приложения к продуктам, одобренным в 2021 году» . Здоровье Канады . 3 августа 2022 г. Проверено 25 марта 2024 г.
- ^ Перейти обратно: а б с «Суноси ЭПАР» . Европейское агентство лекарственных средств (EMA) . 12 ноября 2019 года . Проверено 26 сентября 2020 г.
- ^ Перейти обратно: а б Пауэлл Дж., Пищатоски С., Гарланд С. (октябрь 2020 г.). «Солриамфетол от чрезмерной сонливости при нарколепсии и обструктивном апноэ во сне». Энн Фармакотер . 54 (10): 1016–1020. дои : 10.1177/1060028020915537 . ПМИД 32270686 . S2CID 215605290 .
- ^ Абад В.К., Гиймино С. (декабрь 2018 г.). «Солриамфетол для лечения дневной сонливости при обструктивном апноэ во сне». Эксперт преподобный Респир Мед . 12 (12): 1007–1019. дои : 10.1080/17476348.2018.1541742 . ПМИД 30365900 . S2CID 53106520 .
- ^ Перейти обратно: а б Гуршахани Х., Джолас Т., Мартин М., Котье С., Хьюз С., Макфадден В. и др. (2023). «Доклиническая фармакология солриамфетола: потенциальные механизмы стимулирования пробуждения». Спектры ЦНС . 28 (2): 222. дои : 10.1017/S1092852923001396 . ISSN 1092-8529 .
Функциональные исследования in vitro показали агонистическую активность солриамфетола в отношении рецепторов TAAR1 человека, мышей и крыс. Значения EC50 hTAAR1 (10–16 мкМ) находились в пределах клинически наблюдаемого диапазона терапевтических концентраций солриамфетола в плазме и перекрывались с наблюдаемой ингибирующей активностью солриамфетола в отношении DAT/NET in vitro. Агонистическая активность TAAR1 была уникальной для солриамфетола; ни модафинил WPA, ни ингибитор DAT/NET бупропион не обладали агонистической активностью TAAR1.
- ^ Перейти обратно: а б с Джи Ён С. (5 марта 2018 г.). «Препарат от нарколепсии от SK Biopharmaceuticals скоро выйдет на рынок США» . Корейский вестник .
- ^ Перейти обратно: а б с д и «Солриамфетол – Джаз Фармасьютикалс/СК Биофармацевтика» . АдисИнсайт . Проверено 13 октября 2023 г.
- ^ Питре Т., Мах Дж., Робертс С., Десаи К., Га Ю., Райан С. и др. (май 2023 г.). «Сравнительная эффективность и безопасность средств, способствующих бодрствованию, при чрезмерной дневной сонливости у пациентов с обструктивным апноэ во сне: систематический обзор и сетевой метаанализ». Энн, интерн, мед . 176 (5): 676–684. дои : 10.7326/M22-3473 . ПМИД 37155992 . S2CID 258558603 .
- ^ Перейти обратно: а б «Федеральный реестр::Запросить доступ» . 17 июня 2019 г.
- ^ Перейти обратно: а б Абад В.К., Гиймино С. (2017). «Новые разработки в лечении нарколепсии» . Природа и наука сна . 9 : 39–57. дои : 10.2147/NSS.S103467 . ПМЦ 5344488 . ПМИД 28424564 .
- ^ Салливан СС, Гиймино С (2015). «Новые лекарства от распространенных состояний сонливости: обструктивного апноэ во сне и нарколепсии». Мнение экспертов о новых лекарствах . 20 (4): 571–82. дои : 10.1517/14728214.2015.1115480 . ПМИД 26558298 . S2CID 7951307 .
- ^ Гард Д (14 января 2014 г.). «Джаз ставит до 397 миллионов долларов на препарат от нарколепсии от Aerial» . Жестокая биотехнология .
- ^ Перейти обратно: а б с «Снимки испытаний наркотиков: Суноси» . США Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) . 16 апреля 2019 года. Архивировано из оригинала 28 сентября 2019 года . Проверено 24 ноября 2019 г.
 В данную статью включен текст из этого источника, находящегося в свободном доступе .
В данную статью включен текст из этого источника, находящегося в свободном доступе .
- ^ «Пакет одобрения лекарств: Суноси» . США Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) . 29 апреля 2019 года . Проверено 24 ноября 2019 г.
 В данную статью включен текст из этого источника, находящегося в свободном доступе .
В данную статью включен текст из этого источника, находящегося в свободном доступе .
- ^ «Одобрение орфанного препарата Солриамфетол» . США Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) . Проверено 24 ноября 2019 г.
 В данную статью включен текст из этого источника, находящегося в свободном доступе .
В данную статью включен текст из этого источника, находящегося в свободном доступе .
- ^ «Неприятно покупать Суноси у джаза» . НАСДАК . Проверено 28 марта 2022 г.
- ^ 21 USC § 812 - Списки контролируемых веществ.
- ^ «Руководства – Руководство для практикующего врача – Раздел V» . Архивировано из оригинала 7 января 2014 года . Проверено 30 мая 2021 г. Проверено 7 января 2014 г.
- ^ Перейти обратно: а б Сурман CB, Уолш Д.М., Хорик Н., ДиСальво М., Фатер CH, Кауфман Д. (октябрь 2023 г.). «Солриамфетол при синдроме дефицита внимания и гиперактивности у взрослых: двойное слепое плацебо-контролируемое пилотное исследование». Дж. Клин Психиатрия . 84 (6). дои : 10.4088/JCP.23m14934 . ПМИД 37819836 . S2CID 263715808 .
- ^ Наги А., Эль-Шешайе А., Элсори Д.Х., Аламири Б. (апрель 2021 г.). «Солриамфетол при синдроме дефицита внимания и гиперактивности» . Спектр ЦНС . 27 (6): 662–663. дои : 10.1017/S1092852921000328 . ПМИД 33870884 .
- ^ «НИЗ начнет длительные клинические испытания COVID для изучения нарушений сна, непереносимости физических упражнений и недомогания после физической нагрузки» . Национальные институты здравоохранения (NIH) . 7 мая 2024 г. Проверено 2 августа 2024 г.