Никотиновый агонист
Никотиновый агонист - это препарат, который имитирует действие ацетилхолина (ACH) на никотиновых рецепторах ацетилхолина (nACHR). NACHR назван в честь его сродства к никотину.
Примеры включают никотин (по определению), ацетилхолин ( эндогенный агонист nachrs), холин , эпибатидин , лобелин , варенклин и цитизин . [ 1 ]
История
[ редактировать ]
Никотин был известен на протяжении веков за его опьяняющий эффект. Сначала он был изолирован в 1828 году от табачного завода немецкими химиками, Пообет и Рейманн. [ 2 ]
Открытие положительных эффектов от никотина на память животных было обнаружено в результате исследований in vivo в середине 1980 -х годов. Эти исследования привели к новой эре в исследованиях никотинового ацетилхолинового рецептора (NACHR) и их стимуляции, но до тех пор фокус был в основном на никотиновой зависимости. [ 3 ] [ 4 ] Развитие агонистов NACHR началось в начале 1990 -х годов после открытия положительных последствий никотина. Некоторые исследования показали возможный вариант терапии в доклинических исследованиях. ABT-418 был одним из первых в серии агонистов NACHR, и он был разработан Abbott Labs . [ 4 ] ABT-418 показал значительное увеличение задержки сопоставления с выборкой (DMTS) в зрелых обезьянах макак разных видов и пола. [ 5 ] ABT-418 также рассматривался как возможное лечение болезни Альцгеймера, болезни Паркинсона и расстройства гиперактивности с дефицитом внимания: эти эксперименты показали положительные результаты. [ 4 ]
Одним из первых активных соединений NACHR, помимо никотина, которое продавалось в виде лекарственного средства, был галантамин растения , алкалоид , который работает в качестве слабого ингибитора холинэстеразы (IC50 = 5 мкМ), а также аллостерический сенсибилизатор для NACHR (EC50 = 50 нм) Полем [ 6 ]
Никотиновые ацетилхолиновые рецепторы и их сигнальная система
[ редактировать ]
Система сигнализации
[ редактировать ]В человеческой нервной системе никотиновые холинергические сигналы расширяются по всей системе, где ацетилхолин нейротрансмиттер (ACH) играет ключевую роль в активации лигандных ионных каналов . [ 7 ] Холинергическая система представляет собой жизненно важный нервный путь, где холинергические нейроны синтезируют, хранят и высвобождают нейротрансмиттер ACH. Основными рецепторами, которые преобразуют сообщения ACH, являются холинергические мускариновые ацетилхолиновые рецепторы , нейрональные и мышечные нахры. Оглядываясь назад на эволюционную историю, ACH считается самой старой молекулой передатчика и стал присутствовать перед нервной клеткой. В нервной системе холинергическая стимуляция, опосредованная через пути, контролирует такие пути, как высвобождение передатчиков и чувствительность к клеткам, которые могут влиять на физиологическую активность, включая сон, тревогу, обработку боли и когнитивные функции. [ 8 ]
Никотиновые ацетилхолиновые рецепторы
[ редактировать ]Нахры представляют собой холинергические рецепторы, обнаруженные в центральной нервной системе (ЦНС), периферических нервных системах (PNS) и скелетных мышцах, эти рецепторы представляют собой лиганд-управляемые ионные каналы с сайтами связывания для ацетилхолина и других молекул. Когда ACH или другие агонисты связываются с рецепторами, он стабилизирует открытое состояние ионного канала, позволяя притока катионов, таких как калий, кальций и ионы натрия. NachR состоит из разных субъединиц, которые определяют четвертичную структуру рецептора, эти субъединицы являются α -субъединицами (α1 -α10), β -субъединиц (β1 -4), одна субъединица, одна субъединица γ и одна субъединица. nachrs могут быть либо гетеромерными , либо гомомерными . Гетеромерные рецепторы, обнаруженные в центральной нервной системе, состоят из двух α -субъединиц и трех β -субъединиц с сайтом связывания на границе α и соседней субъединицы. Эти рецепторы содержат два сайта связывания на рецептор и имеют разное сродство к химическим веществам на основе состава субъединиц. Оба сайта связывания работают вместе, и, следовательно, оба сайта должны быть заняты агонистом NACHR, чтобы иметь место активацию канала. [ 9 ] Было показано, что NACHR, содержащие субъединицы α2 -α6 и β2 -β4, имеют более высокую аффинность к ACH, чем другие рецепторы. Гомомерные рецепторы содержат 5 идентичных субъединиц, они имеют 5 сайтов связывания, расположенных на границе раздела между двумя соседними субъединицами. В 2000 году у людей были идентифицированы два гомомерных рецептора, рецепторы α7 и α8. [ 8 ] [ 10 ] [ 11 ] [ 12 ]
Связующий сайт
[ редактировать ]На гетеромерных nachrs есть два сайта связывания; Чтобы стабилизировать открытую форму nACHR, оба сайта связывания должны быть заняты агонистом, такими как никотин или ACH. [ 11 ]
Сайт связывания ACH NACHR состоит из шести петлей, называемых A - F. Петли A, B и C сайта связывания являются частью α -субъединицы и являются основными компонентами сайта связывания. Смежная субъединица к α -субъединице (γ, Δ, ε или β) содержит петли D, E и F. [ 11 ]
Механизм действия
[ редактировать ]
Агонисты рецепторов α4β2
[ редактировать ]α4β2 NACHR содержат две субъединицы α4 и три субъединицы β2, поэтому они имеют два сайта связывания для ACH и других агонистов . α4β2 nachrs составляют приблизительно 90% NACHR в человеческом мозге, и когда хронически подвергается воздействию никотина или других никотиновых агонистов, приводит к увеличению плотности рецепторов α4β2, что противоположна тому, что обычно происходит, когда другие рецепторы подвергаются хронически подверженности их агонистам. Рецептор α4β2 широко изучался в отношении болезни Альцгеймера, а также для никотиновой зависимости, а в 2009 году на рынке представлены несколько препаратов, которые специально предназначены для α4β2 -nACHR. [ 13 ] [ 14 ]
α7 рецепторных агонистов
[ редактировать ]Рецепторы α7 представляют собой гомомерные нейрональные ацетилхолиновые рецепторы, состоящие из пяти субъединиц α7 и имеют пять сайтов связывания ACH. Сообщалось, что аномалия в экспрессии рецепторов α7 влияет на прогрессирование таких заболеваний, как болезнь Альцгеймера и шизофрения . Считается, что α7 не имеет такого же сродства к никотину, как и гетеромерный рецептор, но вместо этого они показали больше сродства к альфа -бунгаротоксину , который является никотиновым антагонистом, обнаруженным в яде некоторых змей. Считается, что нацеливание на α7 -рецепторы полезно при лечении болезни Альцгеймера и шизофрении. [ 9 ] [ 15 ]
Агонисты рецепторов мышц
[ редактировать ]NACHR обнаружены в нервно -мышечном соединении на скелетных мышцах. Были обнаружены два разных рецептора, один из которых был в основном обнаружен у взрослых, содержит две субъединицы α1, одну β1, один ε и один Δ, другая была обнаружена у плодов и содержит γ -субъединицу вместо ε -субъединицы. NACHR принимают участие в деполяризации мышечной конечной пластины за счет увеличения катионной проницаемости, приводящей к сокращению скелетных мышц. [ 16 ] NACHR, обнаруженные в системе скелетных мышц, имеют два сайта связывания ACH, один из которых обнаруживается на границе между α1 и δ -субъединицами, в то время как другой находится на границе раздела между α1 и γ или ε -субъединицами. Среди антагонистов NACHR, разработанных специально для нервно -мышечной системы, являются нервные газы и другие яды, предназначенные для быстрого убийства людей или других животных и насекомых. [ 12 ]
Связывание
[ редактировать ]ACH связывается с NACHR из -за разницы заряда между молекулой и поверхностью рецептора. При связывании с NACHR ACH вписывается в связывающий карман, вформированную петлями A, B и C, которые принадлежат к α -субъединице и прилегающей субъединице. Когда ACH вписывается в связывающий карман, петли NACHR подвергаются движению, которое приводит к координации молекулы ACH в кармане, усиливая химические связи между молекулой и рецептором. После перемещения петель, которые принадлежат к α -субъединице, иногда можно образует связь, например, соляный мост, к соседней субъединице, усиливающей связи между рецептором и ACh еще дальше. [ 17 ]
Дизайн наркотиков
[ редактировать ]Препараты, которые влияют на NACHR, могут быть агонистами, частичными агонистами или антагонистами . [ 1 ] Агонисты, например, никотин, могут действовать как деполяризующие агенты при столкновении с NACHR в течение некоторого времени (секунды или минуты, в зависимости от концентрации и подтипа NACHR), хроническое воздействие агониста также может привести к длительной функциональной дезактивации из -за быстрого и постоянной десенсибилизации. Частичные агонисты NACHR изучались, так как они, кажется, полезны в прекращении курения. Считается, что частичные агонисты связываются с NACHR и стимулируют высвобождение дофамина в меньших частях, чем агонисты, и, следовательно, компенсируют отсутствие никотина. [ 18 ]
Отсутствие специфичности среди некоторых никотиновых агонистов хорошо известно и является потенциальной проблемой при использовании их для лечения заболеваний, которые требуют нацеливания на конкретный подтип NACHR. Среди этих неспецифических агонистов -, например, ACH, никотин и эпибатидин, которые нацелены на более чем один подтип NACHR. [ 19 ] [ 20 ]
Фармакофор
[ редактировать ]
Развитие агонистского фармакофора NACHR началось в 1970 году, когда было предложено, чтобы связывание агонистов с рецептором зависело от положительно заряженного атома азота и водородной связи, образующейся от атома карбонильного кислорода в ацетилхолевом или атоме низота в (с)- в (с)- в (с)- в (с)- в (с)- в (с)- в никотин. С тех пор было показано, что катионный центр, атомы, которые являются электроотрицательными и способны образовывать водородные связи вместе с центром пиридинового кольца в (ы) -никотин, благоприятны. Стереохимия является частью фармакофора, как ясно видно из (s)- и (r)- никотина, где (S)- энантиомер в 10-100 раз более сильнее. Азабициклическое кольцо эпибатидина является еще одним примером благоприятных стерических взаимодействий с рецепторами. Было высказано предположение, что специфическая дистанция междоподобия n + -Н, важно для агонистского сродства, но дебаты возникли в связи с его влиянием. Более новая теория состоит в том, что расстояние 7-8 Å между точками, которые дополняют протонированный атом азота и акцептор водородной связи, усилит активность. Низкая электронная плотность, близкая к протонированному азоту, и более высокая электронная плотность, близкая к пиридиновому кольцу, предпочитается в протонированных никотиновых лигандах , содержащих пиридиновое кольцо. В последующие годы исследователи проявили больший интерес к рецепторам подтипа α7 и α4β2 в разработке лекарств для лечения никотиновой зависимости и когнитивных нарушений, таких как Альцгеймер. [ 21 ]
Структурные отношения отношений
[ редактировать ]Структурные отношения: мышечные агонисты nachr
[ редактировать ]Различные модели были выполнены, где сродство агонистов NACHR к подтипе рецептора протестирована, чтобы помочь идентифицировать молекулы, группы и стерическую конформацию, которые жизненно важны для большей аффинности. Используя подтип подтипа мышечного рецептора NACHR (α1) 2 β1Δγ Модель. Были получены следующие результаты:
- Анатоксин > эпибатидин > ацетилхолин > dmpp >> цитизин > пирантел > никотин > coniine > tubocurare > lobeline ,
где анатоксин обладал самой высокой эффективностью активности, а Tubocurare - самая низкая. Ацетилхолин, с другой стороны, вызвал гораздо более длительное время открытия рецептора, хотя анатоксин более мощный. Результаты показывают, что производные анатоксина будут полезны для понимания взаимосвязей структур-активности (SAR) для мышечных нахров. [ 22 ]
Хлорид сукцинилхолина , который является препаратом, который уже находится на рынке, представляет собой эфир бишолина и короткий релаксант мышц. Бишлиновые сложные эфиры - это соединения, которые могут выступать в качестве конкурентного агониста на мышечных типах и использовались в исследованиях SAR. В модели Torpedo (α1) 2 β1Δγ nACHR было продемонстрировано, что активность агонистов эфира бисшолина зависит от длины цепи, поскольку потенция увеличивается с более длинными цепями. Эффективность, по -видимому, не зависит от длины цепи, так как самая высокая эффективность наблюдается в бишолиновых сложных эфирах с четырьмя -семью CH
2 единицы и ниже для обоих меньше СН
2 единицы и многое другое. [ 23 ]
Структурные отношения: α4β2 агонисты nachr
[ редактировать ]
Комбинация структурных элементов ACH и никотина, а также снижение конформационной гибкости с помощью циклопропанового кольца привела к обнаружению мощных и селективных лигандов α4β2 NACHR. Модуляция трех структурных элементов, линкера, замена аминогрузки и пиридинового кольца может использоваться для определения влияния на эффективность и селективность лигандов. Факторами, которые уменьшают связывание, являются стерические препятствия для аминогруппы и линкеров, которые являются насыщенными/ненасыщенными углеродными цепями. Эфирные линкеры с короткими целями являются предпочтительными. Полезное влияние на связывание наблюдается с заменой на пиридиновое кольцо как моно-, так и дисквизиции с галогенами среди других групп. Замена аминогрузки тремя различными амидами увеличивала аффинность связывания, где метиламид имел самое высокое связывание. Более низкое связывание в других замещенных амидах было объяснено стерическим препятствием или отсутствием метильной группы, что приводит к потере гидрофобного взаимодействия. Стереохимия пиридинового азота и/или пиридинового кольца и его стереоэлектронное действие оказывают тонкое полезное влияние на связывание с α4β2 nachr. Таким образом, было показано, что пиридиловый эфирный лиганд с заменой бромо на пиридин и металитэмид на аминогруппе имел самую высокую активность. [ 24 ]
Структурные отношения: агонисты α7 nachr
[ редактировать ]

Поиск селективных и мощных агонистов α7 NACHR выдвинул серию соединений, которые имеют хороший потенциал в качестве кандидатов на наркотики. Один из таких поисков произвел SEN12333 /Way-317538 среди других соединений, которые имеют желательные фармакокинетические профили и являются избирательными для α7 nachrs по сравнению с α1, α3 и α4β2 nachrs. Структурные отношения активности для этих соединений были предложены. [ 15 ] Оптимальный фармакофор агониста α7 nachr изготовлен из трех частей. Существует базовая часть, связанная с углеродной цепью, связанной с ароматическим фрагментом амидным мостом. Амидный мост может быть перевернут, не влияя на потенцию агониста. Би -арильная группа показывает большую активность, чем монорильская группа, поскольку ароматический фон и замещение в позиции 2 в более поздней арильной группе еще больше увеличит потенцию. Потенция выше для агонистов с H + донор/акцептор в более поздней арильной группе в группе Biaryl. Большое количество акцепторов водородных связей может снизить проницаемость в рамках барьеры крови -брейна (BBB) из -за площади полярной поверхности, и их необходимо учитывать при разработке агонистов для нацеливания α7 nachrs. [ 15 ]
Различные циклические аминовые группы могут действовать, поскольку основной фрагмент и потенция остаются относительно неизменными, например, арилапепипеперазин , пиперидин и морфолин . Ациклический третичный амин терпит как основной фрагмент, но более крупные стерические группы менее переносятся. [ 15 ]
Известно, что многие производные хинуклидина, такие как амид хинуклидов, являются агонистами α7 nACHR. В исследованиях SAR для амида хинуклидина были выявлены факторы, которые влияют на потенцию и сродство этих агонистов. Замена PARA на киинуклидиновое кольцо и конфигурацию 3- (R) в стереохимии предпочитается. Усиленная активность наблюдается, когда 5 -членное кольцо сливается с ароматическим фрагментом. Дальнейшее улучшение наблюдается, когда плавное кольцо способно поставлять электронный резонанс в амид -карбонил, тогда как активность будет уменьшаться, когда слитое кольцо содержит атом для водородной связи. Жесткость хинуклидина и ортогональная ориентация азотного моста в отношениях с амидной карбонильной группой считаются важными для оптимального связывания. Стабильность некоторых из более сильных производных амидов хинуклидов в моделях крыс in vitro была низкой, однако добавив метильную группу в позицию 2 на кхилуклидиновое кольцо, стабильность значительно увеличилась. [ 25 ]
Разработка лекарств
[ редактировать ]Развитие никотиновых агонистов рецепторов ацетилхолинового рецептора началось в начале 1990 -х годов после открытия положительного эффекта никотина на память животных. [ 3 ] [ 4 ] Развитие никотиновых агонистов рецепторов ацетилхолинового рецептора с тех пор прошло долгий путь. Агонисты никотинового ацетилхолинового рецептора получают все большее внимание, как кандидаты на лекарства при многочисленных расстройствах центральной нервной системы, таких как болезнь Альцгеймера , шизофрения , расстройство гиперактивности с дефицитом внимания (СДВГ) и никотиновая зависимость . [ 26 ] [ 27 ] Никотиновые ацетилхолиновые рецепторы представляют собой рецепторы, обнаруженные в центральной нервной системе , периферические нервные системы и скелетные мышцы. Это ионные каналы, управляемые лигандом, с сайтами связывания для ацетилхолина , а также других агонистов . Когда агонисты связываются с рецептором , он стабилизирует открытое состояние ионного канала, позволяя притока катионов . [ 9 ]
В 2009 году на рынке было по меньшей мере пять препаратов, которые влияют на никотиновые рецепторы ацетилхолина.
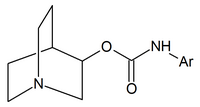
|

|
|
| Хинуклидин карбаматы | Квинуклидиновые амиды | Хинуклидовые эфиры |
Продукты никотинового агониста
[ редактировать ]| Активный ингредиент | Название продукта | Химическое название | Фармацевтическая форма | Фармакодинамические свойства | Терапевтическое использование | Структура |
|---|---|---|---|---|---|---|
| Варенклинарная тартрат | Чампикс, Chantix | 7,8,9,10-тетрагидро-6,10-метано-6H-пиразино [2,3-H] [3] бензазепин [ 27 ] | Пленка с покрытием планшет | Частичный агонист никотинового ацетилхолинового рецептора, подтип α 4 β 2 [ 28 ] | Лечение табачной зависимости [ 28 ] | 
|
| Галантамин Гидробромид | Реминил, Нивалин, Разадин и Разадин - это | 4A, 5,9,10,11,12-гексагидро-3-метокси-11-метил-6H-бензофуро [3A, 3,2-EF] [2] -Benzazepin-6-OL [ 29 ] | Постоянный выброс капсула, планшет с пленкой, пероральный раствор | Ингибитор холинэстеразы и неконкурентный агонист никотинового ацетилхолинового рецептора [ 4 ] | Лечение деменции, вызванное болезнью Альцгеймера [ 30 ] | 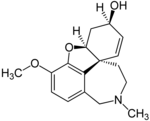
|
| Никотин | Никоретт , Никотинелл, Никейтин, Сапоги Никассист, Коммит, привычка, Никодерма Ск, Никотрол, Трапель | 3-[(2S) -1-метилпирролидин-2-ил] пиридин | Трансдермальный пластырь, жвачка, ингалятор, носовой спрей, Lozenge, Microtab и естественным образом найдены в табаке | Агонист никотинового рецептора, [ 31 ] как тип ганглия, так и α 4 β 2 [ 32 ] | Лечение табачной зависимости [ 33 ] | 
|
| Карбахол | Мио | 2-[(аминокарбонил) Oxy] -n, N, N-триметилатанаминия | Внутриглазной раствор | Холинергический агонист [ 34 ] | Лечение глаукомы | 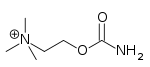
|
| Хлорид суксаметония (хлорид сукцинилхолина) | Анемин, келицин -суксаметоний хлорид | 2,2 '-[(1,4-диоксобутан-1,4-дийл) до (oxy)] к (n, n, n-trimethyllethanamiminium) | Внутривенная или внутримышечная инъекция | Деполяризация нервно -мышечного блокирующего агента [ 35 ] | Короткий актерский релаксант [ 36 ] | |
| Эпибатидин | Не перечислен | 2- (6-хлорпиридин-3-ил) -7-азабицикло [2.2.1] Гептан | Не перечислен | Агонист никотинового ацетилхолинового рецептора [ 37 ] | Не используется в качестве препарата | 
|
Другие никотиновые агонисты, хотя обычно с ограниченным клиническим использованием, включают:
- Lobeline , агонист никотиновых рецепторов типа ганглия , а также поражает чувственные нервные терминалы [ 32 ]
- Эпибатидин , агонист на ганглионе , α4β2 и α7 -рецепторы [ 32 ]
- Decamethonium вызывает блок деполяризации на мышечных рецепторах, аналогично Suxamethonium [ 32 ]
Никотиновая и мускариновая активность
[ редактировать ]| Сравнение холинергических агонистов [ 38 ] | ||||
|---|---|---|---|---|
| Вещество | Рецепторная специфичность | Гидролиз по ацетилхолинэстераза |
Комментарии | |
| Мускариновый | Никотиновый | |||
| Холин | +++ | +++ | ++ | Основное питательное вещество |
| Ацетилхолин | +++ | +++ | +++ | Эндогенный лиганд |
| Карбахол | ++ | +++ | - | Используется при лечении глаукомы |
| Метахолин | +++ | + | ++ | |
| Бетанехол | +++ | - | - | Используется в мочевом пузыре и желудочно -кишечная гипотония. |
| Мускарин | +++ | - | - | Натуральный алкалоид, найденный в определенных грибах. Причина грибного отравления |
| Никотин | - | +++ | - | Природная алкалоид, найденный на табачном растении . |
| Пилокарпин | ++ | - | - | Используется в глаукоме |
| Оксоцреморин | ++ | - | - | |
Текущий статус
[ редактировать ]В настоящее время исследования агонистов и проектирования лекарств на никотиновом рецепторе предназначены для лечения множественных заболеваний и расстройств ЦНС. [ 39 ]
Targacept имеет трех кандидатов на лекарства, которые находятся в клинических испытаниях ; AZD3480 (TC-1734) для СДВГ, который в настоящее время находится в клинических испытаниях II фазы, AZD1446 (TC-6683) для болезни Альцгеймера в сотрудничестве с Astrazeneca и TC-5619 для когнитивных дисфункций в шизофрении.
Фармацевтические препараты памяти с его партнером Roche имеет один кандидат на лекарство, MEM 3454 (RG3487), частичный агонист никотинового рецептора α7 , при болезни Альцгеймера. [ 40 ] [ 41 ]
Abbott Laboratories в партнерстве с Neurosearch имеет двух кандидатов в лекарственные средства в клинических испытаниях, ABT-894 , селективный агонист никотинового рецептора α4β2 для ABD и ABT-560 , модулятор нейронального никотинового рецептора, который был выбран Абботтом в 2006 году в качестве нового кандидата в разработку, который был выбран Абботтом в 2006 году в качестве нового кандидата в разработку, который был выбран Абботтом в 2006 году в качестве нового кандидата в разработку, который был выбран Эбботтом в 2006 году в качестве нового кандидата в разработку. Для когнитивных дисфункций. [ 42 ]
Envivo Pharmaceuticals имеет один кандидат на препарат в клинических испытаниях, EVP-6124, селективный агонист никотинового рецептора α7 для болезни Альцгеймера и шизофрения и одно последующее соединение, EVP-4473, который успешно завершил доклиническое развитие . [ 43 ]
Смотрите также
[ редактировать ]- Мускариновый ацетилхолиновый рецептор
- Мускариновый агонист
- Мускариновый антагонист
- Никотиновый ацетилхолиновый рецептор
- Никотиновый антагонист
- Парасимпатомиметический препарат
Ссылки
[ редактировать ]- ^ Jump up to: а беременный Матера, Карло; Папотто, Клаудио; Dallanoce, Clelia; Де Амичи, Марко (август 2023 г.). «Достижения в селективных лигандах малых молекул для гетеромерных никотиновых рецепторов ацетилхолина» . Фармакологические исследования . 194 : 106813. DOI : 10.1016/j.phrs.2023.106813 . HDL : 2434/978688 .
- ^ Хеннингфилд, Джек Э; Zeller, Mitch (2006), «Никотиновая психофармакологическая исследовательская вклад в Соединенные Штаты и глобальное регулирование табака: оглядываться назад и с нетерпением», Psychopharmacology , 184 (3–4): 286–291, doi : 10.1007/s00213-006- 0308-4 , PMID 16463054 , S2CID 38290573
- ^ Jump up to: а беременный Haroutunian, Vahram; Барнс, Эдвард; Дэвис, К.Л. (1985), «Холинерги -модуляция памяти у крыс», Psychopharmacology , 87 (3): 266–271, doi : 10.1007/bf00432705 , pmid 3001803 , s2cid 20040918
- ^ Jump up to: а беременный в дюймовый и Buccafusco, JJ (2004), «Подтипы нейрональных никотиновых рецепторов: определение терапевтических мишеней» (PDF) , молекулярные вмешательства , 4 (5): 285–295, doi : 10.1124/mi.4.5.8 , PMID 15471911
- ^ Buccafusco, JJ; Джексон, WJ; Терри -младший, ав; Marsh, KC; Декер, MW; Arneric, SP (1995), «Улучшение производительности задержки задачи сопоставления с образцом от обезьян после ABT-418: новый активатор холинергического канала для улучшения памяти», Psychopharmacology , 120 (3): 256–266, doi : 10.1007/bf02311172 , pmid 8524972 , s2cid 23215696
- ^ Ludwig, J.; Höffle-Maas, A. (2010), «Локализация с помощью сайт-направленного мутагенеза сайта связывания галантамин на внеклеточном домене α 7 никотинового ацетилхолинового рецептора», Journal of Reptors и сигнальной трансдукции , 30 (6): 469–483, doi : 10.3109/107999893.2010.505239 , PMID 21062106 , S2CID 9160835
- ^ Лю, Чжаопинг; Чжан, J; Берг, Дарвин К. (2007), «Роль эндогенной никотиновой передачи сигналов в руководящем развитии нейронов», Биохимическая фармакология , 74 (8): 1112–1119, doi : 10.1016/j.bcp.2007.05.022 , PMC 2116993 , PMID 17603025555
- ^ Jump up to: а беременный Готти, С.; Клементи, Ф. (2004), «Нейрональные никотиновые рецепторы: от структуры к патологии», Прогресс в нейробиологии , 74 (6): 363–396, doi : 10.1016/j.pneurobio.2004.09.006 , PMID 15649582 , S2CID 24093369
- ^ Jump up to: а беременный в Патерсон, Дэвид; Nordberg, Agneta (2000), «Нейрональные никотиновые рецепторы в человеческом мозге», Прогресс в нейробиологии , 61 (1): 75–111, doi : 10.1016/s0301-0082 (99) 00045-3 , PMID 10759066 , S2CID 27207955555-3, PMID 10759066 , S2CID 2720795555 .
- ^ Сала, Ф.; Nistri, A.; Criado, M. (2008), «Никотиновые ацетилхолиновые рецепторы хромаффиновых клеток надпочечников» , Acta Physiologica , 192 (2): 203–212, doi : 10.1111/j.1748-1716.2007.01804.x , PMID 18005395 , S2CID 29310750. [ мертвая ссылка ]
- ^ Jump up to: а беременный в Itier, Valérie; Бертран, Даниэль (2001), «Нейрональные никотиновые рецепторы: от структуры белка к функционированию», «Письма FEBS» , 504 (3): 118–125, doi : 10.1016/s0014-5793 (01) 02702-8 , PMID 11532443
- ^ Jump up to: а беременный Lindstrom, JM (2003), «Никотиновые ацетилхолиновые рецепторы мышц и нервов» , Анналы нью -йоркской Академии наук , 998 : 41–52, doi : 10.1196/annals.1254.007 , PMID 14592862 , S2CID 84583356667, PMID 14592862, S2CID 8458335666, PMID 14592862, S2CID 8458335666, PMID 14592862, S2CID 8458335666, PMID 14592862, S2CID 8458335666, PMID 14592862 , S2CID 8458335666 , PMID 14592862, S2CID 8458335666. [ мертвая ссылка ]
- ^ Михайлеску, Стефан; Drucker-Colín, René (2000), «Никотин, никотиновые рецепторы мозга и нейропсихиатрические расстройства», Archives of Medical Research , 31 (2): 131–144, doi : 10.1016/s0188-4409 (99) 00087-9, PMID/S0188-4409 (99) 00087-9 , PMID. 10880717
- ^ Arias, Hugo R. (1997), «Топология сайтов связывания лиганда на никотиновом ацетилхолиновом рецепторе», обзоры исследования мозга , 25 (2): 133–191, doi : 10.1016/s0165-0173 (97) 00020-9 , PMID /S0165-0173 9403137 , S2CID 26453010
- ^ Jump up to: а беременный в дюймовый Хайдар, Саймон Н.; Гирон, Чиара; Беттинетти, Лора; Оба, Хеддрик; Couner, Thomas A.; Данлоп, Джон; Ла Роза, Сальваторе; Микко, Иоланда; Pollastrini, Мартина; Куинн, Джоанна; Ронкарати, Ренза; Скали, Карла; Валакчи, Микела; Варроне, Маурицио; Zaaletti, Riccardo (2009), «SAR и биологическая оценка SEN12333/Way-317538: новая альфа 7 никотиновых агониста рецептора ацетилхолинового рецептора», Bioorganic & Medicinal Chemistry , 17 (14): 5247–5258, Doi : 10.1016/j.bmc. 2009.05.040 , PMID 19515567
- ^ Брунтон, Лоуренс Л.; Лазо, Джон С.; Паркер, Кит Л., ред. (2006), Фармакологическая основа терапии Гудмана и Гилмана (11 изд.), McGraw Hill, ISBN 978-0-07-142280-2
- ^ Unwin, Nigel (2004), «Уточненная структура никотинового рецептора ацетилхолина при разрешении 4 A °», Journal of Molecular Biology , 346 (4): 967–989, doi : 10.1016/j.jmb.2004.12.031 , pMID 15701510
- ^ Касселс, Брюс К.; Бермудес, Изабель; Даджас, Федерико; Abin-Carriquiry, J. Andrés; Воннакотт, Сьюзен (2005), «От дизайна лиганда до терапевтической эффективности: задача для исследования никотиновых рецепторов», Discovery Today , 10 (23–24): 1657–1665, doi : 10.1016/s1359-6446 (05) 0365- 2 , HDL : 10533/176659 , PMID 16376826
- ^ Матера, Карло; Папотто, Клаудио; Dallanoce, Clelia; Де Амичи, Марко (август 2023 г.). «Достижения в селективных лигандах малых молекул для гетеромерных никотиновых рецепторов ацетилхолина» . Фармакологические исследования . 194 : 106813. DOI : 10.1016/j.phrs.2023.106813 . HDL : 2434/978688 .
- ^ Готти, С.; Fornasari, D.; Clementi, F. (1997), «Рецепторы никотинка для нейронов человека», Прогресс в нейробиологии , 53 (2): 199–237, doi : 10.1016/s0301-0082 (97) 00034-8 , PMID 9364611 , S2CID 10421687 .
- ^ Tøndera, Janne E.; Olesena, Preben H.; Хансена, Джон Бондо; Begtrupb, Mikael; Petterssona, Ingrid (2001), «Улучшенный никотиновый фармакофор и стереоселективная комфа-модель для никотиновых агонистов, действующих на центральные никотиновые ацетилхолиновые рецепторы, помеченные [3H] -N-метилкарбамилхолином», журнал компьютерного молекулярного дизайна , 15 (3 (3 (3 (3 (3 (3 ( 3 (3 (3 (3 (3 (3 (3 (3 (3 (3 (3 (3 (3 (3 (3 (3 (3 ): 247–258, bibcode : 2001jcamd..15..247t , doi : 10.1023/a: 1008140021426 , PMID 11289078 , S2CID 80361
- ^ Купер, Джулия С.; Гутброд, Оливер; Витцеманн, Вейт; Methfessel, Christoph (1996), «Фармакология никотинового ацетилхолинового рецептора из мышц крысы плода, экспрессируемых в ооцитах ксенопуса», Европейский журнал фармакологии , 309 (3): 287–298, doi : 10.1016/0014-299 (96) 00298- 4 , PMID 8874153
- ^ Картер, Крис RJ; Цао, Лирен; Каваи, Хидеки; Смит, Питер А.; Драйден, Уильям Ф.; Raftery, Michael A.; Данн, Сьюзен М.Дж. (2007), «Зависимость от длины цепи взаимодействия бисватернарных лигандов с рецептором никотинового ацетилхолина торпедо», биохимическая фармакология , 73 (3): 417–426, doi : 10.1016/j.bcp.2006.10.011 . PMID 17118342
- ^ Чартон, Ив; Гильноно, Клод.; Локхарт, Брайан; Лестажб, Пьер; Goldsteina, Solo (2008), «Профиль подготовки и сродства новых никотиновых лигандов», Биоорганические и лекарственные химические письма , 18 (6): 2188–2193, doi : 10.1016/j.bmcl.2007.12.075 , PMID 18262785
- ^ Уокер, Даниэль П.; Wishka, Donn G.; Пиотровский, Дэвид В.; Цзя, Шаоджуан; Рейтц, Стивен С.; Йейтс, Карен М.; Майерс, Джейсон К.; Vetman, Tatiana N.; Марголис, Брэндон Дж.; Якобсен, Э. Джон; Акер, Брэд А.; Гроппи, Винсент Э.; Вулф, Марк Л.; Торнбург, Брюс А.; Tinholt, Paula M.; Кортес-Бургос, Луз А.; Уолтерс, Родни Р.; Хестер, Мэтью Р.; Seest, Eric P.; Долак, Лестер А.; Хан, Фузен; Олсон, Барбара А.; Фицджеральд, Лора; Staton, Brian A.; Рауб, Томас Дж.; Хаджос, Михали; Хоффманн, Уильям Э.; Ли, Кай С.; Хигдон, Николь Р.; и др. (2006), «Проектирование, синтез, структура -активность и активность in vivo азабициклических ариламидов как агонисты ацетилхолинового рецептора A7, биоорганическая и лекарственная химия , 14 (24): 8219–8248, doi : 10.1016/j. BMC.2006.09.019 , PMID 17011782
- ^ http: //www.envivopharma.com-Никотиновый альфа7-ацетилхолиновый рецептор-агонистская программа агониста архив 2010-01-07 на машине Wayback
- ^ Jump up to: а беременный Rollema, H.; Камеры, LK; Coe, JW; Glowa, J.; Херст, РС; Лебель, Ла; Lu, y.; Мансбах, рупий; Мазер, RJ; Rovetti, CC; Пески, SB; Schaeffer, E.; Шульц, DW; Tangley III, FD; Williams, KE (2007), «Фармакологический профиль α 4 β 2 никотинового ацетилхолинового рецептора частичного агонистского варениклина, эффективная помощь в прекращении курения», Neuropharmacology , 52 (3): 985–994, doi : 10.1016/j.neuropharm.2006.10. .016 , PMID 17157884 , S2CID 53267460
- ^ Jump up to: а беременный «Champix 0,5 мг таблетки с покрытием пленки; таблетки Phampix 1 мг, покрытые пленкой - резюме характеристик продукта (SMPC) - (EMC)» . emc.medicines.org.uk . Архивировано из оригинала 2012-12-24.
- ^ Greenblatt, HM; Kryger, G.; Льюис, Т.; Силман, я; Sussman, JL (1999), «Структура ацетилхолинэстеразы, комплексной с (-)-галанхамином при 2,3 разрешении Angstrom», FEBS Letters , 463 (3): 321–326, DOI : 10.1016/S0014-5793 (99) 01637-3 , PMID 10606746
- ^ «Реминил XL 8 мг, 16 мг и 24 мг длительных капсул высвобождения - сводка характеристик продукта (SMPC) - (EMC)» . emc.medicines.org.uk . Архивировано из оригинала 2012-12-24.
- ^ Дани, Джон А.; Biasi, Mariella DE (2001), «Клеточные механизмы никотиновой зависимости», Фармакологическая биохимия и поведение , 70 (4): 439–446, doi : 10.1016/S0091-3057 (01) 00652-9 , PMID 11796143 12960054, PMID 11796143 , , S2CID S2CID 129600544, PMID 11796143, S2CID 12960054
- ^ Jump up to: а беременный в дюймовый Rang, HP (2003), Фармакология , Эдинбург: Черчилль Ливингстон, ISBN 978-0-443-07145-4 Страница 149
- ^ XI, Zheng-xiong; Спиллер, Криста; Гарднер, Элиот Л. (2009), «Разработка лекарств на основе механизмов для лечения никотиновой зависимости», Acta Pharmacol Sin , 30 (6): 723–739, doi : 10.1038/aps.2009.46 , PMC 3713229 , PMID 19434058 , ProQuest 213027402
- ^ http://www.accessdata.fda.gov/drugsatfda_docs/label/2004/16968s022lbl.pdf [ только URL PDF ]
- ^ Туба, Золтан; Махо, Сандор; Vizi, E. Sylvester (2002), «Синтез и структурная активность и взаимосвязи нейромошечных блокирующих агентов», Current Medicinal Chemistry , 9 (16): 1507–1536, doi : 10.2174/092986702369466 , PMID 12171561 , ProQuest 215095660
- ^ «Инъекция аневтина - сводка характеристик продукта (SMPC) - (EMC)» . emc.medicines.org.uk . Архивировано из оригинала 2012-12-24.
- ^ Кэрролл, Ф. Айви (2004), «Структурные взаимоотношения структурной активности эпибатидина», Биоорганические и лекарственные химические письма , 14 (8): 1889–1896, doi : 10.1016/j.bmcl.2004.02.007 , PMID 15050621
- ^ Если не указано в коробках, то ссылка: Таблица 10-3 в: Цветок жезла; Хамфри П. Рэнг; Морин М. Дейл; Риттер, Джеймс М. (2007), Фармакология Rang & Dale , Эдинбург: Черчилль Ливингстон, ISBN 978-0-443-06911-6
- ^ Матера, Карло; Папотто, Клаудио; Dallanoce, Clelia; Де Амичи, Марко (август 2023 г.). «Достижения в селективных лигандах малых молекул для гетеромерных никотиновых рецепторов ацетилхолина» . Фармакологические исследования . 194 : 106813. DOI : 10.1016/j.phrs.2023.106813 . HDL : 2434/978688 .
- ^ «Рош - трубопровод фармацевтического препарата» . Архивировано из оригинала на 2009-12-25 . Получено 2009-12-21 .
- ^ «Фармацевтические препараты памяти достигают цели регистрации для фазы 2 исследования MEM 3454 в когнитивных нарушениях, связанных с шизофренией» .
- ^ «Разработка наркотиков» . Архивировано с оригинала 2006-10-03 . Получено 2009-12-21 .
- ^ «Программы - Envivo» . Архивировано из оригинала на 2009-08-06 . Получено 2009-12-21 .
Внешние ссылки
[ редактировать ]![]() СМИ, связанные с никотиновыми агонистами в Wikimedia Commons
СМИ, связанные с никотиновыми агонистами в Wikimedia Commons
- Никотиновые+агонисты в Национальной медицинской библиотеке Медицинской библиотеки США (Mesh)
- Сетка Списка агентов 82018722