Метаболизм


| Часть серии о |
| Биохимия |
|---|
 |
Обмен веществ ( / m ə ˈ t æ b ə l ɪ z ə m / , от греческого : μεταβολή Metabolē , «изменение») — совокупность жизнь поддерживающих химических реакций в организмах . Тремя основными функциями метаболизма являются: преобразование энергии пищи в энергию, доступную для запуска клеточных процессов; превращение пищи в строительные блоки белков , липидов , нуклеиновых кислот и некоторых углеводов ; и устранение метаболических отходов . Эти катализируемые ферментами реакции позволяют организмам расти и размножаться, сохранять свои структуры и реагировать на окружающую среду. Слово метаболизм может также относиться к сумме всех химических реакций, происходящих в живых организмах, включая пищеварение и транспортировку веществ в различные клетки и между ними, и в этом случае описанный выше набор реакций внутри клеток называется промежуточным (или промежуточным). ) обмен веществ.
Метаболические реакции можно разделить на катаболические — расщепление соединений (например, глюкозы до пирувата в результате клеточного дыхания ); или анаболический — накопление ( синтез ) соединений (таких как белки, углеводы, липиды и нуклеиновые кислоты). Обычно катаболизм высвобождает энергию, а анаболизм ее потребляет.
Химические реакции метаболизма организованы в метаболические пути , в которых одно химическое вещество посредством ряда стадий превращается в другое химическое вещество, причем каждый этап обеспечивается определенным ферментом . Ферменты имеют решающее значение для метаболизма, поскольку они позволяют организмам запускать желаемые реакции, которые требуют энергии и не происходят сами по себе, связывая их со спонтанными реакциями , высвобождающими энергию. Ферменты действуют как катализаторы — они позволяют реакции протекать быстрее — а также позволяют регулировать скорость метаболической реакции, например, в ответ на изменения в клеточной среде или на сигналы от других клеток.
Система обмена веществ конкретного организма определяет, какие вещества он найдет питательными , а какие ядовитыми . Например, некоторые прокариоты используют в качестве питательного вещества сероводород , однако этот газ ядовит для животных. [1] Скорость основного обмена организма является мерой количества энергии, потребляемой всеми этими химическими реакциями.
Поразительной особенностью метаболизма является сходство основных метаболических путей у совершенно разных видов. [2] Например, набор карбоновых кислот , которые наиболее известны как промежуточные соединения в цикле лимонной кислоты , присутствует во всех известных организмах и встречается у таких разнообразных видов, как одноклеточная бактерия Escherichia coli и огромные многоклеточные организмы, такие как слоны . [3] Эти сходства в метаболических путях, вероятно, обусловлены их ранним появлением в эволюционной истории , а их сохранение, вероятно, обусловлено их эффективностью . [4] [5] При различных заболеваниях, таких как диабет II типа , метаболический синдром и рак , нормальный обмен веществ нарушается. [6] Метаболизм раковых клеток также отличается от метаболизма нормальных клеток, и эти различия можно использовать для поиска мишеней для терапевтического вмешательства при раке. [7]
Ключевые биохимические вещества
[ редактировать ]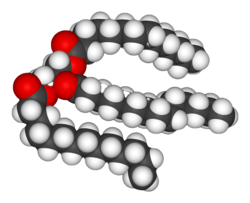
Большинство структур, из которых состоят животные, растения и микробы, состоят из четырех основных классов молекул : аминокислот , углеводов , нуклеиновых кислот и липидов (часто называемых жирами ). Поскольку эти молекулы жизненно важны для жизни, метаболические реакции либо направлены на создание этих молекул во время строительства клеток и тканей, либо на их расщепление и использование для получения энергии путем их переваривания. Эти биохимические вещества можно соединить, образуя полимеры, такие как ДНК и белки , важные макромолекулы жизни. [8]
| Тип молекулы | Название мономерных форм | Название полимерных форм | Примеры полимерных форм |
|---|---|---|---|
| Аминокислоты | Аминокислоты | Белки (состоящие из полипептидов) | Фибриллярные белки и глобулярные белки |
| Углеводы | Моносахариды | Полисахариды | Крахмал , гликоген и целлюлоза |
| Нуклеиновые кислоты | Нуклеотиды | Полинуклеотиды | ДНК и РНК |
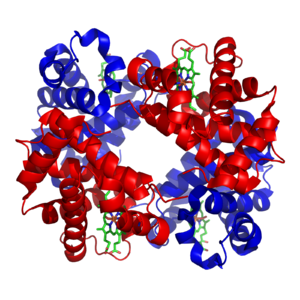
Аминокислоты и белки
[ редактировать ]Белки состоят из аминокислот, расположенных в линейную цепь, соединенную пептидными связями . Многие белки представляют собой ферменты , катализирующие химические реакции обмена веществ. Другие белки выполняют структурные или механические функции, например те, которые формируют цитоскелет — систему каркаса , поддерживающую форму клетки. [9] Белки также важны для передачи сигналов в клетках , иммунных реакций , клеточной адгезии , активного транспорта через мембраны и клеточного цикла . [10] Аминокислоты также способствуют клеточному энергетическому метаболизму, обеспечивая источник углерода для участия в цикле трикарбоновых кислот ( цикл трикарбоновых кислот ). [11] особенно когда основного источника энергии, такого как глюкоза , не хватает, или когда клетки подвергаются метаболическому стрессу. [12]
Липиды
[ редактировать ]Липиды представляют собой наиболее разнообразную группу биохимических веществ. Их основное структурное применение - это часть внутренних и внешних биологических мембран , таких как клеточная мембрана . [10] Их химическую энергию также можно использовать. Липиды содержат длинную неполярную углеводородную цепь с небольшой полярной областью, содержащей кислород. Липиды обычно определяют как гидрофобные или амфипатические биологические молекулы, но они растворяются в органических растворителях, таких как этанол , бензол или хлороформ . [13] Жиры представляют собой большую группу соединений, содержащих жирные кислоты и глицерин ; Молекула глицерина, присоединенная к трем жирным кислотам сложноэфирными связями, называется триацилглицеридом . [14] Существует несколько вариантов базовой структуры, включая основные цепи, такие как сфингозин в сфингомиелине , и гидрофильные группы, такие как фосфат в фосфолипидах . Стероиды, такие как стерол, являются еще одним важным классом липидов. [15]
Углеводы
[ редактировать ]
Углеводы — это альдегиды или кетоны со многими присоединенными гидроксильными группами, которые могут существовать в виде прямых цепей или колец. Углеводы являются наиболее распространенными биологическими молекулами и выполняют многочисленные функции, такие как хранение и транспортировка энергии ( крахмал , гликоген ) и структурных компонентов ( целлюлоза у растений, хитин у животных). [10] Основные углеводные единицы называются моносахаридами и включают галактозу , фруктозу и, что наиболее важно, глюкозу . Моносахариды могут соединяться вместе с образованием полисахаридов практически неограниченным количеством способов. [16]
Нуклеотиды
[ редактировать ]Две нуклеиновые кислоты, ДНК и РНК , представляют собой полимеры нуклеотидов . Каждый нуклеотид состоит из фосфата, присоединенного к сахарной группе рибозы или дезоксирибозы , которая присоединена к азотистому основанию . Нуклеиновые кислоты имеют решающее значение для хранения и использования генетической информации, а также ее интерпретации посредством процессов транскрипции и биосинтеза белка . [10] Эта информация защищена механизмами репарации ДНК и распространяется посредством репликации ДНК . Многие вирусы имеют геном РНК , например, ВИЧ , который использует обратную транскрипцию для создания матрицы ДНК из своего вирусного РНК-генома. [17] РНК в рибозимах, таких как сплайсосомы и рибосомы, аналогична ферментам, поскольку может катализировать химические реакции. Отдельные нуклеозиды получаются путем присоединения нуклеинового основания к сахару рибозе . Эти основания представляют собой гетероциклические кольца, содержащие азот, классифицируемые как пурины или пиримидины . Нуклеотиды также действуют как коферменты в реакциях метаболического переноса группы. [18]
Коэнзимы
[ редактировать ]
Метаболизм включает в себя широкий спектр химических реакций, но большинство из них подпадают под несколько основных типов реакций, которые включают перенос функциональных групп атомов и их связей внутри молекул. [19] Эта общая химия позволяет клеткам использовать небольшой набор метаболических промежуточных продуктов для переноса химических групп между различными реакциями. [18] Эти промежуточные соединения группового переноса называются коферментами . Каждый класс реакций группового переноса осуществляется определенным коферментом, который является субстратом для набора ферментов, его продуцирующих, и набора ферментов, его потребляющих. Таким образом, эти коферменты непрерывно производятся, потребляются и затем перерабатываются. [20]
Одним из центральных коферментов является аденозинтрифосфат (АТФ), энергетическая валюта клеток. Этот нуклеотид используется для передачи химической энергии между различными химическими реакциями. В клетках содержится лишь небольшое количество АТФ, но, поскольку он постоянно регенерируется, человеческий организм может использовать АТФ примерно в своем весе в день. [20] АТФ действует как мост между катаболизмом и анаболизмом . Катаболизм разрушает молекулы, а анаболизм соединяет их. Катаболические реакции генерируют АТФ, а анаболические реакции его потребляют. Он также служит переносчиком фосфатных групп в реакциях фосфорилирования . [21]
Витамин — это органическое соединение , необходимое в небольших количествах, которое не может вырабатываться в клетках. В питании человека большинство витаминов после модификации функционируют как коферменты; например, все водорастворимые витамины фосфорилируются или связываются с нуклеотидами, когда они используются в клетках. [22] Никотинамидадениндинуклеотид (НАД + ), производное витамина В3 ( ниацина ) , является важным коферментом, действующим как акцептор водорода. Сотни отдельных типов дегидрогеназ отрывают электроны от своих субстратов и восстанавливают НАД. + в НАДН. Эта восстановленная форма кофермента затем становится субстратом для любой редуктазы в клетке, которой необходимо переносить атомы водорода на свои субстраты. [23] Никотинамидадениндинуклеотид существует в клетке в двух родственных формах: НАДН и НАДФН. НАД + Форма /НАДН более важна в катаболических реакциях, тогда как НАДФ + /НАДФН используется в анаболических реакциях. [24]
Минерал и кофакторы
[ редактировать ]Неорганические элементы играют решающую роль в обмене веществ; некоторые из них присутствуют в изобилии (например, натрий и калий ), тогда как другие действуют при незначительных концентрациях. Около 99% массы тела человека составляют элементы углерод , азот , кальций , натрий , хлор , калий , водород , фосфор , кислород и сера . Органические соединения (белки, липиды и углеводы) содержат большую часть углерода и азота; большая часть кислорода и водорода присутствует в виде воды. [25]
Обильные неорганические элементы действуют как электролиты . Наиболее важными ионами являются натрий , калий , кальций , магний , хлорид , фосфат и органический ион бикарбонат . Поддержание точного ионного градиента через клеточные мембраны поддерживает осмотическое давление и pH . [26] Ионы также имеют решающее значение для нервов и мышц функции , поскольку потенциалы действия в этих тканях возникают в результате обмена электролитами между внеклеточной жидкостью и клеточной жидкостью, цитозолем . [27] Электролиты входят и покидают клетки через белки клеточной мембраны, называемые ионными каналами . Например, сокращение мышц зависит от движения кальция, натрия и калия через ионные каналы в клеточной мембране и Т-канальцах . [28]
Переходные металлы обычно присутствуют в виде микроэлементов в организмах цинк и железо . , причем наиболее распространены [29] Кофакторы металлов прочно связаны со специфическими участками белков; хотя кофакторы ферментов могут быть модифицированы в ходе катализа, они всегда возвращаются в исходное состояние к концу катализируемой реакции. Металлические микроэлементы попадают в организм с помощью специфических переносчиков и связываются с запасными белками, такими как ферритин или металлотионеин, когда они не используются. [30] [31]
Катаболизм
[ редактировать ]Катаболизм – это совокупность метаболических процессов, которые расщепляют крупные молекулы. К ним относятся расщепление и окисление молекул пищи. Целью катаболических реакций является обеспечение энергией и компонентами, необходимыми для анаболических реакций, в ходе которых строятся молекулы. [32] Точная природа этих катаболических реакций различается от организма к организму, и организмы можно классифицировать на основе источников энергии, водорода и углерода (их основных групп питания ), как показано в таблице ниже. Органические молекулы используются органотрофами в качестве источника атомов водорода или электронов , тогда как литотрофы используют неорганические субстраты. Фототрофы химическую преобразуют солнечный свет в энергию . [33] хемотрофы зависят от окислительно-восстановительных реакций, которые включают перенос электронов от восстановленных молекул-доноров, таких как органические молекулы , водород , сероводород или ионы железа, к кислороду , нитрату или сульфату . У животных в этих реакциях участвуют сложные органические молекулы , которые расщепляются до более простых молекул, таких как углекислый газ и вода. Фотосинтезирующие организмы, такие как растения и цианобактерии , используют аналогичные реакции переноса электронов для хранения энергии, поглощаемой от солнечного света. [34]
| Источник энергии | солнечный свет | фото- | -троф | ||
| молекулы | химио- | ||||
| Водород или донор электронов | органическое соединение | орган- | |||
| неорганическое соединение | член- | ||||
| Источник углерода | органическое соединение | гетеро- | |||
| неорганическое соединение | авто- | ||||
Наиболее распространенный набор катаболических реакций у животных можно разделить на три основные стадии. На первом этапе крупные органические молекулы, такие как белки , полисахариды или липиды , расщепляются на более мелкие компоненты вне клеток. Затем эти более мелкие молекулы поглощаются клетками и превращаются в более мелкие молекулы, обычно в ацетил-коэнзим А (ацетил-КоА), который высвобождает некоторое количество энергии. Наконец, ацетильная группа ацетил-КоА окисляется до воды и углекислого газа в цикле лимонной кислоты и цепи переноса электронов , высвобождая больше энергии и одновременно восстанавливая кофермент никотинамидадениндинуклеотид (НАД) . + ) в НАДН. [32]
Пищеварение
[ редактировать ]Макромолекулы не могут быть непосредственно переработаны клетками. Макромолекулы должны быть разбиты на более мелкие единицы, прежде чем их можно будет использовать в клеточном метаболизме. Для переваривания этих полимеров используются различные классы ферментов. Эти пищеварительные ферменты включают протеазы , которые расщепляют белки на аминокислоты, а также гликозидгидролазы , которые расщепляют полисахариды на простые сахара, известные как моносахариды . [36]
Микробы просто выделяют пищеварительные ферменты в окружающую среду. [37] [38] в то время как животные выделяют эти ферменты только из специализированных клеток кишечника , включая желудок и поджелудочную железу , а также слюнных желез . [39] Аминокислоты или сахара, высвобождаемые этими внеклеточными ферментами, затем перекачиваются в клетки с помощью активных транспортных белков. [40] [41]

Энергия из органических соединений
[ редактировать ]Катаболизм углеводов – это распад углеводов на более мелкие единицы. Углеводы обычно попадают в клетки после того, как они перевариваются до моносахаридов, таких как глюкоза и фруктоза . [42] Попав внутрь, основным путем распада является гликолиз , при котором глюкоза превращается в пируват . образуется молекула-переносчик энергии НАДН . В результате этого процесса из НАД + и генерирует АТФ из АДФ для использования в обеспечении питания многих процессов внутри клетки. [43] Пируват является промежуточным продуктом в нескольких метаболических путях, но большая его часть превращается в ацетил-КоА и участвует в цикле трикарбоновой кислоты , что позволяет производить больше АТФ посредством окислительного фосфорилирования . Это окисление потребляет молекулярный кислород и выделяет воду и углекислый газ. Когда кислорода не хватает или когда пируват временно вырабатывается быстрее, чем он может быть использован в цикле лимонной кислоты (как при интенсивной мышечной нагрузке), пируват превращается в лактат с помощью фермента лактатдегидрогеназы , процесса, который также окисляет НАДН обратно в НАД. + для повторного использования в дальнейшем гликолизе, позволяя продолжать производство энергии. [44] Лактат позже превращается обратно в пируват для производства АТФ, где необходима энергия, или обратно в глюкозу в цикле Кори . Альтернативным путем расщепления глюкозы является пентозофосфатный путь , который производит меньше энергии, но поддерживает анаболизм (синтез биомолекул). Этот путь снижает уровень кофермента НАДФ. + НАДФН и производит пентозные соединения, такие как рибозо-5-фосфат, для синтеза многих биомолекул, таких как нуклеотиды и ароматические аминокислоты . [45]

Жиры катаболизируются путем гидролиза до свободных жирных кислот и глицерина. Глицерин вступает в гликолиз, а жирные кислоты расщепляются путем бета-окисления с высвобождением ацетил-КоА, который затем поступает в цикл лимонной кислоты. Жирные кислоты при окислении выделяют больше энергии, чем углеводы. Стероиды также расщепляются некоторыми бактериями в процессе, аналогичном бета-окислению, и этот процесс распада включает в себя высвобождение значительных количеств ацетил-КоА, пропионил-КоА и пирувата, которые могут использоваться клеткой для получения энергии. M.tuberculosis также может расти на липидном холестерине как единственном источнике углерода, и было подтверждено, что гены, участвующие в пути использования холестерина, важны на различных стадиях жизненного цикла инфекции M.tuberculosis . [46]
Аминокислоты либо используются для синтеза белков и других биомолекул, либо окисляются до мочевины и углекислого газа для производства энергии. [47] Путь окисления начинается с удаления аминогруппы трансаминазой . Аминогруппа подается в цикл мочевины , оставляя дезаминированный углеродный скелет в виде кетокислоты . Некоторые из этих кетокислот являются промежуточными продуктами цикла лимонной кислоты, например α- кетоглутарат, образующийся при дезаминировании глутамата . [48] также Глюкогенные аминокислоты могут превращаться в глюкозу посредством глюконеогенеза . [49]
Энергетические преобразования
[ редактировать ]Окислительное фосфорилирование
[ редактировать ]При окислительном фосфорилировании электроны, удаленные от органических молекул в таких областях, как цикл лимонной кислоты, передаются кислороду, а высвободившаяся энергия используется для производства АТФ. это осуществляется У эукариот с помощью ряда белков в мембранах митохондрий, называемых цепью переноса электронов . У прокариот клетки эти белки находятся во внутренней мембране . [50] Эти белки используют энергию восстановленных молекул, таких как НАДН, для перекачки протонов через мембрану. [51]

Выкачивание протонов из митохондрий создает разницу в концентрации протонов на мембране и создает электрохимический градиент . [52] Эта сила заставляет протоны возвращаться в митохондрии через основу фермента, называемого АТФ-синтазой . Поток протонов заставляет субъединицу стебля вращаться, в результате чего активный центр синтазного домена меняет форму и фосфорилирует аденозиндифосфат , превращая его в АТФ. [20]
Энергия из неорганических соединений
[ редактировать ]Хемолитотрофия — тип метаболизма, обнаруженный у прокариот , при котором энергия получается за счет окисления неорганических соединений . Эти организмы могут использовать водород , [53] восстановленные соединения серы (такие как сульфид , сероводород и тиосульфат ), [1] двухвалентное железо (Fe(II)) [54] или аммиак [55] в качестве источников восстановительной способности и получают энергию от окисления этих соединений. [56] Эти микробные процессы играют важную роль в глобальных биогеохимических циклах, таких как ацетогенез , нитрификация и денитрификация, и имеют решающее значение для плодородия почвы . [57] [58]
Энергия света
[ редактировать ]Энергию солнечного света улавливают растения , цианобактерии , пурпурные бактерии , зеленые серобактерии и некоторые протисты . Этот процесс часто сочетается с преобразованием углекислого газа в органические соединения как часть фотосинтеза, который обсуждается ниже. Однако системы захвата энергии и фиксации углерода могут работать у прокариот отдельно, поскольку пурпурные бактерии и зеленые серные бактерии могут использовать солнечный свет в качестве источника энергии, переключаясь при этом между фиксацией углерода и ферментацией органических соединений. [59] [60]
У многих организмов захват солнечной энергии в принципе аналогичен окислительному фосфорилированию, поскольку предполагает сохранение энергии в виде градиента концентрации протонов. Эта движущая сила протонов затем управляет синтезом АТФ. [61] Электроны, необходимые для управления этой цепью переноса электронов, поступают из светособирающих белков, называемых фотосинтетическим реакционным центром . Реакционные центры подразделяются на два типа в зависимости от природы присутствующего фотосинтетического пигмента : большинство фотосинтезирующих бактерий имеют только один тип, а растения и цианобактерии - два. [62]
У растений, водорослей и цианобактерий фотосистема II использует энергию света для удаления электронов из воды, выделяя кислород в качестве побочного продукта. Затем электроны переходят к комплексу цитохрома b6f , который использует свою энергию для перекачки протонов через тилакоидную мембрану в хлоропласте . [34] Эти протоны движутся обратно через мембрану, управляя АТФ-синтазой, как и раньше. Затем электроны проходят через фотосистему I и могут быть использованы для восстановления кофермента НАДФ. + . [63] Этот кофермент может войти в цикл Кальвина или переработаться для дальнейшего образования АТФ. [ нужна ссылка ]
Анаболизм
[ редактировать ]Анаболизм – это совокупность конструктивных метаболических процессов, при которых энергия, выделяемая в результате катаболизма, используется для синтеза сложных молекул. В общем, сложные молекулы, составляющие клеточные структуры, строятся шаг за шагом из более мелких и простых предшественников. Анаболизм включает три основных этапа. Во-первых, производство предшественников, таких как аминокислоты , моносахариды , изопреноиды и нуклеотиды , во-вторых, их активация в реактивные формы с использованием энергии АТФ и, в-третьих, сборка этих предшественников в сложные молекулы, такие как белки , полисахариды , липиды и нуклеиновые кислоты. . [64]
Анаболизм у организмов может быть различным в зависимости от источника образования молекул в их клетках. Автотрофы, такие как растения, могут создавать в своих клетках сложные органические молекулы, такие как полисахариды и белки, из простых молекул, таких как углекислый газ и вода. С другой стороны, гетеротрофам для производства этих сложных молекул требуется источник более сложных веществ, таких как моносахариды и аминокислоты. Организмы можно далее классифицировать по конечному источнику энергии: фотоавтотрофы и фотогетеротрофы получают энергию от света, тогда как хемоавтотрофы и хемогетеротрофы получают энергию от реакций окисления. [64]
Фиксация углерода
[ редактировать ]
Фотосинтез – это синтез углеводов из солнечного света и углекислого газа (CO 2 ). У растений, цианобактерий и водорослей кислородный фотосинтез расщепляет воду, при этом кислород образуется в качестве побочного продукта. В этом процессе используются АТФ и НАДФН, вырабатываемые реакционными центрами фотосинтеза , как описано выше, для преобразования CO 2 в глицерат-3-фосфат , который затем может быть преобразован в глюкозу. Эта реакция фиксации углерода осуществляется ферментом RuBisCO как часть цикла Кальвина-Бенсона . [65] У растений наблюдаются три типа фотосинтеза: фиксация углерода C3 , фиксация углерода C4 и фотосинтез CAM . Они различаются по пути, по которому углекислый газ поступает в цикл Кальвина: растения C3 напрямую фиксируют CO 2 , тогда как фотосинтез C4 и CAM сначала включает CO 2 в другие соединения в качестве адаптации к интенсивному солнечному свету и засушливым условиям. [66]
У фотосинтезирующих прокариот механизмы фиксации углерода более разнообразны. Здесь углекислый газ может фиксироваться с помощью цикла Кальвина-Бенсона, обратного цикла лимонной кислоты , [67] или карбоксилирование ацетил-КоА. [68] [69] Прокариотические хемоавтотрофы также фиксируют CO 2 посредством цикла Кальвина-Бенсона, но для запуска реакции используют энергию неорганических соединений. [70]
Углеводы и гликаны
[ редактировать ]При анаболизме углеводов простые органические кислоты могут превращаться в моносахариды, такие как глюкоза , а затем использоваться для сборки полисахаридов, таких как крахмал . Образование глюкозы из таких соединений, как пируват , лактат , глицерин , глицерат-3-фосфат и аминокислот, называется глюконеогенезом . Глюконеогенез превращает пируват в глюкозо-6-фосфат через ряд промежуточных продуктов, многие из которых являются общими с гликолизом . [43] Однако этот путь не представляет собой просто обратный гликолиз , поскольку несколько стадий катализируются негликолитическим ферментами. Это важно, поскольку позволяет регулировать образование и распад глюкозы отдельно и предотвращает одновременную работу обоих путей в бесполезном цикле . [71] [72]
Хотя жир является распространенным способом хранения энергии, у позвоночных, таких как человек, жирные кислоты в этих хранилищах не могут быть преобразованы в глюкозу посредством глюконеогенеза , поскольку эти организмы не могут превращать ацетил-КоА в пируват ; У растений есть, а у животных нет необходимого ферментативного аппарата. [73] В результате после длительного голодания позвоночным необходимо производить кетоновые тела из жирных кислот, чтобы заменить глюкозу в тканях, таких как мозг, которые не могут метаболизировать жирные кислоты. [74] У других организмов, таких как растения и бактерии, эта метаболическая проблема решается с помощью глиоксилатного цикла , который обходит стадию декарбоксилирования в цикле лимонной кислоты и позволяет превращать ацетил-КоА в оксалоацетат , где его можно использовать для производства глюкозы. . [73] [75] Помимо жира, глюкоза хранится в большинстве тканей как энергетический ресурс, доступный внутри тканей посредством гликогенеза, который обычно использовался для поддержания уровня глюкозы в крови. [76]
Полисахариды и гликаны образуются путем последовательного добавления моносахаридов с помощью гликозилтрансферазы от реакционноспособного донора сахарофосфата, такого как уридиндифосфатглюкоза (UDP-Glc), к акцепторной гидроксильной группе растущего полисахарида. Поскольку любая из гидроксильных групп в кольце субстрата может быть акцептором, образующиеся полисахариды могут иметь прямую или разветвленную структуру. [77] Образующиеся полисахариды сами могут выполнять структурные или метаболические функции или переноситься в липиды и белки с помощью ферментов олигосахарилтрансфераз . [78] [79]
Жирные кислоты, изопреноиды и стеролы
[ редактировать ]
Жирные кислоты производятся синтазами жирных кислот , которые полимеризуются, а затем восстанавливают звенья ацетил-КоА. Ацильные цепи в жирных кислотах удлиняются за счет цикла реакций, в которых ацильная группа добавляется, восстанавливается до спирта, дегидратируется до алкеновой группы, а затем снова восстанавливается до алкановой группы. Ферменты биосинтеза жирных кислот делятся на две группы: у животных и грибов все эти реакции синтаз жирных кислот осуществляются одним многофункциональным белком I типа, [80] в то время как в растительных пластидах и бактериях каждый этап этого пути выполняют отдельные ферменты типа II. [81] [82]
Терпены и изопреноиды представляют собой большой класс липидов, включающих каротиноиды и образующих самый большой класс растительных натуральных продуктов . [83] Эти соединения производятся путем сборки и модификации изопреновых единиц, полученных из реакционноспособных предшественников изопентенилпирофосфата и диметилаллилпирофосфата . [84] Эти предшественники могут быть получены разными способами. У животных и архей мевалонатный путь производит эти соединения из ацетил-КоА. [85] в то время как у растений и бактерий немевалонатный путь использует в качестве субстратов пируват и глицеральдегид-3-фосфат . [84] [86] Одной из важных реакций, в которых используются активированные доноры изопрена, является биосинтез стеринов . Здесь единицы изопрена соединяются, образуя сквален , а затем сворачиваются и формируются в набор колец, образуя ланостерин . [87] Ланостерин затем может быть преобразован в другие стерины, такие как холестерин и эргостерин . [87] [88]
Белки
[ редактировать ]Организмы различаются по своей способности синтезировать 20 распространенных аминокислот. Большинство бактерий и растений могут синтезировать все двадцать, но млекопитающие могут синтезировать только одиннадцать заменимых аминокислот, поэтому девять незаменимых аминокислот необходимо получать с пищей. [10] Некоторые простые паразиты , такие как бактерии Mycoplasma pneumoniae , лишены синтеза аминокислот и получают аминокислоты непосредственно от хозяев. [89] Все аминокислоты синтезируются из промежуточных продуктов гликолиза, цикла трикарбоновых кислот или пентозофосфатного пути. Азот обеспечивается глутаматом и глютамином . Синтез заменимых аминокислот зависит от образования соответствующей альфа-кетокислоты, которая затем трансаминируется с образованием аминокислоты. [90]
Аминокислоты превращаются в белки путем соединения в цепочку пептидных связей . Каждый отдельный белок имеет уникальную последовательность аминокислотных остатков: это его первичная структура . Точно так же, как буквы алфавита можно комбинировать, образуя почти бесконечное множество слов, аминокислоты могут соединяться в различных последовательностях, образуя огромное разнообразие белков. Белки состоят из аминокислот, которые активируются путем присоединения к молекуле транспортной РНК посредством сложноэфирной связи. Этот предшественник аминоацил-тРНК образуется в результате АТФ -зависимой реакции, осуществляемой синтетазой аминоацил-тРНК . [91] Эта аминоацил-тРНК затем становится субстратом для рибосомы , которая присоединяет аминокислоту к удлиняющейся белковой цепи, используя информацию о последовательности в информационной РНК . [92]
Синтез и спасение нуклеотидов
[ редактировать ]Нуклеотиды образуются из аминокислот, углекислого газа и муравьиной кислоты способами, требующими большого количества метаболической энергии. [93] Следовательно, у большинства организмов есть эффективные системы для спасения предварительно сформированных нуклеотидов. [93] [94] Пурины синтезируются в виде нуклеозидов (оснований, присоединенных к рибозе ). [95] И аденин , и гуанин производятся из предшественника нуклеозида инозинмонофосфата , который синтезируется с использованием атомов аминокислот глицина , глутамина и аспарагиновой кислоты , а также формиата , перенесенного из кофермента тетрагидрофолата . Пиримидины же синтезируются из основания оротата , который образуется из глутамина и аспартата. [96]
Ксенобиотики и окислительно-восстановительный обмен
[ редактировать ]Все организмы постоянно подвергаются воздействию соединений, которые они не могут использовать в пищу и которые будут вредны, если будут накапливаться в клетках, поскольку у них нет метаболической функции. Эти потенциально вредные соединения называются ксенобиотиками . [97] Ксенобиотики, такие как синтетические лекарства , природные яды и антибиотики, детоксифицируются набором ферментов, метаболизирующих ксенобиотики. У человека к ним относятся цитохром Р450 оксидазы , [98] УДФ-глюкуронозилтрансферазы , [99] и глутатион S -трансферазы . [100] Эта система ферментов действует в три этапа, сначала окисляя ксенобиотик (фаза I), а затем конъюгируя водорастворимые группы с молекулой (фаза II). Модифицированный водорастворимый ксенобиотик затем может быть выкачан из клеток и в многоклеточных организмах может подвергаться дальнейшему метаболизму перед выведением из организма (фаза III). В экологии эти реакции имеют особое значение при микробном биоразложении загрязняющих веществ и биоремедиации загрязненных земель и разливов нефти. [101] Многие из этих микробных реакций свойственны многоклеточным организмам, но из-за невероятного разнообразия типов микробов эти организмы способны справляться с гораздо более широким спектром ксенобиотиков, чем многоклеточные организмы, и могут разлагать даже стойкие органические загрязнители, такие как хлорорганические соединения. [102]
Связанной проблемой для аэробных организмов является окислительный стресс . [103] Здесь процессы, включающие окислительное фосфорилирование и образование дисульфидных связей во время сворачивания белка, производят активные формы кислорода, такие как перекись водорода . [104] Эти повреждающие окислители удаляются антиоксидантными метаболитами, такими как глутатион , и такими ферментами, как каталазы и пероксидазы . [105] [106]
Термодинамика живых организмов
[ редактировать ]Живые организмы должны подчиняться законам термодинамики , описывающим перенос тепла и работы . Второй закон термодинамики гласит, что в любой изолированной системе количество энтропии (беспорядка) не может уменьшаться. Хотя удивительная сложность живых организмов, по-видимому, противоречит этому закону, жизнь возможна, поскольку все организмы представляют собой открытые системы , которые обмениваются веществом и энергией с окружающей средой. Живые системы не находятся в равновесии , а представляют собой диссипативные системы , которые поддерживают свое состояние высокой сложности, вызывая большее увеличение энтропии окружающей среды. [107] Метаболизм клетки достигает этого путем объединения спонтанных процессов катаболизма с неспонтанными процессами анаболизма. С термодинамической точки зрения обмен веществ поддерживает порядок, создавая беспорядок. [108]
Регулирование и контроль
[ редактировать ]Поскольку среда большинства организмов постоянно меняется, реакции метаболизма должны тонко регулироваться, чтобы поддерживать постоянный набор условий внутри клеток, состояние, называемое гомеостазом . [109] [110] Метаболическая регуляция также позволяет организмам реагировать на сигналы и активно взаимодействовать с окружающей средой. [111] Две тесно связанные концепции важны для понимания того, как контролируются метаболические пути. Во-первых, регуляция фермента в пути заключается в том, как его активность увеличивается и уменьшается в ответ на сигналы. Во-вторых, контроль, осуществляемый этим ферментом, — это влияние, которое эти изменения его активности оказывают на общую скорость пути ( поток через путь). [112] Например, фермент может демонстрировать большие изменения в активности (т.е. он в высокой степени регулируется), но если эти изменения мало влияют на поток метаболического пути, то этот фермент не участвует в контроле этого пути. [113]
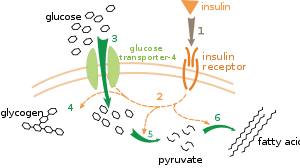
Существует несколько уровней метаболической регуляции. При внутренней регуляции метаболический путь саморегулируется, реагируя на изменения уровней субстратов или продуктов; например, уменьшение количества продукта может увеличить поток через путь для компенсации. [112] Этот тип регуляции часто включает аллостерическую регуляцию активности нескольких ферментов этого пути. [114] Внешний контроль предполагает, что клетка многоклеточного организма меняет свой метаболизм в ответ на сигналы других клеток. Эти сигналы обычно имеют форму водорастворимых посланников, таких как гормоны и факторы роста , и обнаруживаются специфическими рецепторами на поверхности клеток. [115] Эти сигналы затем передаются внутри клетки с помощью систем вторичных мессенджеров , которые часто включают фосфорилирование белков. [116]
Хорошо изученным примером внешнего контроля является регуляция метаболизма глюкозы гормоном инсулином . [117] Инсулин вырабатывается в ответ на повышение уровня глюкозы в крови . Связывание гормона с рецепторами инсулина на клетках затем активирует каскад протеинкиназ , которые заставляют клетки поглощать глюкозу и превращать ее в запасные молекулы, такие как жирные кислоты и гликоген . [118] Метаболизм гликогена контролируется активностью фосфорилазы — фермента, расщепляющего гликоген, и гликогенсинтазы — фермента, который его производит. Эти ферменты регулируются реципрокным образом: фосфорилирование ингибирует гликогенсинтазу, но активирует фосфорилазу. Инсулин вызывает синтез гликогена, активируя протеинфосфатазы и вызывая снижение фосфорилирования этих ферментов. [119]
Эволюция
[ редактировать ]
Описанные выше центральные пути метаболизма, такие как гликолиз и цикл лимонной кислоты, присутствуют во всех трех доменах живых существ и присутствовали у последнего универсального общего предка . [3] [120] Эта универсальная предковая клетка была прокариотом и, вероятно, метаногеном , который имел обширный метаболизм аминокислот, нуклеотидов, углеводов и липидов. [121] [122] Сохранение этих древних путей во время более поздней эволюции может быть результатом того, что эти реакции были оптимальным решением их конкретных метаболических проблем, причем такие пути, как гликолиз и цикл лимонной кислоты, производят свои конечные продукты высокоэффективно и за минимальное количество шагов. . [4] [5] Первые пути ферментативного метаболизма, возможно, были частью метаболизма пуриновых нуклеотидов, в то время как предыдущие метаболические пути были частью древнего мира РНК . [123]
Было предложено множество моделей для описания механизмов развития новых метаболических путей. К ним относятся последовательное добавление новых ферментов к короткому предковому пути, дублирование, а затем дивергенция целых путей, а также вовлечение ранее существовавших ферментов и их сборка в новый путь реакции. [124] Относительная важность этих механизмов неясна, но геномные исследования показали, что ферменты в пути, вероятно, имеют общее происхождение, что позволяет предположить, что многие пути развивались поэтапно с новыми функциями, созданными из ранее существовавших этапов. в пути. [125] Альтернативная модель основана на исследованиях, которые прослеживают эволюцию структур белков в метаболических сетях. Это предполагает, что ферменты повсеместно рекрутируются, заимствуя ферменты для выполнения аналогичных функций в различных метаболических путях (очевидно из базы данных MANET ). [126] Эти процессы рекрутирования приводят к образованию эволюционной ферментативной мозаики. [127] Третья возможность заключается в том, что некоторые части метаболизма могут существовать в виде «модулей», которые можно повторно использовать в разных путях и выполнять схожие функции на разных молекулах. [128]
Помимо развития новых метаболических путей, эволюция также может привести к потере метаболических функций. Например, у некоторых паразитов метаболические процессы, которые не являются необходимыми для выживания, теряются, и вместо этого предварительно сформированные аминокислоты, нуклеотиды и углеводы могут быть удалены из организма хозяина . [129] Аналогичное снижение метаболических возможностей наблюдается у эндосимбиотических организмов. [130]
Расследование и манипуляции
[ редактировать ]
Классически метаболизм изучается с помощью редукционистского подхода, который фокусируется на одном метаболическом пути. Особую ценность представляет использование радиоактивных индикаторов на уровне всего организма, тканей и клеток, которые определяют пути от предшественников к конечным продуктам путем идентификации радиоактивно меченных промежуточных продуктов и продуктов. [131] Ферменты, катализирующие эти химические реакции, затем можно очистить и исследовать их кинетику и реакцию на ингибиторы . Параллельный подход заключается в идентификации небольших молекул в клетке или ткани; полный набор этих молекул называется метаболомом . В целом эти исследования дают хорошее представление о структуре и функциях простых метаболических путей, но недостаточны применительно к более сложным системам, таким как метаболизм целой клетки. [132]
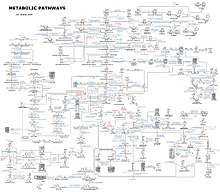
Представление о сложности метаболических сетей в клетках, содержащих тысячи различных ферментов, дает рисунок справа, на котором показаны взаимодействия всего лишь 43 белков и 40 метаболитов: последовательности геномов представляют собой списки, содержащие до 26 500 генов. [133] Однако теперь можно использовать эти геномные данные для реконструкции полных сетей биохимических реакций и создания более целостных математических моделей, которые могут объяснить и предсказать их поведение. [134] Эти модели особенно эффективны, когда они используются для интеграции данных о путях и метаболитах, полученных с помощью классических методов, с данными об экспрессии генов , полученными в результате исследований протеомных микрочипов и ДНК . [135] С помощью этих методов теперь создана модель метаболизма человека, которая будет служить ориентиром для будущих открытий лекарств и биохимических исследований. [136] Эти модели теперь используются в сетевом анализе для классификации болезней человека на группы, которые имеют общие белки или метаболиты. [137] [138]
Бактериальные метаболические сети являются ярким примером « галстука-бабочки». [139] [140] [141] организация, архитектура, способная вводить широкий спектр питательных веществ и производить большое разнообразие продуктов и сложных макромолекул, используя относительно небольшое количество промежуточных общих валют. [142]
Основным технологическим применением этой информации является метаболическая инженерия . Здесь такие организмы, как дрожжи , растения или бактерии, генетически модифицируются, чтобы сделать их более полезными в биотехнологии и способствовать производству лекарств, таких как антибиотики , или промышленных химикатов, таких как 1,3-пропандиол и шикимовая кислота . [143] [144] [145] Эти генетические модификации обычно направлены на уменьшение количества энергии, используемой для производства продукта, повышение урожайности и сокращение образования отходов. [146]
История
[ редактировать ]Термин «метаболизм» происходит от древнегреческого слова μεταβολή — «метабол», означающего «изменение», которое происходит от μεταβάλλειν — «метабаллеин», что означает «изменяться». [147]
Греческая философия
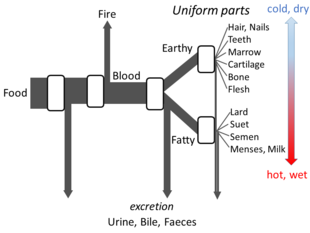
[ редактировать ]Аристотеля В книге «Части животных» изложены достаточно детали его взглядов на метаболизм, чтобы можно было построить модель открытого потока. Он считал, что на каждой стадии процесса материалы из пищи трансформируются, при этом выделяется тепло, как классический элемент огня, а остаточные материалы выделяются в виде мочи, желчи или фекалий. [148]
Ибн ан-Нафис описал метаболизм в своей работе 1260 года нашей эры под названием «Ар-Рисала аль-Камилия фил Сиера ан-Набавия» («Трактат Камиля о биографии Пророка»), которая включала следующую фразу: «И тело, и его части находятся в непрерывном состоянии. растворения и питания, поэтому они неизбежно претерпевают постоянные изменения». [149]
Применение научного метода и современных метаболических теорий
[ редактировать ]История научного изучения метаболизма насчитывает несколько столетий и перешла от изучения целых животных в ранних исследованиях к изучению отдельных метаболических реакций в современной биохимии. Первые контролируемые эксперименты по метаболизму человека были опубликованы Санторио Санторио в 1614 году в его книге Ars de statica medicina . [150] Он описал, как взвешивался до и после еды, сна , работы, секса, голодания, питья и испражнения. Он обнаружил, что большая часть принятой им пищи терялась из-за того, что он называл « неощутимым потом ».

В этих ранних исследованиях механизмы этих метаболических процессов не были идентифицированы, и жизненная сила оживляет живую ткань. считалось, что [151] В 19 веке, изучая ферментацию сахара в спирт с помощью дрожжей , Луи Пастер пришел к выводу, что брожение катализируется веществами внутри дрожжевых клеток, которые он назвал «ферментами». Он писал, что «спиртовое брожение — это процесс, связанный с жизнью и организацией дрожжевых клеток, а не с гибелью или гниением клеток». [152] Это открытие, наряду с публикацией Фридрихом Вёлером в 1828 году статьи о химическом синтезе мочевины , [153] и примечателен тем, что является первым органическим соединением, полученным из полностью неорганических предшественников. Это доказало, что органические соединения и химические реакции, обнаруженные в клетках, в принципе ничем не отличаются от любой другой области химии.
Именно открытие ферментов в начале 20 века Эдуардом Бюхнером отделило изучение химических реакций обмена веществ от биологического изучения клеток и положило начало биохимии . [154] Масса биохимических знаний быстро росла на протяжении начала 20 века. Одним из самых плодовитых современных биохимиков был Ганс Кребс , который внес огромный вклад в изучение метаболизма. [155] Он открыл цикл мочевины, а позже, работая с Гансом Корнбергом , цикл лимонной кислоты и глиоксилатный цикл. [156] [157] [75] Современным биохимическим исследованиям во многом способствовала разработка новых методов, таких как хроматография , рентгеновская дифракция , ЯМР-спектроскопия , радиоизотопная маркировка , электронная микроскопия и моделирование молекулярной динамики . Эти методы позволили открыть и детально проанализировать множество молекул и метаболических путей в клетках. [ нужна ссылка ]
См. также
[ редактировать ]- Антропогенный метаболизм – Материальный и энергетический круговорот человеческого общества.
- Антиметаболит – химическое вещество, препятствующее использованию метаболита.
- Калориметрия - определение теплопередачи в системе путем измерения других ее свойств.
- Изотермическая микрокалориметрия - измерение чистой скорости теплового потока в зависимости от прошедшего времени.
- Врожденные нарушения обмена веществ . Класс генетических заболеваний.
- Гипотеза мира железа и серы - Гипотетический сценарий происхождения жизни, теория происхождения жизни «прежде всего метаболизм».
- Метаболическое расстройство - заболевание, связанное с ошибками в метаболических процессах построения или деградации молекул.
- Микрофизиометрия
- Первичные группы питания - Группа организмов
- Протометаболизм
- Респирометрия – оценка скорости метаболизма путем измерения теплопродукции.
- Поток метаболизма
- Метаболизм серы - совокупность химических реакций с участием серы в живых организмах.
- Термический эффект еды - эффект еды.
- Городской метаболизм - Модель потоков материалов и энергии в городах.
- Водный обмен - аспект гомеостаза, касающийся контроля количества воды в организме.
- Переполненный метаболизм – Клеточные явления
- Онкометаболизм
- Reactome - База данных биологических путей
- KEGG – Коллекция баз данных по биоинформатике
Ссылки
[ редактировать ]- ^ Jump up to: а б Фридрих, CG (1997). Физиология и генетика сероокисляющих бактерий . Достижения микробной физиологии. Том. 39. С. 235–89. дои : 10.1016/S0065-2911(08)60018-1 . ISBN 978-0-12-027739-1 . ПМИД 9328649 .
- ^ Пейс НР (январь 2001 г.). «Универсальная природа биохимии» . Труды Национальной академии наук Соединенных Штатов Америки . 98 (3): 805–8. Бибкод : 2001PNAS...98..805P . дои : 10.1073/pnas.98.3.805 . ПМЦ 33372 . ПМИД 11158550 .
- ^ Jump up to: а б Смит Э., Моровиц HJ (сентябрь 2004 г.). «Универсальность в промежуточном метаболизме» . Труды Национальной академии наук Соединенных Штатов Америки . 101 (36): 13168–73. Бибкод : 2004PNAS..10113168S . дои : 10.1073/pnas.0404922101 . ПМК 516543 . ПМИД 15340153 .
- ^ Jump up to: а б Эбенхё О, Генрих Р. (январь 2001 г.). «Эволюционная оптимизация метаболических путей. Теоретическая реконструкция стехиометрии систем, продуцирующих АТФ и НАДН». Бюллетень математической биологии . 63 (1): 21–55. дои : 10.1006/bulm.2000.0197 . ПМИД 11146883 . S2CID 44260374 .
- ^ Jump up to: а б Мелендес-Эвиа Э., Уодделл Т.Г., Касканте М. (сентябрь 1996 г.). «Загадка цикла лимонной кислоты Кребса: сборка частей химически возможных реакций и оппортунизм в разработке метаболических путей в ходе эволюции». Журнал молекулярной эволюции . 43 (3): 293–303. Бибкод : 1996JMolE..43..293M . дои : 10.1007/BF02338838 . ПМИД 8703096 . S2CID 19107073 .
- ^ Смит Р.Л., Сотерс М.Р., Вюст Р.К., Хауткупер Р.Х. (август 2018 г.). «Метаболическая гибкость как адаптация к энергетическим ресурсам и потребностям здоровья и болезней» . Эндокринные обзоры . 39 (4): 489–517. дои : 10.1210/er.2017-00211 . ПМК 6093334 . ПМИД 29697773 .
- ^ Вандер Хайден М.Г., ДеБерардинис Р.Дж. (февраль 2017 г.). «Понимание взаимосвязей между метаболизмом и биологией рака» . Клетка . 168 (4): 657–669. дои : 10.1016/j.cell.2016.12.039 . ПМЦ 5329766 . ПМИД 28187287 .
- ^ Купер GM (2000). «Молекулярный состав клеток» . Клетка: молекулярный подход (2-е изд.). Архивировано из оригинала 27 августа 2020 года . Проверено 25 июня 2020 г.
- ^ Мичи К.А., Лёве Дж (2006). «Динамические нити бактериального цитоскелета». Ежегодный обзор биохимии . 75 : 467–92. doi : 10.1146/annurev.biochem.75.103004.142452 . ПМИД 16756499 . S2CID 4550126 .
- ^ Jump up to: а б с д и Нельсон Д.Л., Кокс М.М. (2005). Ленингерские принципы биохимии . Нью-Йорк: WH Freeman и компания. п. 841 . ISBN 978-0-7167-4339-2 .
- ^ Келлехер Дж.К., Брайан Б.М., Маллет Р.Т., Холлеран А.Л., Мерфи А.Н., Фискум Дж. (сентябрь 1987 г.). «Анализ метаболизма цикла трикарбоновых кислот клеток гепатомы путем сравнения соотношений 14CO2» . Биохимический журнал . 246 (3): 633–9. дои : 10.1042/bj2460633 . ПМЦ 1148327 . ПМИД 3120698 .
- ^ Хотерсолл Дж.С., Ахмед А. (2013). «Метаболическая судьба повышенного поглощения аминокислот дрожжами после катаболитной дерепрессии» . Журнал аминокислот . 2013 : 461901. doi : 10.1155/2013/461901 . ПМЦ 3575661 . ПМИД 23431419 .
- ^ Фэйи Э., Субраманиам С., Браун Х.А., Гласс СК, Меррилл А.Х., Мерфи Р.К. и др. (май 2005 г.). «Комплексная система классификации липидов» . Журнал исследований липидов . 46 (5): 839–61. doi : 10.1194/jlr.E400004-JLR200 . ПМИД 15722563 .
- ^ «Номенклатура липидов Губ-1 и Губ-2» . qmul.ac.uk. Архивировано из оригинала 6 июня 2020 года . Проверено 6 июня 2020 г.
- ^ Берг Дж.М., Тимочко Дж.Л., Гатто-младший Г.Дж., Страйер Л. (8 апреля 2015 г.). Биохимия (8-е изд.). Нью-Йорк: WH Freeman. п. 362. ИСБН 978-1-4641-2610-9 . OCLC 913469736 .
- ^ Раман Р., Рагурам С., Венкатараман Г., Полсон Дж.К., Сасисекхаран Р. (ноябрь 2005 г.). «Гликомика: интегрированный системный подход к структурно-функциональным взаимоотношениям гликанов». Природные методы . 2 (11): 817–24. дои : 10.1038/nmeth807 . ПМИД 16278650 . S2CID 4644919 .
- ^ Сьерра С., Купфер Б., Кайзер Р. (декабрь 2005 г.). «Основы вирусологии ВИЧ-1 и его репликации». Журнал клинической вирусологии . 34 (4): 233–44. дои : 10.1016/j.jcv.2005.09.004 . ПМИД 16198625 .
- ^ Jump up to: а б Виммер М.Дж., Роуз И.А. (1978). «Механизмы реакций переноса группы, катализируемых ферментами». Ежегодный обзор биохимии . 47 : 1031–78. дои : 10.1146/annurev.bi.47.070178.005123 . ПМИД 354490 .
- ^ Митчелл П. (март 1979 г.). «Девятая лекция сэра Ганса Кребса. Компартментация и коммуникация в живых системах. Лигандная проводимость: общий каталитический принцип в химических, осмотических и хемиосмотических реакционных системах» . Европейский журнал биохимии . 95 (1): 1–20. дои : 10.1111/j.1432-1033.1979.tb12934.x . ПМИД 378655 .
- ^ Jump up to: а б с Димрот П., фон Баллмос С., Мейер Т. (март 2006 г.). «Каталитические и механические циклы в синтезе F-АТФ. Четвертый в серии обзоров циклов» . Отчеты ЭМБО . 7 (3): 276–82. дои : 10.1038/sj.embor.7400646 . ПМЦ 1456893 . ПМИД 16607397 .
- ^ Бонора М., Патерньяни С., Римесси А., Де Марчи Е., Суски Дж.М., Бонони А. и др. (сентябрь 2012 г.). «Синтез и хранение АТФ» . Пуринергическая сигнализация . 8 (3): 343–57. дои : 10.1007/s11302-012-9305-8 . ПМК 3360099 . ПМИД 22528680 .
- ^ Берг Дж. М., Тимочко Дж. Л., Страйер Л. (2002). «Витамины часто являются предшественниками коферментов» . Биохимия. 5-е издание . Архивировано из оригинала 15 декабря 2020 года . Проверено 9 июня 2020 г.
- ^ Поллак Н., Дёлле С., Циглер М. (март 2007 г.). «Сила восстановления: пиридиновые нуклеотиды — маленькие молекулы с множеством функций» . Биохимический журнал . 402 (2): 205–18. дои : 10.1042/BJ20061638 . ПМК 1798440 . ПМИД 17295611 .
- ^ Фатих Ю (2009). Достижения биохимии пищевых продуктов . Бока-Ратон: CRC Press. п. 228. ИСБН 978-1-4200-0769-5 . OCLC 607553259 .
- ^ Хеймсфилд С.Б., Ваки М., Кехайяс Дж., Лихтман С., Дилманиан Ф.А., Камен Ю. и др. (август 1991 г.). «Химический и элементный анализ человека in vivo с использованием улучшенных моделей состава тела». Американский журнал физиологии . 261 (2 ч. 1): E190-8. дои : 10.1152/ajpendo.1991.261.2.E190 . ПМИД 1872381 .
- ^ «Электролитный баланс» . Анатомия и физиология . ОпенСтакс. Архивировано из оригинала 2 июня 2020 года . Проверено 23 июня 2020 г.
- ^ Лодиш Х., Берк А., Зипурски С.Л., Мацудайра П., Балтимор Д., Дарнелл Дж. (2000). «Потенциал действия и проводимость электрических импульсов» . Молекулярно-клеточная биология (4-е изд.). Архивировано из оригинала 30 мая 2020 года . Проверено 23 июня 2020 г. - через NCBI.
- ^ Дулханти AF (сентябрь 2006 г.). «Связь возбуждения-сокращения с 1950-х годов в новое тысячелетие». Клиническая и экспериментальная фармакология и физиология . 33 (9): 763–72. дои : 10.1111/j.1440-1681.2006.04441.x . ПМИД 16922804 . S2CID 37462321 .
- ^ Торрес-Ромеро Х.К., Альварес-Санчес М.Е., Фернандес-Мартин К., Альварес-Санчес Л.К., Арана-Аргаес В., Рамирес-Камачо М., Лара-Рьегос Х. (2018). «Выброс цинка у Trichomonas vaginalis: идентификация и анализ экспрессии CDF-подобных генов in silico». В Оливарес-Кирос Л., Ресендис-Антонио О (ред.). Количественные модели микроскопических и макроскопических биологических макромолекул и тканей . Чам: Международное издательство Springer. стр. 149–168. дои : 10.1007/978-3-319-73975-5_8 . ISBN 978-3-319-73975-5 .
- ^ Казинс Р.Дж., Люцци Дж.П., Лихтен Л.А. (август 2006 г.). «Транспорт, незаконный оборот и сигналы цинка у млекопитающих» . Журнал биологической химии . 281 (34): 24085–9. дои : 10.1074/jbc.R600011200 . ПМИД 16793761 . Архивировано из оригинала 25 июня 2020 года . Проверено 24 июня 2020 г.
- ^ Данн Л.Л., Сурьо Рахманто Ю., Ричардсон Д.Р. (февраль 2007 г.). «Поглощение железа и метаболизм в новом тысячелетии». Тенденции в клеточной биологии . 17 (2): 93–100. дои : 10.1016/j.tcb.2006.12.003 . ПМИД 17194590 .
- ^ Jump up to: а б Альбертс Б., Джонсон А., Льюис Дж., Рафф М., Робертс К., Уолтер П. (2002). «Как клетки получают энергию из пищи». Молекулярная биология клетки (4-е изд.). Архивировано из оригинала 5 июля 2021 года . Проверено 25 июня 2020 г. - через NCBI.
- ^ Рэйвен Дж. (3 сентября 2009 г.). «Вклад аноксигенной и оксигенной фототрофии и хемолитотрофии в потоки углерода и кислорода в водной среде» . Водная микробная экология . 56 : 177–192. дои : 10.3354/ame01315 . ISSN 0948-3055 . Архивировано из оригинала 25 июня 2020 года . Проверено 25 июня 2020 г.
- ^ Jump up to: а б Нельсон Н., Бен-Шем А. (декабрь 2004 г.). «Сложная архитектура кислородного фотосинтеза». Обзоры природы. Молекулярно-клеточная биология . 5 (12): 971–82. дои : 10.1038/nrm1525 . ПМИД 15573135 . S2CID 5686066 .
- ^ Мэдиган М.Т., Мартинко Дж.М. (2006). Микробиология Брока (11-е, исправленное изд.). Мюнхен: исследования Пирсона. стр. 604, 621. ISBN. 3-8273-7187-2 . OCLC 162303067 .
- ^ Демирель Ю. (2016). Энергия: производство, преобразование, хранение, сохранение и соединение (Второе изд.). Линкольн: Спрингер. п. 431. ИСБН 978-3-319-29650-0 . OCLC 945435943 .
- ^ Хезе CC, Финкельштейн Р.А. (декабрь 1993 г.). «Бактериальные внеклеточные цинксодержащие металлопротеазы» . Микробиологические обзоры . 57 (4): 823–37. дои : 10.1128/MMBR.57.4.823-837.1993 . ПМК 372940 . ПМИД 8302217 .
- ^ Гупта Р., Гупта Н., Рати П. (июнь 2004 г.). «Бактериальные липазы: обзор производства, очистки и биохимических свойств». Прикладная микробиология и биотехнология . 64 (6): 763–81. дои : 10.1007/s00253-004-1568-8 . ПМИД 14966663 . S2CID 206934353 .
- ^ Хойл Т. (1997). «Пищеварительная система: связь теории и практики». Британский журнал медсестер . 6 (22): 1285–91. дои : 10.12968/bjon.1997.6.22.1285 . ПМИД 9470654 .
- ^ Суба В.В., Пачитти А.Дж. (1992). «Как аминокислоты попадают в клетки: механизмы, модели, меню и медиаторы». Журнал парентерального и энтерального питания . 16 (6): 569–78. дои : 10.1177/0148607192016006569 . ПМИД 1494216 .
- ^ Барретт, член парламента, Уолмсли, А.Р., Гулд Г.В. (август 1999 г.). «Структура и функции вспомогательных транспортеров сахара». Современное мнение в области клеточной биологии . 11 (4): 496–502. дои : 10.1016/S0955-0674(99)80072-6 . ПМИД 10449337 .
- ^ Белл Дж.И., Бурант К.Ф., Такеда Дж., Гулд Г.В. (сентябрь 1993 г.). «Структура и функции вспомогательных переносчиков сахара у млекопитающих» . Журнал биологической химии . 268 (26): 19161–4. дои : 10.1016/S0021-9258(19)36489-0 . ПМИД 8366068 .
- ^ Jump up to: а б Буше С., Серди С., Кан С.Р., Goldfine AB (октябрь 2004 г.). «Клеточная судьба глюкозы и ее значение при диабете 2 типа» . Эндокринные обзоры . 25 (5): 807–30. дои : 10.1210/er.2003-0026 . ПМИД 15466941 .
- ^ Альфарук К.О., Вердуско Д., Раух С., Муддатир А.К., Адиль Х.Х., Эльхассан Г.О. и др. (18 декабря 2014 г.). «Гликолиз, метаболизм опухоли, рост и распространение рака. Новая этиопатогенетическая перспектива на основе pH и терапевтический подход к старому вопросу рака» . Онсознание . 1 (12): 777–802. doi : 10.18632/oncoscience.109 . ПМК 4303887 . ПМИД 25621294 .
- ^ Крюгер, Николас Дж; фон Шавен, Антье (2003). «Окислительный пентозофосфатный путь: структура и организация». Современное мнение в области биологии растений . 6 (3): 236–246. Бибкод : 2003COPB....6..236K . дои : 10.1016/S1369-5266(03)00039-6 . ПМИД 12753973 .
- ^ Випперман М.Ф., Сэмпсон Н.С., Томас С.Т. (2014). «Патоген оидной ярости: утилизация холестерина микобактериями туберкулеза» . Критические обзоры по биохимии и молекулярной биологии . 49 (4): 269–93. дои : 10.3109/10409238.2014.895700 . ПМЦ 4255906 . ПМИД 24611808 .
- ^ Саками В., Харрингтон Х (1963). «Метаболизм аминокислот». Ежегодный обзор биохимии . 32 : 355–98. дои : 10.1146/annurev.bi.32.070163.002035 . ПМИД 14144484 .
- ^ Броснан Дж. Т. (апрель 2000 г.). «Глутамат на стыке обмена аминокислот и углеводов» . Журнал питания . 130 (дополнение 4S): 988S–90S. дои : 10.1093/jn/130.4.988S . ПМИД 10736367 .
- ^ Янг В.Р., Аджами А.М. (сентябрь 2001 г.). «Глютамин: император или его одежда?» . Журнал питания . 131 (9 Suppl): 2449S–59S, обсуждение 2486S–7S. дои : 10.1093/jn/131.9.2449S . ПМИД 11533293 .
- ^ Хослер Дж.П., Фергюсон-Миллер С., Миллс Д.А. (2006). «Трансдукция энергии: перенос протонов через дыхательные комплексы» . Ежегодный обзор биохимии . 75 : 165–87. doi : 10.1146/annurev.biochem.75.062003.101730 . ПМЦ 2659341 . ПМИД 16756489 .
- ^ Шульц Б.Е., Чан С.И. (2001). «Структуры и стратегии перекачки протонов митохондриальных дыхательных ферментов» (PDF) . Ежегодный обзор биофизики и биомолекулярной структуры . 30 :23–65. doi : 10.1146/annurev.biophys.30.1.23 . ПМИД 11340051 . Архивировано (PDF) из оригинала 22 января 2020 г. Проверено 11 ноября 2019 г.
- ^ Капальди Р.А., Аггелер Р. (март 2002 г.). «Механизм АТФ-синтазы F (1) F (0)-типа, биологического вращательного двигателя». Тенденции биохимических наук . 27 (3): 154–60. дои : 10.1016/S0968-0004(01)02051-5 . ПМИД 11893513 .
- ^ Фридрих Б., Шварц Э. (1993). «Молекулярная биология утилизации водорода аэробными хемолитотрофами». Ежегодный обзор микробиологии . 47 : 351–83. дои : 10.1146/annurev.mi.47.100193.002031 . ПМИД 8257102 .
- ^ Вебер К.А., Ахенбах Л.А., Коутс Дж.Д. (октябрь 2006 г.). «Микроорганизмы, перекачивающие железо: анаэробное микробное окисление и восстановление железа» . Обзоры природы. Микробиология . 4 (10): 752–64. дои : 10.1038/nrmicro1490 . ПМИД 16980937 . S2CID 8528196 . Архивировано из оригинала 2 мая 2019 года . Проверено 6 октября 2019 г.
- ^ Джеттен М.С., Страус М., ван де Пас-Шоонен К.Т., Шалк Дж., ван Донген У.Г., ван де Грааф А.А. и др. (декабрь 1998 г.). «Анаэробное окисление аммония» . Обзоры микробиологии FEMS . 22 (5): 421–37. дои : 10.1111/j.1574-6976.1998.tb00379.x . ПМИД 9990725 .
- ^ Саймон Дж. (август 2002 г.). «Энзимология и биоэнергетика дыхательной аммонификации нитритов» . Обзоры микробиологии FEMS . 26 (3): 285–309. дои : 10.1111/j.1574-6976.2002.tb00616.x . ПМИД 12165429 .
- ^ Конрад Р. (декабрь 1996 г.). «Почвенные микроорганизмы как регуляторы атмосферных микроэлементов (H2, CO, CH4, OCS, N2O и NO)» . Микробиологические обзоры . 60 (4): 609–40. дои : 10.1128/MMBR.60.4.609-640.1996 . ПМК 239458 . ПМИД 8987358 .
- ^ Бареа Х.М., Посо М.Дж., Азкон Р., Азкон-Агилар К. (июль 2005 г.). «Микробное сотрудничество в ризосфере» . Журнал экспериментальной ботаники . 56 (417): 1761–78. дои : 10.1093/jxb/eri197 . ПМИД 15911555 .
- ^ ван дер Меер М.Т., Схоутен С., Бейтсон М.М., Нюбель У., Виланд А., Кюль М. и др. (июль 2005 г.). «Суточные вариации углеродного метаболизма зелеными несероподобными бактериями в щелочных кремнистых микробных матах горячих источников из Йеллоустонского национального парка» . Прикладная и экологическая микробиология . 71 (7): 3978–86. Бибкод : 2005ApEnM..71.3978V . дои : 10.1128/АЕМ.71.7.3978-3986.2005 . ПМК 1168979 . ПМИД 16000812 .
- ^ Тичи М.А., Табита Ф.Р. (ноябрь 2001 г.). «Интерактивный контроль окислительно-восстановительных систем Rhodobacter capsulatus во время фототрофного метаболизма» . Журнал бактериологии . 183 (21): 6344–54. дои : 10.1128/JB.183.21.6344-6354.2001 . ПМК 100130 . ПМИД 11591679 .
- ^ Альбертс Б., Джонсон А., Льюис Дж., Рафф М., Робертс К., Уолтер П. (2002). «Преобразование энергии: митохондрии и хлоропласты». Молекулярная биология клетки (4-е изд.). Архивировано из оригинала 15 декабря 2020 года . Проверено 3 июля 2020 г.
- ^ Аллен Дж. П., Уильямс Дж. К. (октябрь 1998 г.). «Фотосинтетические реакционные центры». Письма ФЭБС . 438 (1–2): 5–9. Бибкод : 1998FEBSL.438....5A . дои : 10.1016/S0014-5793(98)01245-9 . ПМИД 9821949 . S2CID 21596537 .
- ^ Мунекаге И., Хашимото М., Мияке С., Томизава К., Эндо Т., Тасака М., Шиканай Т. (июнь 2004 г.). «Циклический поток электронов вокруг фотосистемы I необходим для фотосинтеза». Природа . 429 (6991): 579–82. Бибкод : 2004Natur.429..579M . дои : 10.1038/nature02598 . ПМИД 15175756 . S2CID 4421776 .
- ^ Jump up to: а б Мандал А (26 ноября 2009 г.). «Что такое анаболизм?» . Новости-Medical.net . Архивировано из оригинала 5 июля 2020 года . Проверено 4 июля 2020 г.
- ^ Мизиорко Х.М., Лоример Г.Х. (1983). «Рибулозо-1,5-бисфосфаткарбоксилаза-оксигеназа». Ежегодный обзор биохимии . 52 : 507–35. дои : 10.1146/annurev.bi.52.070183.002451 . ПМИД 6351728 .
- ^ Додд А.Н., Борланд А.М., Хаслам Р.П., Гриффитс Х., Максвелл К. (апрель 2002 г.). «Обмен толстянковых кислот: пластичный, фантастический» . Журнал экспериментальной ботаники . 53 (369): 569–80. дои : 10.1093/jexbot/53.369.569 . ПМИД 11886877 .
- ^ Хюглер М., Вирсен К.О., Фукс Г., Тейлор К.Д., Зиверт С.М. (май 2005 г.). «Доказательства автотрофной фиксации CO2 посредством восстановительного цикла трикарбоновых кислот членами эпсилон-подразделения протеобактерий» . Журнал бактериологии . 187 (9): 3020–7. дои : 10.1128/JB.187.9.3020-3027.2005 . ПМК 1082812 . ПМИД 15838028 .
- ^ Штраус Г., Фукс Г. (август 1993 г.). «Ферменты нового пути автотрофной фиксации CO2 у фототрофной бактерии Chloroflexus aurantiacus, 3-гидроксипропионатного цикла» . Европейский журнал биохимии . 215 (3): 633–43. дои : 10.1111/j.1432-1033.1993.tb18074.x . ПМИД 8354269 .
- ^ Вуд Х.Г. (февраль 1991 г.). «Жизнь с CO или CO2 и H2 как источник углерода и энергии» . Журнал ФАСЭБ . 5 (2): 156–63. дои : 10.1096/fasebj.5.2.1900793 . ПМИД 1900793 . S2CID 45967404 .
- ^ Шивели Дж. М., ван Кеулен Г., Мейер В. Г. (1998). «Что-то из почти ничего: фиксация углекислого газа у хемоавтотрофов». Ежегодный обзор микробиологии . 52 : 191–230. дои : 10.1146/аннурев.микро.52.1.191 . ПМИД 9891798 .
- ^ Бойте А., Хесс Б. (июнь 1981 г.). «Дизайн гликолиза» . Философские труды Лондонского королевского общества. Серия Б, Биологические науки . 293 (1063): 5–22. Бибкод : 1981РСТБ.293....5Б . дои : 10.1098/rstb.1981.0056 . ПМИД 6115423 .
- ^ Пилкис С.Дж., Эль-Маграби М.Р., Клаус Т.Х. (июнь 1990 г.). «Фруктозо-2,6-бисфосфат в контроле глюконеогенеза в печени. От метаболитов к молекулярной генетике». Уход при диабете . 13 (6): 582–99. дои : 10.2337/diacare.13.6.582 . ПМИД 2162755 . S2CID 44741368 .
- ^ Jump up to: а б Прапорщик SA (июль 2006 г.). «Возврат к глиоксилатному циклу: альтернативные пути микробной ассимиляции ацетата» . Молекулярная микробиология . 61 (2): 274–6. дои : 10.1111/j.1365-2958.2006.05247.x . ПМИД 16856935 . S2CID 39986630 .
- ^ Финн П.Ф., Дайс Дж.Ф. (2006). «Протеолитические и липолитические реакции на голодание». Питание . 22 (7–8): 830–44. дои : 10.1016/j.nut.2006.04.008 . ПМИД 16815497 .
- ^ Jump up to: а б Корнберг Х.Л., Кребс Х.А. (май 1957 г.). «Синтез компонентов клетки из C2-единиц с помощью модифицированного цикла трикарбоновых кислот». Природа . 179 (4568): 988–91. Бибкод : 1957Natur.179..988K . дои : 10.1038/179988a0 . ПМИД 13430766 . S2CID 40858130 .
- ^ Эванс Р.Д., Хизер Л.К. (июнь 2016 г.). «Метаболические пути и нарушения» . Хирургия (Оксфорд) . 34 (6): 266–272. дои : 10.1016/j.mpsur.2016.03.010 . ISSN 0263-9319 . S2CID 87884121 . Архивировано из оригинала 31 октября 2020 года . Проверено 28 августа 2020 г.
- ^ Фриз Х.Х., Харт Г.В., Шнаар Р.Л. (2015). «Предшественники гликозилирования». В Варки А., Каммингс Р.Д., Эско Дж.Д., Стэнли П. (ред.). Основы гликобиологии (3-е изд.). Колд-Спринг-Харбор (Нью-Йорк): Лабораторное издательство Колд-Спринг-Харбор. doi : 10.1101/glycobiology.3e.005 (неактивен 31 января 2024 г.). ПМИД 28876856 . Архивировано из оригинала 24 февраля 2022 года . Проверено 8 июля 2020 г.
{{cite book}}: CS1 maint: DOI неактивен по состоянию на январь 2024 г. ( ссылка ) - ^ Опденаккер Г., Радд П.М., Понтинг К.П., Двек Р.А. (ноябрь 1993 г.). «Концепции и принципы гликобиологии» . Журнал ФАСЭБ . 7 (14): 1330–7. дои : 10.1096/fasebj.7.14.8224606 . ПМИД 8224606 . S2CID 10388991 .
- ^ МакКонвилл М.Дж., Менон А.К. (2000). «Новейшие достижения в клеточной биологии и биохимии гликозилфосфатидилинозитоллипидов (обзор)» . Молекулярная мембранная биология . 17 (1): 1–16. дои : 10.1080/096876800294443 . ПМИД 10824734 .
- ^ Чирала С.С., Вакил С.Дж. (ноябрь 2004 г.). «Структура и функция синтазы жирных кислот животных». Липиды . 39 (11): 1045–53. дои : 10.1007/s11745-004-1329-9 . ПМИД 15726818 . S2CID 4043407 .
- ^ Уайт С.В., Чжэн Дж., Чжан Ю.М. (2005). «Структурная биология биосинтеза жирных кислот II типа». Ежегодный обзор биохимии . 74 : 791–831. doi : 10.1146/annurev.biochem.74.082803.133524 . ПМИД 15952903 .
- ^ Олрогге Дж.Б., Яворски Дж.Г. (июнь 1997 г.). «Регуляция синтеза жирных кислот». Ежегодный обзор физиологии растений и молекулярной биологии растений . 48 : 109–136. дои : 10.1146/annurev.arplant.48.1.109 . ПМИД 15012259 . S2CID 46348092 .
- ^ Дубей В.С., Бхалла Р., Лутра Р. (сентябрь 2003 г.). «Обзор немевалонатного пути биосинтеза терпеноидов в растениях» (PDF) . Журнал биологических наук . 28 (5): 637–46. дои : 10.1007/BF02703339 . ПМИД 14517367 . S2CID 27523830 . Архивировано из оригинала (PDF) 15 апреля 2007 года.
- ^ Jump up to: а б Кузуяма Т., Сето Х (апрель 2003 г.). «Разнообразие биосинтеза изопреновых единиц». Отчеты о натуральных продуктах . 20 (2): 171–83. дои : 10.1039/b109860h . ПМИД 12735695 .
- ^ Гроховски Л.Л., Сюй Х., Уайт Р.Х. (май 2006 г.). «Methanocaldococcus jannaschii использует модифицированный мевалонатный путь для биосинтеза изопентенилдифосфата» . Журнал бактериологии . 188 (9): 3192–8. дои : 10.1128/JB.188.9.3192-3198.2006 . ПМЦ 1447442 . ПМИД 16621811 .
- ^ Лихтенталер Гонконг (июнь 1999 г.). «1-дезокси-D-ксилулозо-5-фосфатный путь биосинтеза изопреноидов в растениях». Ежегодный обзор физиологии растений и молекулярной биологии растений . 50 : 47–65. doi : 10.1146/annurev.arplant.50.1.47 . ПМИД 15012203 .
- ^ Jump up to: а б Шрёпфер Г.Дж. (1981). «Биосинтез стерола». Ежегодный обзор биохимии . 50 : 585–621. дои : 10.1146/annurev.bi.50.070181.003101 . ПМИД 7023367 .
- ^ Лиз Н.Д., Скэггс Б., Кирш Д.Р., Бард М. (март 1995 г.). «Клонирование поздних генов пути биосинтеза эргостерина Saccharomyces cerevisiae - обзор». Липиды . 30 (3): 221–6. дои : 10.1007/BF02537824 . ПМИД 7791529 . S2CID 4019443 .
- ^ Химмельрайх Р., Гильберт Х., Плагенс Х., Пиркл Э., Ли Б.К., Херрманн Р. (ноябрь 1996 г.). «Полный анализ последовательности генома бактерии Mycoplasma pneumoniae» . Исследования нуклеиновых кислот . 24 (22): 4420–49. дои : 10.1093/нар/24.22.4420 . ПМК 146264 . ПМИД 8948633 .
- ^ Гайтон AC, Холл JE (2006). Учебник медицинской физиологии . Филадельфия: Эльзевир. стр. 855 –6. ISBN 978-0-7216-0240-0 .
- ^ Ибба М., Сёлль Д. (май 2001 г.). «Ренессанс синтеза аминоацил-тРНК» . Отчеты ЭМБО . 2 (5): 382–7. doi : 10.1093/embo-reports/kve095 . ПМЦ 1083889 . ПМИД 11375928 . Архивировано из оригинала 1 мая 2011 года.
- ^ Лендьел П., Сёлль Д. (июнь 1969 г.). «Механизм биосинтеза белка» . Бактериологические обзоры . 33 (2): 264–301. дои : 10.1128/ММБР.33.2.264-301.1969 . ПМК 378322 . ПМИД 4896351 .
- ^ Jump up to: а б Рудольф Ф.Б. (январь 1994 г.). «Биохимия и физиология нуклеотидов» . Журнал питания . 124 (1 доп.): 124S–127S. дои : 10.1093/jn/124.suppl_1.124S . ПМИД 8283301 . Зреннер Р., Ститт М., Зонневальд У., Болдт Р. (2006). «Биосинтез и деградация пиримидинов и пуринов в растениях». Ежегодный обзор биологии растений . 57 : 805–36. doi : 10.1146/annurev.arplant.57.032905.105421 . ПМИД 16669783 .
- ^ Стасолла С., Катахира Р., Торп Т.А., Ашихара Х. (ноябрь 2003 г.). «Обмен пуриновых и пиримидиновых нуклеотидов у высших растений». Журнал физиологии растений . 160 (11): 1271–95. Бибкод : 2003JPPhy.160.1271S . дои : 10.1078/0176-1617-01169 . ПМИД 14658380 .
- ^ Дэвис О., Мендес П., Смоллбоун К., Малис Н. (апрель 2012 г.). «Характеристика множественных субстрат-специфичных (d)ITP/(d)XTPase и моделирование метаболизма дезаминированных пуриновых нуклеотидов» (PDF) . Отчеты БМБ . 45 (4): 259–64. дои : 10.5483/BMBRep.2012.45.4.259 . ПМИД 22531138 . Архивировано (PDF) из оригинала 24 октября 2020 г. Проверено 18 сентября 2019 г.
- ^ Смит Дж.Л. (декабрь 1995 г.). «Ферменты синтеза нуклеотидов». Современное мнение в области структурной биологии . 5 (6): 752–7. дои : 10.1016/0959-440X(95)80007-7 . ПМИД 8749362 .
- ^ Теста Б, Кремер С.Д. (октябрь 2006 г.). «Биохимия метаболизма лекарств. Введение: часть 1. Принципы и обзор». Химия и биоразнообразие . 3 (10): 1053–101. дои : 10.1002/cbdv.200690111 . ПМИД 17193224 . S2CID 28872968 .
- ^ Дэниелсон П.Б. (декабрь 2002 г.). «Суперсемейство цитохрома P450: биохимия, эволюция и метаболизм лекарств у человека». Современный метаболизм лекарств . 3 (6): 561–97. дои : 10.2174/1389200023337054 . ПМИД 12369887 .
- ^ Кинг К.Д., Риос Г.Р., Грин М.Д., Тефли Т.Р. (сентябрь 2000 г.). «УДФ-глюкуронозилтрансферазы». Современный метаболизм лекарств . 1 (2): 143–61. дои : 10.2174/1389200003339171 . ПМИД 11465080 .
- ^ Шихан Д., Мид Дж., Фоли В.М., Дауд Калифорния (ноябрь 2001 г.). «Структура, функции и эволюция глутатионтрансфераз: значение для классификации представителей древнего суперсемейства ферментов, не относящихся к млекопитающим» . Биохимический журнал . 360 (Часть 1): 1–16. дои : 10.1042/0264-6021:3600001 . ПМК 1222196 . ПМИД 11695986 .
- ^ Гальван Т.К., Мон В.В., де Лоренцо V (октябрь 2005 г.). «Изучение генофонда микробной биодеградации и биотрансформации». Тенденции в биотехнологии . 23 (10): 497–506. дои : 10.1016/j.tibtech.2005.08.002 . ПМИД 16125262 .
- ^ Янссен Д.Б., Динкла И.Ю., Поеларендс Г.Дж., Терпстра П. (декабрь 2005 г.). «Бактериальная деградация ксенобиотических соединений: эволюция и распространение новых ферментных активностей» (PDF) . Экологическая микробиология . 7 (12): 1868–82. Бибкод : 2005EnvMi...7.1868J . дои : 10.1111/j.1462-2920.2005.00966.x . ПМИД 16309386 . Архивировано (PDF) из оригинала 11 ноября 2019 года . Проверено 11 ноября 2019 г.
- ^ Дэвис К.Дж. (1995). «Окислительный стресс: парадокс аэробной жизни». Симпозиум Биохимического общества . 61 : 1–31. дои : 10.1042/bss0610001 . ПМИД 8660387 .
- ^ Ту Б.П., Вайсман Дж.С. (февраль 2004 г.). «Окислительное сворачивание белков у эукариот: механизмы и последствия» . Журнал клеточной биологии . 164 (3): 341–6. дои : 10.1083/jcb.200311055 . ПМЦ 2172237 . ПМИД 14757749 .
- ^ Сис Х (март 1997 г.). «Окислительный стресс: оксиданты и антиоксиданты» . Экспериментальная физиология . 82 (2): 291–5. doi : 10.1113/expphysicalol.1997.sp004024 . ПМИД 9129943 . S2CID 20240552 .
- ^ Вертуани С., Ангусти А., Манфредини С. (2004). «Сеть антиоксидантов и проантиоксидантов: обзор». Текущий фармацевтический дизайн . 10 (14): 1677–94. дои : 10.2174/1381612043384655 . ПМИД 15134565 . S2CID 43713549 .
- ^ фон Стокар У, Лю Дж (август 1999 г.). «Всегда ли микробная жизнь питается отрицательной энтропией? Термодинамический анализ роста микробов» . Biochimica et Biophysica Acta (BBA) — Биоэнергетика . 1412 (3): 191–211. дои : 10.1016/S0005-2728(99)00065-1 . ПМИД 10482783 .
- ^ Демирель Ю., Сэндлер С.И. (июнь 2002 г.). «Термодинамика и биоэнергетика» . Биофизическая химия . 97 (2–3): 87–111. дои : 10.1016/S0301-4622(02)00069-8 . ПМИД 12050002 . S2CID 3754065 . Архивировано из оригинала 4 августа 2020 года . Проверено 22 сентября 2019 г.
- ^ Альберт Р. (ноябрь 2005 г.). «Безмасштабные сети в клеточной биологии». Журнал клеточной науки . 118 (Часть 21): 4947–57. arXiv : q-bio/0510054 . Бибкод : 2005q.bio....10054A . дои : 10.1242/jcs.02714 . ПМИД 16254242 . S2CID 3001195 .
- ^ Бренд MD (январь 1997 г.). «Анализ регуляции энергетического обмена» . Журнал экспериментальной биологии . 200 (Часть 2): 193–202. дои : 10.1242/jeb.200.2.193 . ПМИД 9050227 . Архивировано из оригинала 29 марта 2007 года . Проверено 12 марта 2007 г.
- ^ Сойер О.С., Салате М., Бонхеффер С. (январь 2006 г.). «Сети передачи сигналов: топология, реакция и биохимические процессы». Журнал теоретической биологии . 238 (2): 416–25. Бибкод : 2006JThBi.238..416S . дои : 10.1016/j.jtbi.2005.05.030 . ПМИД 16045939 .
- ^ Jump up to: а б Солтер М., Ноулз Р.Г., Погсон К.И. (1994). «Метаболический контроль». Очерки по биохимии . 28 : 1–12. ПМИД 7925313 .
- ^ Вестерхофф Х.В., Гроен А.К., Вандерс Р.Дж. (январь 1984 г.). «Современные теории метаболического контроля и их приложения (обзор)». Отчеты по биологическим наукам . 4 (1): 1–22. дои : 10.1007/BF01120819 . ПМИД 6365197 . S2CID 27791605 .
- ^ Фелл Д.А., Томас С. (октябрь 1995 г.). «Физиологический контроль метаболического потока: необходимость многосайтовой модуляции» . Биохимический журнал . 311 (Часть 1): 35–9. дои : 10.1042/bj3110035 . ПМК 1136115 . ПМИД 7575476 .
- ^ Хендриксон, В.А. (ноябрь 2005 г.). «Передача биохимических сигналов через клеточные мембраны». Ежеквартальные обзоры биофизики . 38 (4): 321–30. дои : 10.1017/S0033583506004136 . ПМИД 16600054 . S2CID 39154236 .
- ^ Коэн П. (декабрь 2000 г.). «Регуляция функции белка путем многосайтового фосфорилирования - обновление за 25 лет». Тенденции биохимических наук . 25 (12): 596–601. дои : 10.1016/S0968-0004(00)01712-6 . ПМИД 11116185 .
- ^ Линхард Г.Е., Слот Дж.В., Джеймс Д.Е., Мюклер М.М. (январь 1992 г.). «Как клетки поглощают глюкозу». Научный американец . 266 (1): 86–91. Бибкод : 1992SciAm.266a..86L . doi : 10.1038/scientificamerican0192-86 . ПМИД 1734513 .
- ^ Роуч Пи Джей (март 2002 г.). «Гликоген и его метаболизм». Современная молекулярная медицина . 2 (2): 101–20. дои : 10.2174/1566524024605761 . ПМИД 11949930 .
- ^ Ньюгард CB, Брэди М.Дж., О'Доэрти Р.М., Салтиел А.Р. (декабрь 2000 г.). «Организация утилизации глюкозы: новая роль субъединиц протеинфосфатазы-1, нацеленных на гликоген» (PDF) . Диабет . 49 (12): 1967–77. дои : 10.2337/диабет.49.12.1967 . ПМИД 11117996 . Архивировано (PDF) из оригинала 19 июня 2007 года . Проверено 25 марта 2007 г.
- ^ Романо А.Х., Конвей Т. (1996). «Эволюция путей метаболизма углеводов» . Исследования в области микробиологии . 147 (6–7): 448–55. дои : 10.1016/0923-2508(96)83998-2 . ПМИД 9084754 .
- ^ Кох А (1998). Как появились бактерии? . Достижения микробной физиологии. Том. 40. С. 353–99. дои : 10.1016/S0065-2911(08)60135-6 . ISBN 978-0-12-027740-7 . ПМИД 9889982 .
{{cite book}}:|journal=игнорируется ( помогите ) - ^ Узунис С., Кирпидес Н. (июль 1996 г.). «Появление основных клеточных процессов в эволюции» . Письма ФЭБС . 390 (2): 119–23. Бибкод : 1996FEBSL.390..119O . дои : 10.1016/0014-5793(96)00631-X . ПМИД 8706840 . S2CID 39128865 .
- ^ Каэтано-Аноллес Дж., Ким Х.С., Миттенталь Дж.Е. (май 2007 г.). «Происхождение современных метаболических сетей, выведенное на основе филогеномного анализа белковой архитектуры» . Труды Национальной академии наук Соединенных Штатов Америки . 104 (22): 9358–63. Бибкод : 2007PNAS..104.9358C . дои : 10.1073/pnas.0701214104 . ПМК 1890499 . ПМИД 17517598 .
- ^ Шмидт С., Сюняев С., Борк П., Дандекар Т. (июнь 2003 г.). «Метаболиты: рука помощи в эволюции пути?». Тенденции биохимических наук . 28 (6): 336–41. дои : 10.1016/S0968-0004(03)00114-2 . ПМИД 12826406 .
- ^ Лайт С., Краулис П. (февраль 2004 г.). «Сетевой анализ эволюции метаболических ферментов Escherichia coli» . БМК Биоинформатика . 5:15 . дои : 10.1186/1471-2105-5-15 . ПМК 394313 . ПМИД 15113413 . Алвес Р., Шалей Р.А., Штернберг М.Ю. (июль 2002 г.). «Эволюция ферментов метаболизма: сетевая перспектива». Журнал молекулярной биологии . 320 (4): 751–70. дои : 10.1016/S0022-2836(02)00546-6 . ПМИД 12095253 .
- ^ Ким Х.С., Миттенталь Дж.Э., Каэтано-Аноллес Дж. (июль 2006 г.). «MANET: отслеживание эволюции белковой архитектуры в метаболических сетях» . БМК Биоинформатика . 7 : 351. дои : 10.1186/1471-2105-7-351 . ПМЦ 1559654 . ПМИД 16854231 .
- ^ Тейхманн С.А., Райсон С.С., Торнтон Дж.М., Райли М., Гоф Дж., Чотия С. (декабрь 2001 г.). «Низкомолекулярный метаболизм: ферментативная мозаика». Тенденции в биотехнологии . 19 (12): 482–6. дои : 10.1016/S0167-7799(01)01813-3 . ПМИД 11711174 .
- ^ Спирин В., Гельфанд М.С., Миронов А.А., Мирный Л.А. (июнь 2006 г.). «Метаболическая сеть в эволюционном контексте: многоуровневая структура и модульность» . Труды Национальной академии наук Соединенных Штатов Америки . 103 (23): 8774–9. Бибкод : 2006PNAS..103.8774S . дои : 10.1073/pnas.0510258103 . ПМЦ 1482654 . ПМИД 16731630 .
- ^ Лоуренс Дж.Г. (декабрь 2005 г.). «Общие темы в геномных стратегиях патогенов». Текущее мнение в области генетики и развития . 15 (6): 584–8. дои : 10.1016/j.где.2005.09.007 . ПМИД 16188434 . Вернегрин Джей-Джей (декабрь 2005 г.). «К лучшему или к худшему: геномные последствия внутриклеточного мутуализма и паразитизма». Текущее мнение в области генетики и развития . 15 (6): 572–83. дои : 10.1016/j.где.2005.09.013 . ПМИД 16230003 .
- ^ Пал С., Папп Б., Лерчер М.Дж., Чермели П., Оливер С.Г., Херст Л.Д. (март 2006 г.). «Шанс и необходимость в эволюции минимальных метаболических сетей». Природа . 440 (7084): 667–70. Бибкод : 2006Natur.440..667P . дои : 10.1038/nature04568 . ПМИД 16572170 . S2CID 4424895 .
- ^ Ренни MJ (ноябрь 1999 г.). «Введение в использование индикаторов в питании и обмене веществ» . Труды Общества питания . 58 (4): 935–44. дои : 10.1017/S002966519900124X . ПМИД 10817161 .
- ^ Файр Р.Д. (декабрь 1997 г.). «Разработка кинетических моделей в нелинейном мире молекулярно-клеточной биологии» . Метаболизм . 46 (12): 1489–95. дои : 10.1016/S0026-0495(97)90154-2 . ПМИД 9439549 .
- ^ Стерк Л., Ромбаутс С., Вандеполе К., Рузе П., Ван де Пер Ю. (апрель 2007 г.). «Сколько генов у растений (... и почему они там)?». Современное мнение в области биологии растений . 10 (2): 199–203. дои : 10.1016/j.pbi.2007.01.004 . ПМИД 17289424 .
- ^ Бородина И., Нильсен Дж. (июнь 2005 г.). «От геномов к клеткам in silico через метаболические сети». Современное мнение в области биотехнологии . 16 (3): 350–5. doi : 10.1016/j.copbio.2005.04.008 . ПМИД 15961036 .
- ^ Джанчандани Э.П., Бротиган Д.Л., Папин Дж.А. (май 2006 г.). «Системный анализ характеризует интегрированные функции биохимических сетей». Тенденции биохимических наук . 31 (5): 284–91. дои : 10.1016/j.tibs.2006.03.007 . ПМИД 16616498 .
- ^ Дуарте Н.К., Беккер С.А., Джамшиди Н., Тиле И., Мо М.Л., Во Т.Д. и др. (февраль 2007 г.). «Глобальная реконструкция метаболической сети человека на основе геномных и библиомных данных» . Труды Национальной академии наук Соединенных Штатов Америки . 104 (6): 1777–82. Бибкод : 2007PNAS..104.1777D . дои : 10.1073/pnas.0610772104 . ПМК 1794290 . ПМИД 17267599 .
- ^ Го К.И., Кьюсик М.Е., Валле Д., Чайлдс Б., Видал М., Барабаси А.Л. (май 2007 г.). «Сеть болезней человека» . Труды Национальной академии наук Соединенных Штатов Америки . 104 (21): 8685–90. Бибкод : 2007PNAS..104.8685G . дои : 10.1073/pnas.0701361104 . ПМЦ 1885563 . ПМИД 17502601 .
- ^ Ли Д.С., Пак Дж., Кей К.А., Кристакис Н.А., Олваи З.Н., Барабаси А.Л. (июль 2008 г.). «Влияние топологии метаболической сети человека на сопутствующие заболевания» . Труды Национальной академии наук Соединенных Штатов Америки . 105 (29): 9880–5. Бибкод : 2008PNAS..105.9880L . дои : 10.1073/pnas.0802208105 . ПМЦ 2481357 . ПМИД 18599447 .
- ^ Чете М., Дойл Дж. (сентябрь 2004 г.). «Галстуки-бабочки, обмен веществ и болезни». Тенденции в биотехнологии . 22 (9): 446–50. дои : 10.1016/j.tibtech.2004.07.007 . ПМИД 15331224 .
- ^ Ма Х.В., Цзэн А.П. (июль 2003 г.). «Структура связности, гигантский сильный компонент и центральность метаболических сетей». Биоинформатика . 19 (11): 1423–30. CiteSeerX 10.1.1.605.8964 . doi : 10.1093/биоинформатика/btg177 . ПМИД 12874056 .
- ^ Чжао Дж., Ю Х., Луо Дж.Х., Цао З.В., Ли Ю.С. (август 2006 г.). «Иерархическая модульность вложенных галстуков-бабочек в метаболических сетях» . БМК Биоинформатика . 7 : 386. arXiv : q-bio/0605003 . Бибкод : 2006q.bio.....5003Z . дои : 10.1186/1471-2105-7-386 . ПМК 1560398 . ПМИД 16916470 .
- ^ «Макромолекулы: питательные вещества, метаболизм и пищеварительные процессы | Виртуальная средняя школа — KeepNotes» . Keepnotes.com . Проверено 29 декабря 2023 г.
- ^ Тикаер Дж., Нильсен Дж. (январь 2003 г.). «Метаболическая инженерия производства бета-лактамов». Метаболическая инженерия . 5 (1): 56–69. дои : 10.1016/S1096-7176(03)00003-X . ПМИД 12749845 .
- ^ Гонсалес-Пахуэло М., Мейньяль-Сальес И., Мендес Ф., Андраде Х.К., Васконселос И., Сукай П. (2005). «Метаболическая инженерия Clostridium acetobutylicum для промышленного производства 1,3-пропандиола из глицерина». Метаболическая инженерия . 7 (5–6): 329–36. дои : 10.1016/j.ymben.2005.06.001 . hdl : 10400.14/3388 . ПМИД 16095939 .
- ^ Кремер М., Бонгертс Дж., Бовенберг Р., Кремер С., Мюллер У., Орф С. и др. (октябрь 2003 г.). «Метаболическая инженерия микробного производства шикимовой кислоты». Метаболическая инженерия . 5 (4): 277–83. дои : 10.1016/j.ymben.2003.09.001 . ПМИД 14642355 .
- ^ Коффас М., Роберж С., Ли К., Стефанопулос Г. (1999). «Метаболическая инженерия». Ежегодный обзор биомедицинской инженерии . 1 : 535–57. doi : 10.1146/annurev.bioeng.1.1.535 . ПМИД 11701499 . S2CID 11814282 .
- ^ «Обмен веществ | Происхождение и значение метаболизма в онлайн-этимологическом словаре» . www.etymonline.com . Архивировано из оригинала 21 сентября 2017 года . Проверено 23 июля 2020 г.
- ^ Леруа, Арман Мари (2014). Лагуна: как Аристотель изобрел науку . Блумсбери. стр. 400–401. ISBN 978-1-4088-3622-4 .
- ^ Аль-Руби А.С. (1982). Ибн ан-Нафис как философ . Симпозиум по Ибн ан-Нафису, Вторая Международная конференция по исламской медицине. Кувейт: Исламская медицинская организация.
- ^ Экноян Г (1999). «Санторио Санкториус (1561-1636) - отец-основатель исследований метаболического баланса». Американский журнал нефрологии . 19 (2): 226–33. дои : 10.1159/000013455 . ПМИД 10213823 . S2CID 32900603 .
- ^ Уильямс Х.А. (1904). Современное развитие химических и биологических наук . История науки: в пяти томах. Том. IV. Нью-Йорк: Харпер и братья. стр. 184–185 . Проверено 26 марта 2007 г.
- ^ Манчестер КЛ (декабрь 1995 г.). «Луи Пастер (1822-1895) - случай и подготовленный ум». Тенденции в биотехнологии . 13 (12): 511–5. дои : 10.1016/S0167-7799(00)89014-9 . ПМИД 8595136 .
- ^ Кинне-Сафран Э., Кинне Р.К. (1999). «Витализм и синтез мочевины. От Фридриха Велера до Ганса А. Кребса» Американский журнал нефрологии . 19 (2): 290–4. дои : 10.1159/000013463 . ПМИД 10213830 . S2CID 71727190 .
- ↑ Эдуарда Бюхнера 1907 года. Нобелевская лекция Архивировано 8 июля 2017 года на Wayback Machine на http://nobelprize.org. Архивировано 5 апреля 2006 года на Wayback Machine. Доступ 20 марта 2007 года.
- ^ Корнберг Х (декабрь 2000 г.). «Кребс и его троица циклов». Обзоры природы. Молекулярно-клеточная биология . 1 (3): 225–8. дои : 10.1038/35043073 . ПМИД 11252898 . S2CID 28092593 .
- ^ Кребс Х.А., Хензелайт К. (1932). «Исследования образования мочевины в организме животных». З. Физиол. Хим . 210 (1–2): 33–66. дои : 10.1515/bchm2.1932.210.1-2.33 .
- ^ Кребс Х.А., Джонсон В.А. (апрель 1937 г.). «Метаболизм кетоновых кислот в тканях животных» . Биохимический журнал . 31 (4): 645–60. дои : 10.1042/bj0310645 . ПМК 1266984 . ПМИД 16746382 .
Дальнейшее чтение
[ редактировать ]Вводный
- Роуз С., Милеушник Р. (1999). Химия жизни . Пингвин Пресс Сайенс. ISBN 0-14-027273-9 .
- Шнайдер ЕС, Саган Д. (2005). В прохладу: поток энергии, термодинамика и жизнь . Издательство Чикагского университета. ISBN 0-226-73936-8 .
- Лейн Н (2004). Кислород: молекула, создавшая мир . США: Издательство Оксфордского университета. ISBN 0-19-860783-0 .
Передовой
- Прайс Н., Стивенс Л. (1999). Основы энзимологии: клеточная и молекулярная биология каталитических белков . Издательство Оксфордского университета. ISBN 0-19-850229-Х .
- Берг Дж., Тимочко Дж., Страйер Л. (2002). Биохимия . WH Фриман и компания. ISBN 0-7167-4955-6 .
- Кокс М., Нельсон Д.Л. (2004). Ленингерские принципы биохимии . Пэлгрейв Макмиллан. ISBN 0-7167-4339-6 .
- Брок Т.Д. , Мэдиган М.Р., Мартинко Дж., Паркер Дж. (2002). Биология микроорганизмов Брока . Бенджамин Каммингс. ISBN 0-13-066271-2 .
- Да Силва Джей-Джей, Уильямс Р.Дж. (1991). Биологическая химия элементов: неорганическая химия жизни . Кларендон Пресс. ISBN 0-19-855598-9 .
- Николлс Д.Г., Фергюсон С.Дж. (2002). Биоэнергетика . Academic Press Inc. ISBN 0-12-518121-3 .
- Вуд Х.Г. (февраль 1991 г.). «Жизнь с CO или CO2 и H2 как источник углерода и энергии» . Журнал ФАСЭБ . 5 (2): 156–63. дои : 10.1096/fasebj.5.2.1900793 . ПМИД 1900793 . S2CID 45967404 .
Внешние ссылки
[ редактировать ]Общая информация
- Биохимия метаболизма (архивировано 8 марта 2005 г.)
- Sparknotes SAT biochemistry Обзор биохимии. Школьный уровень.
- Гиперучебник по биологии Массачусетского технологического института. Архивировано 19 мая 2016 года в Португальском веб-архиве. Руководство по молекулярной биологии для студентов.
Метаболизм человека
- Темы медицинской биохимии. Руководство по метаболическим путям человека. Школьный уровень.
- Страница медицинской биохимии. Комплексный ресурс по метаболизму человека.
Базы данных
- Блок-схема метаболических путей в ExPASy
- Таблица метаболических путей IUBMB-Николсона
- SuperCYP: База данных по метаболизму цитохромов лекарств. Архивировано 3 ноября 2011 г. в Wayback Machine.
Метаболические пути
- Справочник по метаболизму Pathway. Архивировано 23 февраля 2009 г. в Wayback Machine.
- Азотный цикл и фиксация азота на Wayback Machine (индекс архива)
- ^ Биби, Джейн А.; Фрей, Перри А. (1 октября 1998 г.). «Галактозомутаротаза: очистка, характеристика и исследование двух важных остатков гистидина» . Биохимия . 37 (42): 14989–14997. дои : 10.1021/bi9816047 . ISSN 0006-2960 .
