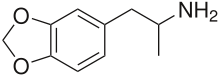
3,4-Метилендиоксиамфетамин
 | |
 | |
| Клинические данные | |
|---|---|
| Маршруты администрация | Перорально, сублингвально, инсуффляционно, внутривенно. |
| код АТС |
|
| Юридический статус | |
| Юридический статус |
|
| Фармакокинетические данные | |
| Метаболизм | Печень ( CYP ) широко вовлечен |
| Экскреция | Реналь |
| Идентификаторы | |
| Номер CAS | |
| ПабХим CID | |
| Лекарственный Банк | |
| ХимическийПаук | |
| НЕКОТОРЫЙ | |
| КЕГГ | |
| ХЭМБЛ | |
| Панель управления CompTox ( EPA ) | |
| Информационная карта ECHA | 100.230.706 |
| Химические и физические данные | |
| Формула | С 10 Н 13 Н О 2 |
| Молярная масса | 179.219 g·mol −1 |
| 3D model ( JSmol ) | |
| | |
3,4-Метилендиоксиамфетамин (также известный как МДА и сасс ) — эмпатоген-энтактоген , психостимулятор и психоделический препарат из семейства амфетаминов , который используется в основном как рекреационный наркотик . По своей фармакологии MDA представляет собой агент, высвобождающий серотонин-норадреналин-дофамин (SNDRA). В большинстве стран наркотик является контролируемым веществом , а его хранение и продажа являются незаконными.
МДА редко используют в качестве рекреационного наркотика по сравнению с другими амфетаминами; однако он по-прежнему широко используется, поскольку является первичным метаболитом, [ 2 ] продукт печеночного N-деалкилирования, [ 3 ] МДМА ( экстази ). Это также распространенная добавка к незаконно производимому МДМА. [ 4 ] [ 5 ]
Использование
[ редактировать ]Медицинский
[ редактировать ]MDA в настоящее время не имеет одобренного медицинского применения.
Рекреационный
[ редактировать ]MDA покупают, продают и используют как рекреационный «наркотик любви» из-за его улучшения настроения и эмпатии . [ 6 ] Рекреационная доза MDA иногда составляет от 100 до 160 мг. [ 7 ]
Побочные эффекты
[ редактировать ]МДА может вызывать серотонинергические нейротоксические эффекты у грызунов. [ 8 ] [ 9 ] Считается, что он активируется начальным метаболизмом MDA. [ 3 ] Кроме того, MDA активирует реакцию нейроглии , хотя после применения она ослабевает. [ 8 ]
Передозировка
[ редактировать ]Симптомы острой токсичности могут включать возбуждение , потливость, повышение артериального давления и частоты сердечных сокращений , резкое повышение температуры тела , судороги и смерть. Смерть обычно наступает в результате сердечного приступа и последующего кровоизлияния в мозг ( инсульт ). [ 10 ] [ нужна медицинская ссылка ]
Фармакология
[ редактировать ]Фармакодинамика
[ редактировать ]MDA является субстратом переносчиков серотонина дофамина , норадреналина , , а и везикулярных моноаминов также TAAR1 агонистом . [ 11 ] и по этим причинам действует как ингибитор обратного захвата и высвобождающий агент серотонина SNDRA , норадреналина и дофамина (то есть, это Tooltip ). [ 12 ] Он также является агонистом серотонина 5-НТ 2А . [ 13 ] 5-ХТ 2Б , [ 14 ] и 5-HT 2C рецепторы [ 15 ] и проявляет сродство к α 2A- , α α 2B- - и HT 2C адренергическим рецепторам и серотониновым 5-HT 1A и 5- 7 рецепторам . [ 16 ]
( S ) -оптический изомер МДА более эффективен, чем ( R ) -оптический изомер , в качестве психостимулятора, обладая большим сродством к трем переносчикам моноаминов .
Что касается субъективных и поведенческих эффектов MDA, считается, что высвобождение серотонина необходимо для его эмпатогенного воздействия, высвобождение дофамина требуется для его эйфорианного ( поощрительного и вызывающего привыкание ) эффекта, высвобождение дофамина и норадреналина необходимо для его психостимулирующего эффекта и прямой агонизм рецептора серотонина 5-HT 2A . Для его мягких психоделических эффектов необходим [ нужна медицинская ссылка ]
Фармакокинетика
[ редактировать ]Сообщается, что продолжительность действия препарата составляет от 6 до 8 часов. [ 7 ]
Химия
[ редактировать ]МДА представляет собой замещенное метилендиоксилированное фенэтиламина и амфетамина производное . По отношению к другим фенэтиламинам и амфетаминам это 3,4-метилендиокси, α-метилпроизводное β-фенилэтиламина , 3,4-метилендиоксипроизводное амфетамина и N - десметилпроизводное МДМА.
Синонимы
[ редактировать ]Помимо 3,4-метилендиоксиамфетамина , МДА также известен под другими химическими синонимами, такими как следующие:
- α-Метил-3,4-метилендиокси-β-фенилэтиламин
- 1-(3,4-Метилендиоксифенил)-2-пропанамин
- 1-(1,3-бензодиоксол-5-ил)-2-пропанамин
Синтез
[ редактировать ]МДА обычно синтезируют из эфирных масел, таких как сафрол или пиперональ . Общие подходы к этим прекурсорам включают:
- сафрола Реакция алкеновой функциональной группы с галогенсодержащей минеральной кислотой с последующим алкилированием амина . [ 17 ] [ 18 ]
- Вакер-окисление сафрола с образованием 3,4-метилендиоксифенилпропан-2-она (MDP2P) с последующим восстановительным аминированием . [ 18 ] [ 19 ] или путем восстановления его оксима . [ 20 ]
- Реакция Генри пипероналя с нитроэтаном с последующим восстановлением нитросоединения . [ 18 ] [ 21 ] [ 22 ] [ 23 ] [ 24 ]
- Реакция Дарценса на гелиотропин была также проведена Дж. Элксом и др. [ 25 ] Это дает MDP2P , который затем подвергают реакции Лейкарта.
- метод «двух собак» или «наркомана» Тайный , начиная с гелиала в качестве прекурсора. Сначала создается оксим с использованием гидроксиламина. Затем проводят перегруппировку Бекмана с ацетатом никеля с образованием амида. Затем перегруппировка Гофмана проводится с образованием свободного основания амина МДА. Затем его очищают кислотно-щелочной экстракцией . [ 26 ]
Обнаружение в жидкостях организма
[ редактировать ]МДА может быть определен количественно в крови, плазме или моче для мониторинга использования, подтверждения диагноза отравления или оказания помощи в судебно-медицинском расследовании дорожного движения, других преступных нарушений или внезапной смерти. Некоторые программы скрининга на злоупотребление наркотиками используют в качестве образцов волосы, слюну или пот. Большинство коммерческих скрининговых тестов иммуноанализа на амфетамин в значительной степени дают перекрестную реакцию с МДА и основными метаболитами МДМА, но хроматографические методы позволяют легко различить и отдельно измерить каждое из этих веществ. Концентрация МДА в крови или моче человека, принимавшего только МДМА, обычно составляет менее 10% от концентрации исходного препарата. [ 27 ] [ 28 ] [ 29 ]
Производные
[ редактировать ]MDA составляет часть основной структуры агониста β-адренергических рецепторов протокилола .
История
[ редактировать ]МДА был впервые синтезирован Карлом Маннихом и В. Якобсоном в 1910 году. [ 20 ] Впервые он был принят в июле 1930 года Гордоном Аллесом , который позже лицензировал препарат компании Smith, Kline & French . [ 30 ] MDA впервые был использован в испытаниях на животных в 1939 году, а испытания на людях начались в 1941 году с целью изучения возможных методов лечения болезни Паркинсона . С 1949 по 1957 год более пятисот человек получали MDA в ходе исследования Смитом, Кляйном и Френчем его потенциального использования в качестве / или аноректического средства антидепрессанта и . Армия Соединенных Штатов также экспериментировала с препаратом под кодовым названием EA-1298, работая над разработкой препарата правды или выводящего из строя агента. Гарольд Блауэр умер в январе 1953 года после того, как ему без его ведома и согласия внутривенно ввели 450 мг препарата в рамках проекта MKUltra . МДА был запатентован Смитом, Кляйном и Френчем как в атарактическое средство 1960 году и как аноректическое средство под торговым названием «Амфедоксамин» в 1961 году. МДА начал появляться на рынке рекреационных наркотиков примерно в 1963–1964 годах. В то время он был недорогим и легко доступным. в качестве исследовательского химиката от нескольких научных поставщиков. Несколько исследователей, в том числе Клаудио Наранхо и Ричард Йенсен , изучали MDA в области психотерапия . [ 31 ] [ 32 ]
Общество и культура
[ редактировать ]
Имя
[ редактировать ]Когда МДА разрабатывался как потенциальный фармацевтический препарат, ему было присвоено международное непатентованное название (МНН) тенамфетамин .
Юридический статус
[ редактировать ]Австралия
[ редактировать ]MDA является запрещенным веществом из списка 9 согласно Стандартам по ядам . [ 33 ] Вещество Списка 9 внесено в список «Вещества, которыми можно злоупотреблять или использовать не по назначению, производство, хранение, продажа или использование которых должно быть запрещено законом, за исключением случаев, когда это требуется для медицинских или научных исследований, или для аналитических, обучающих или учебных целей с одобрение органов здравоохранения Содружества и/или штата или территории». [ 33 ]
Соединенные Штаты
[ редактировать ]MDA является контролируемым веществом Списка I в США.
Исследовать
[ редактировать ]В 2010 году изучалась способность MDA вызывать мистические переживания и изменять зрение у здоровых добровольцев. Исследование пришло к выводу, что MDA является «потенциальным инструментом для исследования мистических переживаний и визуального восприятия». [ 7 ]
В двойном слепом исследовании 2019 года здоровым добровольцам вводили как МДА, так и МДМА. Исследование показало, что МДА имел много общих свойств с МДМА, включая энтактогенный и стимулирующий эффекты, но, как правило, длился дольше и вызывал большее усиление психоделических эффектов, таких как сложные образы, синестезия и духовные переживания. [ 34 ]
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ «ПДК № 804 – Перечни наркотических средств, психотропных веществ, прекурсоров и других веществ, находящихся под особым контролем» [Постановление Коллегии Коллегии № 804]. № 804 - Списки наркотических, психотропных веществ, прекурсоров и других веществ, находящихся под особым контролем]. Бразильское агентство по регулированию здравоохранения (на бразильском португальском языке). Официальный вестник Союза (опубликовано 25 июля 2023 г.). 24 июля 2023 года. Архивировано из оригинала 27 августа 2023 года . Проверено 27 августа 2023 г.
- ^ Крин Р.Д., Дэвис С.А., Фон Хубен С.Н., Лэй CC, Катнер С.Н., Тафф М.А. (октябрь 2006 г.). «Влияние (+/-)3,4-метилендиоксиметамфетамина, (+/-)3,4-метилендиоксиамфетамина и метамфетамина на температуру и активность макак-резус» . Нейронаука . 142 (2): 515–525. doi : 10.1016/j.neuroscience.2006.06.033 . ПМЦ 1853374 . ПМИД 16876329 .
- ^ Jump up to: а б де ла Торре Р., Фарре М., Розет П.Н., Писарро Н., Абанадес С., Сегура М. и др. (апрель 2004 г.). «Человеческая фармакология МДМА: фармакокинетика, метаболизм и расположение». Терапевтический лекарственный мониторинг . 26 (2): 137–144. дои : 10.1097/00007691-200404000-00009 . ПМИД 15228154 .
- ^ «EcstasyData.org: Статистика результатов испытаний: вещества по годам» . EcstasyData.org . Проверено 27 июня 2017 г.
- ^ «Трансъевропейская информация о наркотиках» . idpc.net . Архивировано из оригинала 4 ноября 2021 года . Проверено 27 июня 2017 г.
- ^ Монте А.П., Марона-Левика Д., Коззи Н.В., Николс Д.Е. (ноябрь 1993 г.). «Синтез и фармакологическое исследование бензофурановых, индановых и тетралиновых аналогов 3,4-(метилендиокси)амфетамина». Журнал медицинской химии . 36 (23): 3700–3706. дои : 10.1021/jm00075a027 . ПМИД 8246240 .
- ^ Jump up to: а б с Бэгготт М.Дж., Зигрист Дж.Д., Галлоуэй Г.П., Робертсон Л.К., Койл Дж.Р., Мендельсон Дж.Э. (декабрь 2010 г.). «Исследование механизмов галлюциногенных видений с использованием 3,4-метилендиоксиамфетамина (МДА): рандомизированное контролируемое исследование на людях» . ПЛОС ОДИН . 5 (12): e14074. Бибкод : 2010PLoSO...514074B . дои : 10.1371/journal.pone.0014074 . ПМЦ 2996283 . ПМИД 21152030 .
- ^ Jump up to: а б Херндон Дж. М., Чоланианс А. Б., Лау С. С., Монкс Т. Дж. (март 2014 г.). «Реакция глиальных клеток на 3,4-(+/-)-метилендиоксиметамфетамин и его метаболиты» . Токсикологические науки . 138 (1): 130–138. дои : 10.1093/toxsci/kft275 . ПМЦ 3930364 . ПМИД 24299738 .
- ^ Калант Х (октябрь 2001 г.). «Фармакология и токсикология «экстази» (МДМА) и родственных ему наркотиков» . CMAJ . 165 (7): 917–928. ПМК 81503 . ПМИД 11599334 .
- ^ Диас Дж (1996). Как наркотики влияют на поведение . Энглвуд Клиффс: Прентис Холл.
- ^ Левин А.Х., Миллер ГМ, Гилмор Б. (декабрь 2011 г.). «Рецептор 1, связанный с следовым амином, представляет собой стереоселективный сайт связывания соединений класса амфетаминов» . Биоорганическая и медицинская химия . 19 (23): 7044–7048. дои : 10.1016/j.bmc.2011.10.007 . ПМК 3236098 . ПМИД 22037049 .
- ^ Ротман Р.Б., Бауманн М.Х. (2006). «Терапевтический потенциал субстратов-переносчиков моноаминов» . Актуальные темы медицинской химии . 6 (17): 1845–1859. дои : 10.2174/156802606778249766 . ПМИД 17017961 .
- ^ Ди Джованни Дж., Ди Маттео В., Эспозито Э. (2008). Взаимодействие серотонина и дофамина: экспериментальные данные и терапевтическая значимость . Эльзевир. стр. 294–. ISBN 978-0-444-53235-0 .
- ^ Ротман Р.Б., Бауманн М.Х. (май 2009 г.). «Серотонинергические препараты и пороки сердца» . Экспертное заключение о безопасности лекарственных средств . 8 (3): 317–329. дои : 10.1517/14740330902931524 . ПМЦ 2695569 . ПМИД 19505264 .
- ^ Нэш Дж. Ф., Рот Б. Л. , Бродкин Дж. Д., Николс Д. Е., Гудельский Г. А. (август 1994 г.). «Влияние изомеров R (-) и S (+) МДА и МДМА на оборот фосфатидилинозитола в культивируемых клетках, экспрессирующих рецепторы 5-HT2A или 5-HT2C». Письма по неврологии . 177 (1–2): 111–115. дои : 10.1016/0304-3940(94)90057-4 . ПМИД 7824160 . S2CID 41352480 .
- ^ Рэй Т.С. (февраль 2010 г.). «Психоделики и рецептором человека» . ПЛОС ОДИН . 5 (2): е9019. Бибкод : 2010PLoSO...5.9019R . дои : 10.1371/journal.pone.0009019 . ПМК 2814854 . ПМИД 20126400 .
- ^ Мушинский Э (1961). «[Производство некоторых производных амфетамина]». Акта Польская Фармацевтика . 18 : 471–478. ПМИД 14477621 .
- ^ Jump up to: а б с Шульгин А., Мэннинг Т., Дейли П. (2011). Индекс Шульгина, Том первый: Психоделические фенэтиламины и родственные соединения (1-е изд.). Беркли, Калифорния: Transform Press. п. 165. ИСБН 978-0-9630096-3-0 .
- ^ Ноггл Ф.Т., ДеРуитер Дж., Лонг М.Дж. (1986). «Спектрофотометрическая и жидкостная хроматографическая идентификация 3,4-метилендиоксифенилизопропиламина и его N-метиловых и N-этильных гомологов». Журнал Ассоциации официальных химиков-аналитиков . 69 (4): 681–686. ПМИД 2875058 .
- ^ Jump up to: а б Манних С., Якобсон В., Манних Х.К. (1910). «Об оксифенилалкиламинах и диоксифенилалкиламинах» . Отчеты Немецкого химического общества . 41 (1): 189–197. дои : 10.1002/cber.19100430126 .
- ^ Хо Б.Т., МакИсаак В.М., Ан Р., Тэнси Л.В., Уокер К.Е., Энглерт Л.Ф., Ноэль М.Б. (январь 1970 г.). «Аналоги альфа-метилфенэтиламина (амфетамина). I. Синтез и фармакологическая активность некоторых метокси- и/или метильных аналогов». Журнал медицинской химии . 13 (1): 26–30. дои : 10.1021/jm00295a007 . ПМИД 5412110 .
- ^ Баттерик-младший, Унрау А.М. (1974). «Восстановление β-нитростирола дигидридом бис-(2-метоксиэтокси) алюминия натрия. Удобный путь к замещенным фенилизопропиламинам». Журнал Химического общества, Химические коммуникации . 8 (8): 307–308. дои : 10.1039/C39740000307 .
- ^ Тошитака О, Хироака А (1992). «Синтез производных фенэтиламина как галлюциногена» . Японский журнал токсикологии и гигиены окружающей среды . 38 (6): 571–580. дои : 10.1248/jhs1956.38.571 . Проверено 20 июня 2014 г.
- ^ Шульгин А, Шульгин А (1991). PiHKAL: Химическая история любви . Лафайет, Калифорния: Transform Press. ISBN 978-0-9630096-0-9 .
- ^ Элкс Дж., Эй, Д.Х. (1943). «7. β-3:4-Метилендиоксифенилизопропиламин». Дж. Хим. Соц. : 15–16. дои : 10.1039/JR9430000015 . ISSN 0368-1769 .
- ^ «Использует ли метод тайного синтеза «двух собак» прекурсоры, которые не регулируются законом на восточном побережье Австралии? Виктор Чирута, Роберт Д. Реншоу :: SSRN» . 28 ноября 2021 г. ОГРН 3973132 . Проверено 11 февраля 2024 г.
- ^ Колбрич Э.А., Гудвин Р.С., Горелик Д.А., Хейс Р.Дж., Штейн Э.А., Хьюстис М.А. Фармакокинетика 3,4-метила в плазме
эндиокси метамфетамин после контролируемого перорального приема молодым людям. Там. Препарат Монит. 30: 320–332, 2008. - ^ Барнс А.Дж., Де Мартинис Б.С., Горелик Д.А., Гудвин Р.С., Колбрич Э.А., Хьюстис М.А. (март 2009 г.). «Выделение МДМА и его метаболитов в поте человека после контролируемого введения МДМА» . Клиническая химия . 55 (3): 454–462. дои : 10.1373/clinchem.2008.117093 . ПМЦ 2669283 . ПМИД 19168553 .
- ^ Р. Базелт, Удаление токсичных лекарств и химикатов в организме человека , 9-е издание, Биомедицинские публикации, Сил-Бич, Калифорния, 2011, стр. 1078–1080.
- ^ «Первый трип MDA и измерение «мистического опыта» после MDA, ЛСД и псилоцибина» . Психоделические исследования. 18 июля 2008 г. Архивировано из оригинала 13 июля 2012 г.
- ^ Наранхо С., Шульгин А.Т., Сарджент Т. (1967). «Оценка 3,4-метилендиоксиамфетамина (МДА) как дополнения к психотерапии». Medicina et Pharmacologia Experimentalis. Международный журнал экспериментальной медицины . 17 (4): 359–364. дои : 10.1159/000137100 . ПМИД 5631047 .
- ^ Йенсен Р., Ди Лео Ф.Б., Рхед Дж.К., Ричардс В.А., Соскин Р.А., Турек Б., Курланд А.А. (октябрь 1976 г.). «Психотерапия с помощью MDA амбулаторных пациентов-невротиков: пилотное исследование». Журнал нервных и психических заболеваний . 163 (4): 233–245. дои : 10.1097/00005053-197610000-00002 . ПМИД 972325 . S2CID 41155810 .
- ^ Jump up to: а б Стандарт по ядам (октябрь 2015 г.) comlaw.gov.au
- ^ Бэгготт М.Дж., Гаррисон К.Дж., Койл Дж.Р., Галлоуэй Г.П., Барнс А.Дж., Хьюстис М.А., Мендельсон Дж.Э. (15 марта 2019 г.). «Эффекты психоделического амфетамина MDA (3,4-метилендиоксиамфетамина) на здоровых добровольцах». Журнал психоактивных препаратов . 51 (2): 108–117. дои : 10.1080/02791072.2019.1593560 . ПМИД 30967099 . S2CID 106410946 .
Внешние ссылки
[ редактировать ]- Препараты, которым не присвоен код АТС
- Агонисты 5-НТ2А
- Агонисты 5-HT2B
- Агонисты 5-HT2C
- Бензодиоксолы
- Энтактогены и эмпатогены
- Эйфорианты
- Психоделические наркотики
- Агенты, высвобождающие серотонин-норадреналин-дофамин
- Агонисты рецепторов серотонина
- Стимуляторы
- Замещенные амфетамины
- Агонисты TAAR1
- Ингибиторы VMAT
- Метаболиты рекреационных наркотиков
- Метаболиты лекарств человека
